Monografia Alcanos
Diunggah oleh
Analía CristadulaquisJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Monografia Alcanos
Diunggah oleh
Analía CristadulaquisHak Cipta:
Format Tersedia
COMPUESTOS ORGNICOS: ALCANOS, ALQUENOS Y ALQUINOS
MATERIA: QUIMICA
PROFESORA: LIS ALOMAR
ALUMNOS > ANALIA CRISTADULAQUIS > BEATRIZ LASCANO 1ER. AO TECNICATURA SUPERIOR EN SEGURIDAD, HIGIENE Y CONTROL AMBIENTAL INDUSTRIAL.
INSTITUTO DE FORMACION DOCENTE Y TECNICA NRO. 57 EXT. COBO 19 DE NOVIEMBRE DE 2012.
CONTENIDO
ii
iii
Salute e Sicurezza S.R.L. COMPUESTOS ORGNICOS: .........................................................................................I ALCANOS, ALQUENOS Y ALQUINOS..........................................................................I MATERIA: QUIMICA........................................................................................................I PROFESORA: LIS ALOMAR............................................................................................I ALUMNOS > ANALIA CRISTADULAQUIS....................................................................................................I > BEATRIZ LASCANO......................................................................................................I 1ER. AO TECNICATURA SUPERIOR EN SEGURIDAD, HIGIENE Y CONTROL AMBIENTAL INDUSTRIAL.........................................................................................................I INSTITUTO DE FORMACION DOCENTE Y TECNICA NRO. 57 EXT. COBO...........I 19 DE NOVIEMBRE DE 2012............................................................................................I RESEA.............................................................................................................................V ALCANOS..........................................................................................................................1 PROPIEDADES FISICAS..................................................................................................1 REACCIONES O PROPIEDADES QUIMICAS...............................................................2 ALQUENOS........................................................................................................................3 PROPIEDADES FISICAS..................................................................................................3 REACCIONES O PROPIEDADES QUIMICAS...............................................................3 ALQUINOS.........................................................................................................................5 PROPIEDADES FISICAS..................................................................................................5 REACCIONES O PROPIEDADES QUIMICAS...............................................................5
iv
Salute e Sicurezza S.R.L. BIBLIOGRAFIA...............................................................................................................10
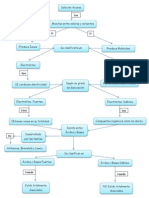
RESEA Los compuestos orgnicos son todas las especies qumicas que en su composicin contienen el elemento carbono (C) y, usualmente, elementos tales como el Oxgeno(O), Hidrgeno (H), Fsforo (F), Cloro (CL), Yodo (I) y nitrgeno (N), con la excepcin del anhdrido carbnico, los carbonatos y los cianuros. Estos compuestos constituyen la mayor cantidad de sustancias que se encuentran sobre la tierra. Contienen desde un tomo de carbono como el gas metano (CH4) que utilizamos como combustible, hasta molculas muy grandes o macromolculas con cientos de miles de tomos de carbono como el almidn, las protenas y los cidos nucleicos. Los compuestos orgnicos formados principalmente por combinaciones diferentes de carbono, hidrgeno, oxgeno y nitrgeno, tienen propiedades especiales que son tiles para el ser humano. Las cadenas carbonadas pueden ser de dos tipos, cadenas abiertas cadenas cerradas. En estos dos grandes grupos se encuentran compuestos binarios formados nicamente por Carbono e Hidrgeno, llamados hidrocarburos, entre los cuales se encuentran los alcanos, alquenos, alquinos y aromticos.
III
ALCANOS Se les denomina tambin hidrocarburos aromticos o parafinas. As como tambin, la denominacin de saturados les viene porque poseen la mxima cantidad de hidrgeno que una cadena carbonada puede admitir. La denominacin de parafinas se refiere a su poca actividad qumica, actividad limitada que obedece a la estabilidad de los enlaces carbono-carbono, y a la firmeza con que los tomos de hidrgeno se unen a la cadena carbonada.
Etano (un enlace carbono-carbono).
Todos los enlaces dentro de la molcula de alcanos son de tipo simple. Los alcanos se obtienen mayoritariamente del petrleo. Son los productos base para la obtencin de otros compuestos orgnicos. PROPIEDADES FISICAS 1. Estado Fsico: a 25C los hidrocarburos normales desde C1 hasta C4 son gases, desde C5 hasta C17 son lquidos y desde C18 en adelante son slidos. 2. Puntos de Ebullicin: Los puntos de ebullicin muestran un aumento constante al aumentar el nmero de tomos de carbono. Sin embargo, la ramificacin de la cadena del alcano disminuye notablemente el punto de ebullicin, porque las molculas que forman el compuesto se van haciendo esfricamente ms simtricas y, en consecuencia, disminuyen las fuerzas de atraccin entre ellas. 3. Puntos de Fusin: los alcanos no muestran el mismo aumento en los puntos de fusin con el aumento del nmero de tomos de carbono. Se observa una alternancia a medida que se progresa de un alcano con un nmero par de tomos de carbono, al siguiente con un nmero impar de tomos de carbono. Por ejemplo, el propano (PF (punto de fusin = -187C) funde a menor temperatura que el etano (PF= -172C) y aun menor temperatura que el metano (PF= -183C). En general, el punto de fusin aumenta con el nmero de tomos de carbono y la simetra de la molcula.
4. Densidad: los alcanos son los menos densos de los compuestos orgnicos. Todos los alcanos tienen densidades considerablemente menores a 1g/mL, (la densidad del agua a 4C). 5. Solubilidad: los alcanos son casi totalmente insolubles en agua debido a su baja polaridad, y a su incapacidad de formar enlaces por puentes de hidrgeno. Los alcanos lquidos son miscibles entre s (que se puede mezclar), y generalmente se disuelven en solventes de baja polaridad. REACCIONES O PROPIEDADES QUIMICAS A temperatura ambiente los alcanos son inertes a la mayora de los reactivos comunes. Entre las reacciones ms importantes de los alcanos se encuentran: 1. Combustin: en presencia del calor producido por una llama, los alcanos reaccionan con el oxgeno atmosfrico originando dixido de carbono y agua (combustin completa). En la reaccin se libera una gran cantidad de calor.
2. Halogenacin: reaccin de sustitucin por radicales libres. En presencia de luz o calentados a temperatura de 300C o ms, los alcanos reaccionan con cloro o bromo dando origen a mezclas de derivados halogenados, y desprendiendo halogenuros de hidrgeno. La mezcla de derivados halogenados indica que todos los tomos de hidrgeno del hidrocarburo son susceptibles de sustitucin. La halogenacin se produce por un mecanismo de radicales libres, en la cual la luz suministra la energa necesaria para que se realice la reaccin. 3. Pirlisis: es la descomposicin de una sustancia por la sola accin del calor. La pirlisis de alcanos, en particular en lo que concierne al petrleo, se conoce como cracking. En el cracking trmico, los alcanos se hacen pasar por una cmara calentada a temperatura elevada, con lo cual los alcanos de cadena larga y alta masa molar, se convierten en alcanos ms livianos, alquenos y algo de hidrgeno. La temperatura oscila entre 400C y 600C y la reaccin se puede ejecutar con catalizador o sin l. La ecuacin qumica general para la pirlisis es:
ALQUENOS Los alquenos son hidrocarburos alifticos que poseen un doble enlace entre dos tomos de carbono consecutivos. El doble enlace es un punto reactivo o un grupo funcional y es el que determina principalmente las propiedades de los alquenos.
Eteno, dos carbonos con enlace doble.
Los alquenos tambin se conocen como hidrocarburos insaturados (tienen menos hidrgeno que el mximo posible). Un antiguo nombre de esta familia de compuestos es oleofinas.
PROPIEDADES FISICAS
1. Estado Fsico: los tres primeros miembros son gases a temperatura ordinaria, del C5 hasta el C18 son lquidos y los dems slidos.
2. Puntos de Ebullicin: son un poco ms bajos (algunos grados) que los alcanos. 3. Puntos de Fusin: son ligeramente mayores que el de los alcanos. 4. Densidad: un poco ms alta que la de los alcanos. 5. Solubilidad: la solubilidad de los alquenos en agua, aunque dbil, es considerablemente ms alta que la de los alcanos, debido a que la concentracin de los electrones en el doble enlace, produce una mayor atraccin del extremo positivo del dipolo de la molcula de agua.
REACCIONES O PROPIEDADES QUIMICAS
1. Combustin: en presencia del calor producido por una llama, los alquenos reaccionan con el oxgeno atmosfrico, originando dixido de carbono y agua. Esto constituye una combustin completa. En la reaccin se libera gran cantidad de calor.
2. Hidrogenacin: adicin de una molcula de hidrgeno (H2 H-H)
Los alquenos al ponerlos en contacto con el hidrgeno (H2) en presencia de un catalizador tal como el Pt, Pd Ni finalmente divididos, dan origen a alcanos.
El doble enlace se rompe.
Halogenacin: adicin de una molcula de halgeno (X2, donde X es F, Cl, Br I).
Los alquenos reaccionan con el bromo (Br - Br), disuelto en tetracloruro de carbono (CCl4), a temperatura ambiente y en ausencia de luz. Se forma un compuesto cuyo nombre general es dihalogenuro vecinal dihaluro vecinal (vic-dihaluro). Se sabe que la reaccin se ha efectuado, porque el color rojo pardo del bromo en el CCl4 desaparece casi instantneamente. La reaccin de adicin se presenta as:
El bromo disuelto en CCl4 es un reactivo til para distinguir entre alquenos y alcanos, ya que estos ltimos no reaccionan con l.
ALQUINOS Los alquinos son hidrocarburos alifticos que poseen un triple enlace entre dos tomos de carbono adyacentes. El triple enlace es un punto reactivo o un grupo funcional y es el que determina principalmente las propiedades de los alquinos. Los alquinos tambin se conocen como hidrocarburos acetilnicos, debido a que el primer miembro de esta serie homloga es el acetileno o etino.
Etino, dos carbonos con enlace triple.
PROPIEDADES FISICAS
1. Estado Fsico: son gases hasta el C5, lquidos hasta el C15 y luego slidos 2. Puntos de Ebullicin: son ms altos que los de los correspondientes alquenos y alcanos 3. Puntos de Fusin: se puede decir lo mismo que para el punto de ebullicin 4. Densidad: igual que en los casos anteriores 5. Solubilidad: se disuelven en solventes no polares
REACCIONES O PROPIEDADES QUIMICAS El triple enlace es menos reactivo que el doble enlace.
1. Combustin: en presencia de calor producido por una llama, los alquinos reaccionan con
el oxgeno atmosfrico, originando dixido de carbono y agua, lo cual constituye una combustin completa. En la reaccin se libera gran cantidad de calor.
2. Hidrogenacin: la hidrogenacin cataltica (Ni, Pt, Pd) conduce primero a la formacin
de un alqueno y luego a la del alcano correspondiente.
3. Halogenacin: los alquinos en presencia de un catalizador reaccionan con dos molculas
de halgeno, originando los tetrahaluros de alquilo.
4. Adicin de agua: se utiliza para formar etanal (aldehdo con dos tomos de carbono), el
cual puede oxidarse luego a cido actico (cido orgnico con dos tomo de carbono). La reaccin se lleva a cabo utilizando H2SO4 y HgSO4 como catalizadores. La adicin de agua a otros alquinos no origina aldehdos, sino cetonas, ya que el OH se fija al carbono menos hidrogenado.
5. Oxidacin de los alquinos: cuando los alquinos se tratan con el reactivo Baeyer sufren
una ruptura oxidativa en forma similar a la que se produce en los alquenos. Los productos de la reaccin (despus de la acidificacin) son cidos carboxlicos fciles de identificar. Esta reaccin permite localizar la posicin del triple enlace en un alquino.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS Alcanos Alquenos Alquinos
Estado Fsico
Desde C1 hasta C4 gases, Tres primeros miembros Son gases hasta el C5, desde C5 hasta C17 son gases, del C5 hasta lquidos hasta el C15 y lquidos y desde C18 en el C18 son lquidos y los luego slidos adelante slidos. dems slidos Aumento constante al aumentar el nmero de tomos de carbono Un poco ms bajos que los alcanos. Ms altos que los de los correspondientes alquenos y alcanos
P. Ebullicin
P. Fusin
Alternancia a medida que se progresa de un alcano con un nmero par de tomos Ligeramente mayores de C, al siguiente con un que el de los alcanos nmero impar de tomos de C Menor a 1g/mL, (la densidad del agua a 4C). Casi totalmente insolubles en agua. Se disuelven en solventes de baja polaridad. Un poco ms alta que la de los alcanos es considerablemente ms alta que la de los alcanos
Ms altos que los de los correspondientes alquenos y alcanos
Densidad
Ms altos que los de los correspondientes alquenos y alcanos se disuelven en solventes no polares
Solubilidad
Propiedades Qumicas Combustin Combustin completa Combustin completa Combustin completa
dan origen a mezclas de Se forma un compuesto derivados halogenados, y Origina los tetrahaluros Halogenacin cuyo nombre general es desprendiendo halogenuros de alquilo. dihalogenuro vecinal de hidrgeno. Pirlisis Se convierten en alcanos mas livianos, alquenos y algo de hidrgeno Dan origen a alcanos Forman un alqueno y luego el alcano correspondiente
Hidrogenacin
Qu es un grupo funcional? Los hidrgenos de los hidrocarburos pueden ser sustituidos por tomos de otro metal o por un agrupamiento de tomos para obtener compuestos derivados que poseen propiedades muy diferentes y que presentan estructuras muy distintas (el tomo o grupo de tomos sustituyentes les confieren otras propiedades fsicas y qumicas). Pues bien, a ese tomo o grupo de tomos que representan la diferencia entre un hidrocarburo y el nuevo compuesto, se le llama grupo funcional. Se puede decir que un grupo funcional es un tomo o grupo de tomos que caracteriza a una clase de compuestos orgnicos. Cada grupo funcional determina las propiedades qumicas de las sustancias que lo poseen; es decir determina su funcin qumica. Entonces, se llama funcin qumica a las propiedades comunes que caracterizan a un grupo de sustancias que tienen estructura semejante; es decir, que poseen un determinado grupo funcional.
Etanol
Por ejemplo, en un alcano, los tomos de hidrgeno pueden ser sustituidos por otros tomos (de oxgeno o nitrgeno, por ejemplo), siempre que se respete el nmero correcto de enlaces qumicos (recordemos que el oxgeno forma dos enlaces con los otros tomos y el nitrgeno forma tres). El grupo OH en el alcohol etlico y el grupo NH2 en la etilamina son grupos funcionales. La existencia de un grupo funcional cambia completamente las propiedades qumicas (la funcin qumica) de la molcula. Por ejemplo, el etano, alcano con dos carbonos, es un gas a temperatura ambiente; el etanol, el alcohol de dos carbonos (derivado del etano por sustitucin), es un lquido.
El etanol, el alcohol que se bebe comnmente, es el ingrediente activo en las bebidas "alcohlicas" como la cerveza y el vino.
10
BIBLIOGRAFIA http://www.profesorenlinea.cl/Quimica/grupos_funcionales.html http://clubensayos.com/Tecnolog%C3%ADa/Alcanos-Alquenos-Y-Alquinos/791.html http://www.estudiantes.info/ciencias_naturales/quimica/quimica-organica.htm http://es.scribd.com/doc/20785199/CLASE-DE-ALCANOS-ALQUENOS-ALQUINOS http://quimicayalgomas.com.ar/quimica-organica/alcanos-alquenos-y-alquinos
11
Anda mungkin juga menyukai
- Investigacion Alcanos Alquenos y Alquinos.Dokumen47 halamanInvestigacion Alcanos Alquenos y Alquinos.JESUS EDUARDO NU�EZ NU�EZBelum ada peringkat
- Trancision ElectronicaDokumen14 halamanTrancision ElectronicaLeonardoBelum ada peringkat
- Quimi09 CineticaDokumen7 halamanQuimi09 CineticaSonidos Renjifo Ccopa CondoriBelum ada peringkat
- Laboratorio Enlace QuimicoDokumen18 halamanLaboratorio Enlace QuimicoLaurita Molina Cabrera67% (3)
- Amidas y Aminas FinalDokumen15 halamanAmidas y Aminas FinalAdrian Arauco CarhuasBelum ada peringkat
- Acidez de Alquinos TerminalesDokumen3 halamanAcidez de Alquinos TerminalesPepe Kaztor MarinBelum ada peringkat
- Física biomédica BIOElectricidad BIOMagnetismoDokumen92 halamanFísica biomédica BIOElectricidad BIOMagnetismothecesar5x0% (1)
- Informe Alcoholes, Fenoles, Aldehidos y Cetonas 2021-IIDokumen20 halamanInforme Alcoholes, Fenoles, Aldehidos y Cetonas 2021-IIJessica Fernanda Coaricona OrtegaBelum ada peringkat
- X Aldehidos y Cetonas PDFDokumen34 halamanX Aldehidos y Cetonas PDFAlcira MendozaBelum ada peringkat
- Informe N°2 Química Laboratorio Enlaces Químicos Grupo 2Dokumen10 halamanInforme N°2 Química Laboratorio Enlaces Químicos Grupo 2Himiko TogaBelum ada peringkat
- Introducción A Los Metales de TransiciónDokumen50 halamanIntroducción A Los Metales de Transiciónripela49011Belum ada peringkat
- Qué Es El Formol y para Que UtilizaDokumen2 halamanQué Es El Formol y para Que UtilizaDavid BryanBelum ada peringkat
- IMINASDokumen12 halamanIMINASAdriana Espejo VargasBelum ada peringkat
- ESTEREOISOMERIADokumen47 halamanESTEREOISOMERIAalexanderBelum ada peringkat
- Halogenuros de AlquiloDokumen4 halamanHalogenuros de AlquiloFransisBelum ada peringkat
- Guias de Practicas de Quimica para MatematicasDokumen51 halamanGuias de Practicas de Quimica para MatematicasFranklin A. Ttito Chañi100% (2)
- Mechero-Llama LuminosaDokumen2 halamanMechero-Llama LuminosaYahir83% (6)
- Cicloalcanos: propiedades y ejemplosDokumen11 halamanCicloalcanos: propiedades y ejemplosWeekly LyricsBelum ada peringkat
- Informe 6Dokumen6 halamanInforme 6Rosalinda Quispe LuyoBelum ada peringkat
- Fuerzas intermoleculares y sus tiposDokumen14 halamanFuerzas intermoleculares y sus tiposJavier Cerda InfanteBelum ada peringkat
- AlcanosDokumen38 halamanAlcanoskatiagelvis80% (5)
- Nomenclatura Cicloalcanos-Reglas IUPACDokumen7 halamanNomenclatura Cicloalcanos-Reglas IUPACMARIABelum ada peringkat
- AlquenosDokumen24 halamanAlquenosronaldBelum ada peringkat
- Aplicaciones de Los AlquenosDokumen2 halamanAplicaciones de Los AlquenosClau GrcBelum ada peringkat
- GUIA DE LABORATORIO 01 Reconocimiento de C, H, O, N, SDokumen6 halamanGUIA DE LABORATORIO 01 Reconocimiento de C, H, O, N, SAustin palao0% (1)
- Mapa Conceptual MDokumen2 halamanMapa Conceptual MMario G. Colmenares100% (1)
- Reconocimiento de compuestos orgánicos e inorgánicosDokumen9 halamanReconocimiento de compuestos orgánicos e inorgánicosBryan Nuñez MuchaBelum ada peringkat
- Marco TeoricoDokumen7 halamanMarco TeoricoYariana MontoyaBelum ada peringkat
- Alquenos: Enlaces dobles y propiedadesDokumen17 halamanAlquenos: Enlaces dobles y propiedadesPareja Pérez CamilaBelum ada peringkat
- AMIDASDokumen21 halamanAMIDASandresBelum ada peringkat
- Identificación de aldehídos y cetonasDokumen11 halamanIdentificación de aldehídos y cetonasDeysy CortezBelum ada peringkat
- Reacciones Químicas MonografíaDokumen25 halamanReacciones Químicas MonografíaLenin DenysBelum ada peringkat
- Química Orgánica ExperimentalDokumen124 halamanQuímica Orgánica ExperimentalFernando Melo100% (1)
- 3) Leyes de Los GasesDokumen52 halaman3) Leyes de Los GasesCarolina Estephanie Flores GuerraBelum ada peringkat
- Reconocimiento Del Carbono Hidrogeno Oxigeno y NitrogenoDokumen11 halamanReconocimiento Del Carbono Hidrogeno Oxigeno y NitrogenoNarro Chigne A. HugoBelum ada peringkat
- Qué Estudia La Química OrgánicaDokumen4 halamanQué Estudia La Química OrgánicaguamushigBelum ada peringkat
- Composicion Quimica de Los Seres VivosDokumen30 halamanComposicion Quimica de Los Seres VivosLuis Alberto GonzalezBelum ada peringkat
- Introduccion Nomenclatura AlcanosDokumen39 halamanIntroduccion Nomenclatura AlcanosFrida Krys100% (3)
- Informe Del Mechero de BunsenDokumen14 halamanInforme Del Mechero de BunsenLorena MuñozBelum ada peringkat
- Alcanos Alquenos y AlquinosDokumen16 halamanAlcanos Alquenos y AlquinosNadim SalomonBelum ada peringkat
- Isomeria 2Dokumen24 halamanIsomeria 2Joseph EstradaBelum ada peringkat
- Aldehidos y Cetonas PracticaDokumen20 halamanAldehidos y Cetonas PracticaAnonymous 2LFdJ7ATHwBelum ada peringkat
- Química GeneralDokumen11 halamanQuímica GeneralFiorella Leon Morales0% (5)
- Propiedades Físicas y Químicas de Los Ácidos CarboxílicosDokumen11 halamanPropiedades Físicas y Químicas de Los Ácidos CarboxílicosFernanda Mateus100% (1)
- IES Manuel Seoane Corrales bibliografía química industrialDokumen1 halamanIES Manuel Seoane Corrales bibliografía química industrialJuanCarlitoz OrnzBelum ada peringkat
- Enlace Covalente DativoDokumen3 halamanEnlace Covalente DativoSebastian Eduardo Chacana MuñozBelum ada peringkat
- Mapa Mental NitrogenadasDokumen1 halamanMapa Mental NitrogenadasEduardo Sanchez Aquino100% (3)
- Compuestos AromaticosDokumen34 halamanCompuestos AromaticosBrian WilliamsBelum ada peringkat
- Informe Final de Obtencion y Reconocimiento de Alcanos, Alquenos y AlquinosDokumen7 halamanInforme Final de Obtencion y Reconocimiento de Alcanos, Alquenos y AlquinosMaría Paula SarastyBelum ada peringkat
- Funciones OxigenadasDokumen29 halamanFunciones Oxigenadasdavid cadillo varillasBelum ada peringkat
- Practica #10 Reacciones de Los Carbohidratos y GlucidosDokumen9 halamanPractica #10 Reacciones de Los Carbohidratos y GlucidosDanni Mayorga MoralesBelum ada peringkat
- Mapa Conceptual Equilibrio Quimico AlexaDokumen1 halamanMapa Conceptual Equilibrio Quimico AlexaAlexis Jose Guarecuco0% (1)
- Reacciones de AlcanosDokumen8 halamanReacciones de AlcanosArturo GarciaBelum ada peringkat
- Quimica Relacion Con La Ingenieria AgroindustrialDokumen10 halamanQuimica Relacion Con La Ingenieria AgroindustrialAntonio Venegas50% (6)
- Tarea para Entrega 2 de Marzo 2012Dokumen9 halamanTarea para Entrega 2 de Marzo 2012sarevakBelum ada peringkat
- Química orgánica: alcanos, alquenos y sus propiedadesDokumen18 halamanQuímica orgánica: alcanos, alquenos y sus propiedadesjocrirojBelum ada peringkat
- Actividades Previas Eq1 P3Dokumen19 halamanActividades Previas Eq1 P3Mitzi De la Rosa HerreraBelum ada peringkat
- Hidro AlifaDokumen23 halamanHidro AlifaIvan Quispe HuaynaBelum ada peringkat
- Propiedades de Los Hidricarburos Saturados e InsaturadosDokumen5 halamanPropiedades de Los Hidricarburos Saturados e InsaturadosbenjaminBelum ada peringkat
- Investigacion de Los AlcanosDokumen14 halamanInvestigacion de Los AlcanosAremi Sireth Gordillo CastañedaBelum ada peringkat
- Trabajo Practico Sistema RespiratorioDokumen14 halamanTrabajo Practico Sistema RespiratorioAnalía Cristadulaquis100% (1)
- Himno Nacional Argentino (Completo)Dokumen3 halamanHimno Nacional Argentino (Completo)Analía CristadulaquisBelum ada peringkat
- Trabajo Práctico GeografíaDokumen8 halamanTrabajo Práctico GeografíaAnalía CristadulaquisBelum ada peringkat
- Precauciones de Seguridad Al Manipular Fibra ÓpticaDokumen1 halamanPrecauciones de Seguridad Al Manipular Fibra ÓpticaAnalía CristadulaquisBelum ada peringkat
- Monografia La CapacitaciónDokumen17 halamanMonografia La CapacitaciónAnalía CristadulaquisBelum ada peringkat
- 1 CarneDokumen39 halaman1 CarneGabriela NarvaezBelum ada peringkat
- Tema 5. BiomoléculasDokumen27 halamanTema 5. BiomoléculasAlmudena Estevez AlvarezBelum ada peringkat
- AlcoholesDokumen22 halamanAlcoholesPatricio Gutierrez MelgarejoBelum ada peringkat
- Corsino GRDokumen157 halamanCorsino GRDelfino Qquehue Maccapa100% (1)
- Tecnología de CarnesDokumen18 halamanTecnología de CarnesJavier Palermo Maita NoelBelum ada peringkat
- CHEMADokumen1 halamanCHEMARojas Iquiapaza ZafariBelum ada peringkat
- Manual de Prácticas de Química HeterocíclicaDokumen41 halamanManual de Prácticas de Química HeterocíclicaJos eBelum ada peringkat
- Ley Federal de Armas de Fuego y ExplosivosDokumen7 halamanLey Federal de Armas de Fuego y ExplosivosHugo Morales BeltránBelum ada peringkat
- Guia BioquimicaDokumen13 halamanGuia Bioquimicastephany RuizBelum ada peringkat
- Capitulo Del Libro. Estructura de Carbohidratos.Dokumen16 halamanCapitulo Del Libro. Estructura de Carbohidratos.Solorzano EnriqueBelum ada peringkat
- AnfoDokumen31 halamanAnfoEdson Isaac Mamani100% (2)
- 36 Travertino Clasico FichaDokumen7 halaman36 Travertino Clasico Fichafer4oca4a4hortalBelum ada peringkat
- Amoxi CompactadaDokumen5 halamanAmoxi CompactadaMarvin ZacariasBelum ada peringkat
- Pirolisis BasuraDokumen5 halamanPirolisis BasuraPAMELA MOLINA DELGADOBelum ada peringkat
- Determinación de ácido acético en vinagreDokumen17 halamanDeterminación de ácido acético en vinagreRosarioBelum ada peringkat
- Problemas Análisis de GrasasDokumen14 halamanProblemas Análisis de GrasasMaria Fernanda Espinosa OrtizBelum ada peringkat
- Investigue Los Tipos y Características de Las Tuberías Utilizadas en Los Circuitos HidráulicosDokumen12 halamanInvestigue Los Tipos y Características de Las Tuberías Utilizadas en Los Circuitos HidráulicosÓsmar SilvaBelum ada peringkat
- Propiedades de las disolucionesDokumen3 halamanPropiedades de las disolucioneselgema0% (1)
- 4 Espesores ANSI B3610Dokumen1 halaman4 Espesores ANSI B3610Maximiliano García Calderón100% (1)
- Materiales en Maquinaria Pesada Semana 3 T.D. N°2 Materiales No FerrososDokumen5 halamanMateriales en Maquinaria Pesada Semana 3 T.D. N°2 Materiales No FerrososDavid DiazBelum ada peringkat
- Suplementacion Con Hierro y MicronutrientesDokumen4 halamanSuplementacion Con Hierro y MicronutrientesCristhina Pérez100% (2)
- Estireno Guia de ManejoDokumen44 halamanEstireno Guia de Manejofernando estrada riosBelum ada peringkat
- Aldehidos Aldehidos QuimicaDokumen7 halamanAldehidos Aldehidos QuimicaSergio A LopezBelum ada peringkat
- Construccio CompositesDokumen34 halamanConstruccio CompositesElber CabezasBelum ada peringkat
- Legislacion de Prevencion Semana 4 (Trabajo)Dokumen6 halamanLegislacion de Prevencion Semana 4 (Trabajo)dina arriagadaBelum ada peringkat
- Biogas Como Combustible Alternativo para Una Estufa y Un Motor de Un Cilindro Ciclo OttoDokumen100 halamanBiogas Como Combustible Alternativo para Una Estufa y Un Motor de Un Cilindro Ciclo OttoRoBinson ZuluagaBelum ada peringkat
- Cuestionario Quimica Analitica 2Dokumen29 halamanCuestionario Quimica Analitica 2ttattalittaBelum ada peringkat
- Gas de Purga INTERPURGE-Catalog208-SpanishDokumen24 halamanGas de Purga INTERPURGE-Catalog208-SpanishrobertBelum ada peringkat
- Enlaces AtómicosDokumen34 halamanEnlaces AtómicosBastian Alvarez Gübelin100% (19)