Bab Iii
Diunggah oleh
Fitriani Indah LestariJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Bab Iii
Diunggah oleh
Fitriani Indah LestariHak Cipta:
Format Tersedia
BAB III
METODOLGI PERCOBAAN
3.1 Bahan Percobaan
3.1.1 Glukosa (C6H12O6)
Fungsi : Sebagai sampel percobaan
Tabel 3.1 Sifat Fisika dan Kimia Glukosa (C6H12O6)
Sifat Fisika
Sifat Kimia
1. Rumus molekul : C6H12O6
1. Mudah larut dalam air, asam asetat
dan pelarut lain
2. Massa molar : 180,16 g/mol
2. Hanya sedikit larut dalam etanol
3. Densitas
: 1,54 g/cm3
3. Berbentuk
rantai
terbuka,
termodinamika tidak stabil
4. Titik leleh : 146 oC
4. Tiga bentuk padat utama glukosa
dapat mengkristal menggunakan air
5. Kelarutan dalam air : 91 g/100 5. Isomer glukosa tunduk pada isomer
ml
rotasi
(MSDS, 2013a )
3.1.2 Maltosa (C12H22O11)
Fungsi : Sebagai sampel percobaan
Tabel 3.1 Sifat Fisika dan Kimia Maltosa (C12H22O11)
Sifat Fisika
1. Rumus molrkul : C12H22O11
2. Massa molar : 342,3 g/mol
3. Titik leleh : 102-105 oC
4. Densitas
: 1, 54g/cm3
5. Kelarutan dalam air :
g/100ml
(MSDS, 2012b)
Sifat Kimia
1. Terbentuk dari reaksi kondensasi
2. Memiliki rasa manis
3. Dihasilkan
ketika
amylase
memecah pati
4. Terbentuk dari dua uni glukosa
1,08 5. Dapat dihasilkan ketika glukosa
terbakar
3.1.3 Sukrosa (C12H22O11)
Fungsi : Sebagai sampel percobaan.
Tabel 3.3 Sifat Fisika dan Kimia Fruktosa (C6H12O6)
Sifat Fisika
Sifat Kimia
1. Rumus molekul : C12H22O11
1. Larut dalam air
2. Massa molar : 342,2 g/mol
2. Berbentuk padatan
3. Densitas : 1,587 g/cm3
3. Larut dalam alcohol
4. Kandungan dalam air : 0,05%
4. Tidak larut dalam dietil eter
5. Berwarna putih
5. Dapat menyebabkan iritasi
(MSDS, 2013c)
3.1.4 Air (H2O)
Fungsi : pelarut dalam membuat sampel larutan
Tabel 3.4 Sifat Fisika dan Kimia Air (H2O)
Sifat Fisika
1. Massa molar : 18,0153 g/mol
2. Densitas : 0,998 g/cm3
3. Titik lebur : 0 oC
4. Titik didih : 100 oC
5. Kalor jenis 4184 J/kg.K
(MSDS, 2012c)
Sifat Kimia
1. Isomer dari 2 - naftol
2. Lebih reaktif daripada fenol
3. Larut di dalam alkohol, eter dan
kloroform
4. Metabolit dari insektisida
carbonyl dan naftalena
5. Diproduksi oleh fusi dari 1 naftol
sulfonic asam
3.1.5
- naftol (C10H8O)
Fungsi : pelarut Molisch untuk sampel
Tabel 3.5 Sifat Fisika dan Kimia
naftol (C10H8O)
Sifat Fisika
Sifat Kimia
1. Rumus molekul : C10H8O
1. Isomer dari 2 - naftol
2. Massa molar : 144,17 g/mol
2. Lebih reaktif daripada fenol
3. Densitas : 1,10 g/cm3
3. Larut di dalam alkohol
4. Titik didih : 278-280 oC
4. Sedikit Larut dalam air
5. Titik leleh : 95-96 oC
5. Metabolit dari insektisida
carbonyl dan naftalena
(MSDS, 2012a)
3.1.6 Asam Sulfat (H2SO4)
Fungsi : Pelarut sampel.
Tabel 3.6 Sifat Fisika dan Kimia Asam Sulfat (H2SO4)
Sifat Fisika
1. Massa molar : 98,08 g/mol
Sifat Kimia
1. Merupakan cairan yang bersifat
higroskopis
2. Densitas : 1,84 g/cm3
2. Merupakan asam kuat
3. Keasaman : - 3
3. Bersifat korosif pada logam
4. Cairan bening, tidak berwarna, tidak 4. Merupakan asam bervalensi dua
berbau
5. Kelarutan penuh dalam air
5. Terurai dengan 95% etil alkohol
(MSDS, 2012b)
3.2 Peralatan Percobaan
1. Tabung reaksi
Fungsi : tempat direaksikannya sampel dan pelarut
2. Pipet tetes
Fungsi : untuk memindahkan larutan dalam skala kecil
3. Gelas ukur
Fungsi : untuk mengukur volume larutan
4. Penjepit tabung
Fungsi : untuk menjepit tabung reaksi
5. Ernlemeyer
Fungsi : sebagai tempat membuat larutan
6. Penjepit tabung
Fungsi : untuk menjepit tabung reaksi
7. Beaker gelas
Fungsi : wadah untuk membuat larutan
8. Neraca Analitik
Fungsi : untuk menimbang sampel
3.3 Prosedur Percobaan
1. Glukosa yang terbentuk padatan ditimbang hingga 1 gram, dilarutkan
kedalam 9ml air agar membentuk larutan glukosa 10% pada beaker gelas
2. Dimasukkan sebanyak 1ml glukosa 10% kedalam tabung reaksi
3. Kemudian ditambahkan 2 tetes larutan
naftol 5%
4. Ditambahkan 5 tetes H2SO4 pekat melalui dinding-dinding tabung
5. Terjadinya warna biru keungu-unguan menunjukkan adanya karbohidrat
6. Diulang prosedur 1 dengan menggunakan sampel maltose dan sukrosa
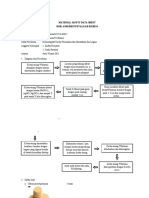
3.4 Flowchart percobaan
Mulai
1 ml larutan sampel dimasukkan ke dalam tabung reaksi
Ditambahkan 2 tetes larutan
naftol 5%
Dihomogenkan
Ditambahkan 5 tetes H2SO4 melalui dinding tabung reaksi
Apakah ada
sampel lain?
Ya
Tidak
Selesai
Gambar 3.1 Flowchart Percobaan Karbohidrat
Anda mungkin juga menyukai
- BAB III KualitatifDokumen12 halamanBAB III KualitatifTika Risyad100% (1)
- ASAM SULFATDokumen4 halamanASAM SULFATAnissa Trizakti Suwarman II100% (1)
- Iodin Padatan Biru-Hitam BermanfaatDokumen2 halamanIodin Padatan Biru-Hitam BermanfaatFachri Rachmat100% (2)
- MSDS ZNNO3Dokumen2 halamanMSDS ZNNO3rrrrrrrrrrrrrrrrrBelum ada peringkat
- MSDS Agno3Dokumen1 halamanMSDS Agno3Alzirhani RahmatBelum ada peringkat
- MSDS BROMTHYMOL BLUEDokumen2 halamanMSDS BROMTHYMOL BLUEErwan PrasetyaBelum ada peringkat
- MSDS Kalsium KarbonatDokumen7 halamanMSDS Kalsium KarbonatFanni BaytaBelum ada peringkat
- MATERIAL KESELAMATAN KALIUM FERRISIANIDADokumen4 halamanMATERIAL KESELAMATAN KALIUM FERRISIANIDAA.zhalzhabilla azzahrah AzzahrahBelum ada peringkat
- Bab I Identifikasi Gugus Fungsi AlkoholDokumen23 halamanBab I Identifikasi Gugus Fungsi AlkoholadlaBelum ada peringkat
- Sifat Fisika Kimia NaclDokumen2 halamanSifat Fisika Kimia NaclMohammadLabibGhiffaryBelum ada peringkat
- IDENTIFIKASI FECL2 DAN FESO4Dokumen4 halamanIDENTIFIKASI FECL2 DAN FESO4Nurma Erlita Damayanti100% (1)
- MSDS UyDokumen6 halamanMSDS UyLarasati DewiBelum ada peringkat
- Kalium PermanganatDokumen8 halamanKalium PermanganatFildzah AdanyBelum ada peringkat
- ASETONDokumen6 halamanASETONawaludinBelum ada peringkat
- Percobaan Viii (Reaksi Redoks)Dokumen34 halamanPercobaan Viii (Reaksi Redoks)Siti Jari Handayani100% (1)
- MSDS KASIUM KLORIDADokumen6 halamanMSDS KASIUM KLORIDAMfc FaridBelum ada peringkat
- MSDS KohDokumen4 halamanMSDS KohHalidazia LoloBelum ada peringkat
- MSDS StoikiometriDokumen6 halamanMSDS StoikiometriRifad KhoiranBelum ada peringkat
- AgNO3Dokumen14 halamanAgNO3Sheren thasya100% (1)
- Laporan Praktikum Pengenalan AnionDokumen19 halamanLaporan Praktikum Pengenalan AnionAuliaMukadisBelum ada peringkat
- Natrium oksalat: identifikasi, sifat, toksikologi, dan pertolongan pertamaDokumen10 halamanNatrium oksalat: identifikasi, sifat, toksikologi, dan pertolongan pertamaMuhammad SaepurrohmanBelum ada peringkat
- MSDS Bahan KimiaDokumen58 halamanMSDS Bahan KimiaVina ChusnaBelum ada peringkat
- Msds ManganDokumen6 halamanMsds ManganElsa ChaniaBelum ada peringkat
- MSDS Ch3coohDokumen7 halamanMSDS Ch3coohDhea Blossomz0% (1)
- Na NO3Dokumen5 halamanNa NO3M Nur M. MahmudBelum ada peringkat
- MSDS Ch3coohDokumen5 halamanMSDS Ch3coohFelba Rama AlbiansyahBelum ada peringkat
- MSDS Helmi (NaNO2 Dan Hidroksilamin Hidroklorida)Dokumen2 halamanMSDS Helmi (NaNO2 Dan Hidroksilamin Hidroklorida)Helmi FauziBelum ada peringkat
- 1. Sifat fisika dan kimia patiDokumen1 halaman1. Sifat fisika dan kimia patiRantyBelum ada peringkat
- Kalsium KhloridaDokumen7 halamanKalsium KhloridayutatsyBelum ada peringkat
- BAHAYA REAGEN DAN BAHAN KIMIA DALAM TINJAUAN PUSTAKADokumen2 halamanBAHAYA REAGEN DAN BAHAN KIMIA DALAM TINJAUAN PUSTAKAAprillia Trinanda KartikaBelum ada peringkat
- Msds - Asam Sulfat (H2so4)Dokumen3 halamanMsds - Asam Sulfat (H2so4)Tito Wahyu PerdanaBelum ada peringkat
- Ferri KloridaDokumen2 halamanFerri Kloridayusufluck100% (1)
- CaCO31Dokumen89 halamanCaCO31Jion No100% (3)
- MSDS Unit IiiDokumen19 halamanMSDS Unit IiiPotto EkaBelum ada peringkat
- MSDS KClDokumen2 halamanMSDS KClKholifatur RossyidahBelum ada peringkat
- ALUMINUM SULFAT SAFETY DATA SHEETDokumen4 halamanALUMINUM SULFAT SAFETY DATA SHEETOKTABelum ada peringkat
- Msds K2cro4Dokumen5 halamanMsds K2cro4Try Saputra100% (1)
- MSDS CuSO4 Versi Bhs IndonesiaDokumen6 halamanMSDS CuSO4 Versi Bhs IndonesiaIsmail NurBelum ada peringkat
- Msds Logam RinganDokumen27 halamanMsds Logam RinganFirdha Aulia Noor FadilahBelum ada peringkat
- Data Fisika Dan Kimia Dan MSDS HgCl2Dokumen3 halamanData Fisika Dan Kimia Dan MSDS HgCl2Asri LailaBelum ada peringkat
- Paper Tembaga (II) Sulfat (CuSO4)Dokumen14 halamanPaper Tembaga (II) Sulfat (CuSO4)Anggraghany Sanggrama WijayaBelum ada peringkat
- Msds NaftalenDokumen1 halamanMsds NaftalenCentri Cahya50% (2)
- Sifat BahanDokumen8 halamanSifat BahanRestia Eka PuspitaBelum ada peringkat
- DETOKS TIMBAL ASETATDokumen10 halamanDETOKS TIMBAL ASETATMutia Nurul OctaviaBelum ada peringkat
- MSDS MgSO4.7H20Dokumen3 halamanMSDS MgSO4.7H20Elisabeth HapsariBelum ada peringkat
- MSDS - Asam Asetat GlasialDokumen10 halamanMSDS - Asam Asetat GlasialAyu MurtiBelum ada peringkat
- Bab IiiDokumen3 halamanBab IiiYayangAfandyBelum ada peringkat
- Bab IiiDokumen3 halamanBab IiiTitaBelum ada peringkat
- METODOLOGI EKSPERIMENDokumen6 halamanMETODOLOGI EKSPERIMENramadhangilangBelum ada peringkat
- Modul Praktikum Biokimia 2020Dokumen10 halamanModul Praktikum Biokimia 2020Mutiara Alvionita TumananBelum ada peringkat
- Riky Setiawan-1908076005-Teknik Pemisahan SederhanaDokumen18 halamanRiky Setiawan-1908076005-Teknik Pemisahan SederhanaRicky SetiawanBelum ada peringkat
- SINTESIS ETIL ASETATDokumen14 halamanSINTESIS ETIL ASETATShabila LintangBelum ada peringkat
- KarbohidratDokumen12 halamanKarbohidratAsep Sef SyafrudinBelum ada peringkat
- Zahra Agustina - D - Benzoilasi Glukosa (LPKMR)Dokumen15 halamanZahra Agustina - D - Benzoilasi Glukosa (LPKMR)Zahra AgustinaBelum ada peringkat
- Judul PraktikumDokumen10 halamanJudul PraktikumDipsi HaechanBelum ada peringkat
- DETEKSI KARBOHIDRAT DENGAN UJI FEHLING DAN TOLLENSDokumen5 halamanDETEKSI KARBOHIDRAT DENGAN UJI FEHLING DAN TOLLENSwulanBelum ada peringkat
- Bab IiiDokumen7 halamanBab IiiDhian Kesuma SitorusBelum ada peringkat
- KROMATOGRAFIDokumen18 halamanKROMATOGRAFIRandi SitorusBelum ada peringkat
- HIDROLISE KARBOHIDRATDokumen11 halamanHIDROLISE KARBOHIDRATEma MuslimahBelum ada peringkat
- Syamsir Analisis Kualitatif KarbohidratDokumen19 halamanSyamsir Analisis Kualitatif KarbohidratSyamsirMBelum ada peringkat
- Lampiran A Tugas Khusus (Repaired)Dokumen20 halamanLampiran A Tugas Khusus (Repaired)Fitriani Indah LestariBelum ada peringkat
- Tugas TPBIDokumen22 halamanTugas TPBIFitriani Indah LestariBelum ada peringkat
- Bab Vi Utilitas Dan Pengolahan LimbahDokumen11 halamanBab Vi Utilitas Dan Pengolahan LimbahFitriani Indah LestariBelum ada peringkat
- Bab III Tinjauan PustakaDokumen9 halamanBab III Tinjauan PustakaFitriani Indah LestariBelum ada peringkat
- Tugas Produk Obat NyamukDokumen2 halamanTugas Produk Obat NyamukFitriani Indah LestariBelum ada peringkat
- Bab IiiDokumen7 halamanBab IiiFitriani Indah LestariBelum ada peringkat
- Kuliah 08Dokumen8 halamanKuliah 08Xanderz95Belum ada peringkat
- Kwitansi PembayaranDokumen1 halamanKwitansi PembayaranFitriani Indah LestariBelum ada peringkat
- Makalah Pengganti UASDokumen47 halamanMakalah Pengganti UASFitriani Indah LestariBelum ada peringkat
- Pengertian Industri KimiaDokumen2 halamanPengertian Industri KimiaFitriani Indah LestariBelum ada peringkat
- PERSAMAAN DIFERENSIAL BIASADokumen6 halamanPERSAMAAN DIFERENSIAL BIASAIdo Aprilian TariganBelum ada peringkat
- Makalah BAKOR Kelompok 4Dokumen24 halamanMakalah BAKOR Kelompok 4Fitriani Indah LestariBelum ada peringkat
- Kuliah 09Dokumen5 halamanKuliah 09Xanderz95Belum ada peringkat
- Kuliah 11Dokumen13 halamanKuliah 11Fitriani Indah LestariBelum ada peringkat
- Fatty Alkohol 3Dokumen3 halamanFatty Alkohol 3Walad WirawanBelum ada peringkat
- Pembuatan Bioetanol Dengan Bahan Baku Kulit DurianDokumen5 halamanPembuatan Bioetanol Dengan Bahan Baku Kulit DurianFitriani Indah LestariBelum ada peringkat
- Grafik 5 Dan 6Dokumen15 halamanGrafik 5 Dan 6Fitriani Indah LestariBelum ada peringkat
- Makalah Pengolahan LumpurDokumen14 halamanMakalah Pengolahan LumpurFitriani Indah Lestari100% (1)
- BAB II FlowchartDokumen6 halamanBAB II FlowchartFitriani Indah LestariBelum ada peringkat
- Absorpsi WWDokumen7 halamanAbsorpsi WWDwi ApriansyahBelum ada peringkat
- Makalah Mekanika Fluida Dan PartikelDokumen9 halamanMakalah Mekanika Fluida Dan PartikelFitriani Indah LestariBelum ada peringkat
- Daftar PustakaDokumen6 halamanDaftar PustakaFitriani Indah LestariBelum ada peringkat
- Bab I PendahuluanDokumen2 halamanBab I PendahuluanFitriani Indah LestariBelum ada peringkat
- Makalah Pengolahan LumpurDokumen14 halamanMakalah Pengolahan LumpurFitriani Indah Lestari100% (1)
- Grafik WordDokumen2 halamanGrafik WordFitriani Indah LestariBelum ada peringkat
- AbsorpsiDokumen68 halamanAbsorpsiFitriani Indah LestariBelum ada peringkat
- ATK Kelompok VDokumen10 halamanATK Kelompok VFitriani Indah LestariBelum ada peringkat
- Pengertian Industri KimiaDokumen2 halamanPengertian Industri KimiaFitriani Indah LestariBelum ada peringkat
- Penghampiran NumerikDokumen12 halamanPenghampiran NumerikFitriani Indah LestariBelum ada peringkat
- Isi LaporanDokumen19 halamanIsi LaporanFitriani Indah LestariBelum ada peringkat