Reacciones de Eliminacion
Diunggah oleh
Ricardo0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
139 tayangan4 halamanacerca de las reacciones de eliminacion
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Iniacerca de las reacciones de eliminacion
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
139 tayangan4 halamanReacciones de Eliminacion
Diunggah oleh
Ricardoacerca de las reacciones de eliminacion
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 4
Reacciones de Eliminacion
En qumica orgnica, una reaccin de eliminacin es el proceso inverso a
una reaccin de adicin. Es una reaccin orgnica en la que
dos sustituyentes son eliminados de una molcula, crendose tambin
una insaturacin, ya sea un doble o triple enlace, o un anillo. En el caso
particular de que los dos grupos sean eliminados de un mismo centro el
resultado sera un carbeno :CR2.
Las reacciones de eliminacin ms importantes son aquellas en las que los
dos grupos que se eliminan estn situados en tomos adyacentes, dando
lugar a una nueva insaturacin en la forma de un alqueno, un alquino o
un carbonilo.
Eliminacion unimolecular
La eliminacin unimolecular o E1 tiene lugar sobre derivados alqulicos
secundarios o terciarios segn un mecanismo de dos tapas. En la primera
se produce la salida del grupo saliente para formar el carbocatin y a
continuacin la prdida de un protn en para formar un doble enlace.
Eliminacion bimolecular
La eliminacin bimolecular o E2 consiste en un mecanismo concertado de
abstraccin de un protn por parte de una base fuerte y la salida simultnea
de un grupo saliente situado en , en el carbono contiguo, formndose una
insaturacin (doble enlace).
Sustitucion contra eliminacin
Cuando los halogenuros de alquilo se tratan con un nucleofilo, pueden sufrir ya
sea sustitucion o eliminacion. Son muchos los factores que influyen en la
competencia: disolvente, naturaleza del nucleofilo, estructura del halogenuro de
alquilo y condiciones de reaccin. El factor mas importante para determinar que va
a ocurrir suele ser la estabilidad del alqueno que se podria formar por eliminacion
en caso de que sta predomine. La estabilidad de los alquenos aumenta con el
numero de sustituyentes alquilo. Debido a que un halogenuro terciario esta mas
altamente sustituido que uno primario, ordinariamente forma un alqueno mas
altamente sustituido. Por lo tanto los halogenuros terciarios tienen tendencia
mayor hacia la eliminacion, puesto que forman alquenos muy estables.
Sustitucion electrofila aromatica
La sustitucin electrfila aromtica (SEAr) es una reaccin , en el curso de la cual
un tomo, normalmente hidrgeno, unido a un sistema aromtico es sustituido por
un grupo electrfilo. Esta es una reaccin muy importante en qumica orgnica,
tanto dentro de la industria como a nivel de laboratorio. Permite
preparar compuestos aromticos sustituidos con una gran variedad de grupos
funcionales segn la ecuacin general:
ArH + EX ArE + HX
donde Ar es un grupo arilo y E un electrfilo.
La primera etapa del mecanismo es una adicin en el curso de la cual el
compuesto electrfilo reacciona con un par de electrones del sistema
aromtico, que en el caso ms simple es benceno. Esta etapa necesita
generalmente ser catalizada con un cido de Lewis. Esta adicin conduce a
la formacin de un carbocatin ciclohexadienilo, (catin arenio o intermedio
de Wheland). Este carbocatin es inestable, debido a la presencia de la
carga sobre la molcula y a la prdida de la aromaticidad. Esto es en parte
compensado por la deslocalizacin de la carga positiva por resonancia.
En el transcurso de la segunda etapa la base conjugada del cido de Lewis,
(o un anin presente en el medio de reaccin), arranca el protn (H+) del
carbono que haba sufrido el ataque del electrfilo, y los electrones que
comparta el tomo de hidrgeno vuelven al sistema recuperndose la
aromaticidad.
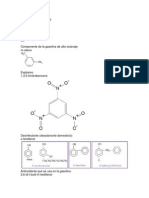
Principales sustituciones aromaticas
La halogenacin aromtica con bromo o cloro conduce a los
correspondientes haluros de arilo usando como catalizadores haluros de
hierro (FeX3) o de aluminio (AlX3).
La nitracin aromtica para formar compuestos nitro aromticos tiene lugar
mediante la generacin de un ion nitronio (NO2+) a partir de cido
ntrico y cido sulfrico.
La sulfonacin aromtica del benceno con cido sulfrico fumante produce
cido bencenosulfnico.
La reaccin de Friedel-Crafts en sus dos versiones de alquilacin y
acilacin. Teniendo como reactivos respectivamente haluros de
alquilo o haluros de acilo (tambin conocidos como haluros de cido o
haluros de alcanolo). Habitualmente el cloruro de aluminio (AlCl3) es
el catalizador.
Sustitucion nucleofila aromatica
Una sustitucin nuclefila aromtica es un tipo de reaccin de sustitucin
nuclefila en la que el nuclefilo desplaza a un buen grupo saliente, como
un haluro, en un anillo aromtico.
Esta reaccin, con este mecanismo, en el que el nuclefilo se adiciona a la
posicin del grupo saliente, el cual a continuacin es eliminado
recuperndose la aromaticidad, es la que se ha quedado con el nombre de
sustitucin nuclefila aromtica (SNAr). Tiene lugar si existen grupos
fuertemente atractores de electrones, tpicamente grupos nitro (-NO2), en
las posiciones orto y para al grupo saliente. Esto tiene dos efectos:
consigue que el anillo sea menos rico en electrones, por tanto ms
susceptible a los ataques nuclefilos, y la estabilizacin por resonancia de
la carga negativa del anin ciclohexadienilo intermedio. Esto hace que en
cambio sean anillos aromticos desactivados frente a la SEAr. Este es el
caso tambin de un compuesto heteroaromtico -deficiente como
la piridina, que est desactivada frente a la SEAr, pero que da reacciones
de SNAr fcilmente.
Mecanismo de eliminacin-adicin (va bencino):
Sobre un haluro de arilo, la base fuerte arranca el protn contiguo al grupo
saliente, producindose, a travs de un anin fenilo intermedio ([C6H4-X]),
la eliminacin de HX, lo que conduce al bencino. El bencino es inestable, de
tal modo que inmediatamente el nuclefilo se adiciona por cualesquiera de
ambos extremos de igual reactividad del triple enlace, dando lugar al
producto.
A travs de sales de diazonio aromticas:
Las sales de diazonio aromticas, derivadas de la correspondiente anilina,
son relativamente estables a baja temperatura, (bao de hielo, 0 C),
debido a la estabilizacin por resonancia. Al subir la temperatura se
libera nitrgeno y se forma el catin arlico, que inmediatamente reacciona
con cualquier nuclefilo presente.
Anda mungkin juga menyukai
- Presentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaDokumen47 halamanPresentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaAna Belen ZuritaBelum ada peringkat
- RESUMENDokumen7 halamanRESUMENSalma MedinaBelum ada peringkat
- Sintesis de MetadinitrobencenoDokumen16 halamanSintesis de Metadinitrobencenojeremias75% (4)
- Bolas Contra Las PolillasDokumen7 halamanBolas Contra Las PolillasvictormmcBelum ada peringkat
- Halogenacion JuankDokumen14 halamanHalogenacion JuankSantiago Nuñez JimenezBelum ada peringkat
- Capitulo 3 Sustitucion ElectrofilicaDokumen9 halamanCapitulo 3 Sustitucion ElectrofilicaCarmen Marisol Rufino SegoviaBelum ada peringkat
- Las Reacciones de EliminaciónDokumen60 halamanLas Reacciones de EliminaciónLu-ann Belén Valenzuela RojoBelum ada peringkat
- Tarea Clase 13 - 10 - 2021Dokumen6 halamanTarea Clase 13 - 10 - 2021Romel Esteban ReyesBelum ada peringkat
- Teoría Qo 05 Mat Abr.23 2023-IDokumen24 halamanTeoría Qo 05 Mat Abr.23 2023-IAlvaro CotrinaBelum ada peringkat
- Folleto de Hidrocarburos Aromaticos 2022Dokumen24 halamanFolleto de Hidrocarburos Aromaticos 2022EDUARDO JOSUE BLANDON LARGAESPADABelum ada peringkat
- AromaticidadDokumen32 halamanAromaticidadAlex Sotelo ContrerasBelum ada peringkat
- Sustitución Electrofílica AromáticaDokumen28 halamanSustitución Electrofílica AromáticaVictoria Daniela Quisberth Bautista50% (2)
- MentoríaDokumen27 halamanMentoríaPercy PaucarBelum ada peringkat
- Sintesis y Reactividad de Compuestos Aroma Ti CosDokumen36 halamanSintesis y Reactividad de Compuestos Aroma Ti CosGvillermo OviedoBelum ada peringkat
- Aromaticidad Del BencenoDokumen10 halamanAromaticidad Del BencenoMiranda DanielBelum ada peringkat
- El Mecanismo de La Sustitución Electrófila AromáticaDokumen28 halamanEl Mecanismo de La Sustitución Electrófila AromáticaNellyGarciaSuarezBelum ada peringkat
- Eliminación de Primer OrdenDokumen15 halamanEliminación de Primer OrdenValeria cBelum ada peringkat
- Resumen Aromaticos PDFDokumen14 halamanResumen Aromaticos PDFManuel EhuanBelum ada peringkat
- Sintesis y Reactividad de Compuestos Aroma Ti CosDokumen35 halamanSintesis y Reactividad de Compuestos Aroma Ti Coschicharoo21Belum ada peringkat
- INFORMEDokumen6 halamanINFORMEjuanBelum ada peringkat
- Sustituciòn Electrofilica AromaticaDokumen10 halamanSustituciòn Electrofilica Aromaticathelma orellanaBelum ada peringkat
- Tema 4Dokumen14 halamanTema 4LUCIA RODRIGO FLORESBelum ada peringkat
- Tema Quimica Organica 1Dokumen15 halamanTema Quimica Organica 1Francisco José Pardo JusticiaBelum ada peringkat
- Introducción A Los Mecanismos de ReacciónDokumen38 halamanIntroducción A Los Mecanismos de ReacciónElmer Ivan MamaniBelum ada peringkat
- Reacciones de Comp. AromaticosDokumen19 halamanReacciones de Comp. AromaticosOscar Soto RuizBelum ada peringkat
- Aldehídos y Cetonas 2022Dokumen18 halamanAldehídos y Cetonas 2022eliana vegaBelum ada peringkat
- Sustitución Electrofilica AromáticaDokumen29 halamanSustitución Electrofilica AromáticaAdrian Alberto López CenBelum ada peringkat
- Reacciones de Sustitucion en H. SaturadosDokumen7 halamanReacciones de Sustitucion en H. SaturadosFrank RodgersBelum ada peringkat
- Previo de Obtención de Acido PicricoDokumen10 halamanPrevio de Obtención de Acido PicricoCarlos CastilloBelum ada peringkat
- Halogenuros de AlquiloDokumen33 halamanHalogenuros de AlquiloOscar AriasBelum ada peringkat
- Cap7Parte3 Reactividad Alquenos Alquinos DienosDokumen50 halamanCap7Parte3 Reactividad Alquenos Alquinos DienosSamuel Espinoza GarciaBelum ada peringkat
- Reacciones de Haluros de AlquiloDokumen14 halamanReacciones de Haluros de AlquiloRicardo0% (1)
- Alquenos y AlquinosDokumen7 halamanAlquenos y AlquinosJesúsHenriquezBelum ada peringkat
- Informe Organica 12Dokumen3 halamanInforme Organica 12Anthony Josue Pope GuidoBelum ada peringkat
- Reacciones QuímicasDokumen6 halamanReacciones QuímicasJavier GarciaBelum ada peringkat
- HIDROCARBURODokumen14 halamanHIDROCARBUROmiguelBelum ada peringkat
- BencenoDokumen2 halamanBencenoestefany villcaBelum ada peringkat
- Activantes y DesactivantesDokumen7 halamanActivantes y DesactivantesEvelin ChandiBelum ada peringkat
- Reacciones AromaticasDokumen24 halamanReacciones AromaticasMirthza Aguilar YeBelum ada peringkat
- Química Orgánica I Sustitucion Nucleofilica AromaticaDokumen8 halamanQuímica Orgánica I Sustitucion Nucleofilica AromaticaClaudiaBelum ada peringkat
- Nitracion Del BencenoDokumen45 halamanNitracion Del Benceno2584862Belum ada peringkat
- Previo - Obtención Del Ácido PicricoDokumen15 halamanPrevio - Obtención Del Ácido PicricoDisco17Belum ada peringkat
- T2 - U4 Rodriguez Perez Norma AlejandraDokumen28 halamanT2 - U4 Rodriguez Perez Norma AlejandraAlejandra rodriguezBelum ada peringkat
- TAREA QUÍMICA ORGANICA LLDokumen7 halamanTAREA QUÍMICA ORGANICA LLMiriam Yaneth Aangeles QuiiterioBelum ada peringkat
- Sustitución Nucleofílica Aromática Halogenuros de AriloDokumen12 halamanSustitución Nucleofílica Aromática Halogenuros de AriloWendy Olmos100% (2)
- Reducción de Ácidos CarboxílicosDokumen17 halamanReducción de Ácidos CarboxílicosJorge Mario Fernandez PeñaBelum ada peringkat
- Departamento de Química Laboratorio de Química OrgánicaDokumen8 halamanDepartamento de Química Laboratorio de Química OrgánicaMelviisaBelum ada peringkat
- Sustitucion Electrofilica AromaticaDokumen20 halamanSustitucion Electrofilica AromaticaEzequiel HernándezBelum ada peringkat
- Haluros de Arilo RealDokumen10 halamanHaluros de Arilo RealAnDreBelum ada peringkat
- Explicación Experimento No. 1. Alquilación de Friedel y CraftsDokumen7 halamanExplicación Experimento No. 1. Alquilación de Friedel y CraftsPAULINA PEREZ CAMPOSBelum ada peringkat
- Tema Quimica Organica 2Dokumen43 halamanTema Quimica Organica 2Francisco José Pardo JusticiaBelum ada peringkat
- Mecanismos de Reacción-2015Dokumen45 halamanMecanismos de Reacción-2015Yosef Camposano RodriguezBelum ada peringkat
- ExpoDokumen12 halamanExpobahena aguilar marthaBelum ada peringkat
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaDari EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaPenilaian: 5 dari 5 bintang5/5 (1)
- QO-Alcanos-HalurosDokumen33 halamanQO-Alcanos-HalurosSOFIA GERALDINE VACA CACERESBelum ada peringkat
- Historia de La Química OrganometálicaDokumen15 halamanHistoria de La Química OrganometálicaJuan Gabriel FernándezBelum ada peringkat
- Efecto Inductivo Mesomerico EtcDokumen77 halamanEfecto Inductivo Mesomerico EtcMario Leonardo Guevara EscalanteBelum ada peringkat
- Programas de Estudio 2023 - FCQ UnaDokumen18 halamanProgramas de Estudio 2023 - FCQ UnaRossana DuarteBelum ada peringkat
- Anexo 1 - Tarea 1 - Pretarea - ContextualizaciónDokumen10 halamanAnexo 1 - Tarea 1 - Pretarea - Contextualizaciónmedicalsur 3mBelum ada peringkat
- Los AlquinosDokumen5 halamanLos AlquinosEdris CompresBelum ada peringkat
- Classgap DocDokumen5 halamanClassgap DocAbigail GallardoBelum ada peringkat
- Quimica 11 Elmer Arenas RiosDokumen4 halamanQuimica 11 Elmer Arenas RioscalosraBelum ada peringkat
- Tema 12. Problemas PDFDokumen14 halamanTema 12. Problemas PDFRossy MoralBelum ada peringkat
- Alcohol EsDokumen20 halamanAlcohol EsjanssenBelum ada peringkat
- Cuestionario P1 - Palacios Cabrera Moises - Tecno EnzimaticaDokumen1 halamanCuestionario P1 - Palacios Cabrera Moises - Tecno EnzimaticaMoises PcBelum ada peringkat
- Práctica 5. Reaccion SEAr Síntesis de P-Nitroacetanilida PDFDokumen2 halamanPráctica 5. Reaccion SEAr Síntesis de P-Nitroacetanilida PDFCarlos Alfonso RicaurteBelum ada peringkat
- Clase Aromaticos FullDokumen54 halamanClase Aromaticos FullAndres SernaBelum ada peringkat
- Alcoholes 2º ..-11-2021Dokumen38 halamanAlcoholes 2º ..-11-2021Fabián MontielBelum ada peringkat
- Introduccion A La Quimica Organica Cuarto de SecundariaDokumen7 halamanIntroduccion A La Quimica Organica Cuarto de SecundariaMilagros FabianBelum ada peringkat
- Derivados HalogenadosDokumen3 halamanDerivados HalogenadosDiego Muñoz ArellanoBelum ada peringkat
- Preguntas Organica 21Dokumen4 halamanPreguntas Organica 21Lina Yazmin Arevalo ParraBelum ada peringkat
- Listado de Productos QuimicosDokumen54 halamanListado de Productos QuimicosSilvia Aguayo GarciaBelum ada peringkat
- Al Can Os Completo 1Dokumen59 halamanAl Can Os Completo 1Daniel JoeBelum ada peringkat
- 4IV53 EQ6 Ac - SulfanilicoDokumen21 halaman4IV53 EQ6 Ac - SulfanilicoPaolaBelum ada peringkat
- Taller Sem 5-11Dokumen6 halamanTaller Sem 5-11Ilian Gabriela ForeroBelum ada peringkat
- Clase Polimerización Por PasosDokumen22 halamanClase Polimerización Por PasosJenniffer KanocBelum ada peringkat
- Ganodema Lucidum El Hongo de La InmortalidadDokumen40 halamanGanodema Lucidum El Hongo de La InmortalidadFélix Alexei Alvarado SotolongoBelum ada peringkat
- Hidrocarburos Aromaticos MEDRANODokumen20 halamanHidrocarburos Aromaticos MEDRANOJhonn ChoqueBelum ada peringkat
- Reacciones de Las AminasDokumen7 halamanReacciones de Las AminasKaren Patricia Polo LozanoBelum ada peringkat
- Taller Químico Del Carbono 1Dokumen4 halamanTaller Químico Del Carbono 1vmin patronesBelum ada peringkat
- PT Química Sem 10 Sesión 19 2022 2 RMDokumen43 halamanPT Química Sem 10 Sesión 19 2022 2 RMValeria EgoavilBelum ada peringkat
- Quimica 11 Guia 3Dokumen7 halamanQuimica 11 Guia 3MARIA VALENTINA ARANA VASQUEZBelum ada peringkat
- 11º Guía 25 Hidrocarburos de Cadena Cerrada - Cicloalquinos DDokumen2 halaman11º Guía 25 Hidrocarburos de Cadena Cerrada - Cicloalquinos DLiliana HernándezBelum ada peringkat
- Informe IX. SINTESIS DEL ACIDO FORMICODokumen3 halamanInforme IX. SINTESIS DEL ACIDO FORMICOChiquinquira AnguloBelum ada peringkat