Seminario 5: Mecanismos de Evasión de La Respuesta Inmune
Diunggah oleh
Juan José Gómez ToscanelliHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Seminario 5: Mecanismos de Evasión de La Respuesta Inmune
Diunggah oleh
Juan José Gómez ToscanelliHak Cipta:
Format Tersedia
USMP - Facultad de Medicina Humana
SAN MARTIN DE PORRES
FACULTAD DE MEDICINA
SEMINARIO DE INMUNOLOGA
MECANISMOS DE EVASION DE LA RESPUESTA INMUNE
2015 II
INTEGRANTES
:
Gmez Toscanelli Juan
Jos
Malca Flores Claudia
Alejandra
Ramirez Estela Katerin
DOCENTE
:
Dr. Llimpen
SECCIN
:
04C
USMP - Facultad de Medicina Humana
PIMENTEL, Septiembre del 2015
USMP - Facultad de Medicina Humana
INTRODUCCIN
La mayora de los microorganismos infecciosos no logran ingresar al individuo, gracias
a las barreras fsicas y qumicas que ste presenta. La barrera fsica ms importante es la
piel; la integridad de sta, junto a la secrecin de mediadores qumicos, evita el ingreso
de microorganismos patgenos. Asimismo, las mucosas poseen una serie de atributos
(secreciones, flujo ciliar) que dificultan el ingreso de microorganismos por esa va.
Adems, la existencia de poblaciones microbianas no patgenas residentes (flora
normal), tambin impide la colonizacin de las mucosas por agentes infecciosos. La
mayora de los microorganismos que logran evadir estas barreras y producir infeccin,
son destruidos en pocas horas por mecanismos no especficos de induccin rpida
(inmunidad innata). Sin embargo, si un agente infeccioso es capaz de superar esas
primeras lneas de defensa, se activar, en la mayora de los casos, un tipo de respuesta
de defensa (inmunidad adaptativa), altamente especializada y especfica. sta lograr,
en la mayora de las situaciones, controlar la infeccin y suprimir la enfermedad. Pero
en algunos casos ciertos patgenos logran evadir la respuesta inmune del hospedero
mediante diversos factores, favorecindose as de este y en algunos casos destruyendo
tejidos o viviendo a expensas de este.
USMP - Facultad de Medicina Humana
I.
II.
OBJETIVOS
Conocer mecanismos de evasin de la respuesta inmune de algunos patgenos y
los procesos que involucra.
Conocer que tipos de bacterias, helmintos y patgenos de mayor importancia
clnica y cada uno de sus mecanismos de evasin.
MARCO TERICO
Los agentes infecciosos se han adaptado de la manera ms conveniente para su propia
supervivencia, desarrollando sofisticados sistemas de evasin de las respuestas
protectivas del hospedador. As, ciertos parsitos intracelulares facultativos,
especialmente protozoos y bacterias, estn protegidos de gran parte de los sistemas
efectores inmunes, debido a su localizacin intracelular y aunque la clula hospedadora
puede expresar Ags del parsito en su membrana, stos, de hecho, no suelen
desencadenar una respuesta inmune protectiva frente a las clulas infectadas, a
diferencia de lo que ocurre con infecciones virales.
Otros muchos parsitos han desarrollado diversas estrategias para evitar el
reconocimiento antignico del cual dependen todos los mecanismos inmunolgicos:
mimetismo, debido a la absorcin de protenas del hospedador o por imitacin de las
protenas de superficie del hospedador; liberacin de Ags al medio bloqueando la
interaccin de los Acs con el microorganismo; cambio de Ags durante las diferentes
fases del desarrollo.
Las bacterias son parsitos y la evasin de las respuestas protectoras del hospedador
supone una ventaja selectiva. Lgicamente, cuanto mayor es el perodo en que una
infeccin bacteriana permanece en el hospedador, mayor es el tiempo del que las
bacterias disponen para proliferar y producir dao.
Por tanto, las bacterias que pueden evitar o inutilizar las defensas del hospedador
presentan una mayor capacidad potencial de produccin de enfermedad. Las bacterias
han desarrollado diversos mecanismos para eludir las principales defensas
antibacterianas, al eludir su reconocimiento y destruccin por las clulas fagocticas,
inactivar o evitar el sistema de complemento y anticuerpos, e incluso mediante la
proliferacin intracelular con el fin de esconderse de estas respuestas del hospedador.
USMP - Facultad de Medicina Humana
III.
CUESTIONARIO
1. Cules son los principales mecanismos de evasin de la respuesta inmune que
usan los patgenos?
Defensas microbianas frente a los mecanismos inmunolgicos del hospedador:
Encapsulacin
Mimetismo antignico
Enmascaramiento antignico
Cambio antignico
Produccin
de
proteasas
antiinmunoglobulinas
Destruccin de los fagocitos
Inhibicin de la quimiotaxis
Inhibicin de la fagocitosis
Inhibicin de la fusin fagolisosmica
(Salmonella,
M.
tuberculosis,
Chlamydia)
Resistencia a las enzimas lisosomales
Replicacin intracelular
USMP - Facultad de Medicina Humana
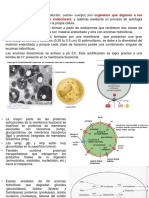
2. Por qu algunos parsitos prefieren quedarse en el citoplasma de los
macrfagos?
Los parsitos, que son considerados cualquier microorganismo que vive a expensas de
un husped, en algunos casos; cundo invaden a una clula, lo que hacen es primero
hacer que la clula lo fagocite; y vivir en el citoplasma; cuando se encuentra en el
lisosoma; la bacteria rompe esto y dentro del citoplasma realiza su reproduccin;
entonces esto quiere decir que si no se produce la unin del fagosoma y el lisosoma; el
microorganismo no va a ser presentado por la APC y por ende no habr activacin del
Sistema Inmune adaptativo, adems si una bacteria prefiere mantenerse en el citoplasma
se debe a que no posee factores de virulencia para poder estar en este medio
extracelular.
3. Cmo se aprecia la supresin de la respuesta inmune del hospedador en beneficio
del patgeno?
A pesar de los variados dispositivos de proteccin que el hospedador elabora en contra
de la gran cantidad de antgeno que el parsito presenta, este es capaz de sobrevivir por
largo tiempo utilizando mecanismos de evasin que han desarrollado a lo largo de su
existencia. La cronicidad de las infecciones parasitarias es una indicacin de que el
sistema inmune (SI) es incapaz de erradicar al parsito, y esto se debe a que el invasor
posee los instrumentos para eludir la respuesta inmune (RI). En algunas parasitosis se
conocen las bases moleculares de la evasin inmune, como en la tripanosomiasis
Africana y la malaria, mientras que en otras las evidencias son claras pero los
mecanismos se desconocen.
4. Cmo se aprecia las conversiones la respuesta inmune del hospedador en
beneficio del patgeno?
La infeccin por M. tuberculosis es un proceso complejo. Luego de la exposicin
inicial, el bacilo puede penetrar y replicarse dentro de los macrfagos no activados.
Subsecuentemente, la respuesta inmune del hospedero mediada por los linfocitos T
auxiliadores tipo I (Th1), con la liberacin de IL-12, IFN- TNF-, resulta en la
formacin del granuloma, tejido constituido por macrfagos y linfocitos que rodean un
rea central de necrosis. Otros estudios sealan la presencia del bacilo tuberculoso
latente, no slo en los macrfagos de los granulomas, sino tambin en las clulas
fagocticas no profesionales. De hecho M. tuberculosis se asla de biopsias de pulmn
con una apariencia normal.
El granuloma se caracteriza por poseer un ambiente hipxico, situacin responsable de
mantener bajos los niveles de replicacin bacteriana. As mismo, en su interior pueden
formarse lesiones necrticas que permiten la presencia de M. tuberculosis en el espacio
USMP - Facultad de Medicina Humana
extracelular, favorecindose la existencia de microambientes con reas anaerbicas. De
este modo, la adaptacin a los bajos niveles de oxgeno es un factor importante que
incrementa la capacidad de M. tuberculosis para persistir en el hospedero. Sin embargo,
el desarrollo de la necrosis no conduce necesariamente a la diseminacin y puede
proveer un ambiente que prevenga la transmisin y dispersin de la TB. En modelos
animales se demuestra que el TNF- desempea un papel esencial en la respuesta
inmune del hospedero contra la TB, incluyendo la formacin del granuloma y la
contencin de la enfermedad.
La mayor parte de los componentes estructurales de las micobacterias son de naturaleza
sacardica, estructuras reconocidas por diversos receptores en los macrfagos y otros
tipos celulares (linfocitos T). Algunas de estas estructuras moleculares de las
micobacterias son tambin responsables de los mecanismos de evasin de la respuesta
inmune del hospedero, pues son capaces de inhibir o interferir con los mecanismos
microbicidas del macrfago infectado.
El medio intracelular confiere ventajas importantes a las micobacterias debido a que
quedan protegidas de los mecanismos efectores de la respuesta inmune del hospedero,
como la lisis por el complemento; adems, las caractersticas estructurales de su
envoltura le proporcionan resistencia a los agentes microbicidas, a los frmacos y a la
destruccin por el calor . El establecimiento de la infeccin tambin depende de la
interaccin inicial entre los componentes de superficie de las micobacterias con los
receptores de la clula hospedera.
Al utilizar receptores como el CR3, la entrada de las micobacterias patgenas puede
inhibir los mecanismos microbicidas del macrfago, de manera que esta interaccin
inicial resulta crtica en la patognesis de la TB y en la persistencia de la bacteria en el
interior de la clula hospedera.
5. Cmo se aprecia la diversificacin de la respuesta inmune del hospedador en
beneficio del patgeno?
Los virus son parsitos intracelulares obligados, requiriendo de la maquinaria
metablica de una clula para replicarse. Su estructura bsica incluye un cido nucleico,
que puede ser DNA o bien RNA, rodeado por una envoltura proteica o cpsula que le
permite ingresar a las clulas. Una infeccin viral comprende una etapa extracelular y
una etapa intracelular, por lo tanto la respuesta inmune puede interferir con ellos en
estos
dos
niveles.
Los virus ingresan al organismo por diversas vas incluyendo la respiratoria, la
gastrointestinal, la transcutnea la genitourinaria y la rectal. Luego de ingresar, se
produce una etapa de replicacin primaria para luego diseminarse e introducirse en su
tejido blanco final. Las infecciones virales pueden ser lticas, latentes o persistentes. La
USMP - Facultad de Medicina Humana
respuesta inmune adquiere caractersticas y efectividad diferentes de acuerdo a la va de
ingreso
del
virus
y
al
tipo
de
infeccin
que
provoca.
La respuesta inmune en sentido amplio frente a estos microorganismos comprende
mecanismos inespecficos y especficos con caractersticas y efectividad particulares
que dependen de la naturaleza de cada virus. Entre los mecanismos inespecficos, los de
mayor relevancia incluyen la produccin de interfern tipo I, la presencia de clulas NK
y la activacin del complemento. La respuesta inmune adaptativa antiviral incluye
mecanismos efectores humorales y celulares, siendo estos ltimos los ms eficaces.
El organismo cuenta con una serie de elementos para impedir o dificultar el ingreso de
virus al organismo. As por ejemplo, en la va respiratoria, los virus deben sobrepasar el
efecto neutralizante de IgA secretora, la accin ltica de clulas NK y la funcin
fagoctica de macrfagos. En el sistema gastrointestinal existen una serie de elementos
que limitan la persitencia e ingreso de partculas virales. Entre ellos tienen importancia
el pH cido gstrico, las sales biliares, enzimas proteolticas e IgA secretora. En la piel,
el estrato crneo constituye una barrera fsica que es sobrepasada cuando los virus
ingresan mediante picaduras de insectos, mordida de animales o bien por el uso de
jeringas contaminadas. La transmisin sexual ha adquirido especial importancia a raz
del SIDA. En este caso, la mucosa y la IgA se oponen al ingreso del virus HIV.
Si los virus logran sobrepasar estas barreras, se ven enfrentados a diversas modalidades
de la respuesta inmunolgica cuya eficiencia depender de la etapa del ciclo infectivo
viral
en
que
acten.
En una fase precoz de la infeccin tiene importancia la actividad ltica de las clulas NK
las que lisan clulas infectadas por virus ya sea directamente o bien a travs del
mecanismo ADCC y la activacin del complemento por via alterna.
Ms adelante, los virus, al ser en general muy inmunognicos, estimulan respuestas T y
B. Los linfocitos T CD4+ reconocen pptidos virales en el contexto de molculas MHC
clase II en clulas presentadoras de antgeno ejerciendo su funcin cooperadora con
respuestas de linfocitos B y T CD8+. La respuesta celular en su modalidad citotxica es
la ms efectiva ya que los linfocitos T CD8+ activados, al reconocer pptidos
antignicos de origen viral en molculas MHC clase I en clulas infectadas por virus,
son
capaces
de
lisarlas
Los anticuerpos cumplen un papel relativamente pobre en las infecciones virales
agudas, sin embargo son importantes en la prevencin de reinfecciones. Los
anticuerpos, al unirse a epitopos presentes en protenas ubicadas en la superficie de la
partcula viral (anticuerpos neutralizantes), pueden reducir su infectividad. Esto lo
logran inhibiendo diversas etapas del ciclo reproductivo viral tales como unin a la
membrana celular y penetracin a la clula. Adems pueden producir agregados de
viriones, acelerar su degradacin en vesculas y facilitar su fagocitosis al opsonizarlos.
La activacin del complemento es otro mecanismo defensivo antiviral. Este sistema
puede ser activado por va clsica y alterna, conduciendo a la opsonizacin por C3b y a
la lisis de virus con cpsula o de clulas infectadas por virus. Su eficacia en el hombre
es sin embargo relativa, ya que pacientes deficientes en factores del complemento, no
presentan una mayor incidencia ni gravedad en infecciones de este tipo.
USMP - Facultad de Medicina Humana
Finalmente, durante la infeccin viral se induce la sntesis de protenas llamadas
interfern en las clulas del husped. El interfern es liberado al extracelular y acta
sobre clulas vecinas unindose a un receptor e induciendo la sntesis de una protena
kinasa que fosforila un factor de iniciacin de la sntesis protica. Mediante este
mecanismo, se interfiere con la sntesis de protenas virales. Adems el interfern activa
a endonucleasas que degradan el mRNA viral y estimulan a otras clulas que participan
en la respuesta inmune tales como celulas NK y linfocitos T citotxicos.
IV.
CONCLUSIONES
El sistema inmune permite que los individuos sobrevivan al contacto con
diferentes tipos de patgenos. Los mecanismos iniciales de defensa provistos
por la inmunidad innata permiten eliminar muchos de los agentes infecciosos
y sientan las bases para el desarrollo de una respuesta inmune adaptativa con
alto grado de especificidad por el patgeno que logra quebrar esa primer
lnea de defensa. Los mecanismos efectores relevantes para eliminar
distintos tipos de microorganismos, varan segn las caractersticas de
virulencia y patogenicidad de ste. La resolucin de una infeccin se
acompaa de la muerte de la mayora de las clulas efectoras y de la
generacin de clulas de memoria. Muchos microorganismos han
desarrollado sistemas que le permiten evadir la respuesta inmune.
El VIH utiliza diversos trucos para evadir las respuestas inmunitarias
montadas contra l. Una de las ventajas del virus es que ataca e infecta,
principalmente, a las clulas-T CD4, un componente bsico de la respuesta
inmunitaria adaptativa contra el VIH. La capacidad del virus para mutar de
manera constante le permite tambin evadir las respuestas de anticuerpos.
Sin embargo, an no se entiende por completo el modo en que el VIH
manipula el sistema inmunitario innato. Es posible que los macrfagos y las
clulas dendrticas estn ayudando involuntariamente al virus de la
inmunodeficiencia humana transportando partculas del mismo directamente
a sus clulas-T CD4 diana, a las que infecta con posterioridad. Tambin se
cree que el VIH afecta a otras funciones del sistema inmunitario innato,
incluyendo la capacidad funcional de un subgrupo de clulas, denominadas
clulas asesinas naturales, que, de otro modo, reconoceran y destruiran a las
clulas infectadas por el VIH.
USMP - Facultad de Medicina Humana
V.
RESUMEN DEL ARTCULO
La inmunidad innata es la primera lnea de defensa en la respuesta del husped a la
invasin viral. Las clulas que participan en la respuesta inmune innata incluyen
monocitos, macrfagos, clulas dendrticas, leucocitos y clulas natural killer (NK) que
estn equipadas con receptores para la deteccin de patgenos y estn presentes en el
hgado. En los pacientes infectados con virus de hepatitis B y C (HVB y HVC), el rasgo
caracterstico es la persistencia viral que adems constituye uno de los mayores
problemas. Como consecuencia de la enfermedad heptica crnica los pacientes pueden
evolucionar hacia la cirrosis o hepatocarcinoma. Los mecanismos de persistencia viral
son an desconocidos, pero se cree que en la mayora de los casos est involucrada una
deficiente respuesta inmune innata y/o adaptativa del husped. Para mantener el estado
de cronicidad algunos virus han desarrollado mecanismos especficos para evadir la
deteccin y activacin de las clulas natural killer (NK). Adems se ha propuesto que un
desbalance en la respuesta Th1/Th2 hacia un perfil Th2 en el sitio de replicacin viral,
sera uno de los mecanismos principales de evasin que favorecen la persistencia viral.
Los componentes de la inmunidad natural, innata o inespecfica estn presentes desde el
nacimiento, careciendo de especificidad y de memoria.
VI.
COMENTARIO
Las bacterias de por si van a seguir evolucionando y siempre habr una manera en la
cual ellas puedan sobrevivir, por lo cual si mecanismo de persistencia seguir y
evolucionar con el pasar el tiempo. Pero eso no quita el hecho de que debamos seguir
buscando nuevos mtodos de defensa frente a los nuevos mtodos de evasin de la
respuesta inmune frente a patgenos, helmintos o parsitos. Desarrollar nuevas terapias
preventivas y curativas para la deteccin de estos ser lo primordial.
VII.
BIBLIOGRAFIA
Raul Romero Cabello. Microbiologia y parasitologia humana : bases etiologicas
de las enfermedades infecciosas y parasitarias. Mexico : Medica Panamericana
Espaol (spa) : 3a , 2007. Disponible en :
https://books.google.com.pe/books?
id=Wv026CUhR6YC&pg=PA148&dq=mecanismos+de+evasion+de+la+respues
ta+inmune&hl=es419&sa=X&ved=0CDUQ6AEwBWoVChMIj6XO5aPjxwIVzI0NCh05Eg_d#v=one
page&q=mecanismos%20de%20evasion%20de%20la%20respuesta
%20inmune&f=false
USMP - Facultad de Medicina Humana
Mecanismos de evasin inmunitaria del Virus de Hepatitis C.
Revisin.
Leticia Porto-Espinoza, Csar Cuadra-Snchez, Reyna Moronta, Francisca
Monsalve-Castillo y Diana Callejas-Valero.
Laboratorio Regional de Referencia Virolgica, Facultad de Medicina, Universidad del
Zulia, Maracaibo, Venezuela. Correo electrnico: letiporto@yahoo.com
Resumen.
El virus de Hepatitis C (VHC) constituye un problema de salud pblica mundial. La
mayora de las infecciones se tornan crnicas, ocasionando con frecuencia cirrosis
heptica y carcinoma hepatocelular a largo plazo, precisndose no pocas veces de
transplantes hepticos para prolongar la vida del individuo. El mantenimiento de
una infeccin crnica implica la evasin al sistema inmunitario del hospedero. Los
mecanismos virales involucrados en dicha evasin estn siendo estudiados
arduamente con el fin de desarrollar nuevas terapias preventivas y curativas
efectivas contra el virus. Una caracterstica importante, la extrema variabilidad
gentica del virus, se cree que contribuya al escape inmunitario al cambiar
continuamente los eptopos expuestos a la deteccin; sin embargo, algunos
trabajos sugieren que no es necesaria para el establecimiento de la cronicidad de la
infeccin. Por otra parte, el estudio comparativo de la respuesta inmunitaria de los
pacientes que se recuperan espontneamente con la de aquellos infectados de
manera crnica, seala que algunas protenas virales podran inducir cierta
inmunosupresin indispensable para la persistencia en el hospedero.
Concretamente, se cree que las protenas NS5A, E2 y core modulan ciertos
mecanismos de las respuestas innata y especfica. El anlisis de los hallazgos
relacionados con el tpico permite sugerir la existencia de una sinergia entre la
variacin gentica y la inmunosupresin para evadir de manera continua la
deteccin y destruccin por parte del sistema de defensas del individuo.
Palabras clave: Virus de Hepatitis C, evasin inmunitaria, variacin gentica,
inmunosupresin viral.
Immune evasion mechanisms of Hepatitis C virus. Review.
Abstract.
Hepatitis Virus C (HCV) is a major worldwide health care problem. HCV infection
usually tends to become chronic and can generate long term hepatic cirrhosis and
hepatocellular carcinoma. These affections frequently require a liver transplant to
prolong the patients life. Maintenance of the chronic infection implies evasion of the
host immune responses. Viral mechanisms involved in this evasion are being
profusely studied in order to develop new and effective therapies and vaccines
against HCV. An important HCV characteristic, its high genetic variability, has been
proposed to contribute to immune evasion by means of antigenic change and
variation. On the other hand, some studies suggest that genetic variability is not
necessary to establish a chronic infection. Other studies related to immune
responses in patients with spontaneous virus clearance and patients with chronic
infection show a possible immunosuppression caused by some viral proteins, that
may be essential to persist in the host. Specifically, it is believed that viral proteins
USMP - Facultad de Medicina Humana
NS5A, E2 and Core modulate some innate and specific immune mechanisms. The
analysis of all data related to this topic suggests the existence of synergistic
cooperation between viral variation and immunosuppression to overcome the
immune defenses of the host.
Key words: Hepatitis
immunosuppression.
virus,
immune
evasion,
antigenic
variation,
viral
Recibido: 13-02-2004. Aceptado: 26-05-2005.
INTRODUCCIN
El Virus de Hepatitis C (VHC) es un flavivirus que tiene una distribucin mundial
(1). Su hospedero natural es el hombre en el que causa, cuando la infeccin se
cronifica, una enfermedad heptica progresiva que puede hacer necesario un
transplante de hgado (2). Los pacientes afectados crnicamente por este virus
necesitan cuidados permanentes y tienen un mayor riesgo que las personas sanas
de sufrir cirrosis heptica y carcinoma hepatocelular (3-5).
La Organizacin Mundial de la Salud (OMS) ha declarado al VHC como un problema
de salud pblica (6). Actualmente se encuentra infectando aproximadamente al 3%
de la poblacin mundial, es decir 170 millones de personas, de las cuales mueren
476.000 al ao por complicaciones en la fase final de la enfermedad heptica
crnica (7).
Especficamente en Venezuela, se ha sealado una prevalencia del 1% para la
poblacin general (8); sin embargo, en otros grupos de personas se puede
conseguir al VHC con mayor frecuencia (8, 9).
El VHC es el causante del 20% de todas las hepatitis agudas y gran cantidad de los
infectados (>85%) desarrolla una infeccin crnica (10, 11); la cual implica evasin
continua del sistema inmunitario del hospedero, sin embargo, al analizar las
caractersticas del ciclo de vida del VHC, se encuentran detalles atpicos en relacin
a otros virus generadores de infeccin crnica, como la ausencia de un periodo de
latencia (12), por el contrario en todo momento de la infeccin por VHC hay
produccin de nuevos viriones en mayor o menor grado. As pues, a pesar de
encontrarse expuesto a la deteccin por el sistema inmunitario, este virus logra la
mayora de las veces perpetuarse en su hospedero (13).
Para conseguir esto, el VHC ha desarrollado todo un sistema de evasin y supresin
del sistema inmunitario, que consta de sofisticados recursos, muchos de ellos no
estudiados del todo (14). Sin embargo, la variabilidad gentica del virus y la
alteracin de los patrones de respuesta inmunitaria parecen ser los dos factores
que contribuyen en mayor cuanta a la generacin de la cronicidad (15).
El conocimiento en detalle del ciclo biolgico del VHC, especialmente de estos
mecanismos de persistencia, es sumamente importante para desarrollar nuevas
terapias y vacunas que puedan prevenir y controlar esta afeccin (16). De hecho,
parte del tratamiento disponible actualmente, se basa en la potenciacin del
sistema inmunitario del individuo afectado mediante la administracin de Interfern
(17).
USMP - Facultad de Medicina Humana
CARACTERSTICAS DEL VHC
Como en todos los virus pertenecientes a la familia Flaviviridae, el genoma del VHC
est compuesto por una nica cadena lineal de ARN con sentido positivo (18). sta
tiene una longitud cercana a los 9,7 Kbp (19). El ARN viral se comporta como ARN
mensajero y su traduccin produce un precursor poliproteico de 3000 aminocidos
aproximadamente, a partir del cual, se generan las distintas protenas funcionales,
estructurales y no estructurales, por modificacin cotraduccional (12, 20).
Los genes estructurales: core (C) y envoltura (E1 y E2), estn localizados en la
zona prxima al extremo 5 del genoma, mientras que los genes no estructurales
(NS2, NS3, NS4A, NS4B, NS5A, NS5B) son adyacentes al extremo 3 (20). Los
extremos 5 y 3 son secuencias no codificantes (UTR, unstranlated region) de
secuencias muy conservadas entre diferentes cepas del virus (Fig. 1) (19, 21).
EL VHC se caracteriza por una gran variabilidad gentica (21). Se han descrito 6
genotipos diferentes de VHC (4). Las zonas con mas variacin estn ubicadas en la
porcin aminoterminal de la protena E2, en las zonas designadas como regin
hipervariable 1 y 2 (HVR1 y HVR2) (19, 20). En cada genotipo se han conseguido
un nmero variable de subtipos, que se denominan 1a, 1b, 2a, 2b, etc. (20).
En un paciente infectado, coexisten varias formas genmicas del VHC denominadas
cuasiespecies, las cuales se encuentran relacionadas entre s pero son ligeramente
diferentes en la secuencia de sus bases nitrogenadas (22). La aparicin de
cuasiespecies se debe a una caracterstica de la ARN polimerasa viral, su
incapacidad de corregir errores en la incorporacin de nucletidos durante el
proceso de replicacin, lo que facilita la aparicin de mutaciones puntuales (19,
23).
MARCADORES DEL CICLO DE VIDA DEL VHC
Uno de los aspectos ms relevantes del ciclo biolgico del VHC es su propensin a
generar una infeccin crnica (17). Usualmente, durante la etapa aguda de la
infeccin, se presentan pocos sntomas y los niveles de transaminasas suben (hasta
10 veces los valores normales) (23).
En el suero de los pacientes infectados es posible detectar ARN del VHC mediante la
reaccin en cadena de la polimerasa (PCR) a partir de siete das posteriores a la
infeccin (3). Los anticuerpos anti-VHC se presentan semanas despus
conjuntamente con el inicio de los sntomas (en caso de que aparezcan) (24). El
ARN viral permanece en niveles sricos detectables mientras exista replicacin, es
decir, durante unas semanas en los casos de hepatitis autolimitada y de manera
indefinida en los casos crnicos (25). Los ttulos de anti-VHC decrecen
progresivamente en los pacientes con hepatitis autolimitada y sern indetectables
USMP - Facultad de Medicina Humana
despus de unos aos. En los pacientes con hepatitis crnica perdurarn
indefinidamente (21).
DIVERSIDAD GENTICA COMO MECANISMO DE PERSISTENCIA
Aunque los mecanismos por los cuales el VHC permanece en el hospedero causando
una infeccin crnica no se comprenden totalmente, se ha sugerido que la
variabilidad gentica del virus puede jugar un papel importante en la persistencia
(23, 26). Segn esta hiptesis, la evolucin gentica del virus facilitara que ste
escape a la vigilancia del sistema inmunitario (26). En este sentido, algunos autores
han demostrado que los cambios genticos que se van generando en el virus
aparecen de manera compatible con la evasin a la respuesta inmunitaria (21).
Lgicamente, por ser la HVR1 la regin con una mayor variabilidad gentica, la
mayora de los estudios la han involucrado en el escape del sistema inmunitario
(19, 26). As pues, se ha comprobado que despus de la aparicin de anticuerpos
contra la secuencia predominante de la HVR1 surge una nueva variante del VHC con
una secuencia HVR1 que no es reconocida por los anticuerpos previos (21).
Tambin se conoce que los anticuerpos generados contra la secuencia dominante de
la regin HVR1 de un aislado del virus pueden neutralizar a la cepa mayoritaria de
VHC in vitro, pero no a otras cepas menores con secuencias levemente diferentes
presentes en el mismo aislado (23).
El escape a la respuesta inmunitaria por variacin gentica, no se produce
solamente como consecuencia de la presin inmunitaria ejercida por anticuerpos
especficos (22). Existe informacin sobre la aparicin de mutantes de escape a la
respuesta inmunitaria celular ejercida por linfocitos citotxicos (CTL) frente a
eptopos localizados en regiones conservadas como la protena NS3 (23).
No obstante toda esta informacin, la evolucin gentica del virus aparentemente
no es el nico mecanismo causante de la persistencia (19). Dos grupos de
investigadores lograron construir clones infecciosos del VHC e inocularlos a
chimpancs, nico animal de experimentacin en que el VHC es capaz de
replicarse. La mayora de los animales infectados con este virus resultaron con una
infeccin crnica, a pesar de que el inculo contena una secuencia viral nica sin
variacin (22). Adems, el estudio de las secuencias nucleotdicas realizado en
distintos puntos de la evolucin de la infeccin confirm que el VHC puede persistir
sin que aparezcan mutaciones en las regiones estructurales del genoma viral (22).
Muy sugerentes fueron los resultados que se obtuvieron tras disear un clon
infeccioso del VHC al que se haba eliminado la regin hipervariable (HVR1) (22);
no obstante de la gran variabilidad de esta regin y de estar habitualmente
involucrada en la produccin de mutantes de escape, uno de los dos animales
inoculados con este virus "defectuoso" desarroll una infeccin permanente (23).
Esto demuestra que la HVR1 no es indispensable para establecer una infeccin
crnica (22).
RESPUESTA INMUNITARIA INSUFICIENTE
Se ha propuesto la existencia de una respuesta inmunitaria dbil o insuficiente en
los pacientes infectados como una de las causas principales por la cual el VHC
puede permanecer en el organismo (4). Un estudio que apoya esta afirmacin
encontr que algunos pacientes inmunosuprimidos (Receptores de transplantes),
que se infectaron con el VHC, pudieron erradicar la infeccin de manera espontnea
USMP - Facultad de Medicina Humana
independientemente de
inmunosupresora (27).
la
progresin
histolgica,
al
cesar
la
terapia
Se conoce poco acerca de la respuesta innata inespecfica contra el VHC, debido a
que no se cuenta con un modelo animal adecuado y a la dificultad para monitorear,
los pacientes inmediatamente despus de la inoculacin con el virus. No obstante,
existen evidencias que indican que la interaccin de las protenas virales con
elementos del sistema inespecfico de defensa, juega un papel decisivo en la
resolucin de la enfermedad (28).
Al parecer, los niveles de una quimiocina, la Protena inducible por Interfern (IP10) producida por los hepatocitos en respuesta a la infeccin, son esenciales para el
reclutamiento de linfocitos en el hgado y sirven como medida predictiva del curso
de la enfermedad, por lo que no es de extraar que ste pueda ser un primer
blanco de ataque o supresin por parte del VHC (29).
Adems se conoce que algunas regiones virales bloquean in vitro las vas de
inmunidad antiviral dependientes de interfern, al parecer, ciertos dominios de las
protenas codificadas por los genes NS5A (30) y E2 (23) se asocian con la protena
kinasa R (PKR), sintetizada durante la respuesta antiviral interfern dependiente. La
PKR funciona interrumpiendo la sntesis celular de protenas y por ende, la sntesis
de protenas virales (22). La unin de las protenas derivadas de NS5A y E2 con la
PKR aparentemente inhibe el efecto antiviral de dicha protena (31-33). La NS5A
adems es capaz de interactuar con elementos del sistema de la quimiocinas (34).
Ms recientemente, se ha descubierto que la protena E2 puede inhibir a las clulas
NK (28, 35) y que la protena del core puede interactuar y modular, in vitro, varias
vas de transduccin de seal relacionadas con la respuesta innata como la JakStat, la xido ntrico Sintetasa inducible (iNOS) (36, 37) y con el receptor para la
porcin Clq del complemento (38, 39), por lo que se piensa que esta protena
tambin pudiese ser clave para establecer una infeccin persistente.
En trminos generales, se sabe que el VHC induce una respuesta celular policlonal
de baja a moderada intensidad (40), que al parecer est relacionada con el
establecimiento de la cronicidad, ya que se ha encontrado que slo se logra eliminar
la infeccin en aquellos pocos individuos donde las respuestas proliferativas de
linfocitos CD4+ contra el virus son ms vigorosas (2, 41).
En concordancia con lo anterior, se han encontrado algunas alteraciones funcionales
en los linfocitos CD8+provenientes de individuos infectados por el VHC como:
respuesta deficientemente a las citocinas antivirales y produccin limitada de
Interfern y Factor de Necrosis Tumoral (TNF) en comparacin con los linfocitos
activados como respuesta a otros virus (42). Esto sugiere que la accin
inmunosupresora del VHC, puede ser aprovechada por otros patgenos. Existen
otras evidencias que apoyan esta idea; recientemente se demostr que los
linfocitos CD8+ especficos contra Citomegalovirus (CMV) de los pacientes
coinfectados con VHC, pierden fcilmente sus marcadores de madurez celular y
expresan menos cantidad de molculas de Fas y perforinas que los de individuos
sanos (43).
Sin embargo, hay datos que sealan que la alteracin de los patrones de respuesta
de los linfocitos CD8+ es un evento posterior a la activacin, ya que se ha
encontrado que la respuesta inicial citotxica es fuerte en fases muy tempranas y
se va suprimiendo con el tiempo (44, 45).
USMP - Facultad de Medicina Humana
En cuanto a los mediadores, parece predominar, en los individuos con infeccin
autolimitada, un perfil de citocinas tipo helper 1 (Th1) con produccin
preponderante de IL-2 e Interfern (4, 14, 18, 46); adicionalmente, otros
trabajos, reafirman la importancia de este tipo de respuesta Th1 en el control y
eliminacin del VHC. Concretamente, se ha logrado la deteccin de linfocitos T
citotxicos reactivos contra antgenos virales en individuos o animales de
experimentacin que han resuelto la infeccin (4).
En cambio, se ha reportado la presencia de citocinas del perfil helper 2 (h2)
como IL-4 e IL-10 en niveles moderados en el suero de pacientes afectados de
manera persistente (47). Esto sugiere que al igual que muchos patgenos
intracelulares el VHC podra desviar la respuesta celular hacia el patrn de
citocinas h2 en detrimento del h1, como una estrategia que permite la
subsistencia dentro del hospedero (23). En este sentido, algunos trabajos
realizados con el Virus de hepatitis B (VHB), el cual es otro virus hepatotropo con
tendencia a causar una infeccin crnica, sealan que es posible controlar este tipo
de infeccin cuando la respuesta celular se dirige hacia el patrn de citocinas h1
(48, 49).
En resumen, los datos aportados por la mayora de las investigaciones, sealan que
los pacientes con infecciones autocontroladas presentan respuestas inmunitarias
contra el virus mucho ms intensas que las de aquellos en los que el virus persiste
(41). Desafortunadamente, no se sabe si esta diferencia es la causante de la
cronicidad o una consecuencia de ella, aunque recientemente se ha publicado
informacin que demuestra que el VHC puede infectar clulas del sistema
inmunitario como Macrfagos, Linfocitos B y , alterando los patrones de respuesta
de dichas clulas, permitiendo as la persistencia del virus (50).
En este sentido, un factor importante en la aparicin de una respuesta celular dbil
podra ser la activacin anormal de linfocitos CD4+. Se ha demostrado que la
expresin de antgenos estructurales del VHC en clulas dendrticas, alteran el
proceso de presentacin antignica, generando una activacin incompleta de
linfocitos CD4+ especficos contra el VHC (51).
Otros trabajos sugieren una causa gentica como la responsable de la baja
respuesta celular (52, 53), ya que existe un grupo de pacientes que tiene una alta
tasa de eliminacin espontnea de la infeccin, aquellos con genes de HLA
especficos (DRB1*1101 y/o DQ1*0301). Las molculas del Complejo Mayor de
Histocompatibilidad de Clase I (CMH I) que exhiben dichos pacientes pueden alojar
a los pptidos virales claves para una efectiva activacin celular (46). Por otra
parte, no existen evidencias que demuestren que el VHC interfiera con la expresin
de las molculas de CMH I en las clulas (54).
Novedosos estudios en chimpancs complican ms el panorama. En dichos ensayos,
no fue necesaria una respuesta inmunitaria celular vigorosa contra el VHC para
lograr la resolucin de la viremia, por lo que los autores sugieren que otros
mecanismos inmunitarios son los responsables del control de la infeccin (55).
En lo que respecta a la inmunidad humoral, la aparicin precoz de anticuerpos
neutralizantes contra el VHC pareciese desempear un rol valioso en la resolucin
de la infeccin, tal y como ocurre en gran cantidad de infecciones virales (14). En
una investigacin utilizando anticuerpos aislados a partir de plasma de donantes
anti-VHC positivos, se trataron varios chimpancs a los cuales se les haba
inoculado previamente el virus y se pudo verificar que ninguno de los chimpancs
USMP - Facultad de Medicina Humana
tratados mostr sntomas de hepatitis aguda y el ARN viral desapareci de
circulacin rpidamente (22).
As mismo, recientemente se encontr que la protena E2 de la envoltura viral es
capaz de unirse a varios receptores presentes en la superficie del hepatocito como
el CD 81, el receptor humano para detritos clase B tipo 1 y el heparan sulfato, de
una manera no competitiva, utilizando diferentes dominios de su estructura para
asegurar la interaccin con la clula. As pues, la neutralizacin de uno o incluso
varios dominios de la E2, no impedira que sta logre unirse a otro receptor en el
hepatocito e iniciar la infeccin (56).
Algunos trabajos en pacientes normales y con agammaglobulinemia, infectados por
el VHC, han demostrado que no es necesaria la aparicin de una respuesta de
anticuerpos especfica para eliminar el virus. El desarrollo de una inmunidad celular
vigorosa y precoz contra el virus basta por si sola para erradicar la infeccin (21,
57). Incluso se ha demostrado que la erradicacin de la viremia puede ocurrir en
individuos normales sin que stos se vuelvan seropositivos (57).
En conclusin, el papel de los anticuerpos en la evolucin de la enfermedad no est
claro.
OTROS MECANISMOS QUE PUEDEN CONTRIBUIR A LA PERSISTENCIA DE LA
INFECCIN
Hay una investigacin que indica que la regin HVR1 pudiera servir de "seuelo",
captando la atencin del sistema inmunitario en menoscabo de otras regiones
antignicas que podran ser ms importantes (22).
En un trabajo llevado a cabo en la etapa aguda de la infeccin, se encontr, en los
individuos con infeccin crnica, una gran cantidad de mutaciones no sinnimas
(que generan un cambio de aminocido) en la HVR1 pero no en la regin que
codifica la protena de envoltura E1 (22), Mientras que en pacientes en los que la
infeccin se autolimit, las mutaciones no sinnimas se concentraban en la protena
E1 y no en la HVR1. Tomando la aparicin de mutaciones no sinnimas como una
determinacin indirecta de la presin inmunitaria que se realiza sobre una regin
especfica (22), es plausible pensar que la presin del sistema inmunitario sobre la
HVR1 no fuera relevante y slo se tratase de un mecanismo viral para apartar la
presin sobre otras regiones (14).
Se ha descrito otro mecanismo de evasin de la accin del interfern por parte del
genotipo 1a y 1b del VHC. Existe una enzima celular, la ARNasa L, cuya accin est
regulada por el interfern, que corta el ARNm del VHC en los puntos AU-UU,
impidiendo la traduccin de las protenas virales. Para evadir esta amenaza, los
genotipos 1a y 1b han acumulado mutaciones silentes (que no afectan el producto
proteico) eliminando muchos puntos AU y UU de sus secuencias en relacin a otros
genotipos como el 2 y 3. Esta podra ser la razn principal de porqu estos
genotipos (1a y 1b) son generalmente refractarios a la terapia con interfern y de
mal pronstico (58).
ltimamente, se han enfocado muchas investigaciones a develar el papel biolgico
de la protena del core, que constituye la primera protena del virus en expresarse y
circular en el torrente sanguneo de los pacientes infectados (20). En este sentido
se han encontrado in vitro muchos hechos interesantes como: Esta protena inhibe
la respuesta proliferativa de Linfocitos a travs de la interaccin con el receptor
USMP - Facultad de Medicina Humana
de complemento que stos presentan, alterando la sealizacin que activa la
produccin de IL-2 (39).
La protena del core, evitara la muerte por apoptosis mediada por F- de clulas
hepticas infectadas por el VHC, interrumpiendo la sealizacin interna de este
evento (59). La protena NS2 tambin parece estar implicada en este proceso
unindose e inhibiendo al CIDE-B, un factor mediador de apoptosis descubierto
recientemente (60).
Esta protena del puede escapar al sistema inmunitario por mimetismo molecular,
ya que muestra cierta homologa en su secuencia con el citocromo p450 humano,
contribuyendo a la persistencia de la infeccin y/o generando efectos patolgicos
(Hepatitis autoinmune) por autorreactividad inducida por el virus (61). El
mimetismo molecular de la protena corrobora algunos estudios en modelos
mridos donde esta protena parece estar implicada en la supresin de la respuesta
inmunitaria contra un virus quimrico (Vaccinia/VHC) recombinante (62).
Sin embargo, otros estudios arrojan resultados contradictorios. Ratones
transgnicos que expresaban protena del core y de la envoltura del VHC en clulas
hepticas, respondieron y resolvieron la infeccin de Adenovirus hepatrotopos de
manera muy similar. Los niveles de IgG, IL-2 y F- en estos animales fueron
semejantes, por los que los autores sugieren que los mecanismos de persistencia
del VHC, no estn relacionados con una profunda inmunosupresin generada por
protenas estructurales (63).
CONCLUSIN
A pesar de todas las investigaciones realizadas sobre los mecanismos de evasin
inmunitaria por parte del VHC, todava no est claro cul es el mecanismo principal
que permite la cronicidad de la infeccin. Al respecto, se han descrito muchos
procesos y prcticamente a todas las protenas virales se le atribuye, por lo menos
in vitro, alguna funcin evasiva.
Es un hecho que la variabilidad gentica en muchos patgenos, es un mecanismo
importante de escape al reconocimiento y destruccin por parte del hospedero. El
VHC presenta zonas altamente variables en su superficie, que tericamente, deben
contribuir a permanecer en el organismo; sin embargo, tambin se ha sealado
cierta inmunosupresin causada por el virus. Lgicamente, estos dos mecanismos
podran actuar sinrgicamente. Un sistema tan complejo y adaptable como el
sistema inmunitario humano, no puede ser confundido mediante un solo proceso o
por la inhibicin de un mecanismo de reconocimiento/efector; se necesita toda una
batera de sofisticados recursos para evadirlo por un tiempo indefinido como lo hace
el VHC.
Hasta que no se descifre el enigma que representa el escape de la respuesta
inmunitaria por parte del VHC, no se podrn crear mejores inmunoterapias y/o una
vacuna efectiva, mientras la salud de muchas personas a nivel nacional y mundial,
infectadas por este virus, seguir perjudicada severamente.
REFERENCIAS
USMP - Facultad de Medicina Humana
1. Uriz J, Briz R. Natural history of hepatitis C virus infection. An Sist Sanit Navar
2004; 27(2):51-58.
[ Links ]
2. Yao F, Terrault N. Hepatitis C and hepatocellular carcinoma. Curr Treat Options
Oncol 2001; 2(6):473-483.
[ Links ]
3. Ramos-Gmez M. Historia natural de la hepatitis crnica C. Rev Gastroenter
2002; 67(2):S17-S20.
[ Links ]
4. Lauer GM, Walker BD. Hepatitis C virus infection. N Engl J Med 2001; 345(1):
41-52.
[ Links ]
5. Freeman AJ, Dore GJ, Law MG, Thorpe M, Von Overbeck J, Lloyd AR, Marinos G,
Kaldor JM. Estimating progression to cirrhosis in chronic hepatitis C virus infection.
Hepatology 2001; 34(4 Pt 1):809-816.
[ Links ]
6. Kenny-Walsh E. The natural history of hepatitis C virus infection. Clin Liver Dis
2001; 5(4):969-77.
[ Links ]
7. Polyak SJ. Hepatitis C virus--cell interactions and their role in pathogenesis. Clin
Liver Dis 2003; 7(1):67-88.
[ Links ]
8. Aguilar MS, Cosson C, Loureiro CL, Devesa M, Martinez J, Villegas L, Flores J,
Ludert JE, Alarcon- Noya B, Noya O, Liprandi F, Pujol FH. Prevalence of infection
with hepatitis C virus in Venezuela, as assessed with an immuno-assay based on
synthetic peptides. Ann Trop Med Parasitol 2001; 95(2):187-195.
[ Links ]
9. Arteaga-Vizcaino M, Blitz-Dorfman L, Echeverria JM, Leon P, Weir-Medina J, DiezEwald M, Vizcaino G, Torres E, Porto-Espinoza L. Hepatitis C in hemophiliac patients
in Maracaibo, Venezuela. Invest Clin 1993; 34(3):113-118.
[ Links ]
10. Feldman M, Friedman LS, Sleisenger MH. Sleisenger & Fordtran's
gastrointestinal and liver disease: pathophysiology, diagnosis, management. 7th ed.
[CD-ROM]. Philadelphia: Saunders; 2002.
[ Links ]
11. Dore GJ, Freeman AJ, Law M, Kaldor JM. Is severe liver disease a common
outcome for people with chronic hepatitis C? J Gastroenterol Hepatol 2002;
17(4):423-430.
[ Links ]
12. Mandell GL, Douglas RG, Bennett JE, Dolin R. Mandell, Douglas, and Bennett's
principles and practice of infectious diseases. 5th ed. [CD-ROM]. Philadelphia:
Churchill Livingstone; 2000.
[ Links ]
13. Valiante NM, D'Andrea A, Crotta S, Lechner F, Klenerman P, Nuti S, Wack A,
Abrignani S. Life, activation and death of intrahepatic lymphocytes in chronic
hepatitis C. Immunol Rev 2000; 174:77-89.
[ Links ]
14. Alvarado-Esquivel C, Leroux-Roels G. Inmunologa de la hepatitis C. Rev Invest
Clin 1999; 51(5):315-322.
[ Links ]
15. Dore GJ, Freeman AJ, Kaldor JM. Immunity against hepatitis C virus infection.
Lancet 2002; 360(9338):1019-20; author reply 1020-1021.
[ Links ]
USMP - Facultad de Medicina Humana
16. Weiner AJ, Paliard X, Selby MJ, Medina-Selby A, Coit D, Nguyen S, Kansopon J,
Arian CL, Ng P, Tucker J, Lee CT, Polakos NK, Han J, Wong S, Lu HH, Rosenberg S,
Brasky KM, Chien D, Kuo G, Houghton M. Intrahepatic genetic inoculation of
hepatitis C virus RNA confers cross-protective immunity. J Virol 2001; 75(15):71427148.
[ Links ]
17. Lara-Ceniceros M, Godnez-Hernndez F, Aillaud-Gonzlez L, Meja A. Hepatitis
C. Med Int Mex 2003; 19(5):311-318.
[ Links ]
18. Bonkovsky HL, Mehta S. Hepatitis C: a review and update. J Am Acad Dermatol
2001; 44(2):159-182.
[ Links ]
19. Rivas-Estilla A, Panduro A. Mecanismos moleculares del virus de la hepatitis C,
potenciales
blancos
teraputicos.
Rev
Invest
Clin
2003;
55(1):5164.
[ Links ]
20. lvarez M, Gmez I. Biologa y mtodos diagnsticos del virus de la hepatitis C.
Rev Biomed 2003; 14(4):253-268.
[ Links ]
21. Drazan KE. Molecular biology of hepatitis C infection. Liver Transpl 2000;
6(4):396-406.
[ Links ]
22. Forns X. Molecular biology of hepatitis C virus: implications for the development
of new therapies and prophylactic vaccine. Med Clin (Barc) 2001; 116(5):191197.
[ Links ]
23. Freeman AJ, Marinos G, Ffrench RA, Lloyd AR. Immunopathogenesis of hepatitis
C virus infection. Immunol Cell Biol 2001; 79(6):515-536.
[ Links ]
24. Montao-Loza A, Meza-Junco J, Remes-Troche J. Patognesis de la infeccin por
virus de hepatitis C. Rev Invest Clin 2001; 53(6):561-568.
[ Links ]
25. Terrs-Speziale AM. Hepatitis C. Historia natural y estado actual de su manejo.
Rev Mex Patol Clin 2003; 50(4):179-189.
[ Links ]
26. Hahn YS. Subversion of immune responses by hepatitis C
immunomodulatory strategies beyond evasion? Curr Opin Immunol
15(4):443-449.
[ Links ]
virus:
2003;
27. Somsouk M, Lauer GM, Casson D, Terella A, Day CL, Walker BD, Chung RT.
Spontaneous resolution of chronic hepatitis C virus disease after withdrawal of
immunosuppression. Gastroenterology 2003; 124(7):1946-1949.
[ Links ]
28. Chang KM. Immunopathogenesis of hepatitis C virus infection. Clin Liver Dis
2003; 7(1):89-105.
[ Links ]
29. Harvey CE, Post JJ, Palladinetti P, Freeman AJ, Ffrench RA, Kumar RK, Marinos
G, Lloyd AR. Expression of the chemokine IP-10 (CXCL10) by hepatocytes in
chronic hepatitis C virus infection correlates with histological severity and lobular
inflammation. J Leukoc Biol 2003; 74(3):360-369.
[ Links ]
30. Gale M, Jr., Kwieciszewski B, Dossett M, Nakao H, Katze MG. Antiapoptotic and
oncogenic potentials of hepatitis C virus are linked to interferon resistance by viral
USMP - Facultad de Medicina Humana
repression
6516.
of
the
[ Links ]
PKR
protein
kinase.
Virol
1999;
73(8):6506-
31. Samuel CE. Antiviral actions of interferons. Clin Microbiol Rev 2001; 14(4):778809.
[ Links ]
32. Polyak SJ, Paschal DM, McArdle S, Gale MJ, Jr., Moradpour D, Gretch DR.
Characterization of the effects of hepatitis C virus nonstructural 5A protein
expression in human cell lines and on interferon-sensitive virus replication.
Hepatology 1999; 29(4):1262-1271.
[ Links ]
33. Gale MJ, Jr., Korth MJ, Katze MG. Repression of the PKR protein kinase by the
hepatitis C virus NS5A protein: a potential mechanism of interferon resistance. Clin
Diagn Virol 1998; 10(2-3):157-162.
[ Links ]
34. Khabar KS, Polyak SJ. Hepatitis C virus-host interactions: the NS5A protein and
the interferon/chemokine systems. J Interferon Cytokine Res 2002; 22(10): 10051012.
[ Links ]
35. Crotta S, Stilla A, Wack A, D'Andrea A, Nuti S, D'Oro U, Mosca M, Filliponi F,
Brunetto RM, Bonino F, Abrignani S, Valiante NM. Inhibition of natural killer cells
through engagement of CD81 by the major hepatitis C virus envelope protein. J Exp
Med 2002; 195(1):35-41.
[ Links ]
36. Miller K, McArdle S, Gale MJ, Jr., Geller DA, Tenoever B, Hiscott J, Gretch DR,
Polyak SJ. Effects of the hepatitis C virus core protein on innate cellular defense
pathways. J Interferon Cytokine Res 2004; 24(7):391-402.
[ Links ]
37. Ray RB, Ray R. Hepatitis C virus core protein: intriguing properties and
functional relevance. FEMS Microbiol Lett 2001; 202(2):149-156.
[ Links ]
38. Yao ZQ, Ray S, Eisen-Vandervelde A, Waggoner S, Hahn YS. Hepatitis C virus:
immunosuppression by complement regulatory pathway. Viral Immunol 2001;
14(4):277-295.
[ Links ]
39. Yao ZQ, Nguyen DT, Hiotellis AI, Hahn YS. Hepatitis C virus core protein inhibits
human T lymphocyte responses by a complement-dependent regulatory pathway. J
Immunol 2001; 167(9):5264-5272.
[ Links ]
40. Barnes E, Lauer G, Walker B, Klenerman P. T cell failure in hepatitis C virus
infection. Viral Immunol 2002; 15(2):285-293.
[ Links ]
41. Lechner F, Wong DK, Dunbar PR, Chapman R, Chung RT, Dohrenwend P,
Robbins G, Phillips R, Klenerman P, Walker BD. Analysis of successful immune
responses in persons infected with hepatitis C virus. J Exp Med 2000; 191(9):14991512.
[ Links ]
42. Gruener NH, Lechner F, Jung MC, Diepolder H, Gerlach T, Lauer G, Walker B,
Sullivan J, Phillips R, Pape GR, Klenerman P. Sustained dysfunction of antiviral
CD8+ T lymphocytes after infection with hepatitis C virus. J Virol 2001;
75(12):5550-5558.
[ Links ]
43. Lucas M, Vargas-Cuero AL, Lauer GM, Barnes E, Willberg CB, Semmo N, Walker
BD, Phillips R, Klenerman P. Pervasive influence of hepatitis C virus on the
USMP - Facultad de Medicina Humana
phenotype of antiviral
1753.
[ Links ]
CD8+
cells.
44. Lechner F, Sullivan J, Spiegel H, Nixon
Pollack H, Barnes E, Dusheiko G, Klenerman
to eliminate hepatitis C virus? Lessons from
complex class I peptide tetramers. Philos
355(1400):1085-1092.
[ Links ]
Immunol
2004;
172(3):1744-
DF, Ferrari B, Davis A, Borkowsky B,
P. Why do cytotoxic T lymphocytes fail
studies using major histocompatibility
Trans R Soc Lond B Biol Sci 2000;
45. Lechner F, Gruener NH, Urbani S, Uggeri J, Santantonio T, Kammer AR, Cerny A,
Phillips R, Ferrari C, Pape GR, Klenerman P. CD8 + T lymphocyte responses are
induced during acute hepatitis C virus infection but are not sustained. Eur J
Immunol 2000; 30(9):2479-2487.
[ Links ]
46. Ward S, Lauer G, Isba R, Walker B, Klenerman P. Cellular immune responses
against hepatitis C virus: the evidence base 2002. Clin Exp Immunol 2002; 128(2):
195-203.
[ Links ]
47. Reiser M, Marousis CG, Nelson DR, Lauer G, Gonzalez-Peralta RP, Davis GL, Lau
JY. Serum interleukin 4 and interleukin 10 levels in patients with chronic hepatitis C
virus infection. J Hepatol 1997; 26(3): 471-478.
[ Links ]
48. Monsalve-De Castillo F, Romero TA, Estevez J, Costa LL, Atencio R, PortoEspinoza L, Callejas D. Concentrations of cytokines, soluble interleukin-2 receptor,
and soluble CD30 in sera of patients with hepatitis B virus infection during acute
and convalescent phases. Clin Diagn Lab Immunol 2002; 9(6):13721375.
[ Links ]
49. Monsalve F, Romero AT, Estevez J, Costa L, Callejas D. Serum levels of soluble
CD30 molecule in hepatitis B virus infection. Rev Med Chil 2001; 129(11):12481252.
[ Links ]
50. Soguero C, Joo M, Chianese-Bullock KA, Nguyen DT, Tung K, Hahn YS. Hepatitis
C virus core protein leads to immune suppression and liver damage in a transgenic
murine model. J Virol 2002; 76(18):9345-9354.
[ Links ]
51. Sarobe P, Lasarte JJ, Casares N, Lopez-Diaz de Cerio A, Baixeras E, Labarga P,
Garcia N, Borras-Cuesta F, Prieto J. Abnormal priming of CD4(+) T cells by dendritic
cells expressing hepatitis C virus core and E1 proteins. J Virol 2002; 76(10):50625070.
[ Links ]
52. Lauer GM, Ouchi K, Chung RT, Nguyen TN, Day CL, Purkis DR, Reiser M, Kim AY,
Lucas M, Klenerman P, Walker BD. Comprehensive analysis of CD8(+)-T-cell
responses against hepatitis C virus reveals multiple unpredicted specificities. J Virol
2002; 76(12):6104-6113.
[ Links ]
53. Nelson DR. The immunopathogenesis of hepatitis C virus infection. Clin Liver
Dis 2001; 5(4):931-953.
[ Links ]
54. Moradpour D, Grabscheid B, Kammer AR, Schmidtke G, Groettrup M, Blum HE,
Cerny A. Expression of hepatitis C virus proteins does not interfere with major
histocompatibility complex class I processing and presentation in vitro. Hepatology
2001; 33(5):1282-1287.
[ Links ]
USMP - Facultad de Medicina Humana
55. Thomson M, Nascimbeni M, Havert MB, Major M, Gonzales S, Alter H, Feinstone
SM, Murthy KK, Rehermann B, Liang TJ. The clearance of hepatitis C virus infection
in chimpanzees may not necessarily correlate with the appearance of acquired
immunity. J Virol 2003; 77(2):862-870.
[ Links ]
56. Heo TH, Chang JH, Lee JW, Foung SK, Dubuisson J, Kang CY. Incomplete
humoral immunity against hepatitis C virus is linked with distinct recognition of
putative multiple receptors by E2 envelope glycoprotein. J Immunol 2004; 173(1):
446-455.
[ Links ]
57. Post JJ, Pan Y, Freeman AJ, Harvey CE, White PA, Palladinetti P, Haber PS,
Marinos G, Levy MH, Kaldor JM, Dolan KA, Ffrench RA, Lloyd AR, Rawlinson WD.
Clearance of hepatitis C viremia associated with cellular immunity in the absence of
seroconversion in the hepatitis C incidence and transmission in prisons study
cohort. J Infect Dis 2004; 189(10): 1846-1855.
[ Links ]
58. Han JQ, Barton DJ. Activation and evasion of the antiviral 2'-5' oligoadenylate
synthetase/ribonuclease L pathway by hepatitis C virus mRNA. 2002; 8(4):512525.
[ Links ]
59. Ray RB, Meyer K, Steele R, Shrivastava A, Aggarwal BB, Ray R. Inhibition of
tumor necrosis factor (TNF-alpha)-mediated apoptosis by hepatitis C virus core
protein. J Biol Chem 1998; 273(4):2256-2259.
[ Links ]
60. Erdtmann L, Franck N, Lerat H, Le Seyec J, Gilot D, Cannie I, Gripon P, Hibner
U, Guguen-Guillouzo C. The hepatitis C virus NS2 protein is an inhibitor of CIDE-Binduced apoptosis. J Biol Chem 2003; 278(20):18256-18264.
[ Links ]
61. Kammer AR, van der Burg SH, Grabscheid B, Hunziker IP, Kwappenberg KM,
Reichen J, Melief CJ, Cerny A. Molecular mimicry of human cytochrome P450 by
hepatitis C virus at the level of cytotoxic T cell recognition. J Exp Med 1999;
190(2):169-176.
[ Links ]
62. Large MK, Kittlesen DJ, Hahn YS. Suppression of host immune response by the
core protein of hepatitis C virus: possible implications for hepatitis C virus
persistence. J Immunol 1999; 162(2):931-938.
[ Links ]
63. Sun J, Bodola F, Fan X, Irshad H, Soong L, Lemon SM, Chan TS. Hepatitis C
virus core and envelope proteins do not suppress the host's ability to clear a hepatic
viral infection. J Virol 2001; 75(24):11992-11998.
[ Links ]
Autor de correspondencia: Leticia Porto. Laboratorio de Referencia Virolgica,
Instituto de Investigaciones Clnicas, Facultad de Medicina, Universidad del Zulia.
Maracaibo 4001, Venezuela. Telfono-Fax: 58-261-7597273. Correo electrnico:
letiporto@yahoo.com
Anda mungkin juga menyukai
- Patogenesis BacterianaDokumen78 halamanPatogenesis BacterianaAlwisJeaniell Vega CBelum ada peringkat
- Inmunodeficiencias PrimariasDokumen34 halamanInmunodeficiencias PrimariasHugo RoldanBelum ada peringkat
- Autoinmunidad y TransplanteDokumen49 halamanAutoinmunidad y TransplanteElia Salazar100% (1)
- Hongos - GeneralidadesDokumen56 halamanHongos - GeneralidadesNatalia RaquelBelum ada peringkat
- Astrid Carballo 15-09-20Dokumen2 halamanAstrid Carballo 15-09-20Astri Carballo PuelloBelum ada peringkat
- Sistema InmuneDokumen48 halamanSistema InmuneGabriela Prado GumielBelum ada peringkat
- Covid 19Dokumen31 halamanCovid 19Henry CruelBelum ada peringkat
- Inmunologia ClinicaDokumen30 halamanInmunologia ClinicaWendy SantacruzBelum ada peringkat
- Enfermeria NeonatalDokumen12 halamanEnfermeria NeonatalJosé Luis Alonso EscamillaBelum ada peringkat
- Trabajo Protozoos Sanguíneos y TisularesDokumen6 halamanTrabajo Protozoos Sanguíneos y TisularesYan Yeberson Chamba ContrerasBelum ada peringkat
- Mecanismos DefensaDokumen38 halamanMecanismos DefensaMario Mendoza TorresBelum ada peringkat
- Evolución y Sus Repercusiones SocialesDokumen8 halamanEvolución y Sus Repercusiones SocialesLuis Roberto Ortiz Zambrano100% (1)
- Virus RespiratoriosDokumen111 halamanVirus RespiratoriosAlejandra GutierrezBelum ada peringkat
- Historia Natural de La Enfermedad COVID19Dokumen2 halamanHistoria Natural de La Enfermedad COVID19Aldo CastañedaBelum ada peringkat
- StreptococcusDokumen57 halamanStreptococcusCarla Federigi100% (2)
- Virus Del Papiloma HumanoDokumen19 halamanVirus Del Papiloma HumanoJosé Manel Madolell SánchezBelum ada peringkat
- ClostridiumDokumen42 halamanClostridiumAaron Villarreal PereyraBelum ada peringkat
- Enfermedades Infecto-Contagiosas PDFDokumen60 halamanEnfermedades Infecto-Contagiosas PDFJoseBelum ada peringkat
- RESUMEN - Metabolismo Del AguaDokumen4 halamanRESUMEN - Metabolismo Del AguamonserratBelum ada peringkat
- Medicamentos Usados Durante El EmbarazoDokumen45 halamanMedicamentos Usados Durante El EmbarazoMelina Piza JaraBelum ada peringkat
- Inmunidad TumoralDokumen8 halamanInmunidad TumoralManuel AlvarezBelum ada peringkat
- Inmunidad Frente A Los TumoresDokumen4 halamanInmunidad Frente A Los TumoresJacs SaulBelum ada peringkat
- Formación de AnticuerposDokumen19 halamanFormación de Anticuerposclarck777Belum ada peringkat
- 20Dokumen14 halaman20Cal LigmtmanBelum ada peringkat
- Respuesta Inmune Innata y Adquirida AntitumorDokumen1 halamanRespuesta Inmune Innata y Adquirida AntitumorYahaira JocelynBelum ada peringkat
- Anemia AplasicaDokumen36 halamanAnemia AplasicaOscar LP QrsBelum ada peringkat
- Mecanismo de Patogenicidad BacterianaDokumen3 halamanMecanismo de Patogenicidad BacterianaKeyla Vente VelascoBelum ada peringkat
- AMEBIASISDokumen7 halamanAMEBIASISRomi Scarlet CanedoBelum ada peringkat
- MicobacteriasDokumen48 halamanMicobacteriasAbraham Kareem Madrigal RinconBelum ada peringkat
- Receptores de AntigenoDokumen5 halamanReceptores de AntigenoGenesis solisBelum ada peringkat
- Programa Respuesta Inmune 20-1Dokumen3 halamanPrograma Respuesta Inmune 20-1Ruth Cobo RosalesBelum ada peringkat
- Seminario #5-Microbiología. RESPUESTA INMUNE INESPECÍFICA O INNATADokumen19 halamanSeminario #5-Microbiología. RESPUESTA INMUNE INESPECÍFICA O INNATALili VanBelum ada peringkat
- MICETOMADokumen5 halamanMICETOMAbRiAn GLópezBelum ada peringkat
- Patogenicidad PDFDokumen61 halamanPatogenicidad PDFLaboratoriosClinicosZaragozaBelum ada peringkat
- Generalidades de Enfermedades Infecciosas PDFDokumen6 halamanGeneralidades de Enfermedades Infecciosas PDFRicardoAlbuja100% (1)
- ITU Comunitaria Por E. Coli BLEEDokumen6 halamanITU Comunitaria Por E. Coli BLEEMarcia SalgadoBelum ada peringkat
- Patogenia ViralDokumen25 halamanPatogenia Viralzthii_orthegaBelum ada peringkat
- Neumococo PDFDokumen18 halamanNeumococo PDFDariansell GarciaBelum ada peringkat
- Cartel Artritis Reumatoide GeneralidadesDokumen1 halamanCartel Artritis Reumatoide GeneralidadesKEILA HITZAMAR GUTIERREZ DOMINGUEZBelum ada peringkat
- Ciclo de Krebs Cadena Respiratoria y Fosforilacion Oxidativa PDFDokumen1 halamanCiclo de Krebs Cadena Respiratoria y Fosforilacion Oxidativa PDFzandra0% (1)
- INFLAMACIONDokumen12 halamanINFLAMACIONMilagros Rodriguez SalaburuBelum ada peringkat
- Estructura y Clasificación de Los VirusDokumen9 halamanEstructura y Clasificación de Los VirusDaifuku17Belum ada peringkat
- Estructura y Clasificación de Los VirusDokumen10 halamanEstructura y Clasificación de Los VirusMariana Gazga ValenciaBelum ada peringkat
- Linfocitos T CitotóxicosDokumen6 halamanLinfocitos T CitotóxicosDaleska Magdeley Villavicencio AndradeBelum ada peringkat
- VacunasDokumen8 halamanVacunasCarol DelgadoBelum ada peringkat
- Mycoplasma y UreaplasmaDokumen17 halamanMycoplasma y UreaplasmaLalo G. MezaBelum ada peringkat
- 02 Patogenia ViralDokumen28 halaman02 Patogenia ViralBlanca GomezBelum ada peringkat
- Deficiencia Selectiva IgaDokumen12 halamanDeficiencia Selectiva IgaValenciaErikBelum ada peringkat
- Sistema Inmune AdaptativoDokumen13 halamanSistema Inmune AdaptativoluledavilaBelum ada peringkat
- Paludismo PDFDokumen3 halamanPaludismo PDFAngela Morales GuillénBelum ada peringkat
- Patogenia ViricaDokumen37 halamanPatogenia ViricaDavid De la CruzBelum ada peringkat
- Función Inmunológica Del Hígado y Páncreasjohanna MancillaDokumen13 halamanFunción Inmunológica Del Hígado y Páncreasjohanna MancillaJohanna MancillaBelum ada peringkat
- Clase 7 Los Antígenos 1Dokumen37 halamanClase 7 Los Antígenos 1victor quispe Castro100% (1)
- Colera Curso Apuntes 2018Dokumen7 halamanColera Curso Apuntes 2018Alfonso Castillo DomínguezBelum ada peringkat
- OrtomixovirusDokumen11 halamanOrtomixovirusRaul Arturo Rincon ContrersBelum ada peringkat
- Inmunidad AdaptativaDokumen6 halamanInmunidad AdaptativaRafael Rovira Gómez-SánchezBelum ada peringkat
- Patogenicidad de BacteriasDokumen4 halamanPatogenicidad de BacteriasLizbeth SalesBelum ada peringkat
- QuimioterapeuticosDokumen66 halamanQuimioterapeuticosKarinaKaterinaQuinteroRodriguezBelum ada peringkat
- Gabarella Apunte InmunoDokumen53 halamanGabarella Apunte InmunoBruna100% (1)
- LisosomasDokumen14 halamanLisosomasAndrea0% (1)
- LepraDokumen27 halamanLepraSt@r goldenBelum ada peringkat
- Vacunas Bacterianas IDokumen20 halamanVacunas Bacterianas IRUBEN JUNIOR LOPEZ AREVALOBelum ada peringkat
- Seminario IV - Pregunta 5 y 6Dokumen2 halamanSeminario IV - Pregunta 5 y 6Juan José Gómez ToscanelliBelum ada peringkat
- Seminario 1 - Pregunta 3Dokumen4 halamanSeminario 1 - Pregunta 3Juan José Gómez ToscanelliBelum ada peringkat
- Pregunta 8 y 9Dokumen9 halamanPregunta 8 y 9Juan José Gómez ToscanelliBelum ada peringkat
- Gases IIDokumen2 halamanGases IIJuan José Gómez ToscanelliBelum ada peringkat
- Seminario 1 - Pregunta 3Dokumen3 halamanSeminario 1 - Pregunta 3Juan José Gómez ToscanelliBelum ada peringkat
- BioeletricidadDokumen26 halamanBioeletricidadJuan José Gómez ToscanelliBelum ada peringkat
- Pregunta 7 y 8 - Seminario 9Dokumen5 halamanPregunta 7 y 8 - Seminario 9Juan José Gómez ToscanelliBelum ada peringkat
- Seminario 2 - InmunologíaDokumen3 halamanSeminario 2 - InmunologíaJuan José Gómez ToscanelliBelum ada peringkat
- Banco de Preguntas para Obtener Licencia de Conducir ADokumen48 halamanBanco de Preguntas para Obtener Licencia de Conducir Asergios7171% (7)
- Lab OratorioDokumen2 halamanLab OratorioJuan José Gómez ToscanelliBelum ada peringkat
- Sistema InmuneDokumen47 halamanSistema InmuneJuan José Gómez ToscanelliBelum ada peringkat
- HistologiaDokumen6 halamanHistologiaJuan José Gómez ToscanelliBelum ada peringkat
- Seminario #VIIDokumen16 halamanSeminario #VIIJuan José Gómez ToscanelliBelum ada peringkat
- BiologíaDokumen1 halamanBiologíaJuan José Gómez ToscanelliBelum ada peringkat
- Ética y AntropologíaDokumen19 halamanÉtica y AntropologíaJuan José Gómez ToscanelliBelum ada peringkat
- Cascada de CoagulaciónDokumen10 halamanCascada de CoagulaciónJuan José Gómez ToscanelliBelum ada peringkat
- MITOCONDRIADokumen4 halamanMITOCONDRIAJuan José Gómez ToscanelliBelum ada peringkat
- El ConocimientoDokumen40 halamanEl ConocimientoJuan José Gómez ToscanelliBelum ada peringkat
- Lectura AntropológicaDokumen18 halamanLectura AntropológicaJuan José Gómez ToscanelliBelum ada peringkat
- Immunocal FuncionaDokumen3 halamanImmunocal Funcionabryanpool6Belum ada peringkat
- Efectos Del Ejercicio en El Adulto Mayor PDFDokumen7 halamanEfectos Del Ejercicio en El Adulto Mayor PDFAlex MolinaBelum ada peringkat
- Zyanopsis de Inmuno 2.0 - Tercer BloqueDokumen28 halamanZyanopsis de Inmuno 2.0 - Tercer BloqueBrittanhy RodriguezBelum ada peringkat
- T1a-Historia de La InmunologiaDokumen14 halamanT1a-Historia de La InmunologiakevinBelum ada peringkat
- Anatomia Monografia Final 00Dokumen43 halamanAnatomia Monografia Final 00Maite Romero CartagenaBelum ada peringkat
- TCR y BCRDokumen7 halamanTCR y BCREsther MoralesBelum ada peringkat
- ToxoplasmosisDokumen21 halamanToxoplasmosisruben cahuayaBelum ada peringkat
- Informe de InflamacionDokumen8 halamanInforme de InflamacionflorcitaBelum ada peringkat
- AFMO 26 EnzimoterapiaDokumen4 halamanAFMO 26 Enzimoterapiajosemaritempra100% (1)
- Oceanografia Observacional o ExperimentalDokumen2 halamanOceanografia Observacional o ExperimentalHiraikHimuraBelum ada peringkat
- Tarea, InflamacionDokumen7 halamanTarea, InflamacionLuis EspinozaBelum ada peringkat
- Generalidades de Los Tejidos BásicosDokumen14 halamanGeneralidades de Los Tejidos BásicosYenifer AriasBelum ada peringkat
- Enfermedades Provocadas Por El Ambiente de A A ZDokumen8 halamanEnfermedades Provocadas Por El Ambiente de A A ZJoseph Ariza QuispeBelum ada peringkat
- Todos Al CampoDokumen309 halamanTodos Al CampoPaula Andrea C FBelum ada peringkat
- Investigacion Productos PDFDokumen76 halamanInvestigacion Productos PDFfernanda marin sernaBelum ada peringkat
- Enfermedades Autoinmunes y El GéneroDokumen4 halamanEnfermedades Autoinmunes y El GéneroVale Valdebenito OcaranzaBelum ada peringkat
- HISTORIA NATURAL DE LA ENFERMEDAD Y SUS NIVELES ModDokumen21 halamanHISTORIA NATURAL DE LA ENFERMEDAD Y SUS NIVELES ModMargaritaSantosViteBelum ada peringkat
- Queloide en EsDokumen10 halamanQueloide en EsAlicia Segura GradosBelum ada peringkat
- Resumen InmunoDokumen20 halamanResumen InmunodannymalcacamposBelum ada peringkat
- InmunoglobulinasDokumen10 halamanInmunoglobulinasCdcgs PWinBelum ada peringkat
- Línea de Defensa Celular - Jeremy BrunoDokumen10 halamanLínea de Defensa Celular - Jeremy BrunoSILVIA ROSARIO CHALCO MENDOZABelum ada peringkat
- El Glucocálix o Cubierta CelularDokumen3 halamanEl Glucocálix o Cubierta CelularAna Isabel Andrade Cedeño100% (1)
- Inmunidad Covy 3meses PDFDokumen6 halamanInmunidad Covy 3meses PDFSkipy RosalesBelum ada peringkat
- Fiebre AmarillaDokumen24 halamanFiebre AmarillaStefhany HernandezBelum ada peringkat
- Tarea Aminoacidos Bioquimica II Fase2Dokumen9 halamanTarea Aminoacidos Bioquimica II Fase2Francisco Edgardo VillegasBelum ada peringkat
- Crucigrama 9 AlejoDokumen2 halamanCrucigrama 9 Alejodufrany50% (2)
- 2014 Demre 17 Resolucion Ciencias Parte3Dokumen20 halaman2014 Demre 17 Resolucion Ciencias Parte3Joaquín CabelloBelum ada peringkat