Informe 1 Quimfi Constantes de Equilibrio para El Naranja de Metilo
Diunggah oleh
Juan ArangoJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Informe 1 Quimfi Constantes de Equilibrio para El Naranja de Metilo
Diunggah oleh
Juan ArangoHak Cipta:
Format Tersedia
Determinacin espectrofotomtrica del pKa de un
indicador
Tabla de contenido
Objetivos..2
Introduccin.2-3
Materiales y reactivos..4
Metodologa.4-5
Datos6-7
Clculos7-8
Resultados y discusin.9-14
Conclusin.....15
Referencias16
Determinacin espectrofotomtrica del pKa de un
indicador
Objetivos
Obtener el espectro de absorcin del naranja de metilo en disoluciones de
diferentes pH.
Relacionar las absorbancias de stas disoluciones con las concentraciones de
indicados en sus formas cida y bsica.
Obtener el pKa del indicador naranja de metilo, a partir de las absorbancias
medidas.
Introduccin
Debido a que los espectros que presentan las sustancias en el rango
ultravioleta-visible (UV-Vis) varan de acuerdo a las condiciones en las que se
encuentran, el estudio de los mismos es utilizado en muchas aplicaciones.
Factores como la temperatura, el pH, el tipo de disolvente o simplemente el
estado fsico de la materia son responsables de que una sustancia presente
diferentes espectros. Estos cambios son relacionados a propiedades
fisicoqumicas de la materia [3].
La espectrofotometra puede ser utilizada para cuantificar analitos;
utilizando la ecuacin Beer-Lambert, mediante cuervas de calibracin, o
determinar el pKa de un indicador usando diversos rangos de pH con el
mismo analito, aplicando la ecuacin de Henderson-Hasselbach si se est
trabajando con soluciones amortiguadoras, como en este caso [1].
Un indicador de pH, es un tinte que cambia de color cuando la
solucin en la que se encuentra presenta cambios en su concentracin de
protones. La variacin en coloracin depende tambin de la cantidad de luz
que la molcula absorbe. Esta propiedad los hace tiles para poder detectar
el punto de equivalencia durante valoraciones cido-base. Igual que los
colores que presenta el indicador, los espectros de absorcin UV-Vis varan de
acuerdo al pH de la solucin. Sin embargo, estos espectros de absorcin
tienen un punto en comn conocido como punto isosbstico. En dicho punto,
la absortividad molar de la forma cida y la alcalina son iguales [2]-[4]. Un
indicador estar en equilibrio con su base conjugada mediante la siguiente
ecuacin:
HIn + H2O In- + H3O+
Para la determinacin del pKa de naranja de metilo se obtuvieron los
espectros de absorcin visible de la especie protonada, deprotonada y tres
soluciones amortiguadoras (25%, 50% y 75%). Los espectros resultantes
fueron registrados en una misma grfica para obtener el punto isosbstico
del indicador. En dicho punto la absorbancia de las cinco especies es la
misma o es muy cercana. Para relacionar el cociente de las concentraciones
2
Determinacin espectrofotomtrica del pKa de un
indicador
se utiliza la frmula de Henderson y Hasselbach ajustada a cada especie bajo
estudio. A partir de esta ecuacin de puede deducir que:
pH= pKa + log (
)
[Hin ]
Lleva a:
A A
A H A
pH= pKa + log (
)
Siendo AH In la absorbancia de la especie protonada de naranja de metilo,
la
absorbancia de la especie deprotonada y A la absorbancia del amortiguador con el
que se est trabajando. Esta relacin nos permite obtener a partir de absorbancias
de espectros con el analito de inters a diferentes pH, el pKa del compuesto.
Sabiendo los pH experimentales de cada disolucin amortiguadora preparada.
De igual forma mediante la ecuacin de Beer Lambert (A=lC), se puede comprobar
tericamente que el coeficiente de absortividad molar (), de la especie en sus
distintos pH coincide. Despejando para en la frmula original de obtiene:
= lc
Donde A representa la absorbancia de las especies en el punto isosbstico
determinado arbitrariamente, l representa el largo del paso ptico en cm, y C
representa la concentracin del indicador de naranja de metilo en mol/L o M.
Determinacin espectrofotomtrica del pKa de un
indicador
Materiales
2 matraces aforados de 250 mL
2 matraces aforados de 25 mL
3 matraces de Erlenmeyer de 250 mL
2 vasos de precipitados de 100 mL
1 pipeta graduada de 25 mL
1 pipeta aforado de 10 mL
1 pipeta graduada de 2 mL
1 bureta de 50 mL
2 clulas de espectrofotmetro de plstico
1 espectrofotmetro UV-VIS
Reactivos
Hidrxido de sodio en hojuelas.
Disolucin de hidrxido de sodio 2M.
Disolucin de naranja de metilo al 96%
cido clorhdrico 12M.
cido frmico 90%
Indicador de fenolftalena
Metodologa
Disoluciones
A partir cido frmico 96%, se prepararon 250 mL de una disolucin
0.1M.
Determinacin espectrofotomtrica del pKa de un
indicador
Se prepararon 250 mL de una disolucin 0.1M de hidrxido de sodio
NaOH.
Procedimiento experimental
Se prepararon las disoluciones de cido frmico y de hidrxido de
sodio.
Se valor la disolucin 0.1M de cido frmico con NaOH 0.1M, usando
fenolftalena como indicador. La valoracin se realiz tres veces.
Espectro de absorcin de la forma acida del indicador
Se prepar un blanco donde se extrajo 10 mL de agua, se le aadi 4
gotas de HCl concentrado y se aforo hasta 25 mL. Luego la disolucin
se pas a una clula del espectrofotmetro.
Se prepar una disolucin de naranja de metilo de 0.002% donde se
extrajo 10 mL, se le aadi 4 gotas de HCl concentrado y se aforo
hasta 25 mL.
Se trabaj en el espectrofotmetro a 100% de absorbancia, con el
blanco y se midi la absorbancia de la disolucin problema.
Espectro de absorcin de la forma bsica del indicador
Se prepar un blanco donde se extrajo 10 mL de agua, se aadi 24
gotas de NaOH 2M y se aforo hasta 25 mL. La disolucin se pas a una
clula del espectrofotmetro.
Se prepar una disolucin de naranja de metilo de 0.002% donde se
extrajo 10 mL, se le aadi 24 gotas de NaOH y se aforo hasta 25 mL.
Se procedi como en el registro del espectro de absorcin de la forma
acida del indicador.
Espectro de absorcin de una disolucin donde estn presentes
ambas formas del indicador
Se prepar una disolucin tampn en un matraz Erlenmeyer con 25 mL
de disolucin 0.1M de cido frmico y luego se le aadi un volumen
de NaOH 0.1M igual al 50% del volumen de NaOH utilizado en la
valoracin promedio del cido frmico. Tambin se prepararon unos
buffer de 25% y 75% del volumen utilizado en la valoracin.
Se prepar un blanco donde se extrajo 10 mL de agua y afor a 25 mL
con la disolucin amortiguadora.
Se prepar una disolucin de naranja de metilo 0.002% y se enraso a
25 mL con la primera disolucin amortiguadora.
Determinacin espectrofotomtrica del pKa de un
indicador
Reactivos
Concentraci
n real
cido frmico 0.1M
0.08
Hidrxido de sodio 0.1
0.1M
Hidrxido de sodio 2M 0.2
Naranja de metilo 0.002%
0.002%
Cantidad
medida
2.0 ml
1.0354 g
Error
medida
0.05ml
0.0001g
4.0012 g
0.0021 g
0.0001g
0.0001g
Datos
Tabla 1.Valoracin del NaOH 0.1M con cido frmico 0.1M
Valoracion
es
#1
#2
#3
Promedio
Volumen ml
18.9
18.6
18.6
18.7
Error
0.05
0.05
0.05
0.14
Tabla 2. Concentraciones calculadas
Reactivos
Concentracin
cido frmico
Hidrxido
de
sodio
Hidrxido
de
sodio
Naranja
de
metilo
0.1M
0.1M
Cantidad
Calculada
2.13 mL
1.0 g
2M
4.0 g
0.002%
2.08 x 10-3 g
Tabla 3. Concentraciones reales
Determinacin espectrofotomtrica del pKa de un
indicador
Clculos
Preparacin de 250 mL de disolucin 0.1M de cido frmico a partir
del cido frmico concentrado 90%.
Mol = 0.1M x 0.5 L = 0.05 mol cido frmico
46 g acido formico
0.05 mol cido frmico x ( 1 mol acido formico
1mL
x ( 1.2 g
x(
100
90
2.13 mL
Concentracin real de cido frmico
2.0 mL x (
1 mol acido formico
1.2 g
x(
46 g acido formico
1mL
x(
100
90
= 0.05 mol cido
frmico
M=
0.05mol acido formico
0.5 L
= 0.08 M
Determinacin espectrofotomtrica del pKa de un
indicador
Preparacin de 250 mL de disolucin 0.1M de hidrxido de sodio
Mol = 0.1M x 0.25L = 0.025 moles NaOH
40 g NaOH
0.025 moles NaOH x ( 1 mol NaOH
=1.0 g NaOH
Concentracin real del NaOH 0.1 M
1.0354 g NaOH x (
M=
1 mol NaOH
= 0.025 mol NaOH
40 g NaOH
0.025mol NaOH
0.25 L
= 0.1M
Preparacin de 500 mL de disolucin 2Mde hidrxido de sodio
Mol = 2M x 0.05L = 0.1 mol NaOH
40 g NaOH
0.1 mol x ( 1 mol NaOH
= 4.0 g NaOH
Concentracin real de NaOH 2M
4.0012 g NaOH x (
M=
0.1mol NaOH
0.05 L
1 mol NaOH
40 g NaOH ) = 0.1 mol NaOH
= 2M
Preparacin de la disolucin de naranja de metilo 0.002% a partir de
solucin 96%
M1= 96g/100ml
V1=x
M2=0.002g/100ml
8
Determinacin espectrofotomtrica del pKa de un
indicador
V2= 100ml
M1xV1=M2xV2
V1=
M 2V 2
M1
V1=
0.002100
3
= 2.08x 10 g
96
o 2.08mg
Concentracin real de naranja de metilo
21.0mg
x
2.08mg 0.002%
X= (21.0 x 0.002)/ 2.08
X= 0.002 %
Resultados
1. Espectros de absorcin de soluciones de naranja de metilo en
forma bsica, acida y buffers al 25%, 50% y 75%.
Determinacin espectrofotomtrica del pKa de un
indicador
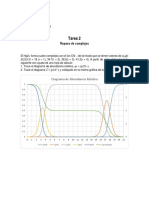
ESPECTROS DE ABOSRCION DE SOLUCIONES DE NARANJA DE METILO A DIFERENTES pH
0.9
0.8
0.7
NARANJA DE METILO BASICO Ph~14
NARANJA BUFFER 25%
NARANJA BUFFER 50%
NARANJA BUFFER 75%
0.6
0.5
Absorbance
0.4
0.3
NARANJA DE METILO ACIDO Ph~1
0.2
0.1
0
390 400 410 420 430 440 450 460 470 480 490 500 510 520 530 540 550 560 570 580 590 600 610 620 630 640 650
wavelenght (nm)
Imagen 1. Espectros de absorcin de las soluciones de naranja de metilo a diferentes pH. Es observable el punto isosbstico.
2. Determinacin de los pKa del indicador a diferentes valores de
longitud de onda.
PKa terico del naranja de metilo: 3.47, [2].
Se escogieron dos longitudes de onda arbitrariamente para determinar los
pKa.
Primera
longitud
de
onda
seleccionada,
punto
escogido
arbitrariamente a la mayor distancia entre espectros: 511nm,
En esta longitud de onda las absorbancias fueron:
Tabla4. Absorbancias de analitos a 511nm y a 472.8nm
Largos de onda seleccionados para clculos del pKa
Absorbancia a
Absorbancia a
Solucin
511nm
472.8nm
Bsica
0.234
0.485
Acida
0.863
0.534
Buffer
25%
0.611
0.515
Buffer
50%
0.434
0.5
Buffer
75%
0.301
0.49
10
Determinacin espectrofotomtrica del pKa de un
indicador
Teniendo en cuenta la formula pH=Pk+log
A Hin A
AA
por lo tanto:
A Hin A
PKa= pH- log ( A A )
Se usan los pH calculados experimentalmente para calcular los PKa
PKa del buffer 25%
0 .8630 . 611
PKa= 3.38 - log ( 0 .6110 . 234 ) = 3.55
PKa del buffer 50%
0 .8630 . 434
PKa = 3.86 - log ( 0 . 4340 .234 ) = 3.53
PKa del buffer 75%
0 .8630 . 301
PKa = 4.43 - log ( 0 .3010 .234 ) = 3.51
Segunda longitud de onda seleccionada, punto seleccionado cerca al
punto isosbstico: 472.8 nm.
En esta longitud de onda las absorbancias fueron:
PKa del buffer 25%
0 .5340 . 515
PKa = 3.38 - log ( 0 .5150 . 485 ) = 3.57
PKa del buffer 50%
0 .5340 . 500
PKa = 3.86 - log ( 0 .5000 . 485 ) = 3.50
PKa del buffer 75%
0 .5340 . 490
PKa= 4.43 - log ( 0 . 4900 . 485 ) = 3.48
Tabla5. Comparacin de los clculos obtenidos para los pKa de los
amortiguadores
11
Determinacin espectrofotomtrica del pKa de un
indicador
Comparacin de los pKa en los dos largos de onda
seleccionados
pKa
pka50
pKa
Prome
% error vs
nm
25%
%
75%
dio
Terico
511
3.55
3.53
3.51
3.53
1.70
472.8
3.57
3.50
3.48
3.52
1.33
La imagen 1 muestra que los espectros de absorcin realizados en efecto se
cruzaron en un punto especfico de absorbancia, punto isosbstico. Lo que
nos confirma que las soluciones de inters fueron realizadas con las
concentraciones correctas.
Para calcular a partir de la informacin de esta imagen los pKa de las
soluciones amortiguadoras, se despejo la ecuacin de Henderson y
hasselbach derivada para el uso de absorbancias para pKa, debido a que el
resto de datos necesarios se saban, como el pH de cada solucin
amortiguadora y la absorbancia en un punto arbitrariamente escogido.
El primer largo de onda que se escogi (511nm) fue un punto en el que los
espectros se encontraran lo ms distante posible entre ellos, mientras que el
segundo punto seleccionado fue un punto cercano al punto isosbstico de la
imagen 1 (478.2nm). Segn la teora, se esperara que en este punto de
mayor distancia entre espectros se obtuvieran pKa ms cercanos al valor
terico.
El valor terico de pK a del naranja de metilo es 3.47, los valores calculados se
presentan en la tabla 6, muestran que en este experimento los valores
calculados en los dos largos de onda seleccionados son muy similares y con
una diferencia entre medias de solo 0.01, y caso contrario a la teora el calor
ms cercano al PKa terico del indicador, se obtuvo en el largo de onda ms
cercano al pinto isosbstico. Se entiende que no necesariamente este
fundamento aplica ya que la eleccin de los largos de onda son arbitrarios en
este caso el punto isosbstico demuestra una relacin buena entre los
analitos en este punto, es decir no se ve una separacin marcada de algn
espectro con respecto a otro. Analizando los % de error de los resultados para
cada uno de los largos de onda escogidos (1.70% para 511nm y 1.33 para
472.8nm) demuestra que la precisin del experimento fue buena y la
desviacin entre resultados no es considerable con respecto al PKa terico.
3. Longitud de onda del punto isosbstico y coeficientes de
absortividad molar de la solucin en forma acida y bsica del
indicador naranja de metilo.
A= lc
=A/lc
Tabla 6. Absorbancias en el punto isosbstico.
12
Determinacin espectrofotomtrica del pKa de un
indicador
Datos para calcular
Indicad Absorbancias en
or
469.6 nm
Acido
0.492
Bsico
0.491
5
Concentracin de la solucin de naranja de metilo: 6.42x 10 M
Largo del paso ptico: 1cm
Coeficiente de absortividad molar del indicador cido:
=
0.492
1 x 6.42 x 105
= 7.66 x
10
Coeficiente de absortividad molar del indicador bsico:
=
0.491
1 x 6.42 x 105
= 7.65 x
103
El valor de largo de onda elegido de manera arbitraria como punto
isosbstico por la similitud o igualdad de absorbancias en este punto fue
469.6nm.
El coeficiente de absortividad molar se puede determinar a partir de la
ecuacin de Beer Lambert, que aplica para este experimento debido a la
dilucin de la soluciones con las que se est trabajando [4]. Despejando para
psilon se, se puede obtener mediante un clculo muy sencillo este dato.
Para calcular la concentracin de la solucin de naranja de metilo en
trminos de molaridad, se tom la cantidad de gramos pesada y se relacion
5
con el volumen de la dilucin, la concentracin calculada fue 6.42x 10 M .
Respecto a los resultados se muestra que es muy similar para el indicador
cido y para el indicador bsico, lo que demuestra que en este punto el
coeficiente de absortividad molar es bastante similar para estas dos formas
del indicador de naranja de metilo.
4. PH de las disoluciones amortiguadoras y comparacin con los pH
determinados experimentalmente.
PKa del cido frmico es 3.75.
PH se calcula usando la ecuacin de Henderson y Hasselbach
PH= PKa + log (
[ Base conjugada]
[acido]
Tabla 7. Volmenes de cido y base usados para cada amortiguador.
13
Determinacin espectrofotomtrica del pKa de un
indicador
Volmenes usados para soluciones amortiguadoras
Volumen
Volumen
Amortigua
(ml), Acido
Volumen
(ml) NaOH
dor
Frmico
total (L)
0.1M
0.1M.
25%
4.7
25
0.0297
50%
9.3
25
0.0343
75%
14
25
0.039
++ H 2 O
Na
HCOO
La reaccin es: HCOOH + NaOH
pH buffer 25:
HCOOHaq
IN
2.5x 10
NaOH aq
+aq + H 2 O
Na
HCOO
4.7x 10 mol
mol
0mol
1 . 87 x 103 mol
0 . 02970 L
EQ
(l)
0 mol
6 . 25 x 10 mol
0.02970 L
2
4.81x 10 M
1.60x
10 M
2
1.60 x 10 M
pH= 3.75 + log (
= 3.27
pH terico del amortiguador 25%: 3.27
pH buffer 50%:
HCOOH
(aq)
NaOH
(aq)
+(aq )+ H 2 O
Na
HCOO
(l)
14
Determinacin espectrofotomtrica del pKa de un
indicador
IN
2.5x 10
9.3x 10 mol
mol
0mol
1 . 25 x 103 mol
0 .0343 L
EQ
0 mol
1 . 25 x 10 mol
0.0343 L
2
3.64x 10 M
3.64x
10 M
2
3.64 x 10 M
pH= 3.75 + log (
= 3.75
pH terico del amortiguador 50%: 3.75
pH buffer 75%:
HCOOHaq
IN
2.5x 10
NaOH aq
1.4x 10 mol
mol
+aq + H 2 O
Na
HCOO
(l)
0mol
6 . 25 x 10 mol
0 . 039 L
EQ
0 mol
1 . 88 x 10 mol
0.039 L
2
1.62x 10 M
4.808x
10 M
2
[4.808 x 10 M ]
PH= 3.75 + log ( [1.62 x 102 M ] = 4.22
PH terico del amortiguador 75%: 4.22
15
Determinacin espectrofotomtrica del pKa de un
indicador
Tabla 8. PH calculados con % de error de los amortiguadores.
Relacin de pH calculados versus medidos
pH
% de
Amortiguador
pH Terico
experimental error
25%
3.27
3.38
3.36
50%
3.75
3.86
2.93
75%
4.22
4.43
4.98
En la tabla 8, se muestran los resultados de los clculos de los PH tericos
para los tres amortiguadores usados durante esta experiencia, junto con el %
de error de cada valor terico obtenido en relacin con los valores
experimentales obtenidos
Para el clculo del ph se us la frmula de Henderson y hasselbach, relacin
que se puede usar fcilmente para calcular el pH de cualquier solucin
amortiguadora, sabiendo las concentraciones del cido usado y por
estequiometria, determinando la concentracin de la base conjugada que se
forma despus de la disociacin parcial de dicho acido (cido dbil).
La tabla 7 muestra los volmenes usados para cada amortiguador, a partir de
estos datos por estequiometria se determinaron las moles iniciales de cido
frmico y de NaOH en la solucin antes de llegar a equilibrio; posteriormente
se procedi a calcular las moles en equilibrio, gracias a la titulacin hecha de
NaOH con la solucin de cido frmico se pudo determinar una relacin
porcentual para poder hacer cada amortiguador y por lo tanto se pudo
tambin determinar la distribucin de moles en la solucin entre acido
frmico y su base conjugada, formiato de sodio.
Ya que la cantidad de moles de cido frmico de mantuvo constante en los
tres amortiguadores, solo fue necesario calcular la distribucin de la misma
cantidad de moles, segn el porcentaje de cada solucin tampn.
Una vez obtenidas la cantidad de moles presentes en equilibrio tanto del
cido como de su base conjugada, se relacion este dato con el volumen
total de la solucin hecha para poder calcular la concentracin de cada una
de estas especies en solucin y as poder calcular el pH usando la formula
previamente mencionada de Henderson y Hasselbach.
Respecto a los resultados de aprecia una cercana entre los datos obtenidos
tericamente con respecto a los datos experimentales, el % de error de cada
uno de los clculos en comparacin con los datos medidos en el laboratorio
sugiere una baja desviacin y supone una correcta practica de laboratorio
adems de un planteamiento correcto del equilibrio mediante el cual se
consigui la concentracin de formiato de sodio, la base conjugada del cido
actico.
16
Determinacin espectrofotomtrica del pKa de un
indicador
Conclusin
La espectroscopia UV-VIS nos brinda una forma relativamente sencilla de
calcular el pKa de un compuesto a partir soluciones con dicho compuesto
a diferentes pH, siendo el pH el factor que me permite diferenciar entre
espectros y relacionarlos a la hora de calcular dicha constante.
A partir de la relacin de Henderson y Hasselbach, se puede derivar una
forma de relacionar absorbancias con constantes de disociacin y pH.
El punto isosbstico sugiere que la preparacin de los analitos fue correcta
en cuanto a pH y a concentracin.
En efecto en el punto isosbstico las absorbancias de los espectros de
cada analito coinciden, por lo tanto al tenerse un indicador en igual
concentracin en la forma bsica o acida, se puede predecir que el
coeficiente de absortividad molar ser muy similar o igual entre especies,
los clculos realizados lo confirman.
Soluciones acidas tienen mayor absorcin de luz que las soluciones
bsicas.
En este experimento no se logr obtener una diferencia significativa entre
los pKa calculados tomando largos de onda en donde se considerara que
los espectros estaban distantes y el largo de onda tomado carca al punto
isosbstico.
La obtencin de los objetivos del experimento sugiere que el mismo fue
correcto y los procedimientos fueron realizados con exactitud.
17
Determinacin espectrofotomtrica del pKa de un
indicador
Referencias
[1]. Pavia D., Lampman G. Introduction to spectroscopy. 2009. Cengage
Learning, Fourth Ed.
[2]. R. Sanjeev, V. Jagannadham, R. Veda Vrath. Implications of a novel
interpretation of the isosbestic point. Chemistry in New Zealand. October 2012.
[3]. Chang, R., Chemistry. McGraw Hill Education. 2009. Ninth Ed.
[4]. Douglas Skoog, Donald West, F. Holler, Stanley Crouch. Fundaments of
Analytical Chemistry, 2013, 9th ed. Cengage Learning.
18
Anda mungkin juga menyukai
- Puntos de Fusión: Factores que Influyen y Métodos de DeterminaciónDokumen3 halamanPuntos de Fusión: Factores que Influyen y Métodos de DeterminaciónAlejandra CéspedesBelum ada peringkat
- PRACTICA No.7 QaDokumen7 halamanPRACTICA No.7 QaCRISTIAN MACIASBelum ada peringkat
- Ejercicios 2do Parcial Quimica Guia 2022Dokumen43 halamanEjercicios 2do Parcial Quimica Guia 2022Wilmer Adhemar Zarzuri TenorioBelum ada peringkat
- QA Problemas de QuímicaDokumen22 halamanQA Problemas de Químicagr4ndeunicornBelum ada peringkat
- Serie 3 Equilibrio Quimico 4540Dokumen2 halamanSerie 3 Equilibrio Quimico 4540Yassel4Belum ada peringkat
- Reporte Post-Laboratorio. Práctica 6Dokumen5 halamanReporte Post-Laboratorio. Práctica 6KarenBelum ada peringkat
- Informe Velocidad de H2o2Dokumen20 halamanInforme Velocidad de H2o2ALEJANDRA LUCERO MEJ�A CRUZBelum ada peringkat
- Laboratorio Analítica Práctica 3Dokumen11 halamanLaboratorio Analítica Práctica 3Ethel DekkerBelum ada peringkat
- (176305948) Practica - Nro3 ReaccionesDokumen13 halaman(176305948) Practica - Nro3 ReaccionesJuan Carlos Calle100% (1)
- Lectura 11Dokumen20 halamanLectura 11Gonzalo A. NazalBelum ada peringkat
- Informe Tema 6Dokumen13 halamanInforme Tema 6Daniel Vargas TrujilloBelum ada peringkat
- Lab Oratorio 8Dokumen18 halamanLab Oratorio 8erickasegoviacaceresBelum ada peringkat
- Determinación de La Constante de Equilibrio de Un IndicadorDokumen5 halamanDeterminación de La Constante de Equilibrio de Un IndicadorMaryjoseLeónBelum ada peringkat
- Problemario U2Dokumen6 halamanProblemario U2JUAN GERARDO CIGARROA RENDONBelum ada peringkat
- Lab 1, Determinacion de La Masa Molar Exacta de Un GasDokumen7 halamanLab 1, Determinacion de La Masa Molar Exacta de Un GasNicolas Riffo LepeBelum ada peringkat
- Descomposicion Peroxido de HidrogenoDokumen8 halamanDescomposicion Peroxido de HidrogenoDaniel PadillaBelum ada peringkat
- Aruquipa Mamani Cristhian Cinetica Quimica 8 PDFDokumen19 halamanAruquipa Mamani Cristhian Cinetica Quimica 8 PDFCristhian Aru.Belum ada peringkat
- Cuestionario Laboratorio 7Dokumen6 halamanCuestionario Laboratorio 7Alvaro Razim Arce DelgadilloBelum ada peringkat
- Análisis GravimetricoDokumen14 halamanAnálisis GravimetricoOscar E RS100% (1)
- E2208004 6 Taller Smog FotoquimicoDokumen8 halamanE2208004 6 Taller Smog FotoquimicoRaul GranadosBelum ada peringkat
- Ejercicios Parcial I Del Dos 2022Dokumen4 halamanEjercicios Parcial I Del Dos 2022Andres RamBelum ada peringkat
- Cuestionario 1 FQIIDokumen4 halamanCuestionario 1 FQIIBryan BautistaBelum ada peringkat
- Determinación de Pureza Del Agua OxigenadaDokumen10 halamanDeterminación de Pureza Del Agua OxigenadaGerson Morales RodriguezBelum ada peringkat
- S13. GravimetriaDokumen28 halamanS13. Gravimetriaeverth sebastian lopez laureanoBelum ada peringkat
- Tallerdeunidadesdeconcentración2020 IDokumen4 halamanTallerdeunidadesdeconcentración2020 ILuis Enrique LagunaBelum ada peringkat
- Taller1 1 2018Dokumen7 halamanTaller1 1 2018Ana M. Galan PérezBelum ada peringkat
- INFORME PRÁCTICA 5 Sulfatos (Autoguardado)Dokumen8 halamanINFORME PRÁCTICA 5 Sulfatos (Autoguardado)Jeremy HernandezBelum ada peringkat
- Valoración ácido-base conductimétrica HClDokumen3 halamanValoración ácido-base conductimétrica HClFede SalasBelum ada peringkat
- Determinación de dureza total en aguasDokumen4 halamanDeterminación de dureza total en aguasRicardo Aragón100% (1)
- Guión Ley de Enfriamiento de NewtonDokumen4 halamanGuión Ley de Enfriamiento de NewtonFrida Arroyo ChavarriaBelum ada peringkat
- Comportamiento de sistemas gaseososDokumen10 halamanComportamiento de sistemas gaseososDavid Fernandez0% (1)
- Ejercicios 2 ResueltaDokumen3 halamanEjercicios 2 ResueltaValeria MeldyBelum ada peringkat
- Calor Molar de Una Reacción QuímicaDokumen6 halamanCalor Molar de Una Reacción QuímicaSebastian PertuzBelum ada peringkat
- Informe 13N ConductividadDokumen17 halamanInforme 13N ConductividadNICK MARALLANOBelum ada peringkat
- Dicromato y TiosulfatoDokumen9 halamanDicromato y TiosulfatoJuan TorresBelum ada peringkat
- Reacciones de CondensacionDokumen10 halamanReacciones de CondensacionMari Marisol RodriguezBelum ada peringkat
- Masa Molar de Un LíquidoDokumen12 halamanMasa Molar de Un LíquidoAlfonso RodríguezBelum ada peringkat
- Síntesis de Bromuro de Isopropilo (Informe)Dokumen12 halamanSíntesis de Bromuro de Isopropilo (Informe)gerson velezBelum ada peringkat
- Separación de Una Solución de Violeta de CristalDokumen7 halamanSeparación de Una Solución de Violeta de CristalAlbita GarciaBelum ada peringkat
- Presión ultracentrífuga agua tubo ensayoDokumen8 halamanPresión ultracentrífuga agua tubo ensayoAracelicitaBelum ada peringkat
- Volumetrías directas y por retrocesoDokumen5 halamanVolumetrías directas y por retrocesojuan paBelum ada peringkat
- Problemas Tema 8Dokumen6 halamanProblemas Tema 8CHOLOSIMEONEBelum ada peringkat
- Para Obtener La Concentración Molar de Iones Hidroxilo en Una Solución de Hidróxido de Calcio Se Debe Calcular El Cociente Entre La Masa en Gramos de CaDokumen4 halamanPara Obtener La Concentración Molar de Iones Hidroxilo en Una Solución de Hidróxido de Calcio Se Debe Calcular El Cociente Entre La Masa en Gramos de CaKarenBelum ada peringkat
- Conductividad electrolítica: propiedades y mediciónDokumen11 halamanConductividad electrolítica: propiedades y mediciónDiego FierroBelum ada peringkat
- 11solubilidad 1Dokumen21 halaman11solubilidad 1Miguel RomeroBelum ada peringkat
- Volumetria Oxido Reducciòn PermanganometriaDokumen6 halamanVolumetria Oxido Reducciòn PermanganometriaAndres MorenoBelum ada peringkat
- Taller 2 Química Física.........................Dokumen12 halamanTaller 2 Química Física.........................OM TfaBelum ada peringkat
- Práctica: Determinación de La Densidad de Un GasDokumen8 halamanPráctica: Determinación de La Densidad de Un GasDiana RojasBelum ada peringkat
- Determinacion de La Curva de Solubilidad FINALDokumen10 halamanDeterminacion de La Curva de Solubilidad FINALmariaBelum ada peringkat
- Equilibrio químico etanol-ácido acéticoDokumen9 halamanEquilibrio químico etanol-ácido acéticosupertokyBelum ada peringkat
- Inf. Lab. 2 ExtraccionDokumen12 halamanInf. Lab. 2 ExtraccionJhenny JimenezBelum ada peringkat
- P10 Marylett Garcia ReporteTermoDokumen10 halamanP10 Marylett Garcia ReporteTermoMary GarcíaBelum ada peringkat
- Cuestionario Punto de FusionDokumen3 halamanCuestionario Punto de FusionALEJANDRA CESPEDES PEREZBelum ada peringkat
- Equilibrio químico y solubilidadDokumen5 halamanEquilibrio químico y solubilidadMariana TreviñoBelum ada peringkat
- 04 Ejercicios Red OxDokumen16 halaman04 Ejercicios Red OxEduard RomeroBelum ada peringkat
- Memoria Práctica 2 PDFDokumen11 halamanMemoria Práctica 2 PDFFran GarnesBelum ada peringkat
- Desplazamiento de Bandas y Determinación Espectrofotométrica Del Pka de Un IndicadorDokumen17 halamanDesplazamiento de Bandas y Determinación Espectrofotométrica Del Pka de Un IndicadorKaysser Alberto Villar CaleroBelum ada peringkat
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDari EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadBelum ada peringkat
- Titulacion Acido BaseDokumen9 halamanTitulacion Acido BaseJuan ArangoBelum ada peringkat
- Campo y Potencial EléctricoDokumen11 halamanCampo y Potencial EléctricoJuan ArangoBelum ada peringkat
- Informe 1 Quimfi Constantes de Equilibrio para El Naranja de MetiloDokumen18 halamanInforme 1 Quimfi Constantes de Equilibrio para El Naranja de MetiloJuan ArangoBelum ada peringkat
- Determination of Equilibrium Constant For The Estherification of Acetic Acid and Ethanol With HCLDokumen17 halamanDetermination of Equilibrium Constant For The Estherification of Acetic Acid and Ethanol With HCLJuan ArangoBelum ada peringkat
- Taller tipo parcial capitulos 3, 4 ,5 ,6Dokumen5 halamanTaller tipo parcial capitulos 3, 4 ,5 ,6Sofía ViteriBelum ada peringkat
- Practica 4 Volumetria de NeutralizacionDokumen29 halamanPractica 4 Volumetria de NeutralizacionAngel Flores CuamatziBelum ada peringkat
- Cuestionario ComplexometriaDokumen1 halamanCuestionario ComplexometriaJhenny RosarioBelum ada peringkat
- Titulacion PotenciometricaDokumen8 halamanTitulacion PotenciometricaRodrigo SilvaBelum ada peringkat
- Teoría de Lewis sobre ácidos y basesDokumen96 halamanTeoría de Lewis sobre ácidos y basesAndres ECBelum ada peringkat
- Redes de BravaisDokumen6 halamanRedes de BravaisArguijo Sergio MiguelBelum ada peringkat
- La Presión Parcial de Un GasDokumen4 halamanLa Presión Parcial de Un GasJess CatotaBelum ada peringkat
- Grados LibertadDokumen20 halamanGrados LibertadXimena GuzmánBelum ada peringkat
- Informe de Ánalisis Químico Con KhejjdalDokumen3 halamanInforme de Ánalisis Químico Con KhejjdalAlbertoBelum ada peringkat
- Grupo 2 Metodos de SeparacionDokumen19 halamanGrupo 2 Metodos de SeparacionAnel GCBelum ada peringkat
- Curva de TitulacionDokumen4 halamanCurva de TitulacionDulce Esmeralda Hernández MartínezBelum ada peringkat
- Reporte de Calculo de PH - 101708 PDFDokumen17 halamanReporte de Calculo de PH - 101708 PDFchochin HernandezBelum ada peringkat
- Analitica. Tarea 2Dokumen4 halamanAnalitica. Tarea 2david Santillán GonzálezBelum ada peringkat
- Cuestionario Equilibrio FisicoDokumen7 halamanCuestionario Equilibrio FisicoKarla OrtegaBelum ada peringkat
- Informe Técnico N°8 - GRUPO 5Dokumen14 halamanInforme Técnico N°8 - GRUPO 5MUÑOZ LUNA GIANCARLOBelum ada peringkat
- Análisis conductimétricoDokumen22 halamanAnálisis conductimétricoSILVIA MILAGROS SOTO CATASIBelum ada peringkat
- Características de Las Principales Funciones Químicas InorgánicasDokumen3 halamanCaracterísticas de Las Principales Funciones Químicas InorgánicasHernan Osorio33% (3)
- TALLERDokumen3 halamanTALLERIsabella Rivera DiazBelum ada peringkat
- 6-Equilibrios Acido Base IDokumen33 halaman6-Equilibrios Acido Base IVaiiolet VaiioletBelum ada peringkat
- Resolución Del Laboratorio Virtual MolaridadDokumen7 halamanResolución Del Laboratorio Virtual Molaridadfiorella larreaBelum ada peringkat
- Extra Problems Final ExamDokumen2 halamanExtra Problems Final ExamMiranda Escamilla PerezBelum ada peringkat
- Universidad Nacional José Faustino Sánchez CarriónDokumen7 halamanUniversidad Nacional José Faustino Sánchez CarriónGabriel ChiritoBelum ada peringkat
- Historia Quimica AnaliticaDokumen6 halamanHistoria Quimica AnaliticaBriellydalia Garcia SanquintinBelum ada peringkat
- Practica 6 Quimica Industrial UPIICSADokumen20 halamanPractica 6 Quimica Industrial UPIICSAIsa Godínez60% (5)
- Guia de Laboratorio 2 - Volumetria de PrecipitacionDokumen3 halamanGuia de Laboratorio 2 - Volumetria de PrecipitacionJohan RojasBelum ada peringkat
- Titulación potenciométrica de KOH con ftalato ácidoDokumen3 halamanTitulación potenciométrica de KOH con ftalato ácidoLeonardo BermudezBelum ada peringkat
- Informe 6 AnaliticaDokumen7 halamanInforme 6 Analiticaana gabriela muñozBelum ada peringkat
- Informe #1 PotenciometriaDokumen9 halamanInforme #1 PotenciometriaMeylin JimenezBelum ada peringkat
- Valoracion de SolucionesDokumen8 halamanValoracion de SolucionesRoberto Figueroa100% (1)
- Determinación de La Constante de Acidez de Un Indicador Ácido Base.Dokumen5 halamanDeterminación de La Constante de Acidez de Un Indicador Ácido Base.Lisa HigginsBelum ada peringkat