Bases Moleculares Del Hipotiroidismo Congénito
Diunggah oleh
Kevin Guevara AlvaradoJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Bases Moleculares Del Hipotiroidismo Congénito
Diunggah oleh
Kevin Guevara AlvaradoHak Cipta:
Format Tersedia
Bases moleculares del hipotiroidismo congnito
Molecular bases of congenital hypothyroidism
Dra. Estefana PinznSerrano, Dra. Vernica Morn Barroso, Dra. Ninel CoyoteEstrada Departamento de Endocrinologa Peditrica, Departamento de Gentica, Hospital Infantil de Mxico Federico Gmez, Mxico, D. F., Mxico. Solicitud de sobretiros: Dra. Vernica Fabiola Morn Barroso Depto. de Gentica, Hospital Infantil de Mxico, Federico Gmez Dr. Mrquez 162, Col. Doctores, Deleg. Cuauhtemoc, C. P. 06720, Mxico, D. F., Mxico. Fecha de recepcin: 07072006 Fecha de aprobacin: 30112006 Resumen Las alteraciones endocrinolgicas constituyen parte importante de la consulta peditrica, la ms frecuente es el hipotiroidismo congnito, grave problema de salud pblica que requiere de diagnstico neonatal. Los avances en el estudio molecular han permitido discernir las alteraciones en los procesos de organognesis y hormonognesis que lo producen. Se describen las principales alteraciones moleculares relacionadas con: diferenciacin tiroidea, sntesis hormonal, hipotiroidismo central y con su accin perifrica. El estudio de las alteraciones moleculares abre posibilidades interesantes, pues a partir del conocimiento preciso de los procesos fisiopatolgicos y moleculares podr realizarse en forma precoz el diagnstico y manejo de estos pacientes, previniendo las secuelas que genera esta enfermedad. Palabras clave. Hipotiroidismo congnito; mutaciones; NKX2.1; FOXE1; PAX8; dishormonognesis. Abstract The endocrinological disorders constitute an important percentage of the pediatric consultations. The most frequently endocrinopathy is congenital hypothyroidism, which is considered a public health problem. Newborn screening is mandatory in Mexico. The advances in the molecular field have allowed differentiating among the alterations caused by this disease with especial relevance in the organognesis and homonogenesis. In this review, the main molecular alterations are analyzed, describing their relationship with thyroid cellular differentiation, hormonal synthesis, central
origin hypothyroidism and peripheral tissues target. The study of the molecular abnormalities open new possibilities as to the precise knowledge of the physiopathological and molecular processes. A better and earlier diagnosis and management of this pathology may arise, which in turn will prevent the severe sequelae that congenital hypothyroidism causes. Keywords. Congenital hypothyroidism; mutations; NKX2.1; FOXE1; PAX8; dyshormonogenesis. Las alteraciones en la funcin tiroidea son la causa ms comn de enfermedad endocrinolgica, afectando pacientes de todas las edades y presentando una gran variabilidad de cursos clnicos, con un espectro que va desde cuadros asintomticos hasta falla multisistmica y en algunos casos neoplsicos, la muerte. El diagnstico temprano, sumado al manejo adecuado de las asociaciones sindromticas de las que se acompaen las alteraciones tiroideas, permiten que el pronstico en general sea favorable. Uno de los aspectos ms recientes e interesantes, estudiado en referencia a las alteraciones tiroideas, es el abordaje molecular, ya que estos estudios han permitido dilucidar cada vez ms cul es la asociacin entre las alteraciones genticas de los trastornos tiroideos con sus manifestaciones clnicas y, en su caso, con el patrn de herencia observado. Lo anterior permite diagnosticar precozmente ciertas alteraciones y facilita al clnico, tanto el estudio familiar como el asesoramiento gentico implicado, adems de correlacionar cules son las estructuras cuya formacin y funcin estos genes regulan de manera habitual en el desarrollo normal. Entre los padecimientos tiroideos, se han descrito las bases moleculares del carcinoma de tiroides con mayor claridad, permitiendo investigar su asociacin con otras neoplasias endocrinas, lo que ha mejorado la calidad de vida de los pacientes con este tipo de padecimientos. En entidades nosolgicas como el hipotiroidismo an no existe un patrn de herencia bien definido, si bien, los estudios publicados a la fecha han encontrado asociacin familiar o una relacin de base gentica con cada uno de los eventos que pueden generar hipotiroidismo clnico tales como eventos de diferenciacin glandular, sntesis hormonal, o regulacin pituitaria de la funcin tirotrpica. El objetivo de la presente revisin es documentar las alteraciones moleculares descritas en la literatura con relacin a enfermedad tiroidea, haciendo especial nfasis en el hipotiroidismo congnito, por considerar que se pueden inferir nuevos puntos de estudio molecular que podran, incluso, correlacionar la presentacin del hipotiroidismo con otro tipo de enfermedades (por ejemplo cardiacas). Lo anterior teniendo en cuenta que el hipotiroidismo congnito es el padecimiento endocrinolgico ms frecuente en la
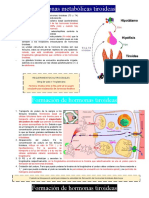
infancia y el estudio en profundidad de esta alteracin permitir mejorar el diagnstico, seguimiento y tratamiento de los nios potencialmente afectados. Glndula tiroides, su embriologa y funcin La glndula tiroides, ubicada en la regin anterior del cuello, es uno de los rganos endocrinos ms activos del organismo; su embriognesis est estrechamente relacionada con el tracto gastrointestinal, teniendo la misma capacidad de metabolizar yodo e incorporarlo en procesos orgnicos como lo pueden hacer las glndulas salivales y gstricas, aunque en estas ltimas no se requiere la estimulacin por tirotropina (TSH). El primordio tiroideo aparece hacia el primer mes de gestacin, al engrosarse el suelo farngeo que posteriormente se transforma en divertculo, deja a su paso el conducto tirogloso, se desplaza progresivamente en sentido caudal para dar origen a una estructura bilobulada que hacia el tercer mes de la gestacin se diferenciar a estructuras tubuliformes y posteriormente tubulares, que se llenarn de coloide, dando forma hacia la semana 29 a la glndula tiroidea propiamente dicha, que tendr la capacidad de sintetizar tiroglobulina. La hipfisis podr formar y segregar TSH desde las semanas 10 a 12, madurando este proceso en las semanas 18 a 26, cuando la hormona liberadora de tirotropina (TRH) es efectiva para la sntesis de TSH.1,2 Las tasas de produccin y degradacin fetales de tiroxina (T4) son ms elevadas en la vida fetal (en unidades relacionadas con masa corporal) que las observadas en el adulto durante los dos primeros aos de vida; su adecuada funcin es vital para el crecimiento y el neurodesarrollo.13 El yodo es indispensable para la sntesis de hormonas tiroideas, calculndose sus requerimientos bsicos en 5060 g/da; se absorbe en el sistema gastrointestinal, distribuyndose en diversos rganos que comparten con la tiroides el mecanismo transportador del yodo, pero se reserva a esta ltima la capacidad de sintetizar hormonas tiroideas bajo la estimulacin de la TSH.4 La disponibilidad del yodo es muy variable dependiendo de su ingesta, de la ubicacin geogrfica y de las costumbres dietarias. Considerando al aporte de yodo como un factor externo en la sntesis de hormonas tiroideas, probablemente es ste el elemento menos relacionado con alteraciones genticas como causa de hipotiroidismo congnito, si bien las variaciones en la ingesta pueden modificar el cuadro clnico. La sntesis de hormonas tiroideas se realiza a travs de la captacin diaria de yodo y la formacin de tiroglobulina, la cual contiene residuos especficos de tirosina, los que son yodados en la porcin apical de la clula tiroidea hasta formar mono y diyodotirosina (MIT, DIT). Finalmente, la enzima tiroperoxidasa (TPO) acopla dos molculas de DIT o una molcula de DIT y una de MIT, dando origen a la tetrayodotironina (T4) o la triyodotironina (T3)
respectivamente, las cuales son posteriormente almacenadas en forma de coloide o como parte de la molcula de tiroglobulina.5 Para que la sntesis de hormonas tiroideas se complete, adems de TPO y tiroglobulina, es necesario que se expresen otras protenas, entre ellas los factores de transcripcin tiroidea 1 y 2 (TTF1 NKX2.1 y TTF2 FOXE1) y PAX 8. Se requiere tambin de la integridad en la estructura del receptor de TSH y la accin de las hormonas tiroideas sobre el rgano blanco. La suma de estos elementos permite una adecuada expresin hormonal.6 El hipotiroidismo congnito puede ser el resultado de alteraciones genticas (objetivo de esta revisin) as como tambin por factores externos o ambientales, entre ellos: infecciosos, medicamentosos y otros que son descritos en el cuadro 1. Entidades que pueden cursar con alteracin de la funcin tiroidea Los padecimientos incluidos en este rubro son muchos, y su clasificacin es compleja pues sta puede relacionarse con la sintomatologa (hiper o hipotiroidismo), etapa de inicio (congnita, adquirida), el lugar de afeccin del eje (primario, secundario o terciario), etc. En el cuadro 1 se han referido las alteraciones que ms frecuentemente se relacionan con distiroidismo para ampliar posteriormente el marco gentico y molecular implicado en estos padecimientos. Hipotiroidismo congnito El hipotiroidismo es la ms frecuente de las enfermedades endocrinas, siendo el congnito el de mayor frecuencia en su presentacin, con una incidencia global de 1 en 3 000 a 4 000 nacidos vivos.3,7 Es causado por malformaciones de la glndula o por defectos en la sntesis hormonal. Dentro de las primeras, se encuentran los defectos en su desarrollo embriolgico, correspondiendo 85% de los casos a las disgenesias tiroideas, incluyndose la agenesia, la hipoplasia y la ectopia. La segunda causa de hipotiroidismo congnito corresponde a las dishormonognesis y son las alteraciones en la organificacin del yodo las ms frecuentes. En algunos de estos casos se ha encontrado relacin con alteraciones en las protenas NKX2.1, FOXE1, PAX8 y GS .7En relacin a esta ltima (codificado por GNAS 1), GS1, se incluye el grupo de trastornos a nivel del receptor para TSH; si bien es cierto que no se ha definido una correlacin sindromtica clara, s se ha demostrado una alteracin a nivel molecular, pues recientemente se describi una mutacin en el gen THRB (receptor de hormonas tiroideas) capaz de producir hipotiroidismo.7 Alteraciones moleculares relacionadas con disgenesia tiroidea
Los tres principales factores de transcripcin implicados en la gnesis de la glndula tiroides son: FOXE1 (Forkhead box E1), tambin llamado FKHL15 y TTF2 NKX2.1, tambin conocido como TITF1 y T/EBP (thyroid enhanced binding protein) PAX8 Figura 1 FOXE1. Gen localizado en el cromosoma 9q22, consistente en un solo exon. Se expresa desde el da 9.5 de gestacin7 en la bolsa de Rathke, estructuras farngeas y folculos pilosos, codificando una fosfoprotena relacionada en la diferenciacin embriolgica y especificacin regional, por lo que est implicada en la agenesia o en la hipoplasia tiroidea.8 Mutaciones en este gen causan el sndrome de Bamforth (OMIM #241850). el cual se caracteriza por agenesia tiroidea y defectos de la lnea media (paladar hendido, atresia de coanas o epiglotis bfida).9 Se han descrito pacientes homocigotos para mutaciones en FOXE1, si bien con fenotipo menos severo, en quienes se sugiere una prdida parcial en la funcin de la protena.7,9 NKX2.1. Factor de transcripcin homeobox de la familia gnica NK 2, correlacionado con la familia de los genes NK2/vnd (ventralnervous system defects) de Drosophila. La superfamilia de genes homeobox codifica protenas reguladoras de transcripcin que actan en puntos crticos de la ontogenia y el desarrollo. NKX2.1 est localizado en el cromosoma 14q1221, comprende tres exones que codifican una protena de 42 kDa.7 El gen del marcador neuroepitelial Nestina, se supone es blanco de NKX2.1, pudiendo ser un efector a travs del cual este ltimo gen juega un papel importante en la organognesis del cerebro anterior. 7,8,10 Mutaciones monoallicas de este gen se han encontrado en pacientes con hipotiroidismo familiar con relacin a la disgenesia tiroidea, la ectopia o la hipoplasia de la glndula tiroides.11 El gen NKX2.1 est implicado tambin en enfermedad respiratoria y algunos autores sugieren que el hipotiroidismo congnito secundario a alteraciones en este nivel, permanece subclnico durante la infancia y es debido a haploinsuficiencia.11,12 Es interesante hacer notar que en el reporte de Doyle y col.,12 se asocia el hipotiroidismo congnito con ataxia y coreoatetosis, sugiriendo un patrn de herencia autosmica dominante. De la misma manera, si bien es cierto que hasta ahora no se ha encontrado una relacin directa de alteracin molecular entre hipotiroidismo y cardiopatas congnitas, con relacin a genes de la familia NKX, por lo menos en un modelo de anlisis en peces zebra13 se ha encontrado la expresin temprana del gen nk2. la en el endodermo adyacente al corazn, lo cual ha despertado el
inters cientfico en correlacionar estas entidades; pues igualmente ha sido descrito en ratones la expresin de nkx2.5 (gen homeobox implicado en el desarrollo cardiaco) en el primordio tiroideo.14 Mutaciones en NKX2.5 han sido reportadas en malformaciones cardiacas en humanos;15 al analizar este gen en 241 pacientes con hipotiroidismo congnito, en cuatro de ellos se identificaron mutaciones sin sentido, en quienes pese a tener tiroides presente, sta se encontraba hipoplsica, demostrando as un papel antes desconocido de NKX2.5 en la organognesis tiroidea.16,17 Debido a que la falta de expresin adecuada de NKX2.3, NKX2.5y tambin de NKX2.6 en tiroides, no necesariamente se correlaciona con alteracin clnica, probablemente algn otro miembro de esta familia gnica podra estar supliendo su funcin.18 La presentacin de cardiopata con organognesis anormal tiroidea sugiere la necesidad de estudiar sistemticamente la morfologa y la funcin tiroidea en todos los pacientes en quienes se sospeche cardiopata congnita causada por mutaciones en alguno de los genes miembros de las familias gnicas descritas, ya que la predominancia clnica de la enfermedad de base pudiese enmascarar o restar importancia a la alteracin tiroidea por ser sta de curso subclnico.14,17,19 PAX8. Gen que codifica un factor de transcripcin, compartido con Drosophila; tiene un papel clave en el desarrollo embriognico de los mamferos. Su locus se encuentra en el cromosoma 2ql2ql4 y consta de 11 exones. En lo referente a tiroides, se ha determinado su papel en la diferenciacin y proliferacin celular. Mutaciones en PAX 8 se han relacionado con hipotiroidismo congnito con patrn de herencia autosmica dominante en al menos cuatro familias y en dos casos espordicos, refirindose en ocasiones una tiroides de tamao normal que posteriormente se hizo hipoplsica.9,20,21 En referencia a esto ltimo, es interesante considerar la posibilidad de que la hipoplasia tarda sea debida al papel que tiene PAX8 en la expresin de TPO y por ende el consecuente defecto en la organificacin hormonal. Hay otros genes expresados durante el desarrollo de la glndula tiroides y analizados en ratn (existiendo su contraparte en humanos) como Hhex, Tshr, y Fgfr2, que no se ha demostrado tengan un papel fundamental en la enfermedad tiroidea y que por lo tanto no se incluyen en esta revisin.18 Alteraciones moleculares relacionadas con dishormonognesis tiroidea Las alteraciones que a continuacin se describen estn relacionadas con la multiplicidad de las vas comprometidas en la sntesis de hormonas tiroideas, como son:8 Pobre respuesta a la TSH: principalmente por alteraciones en el gen TSH, el cual interacta con su receptor para dar inicio al
metabolismo tiroideo a travs de la activacin de protenas G. Se han descrito mutaciones inactivadoras biallicas en pacientes con insensibilidad parcial a la TSH. Tambin se ha implicado al gen GNAS1 relacionado con la transduccin de seal por estimulacin de adenilatociclasa. Mutaciones en GNAS1 se han descrito en diversas entidades endocrinolgicas, ya que su expresin puede variar siendo tanto biallica como presentando regulacin por mecanismos de impronta genmica.7,22 Defectos en el transporte del yodo de la membrana basal: mutaciones en el gen SLC5A57causan alteraciones en la funcin del transporte del yodo, conocido tambin como NIS (natriumiodine symporter), producindose hipotiroidismo grave o moderado y en algunos casos, bocio eutiroideo. Defectos en la sntesis de tiroglobulina: algunos casos de hipotiroidismo congnito se han relacionado con mutaciones en el gen TG, demostrndose un patrn de herencia autosmica dominante. Probablemente sea una de las alteraciones moleculares que ms frecuentemente modifique su presentacin clnica por factores ambientales (grado de ingesta y disponibilidad geogrfica de yodo). Defectos en la organificacin del yodo: por alteraciones en la funcin del gen de la tiroperoxidasa (TPO) cursa con hipotiroidismo clnico y la prueba de descarga de perclorato superior al 90% del yodo despus de la administracin de perclorato confirma el diagnstico. Tambin est implicado el perxido de hidrgeno, ya que ste es necesario para la incorporacin del yodo a la tiroglobulina y el acoplamiento de las tirosinas por la va de la TPO, encontrndose mutaciones en los genes THOX1 y THOX2 en estos pacientes.23 Defectos en el transporte del yodo a la membrana basal: relacionados con el gen SLC26A4, comnmente denominado "pendrina" o PDS. El sndrome de Pendred (OMIM#274600) es un trastorno autosmico recesivo caracterizado por bocio, hipotiroidismo clnico o subclnico y sordera neurosensorial en grado variable. La variabilidad en la presentacin del hipotiroidismo probablemente est relacionada con la existencia de otros factores capaces de transportar el yodo a la membrana basal. Defectos en la deshalogenasa: clnicamente se pueden manifestar como hipotiroidismo congnito o a travs de prdida anormal de MIT y DIT en la orina. Las bases moleculares de este defecto son an motivo de estudio.8 Alteraciones moleculares relacionadas con hipotiroidismo de causa central Se manifiesta clnicamente como hipotiroidismo, tambin conocido como hipotiroidismo secundario y terciario, cuya causa se
encuentra a nivel de pituitaria o a nivel de hipotlamo, respectivamente; tiene una presentacin aproximada de 1:20 000 recin nacidos. Varios linajes celulares participan en los procesos de diferenciacin de estas glndulas, por lo que el hipotiroidismo puede asociarse a otras deficiencias hormonales. Para que se produzcan las hormonas tiroideas se requiere por lo menos de la integridad de cuatro factores: HESX1, LHX3, PROP1 y POU1F1, exceptuando este ltimo factor cuyas alteraciones pueden presentar tanto patrn de herencia autosmica dominante como recesiva, las mutaciones de estos genes tiene un patrn de herencia autosmica recesivo; sus loci se encuentran relacionados en el cuadro 2. Alteraciones moleculares relacionadas con hipotiroidismo perifrico Se incluyen en ste la resistencia a las hormonas tiroideas24 y la resistencia del rgano blanco,25 generando ambas ausencia de los efectos fisiolgicos esperados, pese a la adecuada produccin y distribucin de los productos. En este punto estn implicados los receptores de hormonas tiroideas TSHR A y B cuyos loci se encuentran referidos en el cuadro 2. Por otra parte, se puede encontrar disminucin de la disponibilidad intracelular de las hormonas tiroideas por alteraciones en el mecanismo de las desyodinasas, especialmente DIO1 y 2 encargadas de la conversin de T4 a T3 Finalmente, es motivo de reciente estudio el papel que tienen los disruptores endocrinos, sustancias qumicas capaces de mimetizar a las hormonas tiroideas sin cumplir su funcin y cuyo origen es a partir de los compuestos qumicos generados en la industria.26 La predisposicin gentica y la susceptibilidad para presentar hipotiroidismo por esta causa no estn an bien definidas. Conclusin Las alteraciones moleculares descritas en la literatura con relacin a la enfermedad tiroidea, particularmente en el caso del hipotiroidismo congnito, son variadas y son parte de una compleja interaccin entre diferentes actores. El estudio sistemtico de las alteraciones moleculares y la correlacin clnica (genotipofenotipo) abren posibilidades interesantes para realizar el anlisis molecular al considerar que podran inferirse nuevas alteraciones en los mecanismos tiroideos normales y sus afecciones. Lo anterior seguramente permitir anticipar el momento del diagnstico, mejorar su seguimiento y optimizar el tratamiento de los nios afectados por ste, el ms frecuente de los trastornos endocrinolgicos tiroideos.
Anda mungkin juga menyukai
- Hipo e Hiperfuncion Tiroidea G+Dokumen52 halamanHipo e Hiperfuncion Tiroidea G+Zoom Tecnologico100% (1)
- Glandula HipofisisDokumen24 halamanGlandula HipofisisCristhian Abad Espinoza RamosBelum ada peringkat
- Sistema EndocrinoDokumen19 halamanSistema EndocrinoAlor VerytoBelum ada peringkat
- Envejecimiento Del Sistema Endocrino 2.Dokumen63 halamanEnvejecimiento Del Sistema Endocrino 2.Roley EspinosaBelum ada peringkat
- Tecnicas y ProcedimientosDokumen60 halamanTecnicas y ProcedimientosRafael Sauceda Lopez100% (1)
- Modulo IV. TiroidesDokumen22 halamanModulo IV. TiroidesJulie B BoscanBelum ada peringkat
- Hipertiroidismo e HipotiroidismoDokumen74 halamanHipertiroidismo e HipotiroidismoMario M. Marchand GonzalesBelum ada peringkat
- Hipooo 7Dokumen7 halamanHipooo 7Lachimolala ShopBelum ada peringkat
- Generalidades Del Sistema EndocrinoDokumen8 halamanGeneralidades Del Sistema EndocrinoDUBAN HERRERA PELAEZBelum ada peringkat
- Hormonas Metabólicas TiroideasDokumen12 halamanHormonas Metabólicas TiroideasSolanyi Sandoval RuizBelum ada peringkat
- ACTIVIDAD 1. Clasificación Química de Las HormonasDokumen2 halamanACTIVIDAD 1. Clasificación Química de Las HormonasDulce ArciniegaBelum ada peringkat
- Clase 6 2 B CorregidaDokumen32 halamanClase 6 2 B CorregidaSAUL ANTONIO CORTEZ RIVASBelum ada peringkat
- HipertiroidismoDokumen21 halamanHipertiroidismoAleyda Bonfil LeónBelum ada peringkat
- Sistema EndocrinoDokumen31 halamanSistema EndocrinoemmanuelBelum ada peringkat
- Homologo de Laboratorio de Soat A IssDokumen45 halamanHomologo de Laboratorio de Soat A Issdayana fernanda roseroBelum ada peringkat
- 6 TiroidesDokumen27 halaman6 TiroidesEdgar Ruiz RojasBelum ada peringkat
- 2021 Evaluacion Comparativa DesempenoDokumen40 halaman2021 Evaluacion Comparativa DesempenoJFAIVERBelum ada peringkat
- Enfermedades Metabolicas CongenitasDokumen22 halamanEnfermedades Metabolicas CongenitasSebastian Hernandez MejiaBelum ada peringkat
- Enfermedad Tiroidea y EmbarazoDokumen9 halamanEnfermedad Tiroidea y EmbarazoEloisa TardioBelum ada peringkat
- Alimentos Bociogenos PDFDokumen24 halamanAlimentos Bociogenos PDFNutriólogo Josias AlamillaBelum ada peringkat
- Tesis T3 y T4Dokumen8 halamanTesis T3 y T4Francia ManoloBelum ada peringkat
- Tiroiditis de HashimotoDokumen19 halamanTiroiditis de HashimotoMishel PazmiñoBelum ada peringkat
- Trabajo Final EndocrinologiaDokumen50 halamanTrabajo Final EndocrinologiaValeria EliasBelum ada peringkat
- Sales Minerales PDFDokumen9 halamanSales Minerales PDFRoweBelum ada peringkat
- Guía Lab 4Dokumen3 halamanGuía Lab 4Impresiones SFSBelum ada peringkat
- Termorregulación Fisio GeneralDokumen3 halamanTermorregulación Fisio GeneralEvelyn Jim 3295Belum ada peringkat
- Arancel FONASA 2012 PresupuestosDokumen161 halamanArancel FONASA 2012 PresupuestosPamelha Sánchez Bugueño100% (1)
- TiroidesDokumen82 halamanTiroidesSolanny RosadoBelum ada peringkat
- YODURIAS6Dokumen56 halamanYODURIAS6Carlos Paul Bazo QuesquenBelum ada peringkat
- Cartilla ANATOMÍA ENDOCRINODokumen33 halamanCartilla ANATOMÍA ENDOCRINOcristian lizcanoBelum ada peringkat