Toxotest Hai SP
Diunggah oleh
veronica1570Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Toxotest Hai SP
Diunggah oleh
veronica1570Hak Cipta:
Format Tersedia
Toxotest
HAI
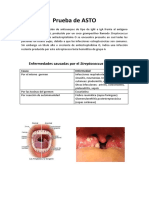
Prueba de hemaglutinacin indirecta (HAI) para la deteccin de anticuerpos contra el Toxoplasma gondii SIGNIFICACION CLINICA La toxoplasmosis es una enfermedad infecciosa generalmente benigna y asintomtica del hombre y de los animales, cuyo agente etiolgico es el Toxoplasma gondii, parsito intracelular obligado de distribucin mundial. Cuando la infeccin por T. gondii se adquiere durante la gestacin, existe un alto riesgo de infeccin en el feto, pudiendo provocar abortos o lesiones graves que son ms severas cuanto ms precoz sea la contaminacin materna. Las determinaciones serolgicas son las ms convenientes y certeras para el diagnstico de la toxoplasmosis y debe establecerse: a) la seroconversin de negativo a positivo, b) un aumento en el ttulo de anticuerpos y c) la presencia de IgM especfica que indicara infeccin activa. FUNDAMENTOS DEL METODO Toxotest HAI se basa en la propiedad que tienen los anticuerpos anti-T. gondii de producir aglutinacin en presencia de glbulos rojos sensibilizados con antgenos citoplasmticos y de membrana del parsito. El empleo de ambos tipos de antgenos incrementa la sensibilidad del mtodo permitiendo la deteccin precoz de la infeccin. Tanto la presencia de anticuerpos heterfilos como la aparicin de IgM, caractersticas del perodo agudo de la parasitosis, se investigan empleando tratamiento con 2-mercaptoetanol (2-ME) y eritrocitos no sensibilizados para control y absorcin de heterofilia. Los anticuerpos heterfilos se absorben con eritrocitos no sensibilizados. En los sueros de pacientes con infeccin aguda tratados con 2-ME, se observa una cada del ttulo en por lo menos dos diluciones comparados con los mismos sueros sin tratar con 2-ME. REACTIVOS PROVISTOS Reconstituyente HAI: solucin fisiolgica tamponada a pH 7. Antgeno HAI: liofilizado de glbulos rojos de carnero sensibilizados con antgenos citoplasmticos y de superficie de T. gondii. GR no sensibilizados: suspensin al 1% de eritrocitos de carnero no sensibilizados, para control y absorcin de heterofilia. Buffer HAI: solucin fisiolgica tamponada con fosfatos a pH 7,5, con colorante inerte. Solucin Proteica: solucin de albmina bovina. 2-Mercaptoetanol: ampolla conteniendo 2-mercaptoetanol (2ME). Control Positivo: suero inactivado conteniendo anticuerpos contra el Toxoplasma gondii. Control Negativo: suero no reactivo, inactivado. REACTIVOS NO PROVISTOS Solucin fisiolgica. INSTRUCCIONES PARA SU USO Antgeno HAI: preparar con 5,2 ml de Reconstituyente HAI. Esperar una hora antes de usar agitando enrgicamente cada 20 minutos para permitir una correcta rehidratacin del reactivo. Cada vez que se emplea homogeneizar mediante agitacin. GR no sensibilizados: homogeneizar mediante agitacin antes de usar, evitando la formacin de espuma. Diluyente de Sueros HAI: agregar 0,2 ml de Solucin Proteica cada 10 ml de Buffer HAI. Mezclar, rotular y fechar. 2-Mercaptoetanol: una vez abierta la ampolla, trasvasar el contenido al frasco vaco provisto, el que se deber tapar inmediatamente despus de usar. 2-Mercaptoetanol al 1%: con el 2-ME provisto, preparar una dilucin 1/100 con solucin fisiolgica en cantidad suficiente de acuerdo al nmero de pocillos que se utilicen. Ejemplo: para 96 pocillos: 25 ul de 2-ME en 2,5 ml de solucin fisiolgica. Controles Positivo y Negativo: listos para usar. PRECAUCIONES - Todas las muestras de pacientes deben manipularse como si fueran capaces de transmitir infeccin. Los controles se encuentran inactivados. Sin embargo, deben emplearse como si se tratara de material infectivo. - Los sueros controles han sido examinados para antgeno de superficie de hepatitis B (HBsAg) y virus de inmunodeficiencia humana (HIV) encontrndose no reactivos. - Todos los materiales empleados en el ensayo deben ser destruidos a fin de asegurar la inactivacin de agentes patgenos. El mtodo recomendado para este procedimiento es autoclavar durante 1 hora a 121oC. Los lquidos de desecho pueden ser desinfectados con hipoclorito de sodio (concentracin final 5%) durante por lo menos 60 minutos. - No intercambiar reactivos de distintos equipos y lotes. - No emplear reactivos de otro origen. - Los reactivos son para uso diagnstico "in vitro". ESTABILIDAD E INSTRUCCIONES DE ALMACENAMIENTO Reactivos Provistos: son estables en refrigerador (2-10oC) hasta la fecha de vencimiento indicada en la caja. No congelar. Diluyente de Sueros HAI: es estable en refrigerador (2-10oC) 5 das a partir de la fecha de su preparacin. GR no sensibilizados: mantener en posicin vertical. 2-Mercaptoetanol al 1%: usar inmediatamente despus de preparado.
870940000 / 00 Pg. 1 de 8
Antgeno HAI: una vez reconstituido es estable durante 4 meses conservado en refrigerador (2-10oC). No congelar. Mantener en posicin vertical. INDICIOS DE INESTABILIDAD O DETERIORO DE LOS REACTIVOS Cuando el Control Negativo y todas las diluciones de sueros son reactivas, puede ser indicio de autoaglutinacin del Antgeno HAI. Verificar destinando un pocillo de la policubeta para mezclar Antgeno HAI y Diluyente de Sueros HAI, sin la muestra. Si an en este caso se observa aglutinacin, el reactivo estar deteriorado. Desechar. La ausencia de reactividad en todas las diluciones de sueros y Control Positivo, puede ser indicio de deterioro de los reactivos. Procesar una muestra con positividad conocida. MUESTRA Suero a) Recoleccin: el paciente debe estar preferentemente en ayunas. Obtener suero de la manera usual. No usar plasma. b) Aditivos: no se requieren. No agregar conservadores. c) Sustancias interferentes conocidas: hemlisis o hiperlipemia (con quilomicronemia) son causa de resultados errneos. d) Estabilidad e instrucciones de almacenamiento: el suero debe ser preferentemente fresco. En caso de no procesarse en el momento, puede conservarse en refrigerador (2-10oC) durante no ms de 72-96 horas contadas a partir del momento de la extraccin. Para perodos ms prolongados de conservacin, congelar (a -20oC) evitando reiterar descongelamientos y congelamientos. Los sueros envejecidos tienden a gelificarse al contacto con el 2-ME, provocando resultados falsos positivos. MATERIAL REQUERIDO 1- Provisto - 1 frasco vaco (para trasvasar el 2-ME de la ampolla) - 5 policubetas con 96 pocillos de fondo en U (8 hileras y 12 columnas) - esptulas-gotero plsticas descartables 2- No provisto - microdilutores (25 ul) - microgoteros (25 ul) - tubos de ensayo y material volumtrico adecuado - cinta adhesiva PROCEDIMIENTO Seleccionar una policubeta con pocillos sin usar de fondo en U. Pasar un trapo hmedo por la base de la policubeta antes de usar, colocarla en forma apaisada sobre el trapo y realizar el ensayo mantenindola en esta posicin. Ver LIMITACIONES DEL PROCEDIMIENTO. I- TITULACION SIN 2-ME 1) Con microgotero de 25 ul, colocar una gota de Diluyente de Sueros HAI en todos los pocillos a usar de la policubeta. 2) Tomar una alcuota de cada suero o controles a en-
sayar con microdilutores de 25 ul (uno para cada muestra) y colocar en los pocillos de la columna 1. Se utilizarn tantas hileras horizontales como sueros o controles deban procesarse. 3) Realizar diluciones a partir de la columna 1 (dilucin 1/2), pasando los microdilutores a la columna 2 (dilucin 1/4) y as sucesivamente hasta la columna 6 (dilucin 1/64). Si se procesaran ms de 8 sueros, se utilizarn las columnas 7 a 12, realizando las diluciones de la manera antes descripta. 4) Colocar en las columnas 1 y 2 (diluciones 1/2 y 1/4) una gota (25 ul) de GR no sensibilizados, para control de heterofilia. Hacer lo mismo en las columnas 7 y 8 en caso de ser empleadas. 5) En el resto de los pocillos, agregar una gota (25 ul) de Antgeno HAI. 6) Agitar la policubeta golpeando con los dedos en las paredes laterales, durante 30 segundos por lo menos. 7) Dejar en reposo, al resguardo de vibraciones, durante 90 minutos. 8) A partir de los 90 minutos, leer. Se puede aumentar la nitidez de la imagen, leyendo sobre un espejo, iluminando la placa desde arriba e interponiendo un papel blanco y traslcido entre la policubeta y la fuente de luz. II- TITULACION CON 2-ME 1) Colocar una gota de suero o controles en cada uno de los pocillos de la columna 1 (y 7 si es necesario), empleando esptulas-gotero descartables (una por cada suero) en posicin vertical. 2) Agregar una gota de 2-Mercaptoetanol al 1% a los mismos pocillos, utilizando una esptula-gotero descartable. 3) Sellar los pocillos con cinta adhesiva y agitar la policubeta golpeando con los dedos en las paredes laterales. 4) Incubar 30-60 minutos a 37oC o 90 minutos a temperatura ambiente. 5) Retirar la cinta adhesiva, pasar un trapo hmedo por la base de la policubeta y, con microgotero de 25 ul, colocar una gota de Diluyente de Suero HAI en los pocillos restantes de las hileras utilizadas. 6) Realizar los pasos 3 al 8 descriptos en la Titulacin I. III- TECNICAS ALTERNATIVAS Cuando se estudian sueros altamente reactivos o en caso de poblaciones con una elevada prevalencia de toxoplasmosis donde habitualmente se encuentran ttulos superiores a 1/32 pueden emplearse algunas de las siguientes tcnicas alternativas: Tcnica alternativa 1: Continuar con las diluciones hasta la columna 12 inclusive con lo que se obtiene una dilucin final de 1/4.096. Tcnica alternativa 2: Colocar en un tubo ad-hoc 50 ul de suero y 350 ul de Diluyente de Sueros HAI (dilucin 1/8). Tomar 25 ul de esta dilucin y colocarla en la columna 1 de la policubeta. Proseguir segn se describe en I, hasta la columna 6. De esta forma se obtiene una dilucin final de 1/512.
870940000 / 00
Pg. 2 de 8
IV- ABSORCION SOBRE GLOBULOS ROJOS NO SENSIBILIZADOS En sueros que presenten heterofilia los anticuerpos heterfilos pueden absorberse sobre GR no sensibilizados de la siguiente forma: en un tubo de hemlisis con tapn colocar 50 ul de GR no sensibilizados provistos + 50 ul de suero en ensayo. Dejar la suspensin durante 30 minutos a 37oC agitando de tanto en tanto. Luego centrifugar a 2.000 r.p.m. durante 5 minutos. Del sobrenadante se toman 50 ul y se emplea como dilucin 1/2, colocndola en la primera columna. Si se emplea en titulacin con 2-ME esta columna corresponde a dilucin 1/4. INTERPRETACION DE LOS RESULTADOS Titulacin sin 2-ME Ttulos 16 significan mayor probabilidad de infeccin toxoplsmica. A fin de determinar una primoinfeccin reciente deben procesarse 2 muestras tomadas con un intervalo de 2-3 semanas. Un aumento de ttulo mayor de 2 diluciones entre la 1ra y 2da muestra indican infeccin recientemente adquirida. Titulacin con 2-ME La aparicin de ttulos bajos en la titulacin sin 2-ME y reactividad con glbulos rojos no sensibilizados que desaparece al efectuar la titulacin con 2-ME y/o absorcin con GR no sensibilizados, seran indicativos de la existencia de heterofilia. Por el contrario, ttulos elevados sin el empleo de 2-ME que disminuyen considerablemente al utilizar 2-ME indicaran la presencia de IgM, caracterstica de infeccin aguda. Los controles de heterofilia en este caso deben dar reaccin negativa en el suero sin tratar o tras absorcin con GR no sensibilizados. IMAGEN NEGATIVA
Es por esta razn que los informes deben ser considerados en trminos de probabilidad. En este caso, mayor o menor probabilidad de parasitosis por T. gondii. Se consideran presumiblemente parasitados aquellos individuos cuyos sueros son reactivos en diluciones mayores o iguales a 1/16. Se debe tener en cuenta que la concentracin de anticuerpos en suero vara en distintas poblaciones, razn por la cual es posible encontrar sueros reactivos correspondientes a individuos no parasitados. Por esta razn es necesario determinar los valores de referencia de la poblacin en estudio. LIMITACIONES DE PROCEDIMIENTO Ver Sustancias interferentes conocidas en MUESTRA. Otras causas de resultados errneos son: - Falta de acondicionamiento previo de la policubeta. Para eliminar la carga electrosttica es necesario pasar un trapo hmedo por la base (ver PROCEDIMIENTO). - Falta de homogeneizacin de los reactivos antes de su uso. - Deficiencias de mezclado. - Vibraciones accidentales durante el reposo necesario para el desarrollo de la reaccin. - Sueros envejecidos o congelados y descongelados repetidamente. - Contaminaciones accidentales de los reactivos o del material empleado en el ensayo. - Policubetas rayadas por uso reiterado. No se aconseja reutilizar pocillos. - Diluyente de Sueros HAI conservado ms de 5 das. - Exceso o defecto de Diluyente de Sueros HAI en los pocillos de la policubetas. - No respetar los tiempos y temperaturas de incubacin en el tratamiento con 2-ME al 1%. - 2-Mercaptoetanol al 1% no preparado en el momento. Debe tenerse en cuenta que en este tipo de infecciones las titulaciones aisladas proveen escasa informacin por lo que se prefiere efectuar determinaciones seriadas cada 15-20 das que permitan observar las variaciones en los ttulos. Para este procedimiento es conveniente conservar congeladas alcuotas de las muestras de distintos das y procesarlas simultneamente con los mismos reactivos y el mismo operador. Recordar que cada componente de Toxotest HAI forma un equipo completo que debe considerarse como unidad. Por este motivo no deben intercambiarse los componentes de distintos equipos. PRESENTACION - 80 determinaciones (Cd. 1743201). BIBLIOGRAFIA - Gomez Lus, R. y Benito Ruesca, R. - Medicine 33-2a serie pg. 1.459 (1984). - Jacobs, L.; Linde, M.N. - J. Parasitol. 43:308, (1957).
IMAGEN POSITIVA
(1) (1) Manto. (2) Punto final (50%).
(2)
No Reactivo: presencia de un sedimento en forma de botn o pequeo anillo de bordes regulares. Reactivo: formacin de una pelcula o manto que cubre el 50% o ms del fondo de los pocillos. VALORES DE REFERENCIA Dentro de las tcnicas inmunolgicas, la HAI es considerada un mtodo confiable para la determinacin de anticuerpos especficos. No obstante, sus resultados, al igual que los de cualquier mtodo serolgico, slo constituyen un dato auxiliar para el diagnstico.
870940000 / 00
Pg. 3 de 8
EXPLICACION DE LOS SIMBOLOS
Antgeno Antgeno HAI Reconstituy. HAI HAI Buffer Buffer HAI GR no sensib. HAI
Reconstituyente HAI Sol. Proteica
GR no sensibilizados 2-ME 2-Mercaptoetanol Control -
Solucin Proteica Control +
Control Positivo
Control Negativo
Los siguientes smbolos se utilizan en todos los kits de reactivos para diagnstico de Wiener lab.
C
V
X
H l
P Representante autorizado en la Comunidad Europea
Uso diagnstico "in vitro" Contenido suficiente para <n> ensayos Fecha de caducidad Lmite de temperatura (conservar a) No congelar Riesgo biolgico Volumen despus de la reconstitucin
Cont.
Este producto cumple con los requerimientos previstos por la Directiva Europea 98/79 CE de productos sanitarios para el diagnstico "in vitro"
?
F
Contenido Nmero de lote Elaborado por: Nocivo Corrosivo / Castico
g
M
Xn
Xi
Irritante Consultar instrucciones de uso Calibrador Control Control Positivo Control Negativo Nmero de catlogo
i
Calibr.
b b c
Wiener Laboratorios S.A.I.C. Riobamba 2944 2000 - Rosario - Argentina http://www.wiener-lab.com.ar Dir. Tc.: Viviana E. Ctola Bioqumica Producto Autorizado A.N.M.A.T. Disp. N: 195/90 - 6293/96
Wiener lab.
2000 Rosario - Argentina
870940000 / 00
Pg. 4 de 8
Anda mungkin juga menyukai
- Hepatitis B Hbsag Elisa SPDokumen4 halamanHepatitis B Hbsag Elisa SPCattlen Lizlie Hilasaca ApazaBelum ada peringkat
- 6374 Chagatest Elisa SPDokumen3 halaman6374 Chagatest Elisa SPMaría José QuirozBelum ada peringkat
- ASO - ManualDokumen8 halamanASO - ManualIxel GonzalezBelum ada peringkat
- Procedimieno EstandarizadoDokumen16 halamanProcedimieno EstandarizadoDaniel Irazabel ZelayaBelum ada peringkat
- Prueba de Latex ASLODokumen2 halamanPrueba de Latex ASLOSantiago MiñanoBelum ada peringkat
- CoombsDokumen6 halamanCoombseduardoBelum ada peringkat
- Bilirrubina Directa Aa Liquida SPDokumen3 halamanBilirrubina Directa Aa Liquida SPRudy Hidalgo TovarBelum ada peringkat
- Sgis04 RPR 2021Dokumen4 halamanSgis04 RPR 2021Andrea CardeñaBelum ada peringkat
- 20 - A - Parasitosis en Pediatria (1°parte) - Pediatria - 19-03-19Dokumen8 halaman20 - A - Parasitosis en Pediatria (1°parte) - Pediatria - 19-03-19Edwin IllanesBelum ada peringkat
- Anti H Pylori IgA AccuBind ELISADokumen5 halamanAnti H Pylori IgA AccuBind ELISARosa Banegas Montaño100% (1)
- Agar CledDokumen1 halamanAgar CledLuis CyferBelum ada peringkat
- AnticoagulantesDokumen10 halamanAnticoagulantesPedro ArigatoBelum ada peringkat
- 14fk10 Rotavirus Ins MinDokumen2 halaman14fk10 Rotavirus Ins Minangelica moran garciaBelum ada peringkat
- Almacenamiento y Conservación de La SangreDokumen2 halamanAlmacenamiento y Conservación de La SangreAntonio SantillanBelum ada peringkat
- H. Pylori Ab Cassette 40t CasDokumen2 halamanH. Pylori Ab Cassette 40t CasJose BMBelum ada peringkat
- RPR CarbonDokumen2 halamanRPR CarbonEmily0% (1)
- Ficha Tecnica RotavirusDokumen13 halamanFicha Tecnica RotavirusBiomedical Cia LtdaBelum ada peringkat
- GGT Suero - PDF-1Dokumen1 halamanGGT Suero - PDF-1Jorge H. CárcamoBelum ada peringkat
- 1 WidalDokumen2 halaman1 WidalHans YoveraBelum ada peringkat
- Prueba de ASTODokumen5 halamanPrueba de ASTOalejandroBelum ada peringkat
- Tincion de Gram HuckerDokumen3 halamanTincion de Gram HuckerFreddy Vallejo LeonBelum ada peringkat
- Diagnóstico Bacteriológico de La TuberculosisDokumen13 halamanDiagnóstico Bacteriológico de La TuberculosisKiArABelum ada peringkat
- Manual de Metodos Analiticos en CoprologiaDokumen22 halamanManual de Metodos Analiticos en CoprologiaKaren BravoBelum ada peringkat
- Poe Manual de Parasitologia 77Dokumen9 halamanPoe Manual de Parasitologia 77Rusmel Santisteban IzquierdoBelum ada peringkat
- Guia KOHDokumen2 halamanGuia KOHDAVID JIMENEZBelum ada peringkat
- Poe de HematologiaDokumen4 halamanPoe de HematologiaÁlvaro José Villamizar JimenezBelum ada peringkat
- Marco Teorico Practica Floculacion InmunoDokumen18 halamanMarco Teorico Practica Floculacion InmunoMiguel Angel Rodas Herrera100% (4)
- Alt GPT BRDokumen2 halamanAlt GPT BRARIEL MAM,ANI100% (1)
- Laboratorio Bacteriologia 3Dokumen17 halamanLaboratorio Bacteriologia 3Luis David Bello Rodríguez100% (2)
- Lavado de Material de HematologiaDokumen6 halamanLavado de Material de Hematologia218omar50% (2)
- Equipo Automatizado HematologiaDokumen8 halamanEquipo Automatizado HematologiaKarla OrozcoBelum ada peringkat
- Citología de Moco FecalDokumen2 halamanCitología de Moco Fecallam96_espbqBelum ada peringkat
- Método Kato KatzDokumen43 halamanMétodo Kato KatzErnesti Sanchez0% (1)
- AmebaDokumen11 halamanAmebakatherine albujaBelum ada peringkat
- Exposicion en MicrobiologiaDokumen15 halamanExposicion en MicrobiologiaHugo Huaman MuñozBelum ada peringkat
- Inserto TSHDokumen5 halamanInserto TSHMelki MiñopeBelum ada peringkat
- Poe Coproparasitologia 2023Dokumen52 halamanPoe Coproparasitologia 2023Stefany Quisbert DiazBelum ada peringkat
- Hemoclasificación NCDokumen8 halamanHemoclasificación NCsergio quinteroBelum ada peringkat
- Grupo Sanguineo en PlacaDokumen5 halamanGrupo Sanguineo en PlacaChuma Chuma ArturoBelum ada peringkat
- Técnica de Capacidad de Fijación de Hierro en SangreDokumen2 halamanTécnica de Capacidad de Fijación de Hierro en SangreQUIMICO CLINICO WILLIANS SANCHEZ100% (1)
- Poes CoproDokumen22 halamanPoes CoproVanessa VargasBelum ada peringkat
- Agar Ogawa MDM Ficha TécnicaDokumen2 halamanAgar Ogawa MDM Ficha TécnicaGeraldine CacaceBelum ada peringkat
- Agar ChocolateDokumen4 halamanAgar ChocolateSergio Domínguez OchoaBelum ada peringkat
- Poe de Pcr-LatexDokumen4 halamanPoe de Pcr-LatexMedina Calizaya Maria IsabelBelum ada peringkat
- Formato POES Uroanalisis QuimicoDokumen4 halamanFormato POES Uroanalisis QuimicoRosiel HerreraBelum ada peringkat
- Urea LabtestDokumen5 halamanUrea LabtestYelthon Sharles Mamani AlanesBelum ada peringkat
- Agar Chocolate GC Con Supl. Versión 3 ValtekDokumen2 halamanAgar Chocolate GC Con Supl. Versión 3 Valteksergio torresBelum ada peringkat
- Manual de Serología - Proyecto - TrabajoDokumen23 halamanManual de Serología - Proyecto - TrabajoViviana ParadaBelum ada peringkat
- IFU ASO Latex MonlabtestDokumen2 halamanIFU ASO Latex MonlabtestBady MagneBelum ada peringkat
- DengueDokumen2 halamanDengueDaniel AriasBelum ada peringkat
- RPR Examen de Reagina Plasmática RápidaDokumen23 halamanRPR Examen de Reagina Plasmática RápidaFer Rivas FrancoBelum ada peringkat
- PRACTICA 1 Determinación de Grupo ABODokumen5 halamanPRACTICA 1 Determinación de Grupo ABOandrea0djaBelum ada peringkat
- Control de Calidad de Medios de CultivoDokumen11 halamanControl de Calidad de Medios de CultivodatitoxBelum ada peringkat
- Acido UricoDokumen7 halamanAcido UricoKarla OrozcoBelum ada peringkat
- Ficha Técnica de Reactivo de CoombsDokumen3 halamanFicha Técnica de Reactivo de CoombsjorgeluisBelum ada peringkat
- Poe Manual de Copro 2016Dokumen5 halamanPoe Manual de Copro 2016Heriberto Richard Illanes100% (2)
- Monografia Control de Calidad en MicologiaDokumen19 halamanMonografia Control de Calidad en MicologiapaolaBelum ada peringkat
- Practica 1 MicologiaDokumen12 halamanPractica 1 MicologiaAlex Ontaneda100% (1)
- Procedimiento Operativo Estandarizado Got/Ast U.V.: Laboratorio Clínico Del Hospital I Héroes Del CenepaDokumen4 halamanProcedimiento Operativo Estandarizado Got/Ast U.V.: Laboratorio Clínico Del Hospital I Héroes Del CenepaOrlando CastilloBelum ada peringkat
- Toxotest HaiDokumen4 halamanToxotest HaiEsperanza CastroBelum ada peringkat
- Anemias IntroduccionDokumen1 halamanAnemias Introduccionveronica1570Belum ada peringkat
- Expo Inmuno OntogeniatDokumen58 halamanExpo Inmuno OntogeniatLiiz GatiiCaaBelum ada peringkat
- Amebas de Vida LibreDokumen4 halamanAmebas de Vida Libreveronica1570Belum ada peringkat
- Cuidados de CADDokumen4 halamanCuidados de CADveronica1570Belum ada peringkat
- Control Instrumental 2010 Version 2003Dokumen21 halamanControl Instrumental 2010 Version 2003veronica1570Belum ada peringkat
- AuditoriaDokumen15 halamanAuditoriaveronica1570Belum ada peringkat
- Guerra Del LitioDokumen10 halamanGuerra Del Litiogtecnica129Belum ada peringkat
- UroanálisisDokumen5 halamanUroanálisisCeja Rodríguez Melany AndreaBelum ada peringkat
- Contabilidad de CostoDokumen15 halamanContabilidad de CostoMaría Dionicio PetroBelum ada peringkat
- CURSO PCP MODULO 3 Programacion JIT KANBAN Capdo - 2018-10-19 PDFDokumen129 halamanCURSO PCP MODULO 3 Programacion JIT KANBAN Capdo - 2018-10-19 PDFJOHNSEDBelum ada peringkat
- Filosofia Pro 5 - 1ºbguDokumen7 halamanFilosofia Pro 5 - 1ºbguLuis FreireBelum ada peringkat
- El Crecimineto Espiritual y Su Importancia para La Vida CristianaDokumen6 halamanEl Crecimineto Espiritual y Su Importancia para La Vida Cristiananotero20Belum ada peringkat
- Trabajo PsiquiatríaDokumen5 halamanTrabajo PsiquiatríaAnildibeth0% (1)
- "Ensayos" de Lewis Mumford.Dokumen15 halaman"Ensayos" de Lewis Mumford.Víctor Sáenz-Díez0% (2)
- Sesion 4Dokumen57 halamanSesion 4zapata19nBelum ada peringkat
- Saga de Los Sistemadores - El Joven JeronDokumen45 halamanSaga de Los Sistemadores - El Joven JeronIwazuki - ChanBelum ada peringkat
- Historia de La Geotecnia16AADokumen3 halamanHistoria de La Geotecnia16AAARIAS100% (1)
- Las EnzimasDokumen12 halamanLas Enzimaslissaird5Belum ada peringkat
- Jerarquias de Color y MestizajeDokumen28 halamanJerarquias de Color y MestizajeNahuel AlonsoBelum ada peringkat
- Brechas en Santander PDFDokumen390 halamanBrechas en Santander PDFTatiana TorresBelum ada peringkat
- Tabasco PrimariaDokumen28 halamanTabasco PrimariaIsabel ChableBelum ada peringkat
- Voleibol Segundo Periodo 7 GradoDokumen6 halamanVoleibol Segundo Periodo 7 GradoIzaura ParraBelum ada peringkat
- La Santidad Interna y ExternaDokumen7 halamanLa Santidad Interna y ExternaJose Castro100% (3)
- Redaccion Mapa ConceptualDokumen1 halamanRedaccion Mapa Conceptualenzo100% (1)
- Act, 01 Urbano 1ro y 2doDokumen3 halamanAct, 01 Urbano 1ro y 2doHipolito Crispin SalcedoBelum ada peringkat
- Historia de Modelos AtómicosDokumen7 halamanHistoria de Modelos AtómicosAndrea Jezabel López GonzálezBelum ada peringkat
- Guias 7 8 Quimica Grado 7°Dokumen6 halamanGuias 7 8 Quimica Grado 7°gladys belen caballero celisBelum ada peringkat
- Tema 8-Selectividad-Lengua-Crónicas de Una Muerte Anunciada-17-18Dokumen33 halamanTema 8-Selectividad-Lengua-Crónicas de Una Muerte Anunciada-17-18Dani VRBelum ada peringkat
- Manuscrito Señor Manda Obreros A Tu MiesDokumen10 halamanManuscrito Señor Manda Obreros A Tu MiesRuben TelloBelum ada peringkat
- LIBRO Biología Evolutiva de La Niñez/ Autora Ana FazDokumen423 halamanLIBRO Biología Evolutiva de La Niñez/ Autora Ana FazMaria JuarezBelum ada peringkat
- Oficio de Invitacion - San Juan TangumiDokumen3 halamanOficio de Invitacion - San Juan TangumiRichard Nuñez AcostaBelum ada peringkat
- Excel IntermedioDokumen15 halamanExcel IntermedioRONBelum ada peringkat
- Ficha de Personal Social 15-05 PDFDokumen7 halamanFicha de Personal Social 15-05 PDFLuis Cárdenas PorrasBelum ada peringkat
- Actividades de Refuerzo Grado 11Dokumen3 halamanActividades de Refuerzo Grado 11Karol YisethBelum ada peringkat
- Lenguaje Figurado y Causa - EfectoDokumen7 halamanLenguaje Figurado y Causa - EfectoMorgan OlivaresBelum ada peringkat
- Asistencia PrenatalDokumen3 halamanAsistencia PrenatalAnahí Adorno GBelum ada peringkat
- Tus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadDari EverandTus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadPenilaian: 4.5 dari 5 bintang4.5/5 (1831)
- Los Secretos De La Mente Millonaria: Domina el juego de la riquezaDari EverandLos Secretos De La Mente Millonaria: Domina el juego de la riquezaPenilaian: 5 dari 5 bintang5/5 (457)
- El Monje Que Vendio Su Ferrari: Una Fábula EspiritualDari EverandEl Monje Que Vendio Su Ferrari: Una Fábula EspiritualPenilaian: 4.5 dari 5 bintang4.5/5 (1698)
- ¡Tómate un respiro! Mindfulness: El arte de mantener la calma en medio de la tempestadDari Everand¡Tómate un respiro! Mindfulness: El arte de mantener la calma en medio de la tempestadPenilaian: 5 dari 5 bintang5/5 (198)
- El juego de la vida y cómo jugarloDari EverandEl juego de la vida y cómo jugarloPenilaian: 5 dari 5 bintang5/5 (4)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDari EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcancePenilaian: 5 dari 5 bintang5/5 (8)
- Resetea tu mente. Descubre de lo que eres capazDari EverandResetea tu mente. Descubre de lo que eres capazPenilaian: 5 dari 5 bintang5/5 (196)
- Fuerza de voluntad: Cómo practicar y dominar el autocontrolDari EverandFuerza de voluntad: Cómo practicar y dominar el autocontrolPenilaian: 4.5 dari 5 bintang4.5/5 (89)
- Entrenamiento Científico con pesas: Fitness InteligenteDari EverandEntrenamiento Científico con pesas: Fitness InteligentePenilaian: 5 dari 5 bintang5/5 (3)
- Grimorio: Cómo lanzar y elaborar hechizos mágicos, aprender las prácticas wiccanas y desvelar los secretos de la brujería a través de un diario ritualDari EverandGrimorio: Cómo lanzar y elaborar hechizos mágicos, aprender las prácticas wiccanas y desvelar los secretos de la brujería a través de un diario ritualBelum ada peringkat
- Las Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishDari EverandLas Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishPenilaian: 4.5 dari 5 bintang4.5/5 (3)
- Cómo Acertar en tu Nueva Relación de Pareja: Todas las claves para saber si tu relación tiene futuro... o te conviene salir corriendo de ahí.Dari EverandCómo Acertar en tu Nueva Relación de Pareja: Todas las claves para saber si tu relación tiene futuro... o te conviene salir corriendo de ahí.Penilaian: 4.5 dari 5 bintang4.5/5 (7)
- Mindfulness para principiantes: Medita sin meditarDari EverandMindfulness para principiantes: Medita sin meditarPenilaian: 5 dari 5 bintang5/5 (53)
- 7 Pasos Para Superar Una Crisis: Cómo atravesar un duelo o una pérdida y salir fortalecidoDari Everand7 Pasos Para Superar Una Crisis: Cómo atravesar un duelo o una pérdida y salir fortalecidoPenilaian: 5 dari 5 bintang5/5 (5)
- Guías Espirituales: ¡Una guía para conectarte y comunicarte con tus guías espirituales!Dari EverandGuías Espirituales: ¡Una guía para conectarte y comunicarte con tus guías espirituales!Penilaian: 4.5 dari 5 bintang4.5/5 (14)
- Ayurveda: Descubriendo los Secretos de la Curación Hindú a Través de la Dieta del Ayurveda, el Yoga, la Aromaterapia y la MeditaciónDari EverandAyurveda: Descubriendo los Secretos de la Curación Hindú a Través de la Dieta del Ayurveda, el Yoga, la Aromaterapia y la MeditaciónPenilaian: 4 dari 5 bintang4/5 (7)
- Herbolario de la senda de los venenos: Hierbas nocivas, solanáceas medicinales y enteógenos ritualesDari EverandHerbolario de la senda de los venenos: Hierbas nocivas, solanáceas medicinales y enteógenos ritualesBelum ada peringkat
- Seguridad en el amor: Cómo superar el apego y la ansiedad en tu relaciónDari EverandSeguridad en el amor: Cómo superar el apego y la ansiedad en tu relaciónPenilaian: 4.5 dari 5 bintang4.5/5 (76)
- Mujeres de luz: Guía para descubrir el poder de tu alma y su propósitoDari EverandMujeres de luz: Guía para descubrir el poder de tu alma y su propósitoPenilaian: 4.5 dari 5 bintang4.5/5 (39)
- En sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésDari EverandEn sintonía con tu ciclo femenino: FLO. Aprende a sincronizarte con tu bioquímica para dar rienda suelta a tu creatividad, mejorar tu vida y hacer más con menos estrésPenilaian: 4.5 dari 5 bintang4.5/5 (11)
- Una mente en calma: Técnicas para manejar los pensamientos intrusivosDari EverandUna mente en calma: Técnicas para manejar los pensamientos intrusivosPenilaian: 4.5 dari 5 bintang4.5/5 (142)
- La vibración de las ondas cerebrales: Recuperar el ritmo de una vida saludable y felizDari EverandLa vibración de las ondas cerebrales: Recuperar el ritmo de una vida saludable y felizPenilaian: 5 dari 5 bintang5/5 (7)