Practica Dos - Catalimetro
Diunggah oleh
Luis Angel YrraHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Practica Dos - Catalimetro
Diunggah oleh
Luis Angel YrraHak Cipta:
Format Tersedia
Determinacin de la Velocidad de la Reaccin Catalasa.
Prctica nmero dos Determinacin de la Velocidad de Reaccin de la Catalasa
Brock Prez Liliana Espinosa Martn del Campo Mauricio Ruz Martnez DayziLizette Snchez Mendoza Adriana Santos Castrejn Oscar Roberto Yrra de la Cruz Luis ngel
604
22 de Noviembre de 2012
Determinacin de la Velocidad de la Reaccin Catalasa.
Determinacin de la Velocidad de Reaccin de la Catalasa
1. Introduccin
El presente trabajo muestra como se lleva a cabo la medicin del oxigeno al ser liberado en una reaccin de catalasa y perxido de hidrogeno, esto a travs de un dispositivo apropiado. Previamente a esto y para la comprensin del escrito es necesario hacer referencia a algunas definiciones que tienen que ver con dicho tema. Empezaremos aclarando los distintos tipos de reacciones y con ello lograr identificar posteriormente la reaccin a la que estamos haciendo referencia. Las reacciones bsicamente se pueden clasificar en dos reversible e irreversible: Una reaccin qumica puede ser reversible, en la que la reaccin puede cumplirse en una u otra direccin, o irreversible en la cual uno de los productos abandona la reaccin. Por su parte tambin existen dos clases de reacciones r de dos clases: endergnica, en la que se absorbe ms energa de la que se libera, o exergnica, donde se libera ms energa de la que se absorbe (Baker, Jw. 1973) Enzimas El protoplasma celular contiene un millar de protenas, cada una de las cuales lleva a cabo muchos cambios qumicos que se requieren para el mantenimiento de la vida. Estas protenas llamadas enzimas son catalizadores. Los catalizadores (orgnicos o inorgnicos) aumentan la velocidad de una reaccin. Las enzimas aceleran las reacciones qumicas en los sistemas biolgicos de modo que pueden efectuarse a temperaturas relativamente bajas. Naturaleza qumica: las enzimas son protenas, hidrosolubles y pertenecen a la clase de protenas globulares simples o a la de los globulares conjugadas. Las enzimas son fcilmente desnaturalizadas por el calor y diversos agentes qumicos (Mertz, E. 1980, p. 93-110). Sabiendo entonces que una enzima es una protena, la desnaturalizacin se refiere al desdoblado de una protena. (Campbell, M. 2004, p. 102) El perxido de hidrgeno es un producto qumico que se produce continuamente como subproducto en las reacciones de las clulas vivas. Es txico
Determinacin de la Velocidad de la Reaccin Catalasa.
y la clula debe descomponerlo inmediatamente antes de que la destruya () esta reaccin recibe ayuda de un catalizador. La enzima catalasa se encuentra en la mayora de los seres vivos; es un ejemplo de enzima que contiene una parte proteica y otra no proteica. La parte proteica de la catalasa est unida a una molcula de una sustancia que contiene hierro llamada hem (). Solo cuando el hem est unido a la protena especfica de la catalasa, ayuda a catalizar la descomposicin de perxido de hidrgeno (Claude, W. 1991, p. 201-205). La tasa de reaccin qumica est definida como la cantidad de reaccin en determinado tiempo () y bsicamente puede expresarse: Tasa de reaccin: cambio de concentracin/cambio de tiempo Las enzimas son catalizadores orgnicos que aumentan la tasa de las reacciones qumicas. Cuando se alcanza el punto en el cual la tasa de reaccin hacia adelante es igual a la tasa inversa podemos hablar de un equilibrio qumico entre las sustancias. (Baker, Jw. 1973) La cintica enzimtica estudia la rapidez de una reaccin, la cual suele expresarse en trminos de un cambio en la concentracin de un reactivo o de un producto en un intervalo de tiempo dado. () La rapidez de reaccin puede se puede expresar en trminos de la rapidez de desaparicin de o de los reactivos o de la rapidez de aparicin del producto. (Campbell, M. 2004, p. 136-138) Un modelo de especial utilidad para estudiar la cintica de las reacciones catalizadas por enzimas fue ideado en 1913 por Leonor Michaelis y Maud Menten. () El mecanismo de una reaccin catalizada por una enzima puede resumirse en la forma K
1
K2
E+S
K -1
ES
E+P
Donde k1 es la contante de rapidez para la formacin del complejo enzima sustrato, ES, a parte de la enzima, E, y el sustrato, S; K -1 es la constante de rapidez para la reaccin inversa, la disociacin del complejo ES para dar enzima y sustratos libres y K 2 es la constante de rapidez para la conversin del complejo ES en el producto P y la subsecuente liberacin del producto de la enzima. La enzima aparece explcitamente en el mecanismo, y por lo tanto, en las ecuaciones
3
Determinacin de la Velocidad de la Reaccin Catalasa.
de rapidez aparecen las ecuaciones tanto de la enzima libre, E, y como del complejo enzima-sustrato, ES. Si medimos la rapidez de una reaccin enzimtica con distintas concentraciones de sustrato, vemos que la rapidez depende de la concentracin del sustrato [S]. () esta velocidad suele denotarse por V 0 para indicar que es la inicial pero es importante recordar que todos los clculos relacionados con la cintica enzimtica suponen que la velocidad medida es la inicial. La concentracin a la que la reaccin se efecta a la mitad de su velocidad mxima tiene importancia especial, se le llama constante de Michaelis. Se denota como KM y puede considerarse una medida inversa de la afinidad de la enzima por el sustrato. Cuanto ms baja es la KM, mas alta es la afinidad. Los exponentes de la reaccin suelen ser 1 o 2. Los valores de los exponentes estn relacionados con el nmero de molculas que intervienen en los pasos detallados que constituyen el mecanismo. El orden total de una reaccin es la suma de todos sus exponentes. Por ejemplo si la rapidez de una reaccin reactivo-> producto est dada por la ecuacin de rapidez Rapidez = k[reactivo]1 Donde k es la constante de rapidez y el exponente de la concentracin del reactivo es 1, la reaccin es de primer orden respecto al reactivo y de primer orden total. (Campbell, M. 2004, p. 136-145) Si la concentracin de sustrato es tan alta que la enzima se satura con sustrato, la reaccin se efecta a la velocidad mxima posible ( Vmax), la cual puede estimarse burdamente en la curva al igual que la KM. La Vmax nos permite relacionar la velocidad observada con cualquier concentracin de sustrato y la rapidez mxima de una reaccin enzimtica: Sustituyendo ecuaciones tenemos que V= Vmax [S] (Campbell, M. 2004, p. 138)
KM + [S]
2. Objetivo
Disear un dispositivo que sea capaz de medir la cantidad de oxigeno producido a travs de la reaccin producida por la combinacin de catalasa con perxido de hidrogeno.
Determinacin de la Velocidad de la Reaccin Catalasa.
3. Metodologa
3.1 Dispositivo
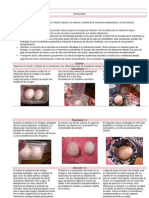
Para la realizacin del dispositivo se empleo el siguiente material: un recipiente de plstico con tapa, una probeta graduada a 50 ml, pinzas, un tornillo, una manguera de hule de aproximadamente 40 cms, plastiloca o bien en cu caso plastilina, una botella de 330 ml preferentemente de pet . Primeramente se elaboraron dos orificios (uno al dimetro de la probeta y otro al de la manguera) con ayuda del tornillo caliente sostenido por las pinzas para mayor seguridad. En el orificio antes mencionado de dimetro de la manguera colocamos a esta, mientras que en el segundo orificio se coloco la probeta; para asi ser sellado por plastilina evitando fugas Posteriormente se realizo una perforacin en un costado de la botella de PET para por este orificio introducir el otro extremo de la manguera y de igual forma ser sellado. Mientras que a la tapa de la botella se hizo un pequeo hoyo del dimetro de una aguja (de jeringa).
3.2 Catalasa
Para la medicin de el oxigeno liberado en la reaccin utilizaremos hgado de pollo macerado, agua del grifo, agua oxigenada y el dispositivo previamente realizado. Empezaremos por llenar tres cuartas partes del dispositivo con el agua de grifo, mientras que la probeta, que se encuentra en la parte superior del dispositivo, ser llenada por completo para as ser tapada. Utilizando una jeringa mediremos 1.5 ml de hgado macerado el cual colocaremos en el interior de la botella para posteriormente ser sellada con su correspondiente tapa, colocaremos la jeringa de 20 ml que previamente fue llenada con agua oxigenada para poder vrtela sobre el hgado en el interior de la botella a una proporcin de 1 ml cada 5 segundos y de esta manera observar la liberacin del oxigeno que se har presente en el cambio del nivel de agua en la probeta. Observaciones: Dicho procedimiento ser repetido tres veces para asi asegurar la precisin de los datos obtenidos.
Determinacin de la Velocidad de la Reaccin Catalasa.
En las reacciones anteriores, es necesario tomar nota de los datos obtenidos para as despus realizar las graficas correspondientes
4. Resultados 5. Discusin
Previamente a nuestra practica, se tomo en cuenta la propiedad de desnaturalizacin de protenas que como menciona Acua, F., (2006) ocurre cuando estas se exponen al calor (temperatura mayor a 50) alterando de esta manera sus estructuras secundaria terciaria y cuaternaria; dejando intacta la estructura primaria por lo que pierde su actividad biolgica. Retomando este principio, podemos explicar la efectividad del hgado crudo y macerado utilizado para la experimentacin, pues como se observo las clulas rotas, permitieron que la catalasa actuara ms rpido sobre la reaccin. De acuerdo con Mertz, E., (1980) que nos dice, que el perxido de hidrogeno, componente de alta toxicidad, producido durante las reacciones de la clulas vivas, es inmediatamente descompuesto por los catalizadores, que aumentan la velocidad de las reacciones. Por nuestra parte podemos decir que estamos en total acuerdo con dicho investigador, pues al colocar agua oxigenada, o bien, perxido de hidrogeno sobre el hgado previamente macerado, durante nuestro experimento (el cual como se sabe posee la enzima catalasa capaz de catalizar la descomposicin del perxido de Hidrogeno cuando el hem est unido a la protena especifica, como lo afirma Claude, W. en 1991) se observa un burbujeo indicndonos con ello la liberacin de oxigeno y la existencia de agua, comprobando efectivamente la descomposicin de el perxido de hidrogeno de la siguiente manera: Catalasa 2 H2O2 2 H20 + O2
Por otra parte vale la pena mencionar, el tipo de la reaccin presente en el dispositivo la cual es irreversible pues el oxigeno liberado en la botella pasa inmediatamente a el recipiente a travs de una manguera, evitando de esta manera que el oxigeno regrese y forme de nuevo nuestro componente de toxico (perxido de hidrogeno). Qumicamente la reaccin se representa con la siguiente
Determinacin de la Velocidad de la Reaccin Catalasa.
ecuacin, donde la doble flecha nos indica la irreversibilidad, debido a que uno de los productos (el oxigeno) abandona la reaccin, escapando en este caso de manera gaseosa. (Baker JW y Allen, GE, 1973) Catalasa 2 H2O2 2 H20 + O2
Dicha reaccin dems de ser irreversible, se logro determinar que es perteneciente a las reacciones de tipo exergonicas, pues como menciona Baker JW y Allen, GE en 1973, las reacciones exergonicas, son aquellas que liberan ms energa de la que absorben; hecho con el que no solo se est de acuerdo si no tambin es comprobable en la experimentacin pues en la botella donde se coloco el hgado y el agua oxigenada se percibi un aumento de temperatura.
Gracias la cintica enzimtica que como afirma Campbell, M., (2004) estudia la rapidez de una reaccin midiendo la desaparicin de o de los reactivos o la aparicin del producto, se pudo determinar con xito la velocidad de la reaccin del hgado molido con agua oxigenada ya que en dicha reaccin se hicieron presentes el agua y el oxigeno (productos) midiendo con ayuda de la graduacin de la probeta, y echando mano de un cronometro, el oxigeno liberado a travs del desplazamiento de agua. Durante la experimentacin se repiti el proceso tres veces, como bien se menciono en la metodologa obteniendo datos parcialmente diferentes y registrndolos en tablas para posteriormente ayudarnos de tasa de reaccin que como bien nos dice Baker JW y Allen, GE, (1973) mide el cambio de concentracin en determinado tiempo, para trazar grficas que nos permitieron observar el cambio a largo de la practica.
6. Conclusiones
El programa de biologa V correspondiente a sexto grado, unidad dos Metabolismo, para el cual se ha realizado dicha prctica, ayudndonos de forma interactiva a comprender, analizar y hacer propio el conocimiento referente a los procesos metablicos entendindose estos mismos como anabolismo el cual
Determinacin de la Velocidad de la Reaccin Catalasa.
comprende reacciones de sntesis, y catabolismo, degradacin.
es decir, reacciones de
Dentro de dichos conceptos, se puede concluir que la descomposicin de perxido de oxigeno al hacerse reaccionar con la enzima catalasa, forma parte de un proceso perteneciente al catabolismo, el cual es llevado a cabo dentro de las clulas vivas; hecho que pudo ser comprobable por medio de la experimentacin Factores a autoevaluar Brock Prez Liliana Espinos a Martin del Campo Mauricio Ruiz Martnez Dayzi Lizette Snchez Mendoza Adriana Santos Castrejon Oscar Roberto Yrra de la Cruz Luis ngel
cientfica. Adems de lo antes dicho podemos rematar con lo efectivo que resulto el uso de un catalmetro, o bien dispositivo para la medicin del oxigeno durante la reaccin pues gracias a este obtuvimos resultados concisos.
Determinacin de la Velocidad de la Reaccin Catalasa.
Inters en el tema Disponibilidad de tiempo Bsqueda de informacin Puntualidad en el envi de la informacin Redaccin y consistencia en las ideas Cumplimiento de material Manejo del formato APA
10 10 10 10
10 10 10 10
10 10 10 10
10 10 10 10
10 10 10 10
10 10 10 10
10
10
10
10
10
10
10 10
10 10
10 10
10 10
10 10
10 10
7. Bibliografa
Acua, F. 2006. Qumica orgnica. EUNED. Costa Rica. 312 Welch, Chaude A. etal. (1991) Ciencias biolgicas. Educational Programs Improvement Corporation. Mxico. p. 201-206
Determinacin de la Velocidad de la Reaccin Catalasa.
Campbell, Mary K. y Farrell, Shawn O. (2004) Bioqumica. Editorial Thomson. Mxico. p. 136-146 Baker, Jw y Allen GE. (1973) Materia, energa y vida. Fondo educativo Interamericano. Mxico.
8. Autoevaluacin
10
Anda mungkin juga menyukai
- Practica 4Dokumen18 halamanPractica 4Manuel Durden100% (11)
- Practica 4 QUIMICA INDUSTRIALDokumen10 halamanPractica 4 QUIMICA INDUSTRIALChak DíazBelum ada peringkat
- Cinética QuímicaDokumen10 halamanCinética QuímicaShalBelum ada peringkat
- Modelamiento y casos especiales de la cinética química heterogéneaDari EverandModelamiento y casos especiales de la cinética química heterogéneaPenilaian: 3 dari 5 bintang3/5 (1)
- 10°. QuímicaDokumen5 halaman10°. QuímicaamaliaBelum ada peringkat
- Practica No.4 Quimica Industrial-E4Dokumen21 halamanPractica No.4 Quimica Industrial-E4Renata Beatríz Castillo RuizBelum ada peringkat
- Cinetica CatecolDokumen9 halamanCinetica CatecolkaruchimBelum ada peringkat
- Laboratorio Cinetica Juan PeñaDokumen10 halamanLaboratorio Cinetica Juan PeñaJUAN MANUEL PENA TORRESBelum ada peringkat
- Cinetica Química, Adrian QuispeDokumen21 halamanCinetica Química, Adrian QuispeAdrian QuispeBelum ada peringkat
- INFORME 9 FICO 2 FinalDokumen26 halamanINFORME 9 FICO 2 FinalAldahir BernalBelum ada peringkat
- Plascencia Brandon P3Dokumen4 halamanPlascencia Brandon P3Brandon PlascenciaBelum ada peringkat
- Practica ArrehniusDokumen12 halamanPractica ArrehniusAnfer MarreroBelum ada peringkat
- Quimicapr 4Dokumen6 halamanQuimicapr 4Eduardo BeltranBelum ada peringkat
- Cinética química laboratorio biofarmaciaDokumen11 halamanCinética química laboratorio biofarmaciageorginaBelum ada peringkat
- Informe de Cinetica.Dokumen15 halamanInforme de Cinetica.MaximilianoRGBelum ada peringkat
- Proyecto de Cinética QuímicaDokumen27 halamanProyecto de Cinética QuímicaMarlen Naranjo100% (2)
- Enzimas Taller PDFDokumen21 halamanEnzimas Taller PDFjennifer cuadradoBelum ada peringkat
- Cinetica QuimicaDokumen12 halamanCinetica QuimicaLucia CeballosBelum ada peringkat
- Las Ecuaciones Termoquímicas Son Aquel5to - TERMOQUIMICA 2Dokumen37 halamanLas Ecuaciones Termoquímicas Son Aquel5to - TERMOQUIMICA 2Belen Vitale100% (2)
- Informe Completo CatalisisDokumen16 halamanInforme Completo CatalisisFRANCO VALENCIA CHINARROBelum ada peringkat
- Informe 15 N CINETICADokumen17 halamanInforme 15 N CINETICANICK MARALLANOBelum ada peringkat
- Cinética Química: Factores que afectan la velocidad de reacciónDokumen18 halamanCinética Química: Factores que afectan la velocidad de reacciónRafa AlemanBelum ada peringkat
- Cinética química: Influencia temperatura y catalizadorDokumen85 halamanCinética química: Influencia temperatura y catalizadorDavidSenderBelum ada peringkat
- Cinética química: factores que afectan la velocidad de reacciónDokumen11 halamanCinética química: factores que afectan la velocidad de reacciónLuis PerezBelum ada peringkat
- VELOCIDAD DE REACCIÓNDokumen8 halamanVELOCIDAD DE REACCIÓNALFONSO HERNANDEZBelum ada peringkat
- Anteproyecto 2. Bojórquez Méndez Edward AntonioDokumen12 halamanAnteproyecto 2. Bojórquez Méndez Edward AntonioEdward MendezBelum ada peringkat
- Cinètica QuìmicaDokumen23 halamanCinètica QuìmicaAndriceilys BritoBelum ada peringkat
- Practica 4 Cinética QuímicaDokumen19 halamanPractica 4 Cinética QuímicaGeovany Leon AlvarezBelum ada peringkat
- 5to INFORME DEL LABORATORIODokumen21 halaman5to INFORME DEL LABORATORIOAlex LennyBelum ada peringkat
- Informe Cinética Fund. 2Dokumen11 halamanInforme Cinética Fund. 2Sara Gabriela CGBelum ada peringkat
- Cinética enzimática: Generalidades y marco teóricoDokumen40 halamanCinética enzimática: Generalidades y marco teóricothania romero ojedaBelum ada peringkat
- Estudio cinético de la oxidación del ioduro de potasio por el persulfato de amonioDokumen14 halamanEstudio cinético de la oxidación del ioduro de potasio por el persulfato de amonioRodrigo DalenceBelum ada peringkat
- Cinética Química YaszDokumen37 halamanCinética Química YaszChely DíazBelum ada peringkat
- Taller Sobre ENZIIMAS.Dokumen7 halamanTaller Sobre ENZIIMAS.omar correa londoñoBelum ada peringkat
- Apuntes CineticaDokumen12 halamanApuntes CineticaSerchecko JaureguiBelum ada peringkat
- Cinetica Inf InoDokumen27 halamanCinetica Inf InoMary Kely Chambi ChoqueBelum ada peringkat
- Enzimas Determinación CuantitativaDokumen14 halamanEnzimas Determinación CuantitativaIngeniero PerezBelum ada peringkat
- Practica #4 Fisicoquimica IIDokumen31 halamanPractica #4 Fisicoquimica IIRicardo BarriosBelum ada peringkat
- Cinetica Quimica 11Dokumen24 halamanCinetica Quimica 11jacqueline sauce canazaBelum ada peringkat
- Art. Inversión de La SacarosaDokumen8 halamanArt. Inversión de La SacarosaLuigy L-aBelum ada peringkat
- 6417 Manuscrito 35995 1 10 20201207Dokumen8 halaman6417 Manuscrito 35995 1 10 20201207ingridcorcollBelum ada peringkat
- Practica 3 Equipo3Dokumen6 halamanPractica 3 Equipo3Flores Acosta Karen SamaraBelum ada peringkat
- Lab 12 QMC 1206Dokumen19 halamanLab 12 QMC 1206jacqueline sauce canazaBelum ada peringkat
- Cinética QuímicaDokumen42 halamanCinética QuímicaMileBelum ada peringkat
- Informe Lab 3 - Orden de ReaccionDokumen9 halamanInforme Lab 3 - Orden de ReaccionHILARIO JUNIOR CACERES MEDINABelum ada peringkat
- Practica 10 Cinetica Química de Una RX CatalizadaDokumen49 halamanPractica 10 Cinetica Química de Una RX CatalizadaDanny GarcíaBelum ada peringkat
- Laboratorio Integral II Ecuacion de ArrheniusDokumen14 halamanLaboratorio Integral II Ecuacion de ArrheniusJose Alfredo Vargas25% (4)
- Practica N - 4Dokumen15 halamanPractica N - 4MARIANOBelum ada peringkat
- Guía de Cinética QuimicaDokumen13 halamanGuía de Cinética Quimicafelipe jaraBelum ada peringkat
- Practica 2 Oxisacion Del Ioduro de PotasioDokumen14 halamanPractica 2 Oxisacion Del Ioduro de PotasioPameCMBelum ada peringkat
- CLASE 1 CinéticaDokumen11 halamanCLASE 1 CinéticacarlarelyBelum ada peringkat
- Reporte Práctica 6Dokumen9 halamanReporte Práctica 6Jesus Miguel Melendez SanchezBelum ada peringkat
- Fisico Quimica Informe 3Dokumen10 halamanFisico Quimica Informe 3heydeee hinostroza obregonBelum ada peringkat
- La Cinética Química Es Un Área de La Fisicoquímica Que Se Encarga Del Estudio de La Rapidez de ReacciónDokumen10 halamanLa Cinética Química Es Un Área de La Fisicoquímica Que Se Encarga Del Estudio de La Rapidez de ReacciónEdgar Huanca AguilarBelum ada peringkat
- Cinética QuímicaDokumen8 halamanCinética QuímicaPiedriTa Jr A AlvarezBelum ada peringkat
- Informe 8 de FisicoquimicaDokumen19 halamanInforme 8 de FisicoquimicaYuli Friney AstoBelum ada peringkat
- Química CinéticaDokumen9 halamanQuímica CinéticajonasBelum ada peringkat
- Ecuacion ADokumen19 halamanEcuacion Anenjijesus123Belum ada peringkat
- Fisicoquimica Unidad I - Silvia MedinaDokumen14 halamanFisicoquimica Unidad I - Silvia MedinaSilvia Medina Cakes and CookiesBelum ada peringkat
- Temario Unidad 2Dokumen2 halamanTemario Unidad 2Luis Angel YrraBelum ada peringkat
- Origami AdnDokumen1 halamanOrigami AdnLuis Angel YrraBelum ada peringkat
- MicrocosmosDokumen10 halamanMicrocosmosLuis Angel YrraBelum ada peringkat
- HemofiliaDokumen20 halamanHemofiliaLuis Angel YrraBelum ada peringkat
- Tabla de FenotipoDokumen3 halamanTabla de FenotipoLuis Angel YrraBelum ada peringkat
- ÓsmosisDokumen3 halamanÓsmosisLuis Angel YrraBelum ada peringkat
- Enfoque de Los Carbohidratos en La Nutrición y Problemas de Salud.Dokumen10 halamanEnfoque de Los Carbohidratos en La Nutrición y Problemas de Salud.Luis Angel YrraBelum ada peringkat
- GalactosemiaDokumen17 halamanGalactosemiaLuis Angel Yrra100% (1)
- Unidad Tres Biologia. Regulación y Continuidad de La VidaDokumen3 halamanUnidad Tres Biologia. Regulación y Continuidad de La VidaLuis Angel YrraBelum ada peringkat
- Temario - NutricionDokumen4 halamanTemario - NutricionLuis Angel YrraBelum ada peringkat
- Guía 13 Grupos Funcionales y Clasif de Com Puestos Orgánicos Parte 2Dokumen3 halamanGuía 13 Grupos Funcionales y Clasif de Com Puestos Orgánicos Parte 2Liliana HernándezBelum ada peringkat
- 160 Química - Jun2014Dokumen4 halaman160 Química - Jun2014Miguel MarínBelum ada peringkat
- Manual Presion 24-Feb-2020Dokumen27 halamanManual Presion 24-Feb-2020luis fernando contrerasBelum ada peringkat
- Analisis Gravimetrico de CobreDokumen20 halamanAnalisis Gravimetrico de CobreLuis Alberto Rondon Gutierrez0% (1)
- DC-LI-FR-001 Practica 6 Estequiometria Relaciones Peso PesoDokumen4 halamanDC-LI-FR-001 Practica 6 Estequiometria Relaciones Peso Pesoangie daniela vanegas vanegasBelum ada peringkat
- Lab. 1 ConcretoDokumen12 halamanLab. 1 ConcretoAlejandro VarelaBelum ada peringkat
- Costos Sacha Inchi - 2018Dokumen24 halamanCostos Sacha Inchi - 2018Carlos Antonio100% (4)
- Manual de Prácticas - HidrocarburosDokumen4 halamanManual de Prácticas - HidrocarburosJuan Camilo CamachoBelum ada peringkat
- Monografia Arsenico+5Dokumen47 halamanMonografia Arsenico+5Gelvi CanalesBelum ada peringkat
- LUMINOLDokumen4 halamanLUMINOLOscar Josue Lopez SepulvedaBelum ada peringkat
- Pigmentos CeramicosDokumen125 halamanPigmentos CeramicosJesus FloresBelum ada peringkat
- Interline 850Dokumen4 halamanInterline 850florhandalBelum ada peringkat
- Lista de Materiales Peligrosos y Matriz de CompatibilidadDokumen16 halamanLista de Materiales Peligrosos y Matriz de CompatibilidadYordi Paredes VilcaBelum ada peringkat
- Bonba de Agua y SoldadoDokumen2 halamanBonba de Agua y SoldadoMihai BouwmeesterBelum ada peringkat
- Cementación del cobre: proceso sencillo para recuperar cobre de soluciones lixiviantesDokumen82 halamanCementación del cobre: proceso sencillo para recuperar cobre de soluciones lixiviantesEmerson SivinchaBelum ada peringkat
- CATALAZADokumen7 halamanCATALAZAerika jimenaBelum ada peringkat
- Quimica en Ingenieria Civil - Metales - R. LopezDokumen14 halamanQuimica en Ingenieria Civil - Metales - R. LopezRhemy DannBelum ada peringkat
- Envases y embalajes: materiales metálicos para envasado alimenticio (hojalata, lámina cromada, aluminioDokumen309 halamanEnvases y embalajes: materiales metálicos para envasado alimenticio (hojalata, lámina cromada, aluminioAlexandro Jimenez HuashuayoBelum ada peringkat
- Enlace CovalenteDokumen5 halamanEnlace CovalentelabeitiBelum ada peringkat
- El PlomoDokumen34 halamanEl Plomobruno100% (1)
- DownstreamDokumen19 halamanDownstreamYris Omar Torrez100% (1)
- SDS Trac 102Dokumen9 halamanSDS Trac 102Operador fs Farma capsulasBelum ada peringkat
- Procesos Neumáticos de AceraciónDokumen43 halamanProcesos Neumáticos de Aceracióncoreano63Belum ada peringkat
- Stok Fermentativo Levapan (Vinaza) 09feb1602Dokumen2 halamanStok Fermentativo Levapan (Vinaza) 09feb1602Cesar Augusto Colorado RamirezBelum ada peringkat
- Reporte P6 Cromatografía en Capa FinaDokumen6 halamanReporte P6 Cromatografía en Capa FinaEmilio ZendejasBelum ada peringkat
- Variables Fisicas Del AguaDokumen1 halamanVariables Fisicas Del AguaAxel Guerrero ingaBelum ada peringkat
- Fugacidad y Coeficientes de Fugacidad para Especies en Solución.Dokumen3 halamanFugacidad y Coeficientes de Fugacidad para Especies en Solución.Andrea Sarahi Izquiy VBelum ada peringkat
- Materiales TP #6 - Yamila OsmanDokumen37 halamanMateriales TP #6 - Yamila OsmanAnonymous HdENZfRBelum ada peringkat
- Obtención de un epóxido y apertura del anilloDokumen9 halamanObtención de un epóxido y apertura del anilloNaty TitiBelum ada peringkat
- Quimica OrganicaDokumen25 halamanQuimica OrganicaAnghii Patricio100% (1)