Trabajo de Pirometalurgia
Diunggah oleh
Juan Carlos Quezada NievesHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Trabajo de Pirometalurgia
Diunggah oleh
Juan Carlos Quezada NievesHak Cipta:
Format Tersedia
Curso:Preparacion y consentracion de minerales E.A.
P :
Ingeniera de Minas
Apellidos y nombres :Quezada Nieves juan carlos
trabajo : Codigo: pirometalurgia del zinc 09160281
1. INTRODUCCIN 1.1. Antecedentes histricos 1.2. Usos del zinc 1.3. Recursos del zinc 1.3.1. Minerales de zinc 2. Tratamientos previos de las menas 2.1. Concentracin de menas 2.2. Tostacin y sinterizacin 2.2.1. El proceso de tostacin 2.2.2. Sinterizacin 3. diferente estapas de produccin del zinc 3.1 separacion de concentracin del zinc 3.2. Refinado 3.3. La Extraccin por va hmeda (por electrlisis o hidrometalurgia) 3.3.1. El Tueste 3.3.2. Lixiviacin 3.3.3. Purificacin de la solucin 3.3.4. Electrolisis 3.4. La Extraccin trmica o pirometalurgia) por va seca (conocida tambin como va 3.4.1. Procesos de reduccin trmica 3.4.2. Proceso de retortas horizontales 3.4.3. Proceso de retortas verticales 3.4.4. Proceso Electrotrmico 3.4.5. Horno de Cuba de zinc. Proceso ISF 4. Compuestos de zinc 5. Polvo de zinc 6. El zinc, el medio ambiente y la toxicidad 7. Conclusiones y discusiones 8. BIBLIOGRAFIA
1 INTRODUCCIN 1.1. Antecedentes histricos. 1.1.1. ZINC El zinc metlico fue conocido probablemente por los pueblos antiguos. De hecho, hay referencias que parecen hablar del zinc, al que Strabos llamaba plata falsa, en Mysia (Grecia), donde se encontraron depsitos de blenda y otros sulfuros. Tambin se hallaron algunos objetos de zinc en diferentes lugares: una estatuilla en Transylvania y un frontal de fuente en las ruinas de Pompeya. Hay referencias romanas del 200 A.C. en las que se puede probar el uso del latn por los romanos e incluso, en tiempos de Augusto, se describe un procedimiento para fabricar latn reduciendo lentamente xido de zinc en un crisol lleno de chatarra de cobre. La chatarra incorporaba lentamente el zinc vaporizado y luego se elevaba la temperatura para proceder a la fusin de la aleacin. En la Edad Media, los alquimistas conocan procedimientos para transmutar cobre en oro; realmente, la operacin consista en fabricar latn. Al parecer, la primera referencia sobre el zinc metal y sus propiedades se encuentra en la obra de Paracelso. Un escritor chino del siglo VII habla del uso del zinc y de cmo hacerlo maleable para fabricar monedas y espejos. En la India hay referencias que dicen que se funda comercialmente en el siglo XIV. En Zawar aparecen una multitud de restos metalrgicos y mineros de metal; en particular, llaman la atencin las retortas de barro cocido, las alargaderas y condensadores y los grandes escriales y escombreras encontradas all, lo cual denota una actividad minera y metalrgica importante sobre miles de toneladas. Durante los siglos XVII y XVIII se importaron de Asia cantidades importantes de zinc en placas llamadas spelter. Los ingleses a mediados del siglo XVIII importaron de China la tecnologa de fabricacin del zinc y montaron un horno en Bristol (figura 2.1.a) similar a los utilizados para vidrio; poda alcanzar 1000C y en l se trataba una mezcla de mena oxidada y carbn dentro de una retorta que destilaba el metal, a travs de una alargadera condensadora, el cual se recoga en un recipiente situado al final del reactor. En Silesia comienza la obtencin de zinc a finales del mencionado siglo en hornos de vidrio (figura 2.1.b) en los que se introducan las retortas, saliendo gases y vapores por la parte alta de la carga a un condensador del que drenaba el metal a un plato. Los belgas desarrollaron un horno de reverbero con la posibilidad de cargar varias filas de retortas horizontales, que finalmente se construyeron de seccin elptica, con sus correspondientes condensadores acoplados en la parte externa del horno.
Figura 2.1. a) Horno ingls para la produccin de zinc. b) Horno Silesia para la reduccin de zinc
Pocos avances se consiguieron en esta segunda mitad del siglo XIX que no sean la mejora de la calidad y la durabilidad de las retortas, algunos ahorros de energa y mejoras en la condensacin y recoleccin del metal. Por esta poca, se puso a punto el proceso para la reoxidacin del metal reducido a travs de una parrilla perforada con el fin de fabricar xido de zinc: Proceso Wetherill. A finalesde siglo, se instalaron regeneradores en los hornos y se introdujo el calentamiento con gas. Los hornos evolucionaron hacia grandes tneles con varias filas de retortas para aumentar la capacidad (200 por cada lado). A finales de siglo se tostaba blenda para obtener cido y el tostado (mal llamado calcine) se enviaba a las plantas para su reduccin. Tambin se comenz a lixiviar el tostado para producir sulfato y se intent electrolizar la disolucin, aunque el proceso result un fracaso. El descubrimiento de la flotacin con espumas a principios del siglo XX revolucion la industria del zinc, en particular cuando se puso en marcha la flotacin diferencial. La Primera Guerra Mundial hizo aumentar la produccin de zinc y fue entonces cuando el proceso electroltico se desarroll de forma industrial. La reduccin vertical en continuo se desarroll con los procesos New Jersey y St. Joseph; sin embargo, la reduccin en horno elctrico comenz a principios de siglo en Suecia; no obstante, no fue hasta que el horno St. Joseph, para la produccin de xido de zinc, se puso en marcha en el ao 1930 que se dispuso de una tecnologa bien desarrollada. Una buena fabricacin de snter y la condensacin del zinc mediante salpiqueo de metal fundido permitieron la obtencin de metal, a escala comercial", en ambos procesos. La elaboracin de zinc en horno de cuba se desarroll en Inglaterra en los cincuenta al ponerse en marcha la tecnologa del horno Imperial Smelting, que conlleva una sinterizacin distinta y un condensador de plomo fundido. Hoy da, a comienzos del siglo XXI, hay que decir que la tecnologa electroltica es el desarrollo que ms tonelaje de metal produce, indudablemente por su economa y por la calidad del metal.
1.2. Usos del zinc. En el diagrama de sectores de la figura 2.2 se resumen los diferentes usos industriales del zinc. Est claro que prcticamente la mitad del metal se usa en galvanizacin y en el recubrimiento del acero por las distintas tecnologas que incluyen el uso de aleaciones mixtas zinc-aluminio. Figura 2.2. Distribucin del consumo del zinc por usos industriales.
El uso siguiente ms extendido hoy es el de la fabricacin de aleaciones base zinc (en 1982 era para bronces y latones); a continuacin, se sita la fabricacin de latones y bronces, despus los semimanufacturados y los compuestos qumicos y, finalmente, el zinc en polvo. En cuanto a usos finales del zinc, la construccin consume el 45%, el transporte un 25%, maquinaria y equipo un 11%, infraestructuras pblicas un 10% y bateras elctricas y otros el 9% restante. 1.3. Recursos del zinc. El contenido en zinc de la corteza terrestre es del 0,0132% lo que supone una cantidad importante ya que solamente en el kilmetro ms externo de dicha corteza hay un contenido de 52 1012 Mg. Sin embargo, slo interesan, para su aprovechamiento, aquellas zonas donde la concentracin es al menos cien veces superior a aquella y en donde, en ocasiones, adems existen otros metales asociados como el cobre, el plomo y la plata.
1.3.1. Minerales de zinc. Estos minerales, en particular la blenda, contienen asociadas importantes cantidades de cadmio, metal que proporciona un sustancial valor aadido. Tambin se asocia la esfalerita a la galena por lo que algunas minas producen, simultneamente, zinc y plomo. La calcopirita tambin suele estar presente, as como pequeas cantidades de plata y oro. Las gangas suelen ser calcita o dolomita y, a veces,cuarzo. La fluorita y la barita tambin estn presentes eventualmente.
Tabla 2.3. Minerales de zinc ms comunes
2. Tratamientos previos de las menas. Como ocurre normalmente en metalurgia extractiva, las distintas menas, antes de su tratamiento qumico extractivo, necesitan de una preparacin fsica y qumica mediante operaciones de muy distinta naturaleza. Por ello, a continuacin, se estudian la concentracin de los minerales y su tratamiento por tostacin y sinterizacin. 2.1. Concentracin de menas. La concentracin por flotacin ha venido a resolver el problema de las menas mixtas las cuales, por otra parte, son cada vez ms comunes. No obstante, antes de esta operacin se hace precisa una molienda que libere los distintos componentes del mineral y que, a veces, exige moler por debajo de 50 m. Hay que plantearse un proyecto de molienda-flotacin que haga el tratamiento de la mena econmico. La prctica normal de la flotacin en menas mixtas es flotar primero los minerales de cobre, deprimiendo los de zinc y plomo. A continuacin, se flota la galena, luego la blenda y. a veces, finalmente, la pirita. La flotacin de minerales de zinc ha evolucionado tanto desde comienzos de siglo que, hoy da, se pueden tratar una gran variedad de menas sulfuradas con un xito econmico asegurado. Se han desarrollado tcnicas, por ejemplo, que llegan a flotar carbonato de zinc activando su superficie con sulfuro sdico y usando colectores 1.2. Tostacin y sinterizacin. Al comienzo de la produccin del zinc metal (1746 en Europa) se usaron las calaminas para la obtencin del metal. Slo era precisa una calcinacin para descomponer el silicato hidratado, y dejar as un silicato activado del que el xido de zinc era reducido, en retortas especiales, con carbn. Pero la blenda, que es un sulfuro y, adems, el ms abundante, pronto se intent beneficiar aunque no pueda reducirse directamente con carbn. Pronto se supo que un tratamiento de tostacin converta el mineral en xido y ste ya se poda reducir, pero no se utiliz este descubrimiento, por lo tedioso del proceso de tostacin, hasta que las calaminas se hicieron escazas. Agotados los yacimientos de calamina hubo que recurrir a la blenda siendo necesario desarrollar una tcnica adecuada para su tostacin. El descubrimiento de la flotacin puso en disposicin de tratamiento cantidades importantes de blenda y hoy se puede decir que casi la totalidad de la produccin mundial de zinc se obtiene a partir de sulfuros concentrados por flotacin. El primer paso es, hoy en da, es la obtencin de un xido por tostacin del sulfuro que, para su reduccin por va trmica en horno de cuba, precisa ser sinterizado facilitndose as las reacciones en el horno.
1.2.1. El proceso de tostacin En este proceso, la blenda tiene que oxidarse y convertirse, progresivamente, en xido a medida que el oxgeno penetra en las partculas slidas y se evacua hacia su superficie el SO2. Esta conversin en xido de la blenda se exige tanto para la va pirometalrgica de tratamiento como para la hidrometalrgica, puesto que el sulfuro no se ataca con facilidad por cidos o bases y, adems, es inerte a la reduccin con carbn. No procede tampoco la fusin para mata al ser un metal muy poco noble. La reaccin bsica es la siguiente:
La tostacin debe efectuarse por encima de los 700C, en aire y con continua agitacin. El exceso de aire hay que controlarlo con el fin de que no baje del 4,5% el contenido de SO2 en los gases del horno; esto para el control del proceso y para los requerimientos de la planta de cido sulfrico. En la figura 3.1 se puede ver el diagrama de Kellog para el sistema Zn-S-O a 800 y 1200 K. En el diagrama de la figura se ha sealado la zona de trabajo del tostador en la que se garantiza la conversin total del sulfuro en xido a la mayor temperatura. A la temperatura de 900C, la reaccin 3.1 se desplaza rpidamente hacia la derecha. Mientras en los antiguos procesos el contenido final de azufre del tostado era del 1%, en la tostacin en lecho fluido moderna el contenido es inferior al 0,5%. Este resultado es debido a que aunque el contenido en oxgeno en el lecho es bajo, 3-5% a la salida de gases, el excelente contacto slido-gas hace que se lleve a cabo la reaccin hasta el extremo indicado; por otra parte, la carga fresca se diluye mucho dentro de la masa de material calcinado del lecho. En condiciones normales de temperatura, por encima de los 900C, el sulfato de zinc no debera estar en el horno (como se muestra en los diagrama de Kellog de la figura 3.1). Se puede demostrar fcilmente que si bien a 725C no existe sulfato en ausencia de SO2, en la atmsfera del horno, con un 6-12% de SO2 se forma un sulfato bsico, el 2ZnSO4ZnO, que es estable hasta 850C.
Figura 3.1. Diagrama de Kellog para el sistema Zn-S-O a 800 y 1200 K.
Se puede producir una sulfatacin del polvo que sale del horno a medida que se enfran los gases. La produccin de SO3 se incrementa con la concentracin de O2 en el gas por lo que el exceso de aire debe ser controlado (10-15%). As el SO3 es inferior al 1% del azufre total tostado y el peligro de sulfatacin disminuye. Figura 3.2. Distribucin del SO2 en una mquina de sinterizacin.
Aunque hubo unos primeros hornos, muy antiguos e imperfectos, para tostar, las tcnicas para conseguir un buen tostado no se tuvieron hasta el desarrollo de los hornos de solera Wedge y Herreshof; estos hornos casi funcionaban de forma autgena con ayuda de pequeas cantidades de combustible. No obstante, presentaban problemas de pegaduras y de altos costos de mantenimiento por lo que, aunque se utilizaron profusamente, hoy estn en desuso habiendo sido reemplazados por los hornos de lecho fluido, que son ideales para tostar los finos de flotacin. As pues, se puede decir que en las plantas hidrometalrgicas actuales (electrolticas) solamente se instalan tostadores de lecho fluido. Estas unidades tienen una capacidad de produccin alta y bajos costos operativos y de mantenimiento. La tostacin no se puede utilizar en plantas con hornos de reduccin dado que se precisan materiales sintetizados con buenas caractersticas mecnicas, y con porosidad y tamao adecuados. La tostacin por suspensin fue un paso intermedio entre el horno Wedge y el horno de lecho fluido. Cuando se vio que el proceso de tostar se produca al caer el material de solera a solera, se pens en mejorar el contacto gas-slido mediante un quemador de blenda fina, cayendo el producto en una cmara de combustin que se mantena a 950C. La blenda se incendia y cae, tostndose rpidamente. La blenda se secaba en las dos soleras superiores, se retiraba del horno para moler y, luego, se enviaba a los quemadores. Aproximadamente, el 40% del producto se retiraba por el conducto de gases del que se separaba utilizando ciclones y filtros. El calor del gas poda recuperarse en una caldera. Las unidades usadas en Canad por Consolidated M.S.C . procesaban 300 Mg de blenda diaria y desplazaron a los tostadores giratorios de soleras (Wedge). Pero el proceso que se impuso definitivamente fue la tostacin en lecho fluido que haba tenido aplicaciones previas para reacciones gas-slido y que se impuso tambin, en este caso, para la tostacin de blenda. El tamao de partcula y la velocidad del aire son fundamentales. Al principio, se pretenda tostar para llegar a un producto que, lixiviado, produjera la mxima cantidad de zinc con la mnima cantidad de hierro debido a los problemas que acarreaba este metal al intentar su separacin como hidrxido gelatinoso. Se sabe que cuando se calientan a cierta temperatura los xidos de zinc y de hierro forman un compuesto: la ferrita de zinc, ZnOFe2O3. Si el hierro est en forma sustitucional en la blenda, la formacin de la ferrita es inmediata y completa. Incluso si el hierro est como pirita, a la temperatura de tostacin de 900C, se fija el 90% del Fe como ferrita. Estos hechos hicieron el que, al principio, la lixiviacin se llevara a un pH en el cual no se disolviera la ferrita para no contaminar la
disolucin. Las capacidades de tratamiento de estos hornos varan entre 500 y 1000 Mg de blenda diaria. Son hornos de bajo coste de mantenimiento y, adems, el gas tiene una concentracin en SO2 que llega al 10% con lo que el rendimiento de la planta de cido sulfrico es excelente. Energticamente, son muy eficaces produciendo en una caldera, a la salida de gases, un kilogramo de vapor de alta por cada kilogramo de blenda tostada. Como tostacin previa a la lixiviacin, el proceso es ideal para la mayora de los concentrados; solamente, si los contenidos de plomo superan el 3%, pueden producirse aglomeraciones que interfieren la operacin del lecho. Este tostado fino slo podra usarse en procesos de piro-reduccin, utilizando un briquetado intermedio. El rendimiento de tostacin es de dos toneladas de azufre por metro cuadrado de superficie de parrilla y da. Si se carga la alimentacin del horno en forma de papilla, el rendimiento baja al 70%. Los tiempos de residencia medios en el lecho son de cinco horas, que disminuyen a una hora para los finos; se considera que el lecho se renueva completamente despus de 20 horas. La eliminacin de azufre como sulfuro llega a ser de hasta del 0,1%, estando el azufre tambin presente como sulfato en cantidades todava mayores que varan entre el 0.5 y el 2,5%. Este sulfato es beneficioso pues sirve para paliar las prdidas de cido en el circuito, eso s, siempre que no sea una cantidad excesiva ya que exigira descargas peridicas. La altura del lecho en los tostadores es de 1-1,5 m. La carga del horno es en slido,por cinta o en papilla. El control de la temperatura es importante, fijndose en 900-980C para evitar aglomeraciones. La exotermicidad de la oxidacin de la blenda es tal que hace que sea preciso refrigerar mediante pulverizadores de agua cuando la carga es seca. El tamao de partcula de las blendas tostadas est entre 50 y 300 m (media 200 m). El volumen de hueco es del 0,6 al 0,8 y la velocidad es de 30 -35 m/s con un exceso de aire del 10% sobre el terico para tostar. El SO2 del gas est entre el 8 y el 10%. Las partculas finas se arrastran y el 40% de la blenda tostada se recoge por los rebosaderos. El gas se enfra en las calderas a 350C y se precisa limpiar los tubos y paredes pues en ellos se producen pegaduras. El gas se limpia en ciclones y, finalmente, en separadores electrostticos. As pues, el material calcinado se recoge, por ejemplo, de esta manera: 40% en los rebosaderos del horno; 20% en las calderas; 35% en los ciclones; y 5% en los precipitadores electrostticos. Estas cantidades varan en funcin de la granulometra de la alimentacin.
1.2.2. Sinterizacin. La sinterizacin de los concentrados de blenda se lleva a cabo en una cinta mquina Dwight-Lloyd (D.LL.). Se carga automticamente con una capa de 15-18 cm de mineral que se enciende, en su parte alta, en la primera caja horizontal, comenzando la aspiracin hacia abajo de los gases de combustin. La zona de reaccin se mueve, por tanto, hacia abajo a una velocidad de 0,25 mm/s siendo la velocidad del gas a travs del lecho 1000 veces superior. La temperatura en la zona de reaccin puede llegar a alcanzar los 1450C. Aproximadamente, en unos veinte minutos el lecho ha reaccionado por completo ajustndose la aspiracin y la velocidad de avance. El contenido de azufre del producto sinterizado se ha reducido por debajo del 1% y se somete a tratamiento de machacado y clasificacin. Es esencial disponer, para producir un buen snter, de una distribucin granulomtrica con las condiciones adecuadas y de una buena mezcla de los ingredientes. El proceso depende, fundamentalmente, de la consecucin de una zona de combustin estrecha que viaje a travs del lecho. Si no hay uniformidad, el producto sinterizado puede estar tostado de forma incompleta. En cuanto al contenido de azufre de la carga, ste debe ser suficiente para conseguir el combustible necesario, pues si hay azufre en defecto, la sinterizacin y tostacin ser parcial, y si lo hay en exceso, la zona caliente fundir y se perder porosidad dando un producto imperfecto. Un 6% de azufre se considera ptimo para la sinterizacin con aspiracin inferior. Como la blenda tiene un 30% de azufre, no se puede sinterizar directamente exigindose bien una tostacin parcial previa o bien recircular los cinco sextos de la carga sinterizada con moliendas intermedias para diluir el material. A pesar de que ste pasa cinco veces por el snter, esta prctica se usa en bastantes plantas. La porosidad del lecho es otro aspecto determinante para producir un flujo uniforme de gases. La operacin fundamental para controlar el tamao del slido es la criba de los materiales ya que son el constituyente mayoritario de la carga. Se realiza tamizando por debajo de 4 mm. La humedad debe estar entre el 6 y el 7% para asegurar un buen contacto de la carga pero si la humedad es excesiva se pierde porosidad. La carga se debe dosificar de la mejor manera posible; el material de retorno, y los minerales y fundentes que se almacenan en las tolvas, se pesan y dosifican en forma continua y se mezclan para producir una carga con la composicin adecuada. Estas operaciones de mezcla se hacen en mezcladores de naturaleza diversa. La mezcla se hace humedeciendo la carga de forma simultnea. Hay tambin dispositivos para alimentar a la mquina D.L.L. la cantidad exacta de lecho sobre las parrillas, lo cual se hace controlando su altura.
El contenido en SO2 de los gases debe de ser suficiente para que funcionen bien las plantas de cido. Para ello, se evitan las entradas de aire por juntas o agujeros en la carga. La distribucin del SO2 en los gases se representa en la figura 3.2 tanto para una mquina con aspiracin superior como con inferior. La mxima concentracin se obtiene en la parte central: 10-12%. Para conseguir enriquecer el gas se utiliza la recirculacin del mismo pasndolo de parte de las cajas aspirantes de nuevo por el lecho en la zona anterior. As, el gas recirculado pasa del 2,5 al 7% de SO2. El cadmio y el plomo sufren movilizaciones en la carga del snter durante el proceso. El 70% del cadmio se volatiliza, fundamentalmente, como sulfuro de cadmio que se condensa en las salidas de gases. Se recupera de las barras de forma automtica por golpeo y se obtiene un producto con un 6% de cadmio que se puede lixiviar. El plomo llega a volatilizarse en un 20% y se recoge en el sistema de purificacin de la planta cida como barros de sulfato de plomo. En la tabla 3.1 se presentan los datos operativos de una instalacin Dwight-Lloyd. Tabla 3.1. Datos operativos de una instalacin Dwight-Lloyd.
El sinterizado aspirado por abajo es adecuado para la carga en retortas. Pero el desarrollo del horno Imperial Smelting (ISF) exige un producto grueso, 2,5-10 cm, y resistente. Adems, surgen problemas en este tipo de horno por la reduccin del plomo cuando se utilizan menas mixtas Zn-Pb, segn la reaccin: 2PbO + PbS = 3Pb + SO2 Ec. 3.2 Ya que se taponan las cajas de viento cuando se aspira por abajo. Por esta razn, se ha desarrollado el sistema de soplado desde abajo que comporta el que el plomo
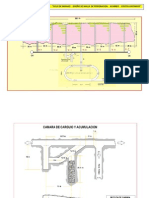
se retenga en el lecho de snter (PortPire y Stolberg) obtenindose el denominado snter duro (figura 3.3). Este desarrollo ha permitido el xito tcnico del horno ISF de reduccin simultnea de Zn y Pb a partir de menas mixtas. Figura 3.3. Diagrama de una instalacin con mquina de sinterizacin de soplado inferior
El funcionamiento de esta sinterizacin invertida requiere de la ignicin por abajo de una capa de coque y de carga del lecho de material que entra inmediatamente en la zona de soplado. Para enriquecer el gas en SO2, las soplantes slo introducen aire en la parte inicial del snter. El gas se recoge y pasa a travs de las parrillas anteriores; lo mismo se hace con el gas de ignicin. En la sinterizacin soplada hacia arriba es muy importante el tamao de las partculas, su buen mezclado y el acondicionado para que no se produzcan arrastres de material. El snter obtenido con el soplado hacia arriba se denomina snter duro porque hay que producir trozos gruesos en oposicin al snter blando producido con aspirado hacia abajo. El material se machaca a menos de 15 cm y luego se tamiza a un tamao de unos 2 cm siendo este producto apto para la carga de los hornos. Lo que queda de menos de 2 cm se tritura hasta menos de 4 mm y se manda al retorno para reducir el azufre de la carga por mezclado (6,5%). Para los procesos en retortas o para el electrotrmico, el sintetizado es una etapa para la reduccin del contenido en azufre, es decir, para la tostacin. Para el ISF el sinterizado supone, adems, la preparacin de la carga. El briquetado del snter blando no es una alternativa econmica para el horno de reduccin ISF. Para los procesos de lixiviacin se siguen las tcnicas antes mencionadas de tostacin en lecho fluido como sistema de obtencin de un producto apto para su ataque.
3. Las diferentes etapas de la produccin de zinc
La extraccin del zinc puede efectuarse en las minas a cielo abierto o en yacimientos profundos. La eleccin del tipo de explotacin depende del entorno y del capital invertido. Cuando se decide explotar una mina a cielo abierto, los mineros cavan huecos con la ayuda de taladros neumticos manuales, en los que colocan cargas explosivas. Una vez extradas, las rocas son transportadas hasta la fbrica de transformacin, que generalmente se encuentra en la misma mina, para comenzar la fase de concentracin.
3.1. Separacin de concentrados de zinc En esta etapa, el mineral es triturado con el fin de obtener partculas muy finas que, segn la naturaleza del mineral, van a ser sometidas a diversos tratamientos qumicos. Se trata de extraer del mineral un mximo de elementos extraos e impurezas. Ms tarde, los diferentes concentrados presentes en la roca son separados por un proceso de flotacin como en el caso de la familia de los platinoides (platino y paladio). Esta tcnica se basa en el hecho de que cuando estn en suspensin, las partculas minerales recubiertas de ciertos productos qumicos se aglutinan en forma de burbujas de aire que son insufladas por la parte de abajo de la clula de flotacin, para subir luego a la superficie. Se forma entonces en la superficie, un depsito espumoso que ser recuperado y enviado a travs de varios filtros. A la salida de este proceso, se recogen diferentes concentrados de zinc. 3.2. Refinado Esta es sin duda la ms importante etapa del proceso. Con el fin de obtener el metal bruto, la industria metalrgica del zinc utiliza dos procedimientos: la hidrometalurgia y la pirometalurgia. 3.3. La Extraccin por va hmeda (por electrlisis o hidrometalurgia) La hidrometalurgia consiste en la produccin, purificacin o la eliminacin de metales o de componentes de metales a travs de reacciones qumicas. Este mtodo es principalmente utilizado en el tratamiento de las rocas que tienen un alto contenido de hierro. Se desarrolla en cuatro fases que son respectivamente: el tueste, la lixiviacin, la purificacin y la electrlisis. 3.3.1. El Tueste El tueste transforma el sulfuro de zinc en xido. El dixido de azufre obtenido permitir obtener cido sulfrico que, por una parte entrar en el proceso de fabricacin de agentes fertilizantes, y por otra parte continuar su proceso hacia la etapa siguiente denominada lixiviacin. El dixido de azufre que se optiene por este proceso es transformado .en acido sulfrico El mieral de zinc despus de la tostacin es llamado calcita.
3.3.2. Lixiviacin Durante la fase de lixiviacin, la calcina es tratada mediante una solucin diluda de cido sulfrico (180-190 g/l). Esta operacin se realiza a una temperatura de aproximadamente 60C y dura entre una y tres horas. En esta fase, queda todava un porcentaje que vara entre 10 y 25% de zinc insoluble que va a ser recuperado gracias a una operacin complementaria. 3.3.3. Purificacin de la solucin Despus de la lixiviacin, algunos elementos externos estn todava presentes en las solucin. Su eliminacin se realizar con la ayuda de polvo de zinc. La cantidad necesaria de polvo de zinc depende del porcentaje de impurezas que contiene la solucin. Esta purificacin dura entre una y ocho horas. Al final del proceso, se recuperan las partculas de zinc por filtracin.
3.3.4. Electrolisis Una vez purificada la solucin, se vierte en depsitos de electrolisis (tanques de cemento revestidos de PVC), constituidos por nodos de plomo y de ctodos de aluminio. Esta operacin necesita entre 30 y 40C y va a permitir al zinc depositarse en el ctodo de dnde se le despegar por pelaje (o stripping) cada 24, 48 o 72 horas, segn el caso. La produccin por celda que contiene hasta 86 ctodos de 1,6 m, puede alcanzar 3 t/da El zinc obtenido es muy puro (99,995 %). Contiene menos de 50 ppm de impurezas, siendo el plomo la principal
Finalmente el zinc obtenido es fundido y moldeado en lingotes, que es como ser comercializado en el mercado industrial. 3.4. La Extraccin por va seca (conocida tambin como va trmica o pirometalurgia) Se presentan, a continuacin, los procesos pirometalrgicos que conducen a la obtencin del zinc metal. Se comienza por los procesos de reduccin trmica y luego se presentarn los procedimientos que acaparan, en la actualidad, el mayor tonelaje de metal. 3.4.1. Procesos de reduccin trmica. Aunque hay vestigios, que datan del siglo XIV, de produccin de zinc en Asia, los procesos que suponan reduccin y condensacin eran totalmente empricos. En 1917, se intent explicar este proceso mediante las reacciones siguientes, de caractersticas reversibles: ZnO(s) + CO(g) = Zn(g) CO (g) 2 + + Ec. C(s) + CO (g) = 2CO(g) 2 + Ec. 4.1 4.2.
Los primeros estudios termodinmicos se hicieron por C.G. Maier en el U.S. Bureau of Mines de EEUU. De los datos termodinmicos calculados se pudo deducir la temperatura a la que se poda producir la reduccin continua del xido de zinc y las proporciones del Zn vapor, CO y CO2 en equilibrio a diferentes temperaturas de tratamiento. De las reacciones anteriores se puede deducir que el CO2 generado en la primera tiende a descomponerse en la segunda. Las condiciones de equilibrio de ambas reacciones se pueden calcular sabiendo que en dichas condiciones G 0 r D = . Por otro lado:
Para la reaccin total, o de reduccin directa, se tiene: ZnO(s) + C(s) Zn(g) + CO(g) Ec. 4.6
Cuya energa libre estndar asociada se calcula sumando la ecuacin 4.3 y 4.4: G[ ] 83380 - 67,52T r 4.6 D = Ec. 4.7
Si ahora se tiene en cuenta la expresin de la isoterma de Vant Hoff, se puede poner que para la reaccin 4.6: r [4.6] Zn CO D G = 83380 - 67,52T + 4,575T log P P Ec. 4.8
En una retorta y suponiendo muy pequea la presin de CO2 a una atmsfera de presin total (mostrada en la figura 4.1 de la cual se deducen los bajos valores de la presin de CO2, para los dos equilibrios anteriores, que a las temperaturas representadas son inferiores a 4 kPa), se tiene entonces PZn=PCO=0,5 atm con lo que: G[ ] 83380 - 67,52T 4,575T log (0,5 0,5) r 4.6 D = + Ec. 4.9
Con lo que a partir de esta expresin se pueden calcular la temperatura de equilibrio la cual resulta ser igual a 1187 K (915C). Se deduce, pues, que la reduccin directa de la blenda no se puede llevar a cabo hasta alcanzar temperaturas superiores a los 915C ya que el proceso no es termodinmicamente posible hasta que se alcanzan dichas condiciones. Existen algunas otras vas de llegar a esta misma conclusin basndose en los equilibrios de las ecuaciones 4.1 y 4.2. En la reduccin directa, de la estequiometra de la reaccin se deduce que Zn O N = N , es decir, que el nmero de tomos de zinc es igual al nmero de tomos de oxgeno y, teniendo en cuenta las reacciones 4.1 y 4.2 los tomos de oxgeno son iguales a las molculas de CO ms dos veces las de CO2 por lo que: ZnO + CO + CO2 N = N + 2 N Y, por tanto, las presiones sern: P = P + 2 P Ec. 4.11 Siendo la presin total igual a: Ec. 4.10
total
En la figura 4.1 se representa la variacin de la PCO (kPa) para los equilibrios de las ecuaciones 4.1 y 4.2 en funcin de la temperatura. Segn esta representacin parece evidente que la reduccin continua del oxido de zinc no tendr lugar por debajo de los 1000C. A temperaturas superiores, debido a que la reaccin 4.6 es ms lenta que la 4.2, se alcanzar el estado de equilibrio con una relacin CO2/CO en el gas cerca de la que determine el equilibrio del xido de zinc; la fuerza impulsora de la reaccin ser la diferencia entre la composicin actual y la requerida para el equilibrio segn la reaccin 4.6 lo que viene representado por las distancias entre las dos curvas de la figura.
Figura 4.1. Presin de equilibrio del CO2 (en kPa) para las reacciones a) 4.1; y b) 4.2.
Ya que se ha considerado que la presin de CO2 es pequea, sustituyendo en las expresiones anteriores los valores de [4.1] K y [4.2] K como funciones de la temperatura, tal como vienen expresados en la isoterma de Van't Hoff, se pueden calcular las distintas presiones de zinc, CO y CO2, y la presin total como funciones de T-1; su representacin se incluye en la figura 4.2.a. Se puede comprobar, una vez ms, que la presin total alcanza 1 atm a los 920C, aproximadamente. En esta figura la presin de vapor del zinc lquido puro est tambin representada en funcin de la temperatura. Se puede ver que a 920C sta es mayor que la presin de zinc en la mezcla reaccionante de lo que se deduce que el zinc se forma como vapor no saturado. Del grfico se deduce que a 1110C la presin del zinc alcanza
la saturacin y los valores que corresponden son PZn = 5 atm y Ptotal = 10 atm, por lo que a altas temperaturas y presiones sera posible obtener zinc, por reduccin directa del ZnO, en forma lquida. A partir de la figura 4.2.b) se pueden explicar tambin las condiciones de reduccin del zinc por va trmica y se pueden ver los efectos de variar las presiones de Zn vapor y de CO. La interseccin de las lneas a presiones de 0,5 atm para ambos gases se produce a 920C, aproximadamente. Del mismo grfico se puede deducir cmo la reduccin del zinc en presencia de cobre, caso de obtencin directa de un latn (como se pudo hacer en tiempos de los romanos), se puede realizar fcilmente.
Si el Zn se recoge como una aleacin Cu-Zn, su actividad pasa a ser, por ejemplo, 0,1 y esta curva corta a la de PCO igual a 1 atm a 890C; como se puede ver, la temperatura de reduccin ha disminuido considerablemente. La cintica de la reduccin del ZnO con C puede explicarse a travs de las siguientes etapas: 1. Reduccin con CO en la superficie del ZnO. 2. Reaccin de Boudouard en la superficie del carbn. 3. Difusin de gases entre las dos superficies. De stas, la etapa que controla el proceso es la tercera. El mtodo utilizado para facilitar este proceso es aumentar el rea superficial y aproximar al mximo los reactivos slidos ZnO y C. Se debe pues tener una mezcla muy ntima de ambos. La temperatura de equilibrio debe sobrepasarse para tener una velocidad de reduccin aceptable (1000-1100C). La velocidad de reaccin intrnseca es mayor entre el gas y el ZnO que entre el gas y el C por lo que un exceso de ste facilita la reduccin del CO2 obtenindose una mayor velocidad en el proceso. Adems, as se aminora la reoxidacin del zinc. Esta reoxidacin del zinc con CO2 por inversin de la reaccin 4.1 es algo que puede suceder. Si no se toman las debidas precauciones, un 1% de CO2 en el gas oxidar un 2% de Zn y el xido de zinc formado cubrir las gotitas de zinc evitando su coalescencia y formando un polvo azul. Contra esto se puede luchar enfriando sbitamente, lo que no es posible en una retorta. El ciclo de la retorta est dibujado en la Lnea a-a de la figura 4.2.b). La reoxidacin se produce cuando se cruza la lnea de presin parcial de zinc de 0,5 atm. Como se ve la relacin CO2/CO disminuye. Cuando la presin del Zn es igual a su presin de saturacin, se condensa el metal. Esto sucede a 840C y a una presin parcial de zinc de 0,5 atm. Para conseguir el 99% de condensacin, la presin parcial del zinc debe ser del orden de 0,01 atm, a una presin total de una atmsfera, lo que sucede a unos 600C. En la prctica, hay un sobreenfriamiento grande: 500C. Se vern ms adelante las formas de evitar la reversin de la reaccin de reoxidacin. La reaccin 4.6 es endotrmica consumiendo 238 kJmol -1. A 1000C, siendo necesario calentar reactivos y productos, adems de evaporar el Zn, el calor pasa a ser de 376 kJmol-1 o, lo que es lo mismo, 5751 kJ por kg de zinc. Como se indicaba, este calor hay que suministrarlo a la retorta a travs de la pared.
Figura 4.2. a) Presiones de equilibrio de Zn, CO y CO2 b) Relacin CO2/CO para la reduccin del ZnO(s) a Zn(l).
La velocidad de reduccin total en la retorta se determina, sin embargo, por la relacin de transferencia de calor de forma que cada elemento de carga alcance una temperatura tal que la velocidad de absorcin de calor, debida a la reaccin, se corresponda con la ganancia de calor por conduccin trmica. Es difcil medir la temperatura de la carga en una retorta, o la temperatura y la composicin del gas. En retortas horizontales, y por mtodos indirectos, parece que anda entre 980 y 1000C. Como en una retorta hay carbn en exceso, la relacin CO2/CO vendr dictada por la reaccin de gasificacin 4.2 producindose una concentracin de CO2 baja. El gas est compuesto, de forma aproximada, por proporciones iguales de Zn vapor y de CO gas con un 1% de CO2, aproximadamente y al enfriar, para recuperar el zinc, se deben tener precauciones especiales. El punto de roco de esta mezcla es de 830C y el zinc comenzar a condensar tan pronto se alcance esta temperatura. El problema que se presenta es que la reaccin 4.1 se invierte tan pronto como la temperatura desciende, producindose la oxidacin del zinc y formndose polvo azul. Si no se enfra rpidamente, la cantidad que se produce de polvo azul puede ser importante. Como ya se ha indicado, el oxido, que cubre al zinc metlico, impide la coalescencia de gotas para formar zinc metal lquido. Sin embargo, si la temperatura desciende mucho, se formar zinc metlico slido que tambin estar en forma de polvo. Por estas razones, la temperatura de los condensadores debe estar por encima de 419C pero con suficiente superficie para eliminar el calor de los vapores. As, el zinc condensa en forma lquida sobre las paredes del condensador recolectndose con menos del 5% de xido. El diseo del condensador deber ser adecuado en cuanto a tamao, forma, conductividad trmica, temperatura, etc. As pues, el producir zinc trmicamente es ms difcil que hacerlo con otros metales. Hasta que el condensador de plomo se desarroll en Inglaterra (1937), el horno de cuba no funcion y se segua produciendo zinc en retortas. Al necesitarse temperaturas sobre los 900C como condicionante termodinmico para producir zinc, se precisaron hornos que alcanzasen este nivel de temperatura dentro de las retortas, y adems por largos perodos de tiempo. El material de las retortas es otro condicionante del proceso, as como el de los condensadores.
3.4.2. Proceso de retortas horizontales. El proceso belga en retortas horizontales produjo el 90% del zinc total hasta el desarrollo, en 1917, del proceso electroltico que supuso un verdadero impulso para la mindustria del zinc. En 1969 haba 26 plantas operando del proceso con retorta horizontal que producan un 15% del zinc mundial. En 1974 solo quedaban 12, de las que hoy no trabaja prcticamente ninguna. El horno tpico se representa en la figura 4.3 en la que se ven cuatro filas de retortas a cada lado del horno. Estos hornos quemaban carbn o gas y utilizaban regeneradores para precalentar el aire. Cada seccin del horno tena 96 retortas de arcilla, cuidadosamente elaborada y cocida. Las retortas, de seccin elptica, medan 1700 270 210 mm3 con una capacidad de 0,07 m3. Cada retorta produca unos 35 kg de zinc diarios. El ciclo de un horno era de 24 horas al final de las cuales se descargaban desmontando previamente los condensadores. Se introduca nueva carga que consista en blenda tostada y snter molido a menos de 6 mm. La mezcla de reaccin estaba formada por 100 partes de snter, 30 de antracita y 2-3 de sal, que beneficiaba la condensacin. La carga y descarga eran manuales y, por tanto, muy penosas. Esto hizo que en EEUU se intentase mecanizar estas instalaciones pero sin buenos resultados. El calentamiento del horno se haca progresivo hasta alcanzar al final de la operacin los 1370C. El metal condensado se retiraba, a intervalos regulares, en cantidades de 7 a 9 kg. El hierro y el plomo incrementaban en las sucesivas descargas concentrndose el cadmio en el primer metal retirado. Se exigan para este proceso las calidades siguientes: Prime (EEUU), con un 1,60% de plomo y un 0,08% de hierro; y G.O.B. (GB), con 1,35% de plomo y 0,04% de hierro. Slo el primer metal obtenido cumpla estas especificaciones por lo que el resto del metal se someta a afino. El metal se verta en un horno de reverbero en el que la tempera era solo ligeramente superior a la de fusin del zinc. En estas condiciones, se produca la sedimentacin del plomo y del hierro. El metal afinado tena 1,1-1,2% de Pb y 0,02-0,025% de Fe, satisfaciendo bien las especificaciones. Para operar en estos hornos se precisaba de un grado alto de pericia y era muy conveniente que las cargas fuesen homogneas conteniendo menos de 1% de azufre. Los americanos utilizaron esta tcnica en Texas por la abundancia de gas natural. Los hornos eran simples y el ciclo de 48 horas con lo que se consegua una vida ms larga de las retortas aunque la productividad era inferior y mayor el consumo de combustible. Las desventajas del proceso de retortas horizontales eran: 1. Exceso de trabajo manual: 20-24 horas-hombre por Mg de zinc (dos a tres veces el necesario en un aplanta moderna). 2. Operacin toxica y peligrosa. 3. Operacin discontinua. 4. Alto consumo energtico: Energa: 540 MJ; Antracita para la reduccin: 540 kg; Carbn para calentamiento: 1800 kg (Proceso Overpelt: 1400 kg); Produccin de vapor de baja: 2000 kg.
Figura 4.3. Horno belga de retortas horizontales para reduccin del zinc.
3.4.3. Proceso de retortas verticales. A finales de los aos 20, la compaa New Jersey Zinc, de Pennsylvania, en EEUU, hizo un esfuerzo notable para resolver los problemas inherentes al desarrollo de una retorta de operacin continua con alta eficacia trmica. El problema estaba en encontrar el material de la retorta que suministrarse el calor necesario para la reaccin 4.6 que requiere 5279 kJ por kg de Zn producido, cantidad muy superior a la necesaria para reducir plomo, estao o cobre. Los vapores de zinc necesitan para llegar a 1100C un calor que se evala en 1172 kJ por kg de Zn. Adems, hay que suministrar calor para calentar la carga y reducir otros xidos metlicos presentes como los de plomo y cadmio. Por tanto, la cantidad total de calor necesaria, por kg de zinc, era del orden de 7227 kJ. Estas retortas verticales (figura 4.4.a) se usaron para la coquizacin del carbn pero, en este caso, el ladrillo de slice era suficiente dadas las necesidades trmicas. Para la destilacin del zinc fue preciso contar con un nuevo material, el carburo de silicio (carborundo), que tiene una conductividad trmica (15,9 W(mkh)-1 a 1300C) nueve veces superior a la del ladrillo de slice. Las retortas se realizan con ladrillos de 115 mm de grueso, 1850 mm de largo y 305 de anchos (figura 4.4.b). Estos ladrillos estn diseados para acoplarse y construir una retorta de 12 m de altura que puede producir diez toneladas de zinc al da. Calentadas por encima de los 1300C, pueden durar tres aos en los que tratan 23000 Mg de carga.
Figura 4.4. a) Horno de retorta vertical New Jersey; y b) Seccin transversal de la retorta.
Sobre la zona calentada hay otra zona de 3-4 m, llamada eliminador, que tiene por fin facilitar la reaccin de reversin 4.1. As, consumido el CO2, de los gases y producido el polvo azul sobre la carga descendente, se evita que dicho polvo llegue al condensador, o que se forme en l, con lo que se permite una mejor coalescencia de las gotas de metal que, como se sabe, tienen tendencia a recubrirse de polvo dificultndose dicha coalescencia. El eliminador tambin ayuda a reducir el contenido de plomo de los vapores que dejan el horno. Las retortas se construyen en bateras de ocho. Se calientan con gas natural o gas de gasgeno. Se precisan 1,8 1010 J por tonelada de zinc, de los que el 30% los suministra el gas CO de tragante. El gas se quema en las cmaras de combustin, con aire caliente y en diferentes puntos, para conseguir una combustin uniforme; esto es muy importante para la vida de la retorta. La temperatura normal es de 1300C. Los gases de combustin pasan los recuperadores que calientan el aire a 550C. Algo que ha sido consustancial al desarrollo del proceso New Jersey ha sido la produccin de briquetas las cuales deben ser de un tamao adecuado para la mejor transmisin del calor. Tienen forma de panecillos, de 100 75 65 mm3 lo que les permite recibir la radiacin de la pared y una transmisin de calor adecuada. Para fabricar las briquetas se prepara una mezcla de blenda sinterizada con carbn bituminoso de alto poder aglutinante, antracita y pequeas proporciones de arcilla y leja de sulfito. Se mezcla bien, se amasa y se conforma en prensas de rodillo. Las briquetas deben cocerse posteriormente en un horno de descenso. La temperatura del horno se mantiene por combustin de la materia voltil del carbn no necesitndose aporte energtico exterior. Despus de cocidas las briquetas, se cargan calientes (800C) en la retorta. En la figura 4.5 se presenta el diagrama completo de una planta de retortas verticales. La condensacin del metal es problemtica. Se sabe que para evitar la reaccin inversa a la 8.1 es decir: Zn CO ZnO CO 2 + Ec. 4.18
Se precisa enfriar los vapores tan rpido como sea posible. Para hacer esto, se hace pasar el vapor que deja el eliminador a una caja en la que se mantiene un bao de zinc fundido regulado constantemente a 500C por medio de tubos refrigerantes. Este bao de zinc se agita mediante una turbina de carborundo producindose una suspensin de gotitas de zinc en la cmara, que enfra instantneamente los gases de la retorta con lo que el zinc condensa en forma metlica sobre las gotas evitando la posibilidad de reoxidacin. Aproximadamente, el 96% del zinc que entra en el condensador condensa como metal y menos del 4% como polvo azul. El gas que deja el condensador se lava en venturis y se alimenta a la cmara de combustin de las retortas aportando el 30% de energa necesaria. El metal colado tiene:0,1 - 0,2% de Pb: 0,03 - 0,06% de Cd; y 0.005 -0,015% de Fe. El futuro de las retortas verticales est casi agotado. A pesar del gran avance que supuso este proceso sobre el de retorta horizontal, las retortas verticales tienen sus propias desventajas. Aunque se consigue un proceso continuo y con ahorro energtico, los costos de primera instalacin son altos, as como los costes de mantenimiento. El proceso est muy determinado por la existencia de carbn bituminoso que es el que da estructura a las briquetas. Adems, los concentrados han de ser bajos en hierro, pues si no, se pueden formar placas de hierro en las retortas que interfieren la marcha de las briquetas. Las briquetas gastadas suponen un problema como residuo a almacenar. As y todo, hasta no hace mucho tiempo, funcionaban algunas plantas en New Jersey, en Estados Unidos, y en Inglaterra; tambin funcionaron en
Francia, Alemania y Japn pero hoy estas plantas estn paradas y no se van a construir nuevas instalaciones en el futuro empleando esta tecnologa. 3.4.4. Proceso Electrotrmico En 1926, a la vez que la New Jersey, la compaa Saint Joseph estaba tratando de desarrollar un proceso alternativo que utilizara un mtodo del calentamiento directo de la carga basndose en los estudios hechos a principios de siglo en Suecia para intentar reducir el zinc en hornos elctricos de arco. Estos primeros intentos fracasaron por el hecho de que no condensaban bien el vapor y no escorificaban bien las cargas. Saint Joseph desarroll un mtodo en el que el calor se generaba sobre la carga por efecto Joule y el proceso era continuo. Hubo que resolver un cierto nmero de problemas tal como se expone a continuacin. En principio, se carg igual cantidad de sinter que de coque y no se intent condensar el zinc vapor, sino que ste se obtena en una cmara que rodeaba al horno en la que el zinc se oxidaba recogindose como xido tipo pigmento. As, se puso de manifiesto la posibilidad de la reduccin y el problema se centraba entonces en desarrollar un mtodo de condensacin. Se intent condensar haciendo pasar los vapores metlicos a travs de una piscina de zinc fundido. Este fue un mtodo exitoso y fue la primera vez que se intent enfriar el vapor con metal lquido. Se conseguan, as, condensar cantidades importantes de zinc metal sin la prctica produccin de polvo azul. Se fij un condensador de este tipo a un horno productor de xido obtenindose un buen resultado: cinco toneladas diarias de zinc. Hoy da, con una sola unidad de condensacin, se pueden producir casi cien toneladas de metal. En la figura 4.6.a se puede ver un esquema de la instalacin Saint Joseph. El horno se construye con una serie de sectores de refractario soportados individualmente. Los vapores producidos en el horno se recogen en un anillo central del que se aspiran a travs del condensador a una temperaturaentre 800 y 850C. Este anillo y el condensador se construyen con ladrillos de carburo desilicio. La corriente elctrica atraviesa el horno por medio de ocho pares de electrodos que entran dentro del mismo: cuatro en la parte alta y cuatro en la baja. La carga de coque y blenda sinterizada se calienta por el CO gas hasta 750C; entonces, se alimenta en el horno a travs de un distribuidor rotatorio y se descarga por el fondo a una cierta velocidad por medio de una mesa giratoria asistida por brazos mecnicos refrigerados. La operacin se gobierna automticamente por un indicador de nivel del horno. La potencia del horno Saint Joseph es 10000 kW. La tensin entre electrodos es de 200-250 V. El consumo del horno es de 3050 kWh por Mg de zinc necesitndose, adems, 0,6 toneladas de coque.
Figura 4.6. a) Planta de produccin de zinc por procedimiento St. Joseph. b) Horno de zinc electrotrmico tipo St. Joseph.
El condensador est formado por dos tubos verticales conectados a una zona inclinada con respecto a la horizontal, con 2 m2 de rea interna. ste est conectado a un pozo enfriador del metal en el que el zinc se enfra mediante serpentines para que la temperatura del metal est entre 480 y 500C. Aproximadamente el 93% del zinc que entra en el condensador se condensa como tal. El gas, con el zinc residual, se lava para separar aquel que tiene una composicin aproximada de 79% de CO, 3% de CO2 y 18% de N2. Este gas pasa por una bomba de vaco que succiona con un efecto de 33,3-40 kPa (250-300 mm Hg). Este vaco es suficiente para hacer pasar el gas a travs del condensador. Se producen 1,42 moles de CO por mol de Zn vaporizado. El gas tiene un poder calorfico de 93 105 Jm-3 el cual se utiliza, en un 60%, para calentar la carga y el resto, en la produccin de vapor. Los residuos del horno precisan ser tratados para extraer de ellos el Zn (aumentando la recuperacin hasta el 95-96%). Un separador magntico elimina los materiales ferrosos. El 90% del coque se recupera en mesas neumticas y, finalmente, un proceso en medios densos recupera un concentrado de zinc; tanto este concentrado como el coque se reciclan. A pesar de los esfuerzos y desarrollos aplicados al proceso Saint Joseph su extensin ha sido limitada. Unidades similares se han desarrollado en la antigua Unin Sovitica, Japn y Alemania. Las unidades mayores producan 100 Mg por da, cantidad considerablemente inferior a la producida por el horno de cuba ISF. Por otro lado, el coste de inversin por unidad de zinc es bastante alto. Adems, se precisan concentrados de bajo contenido en hierro. Por estas razones, se explica que el proceso no se extendiera y que prcticamente las plantas St. Joseph no operen en la actualidad si se excepta la planta de Monaca, en Pennsylvania (EEUU), que trabaja en condiciones ptimas al haber mejorado la tostacin-sinterizacin y teniendo la posibilidad de usar polvos de acera.
3.4.5. Horno de Cuba de zinc. Proceso ISF. Ha habido muchos intentos de producir zinc a travs del horno de cuba; sin embargo, si ya presenta problemas condensar un gas de retorta con un 45% de Zn, un 50% de CO y un 1% CO2, es fcil imaginar el problema que supondra condensar el zinc de un gas que solo tiene un 6-7% de Zn y un 12% de CO2. El proceso desarrollado por la Imperial Smelting Corporation, en Inglaterra, ha sido, en va pirometalrgica, el ms destacado y, en la actualidad, el nico capaz de competir con la obtencin electroltica de zinc. Hubo un primer intento en 1939, con un horno que trataba snter y coque, con soplado superior e inferior, retirndose los vapores por el centro de la cuba. Efectivamente, mediante un enfriamiento rpido en tubos refrigerados se obtena zinc en polvo pero la inversin de la reaccin era suficiente para recubrir de xido este polvo y hacer impracticable la fusin del polvo de zinc ya que este no coalesca. Fue preciso, pues, desarrollar otro mtodo de condensacin. Se propuso condensar el zinc vapor sobre gotas de plomo fundido a una temperatura ligeramente superior a la del punto de fusin del zinc. Una lluvia de gotas de plomo lava los gases de zinc que condensan en forma lquida disolvindose en el plomo. Despus de enfriar este metal, se produca la segregacin del zinc que, as, se separaba al alcanzar la saturacin. El plomo era recirculado al condensador. A continuacin, se resumen las solubilidades, a distintas temperaturas, de plomo y zinc, el uno en el otro y viceversa:
Tabla 4.1. Solubilidad del zinc y plomo a distintas temperaturas.
Despus de la Segunda Guerra Mundial se profundiz en estos primeros estudios con resultados alentadores. Se hicieron estudios termodinmicos que indicaban que era posible reducir el contenido de Zn de las escorias a niveles bajos sin producir hierro metal, hecho este ltimo que hubiera acarreado consumos innecesarios de coque. Esto se confirm en la prctica y tambin que el xido de plomo se reduca en la parte alta del horno por el CO presente. Ya que esta reaccin es exotrmica, no se precisaba coque adicional y la capacidad del horno para producir zinc no se vea afectada. El plomo fundido desciende por la carga y acta como colector del cobre y de los metales preciosos. As, se llegaba a un resultado magnfico: el horno poda usarse para obtener, simultneamente, plomo y zinc a partir de menas mixtas. Esto se comprob pronto, pero se precis de un cierto tiempo para fijar los parmetros del proceso y para hacer que ste trabajase sin problemas. Uno de estos problemas, y adems serio, fue el hecho de que altas cantidades de zinc se depositaban en la parte alta del horno y en los conductos hasta el condensador. El gas sala de la parte alta del horno en condiciones en las que la reaccin de reduccin indirecta estaba en equilibrio por lo que, tan pronto como la temperatura bajaba, se produca la deposicin del xido de zinc. Esto llevaba a que el horno dejase de trabajar por atasco. Se desarroll una solucin simple sacada de la qumica-fsica del sistema. Un gas tpico de horno, en condiciones de equilibrio, puede reaccionar adiabticamente con carbn pero el contenido en CO2, disminuye, la temperatura baja y el gas es ms proclive a producir xido de zinc. Si, por otra parte, el gas reacciona con oxgeno, el aument de temperatura hace posible que el gas pueda reducir al xido de zinc, a pesar de incrementar su contenido en CO2, desapareciendo tambin el peligro reversin de las reacciones. As pues, se propuso adicionar aire en la parte alta del horno para quemar parcialmente el gas y evitar la deposicin de xido de zinc. El principio result eficaz, se simplific el diseo del horno y, aunque el aire de soplado superior produca algo de xido en la parte alta del horno, su aparicin quedaba reducida a la entrada del condensador de donde poda ser retirado. Se precis modificar la calidad del snter y el tipo de mquina para poder tratar menas con plomo. Esto se consigui por la idea Port Pire de sinterizacin con soplado inferior, probada ya con xito para sintetizar la galena. Todo el desarrollo se concret, en 1960, en una instalacin en Gales (Gran Bretaa) que produca, con 17,1 m2 de seccin, 30000 Mg de zinc y 15000 Mg de plomo al ao. Se mejor el diseo inicial, se introdujo aire caliente a 750C, se utiliz un
control automtico ms extendido y se pudo aumentar la produccin. Otro horno entr en produccin en Australia poco despus. En 1962 arranc un horno en Zambia y otro en la Sociedad Pearroya, en Francia. En 1965 se instal un nuevo horno en Duisburg (Alemania), en el 66 otro en Rumania y en Japn, en el 68 en Polonia, en el 69 en Japn nuevamente, en 1972 y 1973 en Italia y Yugoslavia, respectivamente, y en el 78 y 80 en China y en Polonia. En la figura 8.7 se representa un esquema general del horno de cuba ISF. Figura 4.7. Horno de cuba de zinc ISF
4. Compuestos de zinc. Existen varios compuestos de zinc de uso extendido entre los que se pueden citar el sulfuro, el sulfato, el cloruro y el xido. De ellos, el ms importante es el xido de zinc cuyo consumo supone entre el 5 y el 10% de la produccin de zinc de un pas desarrollado. El sulfuro de zinc, que es blanco, se usa en materiales de recubrimiento altos en contenido de pigmento. Tambin en cargas para imprimaciones y en masas plsticas. En pinturas precisa muy poca cantidad de ligante, dispersndose bien, por lo que a veces se mezcla con TiO2 pues, adems, tiene propiedades fungicidas y alguicidas. Se producen unas 200000 t de sulfuro de zinc (litophone). De los compuestos de zinc, el xido supone ms del 80% del consumo y por ello, a continuacin, se hace una mencin especial de sus usos y aplicaciones. Al xido de zinc se le denominaba blanco de zinc cuando su uso estaba restringido a las cargas de pinturas. Su conocimiento viene de antiguo al producirse de forma espontnea en los humos de reduccin del cobre. Se usaba al principio para fabricar latn ("oro blanco") a partir de los humos recogidos. La produccin del xido de zinc se desarroll a mediados del siglo XIX por combustin del vapor de metal. El xido producido reemplaz al xido de plomo por la toxicidad de ste. El procedimiento americano de reduccin del xido mineral y de su reoxidacin en el mismo horno, a la salida, tambin se desarroll a mediados del XIX. En la segunda mitad de ese siglo se desarroll el uso del xido para la goma, pues reduce el tiempo de vulcanizacin. El xido de zinc es un polvo blanco que se vuelve amarillo si se calienta a 300C. El
producto son cristales, ms o menos redondos, con tamaos de entre 0,5 y 5 m. Tiene una densidad de 5,66 g/cm3 y un ndice de refraccin de 2, fundiendo a 1975C. Del xido producido, el 2% se obtiene por va qumica, el 15% por va directa y el resto por va indirecta. La va directa consiste en calentar materiales, con zinc oxidado y residuos, mezclados con carbn, en un horno rotativo. Los gases y vapores producidos se reoxidan produciendo el xido que se recoge en un filtro de mangas. La va indirecta consiste en volatilizar el zinc de las chatarras y residuos, quemando los vapores y obteniendo, as, el xido de zinc. Este proceso se denomina proceso francs. Para conseguir la calidad adecuada, se regula la turbulencia y el exceso de aire de combustin. La pureza depende, fundamentalmente, de la pureza del vapor de zinc. Los hornos usados pueden ser de mufla, con dos cmaras y rotatorios. Tambin se pueden utilizar columnas de destilacin para separar las impurezas y quemar el vapor purificado a la salida. El proceso hmedo produce carbonato bsico, el cual se precipita a partir de disoluciones de cloruro o de sulfato purificadas. Por calcinacin de la sal se obtiene el xido que es de una elevada rea superficial. El producto final tiene unas especificaciones dependientes de la va de produccin segn se muestra en la tabla 6.1. El xido de zinc se usa en la industria de la goma en la que acta como catalizador de la vulcanizacin. Tabla 6.1. Oxido de zinc segn proceso de obtencin.
Para este uso se consume el 50% del xido producido. El xido tambin mejora la durabilidad de la goma y su conductividad trmica. El contenido en la goma vara entre el 2 y el 6%. Tambin se utiliza en pinturas, en recubrimientos, en cosmtica y farmacia, en la industria del vidrio, en la de cermica y en la de esmaltes. Se usa para producir diversos compuestos qumicos, como catalizador (metanol) y para fabricar varistores. El consumo mundial de xido supera las 500000 toneladas.
5. Polvo de zinc. El polvo de zinc se obtiene por dos vas. Una, es la volatilizacin a 900C y el enfriamiento posterior del metal, que se recoge en los filtros en forma de partculas esferoidales fluyentes. El otro, consiste en la dispersin fina (atomizacin) en minsculas gotitas de metal fundido (spray) que se solidifican al aire recubierto de una fina capa de xido de zinc transparente. La reduccin de menas oxidadas, cuando no se propicia una condensacin, produce vapor de zinc que al enfriar se convierte en polvo de zinc oxidado superficialmente. Si a la salida del vapor se favorece la oxidacin en una cmara apropiada, se puede obtener xido de zinc, blanco de zinc, tal como se produca en el horno elctrico St. Joseph. La regulacin de la oxidacin, es decir, la temperatura de contacto vaporaire y la velocidad de enfriamiento, produce o bien xido blanco o bien polvo azul. Las propiedades del polvo de zinc son: ms del 99% de zinc, del cual un 95% debe ser zinc metlico, un tamao de partcula en torno a 3 m y una cantidad de residuo insoluble en cido del 0,1%. 6. El zinc, el medio ambiente y la toxicidad. El zinc metal, y la mayora de sus compuestos, tienen muy baja toxicidad en comparacin con los otros metales pesados. La intoxicacin por zinc, aunque rara, se puede producir por alimentos que lo contienen a partir de los recipientes que los guardan o por inhalacin de vapores del metal o del xido. El zinc es necesario para la vida humana y animal, para el crecimiento, la piel, procesos metablicos, etc. Est ligado a las protenas y se elimina con relativa facilidad. Elcuerpo humano contiene 33 ppm. La ingestin txica se puede producir al tomar alimentos o bebidas acidas con alto contenido de metal, lo que puede producir trastornos gstricos. La ingestin de cloruro de zinc tambin puede ser peligrosa para el estmago, as como para los pulmones lo es la inhalacin de vapores de esta sal. Los vapores de zinc o de su xido se consideran responsables de la denominada fiebre del humo metlico, que aparece dentro de las 6 horas de exposicin y desaparece despus de dos das; es comn a otros metales, el cuerpo se acostumbra y suele reaparecer despus del descanso del trabajador por desintoxicacin y nueva inhalacin. No parece que existan degeneraciones cancerosas en trabajadores en contacto con el zinc por su exposicin a los vapores metlicos. El cloruro de zinc es letal por ingestin de 35 g siendo el sulfato mucho menos daino. La ingestin de agua de tuberas galvanizadas puede producir pequea toxicidad si la contaminacin del agua alcanza 40 ppm.
7. Conclusiones y discusiones. El proceso del zinc es un proceso en que el mineral se obtiene mediante concentracin de menas del mineral, con sus respectivos procesos como la flotacin, la tostacin, la sinterizacin, etc. Al principio se usa la calamina como materia prima principal para la obtencin del metal llegando al proceso en donde se realiza la tostacin de los minerales de zinc, el cual utiliza la blenda como materia fundamental, la que se oxida y se convierte paulatinamente en xido. La produccin del metal se obtiene mediante procesos como son la reduccin trmica, por retortas horizontales y verticales, el proceso electrotrmico y a la utilizacin del horno de cuba para el proceso ISF. Otro punto importante tratado en este informe fue la recuperacin de zinc a travs de chatarras y los aspectos ambientales tanto en la naturaleza como en la salud llegando a laconclusin de que el zinc es metal prcticamente inofensivo y no debe crear mayor problema el trabajar con l.
8. BIBLIOGRAFIA Antonio Ballester, Jos Sancho, Luis Felipe Verdeja: Metalurgia Extractiva Volumen II. Procesos de Obtencin.. Capitulo 6 ( DOCUMENTO PDF )
Anda mungkin juga menyukai
- Metalurgia Del ZincDokumen15 halamanMetalurgia Del Zincdaniel ramosBelum ada peringkat
- Obtencion Del ZincDokumen5 halamanObtencion Del ZincNahuel GaunaBelum ada peringkat
- Zinc ExposicionDokumen19 halamanZinc ExposicionCARLOS DANIEL SOLLER DE LA CRUZBelum ada peringkat
- Zinc, ObtenciónDokumen23 halamanZinc, ObtenciónCynthi7767% (3)
- Tasm 04 de 16Dokumen23 halamanTasm 04 de 16Jesus Maldonado PalmaBelum ada peringkat
- Metalurgia Del ZincDokumen14 halamanMetalurgia Del ZincFrankAlexanderCabreraCedrónBelum ada peringkat
- ZincDokumen23 halamanZincCarlos Rivas MinayaBelum ada peringkat
- Fundamentos de Metalugia Extractiva 1 - 2 - 3Dokumen35 halamanFundamentos de Metalugia Extractiva 1 - 2 - 3Ivan ReynaBelum ada peringkat
- Exposición CobreDokumen14 halamanExposición CobreMariaBelum ada peringkat
- Unidad 1 HidrometalurgiaDokumen13 halamanUnidad 1 HidrometalurgiaISAY ANDUAGA ALARCONBelum ada peringkat
- Trabajo Sobre El ZincDokumen17 halamanTrabajo Sobre El ZincJulio C. Samanés CardenasBelum ada peringkat
- Procesos de reducción y acería del hierroDokumen24 halamanProcesos de reducción y acería del hierroYQ JesusBelum ada peringkat
- Exposicion Mineria en Cuba (Cobre, Cobalto y Niquel)Dokumen5 halamanExposicion Mineria en Cuba (Cobre, Cobalto y Niquel)IvánDavidCamachoBelum ada peringkat
- Capitulo IDokumen84 halamanCapitulo ILisa RobinsonBelum ada peringkat
- Procesos de reducción y afinado del hierroDokumen24 halamanProcesos de reducción y afinado del hierroGerson Cahuana SullcaBelum ada peringkat
- El CobreDokumen13 halamanEl CobreAlejandro QuintanillaBelum ada peringkat
- HIDROMETALURGIADokumen9 halamanHIDROMETALURGIAJerson Ramos HuertaBelum ada peringkat
- Informe Obtencion Del CobreDokumen11 halamanInforme Obtencion Del CobreDeAviSBelum ada peringkat
- Proceso Electro Termico Del ZincDokumen26 halamanProceso Electro Termico Del ZincJoaquin BermudezBelum ada peringkat
- CIANURACIONDokumen13 halamanCIANURACIONRobertoChávezBelum ada peringkat
- Estudio de Las Propiedades Termodinamicas Del Proceso de Recuperación de CobreDokumen32 halamanEstudio de Las Propiedades Termodinamicas Del Proceso de Recuperación de CobreJorge Leonardo Martinez PumarejoBelum ada peringkat
- Guia N°1 Materiales y EnsayoDokumen4 halamanGuia N°1 Materiales y Ensayopelusssa2023Belum ada peringkat
- Refineria y PetroquimicaDokumen8 halamanRefineria y PetroquimicaBryan VillegasBelum ada peringkat
- HIDROMETALURGIADokumen18 halamanHIDROMETALURGIACarlos Aldair VelasquezBelum ada peringkat
- Clasificación de Las FundicionesDokumen13 halamanClasificación de Las FundicioneswinxtexBelum ada peringkat
- Proceso de Producion Del Cobre, Zinc, Alumiio, Plomo, Estaño y TitanioDokumen12 halamanProceso de Producion Del Cobre, Zinc, Alumiio, Plomo, Estaño y TitanioEverardo IdkBelum ada peringkat
- Cobre-Joe MiteDokumen10 halamanCobre-Joe MiteJoe Alan Mite TorresBelum ada peringkat
- Metalurgia Del CobreDokumen16 halamanMetalurgia Del CobreLuis Fernando Tumi TipoBelum ada peringkat
- Manual Del Fundidor - Fundicion - Metal Casting FoundryDokumen153 halamanManual Del Fundidor - Fundicion - Metal Casting Foundrypfranch100% (2)
- CCH Azcapotzalco Obtención Del CobreDokumen16 halamanCCH Azcapotzalco Obtención Del CobreMJHGBelum ada peringkat
- Clase 01 Siderurgia I Semana 1Dokumen31 halamanClase 01 Siderurgia I Semana 1Luis Joel Mejia HerreraBelum ada peringkat
- Reciclado de Polvos de Acerías (Óxidos de Zinc)Dokumen30 halamanReciclado de Polvos de Acerías (Óxidos de Zinc)Antonio Ros MorenoBelum ada peringkat
- Transacciones de Minerales y MetalesDokumen11 halamanTransacciones de Minerales y MetalesutsuisanBelum ada peringkat
- Introducción Del CobreDokumen6 halamanIntroducción Del Cobreelvis2552Belum ada peringkat
- 1obtencion de Metales Apartir de OxidosDokumen7 halaman1obtencion de Metales Apartir de OxidosMiguel PinedoBelum ada peringkat
- Minería en Cuba (Cobre, Cobalto y Niquel)Dokumen5 halamanMinería en Cuba (Cobre, Cobalto y Niquel)IvánDavidCamachoBelum ada peringkat
- Extracción del zinc en el PerúDokumen24 halamanExtracción del zinc en el PerúDanny Vargas HuamanBelum ada peringkat
- Cobre: historia, características y extracciónDokumen9 halamanCobre: historia, características y extracciónRusheadoresBelum ada peringkat
- Geometalurgia Extractiva Capitulo IiiDokumen20 halamanGeometalurgia Extractiva Capitulo IiiMilagros RocioBelum ada peringkat
- Lixiviación en capas delgadas: origen y ventajas del proceso TLDokumen18 halamanLixiviación en capas delgadas: origen y ventajas del proceso TLFlor Noelia Gonzales ArenasBelum ada peringkat
- Proceso Industrial Del AceroDokumen25 halamanProceso Industrial Del AceroAlejandraPinoFuentesBelum ada peringkat
- Trabajo LatonesDokumen15 halamanTrabajo LatonesJessica RamirezBelum ada peringkat
- Obtención de Planchas de Cobre A Partir Del MineralDokumen13 halamanObtención de Planchas de Cobre A Partir Del MineralJean Piero Mauricio HURTADO DIAZBelum ada peringkat
- Prev 4Dokumen8 halamanPrev 4jorgeBelum ada peringkat
- Lixiviación de MetalesDokumen10 halamanLixiviación de MetalesDaniela AbarcaBelum ada peringkat
- Presentacion CobreDokumen12 halamanPresentacion CobreEdwyn MrtinzBelum ada peringkat
- Proceso Industrial de La Obtencion Del ZincDokumen20 halamanProceso Industrial de La Obtencion Del ZincyvanBelum ada peringkat
- Tema 13 Materiales Metálicos - Metales No FerrososDokumen21 halamanTema 13 Materiales Metálicos - Metales No FerrososInes Orozco SevillaBelum ada peringkat
- Mineralurgia Del Cobre I PDFDokumen48 halamanMineralurgia Del Cobre I PDFPauccaraC.AlbertBelum ada peringkat
- Resumen de La Revolución Industrial de Thomas Ashton: RESÚMENES UNIVERSITARIOSDari EverandResumen de La Revolución Industrial de Thomas Ashton: RESÚMENES UNIVERSITARIOSBelum ada peringkat
- Artes & Oficios. El metal: Técnicas de conformado, forja y soldaduraDari EverandArtes & Oficios. El metal: Técnicas de conformado, forja y soldaduraPenilaian: 5 dari 5 bintang5/5 (1)
- Diseño, construcción y pruebas de horno prototipo semicontinuo para producir cerámicaDari EverandDiseño, construcción y pruebas de horno prototipo semicontinuo para producir cerámicaBelum ada peringkat
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADari EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSABelum ada peringkat
- El carbón: origen, atributos, extracción y usos actuales en ColombiaDari EverandEl carbón: origen, atributos, extracción y usos actuales en ColombiaPenilaian: 4.5 dari 5 bintang4.5/5 (2)
- Oficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoDari EverandOficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoPenilaian: 5 dari 5 bintang5/5 (1)
- Constitucion PDFDokumen32 halamanConstitucion PDFJuan Carlos Quezada NievesBelum ada peringkat
- Semana 36 Lunes 03 Setiembre Al Domino 09 Setiembre.Dokumen3 halamanSemana 36 Lunes 03 Setiembre Al Domino 09 Setiembre.Juan Carlos Quezada NievesBelum ada peringkat
- Trabajo PruebaDokumen1 halamanTrabajo PruebaJuan Carlos Quezada NievesBelum ada peringkat
- PiroclasticasDokumen81 halamanPiroclasticasSofi MatteodaBelum ada peringkat
- Semana 30 Lunes 24 Julio Al Domino 30 JulioDokumen3 halamanSemana 30 Lunes 24 Julio Al Domino 30 JulioJuan Carlos Quezada NievesBelum ada peringkat
- Disposicion de Residuos de Actividades Mineras, Desmonte y EscoriaDokumen48 halamanDisposicion de Residuos de Actividades Mineras, Desmonte y EscoriaJuan Carlos Quezada NievesBelum ada peringkat
- Tïa María 60 Días Son SuficientesDokumen1 halamanTïa María 60 Días Son SuficientesJuan Carlos Quezada NievesBelum ada peringkat
- Winnipeg Commodity ExchangeDokumen1 halamanWinnipeg Commodity ExchangeJuan Carlos Quezada NievesBelum ada peringkat
- Resumen de Tesis UchucchacuaDokumen16 halamanResumen de Tesis UchucchacuaJuan Carlos Quezada NievesBelum ada peringkat
- 33a Rsvolcanicas1Dokumen16 halaman33a Rsvolcanicas1Gerad ShullerBelum ada peringkat
- Examen SustitutorioDokumen17 halamanExamen SustitutorioJuan Carlos Quezada NievesBelum ada peringkat
- Flotación Del Plomo para BelgicaDokumen14 halamanFlotación Del Plomo para BelgicaJuan Carlos Quezada NievesBelum ada peringkat
- Modulo 3. Estrategias y Herramientas de RRCC.2013-IIDokumen32 halamanModulo 3. Estrategias y Herramientas de RRCC.2013-IIJuan Carlos Quezada NievesBelum ada peringkat
- 3era Practica Mineria Subterranea IIDokumen8 halaman3era Practica Mineria Subterranea IIJuan Carlos Quezada NievesBelum ada peringkat
- Cemento ExpansivoDokumen2 halamanCemento ExpansivoJuan Carlos Quezada NievesBelum ada peringkat
- Responsabilidad Alta DireccionDokumen1 halamanResponsabilidad Alta DireccionJuan Carlos Quezada NievesBelum ada peringkat
- Gestion de Riesgos Gestion - ServiciosDokumen26 halamanGestion de Riesgos Gestion - ServiciosJuan Carlos Quezada NievesBelum ada peringkat
- La GranjaDokumen3 halamanLa GranjaJuan Carlos Quezada NievesBelum ada peringkat
- Matriz DitribucionDokumen6 halamanMatriz DitribucionJuan Carlos Quezada NievesBelum ada peringkat
- Resinas EPOXIDokumen9 halamanResinas EPOXIDarth AfonsoBelum ada peringkat
- Caso 2Dokumen1 halamanCaso 2Juan Carlos Quezada NievesBelum ada peringkat
- Anitivirus Mayo - JunioDokumen1 halamanAnitivirus Mayo - JunioJuan Carlos Quezada NievesBelum ada peringkat
- Elementos de SostenimientoDokumen49 halamanElementos de SostenimientoJuan Carlos Quezada NievesBelum ada peringkat
- MI Ejercicio N 01Dokumen2 halamanMI Ejercicio N 01Juan Carlos Quezada NievesBelum ada peringkat
- Catalogo 3 PDFDokumen20 halamanCatalogo 3 PDFF Morales MedelesBelum ada peringkat
- Curso Autoclave Accesorios Calderas Que Usan Autoclaves Unidad IVDokumen104 halamanCurso Autoclave Accesorios Calderas Que Usan Autoclaves Unidad IVCARLOS ROJAS QUEZAD50% (2)
- Determinación de Cp,m y Cv,m del aire a partir de su coeficiente adiabático (γDokumen9 halamanDeterminación de Cp,m y Cv,m del aire a partir de su coeficiente adiabático (γAngela aponteBelum ada peringkat
- Compresor Hermético ReciprocanteDokumen3 halamanCompresor Hermético ReciprocanteNICOLE JANETH CASTILLO PILLASAGUABelum ada peringkat
- UNLA: Laboratorio de Química Orgánica - CristalizaciónDokumen14 halamanUNLA: Laboratorio de Química Orgánica - CristalizaciónBreyner SanchezBelum ada peringkat
- Ejercicios Clase 04 PDFDokumen9 halamanEjercicios Clase 04 PDFMayeli CuencaBelum ada peringkat
- Manual de Usuario DigivacDokumen6 halamanManual de Usuario DigivacKiki OlanoBelum ada peringkat
- Interruptores de presión, nivel, temperatura, flujo y límiteDokumen5 halamanInterruptores de presión, nivel, temperatura, flujo y límiteChemita MendezBelum ada peringkat
- Fundamentos y TransmisoresDokumen8 halamanFundamentos y TransmisoresFernando MendezBelum ada peringkat
- Nrf-164-Pemex-2011 PiDokumen24 halamanNrf-164-Pemex-2011 PiyatzylBelum ada peringkat
- Heuristica de ValvulasDokumen7 halamanHeuristica de ValvulasCamila GutierrezBelum ada peringkat
- 7.16 en La Figura 7.21 Mostramos Una Bomba Que Envía 840 L/min de Petróleo Crudo (SG 0.85)Dokumen4 halaman7.16 en La Figura 7.21 Mostramos Una Bomba Que Envía 840 L/min de Petróleo Crudo (SG 0.85)PEREDA ZELADA DANIEL ARTURO100% (1)
- A3 Petrolera Banco de PreguntasDokumen30 halamanA3 Petrolera Banco de PreguntasMauricio Arana CastroBelum ada peringkat
- Bomba DosificadoraDokumen71 halamanBomba DosificadoraEduardo EspinosaBelum ada peringkat
- Logging While Drilling HalliburtonDokumen4 halamanLogging While Drilling HalliburtonpaolaBelum ada peringkat
- Gases Ideales Parte Texto EstudianteDokumen40 halamanGases Ideales Parte Texto EstudianteFamiliaDelNidoSepúlveda0% (1)
- TAREADokumen13 halamanTAREAKmpos PercyBelum ada peringkat
- Guía No#4) HidrodinamicaDokumen6 halamanGuía No#4) HidrodinamicaAmbar Leticia Suriel pinaBelum ada peringkat
- Curso Laboratorio de Cementacion RevisadoDokumen20 halamanCurso Laboratorio de Cementacion RevisadoMarcosBelum ada peringkat
- Presión de Alivio de Señal de ImplementosDokumen14 halamanPresión de Alivio de Señal de ImplementosHector ZárateBelum ada peringkat
- Frenos AbsDokumen22 halamanFrenos AbsJasso KarolBelum ada peringkat
- Golpe de ArieteDokumen24 halamanGolpe de Arietecarlos-roBelum ada peringkat
- Tipos de Piezómetros Medidores de Presión y FlujoDokumen9 halamanTipos de Piezómetros Medidores de Presión y FlujoVVladimir IEBelum ada peringkat
- d-301 GAS NATURAL COMPRIMIDO (GNC) - GLOSARIO DE TÉRMINOS Y DEFINICIONESDokumen16 halamand-301 GAS NATURAL COMPRIMIDO (GNC) - GLOSARIO DE TÉRMINOS Y DEFINICIONESJhonny Rafael Blanco CauraBelum ada peringkat
- Planificación Microcurricular CCNN 10Dokumen29 halamanPlanificación Microcurricular CCNN 10sbodomir100% (1)
- 1 Informe - Propiedades de Los FluidosDokumen19 halaman1 Informe - Propiedades de Los FluidosCrisG4mer FBBelum ada peringkat
- TD 03 Termodinamica Clement-Desormes 2012Dokumen6 halamanTD 03 Termodinamica Clement-Desormes 2012Paola Andrea Fernandez CopaBelum ada peringkat
- Geologia Estructural PDFDokumen36 halamanGeologia Estructural PDFClaudio Javier CerveloBelum ada peringkat
- Manual Del Usuario BoosterDokumen23 halamanManual Del Usuario BoosterangelitaBelum ada peringkat
- Informe FinalDokumen4 halamanInforme FinalPamela RodríguezBelum ada peringkat