Guía Micro Aplicada 2012-I
Diunggah oleh
Edgar Condori MendozaHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Guía Micro Aplicada 2012-I
Diunggah oleh
Edgar Condori MendozaHak Cipta:
Format Tersedia
UNIVERSIDAD INCA GARCILASO DE LA VEGA
FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
MANUAL MANUAL DE PRCTICAS DE MICROBIOLOGA APLICADA
Dr. Q.F. HCTOR ALEXANDER VILCHEZ CCEDA
Mg. EN GERENCIA DE SERVICIOS DE SALUD
LIMA PER 2010
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PROLOGO
La Universidad Inca Garcilaso de la Vega, est empeada en realizar importantes innovaciones en la concepcin y prctica educativa con el propsito de brindar a sus alumnos una formacin profesional ms competitiva, que haga posible su ingreso con xito al mundo laboral, desempendose con eficacia y eficiencia en las funciones que les tocar asumir. El marco referencial est dado por los cambios significativos de la sociedad contempornea, expresados en la globalizacin y los nuevos paradigmas del conocimiento, de la educacin y la pedagoga as como los retos del mundo laboral. Uno de los medios para el logro de nuestros propsitos lo constituye el MANUAL DE PRACTICAS DE MICROBIOLOGA el cual ha sido concebido como un material educativo que va ha servir para afianzar conocimientos, desarrollar habilidades y destrezas, as como orientar la autoeducacin permanente. por ello se ubica como un material de lectura independiente, sirve de informacin y recreacin, desempea un papel motivador, se orienta a facilitar la lectura comprensiva, a ampliar conocimientos en otras fuentes, crear hbitos y actitudes, as como a desarrollar destrezas para el procesamiento de informacin, adquisicin y generacin de conocimientos. El presente Manual, constituye material de apoyo al desarrollo de la asignatura y est organizado en dos unidades: Unidad I: Microbiologa Generalidades, Unidad II: Microbiologa Aplicada comprende: Microbiologa Clnica, Microbiologa Alimentaria, Microbiologa en la Industria Farmacutica y Cosmtica y de un Trabajo de Campo. Los alumnos deben leer detenidamente cada prctica, antes de su realizacin, para una mejor comprensin en la observacin del fenmeno biolgico de cada microorganismo en estudio. Adems debe realizar diagramas de flujo de lo observado el cual ser revisado por el profesor responsable de cada grupo de prctica. El autor agradece anticipadamente la(s) crtica(s) o sugerencia(s) que puedan tener los lectores que sirvan para mejorar el presente trabajo.
Dr. Q.F. HCTOR ALEXANDER VILCHEZ CCEDA DOCENTE DE MICROBIOLOGA
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INDICE
PRLOGO INDICE INTRODUCCIN RESULTADO DE ANLISIS MICROBIOLGICO 01 02 04 06
UNIDAD II: MICROBIOLOGA APLICADA 2.1 MICROBIOLOGA CLNICA PRACTICA N 07 Aislamiento e Identificacin de Staphylococcus y Streptococcus. PRACTICA N 08 Bacilos Gram Negativos de Importancia Medica PRACTICA N 09 Hemocultivo y Coprocultivo PRACTICA N 10 Urocultivo, Recuento de Colonias, Antibiograma. 2.2 MICROBIOLOGA ALIMENTRIA PRACTICA N 11 Anlisis Microbiolgico de Productos Lcteos - Preparacin y Dilucin de las Muestras de Alimentos - Numeracin de Microorganismos Aerobios Mesfilos Viables. - Identificacin de Patgenos. PRACTICA N 12 Anlisis Microbiolgico de una Muestra de Agua
07 08
08
24
36
44 53
54
61
- Preparacin y Dilucin de la Muestra - Numeracin de Coliformes - Determinacin del Numero Ms Probable (NMP). - Identificacin de Patgenos.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
2.3 MICROBIOLOGA EN LA INDUSTRIA FARMACUTICA Y COSMTICA 65 PRACTICA N 13 Monitoreo de Ambientes Superficies y Personal. PRACTICA N 14 Control Microbiolgico de Crema de Baba de Caracol PRACTICA N 15 Control Microbiolgico de Envases. PRACTICA N 16 Control Microbiolgico de Lpices Labiales 74 73 70 66
REFERENCIA BIBLIOGRFICA
77
ANEXO III: ESQUEMA DE RESULTADOS DE MICROBIOLOGA APLICADA 79
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTRODUCCIN
La Microbiologa es la ciencia encargada del estudio de los organismos microscpicos, deriva de 3 palabras griegas: mikros (pequeo), bios (vida) y logos (ciencia) que conjuntamente significan el estudio de la vida microscpica. Son considerados Microbios todos los seres vivos microscpicos consistentes en una sola clula, es decir unicelulares, as como aquellos que forman agregados celulares en los cuales todas las clulas son equivalentes. Los microorganismos pueden ser Eucariotas (Las clulas poseen ncleo), tales como los hongos y los protistas, o Procariotas (clulas carentes de ncleo), como las Bacterias y los Virus (Aunque los virus no son considerados seres vivos estrictamente hablando).
El Qumico Farmacutico y Bioqumico, es el profesional universitario de las Ciencias Mdicas con formacin cientfica, tecnolgica y humanstica, con capacidad gerencial, ejecutiva y de liderazgo. As mismo altamente capacitado para poder ejercer profesionalmente en los campos de la Industria Farmacutica e Industria Cosmtica siendo Jefe de Control de Calidad, del Laboratorio de Anlisis Clnicos y Bioqumicos ejerciendo la Microbiologa Clnica y del Laboratorio de Bromatologa realizando los Controles Microbiolgicos a los Alimentos.
Hoy en da el Profesional Qumico Farmacutico y Bioqumico es el profesional responsable de la produccin de los medicamentos y de los cosmticos de calidad, seguros y eficaces y para lograr este objetivo el control microbiolgico se considera de gran importancia, ya que en estos productos se pueden presentar las condiciones necesarias para la multiplicacin de microorganismos capaces de deteriorar al producto o, lo que es peor, afectar la salud del consumidor.
El cuidado de los alimentos y la industrializacin de los mismos se ha convertido en una ciencia y cada vez ms se estudia e investiga la forma de mejorar la calidad. Da a da surgen nuevas tcnicas, nuevos tipos de envases, nuevos aditivos, nuevos conservadores, etc. Esto ha llevado al establecimiento de normas, al desarrollo de mtodos y sistemas de control, que aseguren la inocuidad de los mismos. Para lograr este objetivo el Qumico Farmacutico y Bioqumico, realiza los Controles Microbiolgicos donde cuantifica e identifica los microorganismos presentes en los alimentos.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Las infecciones intrahospitalarias cada vez ms constituyen un serio problema de salud pblica, ya sea por su efecto sobre la salud de los pacientes, como por los costos que este problema implica. Esto hace, que en el pas se estn aunando esfuerzos para implementar sistemas de vigilancia, prevencin y control, orientados a enfrentar este problema. Por lo que el Medico debe basar su diagnstico en evidencias disponibles, como son los aspectos epidemiolgicos, y la importante contribucin del Laboratorio de Microbiologa, que adems de permitir el diagnstico etiolgico, orienta el manejo clnico teraputico del paciente.
El estudiante de Microbiologa de la Facultad de Ciencias Farmacuticas y Bioqumica de la Universidad Inca Garcilaso de la Vega, en el futuro ser el profesional Qumico Farmacutico y Bioqumico, quien con los conocimientos presentes en este manual estar en la capacidad de poder afrontar y resolver con criterio los problemas presentados ya sea en la Jefatura de Control de Calidad de una Industria Farmacutica Cosmtica, como en un Laboratorio Clnico Microbiolgico un Laboratorio Bromatolgico.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RESULTADO DE ANLISIS MICROBIOLGICO
Nombre: _______________________ Lote: __________________________ Fecha de Ingreso: ____________________
Cdigo: ___________________ Fecha de Anlisis: ___________ N de An lisis: ______________
Resultados: Microorganismos Aerbios 10-1 24 Horas 48 Horas 72 Horas 10-2 10-3 10-4 10-5
Microorganismos Patgenos 10-1 24 Horas 48 Horas 72 Horas Resultado: 10-2 10-3 10-4 10-5
Hongos y Levaduras 10-1 3er Da 5to Da Resultado: 10-2 10-3 10-4 10-5
Observaciones:
Fecha
___________________ Analista
________________________ Jefe de control de Calidad
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
UNIDAD II: MICROBIOLOGA APLICADA
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
2.1
MICROBIOLOGA CLNICA PRACTICA N 07 AISLAMIENTO E IDENTIFICACIN DE STAPHYLOCOCCUS Y STREPTOCOCCUS STAPHYLOCOCCUS
Los estafilococos constituyen un grupo de microorganismos esfricos, Gram positivos, agrupados en forma de racimos, tetradas o aisladas, inmviles no esporulados. El gnero Staphylococcus pertenece a la familia Micrococcaceae. La especie patgena del gnero es Staphylococcus aureus. Este microorganismo puede formar parte de la flora nasal del hombre y tambin es causante de diversos procesos infecciosos tales como imptigo, forunculosis, abscesos, intoxicaciones alimentarias e infecciosas particularmente graves como bacteriemias. La especie patgena produce una enzima llamada coagulasa, que puede estar libre (freecoagulase) o ligada (clumping factor). Algunas especies de Staphylococcus coagulasa negativas, tales como Staphylococcus epidermidis y Staphylococcus saprophyticus considerados hasta hace relativamente poco tiempo como no patgenos, vienen teniendo un papel relevante en cuadros infecciosos bacterimicos y urinarios. MATERIALES Placas petri con agar sangre de carnero. Placas petri con agar Dnasa. Placas petri con agar manitol salado. Placas petri con agar tripticasa soya agar. Tubos con caldo plasma. Asas de platino. Juego de colorantes para Gram. Lminas portaobjetos simples. Caldo nutritivo en tubo. H2O2 al 3%. Lpiz graso Aceite de inmersin.
PROCEDIMIENTO Hacer un frotis en las lminas portaobjetos limpios y desengrasados a partir de la muestra problema, realizar la coloracin de Gram. Observar con el microscopio utilizando objetivos de inmersin, destacando la forma de agrupacin y la coloracin que toma la bacteria. Realizar la siembra en estra de la muestra problema en los siguientes medios de cultivo: Agar sangre de carnero, agar manitol salado y agar TSA. Llevar a la Incubadora a 37C durante 24 48 horas. Realizar una siembra en forma circular o elptica en la placa que contiene agar Dnasa. Llevar a la Incubadora a 37C durante 24 48 horas.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRUEBA DE LA CATALASA Determina la presencia de la enzima catalasa, esta enzima descompone el perxido de hidrgeno en agua y oxgeno. PROCEDIMIENTO Con el asa de siembra recoger el centro de una colonia pura de 18 a 24 horas y colocar sobre un portaobjetos limpio. Agregar una gota de H2O2 al 3% usando un gotero o una pipeta pasteur. No es necesario mezclar el cultivo con el H2O2. Observar una inmediata efervescencia (formacin de burbujas) lo que indica una prueba positiva, de lo contrario se considera la prueba negativa. Desechar el portaobjetos colocndolo en un desinfectante.
NOTA: Al coger la colonia con el asa de siembra tener cuidado de no llevar algo del medio de agar sangre debido a que la catalasa presente en los eritrocitos, puede dar resultados falsos positivos. No invertir el orden del mtodo porque pueden producirse resultados de falsos positivos. PRUEBA DE LA COAGULASA Se realiza para comprobar la facultad de la bacteria de coagular el plasma por accin de la enzima coagulasa, la cual aumenta la velocidad de coagulacin del plasma. El resultado final es la formacin de un cogulo de fibrina. - Prueba en lmina (detecta factor de aglutinacin o coagulasa ligada). - Prueba en tubo (detecta coagulasa libre y ligada). La prueba de coagulasa en tubo es definitiva, y la prueba de coagulasa en lmina puede ser usada como una tcnica de tamizaje rpida para la identificacin de S. aureus. Todas las pruebas negativas en lmina deben repetirse utilizando la tcnica en tubo. NOTA: El plasma humano no debe ser usado a menos que haya sido cuidadosamente probado de no contener algn agente infeccioso, capacidad de coagulacin e inhibidores. PRUEBA EN LMINA La prueba de la coagulasa en lmina es un mtodo nicamente presuntivo. Por esa razn todos los resultados negativos o retardados (ms de 20 segundos) deben ser confirmados por la prueba en tubo. PROCEDIMIENTO Preparar una suspensin densa de la colonia en agua destilada o solucin fisiolgica mezclando bien para homogenizar.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Si hubiera autoaglutinacin no continuar y realizar la prueba en tubo. Agregar una gota de plasma y mezclar con movimientos circulares. Observar la formacin de aglutinacin o precipitado dentro de 20 segundos. Todas las pruebas negativas y positivas retardadas (20 a 60 segundos) debe confirmar-se con la prueba en tubo.
NOTA Es una prueba bastante rpida y econmica pero del 10 a 15 % de S. aureus pueden dar un resultado negativo, por eso, todos los resultados negativos deben repetirse utilizando la tcnica en tubo.
PRUEBA EN TUBO
PROCEDIMIENTO Transferir una colonia aislada del agar sangre de carnero a 0,5 mL de plasma reconstituido (en un tubo de vidrio estril de 13 x 100). Girar el tubo suavemente para lograr la suspensin del organismo. No agitar. Incubar la mezcla a 35 37 C (en bao mara de p referencia) por 4 horas; observar si hay formacin de coagulo inclinando lentamente el tubo. Observar cuidadosamente si hay formacin de coagulo inclinando lentamente el tubo (sin agitar) en intervalos hasta 4 horas. Cualquier grado de coagulacin es una prueba positiva. La mayora de los S. aureus formarn coagulo dentro de una hora. Si es negativa a las 4 horas seguir incubando hasta el da siguiente a temperatura ambiente. Esto es recomendado porque un pequeo nmero de cepas de S. aureus pueden requerir ms de cuatro horas para la formacin del cogulo. Considerar que Staphylococcus produce fibrinolisina, la cual puede lisar el coagulo. Si son estafilococos coagulasa negativos, realizar las pruebas de resistencia a la polimixina B y novobiocina (disco de 5ug) para tener una identificacin presuntiva. S. saprophyticus es resistente a la novobiocina y S. epidermidis es resistente a la polimixina B.
10
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
STAPHYLOCOCCUS Aislamiento e identificacin: Staphylococcus aureus COLONIAS:
MEDIOS A. S. A. M. S. T. S. A. DNASA
TAMAO FORMA PIGMENTO HEMLISIS MANITOL DNASA CATALASA COAGULASA GRAM Aislamiento e identificacin: Staphylococcus epidermidis COLONIAS:
MEDIOS A. S. A. M. S. T. S. A. DNASA
TAMAO FORMA PIGMENTO HEMLISIS MANITOL DNASA CATALASA COAGULASA GRAM Aislamiento e identificacin: Staphylococcus saprophyticus COLONIAS:
MEDIOS A. S. A. M. S. T. S. A. DNASA
TAMAO FORMA PIGMENTO HEMLISIS MANITOL DNASA CATALASA COAGULASA GRAM
11
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTERPRETACIN COLORACIN GRAM
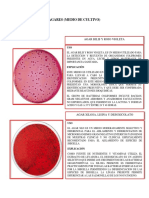
Gram positivos en racimos Estructura pared celular Gram positivo AGAR SANGRE DE CARNERO
Staphylococcus aureus
Staphylococcus epidermidis
Staphylococcus saprophyticus
12
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
AGAR MANITOL SALADO
Staphylococcus aureus
Staphylococcus epidermidis
Staphylococcus saprophyticus (+) AGAR DNASA
Staphylococcus aureus
Staphylococcus epidermidis
Staphylococcus saprophyticus
13
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRUEBA DE LA COAGULASA
Staphylococcus aureus
Staphylococcus epidermidis
Staphylococcus saprophyticus
PRUEBA DE LA CATALASA
Staphylococcus aureus: catalasa positivo Staphylococcus epidermidis: catalasa positivo Staphylococcus saprophyticus: catalasa positivo Streptococcus: catalasa negativo Micrococcus: aerobio estricto, presenta colonias amarillas anaranjadas, catalasa positivo, oxidan, no fermenta. Los micrococos son muy abundantes en la naturaleza, vindose aislado ms frecuentemente del polvo y agua. A menudo se encuentra en utensilios y equipos usados en alimentacin que no han sido adecuadamente limpiados e higienizados.
14
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRINCIPALES CARACTERSTICAS FENOTPICAS DE LAS ESPECIES DE STAPHYLOCOCCUS COMNMENTE AISLADOS EN INFECCIONES
PIGMENTO DE COLONIA HEMOLISINA (*) ESTAFILO COAGULASA FACTOR DE AGLUTINACIN
S. aureus Subespecies aureus S. epidermidis S. haemolyticus S. lugdunensis S. saprophyticus Subespecies saprophyticus S. schleiferi, Schleiferi S. warmeri
+ d d d d
+ (d) (+) (+) (+) (d)
+ -
+ (+) + -
RESISTENCIA A NOVOBIOCINA
RESISTENCIA A POLIMIXINA B
ORNITINA DESCARBOXILASA
ACIDEZ DE MANITOL
S. aureus Subespecies aureus S. epidermidis S. haemolyticus S. lugdunensis S. saprophyticus Subespecies saprophyticus S. schleiferi, Schleiferi S. warmeri
+ -
+ + d -
(d) + -
+ d d d
+ d (+) (*) + (+) (d) -
90% o ms especies o cepas positivas. 90% o ms especies o cepas negativas. 11% - 89% de especies o cepas positivas Reaccin retardada En agar sangre de carnero Zona amplia de hemlisis dentro de 24 36 horas Hemlisis retardada, de una zona moderada a amplia dentro de las 48 72 Horas No hay hemlisis o es retardada No hay hemlisis o hay una zona muy angosta ( 1mm) dentro de las 72 horas. Algunas de las cepas pueden producir in ligero color verdusco o marrn en agar sangre de carnero.
CUESTIONARIO 1. Qu factores son los qu condicionan la patogenicidad del Staphylococcus aureus, en comparacin con otras especies de estafilococos? 2. Qu enfermedades produce el Staphylococcus epidermidis y Staphylococcus saprophyticus?
15
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
STREPTOCOCCUS Y ENTEROCOCCUS INTRODUCCIN Constituye un grupo de microorganismos esfricos o lanceolados, gram positivos, inmviles no esporulados, en cadena cortas o largas. En el gnero Streptococcus estn comprendidas especies patgenas para el hombre tales como Streptococcus pyogenes y Streptococcus pneumoniae, existen portadores asintomticos de ambas especies. Streptococcus pyogenes es causante de faringitis, amigdalitis, otitis, escarlatina, erisipela e imptigo, la fiebre reumtica y la glomrulo nefritis pueden ser secuelas de la infeccin. En placas de agar sangre produce hemlisis tipo beta y puede ser identificada mediante su sensibilidad a la bacitracina. La especie Streptococcus pneumoniae se presenta en forma de diplococo, posee una cpsula ntida asociada con la virulencia del germen, en medio enriquecido como el agar sangre, las cepas encapsuladas de neumococos forman colonias mucoides y son virulentas para los ratones se identifican por su solubilidad en sales biliares, por metabolizar la inulina y por su sensibilidad a la optoquina. Produce hemlisis tipo alfa, carcter que comparte con los Streptococcus alfa hemolticos o Streptococcus viridans. Son los agentes causales ms frecuentes de neumona lobar, sinusitis y meningitis. Las especies del gnero Enterococcus son bacterias que se encuentran en el intestino y algunas veces pueden producir infecciones fuera del intestino. Se identifican por su crecimientros en medios de concentracin alta de cloruro de sodio. MATERIALES Placas petri con agar sangre de carnero. Asas de platino. Juego de colorantes para Gram. Lminas portaobjetos simples. Caldo nutritivo en tubo. H2O2 al 3%. Lpiz graso Aceite de inmersin. Bajalengua. Hisopos de algodn estril.
PROCEDIMIENTO 1. Tome un hisopo estril y un bajalengua. 2. Pida al compaero que se eligi para la prctica que mire hacia arriba, abra la boca y saque la lengua. 3. Con el bajalengua deprima la lengua para tener una mejor visin de la faringe 4. Con el hisopo, toque a manera de raspado la parte posterior de la faringe, las amgdalas y el pilar posterior del velo del paladar. 5. Retire el bajalengua y el hisopo con el exudado de la faringe.
16
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
6. Con el mechero de Bunsen encendido y respetando el margen de esterilidad inocule con el hisopo el material del exudado farngeo en una placa con agar sangre y siembre con una asa con la tcnica de estra mltiple. 7. Queme por la parte de en medio su hisopo para que no sea nuevamente utilizado 8. Incube a 37C durante 24 horas. 9. Transcurrido las 24 horas, saque las cajas de la incubadora y encienda el mechero 10. Haga un frotis de las colonias que crecieron en el agar sangre 11. Tia con la tcnica de Gram 12. Observe con aceite de inmersin el frotis 13. De acuerdo a lo observado en cada uno de los frotis realice las pruebas correspondientes.
Para cocos Grampositivos en cadena de acuerdo a la hemlisis Tomar la cepa sospechosa de estreptococos e inocular la en una placa de agar sangre en un cuadro de aproximadamente 1.5 cm por 1.5 cm por estriacin masiva. En medio del cuadro estriado con la cepa colocar el disco con la Bacitracina Incubarlos a 37C durante 24 horas. En las placas de agar sangre observar las colonias pequeas y rodeadas de hemlisis, sin destapar la placa observar al microscopio con objetivo de 5X la zona de hemlisis tipo beta (destruccin total de los hemates) y la hemlisis tipo alfa.
STREPTOCOCCUS PNEUMONIAE (NEUMOCOCO) Y ENTEROCOCCUS MATERIALES Cultivo de neumococos en caldo nutritivo Cultivo de neumococo en agar sangre y discos de Optochin Cultivo de enterococcus sp. En agar sangre Cultivo de enterococcus sp. En caldo con NaCL 6.5% Lminas portaobjetos simples. Solucin de sales biliares al 10% Caldo esculina.
PROCEDIMIENTO Hacer frotices a partir de las colonias en agar sangre, colorearlos con gram. Observar con lentes de inmersin la morfologa del diplococo lanceolado gram positivo, tpico del neumococo. Observar la discreta y uniforme turbidez en el medio lquido. En la placa de agar sangre observar la colonia pequea aplanada y rodeada de un color verdoso por la hemlisis alfa.
17
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
En las placas de agar sangre con discos de optoquina, observar halo de ausencia de desarrollo con el neumococo. En el medio con inulina constatar la formacin de acidez por metabolismo de este carbohidrato. Observar el aclaramiento in del cultivo lquido al aadirse sales biliares al 10%.
STREPTOCOCCUS Aislamiento del estreptococo beta hemoltico del grupo A.
MEDIOS DE CULTIVO Tamao Forma Hemlisis gram Tipificacin:
AGAR SANGRE
MEDIOS DE CULTIVO Bacitracina Hemlisis STREPTOCOCCUS PNEUMONIAE Aislamiento MEDIOS DE CULTIVO Tamao Forma Hemlisis gram Tipificacin:
AGAR SANGRE
AGAR SANGRE
MEDIOS DE CULTIVO Optoquina Sales biliares Inulina Gram (tinta china)
AGAR SANGRE
* Para Enterococcus, interpretar el desarrollo en el caldo con NaCL 6.5%
18
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRUEBA DE LA ESCULINA EN MEDIO CON BILIS
Para determinar la facultad de un organismo de hidrolizar el glucsido esculina en esculetina y glucosa, en presencia de bilis.
PROCEDIMIENTO Inocular el cultivo en estudio haciendo estras sobre la superficie del pico de flauta o de la placa de agar bilis esculina. Incubar a 35 37 C hasta 72 horas. Se puede controlar peridicamente, y esperar hasta las 72 horas antes de informar como negativo.
LECTURA Positivo: En tubo: Ennegrecimiento difuso en el agar inclinado. En placa: Se observa un halo negro o marrn alrededor de las colonias en la placa. Negativo: No se produce ennegrecimiento del medio o ennegrecimiento de menos de la mitad del tubo despus de 72 horas de incubacin. TOLERANCIA AL CLORURO DE SODIO Para determinar la facultad de un organismo de desarrollar en presencia de una concentracin de 6.5 % de cloruro de sodio. PROCEDIMIENTO Inocular en el caldo TSB con cloruro de sodio un cultivo de 18 - 24 horas de incubacin. Incubar a 35 37 C por 24 horas. Se puede controlar peridicamente, y esperar hasta las 72 horas antes de informar como negativo.
LECTURA Positivo: Hay desarrollo bacteriano Negativo: No se observa crecimiento en el caldo Observar el oscurecimiento del agar indicando si hubo hidrlisis de la esculina y el crecimiento en el caldo con cloruro de sodio. Con estas pruebas tenemos dos identificaciones presuntivas posibles: as todos los enterococos (95%) son esculina positivos y crecen en medios con 6.5% de cloruro de sodio produciendo acidez. 5% 10% de Streptococcus del grupo viridans son bilis esculina positivos.
19
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTERPRETACIN
COLORACIN GRAM
Cocos gram positivos en cadena AGAR SANGRE
Beta hemlisis
Alfa hemlisis
Estreptococo pneumoniae hemlisis parcial
Gama hemlisis no hay cambios
20
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Hisopado de las amgdalas En la placa se observa beta hemlisis posible streptococcus pyogenes mezclada con la alfa normal y gama hemlisis colonias de los estreptococcus viridans que viven normalmente en la garganta.
Estreptococo pneumoniae
Estreptococo pyogenes Sensibilidad a la bacitracina
Estreptococo pneumoniae Sensibilidad a la optoquina
21
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Enterococo faecalis
Caldo S F
Los enterococos en presencia de azida de sodio crecen, fermentan la dextrosa formando acido el cual vira el indicador de pH de un violeta a un color amarillo marrn.
Agar Bilis Esculina
Los enterococos crecen en presencia de sales de bilis. Mientras crecen, hidrolizan la esculina del medio de cultivo aprecindose un color negro en el agar.
Caldo con NaCL 6.5%
Hidrlisis de la esculina En medio bilis esculina
22
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRINCIPALES CARACTERSTICAS FENOTPICAS DE COCOS GRAM POSITIVOS, EN CADENA CATALASA NEGATIVOS
BILIS ESCULINA NACL 6.5% CRECIMIENTO 10 C 45 C HEMLISIS
Enterococcus Streptococcus Lactococcus Vagococcus
+ -a + +
+ -b V +
+ + +
+ V V V
, , , , , ,
a b n + V
De los Streptococcus viridans 5% - 10% son bilis esculina positivas Algunos Streptococcus beta hemolticos crecen en 6,5% de NaCL No hemoltico 95% reacciones positivas 5% reacciones positivas Reacciones variables
Hisopado Farngeo
CUESTIONARIO
1. Recomendara usted, a un paciente que presenta un cuadro de faringoamigdalitis se haga un examen de secrecin farngea, con el fin de descartar la presencia de Streptococcus pyogenes?
23
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 08 BACILOS GRAM NEGATIVOS DE IMPORTANCIA MEDICA Los bacilos Gram negativos conforman un grupo compuesto por mltiples familias bacterianas entre las que destacan la familia Enterobacteriaceae, Vibrionaceae, Pseudomonadaceae y otras. La familia Enterobacteraceae constituye el conjunto mayor y ms heterogneo de bacilos Gram negativos. Se han descrito al menos 27 gneros y 7 grupos entricos con ms de 110 especies. Estos gneros se han clasificado en funcin de la homologa del ADN, propiedades bioqumicas, reacciones serolgicas, susceptibilidad a bacterifagos especficos y patrones de sensibilidad a los antibiticos. Son bacilos Gram negativos, facultativos que fermentan glucosa, son oxidasa negativos, reducen nitratos a nitritos y no requieren ni su desarrollo se acrecienta con NaCl. Pueden ser mviles o inmviles, estas caractersticas sirven para diferenciar miembros de esta familia de otros bacilos Gram negativos facultativos fermentadores de glucosa pertenecientes a la familia Vibrionaceae. Son organismos ubicuos de distribucin mundial, se encuentran en el suelo, agua, vegetacin y formando parte de la microbiota normal del intestino de casi todos los animales incluyendo al humano. Las Enterobacterias pueden dar cuenta del 80% de los aislamientos clnicamente significativos de bacilos Gram negativos en laboratorios de microbiologa clnica y del 50% de todos los aislamientos clnicamente significativos, as mismo pueden causar aproximadamente de un 60 a 70% de enteritis bacteriana aguda. Si bien muchas Enterobacterias han sido implicadas en caso de diarrea solo se han establecido claramente como patgenos entricos miembros de los gneros Escherichia, Salmonella, Shigella y Yersinia. Excepto las especies de Shigella, que rara vez causan infecciones fuera del tracto gastrointestinal, la mayora de las Enterobacterias son capaces de producir una variedad de infecciones extraintestinales. Sin embargo, un pequeo nmero de especies incluyendo Enterobacter aergenes, Enterobacter cloacae, Escherichia coli, Klebsiella pneumoneae, Proteus mirabilis y Serratia marcescens dan cuenta de la gran mayora de las infecciones. Las infecciones del tracto urinario (mas del 70%) principalmente cistitis son las ms comunes, heridas por infecciones respiratorias, de heridas, del torrente sanguneo y del SNC. MATERIALES Placas con Agar Mac Conkey Placas con Agar EMB Placas con Agar XLD Placas con SSAgar Placas con TCBS Tubos con caldo Selenito Tubos con citrato de Simmons Tubos con TSI Tubos con LIA Tubos con Caldo Triptfano Tubos con MIO, MR-VP Reactivo de Kovacs Reactivos para tincin de Gram Asas y aro de siembra
24
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
AISLAMIENTO E IDENTIFICACIN DE ENTEROBACTERIAS GNEROS ESCHERICHIA, KLEBSIELLA ENTEROBACTER, CITROBACTER, SALMONELLA, SHIGUELLA, YERSINIA, PROTEUS INTRODUCCIN Las enterobacterias son bacilos gram negativos no esporulados, aerbicos y anaerbicos facultativos que habitan en el tracto intestinal. Algunos gneros de esta familia son patgenos para el hombre, en cambio otros condicionan su patogenicidad al hbitat que colonizan. La identificacin de las diferentes especies de enterobacterias se realizan estudiando la actividad metablica del microorganismo sobre los diversos sustratos (carbohidratos, protenas, etc) en la practica se estudiarn las especies de mayor importancia medica. Comprenden muchos gneros entre ellos: Escherichia que se encuentra en la flora normal intestinal; en ocasiones puede ser agente de diarreas (E. Coli enteropatgenos, toxignicos, enteroinvasivo, enterohemorrgico, etc.) y en otras, agente de infecciones en el tracto urinario y genital. As mismo los gneros Klebsiella y Citrobacter se encuentran como flora normal y son patgenos condicionales. IDENTIFICACIN BIOQUMICA El reconocimiento de las diversas especies de enterobacterias se realiza observando las reacciones metablicas, por los cambios de color del medio sobre los substratos contenidos en dichos medios diferenciales. SALMONELLA, SHIGELLA, YERSINIA El gnero Salmonella constituye un amplio grupo de bacterias patgenas como por ejemplo: Salmonella typhi, Salmonella paratyphi A y B, que producen la fiebre tifoidea y fiebres paratficas: Salmonella enteritidis que se encuentra en los animales, al infectar al hombre produce gastroenterocolitis. El gnero Shigella produce disentera bacilar que se caracteriza por diarrea con moco y sangre. Esta bacteria slo afecta al hombre. En el gnero Yersinia, una especie importante es Yersinia enterocoltica que es causante de adenitis aguda e iletis terminal (simulando apendicitis), y diarrea en nios. Por una enterotoxina termoestable se cree que es la causa de la diarrea; el reservorio de este gnero son los roedores y el ganado porcino. Estos tres gneros tienen la misma caracterstica morfolgica (bacilos Gram negativos) la Shigella carece de flagelos por lo cual es inmvil en cambio la Salmonella presenta flagelos lo mismo que la Yersinia. Los tres gneros son anaerobios facultativos, desarrollan en medios como en el agar Mac Conkey, y SSagar a una temperatura de 37 C, exc epto la Yersinia que desarrolla mejor a 28 C.
25
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Yersinia pestis es la causa de la peste bubnica que es primariamente una enfermedad de los roedores. El hombre se infecta al ser picado por la pulga de los roedores infectados, desarrollndose una infeccin primaria ganglionar y hay una forma neumnica ms grave porque el contagio es directo de persona a persona. Esta bacteria es de forma coco bacilar, desarrolla a 30 C, en la fase lisa produce una cpsula y forma colonias viscosas. PROCEDIMIENTO Hacer un frotis en las lminas portaobjetos limpios y desengrasados a partir de la muestra problema, realizar la coloracin de Gram. Observar con el microscopio utilizando objetivos de inmersin, destacando la forma de agrupacin y la coloracin que toma la bacteria. Realizar la siembra en estra de la muestra problema en los siguientes medios de cultivo: Agar Mac Conkey, SSAgar, EMB, XLD. Llevar a la Incubadora a 37C durante 24 48 horas. Realizar la siembra en tubos de diferenciacin bioqumica: Agar citrato, TSI, LIA, Indol, Movilidad, Medio MR VP. Llevar a la Incubadora a 37C durante 24 48 horas.
DIFERENCIACIN BIOQUMICA
26
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTERPRETACIN COLORACIN GRAM
Gram negativos bacilos
Estructura pared celular Gram negativo
Flagelos en peritrico propio del Proteus
Flagelos en peritrico propio de la Salmonella.
Proteus mirabilis swarming
TSI 1 2 3 4 5 6
1 2 3 4 5 6
Sin inocular Pseudomona aeruginosa Shiguella sonnei Salmonella typhi Escherichia coli Proteus mirabilis
27
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA MANERA DE REALIZAR LA LECTURA EN LAS PLACAS Y TUBOS
28
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
AGAR XLD
Escherichia coli
Enterobacter cloacae
Klebsiella pneumoniae
Salmonella enteritidis
Shiguella sp. AGAR MAC CONKEY
Proteus vulgaris.
Escherichia coli
Klebsiella pneumoniae
Enterobacter cloacae
Salmonella typhi
Shiguella sonnei
Proteus vulgaris
29
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
AGAR EMB
Escherichia coli
Enterobacter cloacae
Klebsiella pneumoniae
Salmonella typhi
Shiguella sonnei
Proteus vulgaris
SALMONELLA SHIGUELLA AGAR
Yersinia enterocoltica
Salmonella
Escherichia coli
Proteus vulgaris TSA
30
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
TSI CITRATO SIM VP UREA
Proteus mirabilis
Proteus vulgaris
Salmonella paratyphi - A
Salmonella typhimurium
31
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Shiguella sonnei
Klebsiella pneumoniae
AISLAMIENTO E IDENTIFICACIN DE VIBRIONES INTRODUCCIN Los vibriones tienen las siguientes caractersticas: bacilos curvos o rectos. Gram negativos, son mviles por la presencia de flagelos polares y pueden crecer en los medios para las enterobacterias, son oxidasa positivos y anaerbios facultativos. En este gnero la especie Vibrio cholerae es causante del clera epidmico en el hombre. La enfermedad ms devastadora de todos los tiempos por el cuadro de diarreas potencialmente muy severa que produce. En la sptima pandemia se considera al Vibrio cholerae, biotipo El tor, principalmente el serotipo Ogawa. En la octava pandemia se considera al Vibrio cholerae 0139, como el agente causal. Otras especies de Vibrio pueden causar tambin diarrea y son: Vibrio parahaemolyticus, Vibrio fluviales. Las especies asociadas a infecciones extraintestinales como Vibrio alginolyticus. En la prctica estudiaremos al Vibrio cholerae, agente del clera, que se adquiere por la ingesta de alimentos y aguas contaminadas. La mortalidad es elevada si no se restablece de inmediato el equilibrio hidroelectroltico. Para su aislamiento se utiliza muestras de heces o hisopados rectales. Las muestras que llegan al laboratorio deben sembrarse de inmediato. Los hisopados rectales pueden incluirse en el medio de transporte de Cary Blair. El cultivo directo en el Agar TCBS (tiosulfato, citrato sales biliares y sacarosa) y como enriquecimiento en el medio agua peptonada alcalina. Despus de la incubacin por 24 horas las colonias de Vibrio cholerae son circulares de borde entero, de color amarillo (sacarosa positivas) en el agar TCBS. La identificacin bioqumica de Vibrio cholerae se realiza por las siguientes caractersticas: en el medio TSI pico de flauta cido en el fondo sin gas, sin H2S, lisina positivo, indol positivo, rojo de metilo positivo, voges proskauer negativo. Citrato positivo y ureasa negativa. Desarrolla en caldo peptonado con 0% de NaCL.
32
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTERPRETACIN
Vibrio cholerae
Gram Negativo
Deteccin de especies de Vibrios potencialmente patgenas al camarn
Vibrio cholerae Agar TCBS
Vibrio alginolyticus
Vibrio parahaemolyticus
Vibrios en TCBS Agar
33
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
AISLAMIENTO E IDENTIFICACIN DE BACTERIAS NO FERMENTADORES PSEUDOMONAS
Este gnero comprende bacilos rectos Gram negativos con flagelo polar, no formadores de esporas, carente de cpsula y aerobios. De las numerosas especies de este gnero, las ms importantes han sido relacionadas a infecciones en el hombre, como patgenos oportunistas en huspedes comprometidos; son Pseudomona aeruginosa, Pseudomona mallei, Pseudomona pseudomallei, Pseudomona cetcea y Pseudomona maltophilia. De stas, la primera es la especie ms frecuente, se asocia con enfermedades neoplsicas o en quemaduras severas. Tambin pueden ser causa de infecciones oculares, osteomielitis, sepsis post quemaduras, infecciones en vas urinarias y respiratorias. La mayora de cepas de Pseudomonas aeruginosa son identificadas en base a su olor caracterstico, morfologa colonial, produccin de piocianina y fluorescena, desarrolla fcilmente en medios como Agar Nutritivo, Agar Mac Conkey y muchas cepas desarrollan fcilmente en medios selectivos conteniendo cloruro de hexadeciltrimetilamonio (Agar Cetrimida). Examen macroscpico: Observar las caractersticas de la colonia de Pseudomona aeruginosa en Agar Mac Conkey y Agar Nutritivo, percibir el olor y el color. Examen microscpico: Coloracin Gram, visualizar su tamao, forma y reaccin al gram. Caractersticas Bioqumicas: Observar el desarrollo del microorganismo en el medio TSI, Citrato de Simmons, LIA, Indol, Movilidad. Reaccin de la oxidasa: Positivo: Viraje de color hacia el azul -violeta (con el reactivo N, N, N, N, tetrametil-pfenilenediamina) o prpura (con el reactivo N, N, dimetil-p fenilenediamina) despus de 10 - 15 segundos. Negativo: No hay viraje de color (Foto N 23) Alternativamente una solucin de reactivo al 0.5% puede ser goteado directamente sobre la colonia. Demostracin del pigmento: Con una pipeta depositar cloroformo en el tubo con caldo nutritivo con desarrollo bacteriano, luego agitar y dejar reposar. Observar en el fondo del tubo el pigmento azul que es soluble en el cloroformo.
34
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INTERPRETACIN
Gram Negativo
Colonias en TSA
MEDIO HUGH LEIFSON MEDIO PARA OXIDO FERMENTACIN E. coli es fermentador Pseudomonas es oxidador E. coli Pseudomonas Agar Cetrimida
Pseudomonas aeruginosa en Agar Cetrimida Colonias verde-amarillentas, fluorescentes bajo luz UVA de 366 nm (linterna MICROKIT VMT050).
Prueba De la Oxidasa
35
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 09 HEMOCULTIVO Y COPROCULTIVO HEMOCULTIVO INTRODUCCIN
La sangre de los individuos sanos es estril. Una afluencia repentina de bacterias es habitualmente eliminada del torrente circulatorio en un periodo de tiempo corto, de minutos a horas, excepto cuando existe una infeccin masiva o est presente un foco intravascular infectado. Bsicamente cuando las bacterias se multiplican a tasas que exceden la capacidad del sistema reticuloendotelial para eliminarlas se habla de BACTERIEMIA. El trmino FUNGEMIA se utiliza para designar la presencia de hongos en sangre. La invasin del torrente sanguneo se produce desde: Un foco primario, va sistema linftico al sistema vascular. Entrada directa: por infecciones intravasculares (por ejemplo endocarditis), o a travs de dispositivos mdicos contaminados como catteres y agujas.
Siempre que exista una razn para sospechar una bacteriemia se debe practicar el cultivo de la sangre, ya que en muchas ocasiones solo se puede establecer el diagnstico por este procedimiento. El aislamiento de un microorganismo en los hemocultivos es trascendente porque establece el diagnstico etiolgico de la bacteriemia y permite elegir el tratamiento ms eficaz. DIAGNSTICO Es el aislamiento del microorganismo en la sangre mediante el cultivo de esta y aporta una valiosa informacin a la hora de elegir el tratamiento antimicrobiano adecuado. INDICACIONES Fiebre alta, aunque en neonatos y ancianos la bacteriemia puede cursar con hipotermia y deterioro general. Shock no explicado. Infecciones localizadas. Leucopenia, leucocitosis o trombopenias no relacionadas con procesos hematolgicos.
MTODOS Cuantitativos, nos dara el nmero de bacterias por mililitro de sangre. Cualitativo, indica simplemente la presencia de bacterias en sangre, es el que se realiza de forma rutinaria.
36
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
OBTENCION DE MUESTRA DE SANGRE PARA CULTIVO El momento ptimo de obtencin de la muestra para hemocultivo es justo antes del pico mas alto de fiebre, sin embargo esta situacin ideal no es frecuente. Alternativamente las muestras pueden obtenerse de acuerdo con el caso. Por Ej. - BACTEREMIAS CONTINUAS: En cualquier momento, Ej. Endocarditis. - BACTEREMIAS INTERMITENTES: Una hora antes del pico febril, Ej. Brucelosis. Gua para la cronologa y el nmero de cultivos de sangre en adultos: En sepsis: Se debe tomar dos a tres muestras de lugares diferentes en un lapso de diez minutos. En endocarditis aguda: Obtener tres muestras de tres lugares diferentes en un lapso de 1 a 2 horas. En endocarditis subaguda: Obtener tres muestras de tres lugares diferentes a intervalos de al menos quince minutos. Si el cultivo es negativo a las 24 horas, obtener tres muestras ms. En fiebre de origen desconocido: Obtener dos o tres muestras de lugares diferentes con diferencia de una hora o ms entre una y otra muestra. Si el cultivo es negativo a las 24 horas, obtener dos a tres muestras ms.
Obtencin de muestra de sangre mediante uso de jeringa: ver Practica N 01 del Manual de Microbiologa.
La proporcin entre el volumen de sangre obtenida y el volumen del caldo de cultivo debe estar en una relacin de 1:5 - 1:10. El volumen de sangre depender de la edad del paciente; por cada venopuncin se recomienda: Adultos: Nios: Lactantes: Neonatos: 10 - 30 ml 1 - 5 ml 1 - 2 ml 0.5 - 1 ml
INOCULACIN DE LA MUESTRA DE SANGRE AL MEDIO DE CULTIVO Utilizar un medio bifsico o monofsico para este procedimiento. Desinfectar el diafragma del frasco de hemocultivo con alcohol de 70% alcohol yodado. Inocular la muestra de sangre al frasco con medio de cultivo a travs de diafragma. Debe realizarse inmediatamente de obtenida la muestra para evitar que se coagule. Mezclar el contenido del frasco inclinndolo suavemente dos o tres veces. En caso que se use el medio bifsico, baar la fase slida con la sangre. Descartar la aguja y la jeringa en un contenedor resistente a las punturas. No volver a introducir la aguja en su funda. Limpiar la tapa del frasco. Etiquetar el frasco apropiadamente indicando adems el nmero de hemocultivo.
37
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
SIEMBRA PRIMARIA DE MUESTRA DE HEMOCULTIVO OBJETIVO Describir la tcnica de siembra primaria de hemocultivo para el aislamiento de bacterias causantes de infecciones del torrente sanguneo. CAMPO DE APLICACIN Se aplica para el aislamiento bacteriano a partir de hemocultivos en el diagnstico bacteriolgico de infecciones del torrente sanguneo. MATERIALES Y EQUIPOS a) Estufa de 35 37 C b) Mechero Bunsen o Cabina de Flujo laminar c) Jeringa estril d) Guantes de ltex e) Alcohol al 70% f) Contenedor de material contaminado g) Medios de cultivo Medio bifsico Ruiz Castaeda o monofsico Agar sangre de carnero (AS). Agar Mc Conkey (Mc C) Se puede incluir otros medios (Ej. manitol salado) PROCEDIMIENTO Incubar el frasco de hemocultivo a 35 37 C hast a por 7 das. Baar la superficie de agar con el caldo inclinando el frasco suavemente. Examinar visualmente y con luz transmitida los frascos de hemocultivo despus de 12 y 24 horas de incubacin. La observacin de turbidez o lisis de los glbulos rojos es indicativa de crecimiento bacteriano; entonces se realizar una coloracin Gram y un subcultivo. En los medios bifsicos el desarrollo tambin se puede evidenciar en la fase slida mediante la formacin de colonias. Si no se observa lisis de los glbulos rojos o turbidez en el caldo, o colonias en la fase slida, continuar observando todos los das para ver si aparecen signos de crecimiento, hasta siete das despus de haber iniciado el procedimiento.
SUBCULTIVO Los subcultivos deben realizarse en cabina o cerca de un mechero Bunsen. Realizar subcultivos ciegos dentro de las 12 y 24 horas de incubacin. Para realizar los subcultivos desinfectar la superficie de la tapa del frasco con alcohol de 70%.
38
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Con una jeringa estril, extraer a travs del tapn de jebe la muestra de sangre. Inocular una gota de la muestra del hemocultivo en un extremo de la superficie de las placas de agar sangre, agar Mac conkey y colocar cuidadosamente una gota sobre una lmina portaobjetos para hacer un frotis y coloracin Gram. Utilizando el asa de siembra y tomando como referencia central el inoculo de la muestra, realizar la siembra por dispersin agotamiento en los cuatro cuadrantes de la placa, con el propsito de obtener colonias aisladas. Incubar las placas de AS y agar McC a 35 - 37 C p or 24 horas. Observar la lmina coloreada y buscar la presencia de bacterias. Si no hay crecimiento a las 24 horas seguir incubando hasta por 48 horas. Si no hubiera desarrollo bacteriano, repetir el procedimiento al 5 y 7 da.
LECTURA DE SUBCULTIVOS A las 24 horas observar el crecimiento de colonias. Si no se observa desarrollo, incubar 24 horas ms. Cuando se ha confirmado crecimiento bacteriano por subcultivo, se puede descartar el frasco de hemocultivo siguiendo los procedimientos de bioseguridad. En algunos casos el frasco de hemocultivo debe ser retenido para mayor estudio. En la interpretacin de los resultados deben considerarse los datos clnicos individuales. Staphylococcus coagulasa negativo, corinebacterias y especies de Bacillus son contaminantes frecuentes y a menudo se aslan en slo una de tres muestras. Si no hay leucocitos y el paciente no tiene factores de riesgo para bacteriemia por estos grmenes como inmunosupresin, prtesis, lneas de acceso vascular e historia de adiccin a drogas intravenosas se puede concluir que la presencia de estos grmenes se debe a contaminacin. Se informar el resultado de cada frasco de hemocultivo individualmente.
Medio Bifsico Ruiz - Castaeda
Incubar a 37 C 5 -7 / 21 das
Toma de Muestra Sangunea
Coloracin Gram
Seleccin del Medio de cultivo dependiendo de la tincin de Gram
39
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
MICROORGANISMOS ASOCIADOS AL ASPECTO MACROSCPICO DE HEMOCULTIVOS ASPECTO MACROSCPICO MICROORGANISMO ASOCIADO Streptococcus, Staphylococcus, Listeria spp. Hemlisis Clostridium, Bacillus spp. Bacilo gramnegativo aerobio, Turbidez Staphylococcus, Bacteroides spp. Formacin de gas Bacilo gramnegativo aerobio, anaerobios Pseudomonas spp., Bacillus spp., levaduras Formacin de velo Staphylococcus aureus Cogulo Staphylococcus, Streptococcus Colonias visibles (puntiformes) MEDIOS DE CULTIVO UTILIZADOS, SEGN TINCIN DE GRAM
Gram Agar Sangre Agar Chocolate Mac Conkey CNA (*) Agar Anaerobio Agar Brucella
Cocos Gram Positivos Bacilos Gram Positivos Cocos Gram Negativos Bacilos Gram Negativos
x x x x x x x x
x x x
x x x x
(*) CNA: Agar Columbia-Colistin-cido Nalidixico.
Frascos de Hemocultivos (Aerobios y Anaerobios)
40
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
COPROCULTIVO DIAGNOSTICO ETIOLGICO DE DIARREAS BACTERIANAS. La diarrea puede definirse como el proceso que va acompaado del aumento en el nmero de evacuaciones o una disminucin en la consistencia de las heces, siendo una de las enfermedades de mayor frecuencia en nuestro pas, afectando principalmente a nios. Los gneros bacterianos que causan diarrea comnmente son: Shigella, Salmonella, Escherichia, Campylobacter, Vibrio y otros. MUESTRAS La muestra de eleccin para cultivo de agentes bacterianos productores de gastroenteritis es una porcin de heces diarreicas, nunca heces formes. En el caso de heces formadas, el tamao ser la que asemeje a la de una aceituna, en heces lquidas de 10 a 20 mL. La muestra se debe colocar en un frasco limpio, estril, de boca ancha y con tapa rosca. Las muestras de heces se procesarn para el cultivo dentro de las 4 6 horas siguientes a su emisin. Si esto no es posible, es conveniente su conservacin en un medio de transporte adecuado como el de Cary Blair para evitar la alteracin de bacterias patgenas. Para la siembra deben escogerse las porciones con aspecto purulento, sanguinolento o con moco. PROCEDIMIENTO EXAMEN DIRECTO El examen microscpico directo de las heces persigue la observacin de polimorfonucleares, que sugiere infeccin por un patgeno invasivo. Examen en fresco y/o tincin con azul de metileno Tincin de gram permite observar a los polimorfonucleares y flora predominante
INOCULACIN Examen rutinario: el coprocultivo se realiza mediante la preparacin de una emulsin de 1 2 gramos de heces en solucin salina fisiolgica, a partir de la cual se inoculan los medios de cultivo. Placas de Agar Sangre Medios entricos: Mac Conkey; EMB; Endo. Moderadamente selectivos: usar al menos uno de estos medios para inhibir el crecimiento de la mayora de las enterobacterias mientras se permite el crecimiento de Salmonella y Shigella: Hektoen, XLD, SS. Medio lquido: utilizar el medio Selenito para inhibir el crecimiento de la flora normal durante las horas iniciales de incubacin. Se resiembran en medio slido a partir de las 6 horas. Este medio es fundamental para portadores asintomticos.
41
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Vibrio: medio de enriquecimiento: Agua de Peptona Alcalina a partir de 6 horas, subcultivar en TCBS. Medio selectivo: TCBS. Salmonella: Verde Brillante, Bismuto Sulfito. Escherichia coli: los procedimientos de aislamiento en heces de E. coli, habitualmente quedan fuera de la practica rutinaria de la mayora de los laboratorios. Constituye una excepcin la E. coli O157 H7 por las posibles complicaciones (sndrome hemoltico urmico), por lo que para esta cepa, por su gravedad, podra estar indicada la utilizacin de medios especiales para su deteccin o la investigacin de toxinas fundamentalmente en heces hemorrgicas.
RESULTADOS Cultivos negativos de enteropatgenos: se informar ausencia de crecimiento de salmonella shigella, mencionando todos los microorganismos incluidos en el estudio realizado. Cultivos positivos: se informar del aislamiento del agente patgeno y de su sensibilidad si procede.
42
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
COPROCULTIVO
Muestra de Heces
Microscopa
Siembra en Caldo Selenito
SSAgar
Agar Mac Conkey
XLD
Medios de Identificacin Bioqumica
43
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 10 UROCULTIVO Y ANTIBIOGRAMA
INTRODUCCIN El urocultivo es el cultivo de orina para diagnosticar infeccin sintomtica del tracto urinario o infeccin asintomtica (bacteriuria asintomtica) en pacientes con riesgo de infeccin. Est basada en la presencia de un nmero significativo de bacterias (generalmente 100.000 bacterias por mililitro) La piuria junto con la bacteriuria, es un dato muy importante para el diagnstico de infeccin del tracto urinario, ya que prcticamente est presente en todas las infecciones urinarias. Una excepcin es la bacteriuria asintomtica en la que la piuria puede estar ausente. Agentes etiolgicos a investigar rutinariamente Escherichia coli Klebsiella spp. Enterobacter spp. Serratia spp. Enterococcus spp. Proteus spp. Pseudomonas spp. Acinetobacter spp. Cndida spp. Staphylococcus spp. Streptococcus grupo B (imprescindible en embarazadas)
OBTENCION DE MUESTRA DE ORINA PARA CULTIVO OBJETIVO Describir el procedimiento de obtencin de muestras de orina para cultivo, obtenida del chorro medio.
CAMPO DE APLICACIN El presente procedimiento se aplica en la obtencin de muestras de orina de pacientes para el diagnstico de infecciones del tracto urinario.
CONDICIONES GENERALES La orina es un excelente medio de cultivo para la proliferacin bacteriana, por esta razn, la muestra debe ser procesada dentro de las 2 horas despus de haber sido obtenida o debe refrigerarse a 4 C (mximo 24 horas) hasta su procesamiento.
44
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Generalmente el desarrollo de dos o ms tipos de colonias (en pacientes sin sonda vesical) indican que la muestra se ha contaminado por recoleccin incorrecta o demora en la siembra. OBTENCIN DE MUESTRA DE ORINA DEL CHORRO MEDIO
PACIENTES MUJERES MATERIALES Y EQUIPOS a) Guantes de ltex estriles. b) Cinco o ms piezas de gasa estril de tamao adecuado pudiendo ser de 4 x 4 c) Jabn. d) Agua tibia estril. e) Frasco estril de boca ancha para la muestra de orina. PROCEDIMIENTO a) Mantener la privacidad de la paciente. b) Rotular el frasco con el nombre de la paciente, fecha de obtencin de la muestra, hora y el procedimiento a utilizar para la obtencin de la muestra. c) Lavarse las manos con jabn y abundante agua. d) Preparar una pieza de gasa para la limpieza de los genitales externos humedecindola con agua y una pequea cantidad de jabn. Preparar dos piezas ms de gasa para el enjuague con agua tibia. e) Separar los labios mayores con dos dedos de una mano y limpiar el rea expuesta pasando la gasa de adelante hacia atrs. f) Descartar la gasa. g) Con otra gasa humedecida enjuagar el rea de adelante hacia atrs. Repetir el procedimiento con otra gasa. h) Finalmente secar el rea de adelante hacia atrs con un trozo de gasa seca. i) Mantener separados los labios mayores mientras la paciente empieza a orinar. Luego del chorro inicial colocar el frasco estril para colectar el chorro medio. j) Al terminar de orinar, inmediatamente tapar el frasco y limpiar la superficie del mismo. k) Transportar el frasco con la muestra de orina inmediatamente al laboratorio. PACIENTES VARONES MATERIALES a) b) c) d) e) Guantes de ltex. Cinco o ms piezas de Gasa estril. Jabn. Agua tibia estril. Frasco estril de boca ancha para la obtencin de la muestra.
45
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PROCEDIMIENTO
a) Mantener la privacidad de la paciente. b) Rotular el frasco con el nombre de la paciente, fecha de obtencin de la muestra, hora y el procedimiento a utilizar para la obtencin de la muestra. c) Lavarse las manos con jabn y abundante agua. d) Preparar una pieza de gasa con agua y una pequea cantidad de jabn. Preparar dos piezas ms de gasa para el enjuague con agua tibia. e) Realizar la higiene de los genitales. Retraer el prepucio antes de lavar el glande con la gasa humedecida con jabn. Descartar la gasa. f) Enjuagar el glande, usando una gasa hmeda. Repetir el procedimiento con otra gasa. g) Secar la zona, usando uno o ms piezas de gasa seca. h) Indicar al paciente que mantenga el prepucio retirado e inicie la miccin directamente en un recipiente (orina para descartar). i) Despus del chorro inicial colocar el frasco estril para colectar la muestra del chorro medio. j) Obtenida la muestra, inmediatamente tapar el frasco y limpiar la superficie del mismo. k) Transportar el frasco con la muestra de orina inmediatamente al laboratorio. SIEMBRA PRIMARIA DE MUESTRA DE ORINA OBJETIVO Describir el procedimiento para la siembra primaria de muestra de orina CAMPO DE APLICACIN Se aplica para el cultivo de muestra de orina en el diagnstico bacteriolgico de infecciones del tracto urinario. MATERIALES Y EQUIPOS a) Asa calibrada de platino o descartable de 0.001mL, 0.01 mL. b) Estufa de 35 37 C. c) Mechero Bunsen o Cabina de Flujo laminar. d) Guantes de ltex. e) Contenedor de material contaminado. f) Pinza estril. g) Propipeta o pipeteador automtico.
46
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
h) Medios de cultivo Placas con agar sangre de carnero (AS). Placas con agar Mc Conkey (McC)
PROCEDIMIENTO a) Mantener las muestras en refrigeracin (4 C) ha sta su procesamiento por cultivo. b) Los cultivos deben realizarse en una cabina de bioseguridad o cerca del mechero Bunsen. c) Las placas con AS y McC que se utilizarn en el urocultivo deben estar a temperatura ambiente. Rotular las placas. d) Si el asa calibrada no es descartable, esterilizar el asa de siembra flamendola en el mechero Bunsen hasta que se ponga rojo vivo. Dejar enfriar el asa contando hasta 20. e) Tomar el frasco con la muestra de orina, abrir la tapa y flamear la boca del frasco en el mechero Bunsen. f) Tomar la muestra de orina con el asa de siembra estril introducindola y sacndola del frasco en forma vertical. Tapar el frasco con la muestra. g) Inocular en el centro de la placa con AS a partir del cual se extiende la muestra, hacia delante y hacia atrs. h) Luego, sin quemar el asa, el inoculo se disemina uniformemente con trazos perpendiculares a la siembra inicial en toda la placa. i) Proceder de la misma forma para el agar Mc Conkey. j) Esterilizar el asa de siembra en el mechero. k) Concluida la siembra, cerrar la placa y colocarla con la parte que tiene el medio de cultivo hacia arriba. Incubar la placa de AS y Mc Conkey a 35 - 37 C en condiciones aerbicas por 24 horas.
LECTURA a) Realizar la evaluacin a las 24 horas, si no hay crecimiento bacteriano dejar incubar hasta las 48 horas. b) La evaluacin consiste en el recuento de colonias y se multiplica por el factor de dilucin para obtener las UFC por mL. INTERPRETACIN a) En pacientes sin sonda vesical, la cuenta significativa de bacterias en orina
5
es la presencia de mas de 10 UFC / mL de un solo germen.
3 4
b) Los recuentos intermedios (10 - 10 UFC / mL) indican infeccin si el procedimiento de recoleccin de orina fue realizado correctamente. c) Generalmente, el aislamiento de tres o ms especies bacterianas indican que la muestra se ha contaminado por recoleccin inadecuada o demora en la siembra.
47
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
5
d) En pacientes con sonda vesical, cuentas bacterianas menores de 10 UFC / mL pueden tener significado, as tambin se pueden encontrar bacteriurias polimicrobianas hasta en casi 15% de enfermos. e) En pacientes sin catter se puede comprobar si el procedimiento de obtencin de muestra fue realizado correctamente observando la frecuencia
3 4
con la cual se informan recuentos de colonias intermedias entre 10 - 10 UFC / mL. En pacientes sin infecciones del tracto urinario, el recuento es nulo o se reduce a pocas colonias. f) En muestras obtenidas por puncin suprapbica, el desarrollo de una sola colonia en el medio de cultivo indica infeccin del tracto urinario. NOTA 1: Se usar asas de siembra 0.001 mL para todas las muestras de orina a excepcin de aquellas procedentes de aspirados suprapbicos, de infantes, de nios y de pacientes con tratamiento antimicrobiano, las cuales se inocularn con asas de 0.01 mL debido a que en dichos pacientes pueden haber infecciones del
5
tracto urinario asociados a recuentos menores de 10 UFC/ mL. NOTA 2: De no contar con asa calibrada, utilizar tips estriles y micropipeta de 1L o 10L.
Sedimento Urinario
Coloracin Gram
Agar Manitol Sal
TSA Agar Mac Conkey Agar CLED Lactosa (+) Agar CLED Lactosa (-)
48
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Los parmetros utilizados para obtener el recuento de UFC despus del perodo fueron los siguientes: Si exista crecimiento en todas las lneas de siembra, se consideraba un recuento 100,000 UFC/ml. Si creca en la lnea central y hasta la mitad de las lneas que interceptan a sta, el recuento era de 75,000 UFC/ml. Si creca slo en la lnea central era compatible con un recuento de 50,000 UFC/ml. Cuando se obtena crecimiento de slo la mitad de la lnea central de siembra, se consideraba que corresponda a un recuento de 25,000 UFC/ml.
49
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
ANTIBIOGRAMA, MTODOS DE DILUCIN Y DE DIFUSIN INTRODUCCIN En la prctica mdica los quimoterpicos y antibiticos se emplean para el tratamiento de enfermedades infecciosas. Las bacterias se defienden desarrollando varios mecanismos que los llevan a resistir a los antimicrobianos. En la mayora de los casos esta resistencia no es predecible. El laboratorio de microbiologa ayuda al clnico hacindole reconocer la sensibilidad y resistencia de una determinada bacteria por medio del Antibiograma. El antibiograma puede realizarse por mtodos de dilucin o de disco difusin. MTODO DE DILUCIN MATERIALES Solucin de antibitico que contenga 1000 unidades internacionales o microgramos. Tubos de 13 X 100 estriles. Pipetas de 5 mL. Cepa bacteriana, que contenga aproximadamente 100, 000 a 1 000, 000 microorganismos por ML. Caldo de cultivo.
PROCEDIMIENTO Colocar 10 tubos de 13 X 100 estriles y tapados com algodn, enumerados del 1 al 10. Descongelar el antibitico que contenga mil unidades por mililitro y diluir en proporcin 1:5 en caldo estril, obteniendo una concentracin de 200 unidades por mililitro. Por medio de una tcnica asptica, colocar con una pipeta de 5 mL, 0.5 mL de caldo de cultivo estril en los tubos marcados de 2 al 10. Agregar 0.5 mL del antibitico con 200 unidades a los tubos 1 y 2. mezclar el contenido del 2do tubo y trasvasar 0.5 mL al tubo 3, continuando hasta el 9. retirar 0.5 mL del tubo 9; el 10 no recibe antibitico y sirve como control. Agregar a todos los tubos 0.5 mL de la cepa bacteriana. Incubar a 37 C el tiempo necesario para que el tub o control presente turbidez por crecimiento bacteriano, por lo general 12 a 18 horas.
LECTURA E INTERPRETACIN La concentracin de antibitico va de 100 unidades a 0.3 unidades / mL en orden decreciente a la mitad. El ltimo tubo que no presente turbidez, es la mnima concentracin inhibitoria del antibitico y se expresa en microgramos o unidades por mL (M.I.C.)
50
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
B A C T E R I A
DILUCIN DEL ANTIBITICO 4 5 6 7 8
10
100
50
25
12.5
6.5
3.12
1.56
0.78
0.39
MTODO DE DIFUSIN INTRODUCCIN El mtodo de disco difusin en agar es una manera prctica, fcil y rpida de realizar el antibiograma. El recomendado, es el mtodo de Kirby Bauer, con el que se ha logrado uniformizar criterios que toman en cuenta los conceptos de concentracin mnima inhibitoria (M.I.C.) y de la concentracin promedio en sangre de las drogas frecuentemente usadas. MATERIALES Placas petri con agar Mueller Hinton. Torundas estriles. Discos impregnados con diferentes antibiticos y quimioterpicos. Pinzas estriles. Tubos de prueba con 3 mL decado tripticase soya sembrados con una cepa bacteriana, con una turbidez (desarrollo comparable con el tubo N 0.5 de la escala de Mac Farland (150 000, 000 grmenes/mL)
PROCEDIMIENTO Sumergir la torunda en caldo tripticase soya con la cepa bacteriana, escurrir en las paredes del tubo y extender uniformemente en la superficie de la placa de agar Mueller Hinton. Colocar con ayuda de pinzas los discos impregnados con diferentes antibiticos y quimioterpicos sobre la superficie del agar. Los discos deben quedar a una distancia de 20 mm entre ellos. Incubar a 37C durante 24 horas.
LECTURA E INTERPRETACIN El dimetro de la zona de inhibicin se mide con un vernier o una regla milimetrada, colocada debajo de la placa petri. El lmite del rea de inhibicin esta dada por la inhibicin completa del desarrollo tal como se puede apreciar a simple vista. Los milmetros de la lectura sern llevados a la tabla para traducir su interpretacin a los trminos de susceptible, intermedio y resistente.
51
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Antibiticos y Quimioterpicos
Susceptible
Resultados Intermedio
Resistente
EPSILON-TEST Es una tcnica que combina los mtodos de difusin en agar y dilucin para determinar la CIM. La sistemtica es similar al mtodo de difusin en agar pero en lugar de discos utiliza tiras de E-test. Estas tiras contienen un gradiente del antimicrobiano en la superficie inferior que difunde en el agar estableciendo un gradiente continuo del mismo a lo largo de la tira. Despus de la incubacin se forma una zona elptica de inhibicin del crecimiento y la CMI corresponde con el punto donde el rea de inhibicin del crecimiento intersecciona con la tira. CIM (concentracin inhibitoria mnima): menor concentracin de antimicrobiano capaz de inhibir el desarrollo de una cepa bacteriana dada. CBM (concentracin bactericida mnima): menor concentracin de antimicrobiano capaz de destruir una cepa bacteriana dada.
Mtodo de Kirby Bauer
52
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
UNIDAD II: MICROBIOLOGA APLICADA 2.2 MICROBIOLOGA ALIMENTARIA
53
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 11 ANLISIS MICROBIOLGICO DE PRODUCTOS LCTEOS
INTRODUCCIN El nmero total de microorganismos presentes en la leche o sus derivados por unidad de volumen o de peso es indicativo de las condiciones sanitarias de produccin y conservacin, as como de la vida comercial del producto. Recuentos bacterianos muy altos en leche cruda son indicativos de fuerte contaminacin durante las operaciones de ordeo, manipulacin o almacenamiento, o bien de conservacin a temperatura de refrigeracin insuficientes para retardar al crecimiento microbiano. En productos lcteos pasteurizados, altas cuentas bacterianas indican deficiente procesamientos y/o mala conservacin. Los valores obtenidos en los recuentos bacterianos de estos productos se toman como base para su clasificacin en diferentes grados de calidad. De all la gran importancia que esta determinacin reviste, tanto desde el punto de vista del control de calidad a nivel de las industrias del ramo, como del control sanitario de las agencias gubernamentales. Los mtodos comnmente utilizados para el recuento total de microorganismo en la leche y sus productos son el macroscpico en placas de agar y el microscpico directo. Ambos mtodos al igual que otras tcnicas microbiolgicas aplicadas a estos productos, generalmente se rigen por las normas establecidas por la Asociacin Americana de Salud Publica (Standard Methods for the Examination of Dairy Products) que a su vez han sido recomendadas y traducidas por la Organizacin Panamericana de la Salud (Normas para el Examen de Productos Lcteos). TOMA DE MUESTRA PARA EL ANLISIS MICROBIOLGICO Cuando las muestras de leche o derivados lcteos se destinan a anlisis de tipo microbiolgicos, es necesario tomar una serie de precauciones que adems de garantizar la obtencin de muestras verdaderamente representativas, eviten la contaminacin por fuentes externas y la proliferacin de la carga bacteriana ya presente en los productos. Entre esas precauciones destacan las siguientes: a) Todos los equipos empleados en la toma de muestras deben encontrarse estriles y desinfectados antes de cada recoleccin. Por ejemplo, para tomar varias muestras de leche cruda puede emplearse un probador adecuado que se va esterilizando en un bao de agua hirviente (1 minuto) o una solucin que contenga 250 a 500 ppm de cloro residual (esterilizacin qumica) cuyo exceso se elimina por enjuague en agua estril a fin de evitar que el desinfectante contamine el producto, donde actuara como inhibidor microbiano. b) Tomar precauciones para evitar la contaminacin externa, incluso de las manos de la persona que hace la operacin.
54
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
c) Recolectar porciones representativas (no menos de 150 g) directamente de tanques, recipientes de transporte o pesada, pero no de envases al por menor, los cuales deben tomarse completos en numero proporcional al lote. Cuando el producto se encuentra en lata de tamao comercial, se deben recolectar los envases completos cerrados. Una vez en el laboratorio, se eliminan las etiquetas de papel, se lava el exterior de la lata con agua tibia y jabn o detergente, y se desinfecta uno de sus extremos con solucin de fenol al 5% o por inmersin durante 2 minutos en una solucin de cloro conteniendo 100-200 ppm. Seguidamente la lata se agita, seca y se abre con un punzn previamente esterilizado en igual forma que la lata, dejando un orificio lo suficientemente grande como para introducir una pipeta estril, con la cual se extrae la cantidad requerida para el anlisis, o bien se transfiere el contenido a un frasco estril.
En esta prctica se aprender a: Realizar la preparacin y dilucin de las muestras. Realizar el recuento de microorganismos de aerbios mesfilos viables. Identificar patgenos.
MUESTRAS: Leche cruda y pasteurizada, queso de diferentes marcas 1. PREPARACIN Y DILUCIN DE LAS MUESTRAS DE ALIMENTOS: Mtodo recomendado por el Internacional Standard organizatin (ISO). a) EQUIPOS Y MATERIALES 1. Licuadora que alcance velocidades entre 8,000 a 45, 000 rpm. 2. Vasos de licuadora con tapa, resistentes a T de esterilizacin. Vaso estril por cada muestra de alimento a ser analizado. 3. Balanza de capacidad no inferior a 2,500 g. y una sensibilidad de 0.1 g. 4. Tenedores, cuchillos, pinzas, tijeras, cucharas, esptulas previamente esterilizadas en autoclave o por aire caliente. 5. Pipetas bacteriolgicas de 1 mL graduadas al 0.1 6. Matraces o frascos que contienen 90 mL de diluyente. 7. Tubos (150 X 15 mm) que contienen 9 mL de diluyente. b) PROCEDIMIENTO 1. Tarar el vaso vaco y pesar en el 10 +/- 0.1 g. representativos de la muestra del alimento. 2. Aadir un volumen diligente igual a 9 veces la muestra (90 mL). As se obtiene la dilucin 10-1 (el diluyente puede ser agua tamponada con fosfato). 3. Hacer funcionar la licuadora un tiempo suficiente segn su velocidad para conseguir 15, 000 20, 000 revoluciones, teniendo cuidado que la duracin de la operacin no exceda de 2.5 minutos an a bajas velocidades.
55
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
4. Agitar el homogenizado (dilucin 10-1) y pipetear una porcin de 1 mL en un tubo con 9 mL de diluyente, obtenindose la dilucin 10-2 5. Mezclar el lquido cuidadosamente, aspirando 10 veces con pipeta estril. 6. Transferir con la misma pipeta 1mL a otro tubo conteniendo 9 mL de diluyente y mezclar con nueva pipeta estril y se obtendr la dilucin 10-3 7. Repetir los pasos anteriores hasta conseguir el Nde diluciones deseadas.
REPRESENTACIN ESQUEMTICA DE LA TCNICA
Muestra
90 mL Diluyente
B = Contiene 9 mL del Diluyente 1 mL 1 mL
1 mL
1 mL
10 g.
Dilucin 10-1
10
-2
10
-3
10
-4
10
-5
Agregar 1mL de cada dilucin a una placa estril
Agregar 18 mL de Agar TSA licuado a cada placa
Llevar cada placa a la incubadora a 37 C por 24-48 Hrs.
56
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
2. NUMERACIN DE MICROORGANISMOS AEROBIOS MESOFILOS VIABLES: MTODO: recuento estndar en placa o Pour Plate o recuento en placa por siembra en profundidad. Este mtodo se recomienda para productos lcteos (Standard Methods for the Examination of Dairy Products 1972) y para alimentos congelados, enfriados, precocidos o preparados (ADAC, 1975) excepto que el itimo especifica la temperatura de incubacin de 35 C.
a) EQUIPOS Y MATERIALES Requisitos necesarios para la preparacin y dilucin de las muestras de alimentos. Placas petri (100 X 15 mm) Pipetas bacteriolgicas de 1.5 y 10 mL. Bao mara regulada a 44 46C para mantener el agar licuado. Incubadora regulada a 29 31 C. Contador de colonias. Agar plate count.
b) PROCEDIMIENTO 1) Preparar y diluir la muestra de alimento por la tcnica adecuada. 2) Pipetear por duplicado a las placas petri estriles alcuota de 1 mL a partir de la dilucin 10 -1 10 -2 10 -3 10 -4 10 -5 y una alcuota de 0.1 mL de la dilucin 10 -5 para obtener de 10 -1 a 10 -6 g. o mL. De muestra por placa petri. Se sugiere esta serie de diluciones sino se conoce el rango aproximado de N de bacterias. 3) Agregar rpidamente a las placas petri 15 mL de agar licuado y temperado. Entre la preparacin y la adicin del agar no debe transcurrir ms de 10 minutos. 4) Mezclar inmediatamente las alcuotas con el agar mediante movimientos de vaivn y rotacin de las placas petri, se pueden seguir los siguientes pasos: mover la placa de arriba abajo 5 veces en una direccin. Rotar 5 veces la placa en el sentido de las agujas del reloj. 5) Como control de esterilidad, adicionar a placas petri, agar sin inocular y agar inoculado con el diluyente.
6) Una vez solidificado el agar, invertir las placas e incubarlas a 29 c 31 C durante 48 +/- 3 horas. 7) Cmputo del recuento Estndar, en placa: Seleccionar 2 placas correspondientes a una dilucin que contenga entre 30 y 300 colonias utilizando un contador de colonias.
57
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Tomar la media aritmtica de los recuentos y multiplicar por el factor de dilucin (reciproco de la dilucin utilizada). Reportar el resultado como N de microorganismos aerbios mesfilos por gramo o mililitro segn sea el caso S las placas de 2 diluciones consecutivas estn dentro del rango de 30 300, computar el recuento para cada una de las diluciones y establecer la relacin de los 2 recuentos. Si el cociente es menor que 2, reportar el promedio de los 2 valores. Si el recuento mayor contiene 2 veces o ms al menor, en este caso se reportar el recuento menor.
8) Computo del estimado del Recuento Standard en placa. Si las placas de todas las diluciones muestran ms de 300 colonias, dividir cada duplicado de placas de la dilucin, ms alta en secciones radiales convenientes (2, 4, 8) y contar las colonias en una o ms secciones. Multiplicar el total en cada caso por el factor apropiado para obtener el N de colonias por toda la placa. Promed iar los estimados de las 2 placas duplicadas y multiplicar por la dilucin correspondiente. Reportar el resultado como un estimado del nmero. Si hubiese mas de 200 colonias por 1/8 de seccin de la placa, multiplicar 1,600 (200 X 8) por la dilucin y expresar el estimado como mayor que (>) el N resultante. Ejem. 1600 X 10 -3 = 1600, 000/g mL Si no hubiese colonias en placas de la mayor concentracin, reportar el estimado como menor que (<) una vez la dilucin. Ejemplo: 10-1 = 0 colonias. Se reporta como < 10/g mL. Si se hubiese sembrado 0.1 mL, en este mismo caso se reporta < 100/g mL.
9) Expresin de resultados Se deber reportar nicamente 2 dgitos significativos, ellos son el primero y el segundo (comenzando por la izquierda) del promedio de los recuentos. Los dems dgitos se reemplazarn por ceros. Ejemplo: 523, 000 se reportar como 520, 000 = 52 X 104 g mL de alimento segn sea el caso. Si el tercer dgito de la izquierda es 5 mayor que 5, adicionar una unidad al segundo dgito (redondear). Ejemplo: 83, 600 se reportar como 84, 000 = 84 X 103/ g mL de alimento. Si el recuento en placa se utiliza para determinar la aceptacin o rechazo de un lote de alimento, nicamente se considerar el recuento estndar en placa, nunca el estimado del recuento, ste es til solamente como una aproximacin primaria en la determinacin de la calidad microbiolgica.
58
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RECUENTO ESTNDAR EN PLACAS DE AGAR (RECUENTO DE AEROBIOS MESFILOS)
El recuento estndar en placas (REP) o recuento de aerobios mesfilos, es un mtodo macroscpico, emprico, universalmente utilizado para determinar en forma aproximada la carga bacteriana. Esencialmente consiste en determinar el numero de colonias que se desarrollan cuando se siembra una cantidad medida o pesada de muestras, en placas de agar de composicin estndar preparadas bajo condiciones estipuladas, a objeto de obtener reproductividad en los resultados en diferentes laboratorios. Los resultados obtenidos por este mtodo permiten establecer la calidad sanitaria de la leche. Una comparacin de los resultados obtenidos en la leche antes y despus de ser pasteurizadas, permite deducir la resistencia de los microorganismos presentes en el producto a la accin del calor. Un conteo superior en el producto pasteurizado indica recontaminacin post-pasterizacin o bien presencia de microorganismos termoflicos. Este mtodo puede aplicarse tanto a la leche y derivados fluidos como a los productos lcteos semislidos o slidos, variando fundamentalmente el procedimiento de preparacin de las diferentes muestras y de la primera dilucin. Particularmente en los productos slidos es necesario pesar la muestra directamente sobre una botella de dilucin bajo condiciones aspticas. Utilizando un medio selectivo slido en placas como el agar-lactosa- desoxicolatoformiato o agar bilis-rojo neutro-cristal violeta. Los medios slidos se emplean generalmente para el control sanitario de leches pasteurizadas, con el objeto de establecer si cumplen las normas sanitarias (mximo conteo de bacterias/mL). Tienen la ventaja de que permiten obtener resultados cuantitativos en una sola placa. Sin embargo, no se emplean cuando se necesita utilizar volmenes grandes de muestra. Los coliformes crecen fcilmente en el agar lactosa-desoxicolatoformiato, ayudados por la presencia de lactosa que fermentan produciendo cido que hace cambiar el pH y virar el indicador (rojo neutro) de amarillo a rojo; el desoxicolato inhibe el crecimiento de los grmenes Gram positivos. El periodo de incubacin de las placas con este medio, no deber ser mayor a las 24 horas preferiblemente 20 horas, ya que otros microorganismos pueden crecer ocasionando confusin. Por ello solo se cuentan aquellas colonias rojas de dimetro mayor a los 0,5 mm, rodeadas de un alo de desoxicolato de sodio precipitado. Adems las placas se deben preparar con una capa fina superficial de medio, superpuesta, para obtener las colonias de coliformes ligeramente por debajo de la superficie y evitar sean confundidas con colonias superficiales. De manera similar se usa el agar bilis-rojo neutro-cristal violeta, donde la bilis y el colorante inhiben el desarrollo de los microorganismos Gram positivos, mientras que el rojo neutro acta como indicador. Las bacterias coliformes crecen en este medio en 24 horas, formando colonias de color rojo prpura (por debajo de la capa superpuesta) de 1-2 mm de dimetro, rodeadas de una zona rojiza de bilis precipitada.
59
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRUEBA PRESUNTIVA EN MEDIO SLIDO
MATERIALES Y EQUIPOS Pipetas estriles de 1mL; Placas de Petri estriles; Blancos de dilucin 90 mL; Estufa de incubacin; Equipo individual. Agar bilis-rojo neutro-cristal violeta.
MUESTRAS: Las mismas empleadas en la parte anterior. PROCEDIMIENTO 1. Con pipeta de 1 mL, transferir porciones de 1 y 0,1 mL de la muestra homognea a placas de Petri estriles, debidamente rotuladas (diluciones 1 y 10-1). 2. Cuando se requieren mayores diluciones (10-2, 10-3) preparar una dilucin 1:100 (10-2) transfiriendo 1 mL de la muestra a un blanco de dilucin (99 mL). Mezclar bien y sembrar volmenes de 1 y 0,1 mL en placas rotuladas. En general el procedimiento es similar al del recuento estndar en placa. 3. Verter 15-18 mL del medio slido fundido (45 C) y mezclar. 4. Despus que el medio se haya solidificado, agregar a cada placa un pequeo volumen adicional (3-4 mL) del medio fundido para obtener una fina capa superpuesta. 5. Incubar las placas a 32 o 35 C por 18 - 24 horas. 6. Terminado el periodo de incubacin, contar las colonias rojas tpicas que presenten un dimetro de 0,5 mm o mayor; multiplicar el recuento por la dilucin correspondiente y expresar el resultado en trminos de "ufc de coliformes por 100 mL". REQUISITOS MICROBIOLGICOS PARA LA LECHE CRUDA Y PASTEURIZADA La norma COVENIN clasifica la leche cruda segn el nmero de aerobios mesfilos en cuatro categoras:
CATEGORAS Categora A Categora B Categora C Sin clasificacin Para leche pasteurizada se exige lo siguiente: -
UFC/ML Hasta 500.000 500.001 a 1.500.000 1.500.001 a 5.000.000 ms de 5.000.000
Recuentos de Aerobios Mesfilos: mximo: 2,0 x 104 ufc/mL Coliformes Totales: mximo: 93 NMP/mL.
60
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 12 ANLISIS MICROBIOLGICO DE UNA MUESTRA DE AGUA INTRODUCCIN En el agua pueden encontrarse una gran variedad de microorganismos, los cuales afectan en mayor o menor medida a la potabilidad del agua y a sus caractersticas organolpticas. Adems de la flora normal (Bacillus, Pseudomonas, etc.), en el agua pueden existir microorganismos contaminantes. Una de las fuentes principales de contaminacin son las aguas residuales que contienen heces que pueden ser vehculo de transmisin de patgenos. Aparte del problema de transmisin de enfermedades, la contaminacin del agua tambin acarrea otras consecuencias. Por ejemplo, la degradacin biolgica por los microorganismos de grandes cantidades de residuos orgnicos vertidos al agua hace disminuir rpidamente el oxgeno existente, creando un ambiente desprovisto de toda forma de vida que no sea anaerbica: mueren los peces, disminuye la vida vegetal y se produce el hedor caracterstico debido a las actividades de los microorganismos anaerobios. Los microorganismos que aparecen en el agua pueden ser de varios tipos: Bacterias procedentes del agua: tienen una temperatura ptima de crecimiento de 25C. Bacterias procedentes del suelo: generalmente crecen por debajo de 25C. Microorganismos procedentes del intestino del hombre y otros animales, que crecen mejor a 37C.
OBJETIVO Preparacin y Dilucin de las Muestras Numeracin Coliformes Determinacin del Numero Ms Probable (NMP). Identificacin de Patgenos
MATERIALES Muestra de agua (unos 100 ml). Medios de cultivo: Placas de YED (4), tubos de medio Caldo Eosina Azul de Metileno (EMB). Tubos con 1 ml de agua estril para diluciones. Tabla estadstica de Nmero Ms Probable (NMP). Asa de vidrio, mechero
TOMA DE MUESTRA Las muestras que tomaremos para el anlisis deben ser representativas del agua a estudiar, para poder determinar a partir de ellas su calidad microbiolgica de inters sanitario. Las muestras deben reflejar, por consiguiente, la composicin microbiana del agua. Hay normas para la toma de muestras de aguas, segn sus distintas procedencias (grifos, pozos, depsitos, lagos, ros, manantiales, etc.). En cualquier caso, siempre para su recogida deben utilizarse frascos estriles y deben recolectarse cantidades comprendidas entre 500 y 1000 ml.
61
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
El anlisis bacteriolgico debe realizarse lo antes posible, una vez tomada la muestra, procurando que no transcurran ms de 6 horas. En caso de que esto no fuera posible, se debe mantener la muestra a 4C y no retrasar el anlisis ms de 24 horas. PRUEBAS PRESUNTIVAS Las pruebas de fermentacin presuntivas, para establecer la presencia de coliformes en el agua, puede efectuarse siguiendo lo siguiente: a) Utilizando un medio liquido selectivo en tubos de fermentacin (tipo Durham) como el caldo lactosado-bilis-verde brillante (CLBVB) o el caldo lactosadopeptona-recinoleato-formato. Estos medios se recomiendan cuando se desea analizar volmenes relativamente grandes de agua (5 a 100 mL). En el CLBVB, el colorante (verde brillante) y la bilis actan como inhibidores del crecimiento de las bacteria Gram positivas, pero permiten el desarrollo de las Gram negativas; la lactosa sirve como sustrato a las bacterias coliformes que la fermentan en 48 horas a 32 o 35C, formando cido y gas el cual es recolectado en los tubos de fermentacin, demostrando el crecimiento de las bacterias coliformes. Cuando se emplean 5 tubos del medio liquido para cada una de 3 diluciones diferentes de leche (10, 1 y 0,1 mL) es posible obtener valiosa informacin, que con la ayuda de tablas especiales permite hacer un calculo aproximado del numero de bacterias posiblemente presentes en la muestra, resultado que se expresa en trminos del "Nmero Mas Probable" de coliformes por unidad de volumen (Ej.: NMP/100 mL). En forma similar puede emplearse el caldo lactosado peptona-ricinoleato-formato, en el cual el ricinoleato sdico acta como inhibidor de las bacterias Gram positivas, pero no de las Gram negativas, en tal forma que los coliformes crecen formando gas a partir de la lactosa, reaccin que es acelerada por el formato de sodio. NUMERACIN DE COLIOFORMES DETERMINACIN DEL NMERO MS PROBABLE (NMP) Mtodo Norteamericano: recomendado para anlisis de agua y alimentos (ADAC, 1975; APHA, 1976) EQUIPOS Y MATERIALES 1. Los requisitos necesarios para la preparacin y dilucin de la muestra de alimentos. 2. Incubadora a 35 37 C. 3. Pipetas bacteriolgicas de 1 mL; Asa de siembra. 4. Medios de cultivo: Caldo Verde Brillante (Caldo BRILA), volmenes de 10 mL en tubos de 150 X 15 mm, conteniendo tubos de fermentacin invertidos (75 X 10mm) Caldo Laurilsulfato (LST), volmenes de 10 mL en tubos de 150 X 15 mm, conteniendo tubos de fermentacin invertidos.
62
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Agar Eosina Azl de Metileno (EMB) o Agar Endo.
PROCEDIMIENTO
1. Preparar las muestras segn la tcnica ya descrita, para su preparacin y dilucin. 2. Pipetear 1 ml de cada una de las diluciones del homogenizado de alimento en tubos de caldo LST, utilizando 3 tubos por dilucin. 3. incubar los tubos a 35 37 C por 24 horas. 4. Anotar los tubos que demuestren produccin de gas (Prueba presuntiva). 5. De cada tubo que contiene gas, transferir una azada a tubos conteniendo Caldo BRILA o aislar sobre placas con Agar EMB o Agar Endo. 6. Incubar a 35 37 C por 24 48 horas. 7. Confirmar la presencia de bacterias coliformes por: a. La formacin de gas en caldo BRILA b. La formacin de colonias negras o con centro negro o la formacin de colonias mucosas rosado naranjas en agar EMB. c. La formacin de colonias rojas rodeadas de halo rojo en agar endo. 8. Anotar el nmero de tubos confirmados. Referirse a la tabla del NMP para expresar el resultado.
INTERPRETACIN DE LOS RESULTADOS
El agua se considera potable si los valores obtenidos en los ensayos estn dentro de los lmites establecidos por la ley.
Las normas legales vigentes exigen: Aerobios totales: No existe lmite legal pero los valores mximos recomendados son: Coliformes: Coliformes totales: < 1 / 100ml. Coliformes fecales: < 1 / 100ml.
63
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
DETERMINACIN DEL NMERO MS PROBABLE (NMP) DE COLIFORMES
1 mL
1 mL
90 mL Diluyente
Dilucin 10-1
1 mL
10-2
1 mL
9 mL Diluyente AP 10-3
1 mL
EMB
Caldo Brila ENDO
Caldo E.C.
44.5 +/0.2 C X 2448 Hrs. Formacin de gas es + para coliformes fecales.
Tubos con caldo Lauril Sulfato conteniendo tubos de fermentacin invertidos 35-37 C / 2448 Hrs.
35-37 C por 24 hrs.
EMB
ENDO
Diferenciacin Bioqumica
64
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
UNIDAD II: MICROBIOLOGA APLICADA 2.3 MICROBIOLOGA EN LA INDUSTRIA FARMACUTICA Y COSMTICA
65
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 13 MONITOREO MICROBIOLGICO DE AMBIENTES SUPERFICIE Y PERSONAL INTRODUCCIN El local donde se va a elaborar medicamentos o especialmente para este fin. Los ambientes deben iluminacin, ventilacin, temperatura y humedad. reas de procesamiento, superficies de pisos, ayudar a determinar: cosmticos, debe ser construido reunir condiciones adecuadas de El control microbiolgico de las mesas, maquinaria y personal
Si todas las reas han sido apropiadamente limpiadas. Si el equipo esta siendo apropiadamente mantenido. Si los medios de limpieza y desinfeccin especificadas estn siendo usados o han sido cambiados. Si el personal esta siguiendo las instrucciones sealadas. Si la incidencia de patgenos especficos aumenta. Si los programas necesitan ser modificados.
MATERIALES Y MEDIOS DE CULTIVO Tripticasa soya agar pH 7.3 en placas petri de 100 X 15 mm. Agar oxitetraciclina glucosa en placas petri de 100 X 15 mm Torundas estriles de algodn. Plantillas de hojalata o aluminio de 10 x 10 cm. Tubos de prueba con 10 mL de agua peptonada + tween 80. Pipetas de de 1 mL 1/10. Extensores de vidrio estriles.
METODOLOGIA Monitoreo de aire Monitoreo de superficies y Equipos Monitoreo de Personal Mtodo de Sedimentacin Mtodo de Hisopado Mtodo de Hisopado
66
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PROCEDIMIENTO: MTODO DE SEDIMENTACIN: Exponer las placas de la siguiente manera: 1. Una placa por cada 10 a 11 m de rea, con un mnimo de una placa por ambiente o pasadizo. 2. Una placa debe ser expuesta en l rea de trfico mximo, con una corriente normal de aire. 3. Cada placa expuesta por el tiempo indicado de acuerdo al ambiente a controlar (15 a 30 minutos). 4. Para exponer la placa esta se coloca sobre un papel blanco y se retira la tapa a un costado. 5. La incubacin se realiza por el tiempo y la temperatura determinado por los medios de cultivo, as para el caso de TSA ser de 37 C x 48 horas y Agar Oxitetraciclina (OGA) a 22 C x 72 horas. 6. Hacer el recuento de colonias y reportar por placa. METODO DE HISOPADO PARA SUPERFICIES 1. Escoger la superficie a muestrear. 2. Humedecer la torunda con agua peptonada + tween 80, eliminar el exceso. 3. Colocar la plantilla sobre la superficie escogida. 4. Hisopar primero en sentido vertical, luego horizontal y finalmente diagonal. 5. Colocar las torundas en agua peptonada para revivificar por 20 minutos. 6. Sembrar en el agar TSA y OGA 0.1 mL de agua peptonada. 7. Incubar a 37 C y 25 C respectivamente por 48 hor 8. Hacer recuento de colonias y reportar por cm2. METODO DEL HISOPADO PARA EL PERSONAL 1. Escoger la zona a muestrear (manos, puos, gorro, mandil, etc). 2. Seguir el procedimiento para superficies pero sin usar plantilla. 3. La temperatura y tiempo de incubacin son similares que para superficies. 4. Hacer el recuento de colonias y reportar Nde c olonias por zona muestreada. as.
67
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
DIAGRAMA DE TRABAJO CONTROL HIGIENICO DE SUPERFICIES MTODO DEL HISOPADO O DE LAS TORUNDAS
Envase de vidrio estril con 10 mL de A.P.
Torundas estriles
Agua peptonada con Tween 80 10 mL
Revivificar por 20 Min agitando de cuando en cuando
TSA
Agar Mac Conkey
Agar selectivo para Estreptococos
AMS
Agar Sabouraud
Incubar a 32 C por 48 Horas
Incubar a 20-22 C por 5 Das
68
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RECUENTO DE MOHOS Y LEVADURAS
Colonias de levaduras en placa de petri
Colonia de moho en placa de petri
RECUENTO DE BACTERIAS
69
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 14 CONTROL MICROBIOLGICO DE CREMA DE BABA DE CARACOL
INTRODUCCION
Los ensayos de control sobre la contaminacin microbiana deben entenderse tanto en forma cualitativa como cuantitativa. Segn esto, en los medicamentos y cosmticos no debe haber agentes de enfermedades, y el contenido de saprofitos no debe sobrepasar los valores limites definidos, para evitar variaciones de un medicamento y/o cosmtico en cuanto a su aspecto, olor, color, sabor, consistencia, descomposicin, intolerancia, disminucin de activadas y otros. OBJETIVOS
Determinar el nmero de microorganismos aerobios viables, recuento de hongos y levaduras y la ausencia de determinadas especie patgenas. Segn la Farmacopea USA XXX capitulo Microbial Limit Test se prescribe para todos los productos farmacuticos, desde materia prima, producto semielaborado y producto terminado. En industria cosmtica el test es prescrito para cremas, shampoo, sombras, polvos compactos, lpices labiales, existiendo solo una variacin en el procesado de las muestras.
TOMA DE MUESTRAS
Los principios para tomar una muestra representativa en exmenes qumicos y fsicos, as como en ensayo con animales, son tambin validos para los ensayos microbiolgicos. Las muestras se tomaran aspticamente, evitando la posibilidad contaminaciones secundarias. Realizadas por personal especializado. de
La USP XXX prescribe, para el examen microbiolgico de un lote la toma de 03 muestras representativas, cada una conteniendo 10mL o 10g. De estas, una muestra esta destinada a la determinacin del N de grmenes y 2 muestras, a la determinacin del tipo de grmenes. La cantidad de 10mL o 10g deber estar constituida por muestras individuales cuyo contenido ser a su vez 1mL o 1g. La muestra individual deber provenir de por lo menos 10 envase o, en caso de tratarse de material a granel, de por lo menos 10 recipientes.
70
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PREPARACION DE LA MUESTRA LIQUIDOS Pueden ser soluciones verdaderas o suspensiones en vehiculo acuoso, o alcohlico (no mas del 30%). Diluir.
LIQUIDOS INMISIBLES, UNGUENTOS, CREMAS Y CERA. Agregar cantidad mnima de un emulsificante (Tween 80). Homogenizar. Calentar a 40 C. Proceder como para una suspensin. Cuando contienen inhibidores usar el mtodo de filtracin por membrana. Para el examen del nmero de grmenes, la muestra deber diluirse en forma rpida y homognea, bajo condiciones estriles. MEDIOS DE CULTIVO 1. 2. 3. 4. 5. 6. 7. Agar peptona de soya y casena digerido pH 7.3 +- 0.2 Caldo peptona de soya y casena digerido pH 7.3 +-0.2 Caldo lactosa pH 6.9+-0.2 Agar Vogel Jonson Agar Cetrimide Agar Mac Conkey. Agar Xilosa lisina Desoxicolato o Agar SSA.
DILUYENTE: Solucin amortiguadora de fosfatos pH 7,2 +- 0,1 (USP XXX) PROCEDIMIENTO 1. Transferir el contenido de la muestra colectada segn el tipo de producto para baln de 125 mL estril, agitar lentamente, tomar 1mL y transferir para baln de 125ml. Adicionar 9mL de agua peptonada 0.1% estril (dilucin 10-1) tomar 1mL y transferir para baln de 125mL estril, adicionar 9mL de agua peptonada 0.1% estril (diluir 10-2), tomar 1mL y transferir para baln de 125mL estril, adicionar 9mL de agua peptonada 0.1% estril (dilucin 10-3). Efectuar las operaciones en zona asptica. 2. BACTERIAS: Emplear placas de petri 100x20mm. Separar dos placas para cada dilucin, dispersar 1mL de cada dilucin en cada placa y 15-20mL de medio Agar Caso licuehecho a 45C, esperar solidificar incubar a 37C +/- 2C durante 72 horas y hacer la lectura diaria. 3. HONGOS Y LEVADURAS: Emplear placas de petri 100x20mm. Separar dos placas para cada dilucin, dispersar 1mL de cada dilucin en cada placa y 1520mL de medio Sabouraud 4% Dextrose Agar licuehecho a 45C, esperar solidificar. Incubar 20-25C durante 7 das.
71
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
4. CALCULOS: Calcular la media aritmtica de cada dilucin a partir de los valores obtenidos de las placas. Calcular el nmero de microorganismos por gramo o mililitro para cada dilucin, multiplicando el nmero de colonias de la placa por la dilucin usada y relatar la media aritmtica de los resultados. Ejemplo. DILUCION 1:10 1:10 1:100 1:100 1:1000 1:1000 COLONIAS POR PLACA 293 213 119 100 41 12 UFC/G mL 293X101 213X101 119X102 100X102 41X103 12X103
PROMEDIO
2930+2130+11900+10000+41000+12000 6
= 13.326 UFC/G mL
Limites:
Bacterias: 1000 UFC/mL o g. Hongos y Levaduras: 100 UFC/mL o g.
PATOGENOS INOCULACION: Transferir con el auxilio de una pipeta 1mL de la muestra para un tubo de ensayo conteniendo 10mL de Caldo Lactosa conteniendo 1 tubo colocado invertido de Durham y para un tubo de ensayo conteniendo 10mL de Caldo Casena. INCUBACION: Incubar los tubos de Caldo Lactosa y Casena en estufa entre 35 a 37 C por 24 horas.
72
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 15 CONTROL MICROBIOLGICO DE ENVASES MUESTREO Se debe elegir un nmero representativo del lote a examinar que variara de acuerdo al nmero total de unidades. En ningn caso debe ser inferior a 5 el nmero de envases a controlar. MEDIOS DE CULTIVO. Agar triptona extracto de levaduras (TYA) para la numeracin de microorganismo aerobios viables. Agar Sabouraud o Agar glucosa extracto de levaduras (OGA) para la numeracin de hongos y levaduras.
a. METODO Cada uno de los envases seleccionados en el muestreo, se lavan con un volumen conocido de agua peptonada, agitando normalmente el recipiente 25 veces, cada uno de estos volmenes se utilizara luego como si fuera una muestra liquida, procedindose a realizar la siembre de 1 mL y 0,1 mL, por duplicado en placas de petri estriles. Aadir el agar de recuento, mantenido a una temperatura de 45 +-1 C y proceder a la incorporacin de la muestra en el agar mediante movimiento de las placas. Dejar solidificar e incubar a 30 C por 24-48 horas para la numeracin de microorganismos aerobios viables y de 5 das a temperatura ambiente para la numeracin de hongos y levaduras. b. RESULTADOS. Los resultados se expresan siempre en nmero de microorganismos por envase, hay que tener en cuenta las diluciones empleadas. ESQUEMA
1mL 1mL Agregar volumen conocido Agua Peptonada (OGA) (TYA) (TYA) (OGA) TYA: Incubar a 37 C por 24 -48 hrs. OGA: Incubar a 22 C por 3-5 das un de
0.1mL 0.1mL
73
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
PRACTICA N 16 CONTROL MICROBIOLGICO DE LPICES LABIALES PRODUCTO COSMTICO Toda sustancia o preparado destinado a ser puesto en contacto con las diversas partes superficiales del cuerpo humano (epidermis, sistema piloso y capilar, uas, labios y rganos genitales externos) o con los dientes y las mucosas bucales, con el fin exclusivo o principal de limpiarlos, perfumarlos, modificar su aspecto, y/o corregir los olores corporales, y/o protegerlos o mantenerlos en buen estado. El control microbiolgico de productos cosmticos parte desde el anlisis microbiolgico de la materia prima, del producto en proceso y de los productos cosmticos terminados. PREPARACIN DE LAS MUESTRAS Una vez que se recibe una muestra de un producto cosmtico, sta se debe analizar lo ms pronto posible, sin embargo, cuando es necesario almacenarla se debe hacer en un lugar limpio que se encuentre a temperatura ambiente. Las muestras nunca se deben incubar, refrigerar o congelar antes o despus de su anlisis microbiolgico. Es importante inspeccionar cuidadosamente el aspecto que presenta la muestra en el momento que se recibe y se debe anotar cualquier irregularidad que se observe en el envase. Antes de abrir el envase y tomar la muestra del producto para realizar el anlisis microbiolgico, se debe desinfectar su superficie con cualquiera de las siguientes soluciones desinfectantes: Etanol al 70% (v/v) y HCl al 1% en agua. Glutaraldehdo al 2%. Para hacer el anlisis microbiolgico es importante utilizar una porcin representativa del contenido de la muestra. Cuando se trata de productos que contienen menos de 1 g o menos de 1 mL, se debe analizar el contenido completo del envase. Todas las manipulaciones de la muestra se deben realizar aspticamente. CREMAS Y PRODUCTOS CON BASE OLEOSA TOMA DE LA MUESTRA Abrir el estuche y raspar aspticamente la superficie del labial con una esptula estril. Colocar la muestra en un frasco de dilucin o en un tubo estril con tapa de rosca hasta alcanzar el peso deseado.
74
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
INCORPORACIN DE LA MUESTRA AL MEDIO DE CULTIVO Este es el grupo de productos que, por su naturaleza, presenta las mayores dificultades para la incorporacin de la muestra en el medio de cultivo. Para lograr su incorporacin se pueden aplicar los siguientes procedimientos: 1. Tratamiento previo de la muestra con Tween 80. Para ello: Pesar aspticamente la cantidad de muestra requerida en un tubo de ensayo con tapa de rosca o en un frasco de dilucin estril. Aadir Tween 80. Mezclar la muestra con el Tween utilizando una esptula estril. Aadir la mezcla al medio de cultivo e incorporar por agitacin. 2. Agregar Tween 80 al medio de cultivo e incorporar la muestra por agitacin. La cantidad de Tween 80 a aadir (puntos 1 y 2) depender de la cantidad de muestra pesada. NOTA: En los dos casos anteriores (puntos 1 y 2) la cantidad de Tween 80 aadido se toma en cuanta para aadir la cantidad de medio de cultivo adecuada para preparar la dilucin. Por ejemplo si se pes 1 g de muestra y se aadi 1 mL de Tween 80, slo se aaden 8 mL del medio de cultivo. 3. Agitacin. Manual, por agitacin del frasco de dilucin con el medio de cultivo y la muestra. Aadiendo perlas de vidrio estriles al frasco de dilucin que contiene el medio de cultivo y agitar manualmente. Utilizando licuadoras. En este caso se debe: a) Pesar aspticamente la cantidad de muestra necesaria en un frasco de vidrio estril (al que puedan adaptrsele las aspas de la licuadora) que contenga el medio de cultivo. Colocar las aspas de la licuadora previamente esterilizadas. Invertir el frasco y colocarlo sobre el motor de la licuadora. Encender el motor de la licuadora a velocidad media por no ms de un minuto, para evitar que los microorganismos presentes sean destruidos. NOTA Si la muestra ya ha sido pesada en el frasco de dilucin se puede pasar aspticamente todo el contenido del frasco de dilucin (muestra ms medio de cultivo) hacia el frasco con las aspas de la licuadora y licuar. La muestra se puede incubar en el mismo frasco cambiando las aspas de la licuadora por una tapa estril.
75
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
4. Calentamiento Hay productos que funden a bajas temperaturas y esto puede ayudar a la incorporacin de algunas muestras de naturaleza oleosa. Este calentamiento se realiza colocando el frasco de dilucin con la muestra en un bao de mara a una temperatura no mayor de 40C por 3 minutos para evitar la destruccin de los microorganismos presentes. NOTA Estas opciones que se presentan para la preparacin de los productos con base oleosa no son nicas, ni tampoco es necesario aplicarlas en el orden que hemos indicado. Algunas muestras slo necesitan de uno de estos procedimientos para quedar totalmente incorporadas en el medio de cultivo, sin embargo, en otros casos puede llegar a ser necesario utilizarlos todos estos pasos. El procedimiento a seguir va a depender de la naturaleza del producto a analizar y es el microbilogo quien debe tener suficiente criterio para elegir la manera de resolver los problemas a medida que stos se van presentando. La cantidad de Tween 80 a aadir depender de la cantidad de muestra pesada (generalmente se aade la misma cantidad que fue pesada de la muestra). La cantidad de Tween 80 aadido se toma en cuenta para aadir la cantidad de medio de cultivo adecuada para preparar la dilucin. Por ejemplo si se pes 1 g de muestra y se aadi 1 mL de Tween 80, slo se aaden 8 mL del medio de cultivo.
76
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
REFERENCIA BIBLIOGRFICA
Microbiology. Davis B, Dulbecco R, Eisen H, Gisnberg H 4th Edition 1984. Harper & Row Pub. Microbial Life Perry J, Staley JT, Lory S. Sinauer Ass Publishers Inc. MA. 2002. Ecologa microbiana y Microbiologa ambiental Atlas R M, Bartha R Pearson Educacin. Madrid, 4a ed. 1998. Microbial ecology and infectious disease Rosenberg E ed. ASM Press. Washington . 1999. Biologa de los microorganismos. Brock T D, Madigan M T, Martinko J M, Parker J. 8 Ed, Prentice Hall Madrid, 1999. Zinsser. Microbiologa. Joklik W K, Willett H P, Amos D B, Wilfert C M. 20 edicin. Panamericana. 1996. Microbes in action: A laboratory Manual of Microbiology. Seeley H W, Vanderrmark P J, Lee J, Freeman W H. 4th edition 1991. General Microbiology. Schlegel H G 7th edition Cambridge University Press UK 1997. Bacteria in Biology, Biotechnology and Medicine. Singleton J. 3rd Edition Ed. Wiley & Sons, USA. 1995. Encyclopedia of Microbiology. Lederberg J. Academic Press, Inc. USA. 1992. Microbiologa en Prctica Vullo D L, Wachsman M B, Alch L E Editorial Atlante S.R.L. Buenos Aires, 2000. Introduccin a la Microbiologa Tortora G J, Funke B R, Case C L. Editorial Acribia SA, Zaragoza Espaa, 1993. Diagnostic Microbiology Koneman E W, Allen S D, Janda W M, Schreckenberger P C, Winn W C Jr. 5 th Edition, Lippincott, Philadelphia, 1997. Antibiotics in Laboratory Medicine Lorian, Victor Editor, Williams & Wilkins, Baltimore USA, 1980. Inmunologa e Inmunoqumica Margni R A, 5 edicin Editorial Mdica Panamerican a 1996. Inmunologa. Fundamentos Roitt, I M, Delves, P J, 10a Edicin, Editorial Mdica Panamericana, 2003. Pruebas Bioqumicas para la Identificacin de Bacterias de Importancia Clnica
MacFaddin 3ra Edicin, Editorial Mdica Panamericana, 2003.
77
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
MICROBIOLOGA BSICA INTERNET
www.hardydiagnostics.com/.../MacConkeyAgar.htm www.geocities.com/.../microbiologia.html www.biofilmsonline.com/cgi-bin/biofilmsonline... users.stlcc.edu/kkiser/biochem.html http://aulavirtual.usal.es/aulavirtual/demos/microbiologia/unidades/documen/uni_02/58/textht ml/cap804.htm http://www.rlc.dcccd.edu/mathsci/reynolds/micro/lab_manual/water.html http://www.jlindquist.net/generalmicro/102diff.html
MICROBIOLOGA CLNICA INTERNET
escuela.med.puc.cl/.../Laboratorio06.html http://mx.geocities.com/urtis_micro/sesiones/Gram.htm universitas.usal.es/.../Demo1/shigella.html www.ispch.cl/lab_amb/serv_lab/salmonella.html faculty.mc3.edu/jearl/ML/ml-10.htm faculty.mc3.edu/jearl/ML/ml-8.htm medicine.ucsd.edu/.../Translations/Spanish.html colombiamedica.univalle.edu.co/VOL30NO4/urina...
MICROBIOLOGA ALIMENTARIA INTERNET
http://biology.clc.uc.edu/fankhauser/Labs/Microbiology/Meat_Milk/Pour_Plate.htm http://cienciasbiologicas.uniandes.edu.co/lema/nodo.php?id=111 http://biology.clc.uc.edu/fankhauser/Labs/Microbiology/Dilutions.htm http://www.respyn.uanl.mx/vii/2/articulos/quesos_frescos-1.htm http://www3.unileon.es/personal/wwdhtmpm/programa.htm www.ciad.mx/.../servicios/bacteriologia.htm
MICROBIOLOGA INDUSTRIA FARMACUTICA Y COSMTICA INTERNET
http://www.bact.wisc.edu/Microtextbook/index.php?module=Book&func=toc&book_id=3 www.vet.unicen.edu.ar/Tecnologia/TP5.htm http://www.vet.unicen.edu.ar/Tecnologia/TP2.htm http://www.ucv.ve/Farmacia/Micro_web/Catedras02/GuiaMicroCosm2004.pdf
78
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
ANEXO III: ESQUEMA DE RESULTADOS DE MICROBIOLOGA APLICADA
79
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
DILUCIONES Y DILUYENTES. HOMOGENIZACION
1.- Pesaje de la muestra Se pesan 10g del alimento
2.- Homogenizacin de la muestra Se licuan 10g del alimento en 90 ml de peptona 0.1%
3.- Diluciones seriadas Se hacen diluciones pasando 1ml a 9ml de peptona 0.1%
4.- Diluyentes Frasco con Vortex Antes de sembrar 90 ml peptona 0.1% o y al hacer diluciones se Solucin salina estril debe homogenizar
RECUENTO EN PLACA DE AEROBIOS MESOFILOS (RAM)
4. Servir el medio Se sirven aproximadamente 20ml y se homogenizan con el inoculo haciendo forma de 8 suavemente en ambas direcciones. Luego se deja solidificar y se lleva a incubar.
1. Siembra en fondo Se toma 1ml de la dilucin a sembrar
2. Colocar inoculo, Se coloca el inoculo en una caja estril
3. Medio SPC (Standard Plate Count Agar, Se alista el medio caliente
5. Recuento Despus de incubar 48h a 37C Se hace el recuento en ufc/ml
6. RAM Se observan colonias de diferentes morfologias.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RECUENTO EN PLACA DE COLIFORMES TOTALES Y E. coli
1. Coliformes en VRBA La muestra se procesa igual que en RAM. El medio empleado es el Violeta Rojo Bilis Agar. Se observan colonias coliformes color fucsia rojizo.
3. Serie diluciones Se observa una serie de diluciones de coliformes totales. La primera caja vir a amarillo debido a la alta produccin de cido en el medio por la poblacin numerosa de coliformes
2. Diluciones en VRBA Se observan colonias coliformes (Fucsia-violeta) y no coliformes (rosadas claras).
4. Serie diluciones Se observan la distribucin homognea de la muestra, y la congruencia de las diluciones
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RECUENTO DE HONGOS Y LEVADURAS
La muestra se procesa igual que para RAM y recuento de coliformes. El medio que se emplea es el Papa dextrosa Agar acidificado con cido tartrico, el cual inhibe el crecimiento de las bacterias. Se siembra en fondo en PDA
1. Diluciones en PDA Se observa el crecimiento de hongos y levaduras en PDA 2. Hongos en Dilucin 10(-2) Recuento de hongos: 1*10(2) ufc/g ml Recuento de levaduras:<100 ufc/g ml
3. Hongos en PDA Diversidad fngica
4. Levaduras en PDA
RECUENTO DE Staphylococcus aureus COAGULASA POSITIVO
1. Diluciones en Baird Parker S. aureus, por ser telurito positivo origina unas colonias negras. Se siembran las diluciones en superficie del medio ya solidificado (0.1ml)
2. Halos Se observan las colonias negras con los halos opacos de liplisis, y los halos claros de protolisis tpicos de S. aureus.
3. DNAsa Se observa una prueba positiva (Arriba, S. aureus) y negativa (Abajo, S. epidermidis), despus de adicionar HCl 1N al DNAsa agar crecido.
4. Staphylococcus aureus Observe el viraje del medio a amarillo debido a la produccin de cido a partir de la degradacin del manitol. Las colonias negras se deben a la reduccin de telurito
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
DETECCIN DE Salmonella spp
1. Preenriquecimiento no selectivo Se incuban 25g de la muestra en 225ml de peptona 1% por 24h a 37C
2. Enriquecimiento selectivo Se pasa 1ml del caldo de preenriquecimiento a un tubo con 10ml de caldo Rappaport, y se incuba a 44C en bao mara por 24h.
3. Siembra por aislamiento Se siembra por aislamiento en medio selectivos y diferenciales para Salmonella spp. 4. Salmonella en XLT Obsrvese las colonias negras sulfuro +. El medio se observa similar al XLD.
5. Salmonella en Agar Cromognico Las colonias moradas tpicas de Salmonella
6. Salmonella en Bismuto Sulfito Observe las colonias negras tpicas de Salmonella
7. Salmonella en Hektoen Observe la colonia negra verdosa tpica de Salmonella
8. Salmonella-Shigella Agar Observe las colonias lactosa negativa y sulfuros + tpicas de salmonella (Negras con borde transparente)
9. Coliformes y Salmonella XLT Observe la diferencia entre coliformes (lactosa+) y Salmonella (Lactosa-)
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
NUMERO MAS PROBABLE CALDO BILIS VERDE BRILLANTE
2. Crecimiento coliformes Se observa la turbidez, y solo el tercer tubo es positivo para coliformes porque presenta produccin de gas en la campana
3. No Coliformes Aunque se observa turbidez en los tres tubos, no hay coliformes porque no hay produccin de gas en la campana
4. Confirmacin Todos los tubos que den positivos se deben confirmar en Eosin Methylene Blue (EMB) agar. Se observa el brillo metlico tpico de E. coli.
1. CBVB Este medio se debe preparar siempre con campana de durham, la cual debe quedar sin aire para poder detectar la fermentacin de la lactosa con produccin de gas por parte de los coliformes
DETECCION DE Vibrio cholerae
2. Aislamiento Se hace pase por aislamiento en Tiosulfato Citrato Sales Biliares Sacarosa (TCBS) agar y se incuba a 37C por 24 horas
1. Enriquecimiento 25 g del alimento en 225ml de peptona alcalina y se incuban a 37C por 6 horas
3. TCBS Se observan las colonias amarillas, pequeas, sacarosa positivas en el medio TCBS. Se debe confirmar con pruebas bioqumicas al menos 3 colonias.
4. Oxidasa Se pasan 3 colonias a Agar nutritivo para hacer pruebas bioqumicas. Vibrio cholerae es oxidasa positiva (derecha). A la izquierda se muestra un control negativo
5. Azucares Se muestran los azucares, glucosa positivo y sacarosa positivo en medio rojo de fenol el cual vira a amarillo con los cidos producto de la degradacin de las mismas. A la derecha se muestra el tubo control
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
COSMETICOS Y FARMACOS
1. Cosmticos y Frmacos Se analizan Productos Cosmticos y Frmacos para realizar anlisis microbiolgicos. Es importante recordar que para productos grasos como cremas es necesario que el agua peptonada al 0.1% donde se realizar la dilucin contenga Tween 80 al 1% para emulsionar la grasa 3. Toma de la Muestra Se toman 10g o ml de la muestra para realizar diluciones 5. Muestra Homogenizada 7. Siembra en Fondo
2. Desinfeccin Es muy importante desinfectar el envase antes de analizarlo, con Alcohol
2b. Desinfeccin
8. Medio de Cultivo
4. Homogenizacin de la muestra
6. Siembra en Fondo Se procede a sembrar en fondo o en superficie, dependiendo del tipo de anlisis a realizar (Recuento de Aerobios mesfilos, Coliformes Totales, Escherichia coli, Hongos y Levaduras, Bacillus cereus, etc.)
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
CONTROL DE AMBIENTES; SUPERFICIES; OPERARIOS
1. Prueba de Ambientes Se expone una caja abierta de SPC y otra de PDA en el ambiente por 15 minutos. Luego se incuba SPC 48horas a 37C y PDA 5 das a 25C. 3. RODAC La caja RODAC puede prepararse con SPC para aerobios mesfilos y PDA para hongos y levaduras. Se muestrea la superficie por contacto del medio con la misma
2. Hisopado Se muestrea la superficie con un hisopo estril, el cual se humedece en solucin rinse y se pasa por la superficie. Este hisopo se introduce en la solucin rinse y se transporta al laboratorio para su anlisis.
4. RODAC SPC Se observa el crecimiento de aerobios mesfilos
5. RODAC PDA Se observa el crecimiento de Hongos. 6. AMBIENTES SPC Se observa el crecimiento de aerobios mesfilos
7. AMBIENTES PDA Se observa el crecimiento de hongos y levaduras.
8. MANOS Sobre la superficie de Violeta Rojo Bilis Agar se presionan las yemas de los dedos para enumerar coliformes totales. Se incuba la caja a 37C por 24 horas.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
ANLISIS MICROBIOLGICO DEL AGUA
Placa Agar Plate Count 1 Placa 2
10-2
10-3
10-4
10-5
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RESULTADOS TPICOS DEL CRECIMIENTO EN CALDO LAURIL SULFATO TRIPTONA
RESULTADOS TPICOS DEL CRECIMIENTO EN CALDO VERDE BRILLANTE BILIS LACTOSA
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
TABLA DEL MPN EN ESTA TABLA SE CALCULA EL MPN USANDO 3 TUBOS POR DILUSIN
N DE LOS TUBOS POSITIVOS ADENTRO Primero Medio ltimo MPN 0 0 0 <0> 0 0 1 0.03 0 0 2 0.06 0 0 3 0.09 0 1 0 0.03 0 1 1 0.061 0 1 2 0.092 0 1 3 0.12 0 2 0 0.062 0 2 1 0.093 0 2 2 0.12 0 2 3 0.16 0 3 0 0.094 0 3 1 0.13 0 3 2 0.16 0 3 3 0.19 1 0 0 0.036 1 0 1 0.072 1 0 2 0.11 1 0 3 0.15 1 1 0 0.073 1 1 1 0.11 1 1 2 0.15 1 1 3 0.19 1 2 0 0.11 1 2 1 0.15 1 2 2 0.5 1 2 3 0.24
NO DE LOS TUBOS POSITIVOS ADENTRO Primero Medio ltimo MPN 2 0 0 0.091 2 0 1 0.14 2 0 2 0.20 2 0 3 0.26 2 1 0 0.15 2 1 1 0.20 2 1 2 0.27 2 1 3 0.34 2 2 0 0.21 2 2 1 0.28 2 2 2 0.35 2 2 3 0.42 2 3 0 0.29 2 3 1 0.36 2 3 2 0.44 2 3 3 0.53 3 0 0 0.23 3 0 1 0.39 3 0 2 0.64 3 0 3 0.95 3 1 0 0.43 3 1 1 0.75 3 1 2 1.2 3 1 3 1.6 3 2 0 0.93 3 2 1 1.5 3 2 2 2.1 3 2 3 2.9
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
RESULTADOS TPICOS DEL CRECIMIENTO EN EL CALDO E. COLI
Agar EMB se aprecia las tpicas colonias de E. coli y las colonias de Enterobacter que se asemeja al ojo de un pescado.
Mg. Q.F. HCTOR VILCHEZ CCEDA
UNIVERSIDAD INCA GARCILASO DE LA VEGA FACULTAD DE CIENCIAS FARMACUTICAS Y BIOQUMICA
Mg. Q.F. HCTOR VILCHEZ CCEDA
Anda mungkin juga menyukai
- Syllabus Microbiologia ClinicaDokumen63 halamanSyllabus Microbiologia ClinicaSINTHIA COLQUE MAMANIBelum ada peringkat
- Manual de Bioseguridad en El LaboratorioDokumen167 halamanManual de Bioseguridad en El LaboratoriodivatiemiBelum ada peringkat
- Instrumentación y laboratorio. Manual de procedimientos básicosDari EverandInstrumentación y laboratorio. Manual de procedimientos básicosPenilaian: 3 dari 5 bintang3/5 (1)
- Manual de Intro Edc 2013Dokumen80 halamanManual de Intro Edc 2013Luisa L. Berríos0% (1)
- Guia de Practicas de Microbiologia 2019 1Dokumen89 halamanGuia de Practicas de Microbiologia 2019 1Priscila Castillo SilvaBelum ada peringkat
- Dr. Antonio-Manual Practico de Micro 2016-17Dokumen234 halamanDr. Antonio-Manual Practico de Micro 2016-17Otto Alchundia Garcia100% (1)
- Laboratorio HematologicoDokumen66 halamanLaboratorio Hematologicobrenda100% (1)
- Rol de Laboratorio Clínico en Salud PublicaDokumen3 halamanRol de Laboratorio Clínico en Salud PublicaJulioInca100% (1)
- Manual de Laboratorio de Microbiología UcDokumen64 halamanManual de Laboratorio de Microbiología UcJuan Gerardo Villalobos Chávez100% (1)
- Manual de Procedimientos BacteriologicosDokumen85 halamanManual de Procedimientos BacteriologicosAdán SalazarBelum ada peringkat
- Practicas MicrosDokumen55 halamanPracticas MicrosDrJaime R Rojas0% (1)
- Manual Bioquímica General 2015Dokumen50 halamanManual Bioquímica General 2015Mario de la RosaBelum ada peringkat
- Manual BacterIIDokumen67 halamanManual BacterIIDiego Omar Perez CardenasBelum ada peringkat
- Tesis ParasitosisDokumen121 halamanTesis ParasitosisESTEFANY GYTZEL MARTINEZ ATAUCUSI100% (1)
- Silabo Extraccion y Recolec MBHDokumen5 halamanSilabo Extraccion y Recolec MBHJL TPBelum ada peringkat
- Manual de Bioquimica Clinica-HgjDokumen94 halamanManual de Bioquimica Clinica-HgjAdolfo Diaz Ginez100% (1)
- Uroanálisis y determinación de urea en suero sanguíneoDokumen10 halamanUroanálisis y determinación de urea en suero sanguíneoJacmy JulietBelum ada peringkat
- Manual procedimientos urocultivosDokumen69 halamanManual procedimientos urocultivosFernando Aiquipa ZavalaBelum ada peringkat
- Manual Toma y Transporte de Muestra Corregido OkDokumen26 halamanManual Toma y Transporte de Muestra Corregido OkafroditomanBelum ada peringkat
- Análisis de heces: examen coprológicoDokumen12 halamanAnálisis de heces: examen coprológicoJessi Salinas0% (1)
- TEORÍA ESTUDIO DE LOS LEUCOCITOS. LEUCOPOYESIS Semana 7Dokumen37 halamanTEORÍA ESTUDIO DE LOS LEUCOCITOS. LEUCOPOYESIS Semana 7KelletCadilloBarruetoBelum ada peringkat
- DilucionesDokumen15 halamanDilucionesClaudia FariaBelum ada peringkat
- Practicas de Laboratorio Bioanalisis 2013 PDFDokumen127 halamanPracticas de Laboratorio Bioanalisis 2013 PDFSamanthaVillegasBelum ada peringkat
- Protozoos Flagelados (Zoomastigophoros Intestinales)Dokumen25 halamanProtozoos Flagelados (Zoomastigophoros Intestinales)José Gustavo Gaitán FloresBelum ada peringkat
- Guía Práctica de BioquímicaDokumen75 halamanGuía Práctica de BioquímicaDiego MendozaBelum ada peringkat
- Medios de Cultivo y Pruebas BioquimicasDokumen83 halamanMedios de Cultivo y Pruebas Bioquimicasclubdelquimico.blogspot.com100% (25)
- Coprocultivo, Pruebas Bioquimicas para EnterobacteriasDokumen12 halamanCoprocultivo, Pruebas Bioquimicas para EnterobacteriasReyna Quispe MantaríBelum ada peringkat
- Practica 11 - Identificacion de Estafilococo y EstreptococosDokumen13 halamanPractica 11 - Identificacion de Estafilococo y EstreptococosJean Pierre Gomez ArotomaBelum ada peringkat
- TincionesDokumen52 halamanTincionesmarta hdezBelum ada peringkat
- 6 TiroidesDokumen27 halaman6 TiroidesEdgar Ruiz RojasBelum ada peringkat
- Diagnostico BacteriologicoDokumen109 halamanDiagnostico BacteriologicoEricj RodríguezBelum ada peringkat
- Clostridiun Sulfito Reductor en AlimentosDokumen30 halamanClostridiun Sulfito Reductor en AlimentosTania Tarifa RamirezBelum ada peringkat
- Biodiversidad peruana: oportunidades de trabajo y desarrollo sostenibleDokumen2 halamanBiodiversidad peruana: oportunidades de trabajo y desarrollo sostenibleJuan Ernesto Messa RojasBelum ada peringkat
- LeucemiaDokumen15 halamanLeucemiaLesterLopezBelum ada peringkat
- Batería de Pruebas Bioquímicas para Identificación de MicroorganismosDokumen75 halamanBatería de Pruebas Bioquímicas para Identificación de MicroorganismosAlejandra Rivera100% (1)
- 2015 2 GuÃ-A FarmacologÃ-A IDokumen56 halaman2015 2 GuÃ-A FarmacologÃ-A IMilaVargasBelum ada peringkat
- Quimica Clinica 1 PDFDokumen2 halamanQuimica Clinica 1 PDFMiguel Angel Flores Gutierrez100% (1)
- Diseno Curricular Tec en Laboratorio ClinicoDokumen40 halamanDiseno Curricular Tec en Laboratorio ClinicoRodrigo Pacheco Salas100% (1)
- Determinación de GlucosaDokumen12 halamanDeterminación de GlucosaraphaelBelum ada peringkat
- Laboratorio clínico UNAMDokumen48 halamanLaboratorio clínico UNAMEnrique Dirzo MartinezBelum ada peringkat
- Manual de Microbiologia I Medicina 2014 PDFDokumen99 halamanManual de Microbiologia I Medicina 2014 PDFAlexander Cruz100% (1)
- Hemograma 2015Dokumen101 halamanHemograma 2015jona_spBelum ada peringkat
- Practica 3 Medios de Cultivo. COMPLETODokumen14 halamanPractica 3 Medios de Cultivo. COMPLETOErendira Medina100% (1)
- Exudado vaginal: diagnóstico microbiológicoDokumen5 halamanExudado vaginal: diagnóstico microbiológicoAna Encinas100% (1)
- HEMOCULTIVOSDokumen25 halamanHEMOCULTIVOSsaida martinezBelum ada peringkat
- Toma de muestras y análisis in-situ. QUIE0108Dari EverandToma de muestras y análisis in-situ. QUIE0108Belum ada peringkat
- Guía Lab BioMol NormasDokumen3 halamanGuía Lab BioMol NormasGisella QuimiBelum ada peringkat
- Técnicas cinéticas de análisis clínicoDokumen3 halamanTécnicas cinéticas de análisis clínicokatheryn pilco100% (1)
- Lectura S3Dokumen13 halamanLectura S3Patricia Correa CanoBelum ada peringkat
- Manual de Practicas Bioquimica Clinica EspecializadaDokumen99 halamanManual de Practicas Bioquimica Clinica Especializadaoswpar252Belum ada peringkat
- Descripción Física y Uso de La MicropipetaDokumen2 halamanDescripción Física y Uso de La MicropipetaMay BeeBelum ada peringkat
- Pruebas de Shigella y ....Dokumen13 halamanPruebas de Shigella y ....MaritzaBelum ada peringkat
- VACUTAINERDokumen19 halamanVACUTAINERBen CoaritaBelum ada peringkat
- Manual Bioquímica PrácticaDokumen291 halamanManual Bioquímica PrácticaCarlos Romell Cortez ZambranoBelum ada peringkat
- BACILOSDokumen38 halamanBACILOSkynoysFroBelum ada peringkat
- Guía práctica de procedimientos en microbiología médicaDokumen103 halamanGuía práctica de procedimientos en microbiología médicaRosa Maria Mosqueda VazquezBelum ada peringkat
- Exámen Coprológico 1Dokumen4 halamanExámen Coprológico 1Kevin FloresBelum ada peringkat
- Sistema evaluación UASD MicrobiologíaDokumen4 halamanSistema evaluación UASD MicrobiologíaAmaurys OzpereyrBelum ada peringkat
- Iv CmbpiDokumen4 halamanIv CmbpiCarlos AlvaradoBelum ada peringkat
- Unah Cifar Informe Practica Revisiã - N #3Dokumen45 halamanUnah Cifar Informe Practica Revisiã - N #3Andrea FerreraBelum ada peringkat
- Manual de CalidadDokumen10 halamanManual de CalidadEdgar Condori Mendoza100% (4)
- Formato A 2015Dokumen5 halamanFormato A 2015Edgar Condori MendozaBelum ada peringkat
- Estableciendo Límites de Aceptación en La Validación de Limpieza de Formulaciones TópicasDokumen10 halamanEstableciendo Límites de Aceptación en La Validación de Limpieza de Formulaciones Tópicasjljimenez1969100% (3)
- 2 Charla Validaciones FINDokumen57 halaman2 Charla Validaciones FINEdgar Condori MendozaBelum ada peringkat
- Problemas Propuestos de Conteo de Figuras II Ccesa007Dokumen3 halamanProblemas Propuestos de Conteo de Figuras II Ccesa007Demetrio Ccesa Rayme67% (3)
- Calculo de Ld50Dokumen13 halamanCalculo de Ld50carbouBelum ada peringkat
- II Validación de Limpieza PDFDokumen129 halamanII Validación de Limpieza PDFMatias OliveraBelum ada peringkat
- Taller 3 Secuencias Graficas PDFDokumen2 halamanTaller 3 Secuencias Graficas PDFEdgar Condori MendozaBelum ada peringkat
- C 0 MPTWKRKHVWTDVBKXWFDokumen1 halamanC 0 MPTWKRKHVWTDVBKXWFEdgar Condori MendozaBelum ada peringkat
- Medina RH PDFDokumen101 halamanMedina RH PDFfelipemolinajBelum ada peringkat
- Articulo Validacion de Limpieza en La Industria Farmaceutica (Ii) PDFDokumen2 halamanArticulo Validacion de Limpieza en La Industria Farmaceutica (Ii) PDFEdgar Condori Mendoza100% (1)
- Articulo Validacion de Limpieza en La Industria Farmaceutica (III)Dokumen2 halamanArticulo Validacion de Limpieza en La Industria Farmaceutica (III)Jainer Cogollo RojasBelum ada peringkat
- Justificación de Límites para Validación de Limpieza en La Fabricación de Ingredientes ActivosDokumen8 halamanJustificación de Límites para Validación de Limpieza en La Fabricación de Ingredientes Activosjljimenez1969100% (3)
- Validacion Agua Grado FarmaceuticoDokumen134 halamanValidacion Agua Grado FarmaceuticoManuel Gutierrez100% (3)
- Articulo Validacion de Limpieza en La Industria Farmaceutica (I)Dokumen3 halamanArticulo Validacion de Limpieza en La Industria Farmaceutica (I)Miguel VeraBelum ada peringkat
- Draft Guideline Quality Water Pharmaceutical Use en - En.esDokumen10 halamanDraft Guideline Quality Water Pharmaceutical Use en - En.esEdgar Condori MendozaBelum ada peringkat
- Tesis 430Dokumen117 halamanTesis 430Miguel Angel Rubiol GarciaBelum ada peringkat
- Calificacion y Validacion Del Sistema de Tratamiento de Agua Purificada Ro2-Cedi 400L-hDokumen118 halamanCalificacion y Validacion Del Sistema de Tratamiento de Agua Purificada Ro2-Cedi 400L-hEdgar Condori MendozaBelum ada peringkat
- Buenas Practicas de Manofactura de La Oms: Agua para Uso FarmaceuticoDokumen25 halamanBuenas Practicas de Manofactura de La Oms: Agua para Uso FarmaceuticoRaúl Inés Delgadillo80% (5)
- Ficha Tecnica Exquat 50Dokumen5 halamanFicha Tecnica Exquat 50Edgar Condori MendozaBelum ada peringkat
- 12-12 Agua para Inyeccion PDFDokumen5 halaman12-12 Agua para Inyeccion PDFCeCromBelum ada peringkat
- Presentacion BPMDokumen315 halamanPresentacion BPMEdgar Condori Mendoza0% (1)
- 6.1.300.purified-Water - (Aqua-Purificata) The International Pharmacopoeia - Eighth Edition, 2018.en - EsDokumen1 halaman6.1.300.purified-Water - (Aqua-Purificata) The International Pharmacopoeia - Eighth Edition, 2018.en - EsEdgar Condori MendozaBelum ada peringkat
- Lejía Sapolio hoja seguridadDokumen2 halamanLejía Sapolio hoja seguridadLucii Alquizar89% (9)
- 39 Diarrea Aguda de Naturaleza InfecciosaDokumen14 halaman39 Diarrea Aguda de Naturaleza InfecciosaRina DiazBelum ada peringkat
- Indice Combinado USP42-ESPDokumen98 halamanIndice Combinado USP42-ESPEdgar Condori MendozaBelum ada peringkat
- Intro Metabolismo BioenergéticaDokumen44 halamanIntro Metabolismo BioenergéticaFidelcito LuyoBelum ada peringkat
- Industria FarmaceúticaDokumen20 halamanIndustria FarmaceúticaLeticia SanchezBelum ada peringkat
- Manual BPMDokumen107 halamanManual BPMJdaniel Gzr100% (1)
- Guía Sobre Seguridad de en El Muestreo de Suelos PDFDokumen5 halamanGuía Sobre Seguridad de en El Muestreo de Suelos PDFMaría Clau KerguelénBelum ada peringkat
- Manual de MicrobiologiaDokumen5 halamanManual de MicrobiologiaSUGEILY NATALI MORALES LOPEZBelum ada peringkat
- Biorremediación de PesticidasDokumen16 halamanBiorremediación de PesticidasDeimanuel QRBelum ada peringkat
- Genética Aplicaciones IIDokumen37 halamanGenética Aplicaciones IIrubenecar 7Belum ada peringkat
- Clase 3 Relacion Hospedante Patogeno PDFDokumen63 halamanClase 3 Relacion Hospedante Patogeno PDFStefania LizbethBelum ada peringkat
- Capacitación PiscinasDokumen80 halamanCapacitación PiscinasJuan CarlosBelum ada peringkat
- Monera, Protista, FungiDokumen2 halamanMonera, Protista, FungiBryan AnmoBelum ada peringkat
- La CélulaDokumen4 halamanLa CélulaDani Villa ValdebenitoBelum ada peringkat
- Muerte Microbiana Por Agentes Fisicos y QuimicosDokumen8 halamanMuerte Microbiana Por Agentes Fisicos y QuimicosIvanna Andrea CharrisBelum ada peringkat
- Ficha Tecnica Germicin Rev 02-2019Dokumen2 halamanFicha Tecnica Germicin Rev 02-2019walterejaBelum ada peringkat
- Vocabulario de Términos AgronómicosDokumen21 halamanVocabulario de Términos AgronómicosJuan Tizcareño Iracheta73% (11)
- ¿Cuáles Son Los Seis Reinos de La Vida y Cómo Son Identificados?Dokumen5 halaman¿Cuáles Son Los Seis Reinos de La Vida y Cómo Son Identificados?Ricardo Martinez RivadeneiraBelum ada peringkat
- Introduccion Al Potencial RedoxDokumen8 halamanIntroduccion Al Potencial RedoxGero Onofre MogollonBelum ada peringkat
- "Las Bacterias"-Luz Rosaly Velasquez LaymeDokumen33 halaman"Las Bacterias"-Luz Rosaly Velasquez LaymeKatherine alexandra CONDORI QUISPEBelum ada peringkat
- Determinación del pH salival y su relación con la placa bacteriana en pacientes odontológicosDokumen5 halamanDeterminación del pH salival y su relación con la placa bacteriana en pacientes odontológicosSamara Calicho RiosBelum ada peringkat
- Manual de Crianza de Tilapia PDFDokumen49 halamanManual de Crianza de Tilapia PDFivan arango mierBelum ada peringkat
- Capacitación Medicamentos y DesinfectantesDokumen20 halamanCapacitación Medicamentos y DesinfectantesJuan Jose RodriguezBelum ada peringkat
- Catalogo MicroDokumen4 halamanCatalogo MicroAdriian FSBelum ada peringkat
- Práctica 22 Evelyn Ávila - Fisio MicrobianaDokumen5 halamanPráctica 22 Evelyn Ávila - Fisio MicrobianaEve Gabi AvilaBelum ada peringkat
- Curar Con ImanesDokumen6 halamanCurar Con ImanesVíctor Eduardo Silva MuñozBelum ada peringkat
- 1a - PROBLEMAS DE APLICACI N-SeparablesDokumen4 halaman1a - PROBLEMAS DE APLICACI N-SeparablesJohn Harol Giraldo100% (5)
- Inmunología ForenseDokumen14 halamanInmunología ForenseJesus TinoBelum ada peringkat
- Crecimiento Bacteriano en Medios de Cultivos Específicos y Su Influencia Del Medio AmbienteDokumen8 halamanCrecimiento Bacteriano en Medios de Cultivos Específicos y Su Influencia Del Medio AmbienteSirvió100% (1)
- Expo MicroDokumen12 halamanExpo Microivonne judexBelum ada peringkat
- Bacterias NotarioDokumen3 halamanBacterias Notariojoaquín dunxBelum ada peringkat
- Micobiologia ResumenDokumen9 halamanMicobiologia ResumenKamila Andrea Araya BelloBelum ada peringkat
- Practica #2 Tincion Diferencial y SimpleDokumen18 halamanPractica #2 Tincion Diferencial y SimpleAnonymous 4QwqDhLRrR100% (1)
- V4UDOAg PDFDokumen118 halamanV4UDOAg PDFRenny RincónBelum ada peringkat
- Ser y Actuar - Stefan Lanka. Virólogos Estafadores Científicos (13-02-21) (12P) (Copia)Dokumen12 halamanSer y Actuar - Stefan Lanka. Virólogos Estafadores Científicos (13-02-21) (12P) (Copia)serapbeyBelum ada peringkat
- Consolidado Parcial T. FDokumen12 halamanConsolidado Parcial T. FJosé María Rosero VallejoBelum ada peringkat