Libro Quimica y Textiles PDF
Diunggah oleh
Jose LimachiJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Libro Quimica y Textiles PDF
Diunggah oleh
Jose LimachiHak Cipta:
Format Tersedia
1.
TALLERES DE DE CIENCIAS CIENCIAS TALLERES QUMICA Y Y COLOR COLOR EN EN LOS LOS TEXTILES TEXTILES QUMICA
00 | 01
EDITORIAL
Antes de que te sumerjas en el mundo de la qumica, queremos contarte que este libro se origin a partir del taller La qumica y el color en los textiles, a cargo de Marta Maier y Mara dos Santos Afonso, que se lleva adelante en el marco del Programa Talleres de Ciencia organizado por la DOV-Exactas. La idea de este programa es vincular a estudiantes de los ltimos aos de la escuela media con el campo de la ciencia y la tecnologa en el mbito universitario, dandoles a conocer, en el mbito real del quehacer cientfico, el mundo universitario y el trabajo de los investigadores. Para eso, actualmente estamos llevando a cabo siete talleres cuyos contenidos estn relacionados con las distintas carreras que ofrece la Facultad; entre ellas, la Licenciatura en Ciencias Qumicas. La Qumica no es slo una asignatura de la escuela, o una temtica presente en los laboratorios, sino que forma parte de toda nuestra vida cotidiana: en lo que cocinamos, en la ropa que vestimos, en los materiales de los objetos que nos rodean. Es, adems, una disciplina que ofrece amplias posibilidades a quienes quieran dedicarse tanto a la investigacin como a la tecnologa. En particular, en los Talleres de Ciencia intentamos recrear la manera en la que los cientficos trabajan habitualmente; es decir, planteando problemas, ensayando hiptesis, cuestionando resultados, experimentando. Y con este libro pretendemos acercar y compartir la experiencia de asomarse a la realidad a travs de la mirada de la ciencia.
CLAUDIA ZELZMAN | Direccin de Orientacin Vocacional | Facultad de Ciencias Exactas y Naturales - UBA
AL AL QUE QUE QUIERE QUIERE CELESTE CELESTE
MARA DOS SANTOS AFONSO Licenciada en Ciencias Qumicas de la Facultad en Ciencias Exactas y Naturales de la Universida de Buenos Aires. Doctora en Qumica en la Universidad Nacional de La Plata. Desde 1992 es Profesora Adjunta regular con dedicacin exclusiva del Departamento de Qumica Inorgnica, Analtica y Qumico-Fsica de la FCEN-UBA. Dirige un grupo de investigacin en Qumica de los Contaminantes de Aguas Naturales y Suelos. MARTA MAIER Licenciada en Ciencias Qumicas en la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires. Doctora en Ciencias Qumicas en la FCEyN-UBA. Es Profesora Asociada (FCEyN, UBA) e Investigadora Independiente (CONICET) en el Departamento de Qumica Orgnica (FCEyN, UBA). Sus temas de investigacin comprenden el estudio de productos naturales marinos y el anlisis de materiales en objetos artsticos y arqueolgicos. EL EDITOR // GABRIEL STEKOLSCHIK Periodista, bioqumico y Master en Comunicacin Cientfica de la Universidad Pompeu Fabra de Barcelona, Espaa. Integra el Centro de Divulgacin Cientfica de la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires y es docente de Periodismo Cientfico y de Prctica Profesional de Radio de la Universidad CAECE.
2.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
02 | 03
A M ME GUSTA EL AZUL. SIN EMBARGO ELLA PREFIERE EL VERDE.
Estamos eligiendo pantalones, y no nos ponemos de acuerdo sobre cul es el ms lindo. Si todas las cosas tuvieran el mismo color, esta discusin no existira. Sencillamente, porque no tendramos la posibilidad de elegir. Y tal vez todo sera ms fcil pero, tambin, muy aburrido. Quizs, entre otros motivos, haya sido para matar el aburrimiento que el hombre siempre ha tenido necesidad de darle color a las cosas. De hecho, las primeras civilizaciones ya usaban colorantes naturales, extrados de plantas, animales y minerales, para colorear el cuerpo, pintar utensilios y objetos religiosos, y teir la ropa. En efecto, el teido es un arte muy antiguo, que se practicaba en Egipto, Persia, China y la India hace miles de aos. Pero, lgicamente, en aquellos tiempos no se dispona de la variedad de colores con la que contamos actualmente. Hoy, por suerte, podemos elegir entre distintas gamas, tonos, y matices, gracias al amplio desarrollo que han tenido, a partir del siglo XIX, la industria de los colorantes y las tcnicas de teido. Y la principal responsable de todo este embrollo a la hora de elegir el color de nuestras prendas no es nada ms ni nada menos queLA QUMICA!
QU VAMOS A HACER EN
EL LABORATORIO?
AL QUE QUIERE CELESTE...
3.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
AL QUE QUIERE CELESTE
QU VAMOS A HACER EN EL LABORATORIO?
Vamos a hacer lo que hacen habitualmente los investigadores de la Facultad de Ciencias Exactas y Naturales: experimentos. Mediante la experimentacin, los cientficos intentan probar sus hiptesis acerca de cmo funciona la naturaleza. Por ejemplo, algunas de las personas que trabajan en qumica tratan de entender de qu manera se protegen algunos seres vivos de la accin de ciertos virus. Comprender ese proceso podra llevar a descubrir cules son las molculas involucradas en ese mecanismo de proteccin, y determinar la estructura qumica de las mismas. Ello, a su vez, podra ser til en el futuro para producir medicamentos antivirales. En nuestro caso, el objetivo de los experimentos que vamos a realizar es tratar de establecer cul es la manera ms eficaz de teir diferentes tipos de fibras textiles* naturales (algodn, lana, seda) y sintticas (polister, nylon), con un pigmento que extraeremos de un insecto: la cochinilla. Pero como lo que buscamos es descubrir cul es el proceso de teido ms eficaz para cada tipo de fibra, trabajaremos tambin con ciertas sustancias que ayudan a fijar el color a la fibra, conocidas con el nombre de mordientes*. Estos compuestos qumicos no slo ayudan al colorante a unirse a la tela sino que, adems, influyen en la tonalidad del color. Por lo tanto, tambin evaluaremos el efecto que producen diferentes mordientes sobre la coloracin de las fibras. Obtendremos, como resultado, diferentes tonalidades de rojo como las que se observan en la figura.
3.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
04 | 05
Lana teida con cochinilla utilizando diferentes mordientes.
COLORANTES Y MORDIENTES
En definitiva, extraeremos el pigmento de la cochinilla, y prepararemos soluciones del colorante* y de los distintos mordientes, en diferentes concentraciones. Con ellas, probaremos cul es la mejor manera de teir cada tipo de fibra textil. Finalmente: Cmo mediremos la eficiencia del teido en cada caso? Determinando cules de las telas que coloreamos son las que menos destien, tanto en agua fra como en agua caliente: a menor desteido, mayor eficiencia del proceso.
* COLORANTES | SON SUSTANCIAS CAPACES DE TEIR LAS FIBRAS TEXTILES. PARA QUE UN COLORANTE SEA TIL, DEBE UNIRSE FUERTEMENTE A LA FIBRA, Y NO DEBE PERDER SU COLOR POR LAVADO, O POR ACCIN DE LA LUZ. * MORDIENTES | FACILITAN LA FIJACIN DEL COLORANTE A LA FIBRA. ACTUALMENTE SE UTILIZAN SALES SOLUBLES DE METALES (COMO ALUMINIO, COBRE, HIERRO Y ESTAO) COMO MORDIENTES. EL TIPO DE METAL DETERMINA LA TONALIDAD DEL COLOR. ADITIVOS | SI BIEN NO SON PROPIAMENTE MORDIENTES, AYUDAN A FIJAR EL COLOR. TAMBIN DAN SUAVIDAD Y BRILLO A LA FIBRA. ALGUNOS EJEMPLOS: VINAGRE, SAL, LIMN, CREMOR TRTARO.
* FIBRAS TEXTILES | SE PUEDEN CLASIFICAR EN SINTTICAS Y NATURALES. AMBOS TIPOS DE FIBRAS SON POLMEROS, ES DECIR, MACROMOLCULAS FORMADAS POR LA UNIN SUCESIVA DE MOLCULAS PEQUEAS DENOMINADAS MONMEROS. LAS FIBRAS SINTTICAS (POLISTER, NYLON) SE OBTIENEN POR SNTESIS QUMICA (REACCIN DE POLIMERIZACIN) A PARTIR DE MONMEROS SELECCIONADOS POR EL HOMBRE. LAS FIBRAS NATURALES DE ORIGEN VEGETAL (ALGODN, LINO) ESTN COMPUESTAS POR CELULOSA, UN POLISACRIDO QUE PRODUCEN LAS PLANTAS. EN TANTO QUE LAS FIBRAS NATURALES DE ORIGEN ANIMAL (LANA, SEDA) ESTN FORMADAS POR PROTENAS.
4.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
QU VAMOS A HACER EN EL LABORATORIO?
COLORANTES Y MORDIENTES
/// CARMIN O COCHINILLA
Es el colorante con el que trabajaremos, que se obtiene a partir de los cuerpos desecados de las hembras del insecto Dactylopius coccus Costa, popularmente conocido como cochinilla. El valor de este colorante ya era conocido por los aztecas antes de la conquista. All se lo llamaba nocheztli, que significa sangre de tunas, debido al color rojo del pigmento, y a que el insecto crece sobre las hojas de cierto gnero de cactus. Alrededor del ao 1525, los espaoles llevaron la cochinilla a Europa, en donde reemplaz gradualmente a un colorante rojo menos potente: el kermes. La gran demanda de la industria textil para el teido* de telas, especialmente aqullas destinadas a la vestimenta de eclesisticos y cortesanos, convirti entonces a la cochinilla en la especie comercial ms valiosa, luego del oro y la plata. El pigmento de color rojo intenso que produce este insecto es el cido carmnico, una sustancia polar y, por lo tanto, soluble en agua:
Estructura qumica del cido carmnico
HO2C O HO OH O OH OH CH 3 O OH CH2OH OH
HO
4.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
06 | 07
Cochinilla y cochinilla en mortero.
* EL TEIDO | EL TEIDO DE FIBRAS TEXTILES CON COLORANTES SE REALIZA EN UNA SOLUCIN ACUOSA DENOMINADA LICOR O BAO DE TEIDO. EL TEIDO VERDADERO SE PRODUCE SLO SI LA COLORACIN ES RELATIVAMENTE PERMANENTE, ES DECIR, SI NO ES REMOVIDA FCILMENTE CON AGUA O CON LOS PROCEDIMIENTOS
NORMALES DE LAVADO. MS AN, EL COLOR NO DEBE DESTEIRSE RPIDAMENTE POR EXPOSICIN A LA LUZ. MUCHAS PLANTAS Y ANIMALES PRODUCEN COMPUESTOS COLOREADOS, PERO SLO UN NMERO LIMITADO PUEDE SER UTILIZADO PARA TEIR TEXTILES DEBIDO A ESTAS RESTRICCIONES.
/// LOS MORDIENTES
El trmino mordiente es aplicado a cualquier sustancia de origen natural o sinttico que sirva para fijar el colorante a la fibra, de manera uniforme y estable al contacto con la luz y el agua. Antiguamente se empleaba para esa funcin a ciertos productos naturales como, por ejemplo, cenizas, hojas de palta, o cor-
COLORANTES Y MORDIENTES
El carmn o cochinilla tiene mayor afinidad por las fibras textiles de origen animal, como la lana y la seda. Para teir fibras de origen vegetal (algodn, por ejemplo) se requiere de una mayor cantidad de colorante y de un proceso de teido ms prolongado.
4.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
COLORANTES Y MORDIENTES
teza de nogal. Hoy en da se utilizan sales solubles de metales, como aluminio, cobre, hierro y estao. El mordentado de la fibra puede realizarse antes o despus del teido, y generalmente comprende el agregado del mordiente en agua caliente junto con la fibra. Los mordientes se usan en poca cantidad, para no daar la fibra. Utilizados en exceso pueden dejarla rgida y spera. Los mordientes tambin son utilizados para variar las tonalidades del color agregndolos en la parte final del teido.
ADVERTENCIA | SI NO SE TOMAN LAS MEDIDAS ADECUADAS, EL USO DE ESTE TIPO DE COMPUESTOS LLEVA
A LA CONTAMINACIN DE LOS CURSOS DE AGUA DEBIDO AL DESCARTE DE EFLUENTES QUE CONTIENEN METALES PESADOS.
/// CMO ACTA EL MORDIENTE?
Al colocarlo en el agua caliente, el mordiente se disuelve. En ese proceso, la sal se disocia, y el metal queda como catin metlico (in positivo). Entonces, el catin se une a la fibra textil, y forma un complejo con la molcula de colorante. El tipo de metal que forme parte del complejo determina la tonalidad del color. Es decir, para un mismo tipo de colorante y fibra, el agregado de distintos mordientes producir diferentes tonos o colores.
4.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
08 | 09
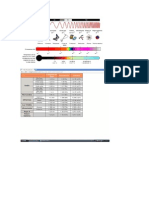
ESQUEMA DEL PROCESO
QU ES EL COLOR?
Cu
+
Al
Fe
grupo amino
grupo carboxilo
grupo sulfuro acido
grupo oxihidrilo
molcula de colorante mostrando el grupo hidroxilo
molcula de colorante mostrando el grupo carbonilo.
La secuencia de los grupos presentes en la superficie de la fibra es solo indicativa. A: colorante unido a la fibra sin mordentar B, C y D: colorante unido a la fibra con mordentado de sales de Cu, Al, o Fe a travs de grupos carboxilo, sulfuro u oxihidrilo
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
COLORANTES Y MORDIENTES
QU ES EL COLOR?
De qu hablamos cuando decimos que algo tiene color? El color en s no existe, no es una caracterstica de los objetos. En realidad, el color es una percepcin de nuestro sentido de la vista. Es una sensacin que se produce en respuesta a la estimulacin de la retina, un tejido que se encuentra en la parte interna del ojo, y que est conectado al nervio ptico. Qu es lo que produce esa estimulacin que nos hace ver colores? La energa de la luz.
/// LA LUZ ES ENERGA
La luz es radiacin electromagntica, es decir, es una combinacin de campos elctricos y magnticos, que se propagan a travs del espacio en forma de onda. Al igual que cualquier otra onda, la radiacin electromagntica puede ser caracterizada en trminos de su longitud de onda (distancia sucesiva entre dos ondas) y su amplitud (diferencia entre los picos mximos y mnimos), tal y como se ilustra en la // FIGURA 1.
// FIGURA 1
..........................................................> . .. ............................................................ .. ............................................................ . . .............................................................. . .............................................................. . . ............................................... . . ..................................... . . ........................... . ................. . ....
. .............. .............. . ........ ........
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
10 | 11
A su vez, las ondas electromagnticas tienen una frecuencia de oscilacin (nmero de ondas por unidad de tiempo), como se ilustra en la // FIGURA 2.
// FIGURA 2
QU ES EL COLOR?
Bajas frecuencias
+
Altas frecuencias
Como podemos deducir de los grficos anteriores, cuanto mayor es la longitud de onda (), menor es la frecuencia (). Es decir, la relacin entre ambas magnitudes es inversamente proporcional, de acuerdo con la siguiente ecuacin:
= c (1)
c=
VELOCIDAD DE LA LUZ . ES UN VALOR ( APROXIMADAMENTE 300.000 KM / S )
CONSTANTE
Por otra parte, la energa (E) de la radiacin electromagntica es directamente proporcional a su frecuencia (a mayor frecuencia, mayor energa, y viceversa):
= h (2)
h=
CONSTANTE DE PLANCK
(6,6260755 X 10 -34 J.s)
(J:Jouse)
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
QU ES EL COLOR?
De (1) y (2) deducimos que:
= hc
Por lo tanto, cuanto mayor longitud de onda tenga una radiacin electromagntica, menor ser su energa, y viceversa: a menor longitud de onda, mayor energa. De esta manera, los diferentes tipos de radiacin electromagntica conforman lo que se ha denominado espectro electromagntico. Como se observa en el esquema del especto electromagntico, nuestro sistema visual apenas es capaz de detectar una pequea parte del espectro electromagntico. As, la retina humana slo puede percibir ondas electromagnticas cuyas longitudes de onda estn, aproximadamente, entre los 400 y los 700 nm. En ese rango, el de la luz visible, estn comprendidos los colores. Por ejemplo, el violeta tiene ondas de entre 380 y 436 nm de longitud, el azul de 436 a 495 nm el verde de 495 a 566 nm el amarillo de 566 a 589 nm el naranja de 589 a 627 nm y el rojo de 627 a 770 nm. La suma de todos los colores es lo que se conoce como luz blanca. La separacin de la luz blanca en los colores que la conforman, que se observa, por ejemplo, durante el fenmeno del arco iris, recibe el nombre de descomposicin de la luz blanca.
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
12 | 13
ESPECTRO ELECTROMAGNTICO | DE ARRIBA HACIA ABAJO, SE OBSERVAN LAS ONDAS ELECTROMAGNTICAS EN ORDEN DECRECIENTE DE ENERGA. LOS RAYOS GAMMA, LOS MS ENERGTICOS, SON LOS QUE POSEEN
MAYOR FRECUENCIA, Y MENOR LONGITUD DE ONDA (MEDIDA EN NANOMETROS) UN NANOMETRO (NM) ES LA MILMILLONSIMA PARTE DE UN METRO (10 -9 M). UN MICROMETRO ( m) ES LA MILLONSIMA PARTE DE UN METRO (10-6 M).
QU ES EL COLOR?
Rayos Gamma
Rayos X Radiacin ultravioleta
400 nm
Luz visible Radiacin infraroja Microondas 700 nm
Ondas de radio
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
QU ES EL COLOR?
/// SI NO HAY LUZ, NO HAY COLOR
Para que un objeto se vea de color, debe estar iluminado por luz visible. Porque lo que nuestro sentido de la vista percibe es la luz que los objetos reflejan. Lo que ocurre cuando percibimos un objeto de un determinado color, es que la superficie de ese objeto absorbe determinadas partes del espectro de luz blanca que recibe, y refleja el resto. Entonces, nuestro sentido visual interpreta estas radiaciones electromagnticas que el objeto devuelve al entorno, como un color. As, si a una tela la vemos de color rojo, es porque las molculas de su superficie reflejan (o sea, no absorben) las ondas cuya longitud corresponde a la parte roja del espectro visible. Y si a otra tela la vemos verde, es porque devuelve radiaciones correspondientes al azul y el amarillo (que al mezclarse se ven verdes). De la misma manera, cuando a un objeto lo vemos negro, es porque absorbe todos los colores o, en otras palabras, no nos devuelve ninguna radiacin que est comprendida dentro del espectro de luz visible por nuestros ojos. Por otra parte, cuando la superficie de un objeto refleja todos los colores, es decir, no absorbe energa proveniente de la radiacin visible, lo vemos blanco. Por eso, se utiliza vestimenta de este color en los lugares calurosos y, por eso tambin, los camiones transportadores de productos alimenticios estn pintados generalmente de blanco, para reducir el calentamiento dentro de los mismos.
5.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
14 | 15
/// POR QU VEMOS LOS OBJETOS CON DISTINTOS COLORES?
El color de cada objeto depende de las molculas que componen su superficie. Porque, segn el tipo y la disposicin de sus tomos, cada molcula se comporta de manera diferente cuando se la ilumina. La parte de una molcula responsable del color, es decir, de la absorcin de determinadas longitudes de onda del espectro visible, se denomina cromforo. Son regiones moleculares que absorben selectivamente la energa de la luz visible. Los siguientes son algunos ejemplos de cromforos: Tambin, otros grupos de tomos de la molcula, llamados auxocromos, tienen influencia en la absorcin de luz visible y, junto con los cromforos, determinan el color de una sustancia. Adems, por ser grupos polares, los auxocromos aumentan la solubilidad del colorante en agua y, por lo tanto, su unin a las fibras. Los siguientes son algunos ejemplos de auxocromos:
C=C -OH
C=O -CO2H
N=N -NH2
C=S -NHR
C=NH -NR 2
MEDIR EL COLOR
En definitiva, el color slo es sensacin de color, producto del rgano de la vista. Porque nuestros ojos reaccionan a la incidencia de la energa, y no a la materia en s. Los rayos de luz son transmisores de informacin que nuestro sistema nervioso decodifica.
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
QU ES EL COLOR?
MEDIR EL COLOR
Como vimos anteriormente, de acuerdo con su composicin qumica particular, cada sustancia absorbe luz de diferentes colores, es decir, absorbe determinadas longitudes de onda del espectro luminoso. Se dice, por lo tanto, que cada sustancia tiene un espectro de absorcin propio. Conocer el espectro de absorcin de una sustancia nos permite medir su concentracin en una solucin. Y esta es una tarea habitual en el laboratorio. Porque, para realizar cualquier experimento, el investigador necesita saber con qu cantidad de una determinada sustancia est trabajando. Pues el mtodo cientfico exige reproducibilidad, es decir, que los resultados de un experimento no se hayan logrado por casualidad, sino que puedan repetirse tantas veces como se quiera, en cualquier lugar del planeta. Y esto solamente es posible si se conocen todos los detalles acerca de cmo fue efectuado el ensayo; entre ellos, la concentracin de las sustancias empleadas. En nuestro caso, para medir la eficacia del proceso de teido, al final de los experimentos deberemos determinar la concentracin de colorante en el agua de desteido. Recordemos que, a menor desteido (y, por lo tanto, a menor concentracin de colorante en el agua de lavado), mayor ser la eficiencia del proceso.
/// EL COLOR ES INFORMACIN
Cuanta ms cantidad de colorante hay en una solucin, ms intenso veremos el color. Esto se debe a que si hay ms molculas de colorante, hay ms cromforos y, por lo tanto, ms color.
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
16 | 17
En otras palabras, la intensidad de color que presenta una determinada sustancia en una solucin es proporcional a la concentracin de esa sustancia en la solucin:
MEDIR EL COLOR
COLOR
CONCENTRACIN
COLOR
CONCENTRACIN
As, midiendo la intensidad de color se puede conocer la concentracin de una solucin. Cmo averiguamos cunto color hay en una solucin coloreada? Colocando una pequea muestra de la solucin en un aparato, como por ejemplo un espectrofotmetro. Este dispositivo, nos permite determinar la cantidad de luz que absorbe una sustancia a una determinada longitud de onda, es decir, nos brinda la Absorbancia (A) de la solucin (ver recuadro: Cmo funciona el espectrofotmetro?) Con ese dato, podemos utilizar la ecuacin de Lambert y Beer, autora de Johann Lambert y August Beer, dos fsicos que establecieron matemticamente cul es la relacin que existe entre la cantidad de luz absorbida por una sustancia y la concentracin de esa sustancia en la solucin):
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
MEDIR EL COLOR
A =L C
LEY DE LAMBERT Y BEER
A = ABSORBANCIA DE LA SOLUCIN L = PASO PTICO ( ES EL ESPESOR DE LA CUBETA
QUE UTILIZAMOS PARA PONER LA MUESTRA DENTRO DEL ESPECTOFOTMETRO .
= ABSORTIVIDAD ( ES UNA CONSTANTE DE PROPOR CIONALIDAD CARACTERSTICA DE CADA SUSTANCIA )
C = CONCENTRACIN DE LA SOLUCIN
Cmo aprovechamos esta ecuacin para conocer la concentracin de nuestra solucin? Construyendo lo que se conoce como curva de calibracin del espectrofotmetro para esa sustancia en particular. Para ello, debemos preparar distintas soluciones (cuyas concentraciones conocemos) de la sustancia a medir (por ejemplo, cochinilla):
solucin 1 concentracin 1
solucin 2 concentracin 2
solucin 3 concentracin 3
solucin 4 concentracin 4
solucin 5 concentracin 5
Y, luego, medir en el espectrofotmetro la absorbancia de cada una de ellas.
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
18 | 19
// FIGURA 3
Absorvancia
Concentracin
Si ahora queremos saber la concentracin de cochinilla en el agua de lavado, simplemente debemos medir la absorbancia de esa solucin, e interpolar el dato en la curva de calibracin // FIGURA 4:
// FIGURA 4
Absorvancia
Concentracin
MEDIR EL COLOR
Con esos datos, se construye un grfico, colocando en el eje horizontal los valores de las concentraciones y, en el eje vertical, la absorbancia de cada una de esas soluciones. Comprobaremos que la ecuacin de Lambert y Beer es una recta // FIGURA 3:
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
MEDIR EL COLOR
De lo anterior podemos deducir que, cuanto menor sea la absorbancia del agua de lavado, menor ser la concentracin de colorante en la misma y, por lo tanto, ms eficaz habr sido el proceso de teido.
Espectrofotmetro en funcionamiento
/// CMO FUNCIONA EL ESPOECTROFOTMETRO?
Este dispositivo descompone el espectro lumnico en cada uno de sus colores, lo cual nos permite iluminar con luz de diferentes longitudes de onda la muestra a analizar. As, este aparato nos posibilita saber dos cosas: por un lado, qu longitudes de onda del espectro absorbe nuestra solucin y, por otro lado, la cantidad de luz absorbida. Para ello, posee una lmpara que emite luz en el rango que va entre los 10nm y los 800nm del espectro, es decir, la parte que corresponde al ultravioleta y al visible. Ese haz de luz es condensado y recortado para que incida sobre un prisma (mono-
6.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
20 | 21
A continuacin puede verse un esquema bsico de los componentes de un espectrofotmetro:
...... .. .. .. .. .. .. ...... .. .. .. .. .. .. .. .... . .. .. .. .. .. .. .. .. .. .... . .. .. .. .. .. .. .. .. .. .. .... . .. .. .. .. .. .. .. .. .. .. .. .... . .. .. .. .. .. .. .. .. .. .. .. .. .... .. .. .. .. .. .. .. .. .. .. .. .. .. .. . . . . . . . .. . . .. . . . . . . .. . . . . . . . . ...... .... .... .. .. .. .. .. .. .. .. . .. .. ...... .... .... .. .. .. .. .. . . . . . . . . . . . . . . . . .... . . ......... .................. .... .......... .. ........ .. .. .. . . .... . . . . . . . . . . . . . . ............... .... .. .. .. .. .. .. .... .......... .. .... .. .. .. .. .. ........... .. .. .... .. .. .. .. .. .. .. .......... .. .... .. .. . .. .. .. .. .. . . .. . . . . . . . .... . . . . . . . . . . . . . . .. .... .. .. .. .... .. .. .. ...... .. .. .... .. .... .. .. .. ...... .. .. .. .... .... .. .. ...... .. .. .. .... .... .. ...... .. .. .. .... .. ...... .. .. .. .. .... .. ...... .. .. .. .... .. ...... .. .. .... .. ...... .. .. . .. ...... ..... .........
lente condensante
monocromador
.... .. .. .. .. .... .. .. .. .. .... .. .. .. .. .... .. .. .. .. . .... .. .. .. .. . .... .. .. .. .. . .... .. .. .. .. .... . . . .. . . ........ .. .. ........ .. .. . ........ ... ........ ... ........ . . ........ .. . ........ .. . . ........ ... ........ . . . ....
rendija cubeta (paso ptico) fuente de luz
DOS CONCEPTOS FINALES
cromador) que descompone el espectro lumnico en cada uno de sus colores. A la salida del prisma, una ranura permite seleccionar la longitud de onda deseada. Esta luz monocromtica (de un solo color) atraviesa la muestra y llega a un detector, que mide la cantidad de luz que pudo atravesar la muestra.
7.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
MEDIR EL COLOR
DOS CONCEPTOS FINALES
/// LONGITUD DE ONDA ( ) DE TRABAJO
Dijimos que el espectrofotmetro nos permite seleccionar la longitud de onda () de la luz con la que queremos iluminar la muestra a analizar. Esto nos lleva a una pregunta: Con qu debemos trabajar para medir la absorbancia de nuestra solucin? Para responder a ese interrogante, debemos saber que la que proporciona la mayor sensibilidad (el menor error de medicin) es la que corresponde al mximo de absorcin de la sustancia en estudio. Es decir, que siempre que sea posible, debemos trabajar con la longitud de onda correspondiente al color ms absorbido por la sustancia. Dado que, como dijimos antes, cada sustancia se comporta de manera diferente cuando es iluminada, lo primero que tenemos que hacer es averiguar cul es su espectro de absorcin caracterstico. Por ejemplo, el espectro de absorcin del colorante que utilizaremos en el laboratorio (el cido carmnico de la cochinilla) es el siguiente:
7.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
22 | 23
0.2000 1
Espectro de absorcin del cido carmnico de la cochinilla.
DOS CONCEPTOS FINALES
0.1500
0.1000
Absorvancia
0.0500
0.0000 400.00 500.00 600.00 700.00 800.00
Longitug de onda (mm)
EL ESPECTRO DE ABSORCIN DE UNA SUSTANCIA ES EL RESULTADO DE GRAFICAR LA CANTIDAD DE LUZ QUE ABSORBE ESA SUSTANCIA (ABSORBANCIA) A MEDIDA QUE ES ILUMINADA
CON LUZ DE DIFERENTES LONGITUDES DE ONDA. ESTE PROCEDIMIENTO SE REALIZA CON EL ESPECTROFOTMETRO.
Como puede observarse en la figura anterior, el cido carmnico absorbe luz en un rango que va de los 400 nm. hasta los 610 nm. de longitud de onda. Es decir, como vimos cuando describamos el espectro electromagntico visible, el cido carmnico absorbe el violeta, el azul, el verde, el amarillo y el naranja. Pero no absorbe el rojo (=627 a 770 nm.) Por eso, al colorante lo vemos de este ltimo color.
7.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
DOS CONCEPTOS FINALES
La misma figura tambin nos muestra que el mximo de absorcin del cido carmnico est entre los 480 nm. y los 500 nm. Por lo tanto, nuestra de trabajo debera estar dentro de esos lmites. El mximo de absorcin no vara con la concentracin de la solucin, es decir, una misma sustancia siempre tiene el mismo mximo de absorcin independientemente de su cantidad en la solucin. Esto se ve claramente cuando se construyen los espectros de absorcin de de diferentes soluciones de cido carmnico:
0.250
Espectro de absorcin de diferentes soluciones decido carmnico.
0.200
/ PATRONES DE CIDO CARMNICO /. 5,37x10-5M 3,58x10-5M 1,79x10-5M 0,15x10-5M
0.150
0.100
Absorvancia
0.050
0.000 400.0 500.0 600.0 700.0 800.0
Longitug de onda (mm)
El grfico anterior nos demuestra que, an variando la concentracin de las soluciones, el mximo de absorcin del cido carmnico es siempre el mismo.
7.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
24 | 25
/// RANGO DE VALIDEZ DE LA LEY DE LAMBERT Y BEER
El uso de la ecuacin A = L C para determinar la concentracin de una solucin, slo es vlido en tanto haya una relacin lineal entre A y C (Figura 3, pg.19), de tal manera que una variacin en la concentracin de la solucin produzca una variacin proporcional en la absorbancia de esa solucin. Este requisito deja de cumplirse a concentraciones muy altas, cuando el detector del espectrofotmetro pierde sensibilidad, o cuando las soluciones son turbias o muy oscuras (Figura 5):
El rango de validez de la ley de Lambert y Beer esta comprendido entre las dos flechas.
RESUMEN
Absorvancia
Concentracin
Es decir, la curva de calibracin solo es vlida en su parte recta. Esto significa que si notamos que nuestras soluciones de lavado son demasiado concentradas como para entrar en la zona de validez de la ecuacin de Lambert y Beer, deberemos diluirlas y, despus, calcular la concentracin multiplicando el valor obtenido por el grado de dilucin de la solucin. Por ejemplo, si para poder medir dentro del rango de validez tuvimos que diluir una solucin a la mitad, entonces, al valor de concentracin obtenido luego de la medicin habr que multiplicarlo por 2, para conocer la concentracin de la solucin de partida.
8.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
26 | 27
RESUMEN
En definitiva, los pasos a seguir para conocer la concentracin de una solucin mediante el mtodo espectrofotomtrico son los siguientes:
1) DETERMINACIN DEL ESPECTRO DE ABSORCIN DE LA MUESTRA 2) DETERMINACIN DEL MXIMO DE ABSORCIN 3) PREPARACIN DE LOS PATRONES DE CONCENTRACIONES CONOCIDAS 4) CONSTRUCCIN DE LA CURVA DE CALIBRACIN 5) LECTURA DE LA ABSORBANCIA DE LA/S MUESTRA/S PROBLEMA (EN NUESTRO CASO, EL AGUA DE LAVADO) 6) INTERPOLACIN DEL VALOR DE ABSORBANCIA DE LA/S MUESTRA/S PROBLEMA EN LA CURVA DE CALIBRACIN ? DETERMINACIN DE LA CONCENTRACIN DESCONOCIDA.
LABORATORIO
9.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
28 | 29
LABORATORIO
ESQUEMA GENERAL DEL TRABAJO PRCTICO
PREPARACIN DE LAS SOLUCIONES DE COLORANTE Y MORDIENTES
LABORATORIO
1. 2. 3.
PREPARATIVOS PARA EL TEIDO
TEIDO
MORENTADO Y TEIDO DE FIBRAS
EVALUACIN DE LA EFICIENCIA DEL TEIDO
LAVADO DE FIBRAS TEIDAS
DETERMINACIN DE LA CONCENTRACIN DE COLORANTES EN LAS SOLUCIONES DE LAVADO
9.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
1.
LABORATORIO
PREPARATIVOS PARA EL TEIDO ///
PREPARACIN DE LAS SOLUCIONES DE COLORANTE
PREPARACIN DE LAS SOLUCIONES DE MORDIENTES
PESAR LA CANTIDAD NECESARIA DE COCHINILLA
alumbre al 15%
alumbre al 25%
alumbre al 15% + cremor trtaro al 4%
MOLER LA COCHINILLA
alumbre al 25% + cremor trtaro al 6%
SO4Cu
SnCl2 + cremor trtaro
EXTRAER EL CIDO CRMICO CON AGUA DESTILADA
CALCULAR LAS CANTIDADES DE CADA MORDIENTE PARA PREPARAR LA SOLUCIN
FILTRAR LA SOLUCIN
PESAR LA CANTIDAD CALCULADA DE CADA MORDIENTE
LLEVAR LA SOLUCIN A VOLUMEN CON AGUA DESTILADA
DISOLVER CADA MORDIENTE EN LA CANTIDAD NECESARIA DE AGUA DESTILADA
9.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
30 | 31
2.
TEIDO ///
FIBRA (LANA / ALGODN / SEDA)
MORDENTADO ALUMBRE 25% MORDENTADO CON CON ALUMBRE
MORDENTADO CON ALUMBRE 15%
MORDENTADO CON ALUMBRE 15% + CT 4%
15%
25%
15% + CT 4%
25% + CT 6%
fibra mordentada con alumbre 15%
fibra mordentada con alumbre 25%
fibra mordentada con alumbre 15% + CT 4%
fibra mordentada con alumbre 25% + CT 6%
TEIDO CON COCHINILLA
FIBRA TEIDA 1
FIBRA TEIDA 2
FIBRA TEIDA 3
FIBRA TEIDA 4
FIBRA TEIDA 5
MORDENTADO CON SnCl2 + CT
FIBRA TEIDA 6
MORDENTADO CON CuSO4
FIBRA TEIDA 7
LABORATORIO
9.
TALLERES DE CIENCIAS QUMICA Y COLOR EN LOS TEXTILES
3.
LABORATORIO
EVALUACIN DE LA EFICIENCIA DE TEIDO ///
FIBRA TEIDA
LAVADO CON AGUA FRA
LAVADO CON AGUA CALIENTE
SOLUCIN DE LAVADO 1
SOLUCIN DE LAVADO 2
DETERMINACIN DE LA CONCENTRACIN DE CIDO CARMNICO
construccin de la curva de calibracin
determinacin de la longitud de onda de trabajo
determinacin del espectro de absorcin del cido crmico
EVALUACIN DE LA EFICIENCIA DEL TEIDO
Anda mungkin juga menyukai
- Química y Color en Los Textiles-Cuencias Extactas y Naturales PDFDokumen33 halamanQuímica y Color en Los Textiles-Cuencias Extactas y Naturales PDFJuan Cho MejiaBelum ada peringkat
- Curtición Al CromoDokumen6 halamanCurtición Al CromoAlex Ccahuana SotoBelum ada peringkat
- Telas No Tejidas - Apunte UPV AITEX - Diploma 2016-2017Dokumen15 halamanTelas No Tejidas - Apunte UPV AITEX - Diploma 2016-2017Pao FrancavillaBelum ada peringkat
- Que Es Un Jersey 21Dokumen4 halamanQue Es Un Jersey 21AlejandraVodaBelum ada peringkat
- Fisica Textil Enric Carrera PDFDokumen196 halamanFisica Textil Enric Carrera PDFWilly Calsina MiramiraBelum ada peringkat
- Prac.5 .Pretratamiento LanaDokumen7 halamanPrac.5 .Pretratamiento LanajaimeangelBelum ada peringkat
- PL1 Identificacion de Tejidos Textiles Por Disolucion QuimicaDokumen8 halamanPL1 Identificacion de Tejidos Textiles Por Disolucion QuimicaAnonymous 9Tky93ktdO50% (2)
- Labo-N10 - Colorantes ÁcidosDokumen15 halamanLabo-N10 - Colorantes ÁcidosJOSE AYALABelum ada peringkat
- La Industria Textil y Su Control de Calidad. VI. Ennoblecimiento Textil. Fidel Eduardo y Lockuán Lavado (2012)Dokumen86 halamanLa Industria Textil y Su Control de Calidad. VI. Ennoblecimiento Textil. Fidel Eduardo y Lockuán Lavado (2012)Claudia SD100% (1)
- Encogimiento de La TelaDokumen5 halamanEncogimiento de La TelaNotlim Otrebla Ollis AzolañepBelum ada peringkat
- Recubrimientos TextilesDokumen11 halamanRecubrimientos TextilesCharl's SanangoBelum ada peringkat
- Identificación de FibrasDokumen13 halamanIdentificación de FibrasLaura CalzadillaBelum ada peringkat
- Teñido Textil PDFDokumen67 halamanTeñido Textil PDFCarlos Pérez JustoBelum ada peringkat
- VII La Industria Textil y Su Control deDokumen65 halamanVII La Industria Textil y Su Control deLorena HS100% (1)
- Fibras sintéticas: Características, usos y procesosDokumen15 halamanFibras sintéticas: Características, usos y procesosRonaldo ApazaBelum ada peringkat
- Tintorería y Acabados TextilesDokumen43 halamanTintorería y Acabados TextilesJimmy Usurin CanchariBelum ada peringkat
- Desarrllo Del Colorante Directo Del Algodon - G - 4b Hallasi AmeliaDokumen31 halamanDesarrllo Del Colorante Directo Del Algodon - G - 4b Hallasi AmeliaGaby F CL100% (1)
- Tipos de Fibras TextilesDokumen4 halamanTipos de Fibras TextilesErick AyabacaBelum ada peringkat
- Test para La Identificación de Fibras TextilesDokumen5 halamanTest para La Identificación de Fibras TextilesCarlos Pérez JustoBelum ada peringkat
- Texturizado PDFDokumen16 halamanTexturizado PDFLisandro Martín MuñozBelum ada peringkat
- Taller 3 Control Calidad 2Dokumen6 halamanTaller 3 Control Calidad 2Jordan PinedoBelum ada peringkat
- Pretreatment AxtDokumen38 halamanPretreatment AxtCarlos Rodríguez Gandarillas100% (1)
- Practicas de Sistema de Numeración de HilosDokumen2 halamanPracticas de Sistema de Numeración de HilosFlorian AlvarezBelum ada peringkat
- TextilesDokumen91 halamanTextilesDeili Noemi Pérez NavarroBelum ada peringkat
- Geo TextilDokumen18 halamanGeo TextilMelissaOrtegaCisnerosBelum ada peringkat
- Tendencias actuales en el procesamiento de prendas de vestirDokumen5 halamanTendencias actuales en el procesamiento de prendas de vestirElvis Medina100% (1)
- Producción textil y tratamientos físico-químicosDokumen12 halamanProducción textil y tratamientos físico-químicosIsabel Moran ArecesBelum ada peringkat
- 16 Ficha de Tejido de PuntoDokumen14 halaman16 Ficha de Tejido de PuntoisaiBelum ada peringkat
- II La Industria Textil y Su Control de Calidad Fibras TextilesDokumen144 halamanII La Industria Textil y Su Control de Calidad Fibras TextilesricardoBelum ada peringkat
- TEMA 1. Fibras TextilesDokumen7 halamanTEMA 1. Fibras TextilesIsabel Ramírez GirónBelum ada peringkat
- Empresas textiles peruanas y sus telaresDokumen15 halamanEmpresas textiles peruanas y sus telaresFabbian ZegarraBelum ada peringkat
- Densidad de TejidoDokumen44 halamanDensidad de TejidoCarlos E. Jvárez MoraBelum ada peringkat
- PDF Suavizantes y Siliconas - CompressDokumen20 halamanPDF Suavizantes y Siliconas - CompressRenzo Vicente GuizadoBelum ada peringkat
- Textil EnnoblecimientoDokumen87 halamanTextil EnnoblecimientoDilan Mendez100% (1)
- FIBRAS TEXTILESDokumen120 halamanFIBRAS TEXTILESEdylito94100% (1)
- Mallas o Sedas para SerigrafíaDokumen3 halamanMallas o Sedas para Serigrafíaenteka666Belum ada peringkat
- Fibras textiles: clasificación, propiedades y tipos principalesDokumen30 halamanFibras textiles: clasificación, propiedades y tipos principalesEucyta VortBelum ada peringkat
- Teñido de Nylon y AcrilicoDokumen27 halamanTeñido de Nylon y AcrilicoKiro Baam0% (1)
- Quimica Textil-202 PDFDokumen39 halamanQuimica Textil-202 PDFTabita QuilumbaquinBelum ada peringkat
- Historia de La TinturaDokumen4 halamanHistoria de La Tinturawilma gutierrezBelum ada peringkat
- ACABADOS Monica Presntacion 1Dokumen29 halamanACABADOS Monica Presntacion 1Alejandra Perez Reyes100% (1)
- 1 Eslabon TextilDokumen14 halaman1 Eslabon TextilEmily FloresBelum ada peringkat
- Tintura de Fibras Con Colorantes ReactivosDokumen8 halamanTintura de Fibras Con Colorantes ReactivosDavid MarceloBelum ada peringkat
- Q60 G65 TDokumen144 halamanQ60 G65 TDianeth Buleje CamposBelum ada peringkat
- Colorantes Cationicos PDFDokumen2 halamanColorantes Cationicos PDFApril0% (2)
- Rayon NitrocelulosaDokumen9 halamanRayon Nitrocelulosakenyi aroquipaBelum ada peringkat
- 20102IEE402PI10T075Dokumen137 halaman20102IEE402PI10T075CHRISTIAN JESUS MERINO NAVARROBelum ada peringkat
- Informe de FieltroDokumen4 halamanInforme de FieltroMarcela RobalinoBelum ada peringkat
- Fabricación no tejidosDokumen26 halamanFabricación no tejidosElena AlonsoBelum ada peringkat
- SerigrafíaDokumen7 halamanSerigrafíaMelody SeaBelum ada peringkat
- TejeduriaDokumen86 halamanTejeduriaJelber Hernandez MartinezBelum ada peringkat
- Acabados textiles: Desengomado, descrude y blanqueo de algodónDokumen12 halamanAcabados textiles: Desengomado, descrude y blanqueo de algodónVivianaPiedraMontoyaBelum ada peringkat
- Análisis Forense de Fibras Textiles PGDokumen4 halamanAnálisis Forense de Fibras Textiles PGJosé David Guerrero ToapantaBelum ada peringkat
- Labo 2 de Control IiiDokumen12 halamanLabo 2 de Control IiiPierreSevillanoBelum ada peringkat
- Tecnología Del TermofijadoDokumen6 halamanTecnología Del TermofijadoCaritoIndumentariaBelum ada peringkat
- Hidrosulfito de SodioDokumen17 halamanHidrosulfito de SodioEva Maria Tenorio CHBelum ada peringkat
- 01.1. Clasificación de Las Fibras TextilesDokumen10 halaman01.1. Clasificación de Las Fibras TextilesPao FrancavillaBelum ada peringkat
- Perlita PlusDokumen4 halamanPerlita PlusMonica Morales100% (2)
- Colorante Natural1Dokumen13 halamanColorante Natural1José GranadosBelum ada peringkat
- Informe Final - Quimica Textil - Grupo 3 FinalDokumen83 halamanInforme Final - Quimica Textil - Grupo 3 FinalTania SolBelum ada peringkat
- Inversor de 25W (Gama Baja)Dokumen4 halamanInversor de 25W (Gama Baja)Tarcisio MacedoBelum ada peringkat
- ColumnasDokumen16 halamanColumnasJose LimachiBelum ada peringkat
- Valoracion de PlasticosDokumen8 halamanValoracion de PlasticosDieguitoOmarMoralesBelum ada peringkat
- Manual de Analisis de SuelosDokumen74 halamanManual de Analisis de SuelosCarlos Egoavil De la Cruz95% (19)
- MicrobiologiaDokumen35 halamanMicrobiologiaJose LimachiBelum ada peringkat
- Articulo KiebDokumen12 halamanArticulo KiebRoger Moina VillegasBelum ada peringkat
- Diario - Concreto en Cimiento CorridoDokumen1 halamanDiario - Concreto en Cimiento CorridoJose LimachiBelum ada peringkat
- Compuestos Volátiles de Las PlantasDokumen26 halamanCompuestos Volátiles de Las PlantasStip Yannin Suárez CruzBelum ada peringkat
- 1 Ds 023 2009 Minam CategoriasDokumen8 halaman1 Ds 023 2009 Minam CategoriasJose LimachiBelum ada peringkat
- Dialnet AnalisisPorDifraccionDeRayosXDeRocasProvenientesDe 4587146 PDFDokumen4 halamanDialnet AnalisisPorDifraccionDeRayosXDeRocasProvenientesDe 4587146 PDFClaudia Llacza CruzadoBelum ada peringkat
- Difraccion de Rayos XDokumen10 halamanDifraccion de Rayos XJose Limachi100% (1)
- CAPITULO III Suelos Agrícolas y Propiedades FísicasDokumen14 halamanCAPITULO III Suelos Agrícolas y Propiedades FísicasJose LimachiBelum ada peringkat
- IntroducciónDokumen3 halamanIntroducciónJose LimachiBelum ada peringkat
- MicrobiologiaDokumen35 halamanMicrobiologiaJose LimachiBelum ada peringkat
- 05-06-15 Met-Bacter.......Dokumen43 halaman05-06-15 Met-Bacter.......Jose LimachiBelum ada peringkat
- LEY DE LAMBERT-BEER COLORIMETRÍADokumen7 halamanLEY DE LAMBERT-BEER COLORIMETRÍAJose LimachiBelum ada peringkat
- 22-05-05 Clase de MicroDokumen61 halaman22-05-05 Clase de MicroJose LimachiBelum ada peringkat
- BIOPLÁSTICOSDokumen13 halamanBIOPLÁSTICOSJose LimachiBelum ada peringkat
- FosforoxidativaDokumen17 halamanFosforoxidativaViridiana Morales ColinBelum ada peringkat
- Cap IV ProteinasDokumen45 halamanCap IV ProteinasJose LimachiBelum ada peringkat
- Determinación de Humedad Por Metodo IndirectoDokumen5 halamanDeterminación de Humedad Por Metodo IndirectoPatriciaLopezLunaBelum ada peringkat
- Bioseguridad en El LaboratoDokumen24 halamanBioseguridad en El LaboratoJose LimachiBelum ada peringkat
- Cálculo Del Contenido en Azúcares TotalesDokumen7 halamanCálculo Del Contenido en Azúcares TotalesLobsang Orion Valbuena CarrilloBelum ada peringkat
- CraqueoDokumen10 halamanCraqueoIan LizarragaBelum ada peringkat
- mcm41 121213194058 Phpapp02Dokumen29 halamanmcm41 121213194058 Phpapp02Jose LimachiBelum ada peringkat
- FERTILISANTEDokumen19 halamanFERTILISANTEJose LimachiBelum ada peringkat
- CarbonDokumen12 halamanCarbonNeyza Fabiola CayojaBelum ada peringkat
- FERTILISANTEDokumen19 halamanFERTILISANTEJose LimachiBelum ada peringkat
- Aislamiento de La Casecina de La LecheDokumen4 halamanAislamiento de La Casecina de La LecheJose LimachiBelum ada peringkat
- CAOLINITADokumen57 halamanCAOLINITACesar Augusto ColoradoBelum ada peringkat
- Metodos Opticos de Analisis de Los Productos Agroindustriales Expicicon 3ra UnidadDokumen42 halamanMetodos Opticos de Analisis de Los Productos Agroindustriales Expicicon 3ra UnidadWaldirPalominoBelum ada peringkat
- Trabajo de AerofotosDokumen6 halamanTrabajo de AerofotosÁngel Morgado0% (1)
- Actividad II Fisica ModernaDokumen7 halamanActividad II Fisica ModernaEdin Son AlvaRaBelum ada peringkat
- Curvas de titulación de aminoácidos: identificación de la glicina y el ácido glutámico mediante análisis de pHDokumen11 halamanCurvas de titulación de aminoácidos: identificación de la glicina y el ácido glutámico mediante análisis de pHLópez DiegoBelum ada peringkat
- Laboratorio 8Dokumen4 halamanLaboratorio 8Seba CarrielBelum ada peringkat
- Elementos de Dibujo Técnico PDFDokumen12 halamanElementos de Dibujo Técnico PDFRAG6565Belum ada peringkat
- Barotrauma y RadiacionesDokumen71 halamanBarotrauma y Radiacionesedgar gonzale zpinedaBelum ada peringkat
- AFEO Planeación Didáctica 12324 JKRDokumen30 halamanAFEO Planeación Didáctica 12324 JKRJorge KarlisBelum ada peringkat
- Disco Newton experimentos casa demostrar luz blanca compuesta coloresDokumen2 halamanDisco Newton experimentos casa demostrar luz blanca compuesta coloressara varas100% (1)
- "TABLA PERIÓDICA Y PROPIEDADES PERIÓDICAS" Química Básica LaboratorioDokumen23 halaman"TABLA PERIÓDICA Y PROPIEDADES PERIÓDICAS" Química Básica LaboratorioArT111094% (18)
- La Fotografia y El LenticularDokumen127 halamanLa Fotografia y El LenticularEduwin FuentesBelum ada peringkat
- Geometría Descriptiva InterseccionesDokumen29 halamanGeometría Descriptiva InterseccionesPablo0% (1)
- Inspeccion Visual I y II (2022)Dokumen229 halamanInspeccion Visual I y II (2022)Adrian HernandezBelum ada peringkat
- Equipos LabinsDokumen95 halamanEquipos LabinsGina AriasBelum ada peringkat
- Espectro CromaticoDokumen4 halamanEspectro CromaticoMiguel MartínezBelum ada peringkat
- pdf24 UnidoDokumen140 halamanpdf24 Unidodaiana amarillaBelum ada peringkat
- Tema 2Dokumen8 halamanTema 2Jhonattan BaraleBelum ada peringkat
- Apreciacion de Las ArtesDokumen13 halamanApreciacion de Las ArtesFridaBelum ada peringkat
- Espectroscopia de Reflectancia AplicadaDokumen26 halamanEspectroscopia de Reflectancia AplicadaHugo PomaBelum ada peringkat
- Teorica Color 2014Dokumen10 halamanTeorica Color 2014PoderCreativo CampoLargoBelum ada peringkat
- Pia Fisica 4Dokumen8 halamanPia Fisica 4Rafa EspiridionBelum ada peringkat
- 4° Guia Teoria Del ColorDokumen10 halaman4° Guia Teoria Del ColorEdwin RosaBelum ada peringkat
- Arduino FDokumen120 halamanArduino FpepecrBelum ada peringkat
- AQI Agrov (L) 02 2020-I UNMSMDokumen10 halamanAQI Agrov (L) 02 2020-I UNMSMLadhiJaniraDextreMartinezBelum ada peringkat
- 2 P - Afeo-03Dokumen27 halaman2 P - Afeo-03Moises57% (14)
- Taller 2 - Espectros Electrónicos-20Dokumen3 halamanTaller 2 - Espectros Electrónicos-20Roco neluBelum ada peringkat
- Espectro ElectromagneticoDokumen25 halamanEspectro ElectromagneticoianelBelum ada peringkat
- Teoria FisicaDokumen20 halamanTeoria Fisicadavid esteban BarraBelum ada peringkat
- 4.dispercion de La LuzDokumen46 halaman4.dispercion de La LuzHira León RodríguezBelum ada peringkat
- Diodo LedDokumen11 halamanDiodo Ledgonzalomarcos2019Belum ada peringkat