Microbiología General y Bucal
Diunggah oleh
drancerboyHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Microbiología General y Bucal
Diunggah oleh
drancerboyHak Cipta:
Format Tersedia
Microbiologa General y Bucal Prctica 1: El laboratorio de Microbiologa
Pgina principal Descripcin Un laboratorio de Microbiologa es un lugar habilitado para manejar y estudiar microorganismos. El trabajo debe realizarse de acuerdo con los estndares tcnicos y de seguridad propios de un laboratorio de Microbiologa Clnica. Es importante recordar que la finalidad es determinar los microorganismos presentes en la muestra por lo que es preciso extremar las precauciones para evitar contaminaciones que den lugar a resultados errneos. Todas las muestras deben ser manejadas con precaucin por su potencial patogenicidad. Para deshacerse del material contaminado se deben utilizar recipientes adecuados que deben ser esterilizados posteriormente. Nunca se puede tirar nada contaminado por el fregadero o al cubo de la basura comn sin haber sido esterilizado previamente. El el laboratorio deben existir unas recomendaciones generales de limpieza y en caso de vertidos: Procedimientos de limpieza de superficies externas mediante papel humedecido con solucin desinfectante (alcohol 70%, desinfectante fenlico diluido, etc.). Aclarar con agua los restos de desinfectante. En caso de usar soluciones de hipoclorito en zonas metlicas, limpiar posteriomente para evitar el efecto corrosivo. En caso de derramamientos de material peligroso o formacin de aerosoles: evitar inspiraciones de esos aerosoles, esperar 30 minutos hasta que las partculas se hayan depositado y limpiar con mascarilla, guantes y otros tiles protectores. En caso de vertido de materiales, cubrir la superficie con desinfectante y posteriormente cubrir con papel humedecido con desinfectante. Dejar durante 15 minutos y limpiar. En caso necesario aclarar con agua. En caso de derramamientos menores limpiar el material vertido mediante papel humedecido y posteriormente aclarar, cuando sea necesario. Los laboratorios debern disponer de los aparatos e instrumental necesario para el correcto desarrollo de su actividad. Debe existir un procedimiento de control de calidad en el laboratorio de Microbiologa Clnica que implique la monitorizacin de los medios e instrumentos, con el fin de asegurar la adecuada realizacin de los aislamientos, identificacin y caracterizacin de los patgenos Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6
y la realizacin precisa de las pruebas de sensibilidad a los antimicrobianos como referencia teraputica. El sistema de la calidad deber contemplar la existencia de registros de formacin de personal. es imprescindible la existencia de un procedimiento sobre medidas de proteccin personal en el manejo de equipos y aparatos. Los equipos del laboratorio deben funcionar de forma que se asegure la reproducibilidad de los resultados de las pruebas diagnsticas. El laboratorio deber estar bajo la direccin y responsabilidad de un facultativo con la especialidad correspondiente, legalmente capacitado para realizar aqullas determinaciones clnicas que el laboratorio tenga autorizadas. El personal tcnico y sanitario del laboratorio deber disponer la titulacin adecuada para las funciones que desarrolla de conformidad con la legislacin vigente. Estructura de un laboratorio de Microbiologa Clnica
rea administrativa rea de recepcin de muestras rea de extraccin que deber: Disponer de material de un solo uso para contacto con muestras biolgicas. Disponer de un rea de extracciones y toma de muestra, una sala de espera para los pacientes y los servicios de higiene correspondientes. Disponer de personal legalmente autorizado para la toma de muestras. Disponer de un manual de extraccin, toma y transporte de muestras. El manual antedicho deber ser elaborado por el responsable rea de trabajo: anlisis y procesado de muestras El puesto de trabajo debe debe de estar limpio y ordenado El material necesario debe prepararse antes de empezar a trabajar y colocarse de forma adecuada para que se facilite su utilizacin asi se evitarn accidentes y se minimizar el riesgo de contaminacin Nunca se debe pipetear con la boca. Utilizar siempre elementos manuales o automticos. Todo el material utilizado debe estar estril.
1. Elementos y materiales ms frecuentes de un laboratorio de Microbiologa Clnica 1.1. Mesas de laboratorio y fregadero
1.2. Vitrinas y armarios
1.3. Mechero Bunsen
Todas las manipulaciones deben realizarse en un radio de 10-15cm de la llama del mechero (zona asptica). En caso de utilizar mechero nunca se debe coger material por encima de la llama Antes de comenzar a trabajar se procurar disponer de todo el material necesario para el procesamiento de la muestra Tomar las medidas necesarias para evitar la contaminacin de las muestras o/ y cultivo por microorganismos ambientales 1.4. Gradillas
1.5. Estufa de incubacin Es una cmara de temperatura controlada para cultivo de microorganismos. Se utiliza para facilitar el desarrollo de los microorganismos a su temperatura ptima de crecimiento (generalmente 35-37).
1.6. Frigorfico o cmaras refrigeradas Se utilizan para conservar tanto materiales (medios de cultivo, reactivos) como microorganismos. Generalmente estn a una temperatura fija de 4C.
1.7. Congeladores Se utilizan para la conservacin de reactivos y microorganismos a temperaturas inferiores a 0C, llegando a -80C (los ms frecuentes son 20, -40 y -80).
1.8. Microscopio ptico
1.9. Centrfuga Aparato que aplica sobre los tubos una fuerza centrfuga lo que permite la separacin de los distintos componentes de la muestra mediante la precipitacin en el fondo del tubo de las partculas en suspensin.
1.10. Cmaras de seguridad biolgica (ver practica 2)
1.11. Desionizador de agua. La mayor parte de los trabajos que se realizan en un laboratorio de Microbiologa Clnica necesitan la utilizacin de agua pura con el fin de evitar cualquier tipo de interferencia. Entre otra caractersticas debe: estar exenta de materiales en suspensin o un pH comprendido entre 5,0 y 7,5. Durante aos se ha utilizado agua destilada, en la actualidad los destiladores se han ido abandonando para dar paso a desionizadores que funcionan con resinas de intercambio inico. Tambin se pueden utilizar otras tcnicas como la smosis inversa.
1.12. Contador de colonias: Es un aparato que mediante la iluminacin de la placa y una lupa, nos permite observar con mayor nitidez las colonias y por tanto facilita su recuento.
1.13. Balanzas
1.14. Baos termostticos: son recipientes que contienen agua y un sistema de regulacin de la temperatura. Se utilizan para atemperar medios de cultivo o incluso para incubar cultivos de microorganismos.
1.15. Agitador/ mezclador
vortex
agitador horizontal
1.16. Jarras de anaerobios: Recipientes que se usan para conseguir una atmsfera libre de oxgeno para el cultivo de microorganismos anaerobios.
1.17. Asas de siembra: Se utilizan para sembrar. Pueden ser metlicas o de plstico, curvas o rectas (para la siembra por picadura).
1.18. Ph-metros:
1.19. Material fungible
Placas de Petri: recipientes para la preparacin de medios de cultivo slidos
Placas de Petri con medio slido
Tubos con medio lquido
Tubos con medio slido
Pipetas de vidrio, de plstico y pipeteadores.
Pipetas
Pipeteador automtico
Pipeteador manual
Pipetas automticas (micropipetas) y puntas de pipeta: Se utilizan para pipetear pequeas cantidades de lquidos. Se utilizan con puntas desechables de distinto tamao y color segn la micropipeta. Existen cuatro tamaos: de 0,5-2m; de 2-20 m; de 20-200 m y de 200-1000 m.
Asas acodadas o Asas de Digralsky: Se utilizan para la extensin de microorganismos sobre la superficie de un medio de cultivo en placa Petri.
Portas y cubres Para realizar las observaciones al microscopio.
Vasos de precipitados y matraces
Cucharas y esptulas:
Se utilizan para pesar muestras o medios de cultivo.
rea de limpieza de material y eliminacin de residuos
Zona donde se procede a la esterilizacin mediante autoclave del material utilizado. El material desechable se elimina y con el material reciclave se procede a la eliminacin de residuos y lavado. De esta manera el material queda dispuesto para ser utilizado. rea de esterilizacin Procedimiento por el que se consigue la muerte de todos los organismos vivos y formas de resistencia en un objeto o producto tratado.
Autoclave Es el equipo ms utilizado. Es un procedimiento de esterilizacin mediante calor hmedo. Se realiza en al autoclave durante 15 20 min, segn el volumen, a 115C 121C, segn la naturaleza del material que se desee esterilizar. Autoclavado: es un procedimiento en el que se emplea vapor a presin (a 1 atmsfera). Como tiene gran poder de penetracin la temperatura y el tiempo utilizados son menores que los que se emplean con el horno Pasteur (121 C, 15-20 minutos).
Se utiliza para esterilizar: Medios de cultivo, ropa, material de plstico resistente al calor hmedo, objetos de metal que no se alteren
con la humedad y sobre todo material de vidrio.
Horno de Pasteur: emplea altas temperaturas (160-180 C) durante un tiempo prolongado (1.5 a 3 horas). Debido a su poca capacidad de penetracin se usa para esterilizar vidrio y metales. Acta principalmente desnaturalizando las protenas y secundariamente oxidando los compuestos celulares.
rea de preparacin de medios Almacn de reactivos rea de seguridad microbiolgica Debe ser una zona diferenciada y aislada para la manipulacin de microorganismos susceptibles de formar aerosoles potencialmente infecciosos.
Microbiologa General y Bucal Prctica 2: Normas bsicas de trabajo
Pgina principal Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6 El estudio de los agentes infecciosos comporta riesgos que dependen del agente infeccioso y de los procedimientos utilizados. Las normas de Seguridad Biolgica pretenden reducir a un nivel aceptable el riesgo inherente a la manipulacin de material peligroso. La actitud y el modo de proceder de aquellos que trabajan en el Laboratorio de Microbiologa determinan su propia seguridad, as como la del resto del personal. El riesgo puede ser alto o muy limitado y depende del personal, de la infraestructura y de la metodologa empleada. Cada persona debe responsabilizarse de su propia seguridad y de la del resto de trabajadores.
1.- Normas generales
Son de obligado cumplimiento en cualquier rea del laboratorio. - El acceso al laboratorio debe estar limitado al personal autorizado. - No deben entrar en el mismo familiares ni amigos. - El personal del laboratorio debe implicarse en el cumplimiento de las normas de seguridad. - Todas las reas estarn debidamente marcadas con la seal de riesgo biolgico y su nivel de contencin. - Las puertas y ventanas deben permanecer cerradas para mantener la adecuada contencin biolgica. - Todas las superficies de trabajo se limpiarn y desinfectarn diariamente y siempre que se produzca un derrame. - Los residuos y muestras peligrosas que van a ser incinerados fuera del laboratorio deben ser transportados en contenedores cerrados, resistentes e impermeables siguiendo las normas especficas para cada tipo de residuo. - El laboratorio debe permanecer limpio y ordenado y no es aconsejable utilizar los pasillos como almacn. Siempre debe quedar un
espacio libre no inferior a 120 cm para poder evacuar el laboratorio en caso de emergencia. - El transporte de las muestras dentro o entre laboratorios se realizar de tal manera que, en caso de cada, no se produzcan salpicaduras. Lo recomendable es hacerlo en cajas hermticas o neveras transportables. Estas cajas o neveras debern ser rgidas y resistentes a los golpes, contar con materiales absorbentes en su interior y de fcil desinfeccin. Se etiquetarn o identificarn de forma oportuna y no podrn ser utilizadas para otros fines. No se puede transportar las muestras a mano. - La ropa protectora, fcilmente ajustable y confortable, as como guantes, gafas, etc. debe estar disponible en todo momento. La ropa protectora de las reas con nivel de contencin 3 (cubrebatas) nunca debe ser usada fuera del rea de trabajo y si se quita debe de ser desechada automticamente en una bolsa de material contaminado.Nunca debe volver a ser usada. - Todo el personal debe poner especial cuidado en evitar el contacto de la piel con materiales potencialmente infecciosos. Con este fin deben usarse guantes cuando se manipulen muestras o cultivos que contengan posibles patgenos. Los guantes siempre sern desechados antes de salir del rea de trabajo. Nunca se saldr del laboratorio con los guantes puestos, ni se coger el telfono con ellos puestos, se tocarn los volantes, etc. - Tras quitarse los guantes, se realizar un lavado de manos. - Se usarn gafas protectoras y mascarillas faciales si existe riesgo de salpicaduras y/o aerosoles. - Se pondr extremo cuidado en minimizar el riesgo de autoinoculacin y de generacin de aerosoles. - Los derrames y accidentes deben ser informados inmediatamente al Supervisor y al Jefe del Laboratorio y hacerse constar por escrito. - Nadie podr trabajar en el rea de tuberculosis con una prueba de Mantoux negativa. - Est rigurosamente prohibido pipetear con la boca. Se realizar pipeteo automtico con material adecuado y cada trabajador ser instruido para manejarlo debidamente. - En la zona de trabajo no debe colocarse material de escritorio ni libros ya que el papel contaminado es de muy difcil esterilizacin. - No debern usarse lentes de contacto. - El personal con el cabello largo debe llevarlo recogido. - Comer, beber, fumar y aplicarse cosmticos esta formalmente prohibido en el rea de trabajo del laboratorio, as como el almacenamiento de comida o bebida. - El personal debe lavarse las manos frecuentemente durante las actividades rutinarias, tras acabar la jornada laboral y siempre antes
de abandonar el laboratorio. Se usar un jabn antisptico y el secado se realizar con papel. - Las heridas y cortes deben ser convenientemente vendados y despus es imprescindible ponerse guantes. - El uso de agujas hipodrmicas y jeringas debe ser limitado. Slo deben usarse las unidades ya montadas. - Nunca se debe volver a poner la capucha a las agujas y stas no deben ser torcidas ni separadas de la jeringa. - Las agujas y jeringas usadas, as como los bisturs, deben ser desechados slo en contenedores especiales destinados a este propsito.
2.- Clasificacin de los agentes biolgicos por grupos de riesgo
Agente biolgico del grupo 1. Aqul que resulta poco probable que cause una enfermedad en el hombre. Agente biolgico del grupo 2. Aqul que puede causar una enfermedad en el hombre y puede suponer un peligro para los trabajadores, siendo poco probable que se propague a la colectividad y existiendo generalmente profilaxis o tratamiento eficaz. Agente biolgico del grupo 3. Aqul que puede causar una enfermedad grave en el hombre y presenta un serio peligro para los trabajadores, con riesgo de que se propague a la colectividad y existiendo frente a l generalmente profilaxis o tratamiento eficaz. Agenete biolgico del grupo 4. Aqul que causando una enfermedad grave en el hombre supone un serio peligro para los trabajadores, con muchas probabilidades de que se propague a la colectividad y sin que exista generalmente frente a l profilaxis o tratamiento eficaz.
3.-Niveles de contencin
El trmino "contencin" se emplea para describir los mtodos que hacen seguro el manejo de materiales infecciosos en el laboratorio. El propsito de la contencin es reducir al mnimo la exposicin del personal de los laboratorios, otras personas y el entorno a agentes potencialmente peligrosos. La Seguridad Biolgica se fundamenta en tres elementos:
Tcnicas de laboratorio. El elemento ms importante para contener los riesgos biolgicos es el seguimiento estricto de las prcticas y tcnicas estndar microbiolgicas. Como parte de estas prcticas est el desarrollo o adopcin por parte de cada laboratorio de un manual de operaciones (Manual de Seguridad Biolgica) en el que se identifiquen los riesgos que pueda sufrir el personal y que
especifique los procedimientos que puedan minimizar esos riesgos.
Equipo de seguridad (barreras primarias). Se incluyen en este apartado tanto dispositivos o aparatos que garantizan la seguridad (ej. las cabinas de seguridad biolgica), como las prendas de proteccin personal (guantes, mascarillas, batas,...). Diseo y construccin de la instalacin (barreras secundarias). La magnitud de las barreras secundarias depender del tipo de agente infeccioso que se manipule en el laboratorio. Dentro de ellas se incluyen la separacin de las zonas donde tiene acceso el pblico, la disponibilidad de sistemas de descontaminacin (autoclaves), el filtrado del aire de salida al exterior, el flujo de aire direccional, etc.
Niveles: Existen cuatro niveles de contencin o de seguridad biolgica en funcin de la combinacin de los tres elementos descritos. Nivel 1. Es el nivel de seguridad requerido para los agentes biolgicos del grupo 1, es decir, los que no producen enfermedad en el ser humano sano y de susceptibilidad conocida y estable a los antimicrobianos. Es el utilizado habitualmente en los laboratorios de prcticas de universidades o centros docentes donde se emplean cepas no patgenas. Nivel 2. Es el obligado para agentes del grupo 2 como algunos que, perteneciendo a la propia flora habitual del hombre, son capaces de originar patologa infecciosa humana de gravedad moderada o limitada. Deben ser manipulados por personal especializado y son los que con ms frecuencia se estudian en el Laboratorio de Microbiologa Clnica. Nivel 3. Cuando se manipulan agentes biolgicos del grupo 3, microorganismos que causan patologa grave, de difcil y largo tratamiento, que pueden curar con secuelas y a veces producir la muerte. El mayor y ms frecuente peligro que entraan stos es la infeccin adquirida a travs de aerosoles y por fluidos biolgicos. Por ello, las principales medidas a tomar en este caso son la correcta manipulacin y la utilizacin de cabinas de seguridad. En este grupo estn: M. tuberculosis, Brucella, Coxiella burneti, etc. Slo pueden ser procesados por personal cualificado y en una zona con la infraestructura apropiada para el Nivel de Contencin 3, es decir, con aire acondicionado independiente, sin recirculacin de aire, con gradiente de presin, cabinas de bioseguridad, etc. Nivel 4. Nivel requerido cuando se procesa con certeza o se sospecha un agente especialmente patgeno e infectocontagioso, extico o no, que produce alta mortalidad y para el que no existe tratamiento y/o es poco fiable. Normalmente son microorganismos de dosis infectiva baja y alta contagiosidad. Este nivel tambin puede utilizarse para trabajar con animales de experimentacin infectados por microorganismos del grupo 4. En este grupo estn los virus de la fiebre de Lassa, virus Machupo, virus Ebola, etc. Adems, deben incluirse en este nivel de contencin los microorganismos del grupo 3 que adquieran propiedades patgenas que los eleven al grupo 4 (Mycobacterium multirresistente). En general, la naturaleza infecciosa del material clnico es desconocida y al Laboratorio de Microbiologa suelen remitirse muestras
muy diversas. Excepto en casos excepcionales, el procesamiento inicial de las muestras clnicas y las pruebas serolgicas pueden realizarse de forma segura en un nivel 2, que es el recomendado para trabajar con patgenos que se transmiten por va sangunea (virus de la hepatitis B, VIH, etc.), a lo que habra que aadir las precauciones universales que deben ser tomadas con todas las muestras de sangre y otros materiales potencialmente infecciosos.
4.- Equipos proteccin
Los equipos de proteccin individual que pueden ser necesarios, en algn momento, en un Laboratorio de Microbiologa Clnica: los protectores de los ojos y de la cara (gafas de seguridad, pantallas faciales), los protectores de las vas respiratorias (mascarillas, mscaras), los protectores de manos y brazos (guantes, manguitos), los protectores de la totalidad del cuerpo (batas)
Cabinas de seguridad biolgica (CSB)
Son cmaras de circulacin forzada que, segn sus especificaciones proteccin. Imprescindibles en un Laboratorio de Microbiologa Clnica.
diseo,
proporcionan
diferentes
niveles
de
Es necesario distinguir entre las campanas de extraccin de gases, las cabinas de flujo laminar y las cabinas de Seguridad Biolgica. La campana de gases es un recinto ventilado que captura los humos y vapores procedentes de la manipulacin de los productos qumicos. Es un equipo muy til en la contencin del riesgo qumico, NO ofrece proteccin frente a riesgos biolgicos. Las cabinas de flujo laminar son recintos que emplean un ventilador para forzar el paso del aire a travs de un filtro HEPA (High Efficiency Particulate Air) barriendo la superficie de trabajo. Estas cabinas ofrecen proteccin nicamente al material que se maneja en su interior, nunca al operador (no son recomendables en un Laboratorio de Microbiologa Clnica). Las cabinas de Seguridad Biolgica son recintos ventilados diseados para limitar al mximo el riesgo del personal de laboratorio expuesto a agentes infecciosos (aerosolos, etc.). Estos equipos proporcionan una zona de trabajo que minimiza la probabilidad que una partcula transportada por el aire pueda escapar hacia el exterior de la cabina y contaminar al operario y a la zona que le rodea. Adems, algunas de ellas, ofrecen proteccin al material que se manipula. Una cabina nunca es un sustituto de una tcnica microbiolgica adecuada.
Clasificacin: segn el nivel y tipo de proteccin. Las CSB disponen de dos sistemas que impiden la salida de contaminacin: las barreras de aire y los filtros. Las barreras de aire se crean permitiendo que ste fluya en una sola direccin y a una velocidad constante dando lugar a una verdadera "cortina" de aire (flujo de aire laminar). Es un flujo con ausencia de turbulencias. Los filtros tienen como finalidad atrapar las partculas contenidas en este flujo de aire y los empleados habitualmente son los HEPA, que retienen con una eficacia del 99,97% partculas de hasta 0,3 micras de dimetro. Existen tres categoras: Cabinas de clase I. Son cmaras cerradas con una abertura al frente para permitir el acceso de los brazos del operador. El aire penetra el frontal, atraviesa la zona de trabajo y sale al exterior a travs de un filtro HEPA. Son apropiadas para manipular agentes biolgicos de los grupos 1, 2 3. No proporcionan proteccin al material con el que se trabaja, no evita que se pueda contaminar. Cabinas de clase II. Se diferencian de las de clase I en que, adems ofrecen proteccin al material frente a la contaminacin. La superficie de trabajo est atravesada por aire limpio que ha pasado a travs de un filtro HEPA. La salida del aire se produce a travs de otro filtro HEPA. Son equipos vlidos para el manejo de agentes biolgicos de los grupos 1, 2 3. Existen varios tipos de cabinas de clase
II, A, B1, B2 y B3, segn sus caractersticas de construccin, flujo de aire y sistema de extraccin. Cabinas de clase III. Constituyen el mximo nivel de seguridad. Son recintos hermticos en presin negativa y, por ello, su interior est completamente aislado del entorno. Se opera en ellas por medio de unos guantes, con trampa para introducir el producto, el aire entra a travs de un filtro HEPA y se expulsa al exterior a travs de dos filtros HEPA. Se recomiendan para el manejo de agentes de los grupos 1, 2, 3 4.
Clase I
Clase II
Clase III
Eleccin del equipo
Procedimiento de trabajo
Al inicial el trabajo: 1. Poner en marcha la cabina durante 5-10 minutos, a fin de purgar los filtros y "lavar" la zona protegida. 2. Comprobar que el manmetro situado en la parte superior del frontal se estabiliza e indica la presin adecuada (vara con el modelo de cabina). 3. Apagar la luz ultravioleta (si estuviera encendida) y encender la luz fluorescente. 4. Limpiar la superficie de trabajo con un producto adecuado (por ejemplo, alcohol etlico al 70%). 5. Antes y despus de haber trabajado en una cabina deberan lavarse con cuidado manos y brazos, prestando especial atencin a las uas 6. Se deben usar batas de manga larga con bocamangas ajustadas y guantes de ltex. 7. En determinados casos, adems es recomendable el empleo de mascarilla. Durante la manipulacin: 1. Todo el material a utilizar se sita en la zona de trabajo antes de empezar. 2. Es aconsejable haber descontaminado el exterior del material que se ha introducido en la cabina.
3. Este material se coloca con un orden lgico, de manera que el material contaminado se sita en un extremo de la superficie de trabajo y el no contaminado ocupa el extremo opuesto de la misma. 4. Segn el tipo de manipulacin y el modelo de la cabina, la zona de mxima seguridad dentro de la superficie de trabajo vara. En general, se recomienda trabajar a unos 5-10 cm por encima de la superficie y alejado de los bordes de la misma. Especial atencin se prestar a no obstruir las rejillas del aire con materiales o residuos. 5. Una vez que el trabajo haya comenzado y sea imprescindible la introduccin de nuevo material, se recomienda esperar 2-3 minutos antes de reiniciar la tarea. 6. Mantener al mnimo la actividad del laboratorio en el que se localiza la cabina en uso, a fin de evitar corrientes de aire que perturben el flujo. 7. Evitar los movimientos bruscos dentro de la cabina. El movimiento de los brazos y manos ser lento, para as impedir la formacin de corrientes de aire que alteren el flujo laminar. 8. Al igual que en el resto del laboratorio, no debe utilizarse el mechero Bunsen, cuya llama crea turbulencias en el flujo y adems puede daar el filtro HEPA. 9. Cuando deban emplearse asas de platino es aconsejable el incinerador elctrico o, mejor an, asas desechables. 10. Si se produce un vertido accidental de material biolgico se recoger inmediatamente, descontaminado la superficie de trabajo y todo el material que en ese momento exista dentro de la cabina. 11. No se utilizar nunca una cabina cuando est sonando alguna de sus alarmas. Al finalizar el trabajo: 1. Limpiar el exterior de todo el material que se haya contaminado. 2. Vaciar la cabina por completo de cualquier material. 3. Limpiar y descontaminar con alcohol etlico al 70%. 4. Dejar en marcha la cabina durante al menos 15 minutos. 5. Conectar si fuera necesario la luz ultravioleta (UV) y recordar que su capacidad descontaminante es muy limitada. Limpieza y desinfeccin de la CSB 1. Se llevar a cabo una desinfeccin completa en las siguientes situaciones: a) en caso de que se haya producido un vertido importante; b) antes de cualquier reparacin; c) antes de iniciarse los chequeos peridicos; d) siempre que se cambie el programa de
trabajo; e) cuando se substituyan los filtros HEPA y f) al cambiarla de lugar (incluso dentro del mismo laboratorio). 2. Se realizar con vapores de formaldehdo y siempre por personal debidamente entrenado y con las prendas de proteccin personal adecuadas. 3. Una buena limpieza de la zona de trabajo es una garanta de ausencia de polvo y otros contaminantes. 4. Es conveniente una vez a la semana levantar la superficie de trabajo y limpiar y descontaminar por debajo de ella. 5. Nunca se debe utilizar la cabina como almacn transitorio de equipo o material de laboratorio. 6. Evitar introducir en la cabina materiales que emitan partculas fcilmente como algodn, papel, madera, cartn, lpices... Control de aerosoles infecciosos. Se generan en el procesamiento de muestras o cultivos como: a.- Manipulacin de microorganismos del grupo de riesgo 3. b.- Machacamiento de tejidos. c.- Descontaminacin de muestras para cultivo de Micobacterias. d.- Procedimientos de identificacin de hongos. e.- Utilizacin del Vortex para mezclar muestras con microorganismos del grupo de riesgo 3. f.- Decantacin de lquidos en muestras con microorganismos del grupo de riesgo 3. Proteccin de muestras o materiales de la contaminacin externa: a.- Procesamiento de lquidos orgnicos estriles con microorganismos del grupo de riesgo 3. b.- Cultivos celulares. c.- Preparacin de soluciones de medios y reactivos que deban ser estriles.
Microbiologa General y Bucal Prctica 3: Toma de muestras, transporte y conservacin
Pgina principal Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6 Las principales dificultades para realizar un estudio clnico-microbiolgico son: a) obtener una muestra fehaciente que est exenta de contaminacin con los fluidos orales y/o otros contaminantes b) el utilizar medios y condiciones de cultivo ptimas para la reproduccin del mximo posible de microorganismos c) emplear mtodos precisos para la identificacin y la tipificacin de los microorganismos reproducidos.
Normas generales
Obtencin de muestras:
Deben realizarse en condiciones de mxima asepsia, evitando contaminaciones ambientales, del personal mdico y del propio enfermo. No debe estar en contacto con sustancias desinfectantes.
Volante de peticin: se har constar al menos:
Identificacin del paciente. Identificacin del mdico. Datos de la muestra (hora de recogida, tipo de muestra, localizacin anatmica, procedimiento de obtencin de la muestra). Determinaciones solicitadas.
Identificacin de la muestra: Cada muestra debe estar acompaada siempre de un volante. El recipiente debe identificarse con nombre y apellidos, tipo de muestra, fecha, y hora de extraccin (imprescindible en los hemocultivos). Debern tener
etiqueta de color segn su conservacin (en estufa, en nevera o a temperatura ambiente).
Transporte
Se realizar de forma inmediata y se utilizar: 1. Envase estril de boca ancha:
Para: biopsias, tejidos, orinas, escamas, lquidos, esputos, secreciones bronquiales.
2. Port-A-Cul vial (medio de Cary Blair):
Para: lquidos y exudados obtenidos por aspiracin.
3. Port-A-Cul tubo (medio de Cary Blair):
Para: raspados de heridas, escaras, abscesos, lceras, pequeas biopsias y tejidos.
4. Hisopo con medio de transporte Stuart:
Para: abscesos y heridas recogidas con escobilln. No vlido para: anaerobios y micobacterias.
5. Tubo estril:
Para: lquidos estriles. No vlido para: anaerobios, ni para lquidos con alto contenido hemtico.
6. Medio de transporte para virus:
Para: aspirados nasofarngeos, exudados y biopsias.
7. Tubo de plstico estril:
Para: catteres (no ms de 4 cm), tejidos y lquidos.
8. Hemocultivos:
Para: sangre y lquidos estriles.
8: distintas posibilidades de hemocultivos
Conservacin de las muestras
Muestras para Bacteriologa:
A temperatura ambiente: mdula sea, lquidos estriles (pleural, peritoneal, articular,...), muestras oculares, muestras de cavidad oral, heridas, abscesos, fstulas, adenopatas, del tracto genital, y biopsias. En NEVERA: orinas, heces, catteres. En ESTUFA: hemocultivos, LCR, placas y tubos inoculados.
Muestras para anaerobios: a Temperatura ambiente. Muestras para micobacterias: en NEVERA, salvo contenido gstrico. Muestras para virus: en NEVERA, salvo sangre, mdula sea, y Ag CMV. Muestras para hongos: en NEVERA, salvo LCR, piel, pelo, uas, vaginal y balano-prepucial. Segn el microorganismo a investigar:
ANAEROBIOS: Mxima asepsia. ASPIRAR. Conservacin a T ambiente. Enviar en PORT-A-CUL. MICOBACTERIAS: No recoger con escobilln. Conservar en nevera. Enviar en envases estriles de boca ancha. Rapidez en envo. HONGOS: ASPIRAR Y RASPAR. Conservar en nevera (excepto tracto genital, uas, pelo,...). Rapidez en envo.
VIRUS: Tomar muestras en estadio precoz. Transporte especfico. Conservacin en nevera.
Estufa
Nevera
Criterios de rechazo de una muestra
Mala cumplimentacin del volante y/o de la muestra. Muestras derramadas, o rotas,... Muestra no adecuada para la prueba solicitada. Muestras sin medio de transporte adecuado.
Toma de muestras en odontologa:
Principios generales La toma de muestra en la cavidad bucal no es tarea fcil ya que es un ecosistema abierto donde conviven tejidos duros y blandos tapizados por mucosa colonizada con un gran nmero de microorganismos. La mayora de los procesos suelen ser de origen polimicrobianos, siendo las bacterias anaerobias estrictas los agentes etiopatognicos ms frecuentes. Las muestras odontolgicas son totalmente distintas a las de otras localizaciones. Las tomas obtenidas mediante biopsias y los volmenes obtenidos de punciones de abscesos o fluidos creviculares, son pequeos y estos ltimos pueden incluso encontrarse absorbidos en puntas de papel. Es importante que sean recogidas y manipuladas correctamente cumpliendo con normas de bioseguridad y protocolos estandarizados.
Caractersticas de la muestra 1. Deben ser representativas del proceso a investigar tanto en cantidad como en calidad de la muestra. 2. Estar libre de contaminacin de la microbiota de la boca. 3. Usar un medio de transporte adecuado. 4. Identificacin adecuada 5. La conservacin debe ser correcta tanto en temperatura y atmsfera 6. Enviar al laboratorio en el menor tiempo posible El incumplimiento de estas indicaciones puede dar lugar a una contaminacin de la muestra con microorganismos de la microbiota, la no viabilidad de los microorganismos etiopatognicos o un sobrecrecimiento de microorganismos acompaantes. Si esto ocurre el informe microbiolgico ser incorrecto y las medidas teraputicas inadecuadas
Material necesario - Algodn - Hisopos. - Puntas de papel.
- Anestsico local. - Cureta. - Sistema para el transporte de anaerobios. Las muestras se remiten rpidamente, evitando el contacto con el oxgeno y la desecacin. Es utilizado medios de transporte adecuados.
Tipos de muestra
Deteccin de hongos (candidiasis oral) Obtencin de la muestra: Solicitar al paciente que se enjuague la boca con agua. Frotar las lesiones con una torunda humedecida con suero fisiolgico. Hacer una extensin sobre un portaobjetos. Repetir la toma con una torunda para el cultivo. Si no se dispone de portaobjetos, enviar las dos torundas sin medio de transporte. Envo al Laboratorio: rpido. Mientras tanto conservar a 4 C. Enviar la torunda sin medio de transporte.
Cultivo absceso perioral/gingival
Obtencin de la muestra: La muestra debe recogerse por aspiracin y drenaje a travs de la superficie externa de la piel no afectada. Si fuere necesario recogerla a travs de las membranas mucosas de la cavidad oral, se aislar la zona con rollos de algodn, se secar con torundas de algodn y se desinfectar con Povidona durante 1 minuto antes de insertar la aguja. Aspirar el contenido del absceso. Reemplazar la aguja por otra nueva, eliminar el aire con algo de muestra, e inocularla en un medio de transporte de muestras de anaerobios, evitando la entrada de aire. La flora presente en las secreciones orales es la que se encuentra normalmente en los abscesos periorales, por tanto es esencial evitar la contaminacin durante el proceso de recogida. Las torundas de sitios orales no sirven para el cultivo. El volumen mnimo recomendado es de 1 ml. Envo al Laboratorio: debe ser inmediato. Mientras tanto mantenerla a temperatura ambiente. La muestra debe ir en el medio de transporte adecuado.
Cultivo de placa subgingival/supragingival Obtencin de la muestra: Tras aislar la zona de donde se obtendr la muestra con rollos de algodn y secarla con torundas de algodn, obtener la mayor cantidad posible de muestra con cureta estril. Introducir en un tubo de caldo tioglicolato. Envo al Laboratorio: rpido. Mientras tanto mantenerla a 35 - 37C. Se debe enviar la mayor cantidad posible en tubo de caldo tioglicolato.
Cultivo de canal dental Obtencin de la muestra: Se desinfecta y se introduce en el canal 1 2 puntas de papel estril hasta el fondo del canal y se dejan 10 segundos. Introducir las puntas en el fondo de un tubo de caldo tioglicolato. Obtener la mayor cantidad posible Envo al Laboratorio: debe ser inmediato. Mientras tanto mantener a 35-37C.
Cultivo de bolsa periodontal Obtencin de la muestra: El rea de donde se toma la muestra se asla con rollos de algodn y se seca con torundas de algodn estriles. Para desinfectar y secar la superficie
puede usarse etanol al 70%. Eliminar la placa supragingival y obtener la muestra con cureta estril introducindola lo ms vertical posible hasta el fondo de la bolsa periodontal. Obtener la mayor cantidad posible. Introducir la muestra en un tubo de caldo tioglicolato. Envo al Laboratorio: debe ser inmediato. Mientras tanto mantener a 35-37C. Se debe enviar la mayor cantidad posible en un tubo de caldo tioglicolato.
Microbiologa General y Bucal Prctica 4: Diagnstico microbiolgico directo
Pgina principal Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6
En el Laboratorio de Microbiologa el microorganismo o sus productos pueden detectarse a travs de: 1.- Visualizacin Uno de los procedimientos bsicos y no por ello menos importante es la visualizacin del microorganismo en las muestras.
El microscopio ptico es el ms utilizado en los laboratorios de microbiologa de forma rutinaria. Tambin pueden emplearse el de campo oscuro,contraste de fases, fluorescencia o electrnico.
El examen microscpico requiere la utilizacin del microscopio. Puede hacerse una visualizacin microscpica en 2 momentos: a) directamente de la muestra clnica y b) a partir de los microorganismos obtenidos por cultivo como primer escaln en la identificacin.
Cmo se pueden ver los microorganismos?
Puede realizarse 1-Directamente: examen en fresco. Se estudian las bacterias "al natural", sin teir. Tiene el inconveniente de que las bacterias tienen una densidad ptica similar a la del agua (transparentes) por lo que es difcil examinarlas.
2-Mediante una tcnica denominada gota pendiente que se utiliza para observar la movilidad. 3-Tinciones negativas (Tinta china). No son una verdadera tincin. Se llaman as porque lo que realmente se tie es el fondo sobre el que estn los microorganismos apareciendo los microorganismos sin teir. Se emplea para ver la cpsula de S. pneumoniae y Cryptococcus neoformans en LCR.
4-Tinciones. Existen muchas y en general se pueden clasificar en:
4.1. simples (utilizan un solo colorante). Por ejemplo: azul de metileno para observacin de levaduras y protozoos intestinales 4.2. diferenciales (utilizan ms de un colorante y permiten la agrupacin de las bacterias de acuerdo a su diferente afinidad tintorial). Destacan latincin de Gram que agrupa a las bacterias en dos grandes bloques, bacterias grampositivas y bacterias gramnegativas, y la de Ziehl-Neelsenutilizada, entre otros, para la tincin de micobacterias.
4.3. especiales: tinciones fluorescentes, tinciones de determinadas estructuras como la tincin del esporo, tincin de flagelos...
Tincin de Gram:
PASOS Colorante principal: cristal violeta Mordiente: Lugol Decolorante: acetona Colorante contraste:safranina
GRAMPOSITIVAS Violeta
GRAMNEGATIVAS Violeta
Violeta alcohol- Violeta
Violeta Transparente
de Violeta
Rojo
Cmo se ven las bacterias tras realizar una tincin de Gram?
A travs de la tincin de Gram pueden valorarse la afinidad tintorial, forma y agrupaciones de las bacterias. -Afinidad tintorial. Permite dividir a las bacterias en 1) grampositivas (violetas) que retienen el colorante principal tras la decoloracin con alcohol o alcohol-acetona y 2) gramnegativas (rojas) que pierden el colorante principal tras la decoloracin por lo que es necesario aplicar un colorante de contraste para visualizarlas. Esta diferencia de coloracin est basada en la diferencia estructural de la pared. En las grampositivas el colorante se fija fuertemente al peptidoglicano que lo "retiene" e impide que "salga" con el decolorante. En las gramnegativas el colorante es retenido con menos fuerza al ser ms delgada la capa de peptidoglicano. Adems la mayor cantidad de lpidos presentes hace que el colorante se elimine al solubiliarse los lpidos en el alcohol. - Pueden tener diferentes formas: - esfricas: cocos (Streptococcus spp., Staphylococcus spp., etc) - cilndricas: bacilos (enterobacterias, Pseudomonasspp., etc...) - espiroquetas: Treponema pallidum, Borrelia burgdorferi - Pueden aparecer aisladas o asociarse en parejas [diplococcos: (Neisseria gonorrhoeae, Streptococcus pneumoniae)], cadenas (estreptococcos), tetradas, sarcinas, racimos (estafilococos), "letras chinas" (corinebacterias), etc - Tamao: las bacterias se miden en metros (1metro = 10-3 mm) y, en general y como ejemplo, las bacterias esfricas tienen un dimetro de 1m y las bacterias alargadas 1.5-8 m de longitud, aunque este parmetro vara en funcin de los diferentes gneros bacterianos.
Cocos grampositivos
Bacilos grampositivos
Bacilos gramnegativos
Visualizacin de la tincin de Gram
2.- Aislamiento en cultivo y posterior identificacin por sus caractersticas fenotpicas (morfologa, caractersticas metablicas -pruebas bioqumicas y enzimticas-, etc.) Cmo se cultivan en el laboratorio? Se utilizan medios de cultivo compuestos por una mezcla de nutrientes (protenas, hidratos de carbono, minerales, oligoelementos...) que permiten el crecimiento de las bacterias en el laboratorio, in vitro. Los medios de cultivo pueden clasificarse atendiendo a varios parmetros: a) Segn su origen pueden ser 1) naturales: constituidos por sustancias naturales de composicin compleja y en ocasiones variable
(extracto de carne, extracto de levadura, patata...), 2) sintticos o qumicamente definidos en los que se conoce la participacin exacta de hidratos de carbono, aminocidos.... y 3) semisintticos. b) Segn su consistencia pueden ser 1) lquidos, 2) slidos: son medios lquidos a los que se les aade para darles consistencia una sustancia gelificante (agar-agar) obtenida de algas marinas y 3) semislidos: lquidos a los que se les aade menor concentracin de agar que a los slidos. Cada uno tiene sus finalidades. En la superficie de los medios slidos es posible ver las colonias resultantes de la multiplicacin bacteriana. Los medios lquidos facilitan el crecimiento de las bacterias pero en ellos no se ven colonias, el crecimiento suele detectarse por turbidez. Los medios semislidos suelen utilizarse para valorar la movilidad de los microorganismos. c) De acuerdo a su finalidad y aplicacin pueden ser: 1.- Bsicos: aquellos que llevan todos los elementos bsicos para el desarrollo de los microorganismos no exigentes. 2.- Enriquecidos: incorporan diferentes sustancias para permitir el crecimiento de microorganismos ms exigentes. Ej.: agar sangre, agar chocolate,...
3.- Selectivos: medios a los que se aaden diferentes sustancias (colorantes, sales biliares, antibiticos...) que son capaces de inhibir a
determinados microorganismos y permitir el crecimiento de otros. En general se utilizan para inhibir el crecimiento de la flora acompaante y permitir el crecimiento del patgeno. Tambin colaboran en la identificacin pues proporcionan un parmetro ms: no se inhibe por... 4.- Diferenciales: se les aade un hidrato de carbono y un indicados de pH de forma que si el microorganismo es capaz de utilizar ese hidrato de carbono se produce un cambio de pH que hace que el indicador cambie de color y evidencie la reaccin. As las colonias son fcilmente reconocibles por su color.
5.- Otros medios: de enriquecimiento (son medios lquidos a los que se les aades sustancias que inhiben el crecimiento de microorganismos acompaantes favoreciendo el crecimiento de otros (los patgenos buscados), de transporte, etc.
Siembra de los medios de cultivo Lo primero que hay que hacer es sembrar la muestra en los medios de cultivo reseados. Una vez cultivada se procede al aislamiento en cultivo y posterior identificacin por sus caractersticas fenotpicas (morfologa, caractersticas metablicas -pruebas bioqumicas y enzimticas-, etc.).
Prodecimientos de siembra 1 Procedimientos de siembra 2 Esquemas
Cuando la siembra se realiza a partir de un cultivo debe obtenerse una pequea porcin del mismo. Condiciones de cultivo -Temperatura: la mayora crecen bien a temperaturas entre 35-37C aunque hay excepciones -Tiempo de incubacin: depende del tiempo de generacin (tiempo requerido para que el nmero de bacterias se duplique) de cada microorganismo. Generalmente 18-24 h. Otros requieren ms tiempo de incubacin: Brucella spp. , M. tuberculosis. -Atmsfera de incubacin. Los microorganismos respecto al tipo de respiracin pueden ser: 1.- Aerobios: requieren la presencia de oxgeno molecular. 2.- Anaerobios facultativos: pueden vivir y multiplicarse en presencia o en ausencia de oxgeno. 3.- Anaerobios: el oxgeno libre es txico para ellos (algunos son aerotolerantes). 4.- Microaerofilos: necesitan la presencia de oxgeno libre pero a una concentracin menor que la atmosfrica (2-10%). Este hecho tiene como consecuencia que haya que incubarlos en estas condiciones. Otros hay que incubarlos en una atmsfera con un 5-10% de CO2 (no es tipo de respiracin sino un requerimiento): se denominan capnfilos
Identificacin Se valoran entre otros parmetros: 1) morfologa y aspecto de las colonias (masa constituida por bacterias que es visible a simple viste en la superficie de los medios slidos).
2) capacidad de crecer a una determinada temperatura 3) crecimiento en medios selectivos y diferenciales
4) presencia de hemlisis que en los medios con sangre da lugar a la aparicin de un halo alrededor de la colonia. Puede ser transparente (hemlisis total o -hemlisis), verdoso (hemlisis parcial o -hemlisis o no aparecer (no hemolticas o hemlisis)
5) pruebas bioqumicas y enzimticas adecuadas para la bacteria que se sospeche por las pruebas preliminares
6) movilidad
3.- deteccin de productos estructurales: antgenos (reacciones antgeno-anticuerpo), cidos nucleicos (hibridacin, PCR, etc)
3.1. deteccin de antgenos se vern con ms detalle al estudiar las reacciones antgeno-anticuerpo
3.2. tcnicas genticas de deteccin de cidos nucleicos: hibridacin, Reaccin en Cadena de la Polimerasa (PCR), etc. 3.2.1. Reaccin en Cadena de la Polimerasa (PCR): En 1983, Kary Mullis dio a conocer la tcnica de la reaccin en cadena de la polimerasa que es una tcnica para la sntesis in vitro de secuencias especficas de DNA evitandop de esta forma uno de los principales problemas que se planteaban que era la insuficiente cantidad de ADN para realizar ciualquier procedimiento de laboratorio. La tcnica se basa en la replicacin del ADN inducida por la DNA polimerasa, enzima que es capaz de real9izar una sntesis de una cadena complementaria de ADN en el sentido 5-> 3 usando un molde de cadena sencilla, pero a partir de una regin de doble cadena. Para crear esta regin doble cadena se usan los denominados iniciadores (primers). Son una pareja de oligonucletidos sintetizados de manera que sean complementarios a cada uno de los extremos 3 del fragmento de ADN que se desea amplificar.
Partiendo de este principio, la PCR se basa en la repeticin de ciclos que estn formados por tres etapas: 1.- Desnaturalizacin del ADN doble cadena: la doble hlice de ADN se separa en dos hebras. Para ello se realiza una incubacin de la muestra a altas temperaturas (93-97C). La renaturalizacin se producir cuando la temperatura disminuya. 2.- Hibridacin de los iniciadores a la zona 3 especfica de cada una de las hebras: los cebadores, iniciadores o primers se unen a las zonas 3 complementarias que flanquean el fragmento que queremos amplificar. Se realiza gracias a la bajada de la temperatura (50-65 C). 3.- Extensin del cebador por actuacin de la DNA polimerasa (elongacin): se produce la sntesis de una cadena sencilla (producindose un fragmento de doble cadena por la complementariedad) en la direccin 5-> 3 mediante la enzima DNA polimerasa, la cual incorpora los desoxinucletidos fosfato presentes en el medio siguiendo la cadena molde. Este proceso se lleva a cabo en un equipo llamado termociclador que realiza los ciclos en los tiempos y temperaturas programadas.
Esquemas de trabajo
Elementos qumicos necesarios para realizar la PCR
Termociclador
Carga de un gel de agarosa
Lectura de un gel de agarosa, teido con bromuro de etidio, bajo la luz ultravioleta
3.2.2. Hibridacin La hibridacin o renaturalizacin de cidos nucleicos (ARN o ADN) es un proceso por el cual se combinan dos cadenas de cidos nucleicos antiparalelas y con secuencia de bases complementarias, en una nica molcula de doble cadena, que toma la estructura de doble hlice, donde las bases nitrogenadas quedan ocultas en el interior. Se utiliza una cadena sencilla de ADN marcada por un mtodo fsico-qumico, bien sea radiactivo o con un fluorocromo. Esta cadena tiene
una secuencia de nucletidos conocida y se utiliza como sonda para detectar otras molculas de ARN o ADN de cadena sencilla de secuencia parecida. En el esquema est representado el fundamento de la tcnica.
Para saber ms
4.- deteccin de productos metablicos: Cromatografa (anaerobios, micobacterias), ATP bacteriano (bioluminiscencia), toxinas, etc. 4.1. cromatografa se basa en la identificacin de microorganismos a partir de productos de su metabolismo (alcoholes, cidos grasos) o de componentes de la pared celular. Se emplea sobre todo para la identificacin de micobacterias y anaerobios.
Algunas de estas tcnicas como la PCR pueden utilizarse para realizar el diagnstico directamente sobre la muestra clnica sin necesidad de hacer un cultivo previo.
REACCIONES ANTGENO ANTICUERPO Son estrategias de laboratorio que permiten detectar que una reaccin antgeno-anticuerpo producida en el laboratorio ha tenido lugar. Se basan en la especificidad de la reaccin, es decir, en que un anticuerpo slo reaccionar con el antgeno que haya dado lugar a su formacin. Pueden utilizarse para realizar tanto diagnstico directo como indirecto. Si conocemos el anticuerpo (estn disponibles en el laboratorio, por ej. anticuerpos monoclonales) podremos identificar el antgeno (en la muestra clnica) que reacciona especficamente con l: diagnstico directo. Ejemplo de identificacin serolgica de estreptococos del grupo A (parte 1) Ejemplo de identificacin serolgica de estreptococos del grupo A (parte 2)
La inmunofluorescencia es una tcnica que emplea anticuerpos conjugados a fluorocromos. Los fluorocromos son molculas que al ser excitadas con la energa de una determinada longitud de onda son capaces de emitir energa de una longitud de onda mayor. Una de las tcnicas ms utilizadas es la Inmunofluorescencia Directa que permite la deteccin de antgenos en un paso. Utiliza anticuerpos conjugados a isotiocianato de fluorescena. La lectura se realiza en un microscopio de fluorescencia, que emite luz ultravioleta de una determinada longitud de onda.
Reaccin positiva Reaccin negativa La inmunofluorescencia indirecta permite la deteccin de anticuerpos circulantes. Si el antgeno es conocido (disponible en el laboratorio), detectaremos los anticuerpos que se encuentran en la muestra clnica y por tanto son desconocidos y que reaccionan especficamente con ellos:diagnstico indirecto.
Otras tcnicas que se emplean en el diagnstico microbiolgico directo son: deteccin de antgeno capsular mediante tcnicas de aglutinacin con anticuerpos unido a partculas de ltex, CIE, RIA y EIA. La descripcin de estas tcnicas se vern en la prctica 5.
Microbiologa General y Bucal Prctica 5: Diagnstico microbiolgico indirecto
Pgina principal Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6 Se realiza en muestras de suero, utilizando diversos tipos de reacciones antgeno-anticuerpo: aglutinacin, precipitacin, fijacin del complemente, etc. El diagnstico indirecto suele utilizarse entre otros ante: - Imposibilidad de realizar un diagnstico directo - Cuando la realizacin del diagnstico directo es muy complicada o costosa - Estudios epidemiolgicos (por ejemplo para saber que porcentaje de poblacin ha tenido contacto con un determinado patgeno). Algunos conceptos importantes son: - Ttulo de un suero: es un concepto cuantitativo que determina la concentracin de anticuerpos de un suero determinado. Se realiza por una tcnica de diluciones seriadas. - Seroconversin: se define como el incremento (generalmente 4 veces) en la concentracin de anticuerpos especficos al comparar dos muestras de suero separadas en el tiempo, habitualmente 2 semanas. Indica la presencia de un estmulo antignico en ese momento. - Deteccin de IgM: determina infeccin aguda.
Algunas de las pruebas que se utilizan en el diagnstico microbiolgico indirecto son: Enzimoinmunoanlisis (Inmunoanlisis ligado a enzimas o tambin llamado enzimoinmunoanlisis de adsorcin): Tcnica inmunoqumica cuantitativa basada en reacciones antgeno-anticuerpo. El marcaje se hace con un enzima. Se puede marcar tanto el antgeno como el anticuerpo (hay distintas estrategias). La cuantificacin se hace, por tanto, basndose en la medida de la actividad del enzima marcador.Tras la formacin del complejo antgeno-anticuerpo, en el momento adecuado, seaade un sustrato que es catalizado por el enzima transformndose en un compuesto coloreado lo que permite la medida de la actividad enzimtica con ayuda de un espectrofotmetro.
ELISA. Es una variedad del EIA en la que se utiliza una fase slida como mtodo de separacin, lo que es lo ms habitual, recibe el nombre de ELISA (enzyme linked immunosorbent assay).
Reaccin de precipitacin:
Microbiologa General y Bucal Prctica 6: Antibiograma
Pgina principal Prctica 1 Prctica 2 Prctica 3 Prctica 4 Prctica 5 Prctica 6 PRUEBAS DE SENSIBILIDAD BACTERIANA Las pruebas de sensibilidad bacteriana se llevan a cabo mediante el antibiograma que sirve para medir la sensibilidad de una cepa bacteriana a uno o varios antibiticos. El estudio de la sensibilidad in vitro es uno de los requisitos previos para la eficacia in vivo de un tratamiento antibitico. Tambin es importante para realizar estudios sobre la evolucin de las resistencias bacterianas que permite revisar los protocolos de la antibioticoterapia emprica. Conceptos: La determinacin de la Concentracin Mnima Inhibidora (CMI) es la medida de la sensibilidad de una bacteria a un antibitico. Es la mnima cantidad de ntimicrobiano que es capaz de impedir el crecimiento de un microorganismo en unas condiciones normalizadas. Es el mtodo habitual utilizado en los laboratorios de Microbiologa Clnica. Para llevarlo a cabo es necesario utilizar cepas control (de referencia) con el fin de que los resultados sean reproducibles y comparables. Este mtodo nos ofrece informacin sobre la sensibilidad de las bacterias S (sensible), I (intermedia) y R (resistente). Sensible, si existe una buena probabilidad de xito teraputico en el caso de un tratamiento a la dosis habitual. Resistente, si la probabilidad de xito teraputico es nula o muy reducida. No es de esperar ningn efecto teraputico sea cual fuere el tipo de tratamiento. Intermedia, cuando el xito teraputico es imprevisible. Se puede conseguir efecto teraputico en ciertas condiciones (fuertes concentraciones locales o aumento de la posologa). Existen diferentes tcnicas de laboratorio que permiten medir o calcular de forma rutinaria, y de manera semicuantitativa, las CIM (mtodos manuales y mtodos automatizados o semiautomatizados). Se puede realizar mediante: 1.- Difusin en agar: Disco placa y E test 2.- Dilucin: Medio slido y Medio lquido (micro/macrodilucin)
3.- Mecanizados y Automatizados
La Concentracin Mnima Bactericida (CMB) es la mnima cantidad de antibitico capaz de destruir el 99,9% de una muestra inoculada en condiciones estandarizadas. Mtodos En un primer momento, el mtodo estndar utilizado para las pruebas in vitro fue el de dilucin en caldo, que proporcionaba un resultado cuantitativo. Actualmente existen varios mtodos que se utilizan para llevar a cabo los estudios de sensibilidad a los antibiticos y todos ellos se realizan bajo condiciones entandarizadas por organismos internacionales.
Dilucin en caldo
Se colocan concentraciones decrecientes del agente antimicrobiano, generalmente diluciones 1:2, en tubos con un caldo de cultivo que mantiene el desarrollo del microorganismo. Los antibiticos se preparan en "soluciones madre" concentradas y luego se diluyen en caldo hasta obtener las concentraciones apropiadas. Un tubo de caldo se mantiene sin inocular como control negativo de crecimiento. Despus de un periodo de incubacin adecuada se observa la turbidez de los tubos que indica el desarrollo bacteriano. El microorganismo crecer en el tubo control y en todos los que no contengan suficiente antibitico que sea capaz de inhibir su desarrollo. La concentracin de antibitico que presente ausencia de crecimiento es la Concentracin Mnima Inhibitoria. Para medir la CMB se debe realizar la prueba de actividad bactericida, que emplea el mismo sistema de dilucin en caldo que para medir la sensibilidad. A partir de la CMI, se siembra una cantidad conocida de inculo de cada uno de los tubos de caldo que no tienen turbidez en placas de agar, y el nmero de colonias que crece en estos subcultivos, despus de incubar durante la noche, se compara con el nmero de UFC/ml del cultivo original. La mnima concentracin del agente antibacteriano que permite sobrevivir a menos de 0,1 % del inculo original se denomina concentracin bactericida mnima (CBM). Difusin en agar Este mtodo incorpora el antimicrobiano a discos de papel de filtro. Su introduccin permiti agilizar la determinacin de la sensibilidad de las cepas bacterianas frente a un nmero importante de antimicrobianos de forma simultanea. El empleo de los discos de papel de filtro para las pruebas de sensibilidad est estandarizado y se correlaciona con las CMIs. Durante muchos aos, y a pesar de ser una tcnica puramente cualitativa, el mtodo de difusin por disco (o mtodo Kirby-Bauer), en funcin sobre todo de su comodidad, economa y fiabilidad, ha sido uno de los ms utilizados en los laboratorios.
El microorganismo a investigar se inocula en una o varias placas de agar y sobre su superficie se disponen los discos correspondientes a varios antibiticos. Se incuban las placas durante 16-24 horas y se estudia el crecimiento en ellas. Se valora el dimetro de la zona de inhibicin que se forma alrededor de cada disco y se compara con las referencias oportunas publicadas por la NCCLS. De esta manera se sabe si el microorganismo es Sensible, Intermedio o Resistente a cada uno de los antibiticos.
Mtodo de E-test Es un mtodo ms reciente, es una combinacin de caractersticas de los mtodos anteriores. Se trata de una tcnica cuantitativa en placa que permite obtener una lectura directa de CMI en g/ml, ya que se emplean tiras plsticas impregnadas en concentraciones crecientes de antibitico. El microorganismo se inocula en una placa y sobre ella se deposita la tira del antibitico (o antibiticos) a ensayar. Se incuba durante 16-24 horas a 35C y se valora la zona de inhibicin alrededor de cada tira. La CMI se lee directamente observando el punto ms bajo de la elipse que presente el crecimiento.
E-Test
Mtodos automatizados La mayora de estos mtodos utilizan sistemas de microdilucin en medio lquido sobre microplacas con pocillos en "U" e interpretan el crecimiento bacteriano en los diferentes pocillos por medio de un autoanalizador (mediciones por turbidez o fluorescencia). Anteriormente se hacia por lectura ptica del tcnico a travs de un espejo invertido. Son sistemas fciles y rpidos, generalmente automatizada o semiautomatizada. Son mtodos ideales para grandes volmenes de trabajo. Una de sus grandes limitaciones es que slo ofrecen garanta para investigar microorganismos de crecimiento rpido y que no tengan requerimientos especiales.
Anda mungkin juga menyukai
- Pasos para Hacer Un Cuadro Sinoptico y Mapa ConceptualDokumen7 halamanPasos para Hacer Un Cuadro Sinoptico y Mapa ConceptualdrancerboyBelum ada peringkat
- Ciclo Hidrologico PDFDokumen44 halamanCiclo Hidrologico PDFJorge Antonio Limachi CastilloBelum ada peringkat
- Informe de TesisDokumen124 halamanInforme de TesisdrancerboyBelum ada peringkat
- Ley 29849 Eliminación Progresiva Del CAS PDFDokumen3 halamanLey 29849 Eliminación Progresiva Del CAS PDFJaime Ricardo Paz GómezBelum ada peringkat
- Economía Digital para El Cambio Estructural y La IgualdadDokumen132 halamanEconomía Digital para El Cambio Estructural y La IgualdadJoaquín Vicente Ramos RodríguezBelum ada peringkat
- EUGENESIADokumen24 halamanEUGENESIAdrancerboyBelum ada peringkat
- Recursos Hidricos de La Región TacnaDokumen11 halamanRecursos Hidricos de La Región TacnadrancerboyBelum ada peringkat
- Cultura Ambiental PDFDokumen119 halamanCultura Ambiental PDFzoilachavezBelum ada peringkat
- Presentacion Mamuta TruchasDokumen20 halamanPresentacion Mamuta TruchasdrancerboyBelum ada peringkat
- Aplicacion de La Metologia Fpeir en El Diagnostico Ambiental Del Rio UchusumaDokumen27 halamanAplicacion de La Metologia Fpeir en El Diagnostico Ambiental Del Rio UchusumadrancerboyBelum ada peringkat
- Aplicacion de La Metologia Fpeir en El Diagnostico Ambiental Del Rio UchusumaDokumen27 halamanAplicacion de La Metologia Fpeir en El Diagnostico Ambiental Del Rio UchusumadrancerboyBelum ada peringkat
- Reporte TecnicoDokumen7 halamanReporte TecnicodrancerboyBelum ada peringkat
- Tratamiento de Desinfección Del Agua Potable PDFDokumen132 halamanTratamiento de Desinfección Del Agua Potable PDFJesus Gomez PolancoBelum ada peringkat
- 6th Central Pay Commission Salary CalculatorDokumen15 halaman6th Central Pay Commission Salary Calculatorrakhonde100% (436)
- Analisis Canonico de CorrespondenciaDokumen17 halamanAnalisis Canonico de CorrespondenciadrancerboyBelum ada peringkat
- Contaminacion Por Metales Pesados PreguntasDokumen1 halamanContaminacion Por Metales Pesados PreguntasdrancerboyBelum ada peringkat
- Parasitosis intestinales agudas y crónicasDokumen14 halamanParasitosis intestinales agudas y crónicasdrancerboyBelum ada peringkat
- Clinica ClaseDokumen32 halamanClinica ClaseCristian QuispeBelum ada peringkat
- Completo Triptico de HelmintoDokumen2 halamanCompleto Triptico de HelmintodrancerboyBelum ada peringkat
- Beneficios de la linaza y el té verdeDokumen1 halamanBeneficios de la linaza y el té verdeJuan CarlosBelum ada peringkat
- Ciencias Naturales EsquemasDokumen74 halamanCiencias Naturales EsquemasAAAAABelum ada peringkat
- Anti Inflamatorios No Esteroideos Aines.Dokumen55 halamanAnti Inflamatorios No Esteroideos Aines.Angélica ContrerasBelum ada peringkat
- Amenaza de AbortoDokumen5 halamanAmenaza de AbortoRubi BarbozaBelum ada peringkat
- Manejo de Plagas UrbanasDokumen56 halamanManejo de Plagas UrbanasOK Servicio de fumigacion y control de plagas100% (2)
- Salud en La Republica de BoliviaDokumen17 halamanSalud en La Republica de BoliviaNorma VargasBelum ada peringkat
- MODELO - PRE - ACTA (MILAGRITOS UnidoDokumen8 halamanMODELO - PRE - ACTA (MILAGRITOS UnidoJHONATHAN ALEJANDRO BARROS DE LA CRUZBelum ada peringkat
- HemostasiaDokumen16 halamanHemostasiaEderth CorderoBelum ada peringkat
- Capitulo 7 ZygomycotaDokumen44 halamanCapitulo 7 ZygomycotaBelu AntiecoBelum ada peringkat
- Evaluacion 2, P Ii, 2° AñoDokumen9 halamanEvaluacion 2, P Ii, 2° AñoMateo Alejandro SnchzBelum ada peringkat
- Salud Bucal - Grupo 1Dokumen38 halamanSalud Bucal - Grupo 1Rosa ArrascueBelum ada peringkat
- Cultivo de CítricosDokumen6 halamanCultivo de CítricosJ.A. Barcena AlvarezBelum ada peringkat
- Cardiovascular DiseaseDokumen24 halamanCardiovascular DiseaseJormaris M. RuizBelum ada peringkat
- Plan HACCP CarozosDokumen20 halamanPlan HACCP Carozosdarwinismosilva100% (2)
- Nutrición Clínica - Lactancia Materna y Alimentación ComplementariaDokumen74 halamanNutrición Clínica - Lactancia Materna y Alimentación ComplementariaUSMP FN ARCHIVOSBelum ada peringkat
- Manual Sistema Gerencial Promotor SaludDokumen94 halamanManual Sistema Gerencial Promotor SaludLisset Portugal EspinozaBelum ada peringkat
- Situación Epidemiológica de Las Infecciones Respiratorias AgudasDokumen36 halamanSituación Epidemiológica de Las Infecciones Respiratorias AgudasVilly Nuñez Mejia100% (1)
- Monografia Caries DentalDokumen16 halamanMonografia Caries Dentalsiervajms88% (8)
- CriogenaDokumen2 halamanCriogenaJuan Henry SBelum ada peringkat
- Decreto 1338-96 de La Ley 24557Dokumen4 halamanDecreto 1338-96 de La Ley 24557Pablo Leonel Rodriguez0% (1)
- Examen clínico cardiológico de perros y gatosDokumen4 halamanExamen clínico cardiológico de perros y gatosLuis Alfredo Diaz OrtegaBelum ada peringkat
- Importancia regentes farmacia salud públicaDokumen6 halamanImportancia regentes farmacia salud públicaDaniela Sanchez0% (2)
- Ácido glutámico: el aminoácido clave para la salud cerebral y muscularDokumen3 halamanÁcido glutámico: el aminoácido clave para la salud cerebral y muscularKevin Cáceres ContrerasBelum ada peringkat
- 3 Repensando Los Orígenes de La Disforia de Género PDFDokumen18 halaman3 Repensando Los Orígenes de La Disforia de Género PDFAntonio Arroyo CornejoBelum ada peringkat
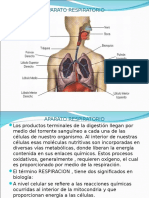
- Aparato RespiratorioDokumen22 halamanAparato RespiratorioLoreto Alejandra Henriquez PerezBelum ada peringkat
- 5 - Vértigo Posicional ParoxísticoDokumen3 halaman5 - Vértigo Posicional ParoxísticoValeria Rubilar LeclerBelum ada peringkat
- Estudio de La Actividad Antimicrobiana de Extractos Naturales y Acidos Organicos.Dokumen0 halamanEstudio de La Actividad Antimicrobiana de Extractos Naturales y Acidos Organicos.DiaNii HeRnandezBelum ada peringkat
- HCG, Rotavirus, TubosDokumen9 halamanHCG, Rotavirus, TubosBryan Steven Bazurto AcuñaBelum ada peringkat
- Guía de Actividades y Rúbrica de Evaluación - Paso 2. Reconocer Algunas de Las Principales Enfermedades de Origen ViralDokumen12 halamanGuía de Actividades y Rúbrica de Evaluación - Paso 2. Reconocer Algunas de Las Principales Enfermedades de Origen ViralAnonymous qcRLS49EPBelum ada peringkat
- Absorción de Fármacos y Vías de AdministraciónDokumen124 halamanAbsorción de Fármacos y Vías de AdministraciónGerardo Zaragoza Morales100% (1)