p.3 (Tramadol)
Diunggah oleh
Aprilia Ristian0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
159 tayangan16 halamanLaporan praktikum ini menjelaskan tentang penetapan kadar tramadol HCl dalam sediaan farmasi dengan metode titrasi redoks (iodometri). Tahapan yang dilakukan meliputi isolasi sampel, pembuatan larutan baku iodium dan natrium tiosulfat, serta penetapan kadar sampel dengan memanfaatkan reaksi oksidasi-reduksi antara iodium dengan tramadol HCl yang dititrasi dengan larutan natrium tiosulfat. Hasilnya menunjukkan
Deskripsi Asli:
tramadol
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOC, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniLaporan praktikum ini menjelaskan tentang penetapan kadar tramadol HCl dalam sediaan farmasi dengan metode titrasi redoks (iodometri). Tahapan yang dilakukan meliputi isolasi sampel, pembuatan larutan baku iodium dan natrium tiosulfat, serta penetapan kadar sampel dengan memanfaatkan reaksi oksidasi-reduksi antara iodium dengan tramadol HCl yang dititrasi dengan larutan natrium tiosulfat. Hasilnya menunjukkan
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
159 tayangan16 halamanp.3 (Tramadol)
Diunggah oleh
Aprilia RistianLaporan praktikum ini menjelaskan tentang penetapan kadar tramadol HCl dalam sediaan farmasi dengan metode titrasi redoks (iodometri). Tahapan yang dilakukan meliputi isolasi sampel, pembuatan larutan baku iodium dan natrium tiosulfat, serta penetapan kadar sampel dengan memanfaatkan reaksi oksidasi-reduksi antara iodium dengan tramadol HCl yang dititrasi dengan larutan natrium tiosulfat. Hasilnya menunjukkan
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 16
LAPORAN PRAKTIKUM
KIMIA FARMASI ANALISIS KUANTITATIF II
Penetapan Kadar Sampel Tramadol HCl dengan metode Titrasi Redeoks
( Iodimetri )
Oleh :
Kelompok 8
Fui Prati!i : ("####$%&)
'unung 'ur(anah : ("####$)#)
PRODI S1 FARMASI
STIKes BAKTI TUNAS HUSADA TASIKMALAYA
2014
*+ Tu(uan
,apat menentukan kadar Tramadol HCl dalam sediaan -armasi
dengan menggunakan metode Titrasi Redoks .iodimetri/+
0+ ,asar teori
Tramadol merupakan deri1at2sikloheksanol sintetis 3aitu 4ampuran
rasemis dari dua isomer+ Khasiat analgetikn3a sedang dan 5erda3a
mengham5at reuptake noradrenalin dan 5eker(a antitusi- (anti25atuk)+ O5at ini
di se5agian negara dianggap se5agai analgetikum opiate karena 5eker(a pusat6
3akni melalui pendudukan reseptor 72opioid oleh 4is2isomern3a+ 8eskipun
demikian at ini tidak menekan pernapasan6 praktis tidak mempengaruhi
sistem kardio1askuler atau motilitas lam5ung2usus+
Struktur 8olekul Tramadol
Rumus Kimia : C
#9
H
:&
'O
:
Sinonim :trans2:2dimeth3laminometh3l2#("2metho;3phen3l) 434lo2
he;anol
0erat molekul ::9"6< gram=mol
Kelarutan : >arut dalam air dan etanol
Suhu le5ur : antara #8$
o
2 #8#
o
C
pKa : 8+"2)+<#
Koe-isien partisi : "6$#
Khasiat : Se5agai analgesik6 namun tidak dian(urkan dikonsumsi
selama kehamilan dan laktasi+
Spektrum Serapan ?@ : larutan asam :%: nm (*##A%$a) le5ih 5aik :%) nm+
Tramadol HCl adalah suatu o5at analgetik 3ang di5erikan se4ra oral dan
parenteral 3ang se4ara klinik e-ekti- 5eker(a se4ara sentral dengan mekanisme
opioid dannon2opioid+ ,i *merika6 Tramadol HCl ter5ukti oleh F,* dapat
digunakan untuk n3eri moderate pain (n3eri intensitas sedang) hingga se1er pain
(n3eri intensitas tinggi)6 dan di *merika Tramadol se4ara klinik han3a tersedia
dalam 5entuk oral+
Terdapat kesamaan struktural antara tramadol dan deri1at opioid lainn3a+
Seperti haln3a Kodein6 tramadol mempun3ai rantai su5titusi met3l pada se5agian
rantai phenol 3ang mempun3ai a-initas 3ang lemah terhadap reseptor+
Struktur Tramadol HCl
8etode analisis dengan reaksi reduksi2oksidasi (redoks) adalah analisis
3ang terdiri dari peru5ahan 1alensi dari 5ahan25ahan 3ang 5ereaksi+ Reaktan 3ang
mengalami kehilangan elektron dalam reaksi redoks adalah bahan pereduksi dan
dapat diidenti-ikasi dari persamaan untuk reaksi dimana atom reaktan dikon1ersi
ke tingkat 3ang le5ih tinggi (*del5ert 86 #)&)) :
Fe:B Fe"B B e
:I2 I: B :e
8aka6 bahan pengoksidasi adalah reaktan 3ang menerima elektron dalam
reaksi redoks+
Reaksi 3ang re1ersi5le dari :I2 I: B :e dapat diaplikasikan dalam analisis
5ahan25ahan pereduksi seperti tiosianat dan arsenit+ (*del5ert 86 #)&))
Iodimetri adalah oksidasi kuantitati- dari sen3a!a pereduksi dengan
menggunakan iodium+ Iodimetri ini terdiri dari :6 3aitu (*shutosh Kar+:$$&)C
a+ Iodimetri metode langsung6 5ahan pereduksi langsung dioksidasi dengan
larutan 5aku Iodium+ Contohn3a pada penetapan kadar *sam *skor5at+
5+ Iodimetri metode residual (titrasi 5alik)6 5ahan pereduksi dioksidasi
dengan larutan 5aku iodium dalam (umlah 5erle5ih6 dan kele5ihan iod
akan dititrasi dengan larutan 5aku natrium tiosul-at+ Contohn3a pada
penetapan kadar 'atrium 0isul-it+
Iodometri adalah 5ahan pengoksidasi 3ang mengoksidasi Kalium iodide
(KI) dalam suasana asam6 sehingga Iod 3ang di5e5askan kemudian ditentukan
dengan menggunakan larutan 5aku 'atrium tiosul-at+ Contohn3a pada penetapan
kadar Tem5aga (II) sul-at+ (*shutosh Kar :$$&)
Hal2hal 3ang harus diperhatikan (*shutosh Kar D I+8+ Kolltho-- :$$&):
a+ Pada umumn3a oksidasi langsung dengan iod (Iodimetri) dilakukan
untuk 5ahan25ahan dengan potensial oksidasi 3ang le5ih rendah dari
Iod6 dan se5alikn3a+
5+ Oksidasi oleh oksigen atmos-er pada reaksi oksidasi KI dalam medium
asam kuat6 dapat menghasilkan nilai titer 3ang salah sehingga
men3e5a5kan kesalahan estimasi=perkiraan+
4+ Iodometri tidak pernah dilakukan dalam medium 5asa karena reaksi
antara Iod (I:) dengan hidroksida akan menghasilkan ion hipoiodit dan
iodat akan akan men(adi :I2+ ,imana : mol I2 akan mengoksidasi
parsial tiosul-at men(adi 5entuk oksidasi 3ang le5ih tinggi seperti SO<
:2
Penentuan titik akhir titrasi (#6:6"6<) :
a+ Indikator kan(i ( konsentrasi $6&E 3ang di5uat segar dengan
menggunakan pati larut 3aitu F2amilosa)+
5+ Instrument : Potensiometri atau amperometri+
4+ Garna iod dalam pelarut organik misaln3a kar5on tetraklorida dan
kloro-orm+ (khusus untuk titrasi 3ang tidak memungkinkan penggunaan
indi4ator kan(i6 sehingga tidak perlu ditam5ahkan indikator)+ Garna
merah ungu dari iodin dalam kar5on tetraklorida dapat dilihat pada
larutan iodin dengan kepekatan 3ang sangat rendah6 si-at inilah dipakai
untuk menentukan titik akhir titrasi dengan hilangn3a !arna merah
ungu pada lapisan kar5on tetraklorida+Selain kar5on tetraklorida6 dapat
(uga dipakai kloro-orm se5agai indikator dengan si-at 3ang sama
dengan kar5on tetraklorida+
>arutan 5aku dan 5aku primer=sekunder (*del5ert 86dkk #)&)) :
a+ >arutan 5aku Iodium 3ang di5akukan dengan *rsen trioksida se5agai
5aku primer atau di5akukan dengan larutan 5aku natrium tiosul-at
se5agai 5aku sekunder+
5+ >arutan 5aku natrium tiosul-at 3ang di5akukan dengan Kalium
5ikromat se5agai 5aku primer atau di5akukan dengan larutan 5aku
Iodium se5agai 5aku sekunder+
4+ >arutan 5aku Kalium 0romat 3ang di5akukan dengan larutan 5aku
natrium tiosul-at se5agai 5aku sekunder+ ( dipakai untuk penetapan
kadar se4ara iodometri 3ang meli5atkan su5stitusi 5romine dengan
iod6 misaln3a penetapan kadar tiroid)
d+ >arutan 5aku kalium Iodat 3ang di5akukan dengan larutan 5aku
natrium tiosul-at+ (dipakai untuk penetapan kadar se4ara iodometri
dimana kalium iodat 5ertindak se5ahan 5ahan pengoksidasi6 hasil
reaksi mem5e5askan iod 3ang kemudian dititrasi dengan larutan 5aku
natrium tiosul-at6 misaln3a penetapan kadar Kalium iodide)+
C+ *lat dan 0ahan
*lat :
#+ 0uret
:+ Stati-
"+ Klep
<+ Hrlenme3er
&+ Corong
9+ Ielas kimia
%+ Ielas ukur
8+ >a5u ukur
)+ Pipet 1olume
#$+ Pipet tetes
0ahan :
#+
I
:
:+
'a
:
S
:
O
"
"+
*Juadest
<+
*m3lum
&+
KI
9+
K
:
Cr
:
O
%
,+ PROSH,?R
a+
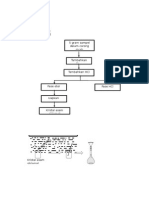
Isolasi analit dari matrikn3a
@orte;
Residu
Filtrat
Sampel
B *Juades
sentri-ius
sentri-ius
Residu
B *Juades
?(i Kualitati- :
,engan 4ara residu ditam5ahkan
air B *g'O" tidak ada endapan
analit sudah tidak ada
B*Juades
sampai #$$ml
F
iltra
t
Pipet #$ ml
B*Juades
sampai #$$ml
Pipet #$ ml
B*Juades
sampai #$$ml
Pengen4eran #$$ ;
5+
Pem5akuan 'a
:
S
:
O
"
$6# ' dengan K
:
Cr
:
O
%
4+
Pem5akuan I
:
$6# ' dengan 'a
:
S
:
O
"
d+
Penetapan kadar sampel Tramadol HC> dengan'a
:
S
:
O
"
H+ ,ata Pengamatan
a)
Pem5akuan 'a
:
S
:
O
"
deangan K
:
Cr
:
O
%
'o 8g K
:
Cr
:
O
%
@olume 'a
:
S
:
O
"
# #<% mg #$6& ml
: #<% mg #$6< ml
" #<% mg #$69 ml
'+ 'a
:
S
:
O
"
A
#+ '+ 'a
:
S
:
O
"
A A $6$)& '
:+ '+ 'a
:
S
:
O
"
A A $6$)9 '
"+ '+ 'a
:
S
:
O
"
A A $6$)< '
'+ 'a
:
S
:
O
"
rata2rata A $6$)& B $6$)9 B $6$)< A A $6$)& '
5)
Pem5akuan I
:
oleh 'a
:
S
:
O
"
'o @olume I
:
@olume 'a
:
S
:
O
"
# #$ ml #$6) ml
: #$ ml #$68 ml
" #$ ml #$69 ml
'+ I
:
A
#+ '+ I
:
A A$6$)8 '
:+ '+ I
:
A A$6$)% '
"+ '+ I
:
A A$6$)& '
'+ I
:
rata2rata A $6$)8B$6$)%B$6$)& A A $6$)9 '
4)
Penetapan kadar sampel
'o @olume
sampel
@olume 'a
:
S
:
O
"
# #$ ml ::6) ml
: #$ ml ::68 ml
" #$ ml :" ml
Rata K rata 1olume 'a
:
S
:
O
"
A ::6)B::68B:" A A ::6) ml
#+
@olume I
:
3ang 5ereaksi dengan 'a
:
S
:
O
"
@+I
:
; '+I
:
A @+ 'a
:
S
:
O
"
; '+ 'a
:
S
:
O
"
@+ I
:
; $6$)9 A ::6) ; $6$)&
@+I
:
A A A ::69 ml
:+
@olume I
:
3ang 5ereaksi dengan sampel
@+ I
:
3ang ditam5ahkan K @+I
:
3ang 5ereaksi dengan 'a
:
S
:
O
"
:& K ::69 A :6< ml
"+
Kadar sampel A '+Sampel A
A
A $6$:" ; #$$ (pengen4eran)
A :6" '
mg A 0H ; @ ; '
A :9"6< ; $6$# ; :6"
A 96$& mg
E kadar sampel A ; #$$E
A ; #$$E A 96$& E
F+ Pem5ahasan
Pada praktikum kali ini dilakukan penetapan kadar Tramadol HCl + Hal
3ang pertama dilakukan 3aitu mengisolasi sampel+ Tu(uan dari isolasi 3aitu
untuk memisahkan analit dari matrikn3a+ Pelarut 3ang digunakan pada proses
isolasi 3aitu aJuades karena sampel tramadol HCl larut dalam aJuades+
?ntuk penetapan kadar sampel digunakan metode titrasi iodimetri
(tidak langsung) 5erdasarkan prinsi- oksidasi dan reduksi+
Iodium merupakan oksidator 3ang relati- kuat dengan nilai potensial
oksidasi +Pada saat reaksi oksidasi6 iodium akan direduksi men(adi iodide
sesuai dengan reaksi :
I
2
+ 2e 2I
-
Iodium akan mengoksidasi sen3a!a2sen3a!a 3ang memiliki potensial
reduksi 3ang le5ih ke4il++
>arutan 5aku natrium tiosul-at 3ang telah di5akukan dapat digunakan
untuk mem5akukan iodium+ Iodium 3ang di5e5askan dititrasi dengan larutan
natrium tiosul-at sehingga menghasilkan reaksi :
:S
:
O
"
:2
B I
:
S
<
O
9
:2
B :I
2
Pada pem5akuan natrium tiosul-at harus dalam suasana asam dengan
penam5ahan H
:
SO
<
9' se5a5 larutan 3ang terdiri dari kalium dikromat dan
klium iodida 5erada dalam kondisinetral atau memiliki ke asaman 3ang
sangat rendah+ Reaksi peru5ahan !arna 3ang ter(adi men(adi kuning (erami6
kemudian ditam5ahkan indikator amilum dan !arnan3a pun men(adi 5iru tua
dan di titrasi 5alik hingga larutan 5ening +
Pada penetapan kadar sampel tramadol HCl dilakukan titrasi iodimetri (
tidak langsung ) dengan 4ara penam5ahan I
:
5erle5ih dimana I
:
akan 5ereaksi
dengan analit kemudian kele5ihan I
:
akan 5reaksi dengan larutan 5aku
natrium tiosul-at6 untuk mempermudah mengetahui titik akhir titrasi maka
diguankan indikator amilum pada kondisi terse5ut sehingga ter5entuk larutan
5er!arna 5iru dan hasil akhir titrasi di tandai dengan peru5ahan !arna dari
kuning (erami men(adi 5ening+
I+ Kesimpulan
,ari praktikum 3ang dilakukan dapat disimpulkan :
#+ Penentuan kadar Tramadol HCl dilakukan dengan metode titrasi
Iodimetri (tidak langsung)+
:+ Penetapan kadar Tramadol HCl dengan 'a
:
S
:
O
"
titik akhir titrasi
ditandai dengan peru5ahan !arna kuning (erami men(adi 5iru dan
dititrasi 5alik men(adi 5ening+
"+ Kadar Tramadol HCl adalah 96$& E+
,*FT*R P?ST*K*
*del5ert 8+ Kne1el + LenkinMs + #)&)+ Nuantitati1e Pharma4euti4al
Chemistr3+ 8C2Ira! Hill 0ook Compan3 : 'e! Oork+
*shutosh Kar+ :$$&+ Pharma4euti4al ,rug *nal3sis++ 'e! *ge
International >imited Pu5lishers : 'e! ,elhi+
I+8+ Kolltho-- + @olumetri4 *nal3sis+ 8C2Ira! Hill 0ook Compan3+ 'e!
Oork+
,epartemen Kesehatan Repu5lik Indonesia +#)%)+ Farmakope Indonesia
ed 3.L akarta:Kopri Su5 ?nit ,irektorat Lenderal Penga!asan O5at
dan 8akanan
Anda mungkin juga menyukai
- Bab 2 - IodoDokumen16 halamanBab 2 - Iodomaya_rajindra_hafifBelum ada peringkat
- Latihan To 1 PG 2023Dokumen13 halamanLatihan To 1 PG 2023matthew.owenBelum ada peringkat
- Laporan Tramadol HCLDokumen11 halamanLaporan Tramadol HCLiqlimasarahBelum ada peringkat
- TITRASI REDOKSDokumen49 halamanTITRASI REDOKSAnssBelum ada peringkat
- Edoc - Pub Indikator Metil MerahDokumen19 halamanEdoc - Pub Indikator Metil Merahjodohnya xuxiBelum ada peringkat
- Soal KimiaDokumen6 halamanSoal KimiaQuantum SouvenirBelum ada peringkat
- Pembuatan dan Analisa Kalium IodatDokumen16 halamanPembuatan dan Analisa Kalium IodatCosnert RabbaniBelum ada peringkat
- Percobaan V Hidrogen Peroksida Dengan Asam IodidaDokumen16 halamanPercobaan V Hidrogen Peroksida Dengan Asam Iodidanur100% (1)
- Titrasi RedoksDokumen18 halamanTitrasi RedoksNina RishantiBelum ada peringkat
- 01K7285U18ADokumen11 halaman01K7285U18ALaura SaraswatiBelum ada peringkat
- REDOKSIMETRIDokumen3 halamanREDOKSIMETRIChristiannaftali1995Belum ada peringkat
- Kimia 4Dokumen10 halamanKimia 4Adela dwi oktavianaBelum ada peringkat
- Laporan Kiman VI (Bromatometri)Dokumen5 halamanLaporan Kiman VI (Bromatometri)Arya MahardikaBelum ada peringkat
- Titrasi RedoksDokumen18 halamanTitrasi Redoksshendi suryanaBelum ada peringkat
- DIKROMATOMETRIDokumen15 halamanDIKROMATOMETRIgede alvendyBelum ada peringkat
- 12Dokumen11 halaman12Meyna SulistyaningrumBelum ada peringkat
- KIMIADokumen48 halamanKIMIAWiwie Mo SajaBelum ada peringkat
- Titrasi Iodometri Adalah Salah Satu Titrasi Redoks Yang Melibatkan IodiumDokumen13 halamanTitrasi Iodometri Adalah Salah Satu Titrasi Redoks Yang Melibatkan IodiumDennis Azis Wardana Setiawan0% (1)
- Titrasi DikromatometriDokumen15 halamanTitrasi DikromatometriDigna Renny TLMBelum ada peringkat
- Laporan Praktikum Kimia DasarDokumen19 halamanLaporan Praktikum Kimia DasarIvanBelum ada peringkat
- KloroformDokumen6 halamanKloroformerni yunitaBelum ada peringkat
- REDOKS TITRASIDokumen24 halamanREDOKS TITRASIokta nursantiBelum ada peringkat
- BromometriDokumen24 halamanBromometriRido GintingBelum ada peringkat
- Modul IkdDokumen102 halamanModul Ikdahmad sidik mandarBelum ada peringkat
- Titrasi RedoksDokumen32 halamanTitrasi RedoksZellaBelum ada peringkat
- Titrasi RedoksDokumen4 halamanTitrasi RedoksArifendiBelum ada peringkat
- Materi KimiaDokumen8 halamanMateri Kimia07012007Belum ada peringkat
- Macam Macam OksidatorDokumen6 halamanMacam Macam OksidatorPrimadi AhsanuBelum ada peringkat
- Macam-Macam Titrasi Redoks Dan AplikasinyaDokumen38 halamanMacam-Macam Titrasi Redoks Dan AplikasinyaHotnida Novalia TobingBelum ada peringkat
- Macam-macam titrasi redoks dan aplikasinyaDokumen38 halamanMacam-macam titrasi redoks dan aplikasinyaLee'man Doank100% (1)
- Penentuan Kadar CL Dengan Metode Mohr PDFDokumen6 halamanPenentuan Kadar CL Dengan Metode Mohr PDFBangbenz Syarifhidayat Al-asysyathri100% (1)
- Reaksi TriiodometanaDokumen12 halamanReaksi TriiodometanaAgus TiniBelum ada peringkat
- Laporan Praktikum Kimia Analitik I Titrasi RedoksDokumen21 halamanLaporan Praktikum Kimia Analitik I Titrasi RedoksRisal RamboBelum ada peringkat
- TITRASI REDOKS PRINSIP DAN METODEDokumen18 halamanTITRASI REDOKS PRINSIP DAN METODED'ma100% (2)
- Jawaban Ujian Sintesa Bahan Obat BaruDokumen5 halamanJawaban Ujian Sintesa Bahan Obat BaruHepniBagariangBelum ada peringkat
- DIKROMATOMETRIDokumen15 halamanDIKROMATOMETRILinaBelum ada peringkat
- OKSIDIOMETRIDokumen21 halamanOKSIDIOMETRIAhmad SyahputraBelum ada peringkat
- Iodo/Iodometri AnalisisDokumen18 halamanIodo/Iodometri AnalisisEunike SukestiBelum ada peringkat
- Oksidimetri 2Dokumen21 halamanOksidimetri 2Baiq Safika WulansariBelum ada peringkat
- Laporan KFA 2 Kelompok 23 AmoksilinDokumen10 halamanLaporan KFA 2 Kelompok 23 AmoksilinDamas Anjar PurnamaBelum ada peringkat
- Sirup Maple BerkhasiatDokumen7 halamanSirup Maple BerkhasiatKazuki TakahiroBelum ada peringkat
- Vitamin CDokumen29 halamanVitamin CAyu NingrumBelum ada peringkat
- ANALISIS KHLORIDADokumen13 halamanANALISIS KHLORIDAMuhammad GinanjarBelum ada peringkat
- Metode IodometriDokumen2 halamanMetode IodometriputrilunitaBelum ada peringkat
- ARGENTOMETRIDokumen16 halamanARGENTOMETRITilana maduraniBelum ada peringkat
- Analitik 1 PascamidDokumen38 halamanAnalitik 1 PascamidSulpia Farhika Reyaldhi NugrahaBelum ada peringkat
- Laporan Praktikum IodometriDokumen12 halamanLaporan Praktikum IodometriElang100% (1)
- Macam-Macam Titrasi Redoks Dan AplikasinyaDokumen38 halamanMacam-Macam Titrasi Redoks Dan AplikasinyaDamai HuluBelum ada peringkat
- Soal Bimbel Tahap II Paket 4 - 2023Dokumen6 halamanSoal Bimbel Tahap II Paket 4 - 2023Titan SultanBelum ada peringkat
- PENERAPAN TITRASI REDOKSDokumen8 halamanPENERAPAN TITRASI REDOKSQofifahBelum ada peringkat
- MENGHITUNG KADAR KLORDokumen13 halamanMENGHITUNG KADAR KLORchiciwlandBelum ada peringkat
- IODIMETRIDokumen10 halamanIODIMETRIAmanda Jr.Belum ada peringkat
- Latihan SOAL US KIMIA 2022Dokumen13 halamanLatihan SOAL US KIMIA 2022Fajrirahma RamadaniBelum ada peringkat
- Tiosulfat Formalin HidrosulfitDokumen9 halamanTiosulfat Formalin HidrosulfitSelvia EgalitaBelum ada peringkat
- Kisi Kisi Dan Contoh Soal Osn KimiaDokumen10 halamanKisi Kisi Dan Contoh Soal Osn Kimiaibrahim.gaisan25Belum ada peringkat
- Peraturan Menteri KesehatanDokumen28 halamanPeraturan Menteri KesehatanImam Bagus Sumantri100% (1)
- 86ca1 6. DEWIi JadiDokumen6 halaman86ca1 6. DEWIi JadiDhini AndriyaniBelum ada peringkat
- Proposal Kewirausahaan UsahaDokumen12 halamanProposal Kewirausahaan UsahaAprilia RistianBelum ada peringkat
- Formulir Aplikasi KerjaDokumen4 halamanFormulir Aplikasi KerjaAprilia RistianBelum ada peringkat
- Tugaslimbahudhfix 121121063646 Phpapp01Dokumen14 halamanTugaslimbahudhfix 121121063646 Phpapp01Agus SufianBelum ada peringkat
- Kumpulan Soal ItbDokumen7 halamanKumpulan Soal ItbbustamimoehBelum ada peringkat
- Teks TantanganDokumen2 halamanTeks TantanganAprilia Ristian0% (1)
- KlasifikasiDokumen1 halamanKlasifikasiAprilia RistianBelum ada peringkat
- DAFUSDokumen1 halamanDAFUSAprilia RistianBelum ada peringkat
- Bab IiDokumen17 halamanBab IiAprilia RistianBelum ada peringkat
- Bab VDokumen1 halamanBab VAprilia RistianBelum ada peringkat
- Organisasi Kelas Viii-HDokumen1 halamanOrganisasi Kelas Viii-HAprilia RistianBelum ada peringkat
- Peristiwa RengasdengklokDokumen5 halamanPeristiwa RengasdengklokAprilia RistianBelum ada peringkat
- Dasar TeoriDokumen15 halamanDasar TeoriAprilia RistianBelum ada peringkat
- OPTIMALKAN KADAR PARASETAMOL DENGAN HPLCDokumen42 halamanOPTIMALKAN KADAR PARASETAMOL DENGAN HPLCAprilia RistianBelum ada peringkat
- CoverDokumen1 halamanCoverAprilia RistianBelum ada peringkat
- Bab IiDokumen12 halamanBab IiAprilia RistianBelum ada peringkat
- Skrining FitokimiaDokumen2 halamanSkrining FitokimiaAprilia RistianBelum ada peringkat
- Data PerhitunganDokumen4 halamanData PerhitunganAprilia RistianBelum ada peringkat
- Data PerhitunganDokumen4 halamanData PerhitunganAprilia RistianBelum ada peringkat
- Kata PengantarDokumen4 halamanKata PengantarAprilia RistianBelum ada peringkat
- Cara Membuat Pernik Dari Tutup BotolDokumen10 halamanCara Membuat Pernik Dari Tutup BotolAprilia RistianBelum ada peringkat
- Kata PengantarDokumen4 halamanKata PengantarAprilia RistianBelum ada peringkat
- Pemba Has AnDokumen3 halamanPemba Has AnAprilia RistianBelum ada peringkat
- Kadar AirDokumen3 halamanKadar AirAprilia RistianBelum ada peringkat
- Kadar AirDokumen3 halamanKadar AirAprilia RistianBelum ada peringkat
- Kadar AirDokumen3 halamanKadar AirAprilia RistianBelum ada peringkat
- Alat Dan BahanDokumen7 halamanAlat Dan BahanAprilia RistianBelum ada peringkat
- Pemba Has AnDokumen3 halamanPemba Has AnAprilia RistianBelum ada peringkat
- Laporan PraktikumDokumen10 halamanLaporan PraktikumAprilia RistianBelum ada peringkat