Curso de Hidrometalurgia Del Au Ag y Cu
Diunggah oleh
Ignacio GarciaHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Curso de Hidrometalurgia Del Au Ag y Cu
Diunggah oleh
Ignacio GarciaHak Cipta:
Format Tersedia
HIDROMETALURGIA DEL Au, Ag, Cu
TERMODINAMICA
CONTENIDO
Generalidades
Diagrama eh-pH del agua
Construccin de los diagramas eh-pH
Influencia de los acomplejants
Usos y Abusos de los diagramas eh-pH
TRANSFERENCIA DE MASA Y CINETICA
CONTENIDO
Introduccin
Cintica Homognea
Cintica Heterognea
1. Efecto de la velocidad del fluido
2. Efecto de la temperatura
3. Naturaleza electroqumica
LIXIVIACIN DE METALES
CONTENIDO
Solubilidad de Au y Ag en soluciones de cianuro
1. Efecto de la concentracin de cianuro
2. Efecto del pH
3. Efecto de la concentracin de cianuro
Cintica de la cianuracin
1. Efecto de iones extraos
METODOLOGIA DE LA HIDROMETALURGIA Au y Ag
CONTENIDO
Lixiviacin en montn
Lixiviacin por agitacin
Adsorcin en carbn activado
Precipitacin con zinc en polvo
Extraccin por solventes orgnicos.
LIXIVIACIN DEL Cu
CONTENIDO
Lixiviacin de CuOx
Pgina 2 de 30
Lixiviacin de sulfuros de Cu
Cintica de la lixiviacin
Lixiviacin en Montn
Lixiviacin por agitacin
RECUPERACIN DEL Cu
CONTENIDO
Precipitacin de Cu con chatarra de Hierro
Extraccin por solventes orgnicos
1. Teora bsica
2. Reaccin principal.
3. Dispersin estable
4. Degradacin de extractants.
Pgina 3 de 30
Introduccin
La hidrometalurgia es la rama de la metalurgia extractiva que comprende los
procesos de obtencin de metales y compuestos, a partir de minerales o fuentes
secundarias, mediante reacciones que tienen lugar en soluciones acuosas u
orgnicas y por lo tanto se desarrollan a temperaturas relativamente bajas.
Las tcnicas empleadas incluyen. Preparacin y pre-tratamiento del mineral o
material inicial, lixiviacin de los valores metlicos usando reactivos qumicos o
accin bacterial, separacin y lavado de residuos slidos, purificacin final del
metal o compuesto deseado.
Para cada una de estas etapas se dispone de una gran variedad de tratamientos
alternativos; as por ejemplo, la lixiviacin puede realizarse por percolacin,
agitacin. In-situ o en pilas y botaderos. La purificacin de las soluciones puede
realizarse por control del pH, intercambi inico, extraccin por solventes
orgnicos, etc. La precipitacin puede ser por cementacin, electrodeposicin o
precipitacin con gases.
Las primeras aplicaciones de la hidrometalurgia moderna las constituyen los
procesos de cianuracin de minerales de oro y plata. Estos procesos dieron
origen a un rpido desarrallo de la mayora de los equipos indispensables en los
procesos hidrometalrgicos actuales: agitadores, espesadores, filtros, bombas de
lodos, etc.
Posteriormente aparecieron procesos tan importantes como el intercambio inico,
extraccin por solventes orgnicos y el carbn activado que abrieron un campo
an ms grande de aplicacin.
Actualmente
se
extraen
refinan,
comercialmente,
mediante
mtodos
hidrometalrgicos, un gran nmero de metales, como por ejemplo: cobre, nquel,
aluminio, oro, plata, cobalto, zinc, uranio, zirconio, hafnio, etc. Pudiendo
Pgina 4 de 30
emplearse en forma total o parcial para prcticamente todos, excepto 6 o 7, de los
82 elementos metlicos conocidos. Generalmente los metales alcanzan un grado
de pureza mayor que los producidos por otros mtodos.
Pgina 5 de 30
TERMODINAMICA
Generalidades.
Los Geoquimicos y Gelogos, los diagramas de equilibrio lo representan entre la
Lithosfera, Hidrosfera y Atmsfera; a los Fsicos, Metalurgistas y Qumicos les
provee un grafico muy usual y describe la pasividad, corrosin y disolucin de
minerales.
Las relaciones existentes entre la hidrosfera, lithosfera y atmsfera son
representadas en la siguiente fig.:
Las reacciones son homogneas heterogneas dependiendo sobre si o no ellos
ocurren dentro de una simple fase o en los lmites entre fases.
La Hidrosfera se refiere a la porcin liquida de la tierra, La Lithosfera es la corteza
terrestre y la atmsfera es la parte gaseosa que envuelve la tierra y los gases
dentro de la tierra.
La qumica-fsica de la mineralizacin es una gua importante y usual para los
metalurgistas desde que representa un gran inventario de reacciones importantes
en el sistema hidrometalurgico.
La principal diferencia es que los factores cinticos llega hacerse predominante
para un metalurgista, desde que las reacciones deben ocurrir en un tiempo
relativamente cortos para ser de importancia comercial.
La siguiente fig. ilustra la clase de reacciones de importancia para la
hidrometalurgia. La reaccin I, representa el equilibrio entre la atmosferahidrosfera y la reaccin II entre la hidrosfera-lithosfera, las cuales son de
importancia primaria y deben ser tratadas con detalle.
Pgina 6 de 30
Cada tipo de reaccin tiene especial implicacin para los metalurgistas. Tambin
el agua, el solvente universal, tiene propiedades nicas que hace posible no
solamente una mineralizacin, si no una rpida disolucin, transporte, procesos
de separacin y precipitacin que es vital para la aplicacin comercial en la
hidrometalurgia.
Homogeneas
Reacciones Quimicas
Disociacin Gaseosa
Difusin
atm
Homogeneas
Disociacin Electrolitica
Hidrlisis
Formacin de Complejos
Difusin de iones solubles
Heterogeneas
Disociacin
Disolucin Gaseosa
Evaporacin
Hidro
Tierra
II
Heterogeneo
Sublimacin
Oxidacin
Reduccin
Dehidratacin
Descomposicion
Heterogeneo
Precipitacin
Corrosin
Disolucin
(Reacciones Electroquimicas)
Litho
Homogeneo y
Difusin
Fundicin
Reacciones
Quimicas
Heterogeneo
Nucleacin
Precipitacin
Reacciones
Electroquimicas
La siguiente tabla da los elementos mas importantes en la lithosfera e hidrosfera
(Wells, 1962). Virtualmente todos los metales bases estn presentes en pequeas
cantidades
en
cantidades
trazas.
Afortunadamente
los
procesos
de
mineralizacin dentro de la tierra, ambos la hidro y la piro, tienen como resultado
en la concentracin de los metales, bases importante.
Un segundo punto de inters es que sobre un volumen base, sobre el 90% de la
corteza terrestre esta compuesto de oxigeno.
De los metales, tales como el Aluminio, Hierro y magnesio son los mas
abundantes; La slice es el elemento mas abundante y otros como el oxigeno,
Pgina 7 de 30
Sodio, Magnesio, Calcio y Potasio son componentes prominentes de ambos la
lithosfera y la hidrosfera.
Lithosfera
Hidrosfera
Elemento
Peso (%)
Volumen(%) Elemento Peso (%)
46.59
91.77
85.89
Si
27.72
0.80
10.80
Al
8.13
0.76
Cl
1.93
Fe
5.01
0.68
Na
1.07
Mg
2.09
0.56
Mg
0.13
Ca
3.63
1.48
0.09
Na
2.85
1.60
Ca
0.04
2.60
2.14
0.04
Ti
0.63
0.22
Otros
<0.01
Menas
Pequeas
metlicas, cantidades
mineral
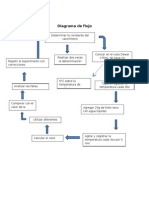
Diagrama Tensin-pH del agua.
a)
Asociacin con minerales .
El agua puede ser parte de la lithosfera cuando se encuentra qumicamente con
ciertos minerales.
Se encuentra en 2 formas:
Agua de Cristalizacin, es agua que esta presente como agua en la estructura del
mineral. Ejemplos son: CaSO4.2H2O y MgCl.6H2O.
La dehydratacin puede resultar en la simple remocin del agua por simple
calentamiento, tal como el caso del Gypsum para la fabricacin del yeso:
CaSO4.2H2O + CaSO4 + 2H2O
Pgina 8 de 30
La forma final es el mineral anhydro anhidrita, en el caso del MgCl2.6H2O, la
descomposicin puede resultar en la formacin de un xido (McDonald y
Wadsworth, 1972).
MgCl2.6H2O + MgO + 2HCl + 5H2O
El agua puede estar presente como el in hidroxilo en la red de un cristal como es
el caso de la mica potasica KAl3Si3O10(OH)2 como en las arcillas tal como la
caolinita Al2Si2O5(OH)4, remover el in hidroxilo de estos minerales requieren muy
altas temperaturas.
b)
Reacciones dentro de la hidrosfera
Muchos tipos de reacciones homogneas ocurren dentro de la hidrosfera. Una de
estas es la disociacin electroltica. El agua misma es un ejemplo de acuerdo a la
reaccin:
H2O(l) = H+(aq) + OH-(aq)
La constante de Equilibrio K es la constante de Ostwald. En el caso del agua , K
tiene el valor 10-14 a temperatura ambiente y es igual al producto de actividades:
K(Ostwald) = aH+*aOHLa actividad del agua es tomada como la unidad
Por convencin la actividad es interpretada como sigue:
Iones y Molculas en soluciones diluidas:
La actividad es aproximadamente igual a la concentracin en moles /litro.
El solvente en una solucin diluida:
La actividad es igual a la fraccin molar del solvente y es aproximadamente
la unidad.
Pgina 9 de 30
Slidos lquidos puros en equilibrio con una solucin:
La actividad es exactamente la unidad.
Gases en equilibrio con una solucin:
La actividad es la presin parcial del gas en atmsferas.
Mezcla de lquidos:
La actividad de un componente dado es aproximadamente igual a la
fraccin molar.
En una solucin ideal la actividad es proporcional a la fraccin molar X, en
solucin y esta relacionado al potencial qumico por la ecuacin:
= o + RTlnX
o
donde es el potencial qumico estndar.
En una solucin no ideal, la fraccin molar y la actividad no son idnticas,
requiriendo una correccin de la fraccin molar por el coeficiente o
= o + RTlnX = = o + RTlna
para soluciones diluidas la fraccin molar puede ser reemplazada por la
concentracin , normalmente el estado estndar es tomado como la unidad.
La constante de equilibrio K esta relacionado a la energa libre de Gibbs por la
ecuacin:
-RTlnK = G = H-TS
Pgina 10 de 30
donde
G, H y S
reaccin, en la cual
son la energa libre estndar, entalpa y entropa de la
y
son funciones de la temperatura, pero para
pequeos cambios de temperatura ellos pueden ser asumidos constantes y por lo
tanto
puede se calculada por la ecuacin anterior para alguna temperatura
intermedia.
El cambio de energa libre estndar para cualesquiera reaccin qumica es la
suma de los potenciales qumicos de los productos menos la suma de los
potenciales qumicos de los reactantes.
Por ejemplo para la reaccin del agua:
H2O(l) = H+(aq) + OH-(aq)
G = H+ + OH--H2O
o tambin:
G = producto iproductos - reactantes reactantes
o en forma general:
G = i i
La constante de equilibrio K para esta reaccin es dada por la ecuacin
termodinmica:
K = aH+ * aOH- / aH2O
Para soluciones bastante diluidas el H+ = 1, y lo mismo para OH+ = 1, por lo tanto
se igualan a la concentracin y en el caso del agua como se trata de un lquido
puro la actividad es la unidad de acuerdo a esto tenemos que:
K = [ H+][OH-]
Pgina 11 de 30
Para el caso de una reaccin qumica podemos aplicar la siguiente ecuacin
termodinmica:
G = G + RTlnQ
En el equilibrio : G = 0 , por lo tanto tenemos que :
G = -RTlnK
por lo tanto:
lnK = -G/RT = - i i/RT
Transformando a logaritmo decimal y a temperatura ambiente tenemos:
logK = - i i/1364
En este caso de los potenciales qumicos para el agua se da en la siguiente tabla:
elemento
H+
OH-
H2 O
i(cal/mol)
-37,595
-56,690
Por lo tanto tenemos:
G = 19,075 Caloras / mol.
Aplicando la ecuacin tenemos:
log K = -14
entonces K = 10 14
Para el caso del agua pura tenemos que:
[ H+] = [OH-]
10-14 = [ H+] [OH-]
entonces
[ H+] = [OH-] =10-7
La ecuacin (5) la podemos escribir en forma logartmica:
PK = PH + POH = 14
Por lo tanto para la solucin neutra (agua pura):
PH = 7 = POH = -log[OH-]
Pgina 12 de 30
Si adicionamos H+ al agua pura en la forma de un cido, entonces la
concentracin de iones H+ se incrementa, de acuerdo a la ecuacin (1) el pH
decrece del valor neutro de 7.
Por ejemplo: En una solucin 0.01 molar de H2SO4, la concentracin molar de [H+]
= 0.02 M por lo tanto el
pH = - Log [0.02] = 1.70
En algunas partes del mundo, la acidez de la lluvia cae por debajo de pH=5.6, en
el NE de EE.UU. por ejemplo el pH promedio de las lluvias es 4.6 y no es inusual
tener lluvias con pH=4.0 que es 1,000 veces ms cida que el agua destilada.
Otro tipo de reaccin que puede ocurrir dentro de la hidrosfera es la hidrlisis. Por
ejemplo el in cianuro reacciona con el agua para formar el HCN que se disocia
de acuerdo a la reaccin:
CN- + H2O HCN + OHLa hidrlisis de los iones ferricos en solucin, formndose un producto hidrolizado
soluble para formar la goethita de acuerdo a la reaccin siguiente:
Fe3+ + 2 H2O 4 FeO(OH) + 3 H+
En la construccin de los diagramas eh-pH, lo primero que hacerse es la
construccin de la zona de estabilidad del agua.
Pgina 13 de 30
Se va a considerar las siguientes especies presentes:
H+, OH-, H2O, O2 y H2
Extrayendo los potenciales qumicos de tablas tenemos:
Compuestos
H+
i(cal/mol)
OH-
H2 O
-37,595 -56,690
O2
H2
Las reacciones posibles a considerar son las siguientes se va a considerar los
siguientes parmetros tC= 25, [Mi]= 1M y pi = 1atm:
a) Encima del lmite u oxidacin del agua:
O2 + 4H+ + 4e 2H2O
Aplicando la ecuacin de Nerst tenemos:
De acuerdo a los parmetros se llega a la ecuacin sintetizada siguiente:
Determinando el
tenemos:
G= 2*(-56690) - [1*0 + 1*0] = -113380 cal/mol
Por lo tanto:
= -[-113380/23060*4] = 1.23 V
Por lo tanto la ecuacin a considerar para la oxidacin del agua es:
b) Bajo el lmite o reduccin del agua:
Pgina 14 de 30
Se puede considerar bajo dos formas:
2H+ + 2e H2
2H2O + 2e H2 + 2OH-
1)
2)
Pero el que mas se usa es la reaccin (1)
Aplicando la ecuacin de Nerst tenemos:
De acuerdo a los parmetros se llega a la ecuacin sintetizada siguiente:
Determinando el
tenemos:
G= 1*0 - [2*0] = 0.00 cal/mol
Por lo tanto:
= -[0.00/23060*4] = 0.00 V
Por lo tanto la ecuacin a considerar para la reduccin del agua es:
Encima y bajo el lmite de estabilidad depende de la presin, en un rango de
condiciones de fuerte oxidacin y fuerte reduccin, es tambin interesante que
cambios de presiones grandes afecten el voltaje (o lmites) solo ligeramente:
La siguiente figura ilustra la regin de estabilidad del agua entre una atmsfera de
oxigeno y una atmsfera de hidrogeno:
Pgina 15 de 30
Construccin de los diagramas tensin-pH.
Para la construccin de los diagramas eh-pH, hay que tener en cuenta las
siguientes consideraciones:
I.
II.
Listado de todos los compuestos a ser considerados
Ordenamiento en orden creciente de los compuestos de acuerdo a su
estado de oxidacin y por pisos.
Pgina 16 de 30
III.
IV.
V.
Establecimiento de las reacciones electroqumicas qumicas entre dos
de los compuestos de acuerdo a su estado de oxidacin, completando
las reacciones con H2O, H+ y e-.
Aplicacin de las relaciones termodinmicas sobre el equilibrio
termodinmico qumico.
Dibujar finalmente el diagrama con las reacciones caractersticas del
sistema.
Para mayor claridad, construiremos primero el diagrama Ag-H2O, dada la nobleza
de este metal, es bastante simple y se construye solo con tres ecuaciones ya que
los compuestos estables en el rango de pH de 0-14 son:
Ag, Ag+ y Ag2O
Se puede observar que esta ordenado en forma creciente de acuerdo a su estado
de oxidacin
Luego lo ordenamos en pisos de acuerdo a su estado de oxidacin:
Estado de
oxidacin
+1
0
Ag+
Ag2 O
Ag
Luego se entrelaza los compuestos entre los diferentes estados de oxidacin y del
mismo estado de oxidacin, tal como se observa a continuacin:
Pgina 17 de 30
Estado de
oxidacin
3
+
+1
Ag
Ag2 O
Ag
De esta forma observamos que solo existen tres reacciones a ser considerados
para la construccin de este diagrama eh-pH.
Luego
estamos
dispuestos
establecer
las
reacciones
qumicas
electroqumicas respectivas:
Comenzaremos con la reaccin 1, observen que estamos poniendo esta en
reduccin:
Ag+ + e Ag
1)
2)
3)
Ag2O + 2H+ + 2e 2Ag + H2O y
Ag2O + 2H+ 2Ag + H2O
Una vez establecido las respectivas reacciones se va a tablas para extraer los
respectivos potenciales electroqumicos:
Compuestos
Ag
i(cal/mol)
Ag+aq
Ag2O
+18,448 -2,395
H2 O
-56,690
Y luego se aplica las respectivas relaciones termodinmicas para establecer las
ecuaciones respectivas, considerando una temperatura de 25C y [Mi]= 10-6M:
1)
eth = eth + 0.06log[aAg+]
todos los datos los conocemos a excepcin del eth.
Pgina 18 de 30
G = 0-[18,448] = -18,448 cal/mol.
eth = -[-18,448/(23060*1)] = 0.78V.
Por lo tanto
eth = 0.78 + 0.06log[Ag+]
Luego tenemos:
Y como vamos a trabajar a una concentracin de todas las especies inicas de
10-6M. tenemos que:
eth= 0.42 V
eth = eth + 0.03log[aAg2O][aH+]2/[aAg][aH2O]
2)
por convencin sabemos que todos los compuestos slidos y lquidos puros sus
actividades es la unidad, por lo tanto tenemos que:
eth = eth + 0.06log [H+]
eth = eth - 0.06pH
Calculando
G = -56,690 + 0 -[-2,395 + 0] = -54,295 Cal/mol.
Por lo tanto
eth = -[-54,295]/(23,060*2)] = 1.18V.
Luego tenemos que:
eth = 1.18 - 0.06pH
3) Como es una reaccin qumica aqu no interviene la ecuacin de Nerst, por lo
tanto tenemos que:
K = [aAg+]2[ aH2O]/[aAg2O][ aH+]2 = [Ag+]2/[ H+] 2
Tomando logaritmos, tenemos:
logK = 2log[Ag+] - 2log[ H+]
Calculando G = 2*18,448 56,690 -[-2,395 + 2*0] = -17399 cal/mol.
Por lo tanto:
logK = -(-17399/1364) = 12.75
Luego tenemos que: 12.75 = 2log[Ag+] + 2pH
Pgina 19 de 30
Por lo tanto tenemos que: pH = 6.38 - log[Ag+]
Donde
pH = 12.38
Una vez que tenemos todas estas relaciones, procedemos a realizar los
siguientes clculos:
1) eth= 0.42 V
2) eth = 1.18 - 0.06pH, calculando para pH = O tenemos eth =1.18V y para pH
= 14 tenemos eth =0.34V
3) pH = 12.38
con estos datos se construye el diagrama eth pH para la Ag-H2O, tal como se da
a continuacin:
Influencia de elementos acomplejants en los diagramas tensin-pH.
Pgina 20 de 30
Veamos ahora lo que sucede al campo de estabilidad de la plata en presencia de
iones CN- , cunado se construye este diagrama, demostraremos que conocida la
cantidad de CNNa total agregado, es posible encontrar una relacin entre el CNy el pH:
Si agregamos NaCN al agua, tendremos las siguientes relaciones de equilibrio:
NaCN Na+ + CN-
(1)
H+ + CN- HCN
(4)
cuya constante de equilibrio de esta ltima reaccin es: k= 2.512x109 1x109.4
por otra parte sabemos que:
[NaCN]total = [HCN] + [CN-]
de (4) tenemos :
HCN
log H CN = 9.4
(5)
(6)
de esta ltima relacin despejamos la concentracin de cianuro:
[CN-] = [HCN]x10(pH-9.4)
(7)
Reemplazando (7) en (5) tenemos:
[NaCN]total = [HCN]x{1 + 10(pH-9.4)}
(8)
Si tomamos logaritmo y transponiendo trminos tenemos:
log[HCN] = log[NaCN]total - log{1 + 10(pH-9.4)} (9)
Pgina 21 de 30
de la ecuacin (7) tomando logaritmo y transponiendo trminos tenemos:
log[HCN] = log[CN-] pH + 9.4
(10)
Igualando (9) y (10) y despejando la concentracin de CN-:
log[CN-] = log[NaCN]total -log{1 + 10(pH-9.4)} + pH-9.4
(11)
Esta ltima relacin nos permite conocer la concentracin de cianuro libre en
funcin del pH para una concentracin de cianuro de sodio conocida; en funcin
de esto para una [NaCN]total = 10-2 M que corresponde aproximadamente a 0.05%
NaCN, podemos determinar la concentracin de cianuro libre para diferentes pH
tal como podemos apreciar en el siguiente cuadro:
pH
14
13
12
11
10
9.4
9
8
2
CN0.0099997488
0.0099974887
0.0099749441
0.0097549663
0.0079923999
0.0050000000
0.0028474725
0.0003828650
0.0000000004
Tal como se puede apreciar en la siguiente grafica:
Pgina 22 de 30
Desde el punto de vista termodinmico, la estabilidad del cianuro lo podemos
observar en el diagrama e h-pH para el caso del CN- -H2O si tomamos en
consideracin las siguientes reacciones:
HCNO CNO- + H+
(12)
HCN CN- + H+
(13)
HCNO + 2H+ + 2e HCN + H2O
(14)
CNO- + 3H+ + 2e HCN + H2O
(15)
CNO- + 2H+ + 2e CN- + H2O
(16)
tomando en cuenta la ecuacin de Nerst y los potenciales qumicos de las
sustancias que estn presentes y que se indican a continuacin:
Compuesto
i (Cal/mol)
HCN
CN-
HCNO
CNO-
H2O
+29600 +39370 -28980 -23750 -56690
Podemos obtener el siguiente grafico de eh pH para el CN- - H2O:
Pgina 23 de 30
Para el caso del oro, plata y CN- se tiene que adicionar las siguientes reacciones y
ecuaciones que a continuacin se indican y tomando en cuenta los potenciales
qumicos siguientes:
Compuesto AgCN2-aq
i (Cal/mol)
4)
+72,047
AgCN
Au+
AuCN2-aq AuCN
+38,499 39,000
Ag+ + 2CN- AgCN2K = [AgCN2-]/[Ag+][CN-]2 = 1018.8
log[Ag+]/[Ag(CN)2-] = -2log[CN-] 18.8
pCN = 9.4 + 0.5log[Ag+]/[Ag(CN) 2-]
4)
Au+ + 2CN- AuCN2K = [AuCN2-]/ [Au+] [CN-]2 = 1038
log[Au+]/[Au(CN)2-] = -2log[CN-] 38
pCN = 9.4 + 0.5log[Au+]/[Au(CN) 2-]
5)
AgCN2- + e Ag + 2CNeth = eth + 0.06log [AgCN2-]/ [CN-]2
eth = -0.31V
eth = -0.31 - 0.12log[CN-] + 0.06log[AgCN2-]
eth = -0.664 - 0.12log[CN-]
Pgina 24 de 30
5a)
AuCN2- + e Au + 2CNeth = eth + 0.06log[AuCN2-]/[CN- ]2
eth = -0.60V
eth = -0.60 - 0.12log[CN-] + 0.06log[AuCN2-]
eth = -0.96 - 0.12log[CN-]
De acuerdo a esto se construyo la figura que se da a continuacin para una
concentracin de CNNa total = 10-2M que corresponde aproximadamente a 0.05%
NaCN,
Pgina 25 de 30
las actividades del [AuCN2-] y el [AgCN2-] estn a 10-4 M que corresponde a una
concentracin de Ag y Au de 10 y 20 g/m3 respectivamente, por lo tanto la
condiciones a la que se ha construido este diagrama es a operaciones practicas.
De este diagrama se puede sacar las siguientes conclusiones:
El Au y la Ag son metales muy nobles ya que se encuentra dentro de la
zona de estabilidad del agua en la regin de bajos pH, pero son menos
nobles a altos pH en soluciones de cianuro. Notablemente la plata es mucho
mas inerte que el oro en presencia de CN-
Las reacciones de oxidacin (5) involucran el ceder un electrn que
necesita ser aceptada por alguna de las siguientes reacciones de reduccin:
2H+ +2e H2
(1)
O2 + 4H+ + 4e 2H2O
(2)
O2 +2H+ +2e H2O2
H2O2 + 2H+ + 2e 2H2O
(3)
(4)
Estas reacciones son ilustradas asumiendo una actividad unitaria para
el H2O2 y las especies gaseosas.
Muchos investigadores tienen confirmada que la disolucin de Au y Ag
es acompaada por la produccin de H2O2 y de este modo la ecuacin 3
necesita ser considerado como reaccin de reduccin.
Muchos investigadores indican que la fuerza del agente oxidante tal
como el H2O2 puede convertir CN- en cianato, el cual no es capaz de oxidar
el oro y la plata.
La reaccin de disolucin:
Pgina 26 de 30
ZnCN4-2 + 2e Zn + 4CNEs tambin ploteada, por que la cementacin con Zn es comnmente
usada para recuperar ambos elementos el oro y la plata.
Pgina 27 de 30
Pgina 28 de 30
Pgina 29 de 30
Pgina 30 de 30
Anda mungkin juga menyukai
- Previo Practica 4 Medicion de Potenciales de Celda y Media CeldaDokumen8 halamanPrevio Practica 4 Medicion de Potenciales de Celda y Media CeldaIgnacio GarciaBelum ada peringkat
- Serie 3 - 2015 AsrDokumen2 halamanSerie 3 - 2015 AsrIgnacio Garcia0% (2)
- P4 Medicion de Potenciales de Celda y Media CeldaDokumen10 halamanP4 Medicion de Potenciales de Celda y Media CeldaIgnacio GarciaBelum ada peringkat
- Determinación de La Constante de Enfriamiento de Un LiquidoDokumen3 halamanDeterminación de La Constante de Enfriamiento de Un LiquidoIgnacio Garcia0% (3)
- P1 Movilidad IonicaDokumen4 halamanP1 Movilidad IonicaIgnacio GarciaBelum ada peringkat
- P3 Numero de TransporteDokumen6 halamanP3 Numero de TransporteIgnacio GarciaBelum ada peringkat
- Reporte 8 FlotacionDokumen5 halamanReporte 8 FlotacionIgnacio GarciaBelum ada peringkat
- Informe 6 - Mesa WilfleyDokumen5 halamanInforme 6 - Mesa WilfleyIgnacio Garcia67% (3)
- Materiales de Ingenieria Rincon Del VagoDokumen57 halamanMateriales de Ingenieria Rincon Del VagoIgnacio GarciaBelum ada peringkat
- Reporte Práctica 1,2. HIDRODokumen4 halamanReporte Práctica 1,2. HIDROIgnacio GarciaBelum ada peringkat
- Electrobeneficio de CobreDokumen5 halamanElectrobeneficio de CobreIgnacio GarciaBelum ada peringkat
- Fundición Tarea 9 (2015-1)Dokumen4 halamanFundición Tarea 9 (2015-1)Ignacio GarciaBelum ada peringkat
- Calor Latente Fusion Hielo COMPLETADokumen7 halamanCalor Latente Fusion Hielo COMPLETAIgnacio GarciaBelum ada peringkat
- 1er Inf. Ensayos Por Via SecaDokumen7 halaman1er Inf. Ensayos Por Via SecaReforzamiento Hex UniBelum ada peringkat
- EXAMEN Uniones QcasDokumen4 halamanEXAMEN Uniones Qcaslauraghione100% (1)
- Los HalógenosDokumen4 halamanLos HalógenosLinda PinedaBelum ada peringkat
- ATOMOSDokumen10 halamanATOMOSPamela PalominoBelum ada peringkat
- El Factor ClarkDokumen9 halamanEl Factor ClarkCristian Eduardo Perez EspejoBelum ada peringkat
- Modulo 3 Agua para Fertirriego Flores PDFDokumen40 halamanModulo 3 Agua para Fertirriego Flores PDFWilliam PachonBelum ada peringkat
- Tarea de QuimicaDokumen4 halamanTarea de QuimicaMaricel GarciaBelum ada peringkat
- Ensayo A La LlamaDokumen13 halamanEnsayo A La LlamaCindy VillacisBelum ada peringkat
- 8cienciascuadernillo 1 8voDokumen10 halaman8cienciascuadernillo 1 8vosofia caceresBelum ada peringkat
- Sustancias SimplesDokumen11 halamanSustancias Simplesdetodounpoco57Belum ada peringkat
- Reconocimiento de Moléculas OrgánicasDokumen16 halamanReconocimiento de Moléculas Orgánicasvictor garridoBelum ada peringkat
- Quimica InorganicaDokumen48 halamanQuimica InorganicaJaime Olazo MolloBelum ada peringkat
- Clase 16 VolumetríaDokumen21 halamanClase 16 VolumetríaEltunche 1234Belum ada peringkat
- Energia ReticularDokumen3 halamanEnergia ReticularMiguel SánchezBelum ada peringkat
- Calculo FertilizanteDokumen11 halamanCalculo FertilizantepacorosadesaronBelum ada peringkat
- Titulación ComplexométricaDokumen8 halamanTitulación ComplexométricaCeleni Jaime BadaBelum ada peringkat
- Evaluacion de Quimic4 29-07-2022Dokumen3 halamanEvaluacion de Quimic4 29-07-2022Duvan Sanchez CanabalBelum ada peringkat
- Nutrición y Fertilización en PitayaDokumen28 halamanNutrición y Fertilización en Pitayaisneida elizabeth quiñones martine0% (1)
- Estructura BCCDokumen11 halamanEstructura BCCJesús Cabrera CamachoBelum ada peringkat
- Estudio de Estabilidad Del Nitroprusiato de Sodio Frente A Diferentes Condiciones de PH, Temperatura, Luz, OxígenoDokumen16 halamanEstudio de Estabilidad Del Nitroprusiato de Sodio Frente A Diferentes Condiciones de PH, Temperatura, Luz, OxígenoPaola Espinosa LopezBelum ada peringkat
- Guia QMC Gral I - 2024 - 1er ParcialDokumen32 halamanGuia QMC Gral I - 2024 - 1er ParcialEugenio RamírezBelum ada peringkat
- Triptico de UranioDokumen3 halamanTriptico de Uranioheder pauccarBelum ada peringkat
- Tipos de Reacciones - ShortDokumen2 halamanTipos de Reacciones - ShortAleeida Heydi Ruiz PérezBelum ada peringkat
- Quimica InformeDokumen5 halamanQuimica InformeDaniel Gomez AgredoBelum ada peringkat
- Decimo Tabla PeriodiocaDokumen3 halamanDecimo Tabla PeriodiocaJhon Mario DiazBelum ada peringkat
- Estequiometria 2Dokumen4 halamanEstequiometria 2Beatriz Beaus GuerolaBelum ada peringkat
- Compuestos Iónicos y Sus FórmulasDokumen12 halamanCompuestos Iónicos y Sus FórmulasMariaFonsecaBelum ada peringkat
- GUIA 2 DE QUIMICA RESUMEN Y EJERCICIOS (Masa Atómica, Molecular y Mol)Dokumen3 halamanGUIA 2 DE QUIMICA RESUMEN Y EJERCICIOS (Masa Atómica, Molecular y Mol)Ana AndradeBelum ada peringkat
- Memoria Descriptiva de Los Equipos para 800 TMDDokumen7 halamanMemoria Descriptiva de Los Equipos para 800 TMDJuan ValerBelum ada peringkat
- Articulo ZirconioDokumen17 halamanArticulo ZirconioJohann Manuel Londoño ReyesBelum ada peringkat