Laboratorio Química 1 General
Diunggah oleh
Wilberto Yanes0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
21 tayangan4 halamanquímica 1 general
Judul Asli
Laboratorio química 1 general
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Iniquímica 1 general
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
21 tayangan4 halamanLaboratorio Química 1 General
Diunggah oleh
Wilberto Yanesquímica 1 general
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 4
WILBERTO YANES
13.139.260
SECCIN EI
LABORATORIO DE QUMICA GENERAL
PRCTICA N 3
DEMOSTRAR EXPERIMENTALMENTE LA LEY DE LA
CONSERVACIN DE LA MASA
Objetivos a desarrollar:
Manejo correcto de la balanza, identificando las causas ms
frecuentes del error en las pesadas.
En una reaccin qumica, determinar la masa de reactantes y de
productos.
Determinar la frmula emprica de una sal formada por los elementos
Cinc y Cloro.
Establecer una ecuacin qumica en funcin de la Ley de la
Conservacin de la Masa.
Instrucciones Previas:
Manejo del cido Clorhdrico: Se debe tener cuidado al trabajar
experimentalmente con cidos, hidrxidos u otras sustancias que
sean altamente corrosivas o venenosas. El cido clorhdrico o cido
muritico, es un cido fuerte de color amarillo o incoloro con olor
penetrante, sus vapores son irritantes a los ojos y a las mucosas. Al
momento de agregar el metal (Cinc) sobre el cido, tratar de evitar
salpicaduras y utilizar la campana de extraccin evitando as la
inhalacin de vapores txicos.
Constatar que el metal se consuma completamente en la reaccin, y
que el producto slido obtenido est completamente seco antes de
ser pesado.
Para acelerar la reaccin qumica y evaporar el exceso de cido
clorhdrico, se har recurso del Mechero Bunsen. Calentar
suavemente la disolucin dispuesta en el Erlenmeyer hasta su
sequedad utilizando la rejilla amiantada (Bajo campana de
extraccin).
Pre-Laboratorio:
Ley de Conservacin de la Masa: Formulada por el cientfico
francs Antoine Lavoisier la cual establece que, la materia no se crea
ni se destruye, solo se transforma. Por consiguiente, en toda reaccin
qumica la masa total de los reactivos es igual a la masa de los
productos.
Ley de las Proporciones Definidas: Ley enunciada por Joseph
Proust, basada en el principio de que, la proporcin de cada elemento
en un compuesto es fija o constante. Un compuesto qumico tiene
una proporcin de elementos definida por su volumen sin importar la
cantidad del compuesto.
Concepto de Mol: El Mol es la Unidad Internacional Bsica de
Sustancia. Mide la cantidad de sustancia. Se define como la cantidad
de una sustancia que contiene tantas entidades elementales (tomos,
molculas, iones, electrones, radicales u otras partculas) como
tomos hay exactamente en 12 gramos del istopo de carbono-12.
Este nmero se denomina Nmero de Avogadro, en honor al cientfico
italiano Amadeo Avogadro y su valor comnmente aceptado es
6,0221023 unidades elementales.
Frmula Qumica: Representacin abreviada de un compuesto. En
ella se identifican como mnimo los signos de los elementos que
forman parte de dicho compuesto afectados por unos subndices que
nos indican el nmero de tomos de cada elemento presentes en la
molcula. Las frmulas qumicas se clasifican en: Emprica, Molecular,
Semidesarrollada, Estructural o Desarrollada y Espacial.
Frmula Emprica: Indica la relacin mnima de nmeros enteros
entre los tomos que forman un compuesto. Se obtiene mediante la
el anlisis experimental de un compuesto y relacionable con la
frmula molecular conociendo el peso molecular de la muestra.
Frmula Molecular: Frmula de un compuesto que muestra el
nmero y el tipo de tomos presentes en una molcula, pero no la
distribucin de sus tomos. La frmula molecular es un mltiplo
entero (n ) de la frmula emprica.
Frmula Emprica del xido Fosfrico: P2O5
Frmula Molecular del xido Fosfrico: P4O10
Procedimiento Experimental:
Pesar el Matraz Erlenmeyer o fiola, debe estar vaco, limpio y seco.
Introducir en el mismo una granalla de 0,50 g de Cinc.
Medir en un cilindro graduado 2,5 ml de cido clorhdrico y agregarlos
en el Erlenmeyer.
Agregar el metal en el cido bajo campana de extraccin.
Evaporar el lquido hasta comprobar su sequedad (Bajo campana de
extraccin).
Pesar en matraz con el producto slido obtenido.
Determinar la frmula emprica de dicho slido:
ZnCl2 (Cloruro de Cinc)
2HCl + Zn ------- ZnCl2 + H2
(Ecuacin qumica balanceada en funcin de la Ley de la Conservacin
de la Masa)
Post-Laboratorio:
Qu gas se desprende producto de la reaccin?
Se desprende Hidrgeno.
Por qu se debe secar completamente el producto obtenido?
Para lograr evaporar el reactivo que est en exceso dentro de la
reaccin. El cido clorhdrico.
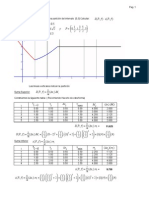
Se hace reaccionar 2,40 g de Mg con un exceso de HCl, obteniendo
9,50 g de producto slido. Cul es la frmula emprica del slido
obtenido?
Se determinan los moles de cada elemento para luego dividir los
resultados obtenidos entre el valor ms pequeo (0,10 moles Mg),
y finalmente con los nmeros enteros obtenidos se determinan los
subndices de la frmula emprica del compuesto.
MgCl2 (Cloruro de Magnesio)
Una muestra de calcio metlico puro que pes 1,35 g reaccion
completamente con oxgeno, obteniendo 1,88 g de producto. Calcule
la frmula emprica del xido formado.
(Base de clculo 0,03 moles Ca)
CaO (xido Clcico)
Anda mungkin juga menyukai
- La Era Prehistórica de La MúsicaDokumen32 halamanLa Era Prehistórica de La MúsicaWilberto YanesBelum ada peringkat
- Capítulo 6Dokumen2 halamanCapítulo 6Wilberto YanesBelum ada peringkat
- Graph SpanishDokumen71 halamanGraph Spanisheber_mermaBelum ada peringkat
- Liderazgo y EmpatíaDokumen10 halamanLiderazgo y EmpatíaWilberto YanesBelum ada peringkat
- Laboratorio 5 JAIRO YANESDokumen5 halamanLaboratorio 5 JAIRO YANESWilberto YanesBelum ada peringkat
- Laboratorio 5 JAIRO YANESDokumen5 halamanLaboratorio 5 JAIRO YANESWilberto YanesBelum ada peringkat
- 5.1.integral DefinidaDokumen9 halaman5.1.integral DefinidaWilberto YanesBelum ada peringkat
- Pertenencia LaboralDokumen11 halamanPertenencia LaboralWilberto YanesBelum ada peringkat
- Laboratorio 5 Wilberto YanesDokumen9 halamanLaboratorio 5 Wilberto YanesWilberto YanesBelum ada peringkat
- SolucionesDokumen13 halamanSolucionesWilberto YanesBelum ada peringkat
- Laboratorio 6 JAIRO YANESDokumen4 halamanLaboratorio 6 JAIRO YANESWilberto YanesBelum ada peringkat
- Laboratorio 2 WILBERTO YANESDokumen5 halamanLaboratorio 2 WILBERTO YANESWilberto YanesBelum ada peringkat
- Graph SpanishDokumen71 halamanGraph Spanisheber_mermaBelum ada peringkat
- Manual MP3Dokumen7 halamanManual MP3Wilberto YanesBelum ada peringkat
- Laboratorio 2 JAIRO YANESDokumen5 halamanLaboratorio 2 JAIRO YANESWilberto YanesBelum ada peringkat
- Curso PDF de BateriaDokumen72 halamanCurso PDF de Bateriaisidrolara25Belum ada peringkat
- 15.2 Presión: A La Fuerza Normal PorDokumen4 halaman15.2 Presión: A La Fuerza Normal Porrosa_pink_SweetBelum ada peringkat
- Libro Fertilidad y Nutrición ForestalDokumen404 halamanLibro Fertilidad y Nutrición ForestalWilliam Brown100% (4)
- 4 Libro 2010 CorregidoDokumen49 halaman4 Libro 2010 CorregidoMaximiliano PortilloBelum ada peringkat
- Manual de FisicaDokumen53 halamanManual de Fisicafrank casahuaman casatilloBelum ada peringkat
- El Vinculo Secreto Entre Hombre y La NaturalezaDokumen18 halamanEl Vinculo Secreto Entre Hombre y La NaturalezaCoral CuBelum ada peringkat
- Clase Termodinámica Biológica PDFDokumen67 halamanClase Termodinámica Biológica PDFDiana Marcela Martinez100% (1)
- 6 - Quimica de La Atmosfera - Contaminacion Al Suelo y ParticuladoDokumen16 halaman6 - Quimica de La Atmosfera - Contaminacion Al Suelo y Particuladokeny hilaryBelum ada peringkat
- EncuestaDokumen5 halamanEncuestaKaren ReyBelum ada peringkat
- Ecología y Pensamiento Revolucionario de Murray BookchinDokumen19 halamanEcología y Pensamiento Revolucionario de Murray BookchinIvan Roemurallas DewarenBelum ada peringkat
- Bulnes Herrera Lizbeth LilianDokumen104 halamanBulnes Herrera Lizbeth LilianMarco antonio Maldonado CevalloBelum ada peringkat
- TRIPTICODokumen2 halamanTRIPTICOBayrin Hernandez100% (1)
- Planeacion Didactica Octubre Biologia ElviaDokumen18 halamanPlaneacion Didactica Octubre Biologia ElviaElvia RochinBelum ada peringkat
- ComosecontaminaelaguaDokumen4 halamanComosecontaminaelagualesly9pantojaBelum ada peringkat
- PRIMERA EVALUACIÓN PARCIAL DE PROCESO - ECOLOGÍA - 2012 2 ImprimirDokumen1 halamanPRIMERA EVALUACIÓN PARCIAL DE PROCESO - ECOLOGÍA - 2012 2 ImprimirAngie Milagros Chistama IglesiasBelum ada peringkat
- Viscosidad de GasesDokumen2 halamanViscosidad de GasesErland VillarroelBelum ada peringkat
- Informe de LaboratorioDokumen4 halamanInforme de LaboratorioCarlos CuellerBelum ada peringkat
- Brasilia Llibre SencerDokumen113 halamanBrasilia Llibre SencerRicardoBelum ada peringkat
- Qui MicaDokumen9 halamanQui MicaDiego Ruiz LópezBelum ada peringkat
- Presuspuesto Cafetin Upeu 1Dokumen22 halamanPresuspuesto Cafetin Upeu 1Will EmgBelum ada peringkat
- Examen ParcialDokumen3 halamanExamen ParcialJuan Jose PachasBelum ada peringkat
- Prelaboratorio No. 3 Densidad''Dokumen11 halamanPrelaboratorio No. 3 Densidad''Fernando BarillasBelum ada peringkat
- Practica 23, Equipo BDokumen19 halamanPractica 23, Equipo BHERIBERTO GAMALIEL VALLE LINDEROBelum ada peringkat
- T1 9° Eras GeológicasDokumen7 halamanT1 9° Eras GeológicasEdna Milena Capera SilvaBelum ada peringkat
- Emisiones A La AtmosferaDokumen4 halamanEmisiones A La AtmosferaAalejandro StarronBelum ada peringkat
- POE SALA DE CALDERAS Zeni IMDokumen2 halamanPOE SALA DE CALDERAS Zeni IMIsa RetuertaBelum ada peringkat
- 5to Evaluación Unidad 4Dokumen3 halaman5to Evaluación Unidad 4Karla Ruiz seguraBelum ada peringkat
- Práctica Nº2 - Rendimiento de Un TamizDokumen6 halamanPráctica Nº2 - Rendimiento de Un TamizJhon Paul SanchezBelum ada peringkat
- Informe de Diseño Sismico - Edificacion de 4 Pisos - Etabs OkDokumen81 halamanInforme de Diseño Sismico - Edificacion de 4 Pisos - Etabs OkOscar Adrian Chavez PanduroBelum ada peringkat
- Quimica Del SueloDokumen6 halamanQuimica Del SueloAdriana Llano100% (1)
- Calculo de Numero de Usuario Por Capacidad de TransformadoresDokumen2 halamanCalculo de Numero de Usuario Por Capacidad de Transformadoresrom_rplBelum ada peringkat