Actividad 1-Cuadro Comparativo Enlaces Quimicos
Diunggah oleh
shagy110879Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Actividad 1-Cuadro Comparativo Enlaces Quimicos
Diunggah oleh
shagy110879Hak Cipta:
Format Tersedia
UNIVERSIDAD
VASCONCELOS DE TABASCO
Actividad I
Cuadro comparativo:
Enlaces qumicos
Materia
Qumica II
Maestra
Ing. Alejandra Hernndez Herrera
Alumno
Alamina Hernndez Paul Alejandro
Paraso, Tabasco.
Mayo de 2015.
Qumica II
ndice
Introduccin
Actividad 1. Enlaces qumicos
1. Definicin
2. Principio fundamental
3. Notacin de Lewis
4. Regla del Octeto
5. Cuadro comparativo
Qumica II
Introduccin
Los elementos qumicos se combinan de diferentes maneras para formar
toda una variedad de compuestos inorgnicos y orgnicos. Hay compuestos
gaseosos, lquidos y slidos, los hay txicos e inocuos, mientras que otros son
altamente benficos para la salud. Las propiedades de cada compuesto
dependen del tipo de elemento qumico que lo forman, el modo cmo se
enlazan (tipo de enlace qumico), la forma y geometra de los agregados
atmicos (molculas) y de cmo estos interactan entre s.
En 1916, el qumico alemn Walther Kossel expuso que en las reacciones
qumicas ocurren perdida y ganancia de electrones por parte de los tomos, y
por ello estos adquieren la configuracin electrnica de un gas noble. Sin duda
Kossel se refera al enlace inico, y por lo tanto a los compuestos inicos.
Posteriormente los qumicos norteamericanos Gilbert Newton Lewis e
Irving Langmuir, cada uno en forma independiente estudiaron los compuestos
inicos y no inicos (covalentes), comprobando que los tomos al formar
enlace qumico adquieren en su mayora la estructura atmica de un gas noble
(8 electrones en el nivel externo), lo que hoy se llama Regla del Octeto.
En 1923, G.N.Lewis plantea su teora de enlace por pares de electrones y
anuncia que el octeto se logra por medio de comparticin de electrones.
Entonces a Kossel lo podemos considerar como el padre del enlace inico, y a
Lewis el padre del enlace covalente.
En 1926, Walter Heitler y Fritz London demostraron que el enlace
covalente en la molcula de H2 se podra explicar mediante la mecnica
cuntica.
La mecnica cuntica describe muy bien a los tomos y estructura
electrnica de los mismos; pero la situacin en la molcula es muy diferente
debido a la mayor complejidad de esta, el aparato matemtico es mucho ms
difcil de formular y los resultados menos fciles de obtener e interpretar.
Hoy en da, los qumicos disponen de mtodos de clculo y de tcnicas
experimentales muy sofisticadas que permiten conocer con exactitud la forma,
geometra y dimensiones de las molculas.
Qumica II
Actividad 1
Enlaces qumicos
1. Definicin
El enlace qumico es la fuerza que mantiene unidos a los tomos delos
elementos qumicos (enlace interatmico) para formar molculas o formar
sistemas cristalinos (inicos, metlicos o covalentes) y molculas (enlace
intermolecular) para formar los estados condensados de la materia (slido y
lquido), dicha fuerza es de naturaleza electromagntica (elctrica y
magntica), predominante fuerza elctrica.
2. Principio fundamental
Los tomos y molculas forman enlaces qumicos con la finalidad de
adquirir un estado de menor energa, para asa lograr una condicin de mayor
estabilidad. En el caso de los tomos, la estabilidad se reflejara en un cambio
de su configuracin electrnica externa.
Veamos la formacin de la molcula de HCl.
La misma energa se requiere como mnimo para romper o disociar el
enlace (energa de disociacin).
Con una grfica veamos la variacin de energa en la formacin del
enlace.
Qumica II
3. Notacin de Lewis
Es la representacin convencional de los electrones de valencia
(electrones que intervienen en los enlaces qumicos), mediante el uso de
puntos o aspas que se colocan alrededor del smbolo del elemento.
En general para los elementos representativos (recordar que el nmero
de grupo indica el nmero de electrones de valencia) tenemos:
4. Regla del Octeto
G.N.Lewis, al estudiar la molcula de hidrgeno (H 2) not que cada
tomo al compartir electrones adquiere dos electrones, o sea la estructura
electrnica del gas noble Helio (2He) y comprob tambin que los dems
tomos que comparten electrones al formar enlace qumico, llegan a adquirir la
estructura electrnica de los gases nobles.
La ley del octeto nos dice como los tomos intercambian electrones
entre si hasta completar ocho electrones en su ltimo nivel de energa, este
comportamiento hace posible la unin qumica de los elementos.
Qumica II
5. Cuadro comparativo
Propiedades
Definicin
Enlace Inico
Es la unin que resulta
de la presencia de
fuerzas de atraccin
electrosttica entre los
iones de distinto signo
y ocurre en la ltima
capa de los electrones
de un tomo.
Enlace Covalente
Es la fuerza
electromagntica que
mantiene unidos a
tomos que comparten
electrones, los cuales
tienen espines o giros
opuestos.
Comportamien
to
Transferencia
electrnica.
Comparticin de
electrones.
Diferencia de
electronegativ
idad
La diferencia entre las
cargas de los iones
provoca entonces una
fuerza de interaccin
electromagntica entre
los tomos que los
mantiene unidos.
La diferencia de
electronegatividades
entre los tomos no es
suficientemente
grande como para que
se efecte una
transferencia de
electrones. De esta
forma, los dos tomos
comparten uno o ms
pares electrnicos en
un nuevo tipo de
orbital, denominado
Enlace Hidrogeno
Enlace Metlico
Es la fuerza atractiva
entre un tomo
electronegativo y un
tomo de hidrogeno
unido covalentemente
a otro tomo
electronegativo.
Es un enlace que
mantiene unido los
tomos (unin entre
ncleos atmicos y los
electrones de valencia,
que se juntan
alrededor de estos
como una nube) de los
metales entre s.
Vinculacin de
electrones por medio
de un tomo de
hidrogeno.
El tomo de hidrogeno
tiene una carga parcial
positiva, por lo que
atrae a la densidad
electrnica de un
tomo cercano en el
espacio.
Liberacin de
electrones.
Es el enlace que se da
entre elementos de
electronegatividades
bajas y muy parecidas,
en estos casos ninguno
de los tomos tiene
ms posibilidades que
el otro de perder o
ganar los electrones.
Qumica II
orbital molecular.
Propiedades
Elementos
qumicos que
lo conforman
Enlace Inico
Este tipos de enlaces
se forman entre
tomos con 1, 2 o 3
electrones en el ltimo
nivel de energa (IA,
IIA, IIIA) en
combinacin con
tomos de 5, 6, o 7
electrones en la ltima
capa (VA, VIA, VIIA).
Enlace Covalente
Los enlaces covalentes
se suelen producir
entre elementos
gaseosos no metales.
Enlace Hidrogeno
Dadores de Hidrogeno:
Grupo hidroxilo
(OH).
Grupo amino (NH).
Un hidrocarburo
(CH).
Dadores de electrones:
Oxgeno.
Azufre.
Nitrgeno.
Halgenos.
Enlace Metlico
Este tipo de enlace se
produce entre
elementos poco
electronegativos
(metales).
Qumica II
Partculas que
lo forman
Catin (carga positiva).
Anin (carga negativa).
Aspecto cristalino y
Caracterstica
s
Molculas.
tomos.
Molculas.
tomos.
A temperatura
Las sustancias
Estructuras
experimentan
cambios en sus
propiedades, como
el punto de fusin.
Cuentan con
diferentes valores
en referente a la
energa de sus
enlaces que se
expresan en KJ/mol.
Cristalinas
compactas.
Temperaturas de
fusin elevadas.
Temperaturas de
ebullicin elevadas.
Principales formas
de modificar las
propiedades de los
elementos
metlicos puros.
frgil.
ambiental pueden
Elevados puntos de
ser slidos, lquidos
fusin y ebullicin.
o gaseosos.
Capacidad de
Algunos son slidos
cristalinos.
conducir la corriente
Generalmente
elctrica.
tienen baja
temperatura de
fusin y ebullicin.
Generalmente son
insolubles en agua,
pero si son solubles
en solventes
apolares.
Son aislantes, son
malos conductores
elctricos.
Cationes.
Anda mungkin juga menyukai
- Plan de Investigación - Enlace QuímicoDokumen37 halamanPlan de Investigación - Enlace QuímicoMaribel LuceroBelum ada peringkat
- Capitulo 4 2021 IDokumen89 halamanCapitulo 4 2021 IDavid FigueroaBelum ada peringkat
- UNIDAD 2 - Química INDDokumen71 halamanUNIDAD 2 - Química INDJonathan Ramiro Grijalva herreraBelum ada peringkat
- Quimica I, Informacion SemanaDokumen11 halamanQuimica I, Informacion SemanaShophia Madalena Huan KooBelum ada peringkat
- ACFrOgB 7ubGBrPTaqcmYGntum ATVFVpkpjUgHM9DJekY2TaY K7H8QxSpY5CFBUCon JCrH1XMRq5AJiA9trm9AFy6iYh6IoKAs5gQi3yfaw8sw-LhakM3Fto5TzXW a52vahaRguld7fTq5MWDokumen78 halamanACFrOgB 7ubGBrPTaqcmYGntum ATVFVpkpjUgHM9DJekY2TaY K7H8QxSpY5CFBUCon JCrH1XMRq5AJiA9trm9AFy6iYh6IoKAs5gQi3yfaw8sw-LhakM3Fto5TzXW a52vahaRguld7fTq5MWDavid FigueroaBelum ada peringkat
- Unidad 2 TemarioDokumen23 halamanUnidad 2 TemarioTony M KroosBelum ada peringkat
- Enlaces Quimicos, Practica 5to PeritoDokumen4 halamanEnlaces Quimicos, Practica 5to PeritoErickson AmadorBelum ada peringkat
- Enlaces Químicos y El Estado Sólido (Cristalino - 1Dokumen9 halamanEnlaces Químicos y El Estado Sólido (Cristalino - 1Christian RicoBelum ada peringkat
- Química ComúnDokumen20 halamanQuímica ComúnClases Particulares SantiagoBelum ada peringkat
- IP Práctica 7 - Equipo 1Dokumen21 halamanIP Práctica 7 - Equipo 1José Luis Urbiola RodríguezBelum ada peringkat
- Informe Ciencias NaturalesDokumen15 halamanInforme Ciencias NaturalesMaria Eleonora Foitzick PalmaBelum ada peringkat
- Quimica N°3Dokumen18 halamanQuimica N°3Deivi Jampier Aguilar EspinozaBelum ada peringkat
- Enlace QuimicoDokumen23 halamanEnlace QuimicoJUNIOR JESUS VALENTE MAYHUIREBelum ada peringkat
- Enlaces QuimicosDokumen12 halamanEnlaces QuimicosRuben Eduardo Vásquez PeñaBelum ada peringkat
- Enlace Químico y Sus ClasesDokumen3 halamanEnlace Químico y Sus Clases1977dianaBelum ada peringkat
- 8°qca Estructura de LewisDokumen5 halaman8°qca Estructura de Lewissylvia lópez navarreteBelum ada peringkat
- Informe de Lab Oratorio 2Dokumen9 halamanInforme de Lab Oratorio 2anon-675389Belum ada peringkat
- Practica 6Dokumen4 halamanPractica 6Genaro AbrahamBelum ada peringkat
- Tema 9Dokumen6 halamanTema 9ElRamen 54Belum ada peringkat
- Informe de Laboratorio 2Dokumen26 halamanInforme de Laboratorio 2Javier Alexander SozaBelum ada peringkat
- Trabajo de QuimicaDokumen80 halamanTrabajo de QuimicaHiram YairBelum ada peringkat
- Enlace QuímicoDokumen26 halamanEnlace QuímicoBruno FernándezBelum ada peringkat
- Qué Son Los Enlaces QuímicosDokumen3 halamanQué Son Los Enlaces QuímicosAndrik Gabriel Cortés MartínezBelum ada peringkat
- Monografia de QuimicaDokumen23 halamanMonografia de Quimicakhkrenth0% (1)
- Trabajo de Enlaces QuimicosDokumen75 halamanTrabajo de Enlaces QuimicosJavier Gallo Espinoza80% (5)
- Enlace QuimicoDokumen6 halamanEnlace QuimicoShirly Torres MejiaBelum ada peringkat
- Unidad 2 Enlaces Quimicos y Compuestos InorganicosDokumen28 halamanUnidad 2 Enlaces Quimicos y Compuestos InorganicosAlvaro DiazBelum ada peringkat
- Enlaces Quimicos, Proyecto FinalDokumen9 halamanEnlaces Quimicos, Proyecto FinalMANUEL BAUTISTA ANETTE MICHELLBelum ada peringkat
- Enlace QuímicoDokumen3 halamanEnlace Químicoanitaperez1Belum ada peringkat
- Informe 5 Enlace Quimico - CompressDokumen15 halamanInforme 5 Enlace Quimico - Compressjosciney davidBelum ada peringkat
- Enlace QuimicoDokumen19 halamanEnlace QuimicoRenzo Augusto Mamani CherresBelum ada peringkat
- ENLACEDokumen12 halamanENLACETevi Thiago AreizaBelum ada peringkat
- Enlaces QuimicosDokumen18 halamanEnlaces QuimicosEdgar MeléndezBelum ada peringkat
- Bloque 2 - Unidad 4 El EnlaceDokumen8 halamanBloque 2 - Unidad 4 El EnlaceMarcos Campayo FernándezBelum ada peringkat
- Cce h11 Enlace QuimicoDokumen9 halamanCce h11 Enlace Quimicoroberto hsBelum ada peringkat
- Enlace QuimicoDokumen14 halamanEnlace QuimicoYesenia SCBelum ada peringkat
- Uniones Quimicas 2019 PDFDokumen68 halamanUniones Quimicas 2019 PDFLucia WalkerBelum ada peringkat
- Propiedades Materiales Con Enlaces Iónicos, Covalentes y PolaresDokumen6 halamanPropiedades Materiales Con Enlaces Iónicos, Covalentes y PolaresAndrea UrrutiaBelum ada peringkat
- Clase #5 IqDokumen9 halamanClase #5 IqGeorgina Franca LioiBelum ada peringkat
- UNIDAD 3 - Enlace Quimico (Cap 9 y 10)Dokumen8 halamanUNIDAD 3 - Enlace Quimico (Cap 9 y 10)Fla TossoliniBelum ada peringkat
- Clei 3 QuimicaDokumen4 halamanClei 3 Quimicajuan catañoBelum ada peringkat
- Enlaces Quimicos P2Dokumen7 halamanEnlaces Quimicos P2Karla GonzálezBelum ada peringkat
- GUIA 8° Enlaces QuimicosDokumen3 halamanGUIA 8° Enlaces QuimicosJacqueline Betancourtt MejíasBelum ada peringkat
- Enlace QuímicoDokumen16 halamanEnlace Químicoaguirre sergio danielBelum ada peringkat
- Enlaces QuímicosDokumen2 halamanEnlaces QuímicosMafeBelum ada peringkat
- Uniones QuimicasDokumen11 halamanUniones QuimicasRosario Lopez MirandaBelum ada peringkat
- Taller 5 Estructuras de LewisDokumen12 halamanTaller 5 Estructuras de Lewisandrea vanegasBelum ada peringkat
- Nociones de Enlace Químico InteratómicoDokumen17 halamanNociones de Enlace Químico InteratómicoJosé Luis Fernandez MirandaBelum ada peringkat
- Guà - A Teã Rica Clase 3Dokumen20 halamanGuà - A Teã Rica Clase 3marce eugeBelum ada peringkat
- Tercer Año 8º Clase QuimicaDokumen13 halamanTercer Año 8º Clase QuimicaGraciela Beatriz acostaBelum ada peringkat
- Enlaces QuímicosDokumen8 halamanEnlaces QuímicosXiu XhonneuxBelum ada peringkat
- Enlaces QuimicosDokumen10 halamanEnlaces QuimicosAdriana Maria Gomez JimenezBelum ada peringkat
- Taller 2 Conceptos Basicos de Enlace Quimico V00Dokumen12 halamanTaller 2 Conceptos Basicos de Enlace Quimico V00jorgeBelum ada peringkat
- Enlace (Química)Dokumen15 halamanEnlace (Química)AnaBelum ada peringkat
- Primera Actividad Del Tercer Momento Quimica 5to AñoDokumen6 halamanPrimera Actividad Del Tercer Momento Quimica 5to AñoTrino Jose Chacon ZambranoBelum ada peringkat
- Enlaces QuímicosDokumen88 halamanEnlaces Químicosjose damasBelum ada peringkat
- EnlaceDokumen11 halamanEnlaceSTEPHANIE HERNANDEZ GARCIABelum ada peringkat
- Practica2 - Enlaces QuimicosDokumen6 halamanPractica2 - Enlaces QuimicosALEJANDRA MONTANTESBelum ada peringkat
- Química - Enlaces QuímicosDokumen11 halamanQuímica - Enlaces QuímicosMariangelis José Lozada AcuñaBelum ada peringkat
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaDari EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaPenilaian: 5 dari 5 bintang5/5 (1)
- Metodos de Control de PozosDokumen34 halamanMetodos de Control de Pozosshagy110879100% (1)
- Control de Pozos ApuntesDokumen191 halamanControl de Pozos Apuntesshagy110879Belum ada peringkat
- Tuberías y Aparejos de ProduccionDokumen25 halamanTuberías y Aparejos de Produccionshagy110879Belum ada peringkat
- PozosDokumen17 halamanPozosshagy110879Belum ada peringkat
- SubjetivismoDokumen3 halamanSubjetivismoshagy110879Belum ada peringkat
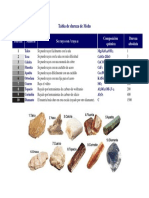
- Tabla de Dureza de MohsDokumen1 halamanTabla de Dureza de Mohsshagy110879Belum ada peringkat
- Elaboracion de CronogramaDokumen4 halamanElaboracion de Cronogramashagy110879Belum ada peringkat
- ComputacionDokumen71 halamanComputacionshagy110879Belum ada peringkat
- APUNTESDokumen368 halamanAPUNTESJesús Santillán100% (2)
- 04TI Bombas CentrífugasDokumen16 halaman04TI Bombas Centrífugasshagy110879Belum ada peringkat
- 01TEC-Bombas Dinamicas PerifericasDokumen11 halaman01TEC-Bombas Dinamicas Perifericasshagy110879100% (1)
- 1) Introducción A La IndumentariaDokumen7 halaman1) Introducción A La IndumentariaAnita MuruaBelum ada peringkat
- Eutanasia en El Perú y Su Regulación Jurídica Como Alternativa A Una Muerte DignaDokumen3 halamanEutanasia en El Perú y Su Regulación Jurídica Como Alternativa A Una Muerte DignaMaria Lluliana Tocto PeñaBelum ada peringkat
- Semiología GastrointestinalDokumen24 halamanSemiología GastrointestinalFelix JhonBelum ada peringkat
- Bio PlaguicidasDokumen27 halamanBio PlaguicidasMaritza CrippaBelum ada peringkat
- TS2 - WeiShenV PDFDokumen505 halamanTS2 - WeiShenV PDFGala DramasBelum ada peringkat
- TDAHDokumen4 halamanTDAHLizbeth herrera reyesBelum ada peringkat
- Fundamentación Científica y TecnológicaDokumen17 halamanFundamentación Científica y TecnológicaJulio ValdezBelum ada peringkat
- Media FiliacionDokumen2 halamanMedia FiliacionASMR CINDYBelum ada peringkat
- Universidad Catolica Andres Bello FacultDokumen14 halamanUniversidad Catolica Andres Bello FacultCaden Prinx ValentBelum ada peringkat
- Cervical GiaDokumen25 halamanCervical Gialuis romero cañasBelum ada peringkat
- Star Trek 06 - Cooper, Sonni - Fuego NegroDokumen143 halamanStar Trek 06 - Cooper, Sonni - Fuego NegroxicmenBelum ada peringkat
- Mascotas Servicio y Apoyo Emocional - AeroméxicoDokumen1 halamanMascotas Servicio y Apoyo Emocional - AeroméxicoCaroBelum ada peringkat
- Bioestrati Pisco PeruDokumen158 halamanBioestrati Pisco PeruDavid Bernardo Altamirano ArevaloBelum ada peringkat
- Shell Corena S4 R 68 - MSDSDokumen16 halamanShell Corena S4 R 68 - MSDStania quispe pilcoBelum ada peringkat
- Plan de Mantenimiento PreventivoDokumen18 halamanPlan de Mantenimiento PreventivoBRICELISBelum ada peringkat
- Morgade. La Educación Sexual Integral Como Proyecto de Justicia SocialDokumen6 halamanMorgade. La Educación Sexual Integral Como Proyecto de Justicia SocialLady in RedBelum ada peringkat
- Distribucion de Probabilidades DiscretasDokumen33 halamanDistribucion de Probabilidades DiscretasSolansh Arlet Ledezma PazBelum ada peringkat
- Película El Discurso Del ReyDokumen2 halamanPelícula El Discurso Del Reymatt joelBelum ada peringkat
- Maquinaria 2021, Uni. 1Dokumen50 halamanMaquinaria 2021, Uni. 1Yena IturraBelum ada peringkat
- Catalogo Foc-Mul MoqueguaDokumen137 halamanCatalogo Foc-Mul MoqueguaJose MendozaBelum ada peringkat
- Toxicologia - Guion de MetalesDokumen5 halamanToxicologia - Guion de MetalesMay CardozoBelum ada peringkat
- Factura LuzDokumen1 halamanFactura LuzAnibal HernandezBelum ada peringkat
- Serie Ambient 30 - Madera 3mm Dokka FloorsDokumen2 halamanSerie Ambient 30 - Madera 3mm Dokka FloorsCOTA ESTUDIO DE ARQUITECTURABelum ada peringkat
- Informe de Test de VinelandDokumen4 halamanInforme de Test de VinelandJorge ReyesBelum ada peringkat
- TicketDokumen2 halamanTicketRodrigo MarineraBelum ada peringkat
- Autoregistro de AnsiedadDokumen8 halamanAutoregistro de Ansiedadps.pablovalderramaBelum ada peringkat
- A Chachai RuDokumen65 halamanA Chachai RuMARITZA QUISPE VILLARREALBelum ada peringkat
- BlindajesDokumen90 halamanBlindajesinmarorBelum ada peringkat
- Requisitos Esenciales de La Procedencia Del AmparoDokumen1 halamanRequisitos Esenciales de La Procedencia Del AmparoYESSICA MARIBEL HERNANDEZ CABRERABelum ada peringkat
- Guia SeduccionDokumen39 halamanGuia Seduccionantonny aybarBelum ada peringkat