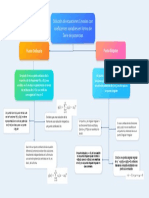
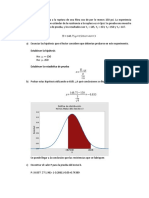
16 Amortiguadores 2 P S PDF
Diunggah oleh
EdwinJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
16 Amortiguadores 2 P S PDF
Diunggah oleh
EdwinHak Cipta:
Format Tersedia
1/9/2015
Captulo 16
Equilbrio Inico Acuoso
Adaptado por:
IleanaNievesMartnez
Copyright 2011 Pearson Education, Inc.
Amortiguadores
Amortiguador o Buffers
Soluciones que resisten pH cuando se aade cido
base
Neutralizan el cido o la base aadido.
Su capacidad tiene un lmite
Es una mezcla del par conjugado:
cido dbil/base conjugada (sal con anin)
o Ejemplo: sangre - mezcla de H2CO3 y HCO3
base dbil/cido conjugado (sal con catin).
o Ejemplo: (NH4+/NH3)
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
1/9/2015
Preparar un amortiguador cido
cido dbil
Base conjugada
Soln
amortiguadora
cido actico
HC2H3O2
Acetato de sodio
NaC2H3O2
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
Cmo fucionan los amortiguadores?
HA(ac) + H2O(l) A(ac) + H3O+(ac)
H2O
A
nuevo
HA
HA
OH
aadido
H3O+
Neutralizacin
HA(ac) + OH(ac) A(ac) + H2O(l)
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
1/9/2015
Cmo fucionan los amortiguadores?
HA(ac) + H2O(l) A(ac) + H3O+(ac)
H2O
HA
nuevo
HA
H3O+
Aadido
H3O+
Neutralizacin
H3O+(ac) + A(ac) HA(ac) + H2O(l)
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
Qu efecto tiene la presencia de un in comn
sobre los amortiguadores?
H2O
HA
nuevo
HA
H3O+
AAadido
HA(ac) + H2O(l) A(ac) + H3O+(ac)
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
1/9/2015
Efecto de In Comn
HA(ac) + H2O(l) A(ac) + H3O+(ac)
A(ac) + H2O(l) HA(ac) + OH(ac)
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
Efecto de In Comn
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
1/9/2015
Ejemplo 16.1: Calcule el pH de un amortiguador que
contiene 0.100 M HC2H3O2 y 0.100 M NaC2H3O2
HC2H3O2 + H2O C2H3O2 + H3O+
0.100
0.100 x
0.100
0.100 +x
= [H3O+]
Ka = [H3O+]
log Ka = log [H3O+]
pKa = pH
Aproximacin vlida
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
Prctica Determine el pH de un amortiguador con 0.14 M
HF (pKa = 3.15) y 0.071 M KF
HF + H2O F + H3O+
0.14
0.14 x
0.071
0.071 + x
Cotejo de Ka
Aproximacin vlida
Tro: Chemistry: A Molecular Approach, 2/e
10
Copyright 2011 Pearson Education, Inc.
1/9/2015
Derivacin de la ecuacin de Henderson-Hasselbalch
H 3O A
Ka
HA
A
log Ka log H 3O log HA
A
pKa pH log HA
Despejando por pH
pH pKa log HA
pH pKa log
anin de la base conjugada
cido dbil 0
Vlida para x pequeo
[HA]0 y [A] 0 > (102 103) x Ka
Tro: Chemistry: A Molecular Approach, 2/e
11
Copyright 2011 Pearson Education, Inc.
Ejemplo 16.2: Calcule el pH del amortiguador 0.050 M HC7H5O2
y 0.150 M NaC7H5O2
Ka (HC7H5O2)= 6.5 x 105
HC7H5O2 + H2O C7H5O2 + H3O+
Tro: Chemistry: A Molecular Approach, 2/e
12
Copyright 2011 Pearson Education, Inc.
1/9/2015
Prctica Determine el pH de amortiguador
0.14 M HF (pKa = 3.15) y 0.071 M KF?
HF + H2O F + H3O+
Tro: Chemistry: A Molecular Approach, 2/e
13
Copyright 2011 Pearson Education, Inc.
Clculo de pH al aadir OH
Equilibrio en el HA + H O A + H O+
2
3
amortiguador
Adicin de base:
HA + OH A + H2O
neutralizacin
Moles inicial
[HA]0
[A-]0
[-y]rx [+y]rx [+y]rx
Moles que rx
Moles despus de rx [HA]0-y
[A-]0+y
Equilibrio nuevo despus
HA + H2O A + H3O+
de la nuetralizacin
[HA]0-y
[A-]0+y
Tro: Chemistry: A Molecular Approach, 2/e
14
Copyright 2011 Pearson Education, Inc.
1/9/2015
Clculo de pH al aadir H3O+
Equilibrio del
amortiguador
B + H2O HB+ + OH
Adicin de cido:
B + H3O+ HB+ + H2O
neutralizacin
Moles inicial
[HB+]0
[B]0
[-y]rx [+y]rx [+y]rx
Moles que rx
[HB+]0+y
Moles despus de rx [B]0-y
Equilibrio nuevo
nuevo despus de
la nuetralizacin
B + H2O HB+ + OH
[HB+]0+y
[B]0-y
Tro: Chemistry: A Molecular Approach, 2/e
15
Copyright 2011 Pearson Education, Inc.
Ejemplo 16.3: Calcule el pH de un amortiguador con 0.100 moles
HC2H3O2 y 0.100 moles de NaC2H3O2 en 1.00 L al que se le aade
0.010 moles NaOH
neutralizacin HC2H3O2 + OH C2H3O2 + H2O
Moles inicial
0.100
0.100
0.010 +y = +0.010
Moles que rx -y = 0.010
Moles despus de rx
0.090
0.110
Si lo que se aade es una base, escriba la
reaccin de OH con HA. Si aade cido,
escriba la reaccin para H3O+ con A.
Tro: Chemistry: A Molecular Approach, 2/e
16
Copyright 2011 Pearson Education, Inc.
1/9/2015
Continuacin del Ejemplo 16.3: Calcule el pH de un amortiguador con 0.100
moles HC2H3O2 y 0.100 moles de NaC2H3O2 en 1.00 L al que se le aade
0.010 moles NaOH
Base aadida con amortiguador
Base aadida sin amortiguador
HC2H3O2 + H2O C2H3O2 + H3O+
pKa for HC2H3O2 = 4.745
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
17
Ecuacin de Henderson-Hasselbalch
para amortiguadores bsicos
B: + H2O H:B+ + OH
Para aplicar HendersonHasselbalch la reaccin se
escribe en forma cida
H:B+ + H2O B: + H3O+
Para aplicar HendersonHasselbalch en forma
bsica
Tro: Chemistry: A Molecular Approach, 2/e
18
Esto no afecta las
concentraciones
Copyright 2011 Pearson Education, Inc.
1/9/2015
Amortiguadores Bsicos
B:(ac) + H2O(l) H:B+(ac) + OH(ac)
Se pueden preparar mezclando una base dbil, (B:),
con una sal que contenga su cido cojugado, H:B+Cl
base
dbil
cido
conjugado
H2O(l) + NH3 (ac) NH4+(ac) + OH(ac)
Soln
amortiguadora
Amoniaco
NH3
Tro: Chemistry: A Molecular Approach, 2/e
19
Cloruro de amonio
NH4Cl
Copyright 2011 Pearson Education, Inc.
Ejemplo 16.4: Calcule el pH de un amortiguador [NH3] = 0.50 M y
[NH4Cl] = 0.20 M (pKb = 4.75) NH3 + H2O NH4+ + OH pKa + pKb = 14
Procedimiento # 1:
Tro: Chemistry: A Molecular Approach, 2/e
Procedimiento # 2:
20
Copyright 2011 Pearson Education, Inc.
10
1/9/2015
Intervalo efectivo para el amortiguador
0.1 < [base]:[cido] < 10
pH ms alto
pH ms bajo
Por lo tanto el intervalo efectivo es pKa 1
Al escojer amortiguador, debe tener el pKa ms
cercano al pH requerido.
Tro: Chemistry: A Molecular Approach, 2/e
21
Copyright 2011 Pearson Education, Inc.
Ejemplo 16.5a: Cul de los cidos a continuacin
ser la mejor eleccin para combinar con su sal de
sodio para hacer un amortiguador con pH 4.25?
cido Cloroso, HClO2
cido Nitroso, HNO2
cido Frmico, HCHO2
cido Hipocloroso, HClO
pKa = 1.95
pKa = 3.34
pKa = 3.74
pKa = 7.54
Respuesta:
cido Frmico, HCHO2
pKa = 3.74
El pKa de HCHO2 es el ms cercano al pH del
amortiguador deseado y junto con su par
conjugado ser el amortiguador ms efectivo.
Tro: Chemistry: A Molecular Approach, 2/e
22
Copyright 2011 Pearson Education, Inc.
11
1/9/2015
Ejemplo 16.5b: Determine la razn NaCHO2 : HCHO2
necesaria para preparar un amortiguador con pH 4.25
cido Frmico, HCHO2, pKa = 3.74
Para preparar el amortiguador
de pH 4.25, usar 3.24 veces
ms cantidad de NaCHO2 que
de HCHO2
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
23
Prctica Determine la masa de NaC2H3O2 que se debe disolver en 300 mL de
una solucin HC2H3O2 0.25 M para preparar un amortiguador de pH 5.09.
(Ka = 1.8 x 10-5)
HC2 H 3O2 H 2O H 3O C2 H 3O2
HC2 H 3O2 0 0.25 M
1.8 x10 5
10 pH
C2 H 3O2 ?
H 3 O C 2 H 3 O 2
Ka
1.8 x10 5
H
C
H
O
2 3 2
5.09
10
C 2 H 3 O 2 8.1 x10 6 C 2 H 3 O 2
0.25
0.25
1.8 x10 0.25 C
5
8.1 x10
g ( m asa ) 0.56
H 3 O 2 0.56 M
m oles
L
x 0.300 L x 82.0 g NmaCol H O
2
g ( m asa ) 14 g de N aC 2 H 3 O 2
Tro: Chemistry: A Molecular Approach
24
Copyright 2011 Pearson Education, Inc.
12
1/9/2015
Titulacin
En titiulacin cido-base,
agente titulante solucin que se aade lentamente desde
una bureta
La solucin aadida - concentracin desconocida
Se aade a solucin - cocentracin conocida
Punto final cuando visiblemente se completa la reaccin
(detectado con indicador)
Indicador especie qumica que cambia en color en
funcin de pH y se aade para detectar el punto final
Punto de equivalencia moles H3O+ = moles OH
Tro: Chemistry: A Molecular Approach, 2/e
25
Copyright 2011 Pearson Education, Inc.
Titulacin monitoreo de pH
Comienzo de la
titulacin
Punto de
equivalencia
Medida de conductividad por [H3O+]
con sensor especfico
El punto final punto de equivalencia
punto de infleccin de la curva
se monitorea con un indicador
Tro: Chemistry: A Molecular Approach, 2/e
26
Copyright 2011 Pearson Education, Inc.
13
1/9/2015
Indicadores
Son cidos dbiles en equilbrio:
HInd(ac) + H2O(l) Ind(ac) + H3O+(ac)
Cambian de color con pH.
Depende de la conentracin relativa de [Ind] : [HInd]
o [Ind] : [HInd] 1, el color mezcla de los colores de [Ind] y [HInd]
o [Ind] : [HInd] > 10, el color ser el color de Ind
o [Ind] : [HInd] < 0.1, el color ser de HInd
Intervalo Efectivo para el indicador:
pH = pKa(indicador) 1
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
27
Fenoftalena
bsico - rosa
cido - incoloro
Tro: Chemistry: A Molecular Approach, 2/e
28
Copyright 2011 Pearson Education, Inc.
14
1/9/2015
Rojo de Metilo
Cambio en color de rojo de metilo
(CH3)2N
H
C
H
C
C
H
C
H
H3O+
H
C
(CH3)2N
OH-
N
H
H
C
C
H
H
C
H
C
CH
NaOOC
H
C
C
C
H
H
C
C
H
CH
C
C
H
NaOOC
Tro: Chemistry: A Molecular Approach, 2/e
29
Copyright 2011 Pearson Education, Inc.
Monitoreo de Titulacin con indicador
pKa de HInd pH en el punto de equivalencia
Indicadores cido-base
Tro: Chemistry: A Molecular Approach, 2/e
30
Copyright 2011 Pearson Education, Inc.
15
1/9/2015
Curva de Titulacin
Grfica de pH vs. cantidad de agente titulante
El punto de infleccin es el punto de equivalencia
Puntos importantes en la curvas
Antes del punto de equivalencia
o La solucin en el matraz cnico est en exceso, (pH observado es
cercano al de la solucin en el matraz)
En el punto de equivalencia
o El pH depende del pH de la sal en solucin
Sal neutral, pH = 7
Sal acdica, pH < 7
Sal bsica, pH > 7
Despus del punto de equivalencia
o La solucin de la bureta est en exceso dentro del matraz cnico (pH se
aproxima al pH de la solucin en la bureta)
Tro: Chemistry: A Molecular Approach, 2/e
31
Copyright 2011 Pearson Education, Inc.
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
Curva de titulacin de cido fuerte con NaOH (base fuerte)
La concentracin de
ambas soluciones es
igual con estequiometra
de 1:1, el volumen
consumido en el punto de
equivalencia es igual al
de la solucin original.
Antes pto. equivalencia
(exceso de cido
Despus del
pto.equivalencia
(base en exceso)
En Punto de Equivalencia
moles HCl = moles NaOH
pH = 7.00
Volumen de NaOH aadidos, (mL)
Tro: Chemistry: A Molecular Approach, 2/e
32
Copyright 2011 Pearson Education, Inc.
16
1/9/2015
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
Inicial: moles H+ = moles HCl
molesiniciales HCl = M1V1 = 0.0250 Lx0.100 mol/L = 2.50 x 103
Punto de equivalencia
HCl(ac) + NaOH(ac) NaCl(ac) + H2O(ac) neutralizacin
M 1V1 M 2V2
V2
Tro: Chemistry: A Molecular Approach, 2/e
M1V1
M2
33
Copyright 2011 Pearson Education, Inc.
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
HCl(ac) + NaOH(ac) NaCl(ac) + H2O(ac)
punto de equivalencia
moles NaOH aadidos = molesiniciales HCl*
0.00 moles HCl y 0.00 moles NaOH (todo reacciona)
Como NaCl es una sal neutral, el pH en el punto de
equivalencia es 7.00
Despus punto de equivalencia: pH NaOH en exceso
Tro: Chemistry: A Molecular Approach, 2/e
34
Copyright 2011 Pearson Education, Inc.
17
1/9/2015
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
pHinicial = log(0.100) = 1.00
Neutralizacin:
Inicial:
HCl ac NaOH ac NaCl ac H 2O
M HCl xVHCl
0.100 moles
L x 0.025 L
2.5 x103 moles
Antes pto. Equivalencia:
+ 5.00 mL NaOH 0.100 M
M NaOH xV NaOH
0.100 moles
L x 0 .005 L
rx:
final:
2.5 x10
5.0 x10 4
5.0 x10 4
2.0 x10 3
5.0 x10 4
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
35
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
neutralizacin : HCl ac NaOH ac NaCl ac H 2 O
inicial :
2 .5 x10 3
En pto. Equivalencia : + 25.00 mL NaOH 0.100 M
0 .100 moles
L x 0 .250 L
rx :
2 .5 x10 3
final
final
2.5 x10
2.5 x10 3
0
2.5 x10 3
agua
Tro: Chemistry: A Molecular Approach, 2/e
36
Copyright 2011 Pearson Education, Inc.
18
1/9/2015
Titulacin de 25 mL de 0.100 M HCl con 0.100 M NaOH
neutralizacin HCl ac NaOH ac NaCl ac H 2 O
inicial
2 .5 x10 3
Despus pto. equivalencia: + 30.00 mL NaOH 0.100 M
0.100 x 0.300
rx :
final
2.5 x10
final
3 .0 x10 3
Tro: Chemistry: A Molecular Approach, 2/e
2 .5 x10 3
5.0 x10 4
37
2 .5 x10 3
Copyright 2011 Pearson Education, Inc.
Aadir 0.100 M NaOH a 0.100 M HCl
+25.0 mL 0.100 M HCl
0.00250 mol HCl
pH = 1.00
Volumen de NaOH aadidos (mL)
Tro: Chemistry: A Molecular Approach, 2/e
38
+ 5.0 mL NaOH
0.00200 moles HCl
pH = 1.18
+10.0 mL NaOH
0.00150 mol HCl
pH = 1.37
+ 15.0 mL NaOH
0.00100 mol HCl
pH = 1.60
+ 20.0 mL NaOH
0.00050 mol HCl
pH = 1.95
+ 25.0 mL NaOH
Punto de equivalencia
pH = 7.00
+ 30.0 mL NaOH
0.00050 mol NaOH
pH = 11.96
+ 35.0 mL NaOH
0.00100 mol NaOH
pH = 12.22
+ 40.0 mL NaOH
0.00150 mol NaOH
pH = 12.36
+ 50.0 mL NaOH
0.00250 mol NaOH
pH = 12.52
Copyright 2011 Pearson Education, Inc.
19
1/9/2015
Aadir 0.100 M NaOH a 0.100 M HCl
+25.0 mL 0.100 M HCl
0.00250 mol HCl
pH = 1.00
Volumen de NaOH aadidos (mL)
Tro: Chemistry: A Molecular Approach, 2/e
+ 5.0 mL NaOH
0.00200 moles HCl
pH = 1.18
+10.0 mL NaOH
0.00150 mol HCl
pH = 1.37
+ 15.0 mL NaOH
0.00100 mol HCl
pH = 1.60
+ 20.0 mL NaOH
0.00050 mol HCl
pH = 1.95
+ 25.0 mL NaOH
Punto de equivalencia
pH = 7.00
+ 30.0 mL NaOH
0.00050 mol NaOH
pH = 11.96
+ 35.0 mL NaOH
0.00100 mol NaOH
pH = 12.22
+ 40.0 mL NaOH
0.00150 mol NaOH
pH = 12.36
+ 50.0 mL NaOH
0.00250 mol NaOH
pH = 12.52
Copyright 2011 Pearson Education, Inc.
39
Titulacin de 25 mL de 0.100 M HCHO2 con 0.100 M NaOH
HA ac H 2O ac A ac H 3 O
Ka = 1.8 x 104
H 3 O Ka HA0 1.8 x10 4 x0.100 4.24 x10 3
pHinicial = log(0.00424) = 2.37
Neutralizacin:
Inicial:
HA ac NaOH ac NaA ac H 2O
M HA xVHA
0
0
moles
Antes
pto.
Equivalencia:
0
.
100
x
0
.
025
L
L
2.5 x103 moles
+ 5.00 mL NaOH 0.100 M
0
.100 moles
L x 0 .005 L
rx:
2.5 x10
final:
5 .0 x10
5 .0 x10 4
2 .0 x10 3
5.0 x10
4
5 .0 x10 4
5 x 104
pH pKa log HA 4 log 2.0 x1030.030
0.030
pH 3.74
Tro: Chemistry: A Molecular Approach, 2/e
40
Copyright 2011 Pearson Education, Inc.
20
1/9/2015
Titulacin de 25 mL de 0.100 M HCHO con 0.100 M NaOH
neutralizacin : HA ac NaOH ac NaA ac H 2 O
inicial :
2 .5 x10 3
En pto. Equivalencia : + 25.00 mL NaOH 0.100 M
0 .100 moles
L x 0 .250 L
rx :
final
2.5 x10
2 .5 x10 3
2.5 x10 3
0
final
2.5 x10 3
A ac H 2O ac HA ac OH
OH Kb A
0
1.0 x10 14
1.8 x10 4
10
x 2.05.x050
1.67 x10 6
0 x10
H 3O 11..67
6.0 x10 9 pH 8.22
x10 6
14
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
41
Titulacin de 25 mL de 0.100 M HCHO con 0.100 M NaOH
neutralizacin HA ac NaOH ac NaA ac H 2 O
inicial
2 .5 x10 3
Despus pto. equivalencia: + 30.00 mL NaOH 0.100 M
0.100 x 0.300
rx :
final
2.5 x10
final
3 .0 x10 3
Tro: Chemistry: A Molecular Approach, 2/e
2 .5 x10 3
5.0 x10 4
42
2 .5 x10 3
Copyright 2011 Pearson Education, Inc.
21
1/9/2015
[HCHO2 ]0 = 0.00250 mol HCHO2
pH = 2.37
Adicin de NaOH a HCHO2
+5.0 mL NaOH
+30.0 mL NaOH
0.00200 mol HCHO2 0.00050 mol NaOH
pH = 3.14
pH = 11.96
Mitad del punto de equivalencia
(pH = pKa
+ 10.0 mL NaOH
0.00150 mol HCHO2
pH = 3.56
+ 35.0 mL NaOH
0.00100 mol NaOH
+ 12.5 mL NaOH
pH = 12.22
0.00125 mol HCHO2
pH = 3.74 = pKa
pto. Eq.
+ 40.0 mL NaOH
0.00150 mol NaOH
+ 15.0 mL NaOH
0.00100 mol HCHO2 pH = 12.36
pH = 3.92
+50.0 mL NaOH
+ 20.0 mL NaOH
0.00050 mol HCHO2 0.00250 mol NaOH
pH = 12.52
pH = 4.34
Volumen de
de NaOH
NaOH (mL)
(mL)
Volumen
Tro: Chemistry: A Molecular Approach, 2/e
43
+ 25.0 mL NaOH
Pto. Eq: 0.00250 mol CHO2
[CHO2]init = 0.0500 M
[OH]eq = 1.7 x 106
pH = 8.23
Copyright 2011 Pearson Education, Inc.
Titulacin de base fuerte con cido fuerte
Si el cido est en la
bureta y se
descarga a una
base en el matraz
cnico, la curva de
titulacin ser la
parecida a la figura.
Base fuerte y cido
fuertes
punto de equivalencia
(pH = 7)
Volumen de HCl aadidos, (mL)
Tro: Chemistry: A Molecular Approach, 2/e
44
Copyright 2011 Pearson Education, Inc.
22
1/9/2015
Equilibrio de Solubilidad
Los compuestos inicos se disuelven en agua.
Solubles = alta solubilidad (s)
Poco solubles = solubilidad intermedia (ps)
Insolubles = baja solubilidad (i)
Equilibrio de las sales, Keq
til para medir la solubilidad relativa en agua.
Para slido inico MnXm, la disociacin es:
MnXm(s) nMm+(ac) + mXn(ac)
El producto de solubilidad es:
Ksp = [Mm+]n[Xn]m
Ejemplo: PbCl2 : PbCl2(s) Pb2+(ac) + 2 Cl(ac)
Ksp = [Pb2+][Cl]2
Tro: Chemistry: A Molecular Approach, 2/e
45
Copyright 2011 Pearson Education, Inc.
Tro: Chemistry: A Molecular Approach, 2/e
46
Copyright 2011 Pearson Education, Inc.
23
1/9/2015
Solubilidad Molar
Solubilidad - es la cantidad de soluto que se
disuelve en una cantidad dada de solucin a una
T dada.
La solubilidad molar es el # de moles de soluto
que se disuelven en 1 L de solucin
Es la M del soluto disuelto en una solucin saturada.
Para la reaccin general MnXm(s) nMm+(ac) + mXn(ac)
Solubilidad molar, sM
Tro: Chemistry: A Molecular Approach, 2/e
Copyright 2011 Pearson Education, Inc.
47
Ejemplo 16.8: Calcule la solubilidad molar de
PbCl2 en agua pura a 25 C, Kps = 1.17 x 10-5
PbCl2 s Pb 2 ac 2 Cl ac
Inicial
Cambio
Equilibrio
[Pb2+]
[Cl]
+S
+2S
2S
2x
2s
K ps Pb 2 Cl s 2 s 4 s 3
Tro: Chemistry: A Molecular Approach, 2/e
48
Copyright 2011 Pearson Education, Inc.
24
1/9/2015
Prctica Determine el Kps de PbBr2 si la solubilidad molar en
agua a 25 C es 1.05 x 102 M
P b B r2 s P b 2 a c 2 B r ac
x
2x
2s
K p s P b 2 B r s 2 s 4 s 3
2
K ps 4 s 3 4 1 .05 x10 2 4 .63 x10 6
3
Otra alternativa :
K ps s 2 s 1 .05 x10 2 2 1 .05 x10 2
2
K ps 1 .05 x10 2 2 .10 x10 2 4 .63 x10 6
2
Tro: Chemistry: A Molecular Approach, 2/e
49
Copyright 2011 Pearson Education, Inc.
Ksp y Solubilidad Relativa
Tomar en consideracin la estequiometra
El efecto de in comn sobre la solubilidad,
(Le Chatelier)
Ejemplo
Aadir NaCl a PbCl2 disminuye la solubilidad de PbCl2
PbCl2(s) Pb2+(ac) + 2 Cl(ac)
Aadir Cl desplaza el equilibrio hacia la izquierda
Tro: Chemistry: A Molecular Approach, 2/e
50
Copyright 2011 Pearson Education, Inc.
25
1/9/2015
Ejemplo 16.10: Calcule la solubilidad molar de CaF2 en 0.100 M
NaF a 25 C
CaF2 s Ca 2 ac 2 F ac
[Ca2+]
[F]
0.100
Inicial
cambio
+S
+2S
equilibrio
0.100 + 2S
ps
C a
0 .1
0 .1 2 s
s 0 . 1
2s
s 0 . 1
2
1 . 4 6 x 1 0 1 0 s 0 . 1
K
ps
1 .4 6 x1 0
0 . 1
10
s 1 .4 6 x1 0
Tro: Chemistry: A Molecular Approach, 2/e
51
Copyright 2011 Pearson Education, Inc.
Prctica Determine la concentracin de los iones
de Ag+ en agua de mar donde [Cl] = 0.55 M
AgCl(s) Ag+(ac) + Cl(ac)
s
Ksp =
Ksp = [Ag+][Cl]
0.55 + s
[Ag+][Cl]
[Ag+]
[Cl]
Inicial
0.55
Cambio
+s
+s
equilibrio
0.55 + s
Ksp = (s)(0.55 + s)
Ksp = (s)(0.55)
Tro: Chemistry: A Molecular Approach, 2/e
52
Copyright 2011 Pearson Education, Inc.
26
1/9/2015
El Efecto de pH en la Solubilidad
Para hidrxidos inicos insolubles,
M(OH)n(s) Mn+(ac) + nOH(ac)
A mayor pH,
[OH ] aumenta,
solubilidad menor
M(OH)n(s) Mn+(ac) + nOH(ac)
OH
A menor pH,
M(OH)n(s)
[OH ] disminuye,
Mn+(ac)
Tro: Chemistry: A Molecular Approach, 2/e
solubilidad mayor
nOH(ac)
OH
53
Copyright 2011 Pearson Education, Inc.
El Efecto de pH en la Solubilidad
Para slidos inicos insolubles con aniones de
cidos dbiles, a menor pH, mayor la solubilidad
M2(CO3)n(s) 2 Mn+(ac) + nCO32(ac)
H3O+
H3O+(ac) + CO32 (ac) HCO3 (ac) + H2O(l)
Tro: Chemistry: A Molecular Approach, 2/e
54
Copyright 2011 Pearson Education, Inc.
27
1/9/2015
Precipitacin
Ocurre cuando la concentracin de los iones excede
la solubilidad del compuesto inico.
Comparar Q con Kps, se determina si hay precipitacin
Q = Kps, solucin saturada,
Q < Kps, solucin insaturada,
Q > Kps, solucin por encima de saturacin,
no-precipita
no-precipita
precipita
Algunas soluciones con Q > Ksp no precipitan a menos
que se perturben solucin sobresaturada
Tro: Chemistry: A Molecular Approach, 2/e
Ocure precipitacin
si Q > Ksp
Tro: Chemistry: A Molecular Approach, 2/e
55
Copyright 2011 Pearson Education, Inc.
Solucin sobresaturada se precipita
si se aade un cristal semilla
56
Copyright 2011 Pearson Education, Inc.
28
1/9/2015
Ejemplo 16.12: Se formar precipitado cuando se mezclan
Pb(NO3)2(ac) con NaBr(ac) si la concentracin al mezclar es
0.0150 M y 0.0350 M respectivamente?
Pb(NO3)2(ac) + 2 NaBr(ac) PbBr2(s) + 2 NaNO3(ac)
NaBr = 0.0350 M
Na+ = 0.0350 M,
Br = 0.0350 M
Pb(NO3)2 = 0.0150 M
Pb2+ = 0.0150 M,
NO3 = 2(0.0150 M)
Ksp de PbBr2 = 4.67 x 106
PbBr2(s) Pb2+(ac) + 2 Br(ac)
Q < Ksp, no hay precipitacin
Tro: Chemistry: A Molecular Approach, 2/e
57
Copyright 2011 Pearson Education, Inc.
Prctica Se formar precipitado cuando Ca(NO3)2(ac) se
mezcla con NaOH(ac) si las concentraciones despus de
mezclar son iguales a 0.0175 M para ambas especies?
Ca(NO3)2(ac) + 2 NaOH(ac) Ca(OH)2(s) + 2 NaNO3(ac)
NaOH = 0.0175 M
Ca(NO3)2 = 0.0175 M
Na+ = 0.0175 M,
Ca2+ = 0.0175 M,
OH = 0.0175 M
NO3 = 2(0.0175 M)
Ksp de Ca(OH)2 = 4.68 x 106
Ca(OH)2(s) Ca2+(ac) + 2 OH(ac)
Q > Ksp, se precipita
Tro: Chemistry: A Molecular Approach, 2/e
58
Copyright 2011 Pearson Education, Inc.
29
Anda mungkin juga menyukai
- ContenidoDokumen15 halamanContenidoEdwinBelum ada peringkat
- Apuntes-Mecanica de Fluidos 2011Dokumen101 halamanApuntes-Mecanica de Fluidos 2011Julio Miguel Fernández PradoBelum ada peringkat
- Hoja de Trabajo 1Dokumen2 halamanHoja de Trabajo 1EdwinBelum ada peringkat
- Gestión Integral de Riesgo de Desastres GuatemalaDokumen5 halamanGestión Integral de Riesgo de Desastres GuatemalaEdwinBelum ada peringkat
- Centroid EsDokumen2 halamanCentroid EsLupita GomezBelum ada peringkat
- EcologiaDokumen2 halamanEcologiaEdwinBelum ada peringkat
- Ensayo Topo2Dokumen5 halamanEnsayo Topo2EdwinBelum ada peringkat
- Discucion HidrostaticaDokumen4 halamanDiscucion HidrostaticaEdwinBelum ada peringkat
- Determinacion de Fluidos No NiutioneanosDokumen10 halamanDeterminacion de Fluidos No NiutioneanosJRaugusto0409Belum ada peringkat
- Tipos de Nivelación PDFDokumen15 halamanTipos de Nivelación PDFEdwinBelum ada peringkat
- Tercera Unidad Primera ParteDokumen37 halamanTercera Unidad Primera ParteEdwinBelum ada peringkat
- FVC-Fernandez GabrielDokumen4 halamanFVC-Fernandez GabrielEdwinBelum ada peringkat
- La Contaminación Ambiental y El Cambio GlobalDokumen58 halamanLa Contaminación Ambiental y El Cambio GlobalEdwinBelum ada peringkat
- Cuadro Ejemplo para El Método de Secciones TransversalesDokumen1 halamanCuadro Ejemplo para El Método de Secciones TransversalesEdwinBelum ada peringkat
- Mapa Conceptual 1er ParcialDokumen1 halamanMapa Conceptual 1er ParcialEdwinBelum ada peringkat
- ViernesDokumen1 halamanViernesEdwinBelum ada peringkat
- Ilovepdf Merged MergedDokumen119 halamanIlovepdf Merged MergedEdwinBelum ada peringkat
- CaratulaDokumen1 halamanCaratulaEdwinBelum ada peringkat
- 10 Problemas Equilibrio de Particulas en El EspacioDokumen4 halaman10 Problemas Equilibrio de Particulas en El EspaciopedorBelum ada peringkat
- Mecanica Vectorial para Ingenieros Estat-67-71Dokumen5 halamanMecanica Vectorial para Ingenieros Estat-67-71EdwinBelum ada peringkat
- Estadisticas Ejecicio SDokumen19 halamanEstadisticas Ejecicio SEdwinBelum ada peringkat
- Fuerzas en estructurasDokumen11 halamanFuerzas en estructurasEdwinBelum ada peringkat
- Viscosidad 3Dokumen7 halamanViscosidad 3EdwinBelum ada peringkat
- 9 Problemas Componentes Rectangulares en El EspacioDokumen4 halaman9 Problemas Componentes Rectangulares en El Espaciopedor100% (2)
- ViscosidadDokumen11 halamanViscosidadEdwinBelum ada peringkat
- 22 Agosto Ejercicio de InventarioDokumen3 halaman22 Agosto Ejercicio de InventarioEdwinBelum ada peringkat
- Composicion y Descomposicion de Fuerzas 2D EJERC1Dokumen3 halamanComposicion y Descomposicion de Fuerzas 2D EJERC1YOHAN DANIEL SANDOVAL BARRERABelum ada peringkat
- Conclusion y Recomendacion de ViscodidadDokumen4 halamanConclusion y Recomendacion de ViscodidadEdwinBelum ada peringkat
- Informe de ViscodiadDokumen9 halamanInforme de ViscodiadEdwinBelum ada peringkat
- 22 Agosto Ejercicios de DepreciaciónDokumen1 halaman22 Agosto Ejercicios de DepreciaciónEdwinBelum ada peringkat
- Laboratorio PerfumeDokumen2 halamanLaboratorio PerfumeRolando Alvarado VillamilBelum ada peringkat
- Influencia de La Deshidratación Osmótica y de La Adición de Cloruro de Calcio en La Conservación de Kiwis Mínimamente ProcesadosDokumen6 halamanInfluencia de La Deshidratación Osmótica y de La Adición de Cloruro de Calcio en La Conservación de Kiwis Mínimamente ProcesadosNey RuchBelum ada peringkat
- Informe de Reacciones de Oxidacion y ReduccionDokumen21 halamanInforme de Reacciones de Oxidacion y ReduccionIvan Daniel Condori Mamani0% (1)
- Diseño de Bomba AxialDokumen14 halamanDiseño de Bomba AxialJhonatan Velasquez Castellanos100% (1)
- Aspirina descubrimiento historiaDokumen5 halamanAspirina descubrimiento historiaemily darqueaBelum ada peringkat
- Guía 13 Grupos Funcionales y Clasif de Com Puestos Orgánicos Parte 2Dokumen3 halamanGuía 13 Grupos Funcionales y Clasif de Com Puestos Orgánicos Parte 2Liliana HernándezBelum ada peringkat
- Propiedades y aplicaciones de los plásticos más comunesDokumen20 halamanPropiedades y aplicaciones de los plásticos más comunesCarlomagnoBautistoOrtizBelum ada peringkat
- Practica No. 8 Reacciones QuímicasDokumen4 halamanPractica No. 8 Reacciones QuímicasAngel ZamoraBelum ada peringkat
- Informe Elementos de TransiciónDokumen16 halamanInforme Elementos de TransiciónDANIELA VANESSA HERMOZA SAAZBelum ada peringkat
- Extractiva I.tema 1 2019 IDokumen11 halamanExtractiva I.tema 1 2019 ICarlos Jose BedonBelum ada peringkat
- Acidos Carboxilicos. InfDokumen37 halamanAcidos Carboxilicos. InfIvanov100% (1)
- Organica2 Pre1Dokumen25 halamanOrganica2 Pre1Alejandro ArangoBelum ada peringkat
- Taller de Repaso Fundamentos Primer CorteDokumen5 halamanTaller de Repaso Fundamentos Primer Corteandres silvestreBelum ada peringkat
- Las Cremas y Los EmulsionantesDokumen50 halamanLas Cremas y Los EmulsionantesCosta Pablo100% (1)
- Comercializacion de Minerales y MetalesDokumen52 halamanComercializacion de Minerales y MetalesLuis Macedo80% (5)
- Preparación de BenzocaínaDokumen6 halamanPreparación de BenzocaínaCamilo JcBelum ada peringkat
- GasesDokumen2 halamanGasesAbi C. AlanyaBelum ada peringkat
- Informe de NitrogenoidesDokumen9 halamanInforme de NitrogenoidesDatois TorresBelum ada peringkat
- Formulacion PDFDokumen29 halamanFormulacion PDFAnaJimenezBelum ada peringkat
- Cuestionario Del PetroleoDokumen7 halamanCuestionario Del Petroleojohn A. yupanqui tomasBelum ada peringkat
- OcaDokumen11 halamanOcacarlos robertoBelum ada peringkat
- Preparación de soluciones valoradas y determinación de concentracionesDokumen19 halamanPreparación de soluciones valoradas y determinación de concentracionesYonar Shmit Gallo QuispeBelum ada peringkat
- Equilibrio QuimicoDokumen3 halamanEquilibrio QuimicoDGBBelum ada peringkat
- Reporte 3 Accion de La AmilasaDokumen7 halamanReporte 3 Accion de La Amilasajesus aaron rios lovioBelum ada peringkat
- 01 Metodo de Analisis de Cobre en Concentrado de Cu X Volumetria 2019Dokumen5 halaman01 Metodo de Analisis de Cobre en Concentrado de Cu X Volumetria 2019Anonymous z8jNYXzBelum ada peringkat
- Biología Preguntas Ebau Tema 3 LípidosDokumen8 halamanBiología Preguntas Ebau Tema 3 LípidosAlejandro Rodríguez HernándezBelum ada peringkat
- Quimica Ii - Pre Informe Nro 3 Fiis UniDokumen6 halamanQuimica Ii - Pre Informe Nro 3 Fiis UniRodrigo Sagastegui Messa0% (1)
- Bases11 10Dokumen2 halamanBases11 10Laura Liliana CaglieroBelum ada peringkat
- Cartilla - Nomenclatura de Compuestos OrganicosDokumen73 halamanCartilla - Nomenclatura de Compuestos OrganicosMicaela ChocobarBelum ada peringkat
- Tecnicas para AcetolisisDokumen3 halamanTecnicas para AcetolisisEsaú MayBelum ada peringkat