298 648 2 PB
Diunggah oleh
Renan BaiaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
298 648 2 PB
Diunggah oleh
Renan BaiaHak Cipta:
Format Tersedia
ABSORO EM COLUNA DE RECHEIO
Absoro em coluna de recheio
1. Objetivo
O objetivo da presente prtica ser a familiarizao com um processo comum na
indstria qumica como a lavagem de correntes gasosas contaminadas com um
poluente de natureza cida (ou bsica) com uma soluo bsica (ou cida) mediante um
processo de absoro reativa. No caso, ser estudado o processo de absoro de CO2 em
uma soluo de hidrxido de sdio.
2. Introduo terica
A absoro uma operao unitria consistente em que um ou vrios solutos se
absorvem da fase gasosa e passam lquida. Este processo implica uma difuso
molecular turbulenta ou uma transferncia de massa do soluto atravs do gs B (gs
portador) at um lquido C. O gs ser geralmente insolvel no lquido C, da mesma
forma que o lquido no se volatilizar e passar ao gs B. Este processo pode ser
realizado mediante o contato contnuo ou intermitente entre fases. No sistema
empregado, o contato ser contnuo e ocorrer ao longo da torre de absoro. As
colunas de absoro tm geralmente forma cilndrica, entrando o gs pela parte inferior,
e o lquido pela parte superior atravs de um sistema distribuidor. O gs depurado sai
pela parte superior da torre, enquanto o lquido enriquecido sai pela parte inferior. Na
Figura 1 apresentado um esquema bsico deste tipo de sistema.
Gs limpo
Lquido
Diferentes tipos
de recheios
Gs + soluto
Lquido + soluto
Figura 1. Esquema de um processo de absoro em torre empacotada
O processo de transferncia de matria pode ser melhorado se associado a um
processo reativo. Desta forma, a remoo constante do soluto da soluo torna o
2
Absoro em coluna de recheio
processo muito mais eficiente. Para o desenho deste tipo de sistema sero aplicados os
princpios bsicos de desenho de colunas empacotadas com a adio de um processo
reativo. Suponha-se o processo reativo da equao 1.
A (gl) + bB (l) produto
-rA = kCACB
(1)
No caso de se ter um processo reativo envolvido ao processo de absoro, o perfil de
concentraes que aparecer na coluna ter uma forma similar mostrada na Figura 2.
Interface
Corpo
principal
do lquido
PA
CB
PAi
CAi
CA
CBi
Filme
gasoso
Filme
lquido
Figura 2. Esquema de um processo de absoro reativa
Conforme a figura, devero ser considerados quatro processos: o que acontece
no filme gasoso, no filme lquido, na interface lquido-gs e o processo reativo.
Considerando o caso genrico que envolve todas as resistncias, a expresso que
determina o transporte de A (soluto) desde o seio do gs at a soluo vir dada pela
equao 2.
rA
1
pA
HA
HA
1
k Ag a k Al aE kC B f l
(2)
Absoro em coluna de recheio
O parmetro kAga o coeficiente de transporte de massa volumtrico na fase gs,
kAla o correspondente na fase lquida, HA a constante de Henry, E um fator de
aumento de absoro no filme lquido pelo efeito da reao, k a constante de
velocidade, CB a concentrao do reagente B presente exclusivamente no lquido e fl
a frao ocupada pelo lquido no espao livre da coluna. O primeiro termo do
denominador se corresponde com a resistncia imposta pelo filme gasoso, o segundo
termo se corresponde com a resistncia imposta pela fase lquida e finalmente o ltimo
termo se corresponde com a resistncia imposta pelo corpo do lquido onde acontecer a
reao qumica.
No caso de operar-se com um sistema onde o componente A se encontra puro, a
resistncia da fase gasosa ser desprezvel, resultando na equao 3.
rA
1
HA
HA
k Al aE kC B f l
pA
(3)
O parmetro de desenho deste tipo de sistemas a altura do leito de recheio.
Para seu clculo ser necessrio considerar um elemento diferencial de altura para o
reator dz, onde acontece o processo de transferncia de soluto considerado. Definindo
Fg como ao fluxo de gs portador e Fl ao fluxo de lquido suporte, YA aos mols de
soluto/mols de portador e XB aos mols de reagente B/mols de inerte no lquido, tm-se
as seguintes equaes para o processo reativo.
A perdido 1 B perdido consumo de A
pelo gas b pelo lquido pela reao
1
Fg dYA Fl dX B rASdz
b
(4)
(5)
Pela integrao da equao anterior ser possvel estimar a altura necessria da
torre para um determinado processo de absoro.
z
Fg
YA2
dYA
Fl
X B1
dX B
S Y rA Sb X rA
A1
B2
(6)
Absoro em coluna de recheio
No caso particular do experimento, dado que o componente A (CO2) se encontra
puro e o componente B (NaOH) se encontra diludo, o balano de massa da equao 5
pode ser simplificado resultando na equao 7, onde CT a concentrao total.
FA+dFA
F
dFA l dCB rA aSdz
bCT
Fl CB+dCB
(7)
FA
Fl CB
Aplicando o balano coluna, obtm-se a seguinte equao que permitir saber
qual a quantidade de CO2 absorvida (seo 1 a superior da coluna e seo 2 como
superior; FA = FA2 FA1).
FA2 FA1
Fl
C B1 C B2
bCT
(8)
Com isto ser possvel saber ao longo da coluna a quantidade de CO2 que foi
absorvida. O valor de CB importante, pois influencia na velocidade de absoro de A
(equao 3).
Finalmente, para sistemas diludos, a altura da coluna poder ser calculada pela
equao 9.
Fl
SbCT
C B1
dCB
C r
A
B2
(9)
Absoro em coluna de recheio
A resoluo do presente exerccio vai requerer a integrao numrica da equao
9, tal como mostrado na Figura 3.
-1/(-rA)
rea = zSbCT/Fl
CB
Figura 3. Resoluo grfica para o clculo da altura da torre de absoro
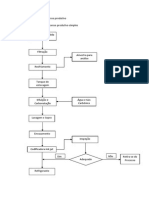
3. Instalao experimental
A instalao experimental consiste em uma coluna de recheio de anis Rasching
de comprimento 0,65 metros e 0,05 metros de dimetro. Na Figura 4 apresentado um
esquema do dispositivo experimental.
CORRENTE DE
GS TRATADO
Distribuidor
na entrada do
lquido
Bomba de
impulso
peristltica
Reservatrio de
lquido (NaOH 1
mol/L)
Fluxo
descendente
de lquido
Reguladores de
presso
Medidor da
condutividade
Fluxo
ascendente
de gs
Rotmetro de
regulao da
vazo de gs
Cilindro de CO2
Entrada do
gs
2,22 mS
Sonda de
condutividade na
sada
CORRENTE DE
SADA LQUIDA
Figura 4. Instalao experimental de absoro
Absoro em coluna de recheio
O gs a tratar, CO2 no caso, se introduz pela parte inferior da coluna com o fluxo
controlado com ajuda de um rotmetro e uma vlvula de agulha de regulao fina. O gs
ascender pela coluna forado pelo sifo de lquido na parte inferior da coluna que
impede a sada do gs. Na parte superior acessar a corrente lquida de NaOH com
ajuda de uma bomba peristltica. Ambas as correntes entraro em contato na coluna em
contracorrente com objeto de tornar mais eficiente a transferncia de massa. Portanto, o
processo que ocorre na coluna definido pela equao 10.
CO2 (gl) + 2 NaOH Na2CO3 + H2O
(10)
Na sada pelo fundo existe uma adaptao para acoplamento de uma sonda de
condutividade, de modo a medir a variao da mesma at atingir um valor estacionrio.
A transferncia de matria ocorre no interior da coluna de absoro onde as duas
correntes entraro em contato. Uma bureta de 10 mL ser utilizada no experimento para
titular a soluo de NaOH efluente com HCl com fenolftalena como indicador. Para
evitar as interferncias dos carbonatos, ser necessria a adio de BaCl2, fazendo com
que os carbonatos precipitem na forma de BaCO3.
4. Materiais
Para a realizao da prtica ser necessrio:
a) Instalao experimental j descrita.
b) Cilindro de dixido de carbono com reguladores de presso (consultar o professor).
c) Hidrxido de sdio (4 litros de soluo 0,1 mol/L).
d) Sonda de condutividade com o correspondente condutivmetro.
e) Bomba peristltica
f) Regulador de vazo do gs com vlvula de agulha includa.
g) Reservatrio de 2 litros de hidrxido de sdio.
h) Cloreto de brio.
i) cido clordrico (1 litro de soluo 0,1 mol/L).
7
Absoro em coluna de recheio
j) Bureta de 10 mL.
5. Procedimento operacional
A seguinte sequncia operacional ser realizada ao longo da prtica:
1. Preparar as solues necessrias na prtica (4 litros de soluo 0,1 mol/L de
NaOH e 1 litro de 0,1 mol/L de HCl).
2. Situar a soluo de NaOH na linha de alimento da bomba.
3. Ligar a bomba na posio correspondente a 40 mL/min e esperar at observar a
sada de lquido pela parte inferior da coluna.
4. Neste momento, anotar a condutividade e coletar uma amostra de 10 mL em em
erlenmeyer para titulao com HCl (lembrar de adicionar uma ponta de esptula
de BaCl2). Titular com a bureta de 10 mL.
5. Ligar o fluxo de gs em uma vazo de 100 mL/min. Checar a sada de gs pela
parte superior da coluna.
6. Monitorar a condutividade cada 2 minutos at chegar a um valor constante.
7. Neste momento, anotar o novo valor e coletar uma amostra de 10 mL para
titulao com HCl (lembrar de adicionar 0,5 g de BaCl2). Titular com a bureta de
10 mL.
8. Repetir o processo com as outras vazes volumtricas: 30, 20 e 10 mL/min nesta
sequncia.
9. Uma vez finalizado o experimento, coletadas e tituladas todas as amostras, a
etapa final ser a lavagem da coluna. Para isto, substituir a soluo de NaOH 0,1
mol/L no alimento da bomba por gua destilada, monitorando a condutividade
at obter um valor prximo ao da gua destilada.
10. Deixar o sistema limpo para o novo grupo de estudantes do dia seguinte.
6. Discusso de resultados
Responder s seguintes questes:
Absoro em coluna de recheio
Representar graficamente a evoluo da condutividade com o tempo para as quatro
vazes utilizadas. Justificar a forma da curva.
Preencher a seguinte tabela
Vazo volumtrica lquido = 10 mL/min
Tempo
[OH-] = CNaOH
0 = ...
[OH-]0 = CNaOH,1 = ...
= ...
[OH-] = CNaOH,2 = ...
Vazo volumtrica lquido = 20 mL/min
Tempo
[OH-] = CNaOH
0 = ...
[OH-]0 = CNaOH,1 = ...
= ...
[OH-] = CNaOH,2 = ...
Vazo volumtrica lquido = 30 mL/min
Tempo
[OH-] = CNaOH
0 = ...
[OH-]0 = CNaOH,1 = ...
= ...
[OH-] = CNaOH,2 = ...
Vazo volumtrica lquido = 40 mL/min
Tempo
[OH-] = CNaOH
0 = ...
[OH-]0 = CNaOH,1 = ...
= ...
[OH-] = CNaOH,2 = ...
Calcular a quantidade de CO2 absorvida aplicado equao 8 (b = 2; CT = 55,6
mol/L) na operao estacionria.
Estimar o valor de kla do sistema de recheio. Para isto, deve ser integrada a equao
9. A princpio, seria necessrio usar a equao 3. Entretanto, ser usada a equao
simplificada 11, supondo que a reao qumica de neutralizao instantnea.
Absoro em coluna de recheio
rCO2 k CO2,l a
PCO 2 H CO 2 D NaOH C NaOH
1
H CO 2
bDCO 2 PCO 2
(11)
Dados: H(CO2) = 25000 Pam3/mol; D(CO2) = 1,810-9 m2/s; D(NaOH) = 3,0610-9
m2/s; P(CO2) = 101300 Pa; concentrao em mol/m3
A altura da torre pode ser estimada pela equao 12.
dC NaOH
Fl H CO 2
1 C NaOH,0
.
bSCT PCO 2 k l a C NaOH, H CO 2 D NaOH C NaOH
1
bD
P
CO
CO
2
2
(12)
A integrao da equao anterior d lugar equao 13, a partir do qual o nico
parmetro desconhecido (kCO2,la).
D CO2 2D CO2 H CO2 D NaOH C NaOH,1
Fl
1
ln
SC T k CO2,l a D NaOH 2D CO2 H CO2 D NaOH C NaOH,2
(13)
Para torres de absoro, o coeficiente de transferncia de massa na fase lquida (kl)
pode ser estimado a partir de uma correlao emprica de dependncia potencial
entre o prprio coeficiente e a velocidade mssica do lquido (GL, Kg/(m2s)),
assumindo que as propriedades do lquido permanecem constantes com
independncia da vazo volumtrica. A equao que define esta correlao a 14,
onde c e c0 so parmetros empricos do ajuste dos dados.
k CO2,l c 0 G cL
(14)
O clculo de GL feito dividindo a vazo volumtrica pela rea transversal da
coluna (S) e corrigindo pela densidade do lquido (L), que ser considerada igual
10
Absoro em coluna de recheio
da gua (1 kg/m3), tal como mostrado na Equao 14. Comparar os valores obtidos
com aqueles disponveis na literatura: MCCABE W.L.; SMITH, J.C.; HARRIOT, P.
Unit Operation of Chemical Engineering, Ed. McGraw-Hill Int., 7th edition, New York,
USA, 2005, pp. 600-601. Que concluses podem ser tiradas dos valores obtidos?
7. Leituras recomendadas
LEVENSPIEL, O. Engenharia das reaes qumicas. So Paulo: Edgard Blcher,
2000.
McCABE W. L.; SMITH, J. C.; HARRIOT, P. Unit operation of Chemical Engineering,
7th edition, New York, USA: McGraw-Hill Int., 2005.
GEANKOPLIS, C. J. Procesos de transporte y operaciones unitarias. Mxico
Cecsa, 1998.
11
Anda mungkin juga menyukai
- Anexo Vi - Declaração de Vínculo EmpregatícioDokumen1 halamanAnexo Vi - Declaração de Vínculo EmpregatícioRenan BaiaBelum ada peringkat
- Anexo Vii - Declaração de Disponibilidade de TempoDokumen1 halamanAnexo Vii - Declaração de Disponibilidade de TempoRenan BaiaBelum ada peringkat
- Estadofins e PrincípiosDokumen7 halamanEstadofins e PrincípiosRenan BaiaBelum ada peringkat
- Carta Da TerraDokumen7 halamanCarta Da TerraRenan BaiaBelum ada peringkat
- 169 - 435 - Conteúdo Programático - Anexo II - EstagiáriosDokumen4 halaman169 - 435 - Conteúdo Programático - Anexo II - EstagiáriosRenan BaiaBelum ada peringkat
- Cobeqic2015 Template Trabalho-Completo 0Dokumen4 halamanCobeqic2015 Template Trabalho-Completo 0wmpoubelBelum ada peringkat
- Fábrica de RefrigerantesDokumen3 halamanFábrica de RefrigerantesRenan BaiaBelum ada peringkat
- 1833330388Dokumen11 halaman1833330388Renan BaiaBelum ada peringkat
- Administração Pública e Governo - Diferenças Básicas. - Artigos - Dinheiro - AdministradoresDokumen3 halamanAdministração Pública e Governo - Diferenças Básicas. - Artigos - Dinheiro - AdministradoresRenan BaiaBelum ada peringkat
- Definição de NegocioDokumen35 halamanDefinição de NegocioRenan BaiaBelum ada peringkat
- 1 Investimentos Iniciais AtualDokumen15 halaman1 Investimentos Iniciais AtualRenan BaiaBelum ada peringkat
- Turn KeyDokumen5 halamanTurn KeyRenan BaiaBelum ada peringkat
- NadaDokumen1 halamanNadaRenan BaiaBelum ada peringkat
- 169 449 C Users Ana Documents ELETRONORTE 2015 Edital de Retificação Estagiário Eletrobras Eletronorte 2014 2º SemestreDokumen1 halaman169 449 C Users Ana Documents ELETRONORTE 2015 Edital de Retificação Estagiário Eletrobras Eletronorte 2014 2º SemestreRenan BaiaBelum ada peringkat
- Volume MolarDokumen1 halamanVolume MolarRenan BaiaBelum ada peringkat
- Modelo Elaboracao MemorialDokumen6 halamanModelo Elaboracao MemorialTerry RobbinsBelum ada peringkat
- 3Dokumen12 halaman3Renan BaiaBelum ada peringkat
- PetrobrásDokumen2 halamanPetrobrásRenan BaiaBelum ada peringkat
- Qual o Plano de Fogo Ideal para Uma Demolição em Rocha Com 3,0m de Profundidade e 0,80m de LarguraDokumen2 halamanQual o Plano de Fogo Ideal para Uma Demolição em Rocha Com 3,0m de Profundidade e 0,80m de LarguraRenan BaiaBelum ada peringkat
- Absorção e stripping de gases: transferência de massa líquido-gásDokumen3 halamanAbsorção e stripping de gases: transferência de massa líquido-gásTatá Reali100% (1)
- Leito Poroso - FiltraçãoDokumen44 halamanLeito Poroso - FiltraçãoRodolfo RomaBelum ada peringkat
- Riscos na InternetDokumen4 halamanRiscos na InternetRenan BaiaBelum ada peringkat
- Re at orDokumen59 halamanRe at orlualvez0% (1)
- Fen - Meno de Transportes Aula1Dokumen11 halamanFen - Meno de Transportes Aula1Renan BaiaBelum ada peringkat
- 10 Dicas para o Seu Marketing PessoalDokumen2 halaman10 Dicas para o Seu Marketing PessoalRenan BaiaBelum ada peringkat
- Resumo 3Dokumen6 halamanResumo 3Renan BaiaBelum ada peringkat
- Cap 4Dokumen3 halamanCap 4Renan BaiaBelum ada peringkat
- Renan BaiaDokumen4 halamanRenan BaiaRenan BaiaBelum ada peringkat
- Cola para o EndersonDokumen2 halamanCola para o EndersonRenan BaiaBelum ada peringkat
- Análise de acidez e alcalinidade em amostras de águaDokumen3 halamanAnálise de acidez e alcalinidade em amostras de águaThais CarolinaBelum ada peringkat
- Aula 4. Mecanismos de Fixação de CO2 em PlantasDokumen7 halamanAula 4. Mecanismos de Fixação de CO2 em PlantasFrancisco Rosario JaimeBelum ada peringkat
- Conteúdo 3 - Exercícios 3 - 1 - Física IIDokumen10 halamanConteúdo 3 - Exercícios 3 - 1 - Física IIAldo Junior Martins CoelhoBelum ada peringkat
- Ligações Químicas e HidrocarbonetosDokumen4 halamanLigações Químicas e HidrocarbonetosFatinha CostaBelum ada peringkat
- Garras eficientes para manuseio de bobinasDokumen6 halamanGarras eficientes para manuseio de bobinasandersonmipa12Belum ada peringkat
- Dissertação de Mestrado Artigo Sobre AmendoimDokumen79 halamanDissertação de Mestrado Artigo Sobre AmendoimGilvan JúniorBelum ada peringkat
- Diretrizes para armazenamento e manuseio seguro de GLPDokumen49 halamanDiretrizes para armazenamento e manuseio seguro de GLPFelipe WagnerBelum ada peringkat
- Enade-2008 2Dokumen31 halamanEnade-2008 2Genilson E Neliane SilvaBelum ada peringkat
- Relatório 04-Efeito ZeemanDokumen4 halamanRelatório 04-Efeito ZeemanJoão Victor Azevedo GonçalvesBelum ada peringkat
- Resumo Sistemas Termicos Prova 2Dokumen4 halamanResumo Sistemas Termicos Prova 2Rúbia Cristina FavrettoBelum ada peringkat
- Classificação Nice listaDokumen80 halamanClassificação Nice listaJuliana LuzBelum ada peringkat
- Análise de Prova Parcial de BromatologiaDokumen8 halamanAnálise de Prova Parcial de BromatologiaFranBelum ada peringkat
- Aços planos e derivados para indústria e construçãoDokumen16 halamanAços planos e derivados para indústria e construçãoEricOsowskiBelum ada peringkat
- Keystone RMI DUBEX Válvula BorboletaDokumen8 halamanKeystone RMI DUBEX Válvula BorboletaMARCIOBelum ada peringkat
- Afdg2 Detector de Gás GLP GN Carvão PDFDokumen12 halamanAfdg2 Detector de Gás GLP GN Carvão PDFmauriciosampaio84Belum ada peringkat
- Equilíbrio térmico e densidadeDokumen2 halamanEquilíbrio térmico e densidadeKariliany MacedoBelum ada peringkat
- Relatorio Dispensa 93019006900012024Dokumen270 halamanRelatorio Dispensa 93019006900012024José PeresBelum ada peringkat
- Fispq Pluron 147 Ag (246) - A-C-I PDFDokumen10 halamanFispq Pluron 147 Ag (246) - A-C-I PDFRhafaelEvangelistaBelum ada peringkat
- Química - Pré-Vestibular Impacto - Cálculo Químico GrandezasDokumen2 halamanQuímica - Pré-Vestibular Impacto - Cálculo Químico GrandezasQuímica Qui100% (1)
- Tipos de Eletrização: Aula 02Dokumen14 halamanTipos de Eletrização: Aula 02Paulo HenriqueBelum ada peringkat
- Modelo Relatório - Introdução Ao LaboratórioDokumen4 halamanModelo Relatório - Introdução Ao LaboratórioOuvinte de Bom GostoBelum ada peringkat
- A importância do controle de qualidade na pintura industrialDokumen30 halamanA importância do controle de qualidade na pintura industrialPedro Henrique Macedo KumairaBelum ada peringkat
- FISPQ 283 - Hexametilenotetramina - Labsynth PDFDokumen5 halamanFISPQ 283 - Hexametilenotetramina - Labsynth PDFNilton Cesar De Matos GonçalvesBelum ada peringkat
- A Água e Seus Efeitos Sobre As BiomoléculasDokumen12 halamanA Água e Seus Efeitos Sobre As BiomoléculasIanne Gonçalves VieiraBelum ada peringkat
- ILMENITA-Matérias PrimasDokumen6 halamanILMENITA-Matérias PrimasRafael TrianiBelum ada peringkat
- Purificação Biomoleculas PDFDokumen22 halamanPurificação Biomoleculas PDFAlinetakaokaBelum ada peringkat
- Sistemas ligantes químicos para moldagem em areiaDokumen58 halamanSistemas ligantes químicos para moldagem em areiaLucasween100% (1)
- FotoproteçãoDokumen30 halamanFotoproteçãoAna Néri GallioBelum ada peringkat
- Energia interna gás 1a lei termodinâmicaDokumen2 halamanEnergia interna gás 1a lei termodinâmicaPaulo Rogério Mancino100% (1)
- Modelo Básico Da FispqDokumen8 halamanModelo Básico Da FispqWagner Prochnow100% (1)