La Acidez de Los Diversos Grupos Funcionales
Diunggah oleh
Isamar Alcantara GomezHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
La Acidez de Los Diversos Grupos Funcionales
Diunggah oleh
Isamar Alcantara GomezHak Cipta:
Format Tersedia
QUIMICA DE LOS HIDROCARBUROS
LA ACIDEZ DE LOS DIVERSOS GRUPOS FUNCIONALES
NITRILOS
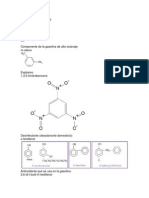
Los grupos funcionales que contienen al grupo funcional (-CN) se llaman nitrilos los
nitrilos se comportan como bases a travs del par solitario del nitrgeno. El cido
conjugado resultante tiene un pKa de -10, lo que indica la escasa basicidad de los nitrilos
comparada con iminas o aminas.
Los nitrilos poseen hidrgenos alfa cidos, con un pKa de 25, que podemos sustraer con
el empleo de bases fuertes, formando los enolatos de nitrilo. Esta desprotonacin de la
posicin alfa permite introducir sustituyentes en dicho carbono (reacciones de alquilacin).
TERES
Los teres son compuestos de frmula R-O-R, donde R y R pueden ser grupos alquilo o
grupos arilo (anillo de benceno). Al igual que los alcoholes, los teres estn relacionados
con el agua, con grupos alquilo que sustituyen a los tomos de hidrogeno. Las sustancias
no polares tienden a ser ms solubles en teres que los alcoholes debido a que los teres
no tienen una red de enlazamiento por puente de hidrgeno para que sea rota por el
soluto no polar. Las sustancias polares tienden a ser casi tan solubles en los teres como
en los alcoholes debido a que los teres tienen momentos dipolares grandes al igual que
la habilidad para actuar como aceptores de enlaces por puente de hidrgeno.
Los teres son no hidroxlicos (sin grupo hidroxilo) y por lo regular no son reactivos hacia
las bases fuertes. Por esta razn, los teres se usan con frecuencia como disolventes
para varias bases polares fuertes (como el reactivo de Grignard) que requieren
disolventes polares.
FENOLES
La propiedad caracterstica que distingue a los fenoles de los alcoholes es la acidez. Los
fenoles son dbilmente cidos como consecuencia de la deslocalizacin de la carga
negativa que se produce por conjugacin con el sistema aromtico (Ka para el fenol es
de alrededor de 10 -10) y se pueden neutralizar con hidrxido de sodio.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
La presencia de grupos dadores de electrones en el anillo aromtico desestabiliza esta
deslocalizacin, en particular cuando se encuentran en las posiciones orto o para
reduciendo la acides de los correspondientes fenoles. Del mismo modo la presencia de
sustituyentes que retiran densidad electrnica aumentara la acidez.
ALCOHOLES
Los alcoholes, con constantes de acidez de 10 -16 a 10-19, son de un milln a mil millones
de veces menos cidos que el fenol y no se neutralizan con hidrxido de sodio.
El pKa de los alcoholes se ve influenciado por algunos factores como son el tamao de la
cadena carbonada y los grupos electronegativos. La acidez disminuye conforme aumenta
la sustitucin en los grupos alquilo, ya que una mayor sustitucin de los grupos alquilo
inhibe la solvatacin del ion alcxido, lo que disminuye la estabilidad del ion alcxido y
ocasiona que el equilibrio de disociacin tienda a la izquierda.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
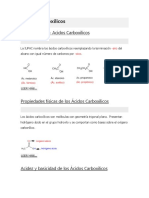
ACIDOS CARBOXILICOS
El que los cidos carboxlicos sean los compuestos orgnicos ms cidos se explica por
la eficaz deslocalizacin de la carga entre dos tomos de oxgeno, lo que se produce en el
anin carboxilato como consecuencia de un efecto resonante muy eficiente.
La conjugacin del grupo R con el grupo carboxilato nunca puede ser muy efectiva. La
existencia de un efecto resonante R solo puede tener lugar mediante la consideracin
del desplazamiento de los dos electrones pi del en C-C hacia el sistema pi con el que se
produce la conjugacin. Ello conducir a la participacin de una forma resonante
sumamente inestable en la que uno de los oxgenos se encuentra cargado positivamente
y adems no llega a poseer su octeto completo. Por su parte, la existencia de un efecto
resonante
+R conducir a considerar la participacin de una forma resonante en la que
los dos oxgenos prximos presentan una carga negativa. Similares formas resonantes
estaran presentes, adems, en el propio grupo carboxilo, por lo que no presentaran una
estabilizacin adicional.
De esta manera, el efecto de los factores estructurales sobre la estabilidad de los distintos
aniones carboxilato y por lo tanto sobre la acidez del cido carboxlico correspondiente,
debe interpretarse en base a la intervencin de los efectos inductivos de distinto signo.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
SULFUROS
Son notablemente ms cidos tienen un Pk= 11.96. Los sulfuros son mucho ms
nucleofilos que los teres. Lo que es comprensible si tenemos en cuenta la menor
electronegatividad del azufre.
HALOGENUROS DE ALQUILO
Un ion halogenuro es una base muy dbil, lo que se refleja en su disposicin a ceder un
protn a otras bases, es decir, en la gran acidez de los halogenuros de hidrgeno. En un
halogenuro de alquilo, el halgeno est unido a un carbono y, al igual que el halogenuro
libera con facilidad un protn, tambin libera carbono nuevamente, hacia otras bases.
Estas bases poseen un par de electrones no compartido y buscan un lugar relativamente
positivo; es decir, buscan un ncleo con el cual compartir su par electrnico.
Reactivos bsicos, ricos en electrones, que tienden a atacar el ncleo del carbono se
conocen como reactivos nucleoflicos o, simplemente, nuclefilos. Cuando este ataque
termina en sustitucin, la reaccin se denomina sustitucin nucleoflica.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
ACETONA.
Se debe a que la base conjugada resultante de la prdida de H+, est estabilizada por
resonancia, adems una de las formas resonantes estabiliza la carga negativa porque le
pone un tomo electronegativo de oxgeno. Pka= 19.3
AMIDAS
Las aminas actan como bases a travs del par libre del nitrgeno. La protonacin del
nitrgeno genera las sales de amonio. Su Pka=36.
Las amidas se encuentran entre los derivados ms estables de los cidos. El tomo de
nitrgeno de una amida no es tan bsico como el nitrgeno de una amina, debido al
efecto atractor de electrones del grupo carbonilo. Las siguientes formas de resonancia
nos ayudan a mostrar por que las amidas son bases muy dbiles:
AMINAS
Las aminas son bases moderadamente fuertes, sus disoluciones acuosas son bsicas.
Una amina puede sustraer un protn del agua formando un ion amonio y un ion hidroxilo.
La constante de equilibrio para esta reaccin se llama constante de disociacin de la base
para la amina simbolizada por Kb. Los valores Kb para la mayora de las aminas son
bastante pequeos alrededor de 10^-3 o menores por lo general presentadas por sus
logaritmos negativos valores de pKb entonces es igual a 3 as cmo usamos los valores
para pKa para indicar la fuerza de acidez el cual resulta ms alto y se determina mediante
la diferencia de pKa=14 - pKb.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
Bibliografa
Wade, L. C. (2011). Qumica Orgnica. Volumen 1. Mxico: 7 Ed. Pearson Educacin
Wade, L. C. (2011). Qumica Orgnica. Volumen 2. Mxico: 7 Ed. Pearson Educacin
J, Stepthen, R, Frank, Stermitz (1988). Qumica Orgnica. Reverte.
V. Santigo, L. Maria, A. Belen (1997). Introduccin a la Qumica Organica. Volumen 6.
Universitat Jaume.
CHAVARRIA CANO ISABEL 2IM32
QUIMICA DE LOS HIDROCARBUROS
CHAVARRIA CANO ISABEL 2IM32
Anda mungkin juga menyukai
- Propiedades de Los Compuestos Nitrogenados-1Dokumen15 halamanPropiedades de Los Compuestos Nitrogenados-1alexis VilcherresBelum ada peringkat
- Ácidos y BasesDokumen24 halamanÁcidos y BasesomarguerrawarBelum ada peringkat
- GresiaDokumen14 halamanGresiaJhon Brayan Perez CruzattBelum ada peringkat
- Hidrocarburos aromáticos y estructura del bencenoDokumen13 halamanHidrocarburos aromáticos y estructura del bencenoLuis Daniel Barrios BarriosBelum ada peringkat
- ACIDEZ DE ACIDOS CARBOXILICOS Jairo Perez PDFDokumen7 halamanACIDEZ DE ACIDOS CARBOXILICOS Jairo Perez PDFAntonio MalaveBelum ada peringkat
- Nomenclatura y Reactividad de Derivados de Ac - CarboxílicosDokumen3 halamanNomenclatura y Reactividad de Derivados de Ac - CarboxílicosPilar MonsalvoBelum ada peringkat
- 2 Reactivos en Qca Org (1era Parte)Dokumen15 halaman2 Reactivos en Qca Org (1era Parte)Nicolás CaicedoBelum ada peringkat
- Clase 3-Acidez y BasicidadDokumen36 halamanClase 3-Acidez y Basicidadlara taschettaBelum ada peringkat
- Aminas - PDF PochoDokumen8 halamanAminas - PDF PochogaboBelum ada peringkat
- Propiedades Fisicas de Los Hidrocarburos AlcanosDokumen2 halamanPropiedades Fisicas de Los Hidrocarburos AlcanosAlejo MuñozBelum ada peringkat
- Acidez en Moléculas OrganicasDokumen109 halamanAcidez en Moléculas OrganicasAlicia SanchezBelum ada peringkat
- Acidez 3 y Mec. BuenoDokumen138 halamanAcidez 3 y Mec. BuenoasdafadBelum ada peringkat
- Acidos Carboxilicos y AminasDokumen10 halamanAcidos Carboxilicos y AminasMontse CgBelum ada peringkat
- Marco Teorico Laboratorio 8Dokumen4 halamanMarco Teorico Laboratorio 8Luis Cossa100% (3)
- Capitulo 12 - Acidos CarboxilicosDokumen40 halamanCapitulo 12 - Acidos CarboxilicosAngel SolanoBelum ada peringkat
- Hidrocarburos Reacciones de CaracterizaciónDokumen12 halamanHidrocarburos Reacciones de CaracterizaciónRosario Huaman Mondragon0% (1)
- ALCANOSDokumen14 halamanALCANOSYASMINA BARRIENTOSBelum ada peringkat
- Acidez de Alquinos TerminalesDokumen3 halamanAcidez de Alquinos TerminalesPepe Kaztor MarinBelum ada peringkat
- ALCANOSDokumen7 halamanALCANOSMitzy Felipe RodriguezBelum ada peringkat
- Resumen AlcanosDokumen3 halamanResumen AlcanosVictor Hugo Lindarte Vega60% (5)
- Teoria Acidos y BasesDokumen19 halamanTeoria Acidos y BasesMaclo OtamendiBelum ada peringkat
- Alquenos y AlquinosDokumen3 halamanAlquenos y AlquinosMikaela VázquezBelum ada peringkat
- Bolas Contra Las PolillasDokumen7 halamanBolas Contra Las PolillasvictormmcBelum ada peringkat
- Hidrocarburos AlcanosDokumen9 halamanHidrocarburos AlcanosMercedezMartinezZapataBelum ada peringkat
- Química Orgánica AlquinosDokumen42 halamanQuímica Orgánica AlquinoskennetBelum ada peringkat
- Trabajo 1Dokumen12 halamanTrabajo 1Arnulfo Antonio Barrios RosadoBelum ada peringkat
- Aldehidos y CetonasDokumen30 halamanAldehidos y CetonasJuanBelum ada peringkat
- Clase 7. Ácidos y Bases Grupos FuncionalesDokumen104 halamanClase 7. Ácidos y Bases Grupos FuncionalesMaria Alejandra Naspiran GuerreroBelum ada peringkat
- De Acidos CarboxilicosDokumen7 halamanDe Acidos CarboxilicosEdwin Loza CoaquiraBelum ada peringkat
- CETONADokumen6 halamanCETONARobin JoshuaBelum ada peringkat
- Informe 2 de Laboratorio Orgánica 2Dokumen24 halamanInforme 2 de Laboratorio Orgánica 2Franck Cristhian Arana AlmonacidBelum ada peringkat
- Trampas Quimicas. ExposicionDokumen27 halamanTrampas Quimicas. ExposicionRaúl FloresBelum ada peringkat
- ALCANOSDokumen11 halamanALCANOSAdrian BaezBelum ada peringkat
- Alquinos y sus propiedadesDokumen15 halamanAlquinos y sus propiedadesThaliaRamosBelum ada peringkat
- Nomenclatura de AlquinosDokumen15 halamanNomenclatura de AlquinosThaliaRamosBelum ada peringkat
- Quimica Organica Ii Iiii SnaDokumen24 halamanQuimica Organica Ii Iiii SnaValery. g18Belum ada peringkat
- Alquenos AlquinosDokumen20 halamanAlquenos AlquinosValeria Carrion AndradeBelum ada peringkat
- Acidos CarboxilicosDokumen9 halamanAcidos CarboxilicosStefaniGarcesBelum ada peringkat
- Cap10 - 02 - Acidos Carboxílicos y DerivadosDokumen31 halamanCap10 - 02 - Acidos Carboxílicos y DerivadosJhordin Dario León AlvaradoBelum ada peringkat
- Sustitucion Electrofilica AromaticaDokumen20 halamanSustitucion Electrofilica AromaticaEzequiel HernándezBelum ada peringkat
- ALQUENOS y ALquinosDokumen18 halamanALQUENOS y ALquinosValentina González100% (1)
- ALQUENOS y ALQUINOS PDFDokumen23 halamanALQUENOS y ALQUINOS PDFAntonella BaptistaBelum ada peringkat
- Aldehidos y Cetonas - Primera ParteDokumen26 halamanAldehidos y Cetonas - Primera ParteBelen Rocio Delmar Flores CaribauxBelum ada peringkat
- Aminas 2023Dokumen10 halamanAminas 2023Octa HerreraBelum ada peringkat
- TP 2 HidrocarburosDokumen6 halamanTP 2 HidrocarburosLeonardo AredresBelum ada peringkat
- Ácidos Carboxílicos... 01Dokumen12 halamanÁcidos Carboxílicos... 01JoseBelum ada peringkat
- AlcanosDokumen7 halamanAlcanosJose AriasBelum ada peringkat
- Alquinos 1Dokumen10 halamanAlquinos 1Patricio Alfaro CerdaBelum ada peringkat
- Compuestos carbonílicos y sus reaccionesDokumen12 halamanCompuestos carbonílicos y sus reaccionesAgostina de MaríaBelum ada peringkat
- Compuestos - Aromaticos 20-21Dokumen42 halamanCompuestos - Aromaticos 20-21Manuel GordilloBelum ada peringkat
- Equipo5 - Ácidos CarboxílicosDokumen23 halamanEquipo5 - Ácidos CarboxílicosLety LagunaBelum ada peringkat
- Propiedades Fisicas de Los AlcanosDokumen8 halamanPropiedades Fisicas de Los AlcanosRudy Zenon Chaquilla100% (3)
- Sustitución Nucleofílica AlifaticaDokumen63 halamanSustitución Nucleofílica AlifaticaLuis E Aguilar RBelum ada peringkat
- S - 4 Alquinos 2023 IDokumen35 halamanS - 4 Alquinos 2023 IRaul GonzalesBelum ada peringkat
- Factores que afectan la acidez de los ácidos carboxílicosDokumen6 halamanFactores que afectan la acidez de los ácidos carboxílicosPatricio Candia InostrozaBelum ada peringkat
- AlcanosDokumen12 halamanAlcanosfernando souzaBelum ada peringkat
- Los Alquenos 2 Estructura y SintesisDokumen23 halamanLos Alquenos 2 Estructura y SintesisJair Villao ABelum ada peringkat
- Modelo Dimã¡nico de Un Electrolizador Alcalino PDFDokumen110 halamanModelo Dimã¡nico de Un Electrolizador Alcalino PDFIsamar Alcantara GomezBelum ada peringkat
- P-10 Campo MagneticoDokumen5 halamanP-10 Campo MagneticoIsamar Alcantara GomezBelum ada peringkat
- Alto HornoDokumen6 halamanAlto HornoIsamar Alcantara GomezBelum ada peringkat
- Instrumentos y Casos Prácticos de NegociosDokumen63 halamanInstrumentos y Casos Prácticos de NegociosALTADIRBelum ada peringkat
- Formula RioDokumen12 halamanFormula RioIsamar Alcantara GomezBelum ada peringkat
- Confidencialidad ImparcialidadDokumen2 halamanConfidencialidad ImparcialidadIsamar Alcantara GomezBelum ada peringkat
- P-10 Campo MagneticoDokumen5 halamanP-10 Campo MagneticoIsamar Alcantara GomezBelum ada peringkat
- Practica 1Dokumen5 halamanPractica 1Isamar Alcantara GomezBelum ada peringkat
- Guap@s Mesa 1 Proyecto XDDokumen4 halamanGuap@s Mesa 1 Proyecto XDIsamar Alcantara GomezBelum ada peringkat
- Diagrama Prac2Dokumen2 halamanDiagrama Prac2Isamar Alcantara Gomez0% (1)
- Rectificacion LotesDokumen14 halamanRectificacion LotesIsamar Alcantara GomezBelum ada peringkat
- Quimica ProgramaDokumen1 halamanQuimica ProgramaIsamar Alcantara GomezBelum ada peringkat
- CalibracionDokumen2 halamanCalibracionIsamar Alcantara GomezBelum ada peringkat
- Prac 1 DiagramasDokumen2 halamanPrac 1 DiagramasIsamar Alcantara GomezBelum ada peringkat
- Conclusión Ley de OhmDokumen1 halamanConclusión Ley de OhmIsamar Alcantara Gomez40% (15)
- P 2 ConclusiónDokumen1 halamanP 2 ConclusiónIsamar Alcantara GomezBelum ada peringkat
- Termo 3 Practica 1Dokumen13 halamanTermo 3 Practica 1Isamar Alcantara GomezBelum ada peringkat
- Ecuación de AntoineDokumen1 halamanEcuación de AntoineIsamar Alcantara GomezBelum ada peringkat
- Practica 1Dokumen20 halamanPractica 1CINL12367% (9)
- Ecuación de AntoineDokumen1 halamanEcuación de AntoineIsamar Alcantara GomezBelum ada peringkat
- FisicaDokumen2 halamanFisicaIsamar Alcantara GomezBelum ada peringkat
- Conclusion C ColumnaDokumen1 halamanConclusion C ColumnaIsamar Alcantara GomezBelum ada peringkat
- FONPLATA - Investor Presentation 2Q-21 Esp Final PDFDokumen26 halamanFONPLATA - Investor Presentation 2Q-21 Esp Final PDFAlejandro LopezBelum ada peringkat
- Costeo de Operaciones InternacionalesDokumen25 halamanCosteo de Operaciones InternacionalesCristian Everardo Flores RamírezBelum ada peringkat
- Concepciones de Salud Mental en El Campo deDokumen14 halamanConcepciones de Salud Mental en El Campo deMartin VelardeBelum ada peringkat
- Patrones de asentamiento Salinar en Cerro SalturDokumen45 halamanPatrones de asentamiento Salinar en Cerro SalturKelita Perez CubasBelum ada peringkat
- Programa de Formacion Musical 1Dokumen7 halamanPrograma de Formacion Musical 1FlorenciaCuccareseBelum ada peringkat
- Torres MoyanoDokumen7 halamanTorres MoyanoMarco OlazabalBelum ada peringkat
- Mejores Navegadores de InternetDokumen42 halamanMejores Navegadores de InternetGarcia WilbertBelum ada peringkat
- Auditoria Protocolos MinsalDokumen18 halamanAuditoria Protocolos MinsalXimena Torres75% (4)
- Teoria Del BuqueDokumen127 halamanTeoria Del BuqueTiago Catuxo100% (1)
- MANEJO DE ALPACAS (Autoguardado)Dokumen16 halamanMANEJO DE ALPACAS (Autoguardado)MarcosBelum ada peringkat
- Consumo Responsable PDFDokumen2 halamanConsumo Responsable PDFMelissa Bances CarlosBelum ada peringkat
- Ejercicios sobre el Neolítico: herramientas, arte rupestre y asentamientosDokumen7 halamanEjercicios sobre el Neolítico: herramientas, arte rupestre y asentamientoslogr054nBelum ada peringkat
- Tarea 1.2 El Sistema Educativo Dominicano, Revisas La Ley 66-97Dokumen4 halamanTarea 1.2 El Sistema Educativo Dominicano, Revisas La Ley 66-97jesus feliz paredezBelum ada peringkat
- Resumen Parcial Proyectivas VecciaDokumen85 halamanResumen Parcial Proyectivas VecciaJuampi Mazza67% (3)
- 100 Ideas para EmprenderDokumen14 halaman100 Ideas para EmprenderDobast100% (1)
- Ley contra la discriminaciónDokumen2 halamanLey contra la discriminaciónClaudia LedesmaBelum ada peringkat
- Autorización representación CCC TGSSDokumen2 halamanAutorización representación CCC TGSSMaría GeBelum ada peringkat
- MALEFICADokumen2 halamanMALEFICAAndrea Carolina Sanchez CamachoBelum ada peringkat
- Memoria DescriptivaDokumen12 halamanMemoria DescriptivaMEDALYSBelum ada peringkat
- Hot Dog - AlpacaDokumen22 halamanHot Dog - Alpacasandra karinne torres palominoBelum ada peringkat
- Ley General de Educación Capítulo VIII InclusiónDokumen3 halamanLey General de Educación Capítulo VIII InclusiónmandoBelum ada peringkat
- Rita Liranzo Alcántara, 100632783, ECN 2230-12, Tarea 3Dokumen18 halamanRita Liranzo Alcántara, 100632783, ECN 2230-12, Tarea 3Rita LiranzoBelum ada peringkat
- Ensayo Evaluación Del AprendizajeDokumen7 halamanEnsayo Evaluación Del AprendizajeMarcelo RoqueBelum ada peringkat
- Perfil normalista religiosoDokumen7 halamanPerfil normalista religiosoMARIA PAULA MENDOZA PINEDABelum ada peringkat
- Iperc Linea BaseDokumen19 halamanIperc Linea Basehenry castillo quispeBelum ada peringkat
- Catalogo Hot SexDokumen32 halamanCatalogo Hot SexJUAN CARLOS ABRIL RAMIREZBelum ada peringkat
- 18 Sesión JULIO LUNES - Docx Bardales RodriguezDokumen60 halaman18 Sesión JULIO LUNES - Docx Bardales RodriguezErika Prints Bardales RodriguezBelum ada peringkat
- Presentación Construcción CiudadanaDokumen7 halamanPresentación Construcción CiudadanaGladis LalyBelum ada peringkat
- Tiempos Fundamentales de La Tecnica QuirurgicoDokumen111 halamanTiempos Fundamentales de La Tecnica QuirurgicoEfraim VirreyBelum ada peringkat
- Licencia Excepcional RS-2020-15059878-APN-MTDokumen2 halamanLicencia Excepcional RS-2020-15059878-APN-MTTodo Noticias100% (1)