Laboratorio Numero 11
Diunggah oleh
Anonymous fPGiYHFYJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Laboratorio Numero 11
Diunggah oleh
Anonymous fPGiYHFYHak Cipta:
Format Tersedia
Universidad Nacional Mayor de San Marcos
I. TABULACION DE DATOS Y RESULTADOS.
CONDICIONES DE LABORATORIO
PRESION
TEMPERATURA
% HUMEDAD
756 mmHg
23 C
96 %
Tabla1: Pesos Moleculares de los Compuestos Utilizados y
Normalidad Terica del NaOH.
PM Biftalato de Potasio.
PM cido benzoico
Normalidad Teo. del NaOH
204.23 g/mol
122.12 g/mol
0.1 N
Tabla 2: Calculo de la Normalidad del NaOH Valorado con el
Biftalato de Potasio.
W Biftalato de Potasio
Volumen del Biftalato
Volumen Gastado de NaOH
Normalidad corregida de NaOH
0.300 g
0.01 L
0.118 L
0.1245 N
Tabla 3: Datos Obtenidos en el Experimento.
T C
20
20
25
25
W Erlenmeyer
Vacio
77.9046 g
74.2779 g
83.2235 g
92.4380 g
W Erlenmeyer +
Solucin
87.7492 g
84.7810 g
93.1078 g
102.2946 g
Volumen gastado
deNaOH
2.10 ml
2.20 ml
2.55 ml
2.30 ml
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.1
Universidad Nacional Mayor de San Marcos
Tabla 4: Determinacin del Peso de la Solucin, el Numero
de Equivalentes y el peso del cido Benzoico, para cada
Temperatura.
T C W Sol= (W Erlenmeyer + Sol)
(W Erlenmeyer Vacio)
20
9.8446 g
20
10.5031 g
25
9.8843 g
25
9.8566 g
#Eq cido
Benzoico
0.0002615
0.0002739
0.0003175
0.0002864
W cido
Benzoico
0.03193 g
0.03345 g
0.03877 g
0.03498 g
Tabla 5: Determinacin del Peso del Agua en la Solucin y la
Concentracin molal del cido Benzoico.
W Agua = W Sol W Ac Benzoico
9.813 g
10.47 g
9.846 g
9.822 g
Molalidad del Ac
0.026645
0.026162
0.032244
0.029163
Benzoico
m
m
m
m
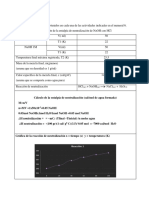
Tabla 6: Datos tericos de Molalidad y temperatura para
Construir el grafico Lnms Vs 1/T y encontrar el H (Calor
Diferencial de Disolucin Terico)
TC
20
25
TK
1/T
Molalidad
Lnms
293.15
0.003411
0.048
-3.03655
298.15
0.003354
0.057
-2.86470
H Calor Diferencial de Disolucin Terico
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.2
Universidad Nacional Mayor de San Marcos
6029.82 cal/mol <> 25.23 KJ/mol
Tabla 7: Datos Experimentales de la Molalidad y
Temperatura para Construir el grafico Lnms Vs 1/T y
encontrar el H (Calor Diferencial de Disolucin
Experimental)
T C
20
25
TK
1/T
Molalidad Prom.
Lnms
293.15
0.003411
0.0264035
-3.63426
298.15
0.003354
0.030705
-3.48333
H Calor Diferencial de disolucin Experimental
5276.72 cal/mol <> 22.08 KJ/mol
Tabla 8: Calculo del porcentaje de error del Calor Diferencial
de Disolucin ( H )
Error Experimental ( Eex % )
12.5 %
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.3
Universidad Nacional Mayor de San Marcos
II.EJEMPLO DE CALCULOS.
Se Trabajo la solucin de cido benzoico a 20C y 25C y se
tomaron dos muestras a una sola temperatura por lo tanto en
los clculos para graficar la molalidad se tomo el promedio de
estas dos (ver tabla 5 y 7) y se realizaron los clculos a estas
temperaturas.
1) Calculo de la Normalidad Corregida del NaOH.
Para hallar la normalidad corregida valoramos la solucin de
NaOH con biftalato de Potasio, usando fenolftaleina como
indicador.
Datos Tericos:
PM de Biftalato de Potasio
Normalidad terica del NaOH
P.Eq-Biftalato de Potasio
P.Eq- Ac Benzoico
= 204,23 g/mol
= 0.1 N
=204.23 g/Eq
= 122.12 g/Eq
Datos Experimentales:
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.4
Universidad Nacional Mayor de San Marcos
W Biftalato de potasio
Volumen Gastado del NaOH
Sabemos que:
Eq - g NaOH =
= 0.300 g
= 11.8 ml = 0.0118 L
Eq - g Biftalato de potasio
V NaOH x Ncorre NaOH = W biftalato de K / P Eq-Biftalato de K
Reemplazando:
Ncorre NaOH = 0.300/204.23 x 0.0118
= 0.1245 N
2) Calculo
del
peso
de
la
Solucin,
el
Numero
de
Equivalentes y el Peso del Ac cido Benzoico, para cada
Temperatura.
Calculo del Peso de la Solucin de Ac Benzoico a 20C.
W1 Erlenmeyer vacio.
W1 Erlenmeyer + Sol.
W2 Erelnmeyer Vacio
W2 Erlenmeyer +Sol.
= 77.9046 g
= 87.7492 g
= 74.2779 g
= 84.7810 g
W Sol= W Erlenmeyer + Sol - W Erlenmeyer vacio
W1 Sol
= 87.7492 77.9046 g
W1 Sol
= 9.8446 g
W2 Sol
= 84.7810 74.2779 g
W2 Sol
= 10.5031 g
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.5
Universidad Nacional Mayor de San Marcos
Calculo del Numero de Equivalentes
del Ac
Benzoico a
20C.
V1 gastado de NaOH= 2.10 ml =0.0021 L
V2 gastado de NaOH
= 2.20 ml =0.0022 L
Se obtiene de la siguiente igualdad:
Eq.- g. Ac. Benzoico = Eq.- g. NaOH
Eq.- g. HBZ = Ncorre NaOH x Vgastado NaOH
Eq1.- g. HBZ =
0.1245 N x 0.0021 L
Eq1.- g. HBZ =
0.0002615 Eq-g
# Eq2.-g HBZ =
0.1245 N x 0.0022 L
# Eq2.-g HBZ =
0.0002739 Eq-g
Calculo del peso de cido Benzoico a 20C
Sabemos que:
Eq.- g. Ac Benzoico =
Despejando tenemos que:
W HBZ
W1HBZ
W1HBZ
W2 HBZ
W2 HBZ
=
=
=
=
=
W HBZ / P. eq. HBZ
Eq - g HBZ x P. eq. - HBZ
0.0002615 eq x 122.12 g /eq
0.03193 g
0.0002739 eq x 122.12 g/eq
0.03345 g
3) Calculo del Peso del Agua en la Solucin y la molalidad
del Ac. Benzoico.
Calculo del Peso del Agua de la Solucin a 20C
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.6
Universidad Nacional Mayor de San Marcos
Se determina por:
W H2 O
=
W Sol - W HBZ
W1 H2O =
(9.8446 - 0.03193) g
W1H2O
=
9.813 g. = 0.009813 kg
W2H2O =
(10.5031-0.03345) g
W2H2O =
10.47 g = 0.01047kg
Calculo del Numero de moles de cido Benzoico a 20C.
Sabemos que:
Moles HBZ
=
W HBZ / P.M HBZ
moles1 HBZ =
0.03193 g / 122.12 g/mol
moles1HBZ
=
0.0002615 mol
moles2HBZ
=
0.03345 g / 122.12 g/mol
moles2HBZ
=
0.000274 mol
Calculo de la molalidad (m) del cido Benzoico a 20C.
Sabemos que:
m=
m1
m1
m2
m2
moles HBZ /Peso en Kg de H2O
= 0.0002615 mol / 0.009813Kg
= 0.026645 mol / kg
= 0.000274 mol / 0.01047kg
= 0.026162 mol/kg
De la misma manera se realiza los clculos para la temperatura
de 25C y los resultados obtenidos se observan en las tablas.
4) Calculo del Calor Diferencial de la Disolucin (H),
(Terico y Experimental), y el Porcentaje de Error.
Sabemos que:
Lnms
H ds 1
C
R T
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.7
Universidad Nacional Mayor de San Marcos
Donde:
Hds = Calor diferencial de la disolucin.
R
= 2 cal/ mol K.
Lnms = Logaritmo natural de la molaliddad de la disolucin.
1/T = inversa de la temperatura en grados absolutos (K).
C
= Constante.
Al construir la grfica Lnms Vs 1/T, podemos aproximarla
mediante una ecuacin lineal de la forma:
y Bx A
Entonces comparando se tiene que:
B= -Hds / R
A= C = cte.
Calculo de la Pendiente y el Hds con los Datos Tericos.
1/T
0.003411
0.003354
Lnms
-3.03655
-2.86470
Entonces:
B= -3014.91 = -Hds / 2 cal/mol K
Se Obtiene:
Hds Teorica= 6029.82 cal/mol (4.184 J/cal)
25.23 KJ/mol
Calculo de la Pendiente
experimentales.
el
(1KJ/1000 J) =
Hds con
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.8
los
Datos
Universidad Nacional Mayor de San Marcos
Como tomamos dos muestras a la misma temperatura tomamos
el promedio de estas para poder graficarlas.
Molalidad del Ac
0.026645
0.026162
0.032244
0.029163
Benzoico
m
m
m
m
Las molalidades resultante fueron:
0.0264035 y 0.030705 que al tomarles su logaritmo natural se
obtienen los datos de la siguiente tabla
1/T
0.003411
0.003354
Lnms
-3.63426
-3.48333
Entonces:
B= -2638.36 = -Hds / 2 cal/mol K
Se Obtiene:
Hds experiemntal= 5276.72 cal/mol (4.184 J/cal) (1KJ/1000 J) =
22.08 KJ/mol
Calculo del Error Experimental:
(Valor Terico Valor Experimental / Valor Terico) X 100
Reemplazando:
(25.23 22.08) / 25.23 = 12.5 %
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.9
Universidad Nacional Mayor de San Marcos
III. DISCUSION DE RESULTADOS.
Al Hallar la normalidad corregida del NaOH, se obtuvo un
valor muy cercano al valor terico, lo cual nos indica que
esta en un rango apreciable.
Con la normalidad corregida se calculo el numero de
equivalentes y con este dato el peso de cido benzoico
presente en la solucin a las diferentes temperaturas
respectivamente. Se puede observar que conforme disminuye
la temperatura el peso de cido benzoico disminuye en la
solucin esto se debe a que el cido benzoico es mas soluble
a una temperatura elevada.
Este experimento afirma lo que tericamente se ha estudiado
En la mayora de los casos, aunque no en todos la solubilidad
de una sustancia slida aumenta con la temperatura.
Los errores cometidos, se pueden deber a diversos factores
como la mala pesada en las muestras slidas y en los
erlenmeyer, al momento de pipetear la solucin de cido
benzoico se pudieron absorber cristales a pesar del filtro
colocado en la pipeta,
otro motivo pudo haber sido que al
empezar a disolver el cido benzoico agitndose la solucin
con una bagueta, perdi un poco de muestra la cual se
adhiri a las paredes de la bagueta. Pero estos errores
cometidos pueden superarse a travs de la experiencia.
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.10
Universidad Nacional Mayor de San Marcos
El valor terico de H obtenido con las molalidades tericas a
las temperaturas ya conocidas es parecida al encontrado
experimentalmente variando en un mnimo porcentaje.
IV. COCLUSIONES.
En la mayora de los casos, pero no en todos, la solubilidad
de una sustancia slida aumenta con la temperatura.
Los slidos apreciablemente se disuelven solo en solventes
polares, particularmente el agua.
La solubilidad de un slido en un liquido es siempre limitada
y el limite para un mismo solvente es diferente segn las
distintas sustancias dependiendo fundamentalmente de la
temperatura.
En general la solubilidad es la concentracin de soluto en
una disolucin saturada.
Se comprob experimentalmente que a medida que la
temperatura disminuye la solubilidad tambin disminuye en
el cido benzoico.
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.11
Universidad Nacional Mayor de San Marcos
V. RECOMENDACIONES.
Lavar y secar en la estufa todo el material de vidrio.
Evitar las perdida de reactivo (Ac Benzoico) ya sea en las
paredes
del
erlenmeyer
o
al
momento
disolverlo
introduciendo la bagueta.
Cuando el slido se ha disuelto totalmente para no perder
tiempo esperando que baje la temperatura
y medir la
solubilidad se recomienda llevar el erlenmeyer a baos de
agua fra, observndose siempre la temperatura a la cual
quieres probar la solubilidad.
Al momento de pipetear la solucin es aconsejable cambiar el
algodn del filtro que se encuentra en la pipeta para evitar
que el slido se acumule en este.
El cido benzoico se debe disolver en agua destilada
previamente calentada, ya que la solubilidad de este es mayor
en caliente.
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.12
Universidad Nacional Mayor de San Marcos
VI. APENDICE.
1.-Defina solucin Saturada.
Se denomina as a la mxima cantidad de soluto que puede ser
disuelta en una cantidad determinada de disolvente (solvente).
2.- Que relacin existe entre el calor diferencial de
disolucin, la temperatura y las caractersticas de la
sustancia?
El calor diferencial es el cambio de calor asociado al proceso de
dilucin. Si cierto proceso de dilucin es endotrmico y la
solucin se diluye con posterioridad, la misma solucin absorbe
mas calor de los alrededores. Lo contrario ocurre en un proceso
exotrmico de disolucin: se libera mas calor si se agrega mas
disolvente, para diluir la disolucin.
3.- En la ecuacin que relaciona la concentracin de la
solucin saturada con la temperatura. Fundamente el uso
de la concentracin molal.
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.13
Universidad Nacional Mayor de San Marcos
Se usa la concentracin molal ya que es la nica formula que
nos relaciona ala ves el numero de moles del soluto y el peso
del solvente (H2O) en kilogramos.
Esta relacin se adecua mas en los problemas de solubilidades
por relacionar soluto y solvente a la ves.
VII. BIBLIOGRAFIA
Fisicoqumica
Ponz Muzzo, Gaston
Sexta edicin
Editorial Universo
Fundamentos de Fisicoqumica
Maron - Prutton
Editorial Limusa
Mxico - 1984
Tratado de Qumica Fsica
Samuel
Glasstone,
Editorial Madrid
SptimaEdicin - 1979
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.14
Universidad Nacional Mayor de San Marcos
Laboratorio de Fisicoqumica II Variacin de la
Solubilidad con la Temperatura.15
Anda mungkin juga menyukai
- Determinación Del Calor de Disolución y NeutralizacionDokumen10 halamanDeterminación Del Calor de Disolución y NeutralizacionMarlli Reyes100% (1)
- Práctica 2. Calor Diferencial de Disolución.Dokumen4 halamanPráctica 2. Calor Diferencial de Disolución.Karen CarrilloBelum ada peringkat
- Informe 8 - Termoquimica y TermodinamicaDokumen5 halamanInforme 8 - Termoquimica y TermodinamicaJeremy Solis Fonseca0% (2)
- Practica 2 Ley de HessDokumen5 halamanPractica 2 Ley de HessOrlando HBelum ada peringkat
- I. Tabulacion de Datos Y ResultadosDokumen15 halamanI. Tabulacion de Datos Y ResultadosMario Salas PastorBelum ada peringkat
- Calor NeutDokumen10 halamanCalor NeutLaura Bustamante CalleBelum ada peringkat
- Informe 3 Lab de Fiqui - Variación de La Solubilidad Con La TemperaturaDokumen6 halamanInforme 3 Lab de Fiqui - Variación de La Solubilidad Con La TemperaturaPIERO MATIAS HERRERA SUAREZBelum ada peringkat
- Calordeneutralizaci N 2Dokumen9 halamanCalordeneutralizaci N 2Laura Bustamante CalleBelum ada peringkat
- Calor de NeutralizacionDokumen10 halamanCalor de NeutralizacionEduardo J Dugarte GBelum ada peringkat
- Solubilidad Del Ácido Benzóico y Determinación de Entalpía de Solución.Dokumen10 halamanSolubilidad Del Ácido Benzóico y Determinación de Entalpía de Solución.Oscar Portillo100% (1)
- Informe Fisicoquimik CALOR DE NEUTRALIZACIÓNDokumen13 halamanInforme Fisicoquimik CALOR DE NEUTRALIZACIÓNCristian DiazBelum ada peringkat
- Informe 8 Termoquimica y Termodinamica PDFDokumen5 halamanInforme 8 Termoquimica y Termodinamica PDFJuan Arias100% (1)
- Laboratorio Nº1 Fisicoquimica I (Plancha 2)Dokumen13 halamanLaboratorio Nº1 Fisicoquimica I (Plancha 2)Jose FernandezBelum ada peringkat
- Lab de Termodinamica 3Dokumen5 halamanLab de Termodinamica 3Daniel Alejandro Salamanca SantiagoBelum ada peringkat
- DETERMINACIÓN DE KSPDokumen5 halamanDETERMINACIÓN DE KSPAngela aponteBelum ada peringkat
- INFORME-7Dokumen7 halamanINFORME-7AnaisBriggitJacintoChavezBelum ada peringkat
- Termoquimica2 Laboratorio de Fisicoquimica UNMSMDokumen19 halamanTermoquimica2 Laboratorio de Fisicoquimica UNMSMwaldir marcelinoBelum ada peringkat
- Informe 03Dokumen15 halamanInforme 03César Rodrigo Lope FloresBelum ada peringkat
- Informe 3 QG Invierno PDFDokumen15 halamanInforme 3 QG Invierno PDFDiana Rita Pomez QuirozBelum ada peringkat
- Determinación de Bicarbonato en AlkaDokumen4 halamanDeterminación de Bicarbonato en AlkaJavier QuirogaBelum ada peringkat
- Conclusiones, Recomendaciones y Cuestionario - Laboratorio 2 de FisicoquímicaDokumen8 halamanConclusiones, Recomendaciones y Cuestionario - Laboratorio 2 de FisicoquímicaMaria AlessandraBelum ada peringkat
- Determinación Del Calor de Reacción de Una Reacción ÁcidoDokumen6 halamanDeterminación Del Calor de Reacción de Una Reacción ÁcidoJuanMiguel Arratia ValderramaBelum ada peringkat
- PRACTICA de Calorimetria IIIDokumen6 halamanPRACTICA de Calorimetria IIIalexander ruelas zapata0% (1)
- Informe Calores de Neutralización y SoluciónDokumen4 halamanInforme Calores de Neutralización y SoluciónPaula Ramirez100% (1)
- Acido-Acetico Imprimir NocheDokumen8 halamanAcido-Acetico Imprimir NocheAbby VásquezBelum ada peringkat
- Práctica Fisicoquimica (Ley de Hess)Dokumen5 halamanPráctica Fisicoquimica (Ley de Hess)yazsancer10Belum ada peringkat
- Equilibrio-Químico MejoradoDokumen8 halamanEquilibrio-Químico MejoradoJhoel Ivan Diaz PaucarBelum ada peringkat
- LAboratorio 1 Quimica Industrial FinalDokumen17 halamanLAboratorio 1 Quimica Industrial FinalXiomiBellQuispeRiveraBelum ada peringkat
- Calores de Neutralizacion y SolucionDokumen6 halamanCalores de Neutralizacion y SolucionANA MARIA GONZALEZ BARRIOSBelum ada peringkat
- Calor de Neutralizacion y de Solucion 1Dokumen8 halamanCalor de Neutralizacion y de Solucion 1Paola SolórzanoBelum ada peringkat
- PRACTICA 2 FisicoquimicaDokumen16 halamanPRACTICA 2 FisicoquimicaCarlos Jhair Rodriguez83% (6)
- Universidad Nacional de IngeníeriaDokumen12 halamanUniversidad Nacional de IngeníeriaClaudiaNoeliaIngaGutierrezBelum ada peringkat
- Informe 4 Ley de HessDokumen6 halamanInforme 4 Ley de HessOrtega Martinez JohanithaBelum ada peringkat
- Determinacion Crioscopica Del Peso Molecular FinalDokumen13 halamanDeterminacion Crioscopica Del Peso Molecular FinalPier Navarro100% (1)
- ESTEQUIOMETRIADokumen8 halamanESTEQUIOMETRIASheyla TRBelum ada peringkat
- Practica. Calor de Neutralizacion 1 1Dokumen9 halamanPractica. Calor de Neutralizacion 1 1Ana Maria RiveraBelum ada peringkat
- Solubilidad Del Ácido Benzoico y Determinación de Su Calor de SoluciónDokumen13 halamanSolubilidad Del Ácido Benzoico y Determinación de Su Calor de SoluciónHector Jesus Roca LoaizaBelum ada peringkat
- Isoterma de AdsorcionDokumen31 halamanIsoterma de AdsorcionOrlando MedinaBelum ada peringkat
- Informe 6Dokumen10 halamanInforme 6Alondra Isabel Canchari CuroBelum ada peringkat
- Calor FisicoquimicaDokumen5 halamanCalor FisicoquimicaManuel Jose Castilla RinconBelum ada peringkat
- Práctica #4 Descenso Del Punto de Congelación de Un Solvente PuroDokumen21 halamanPráctica #4 Descenso Del Punto de Congelación de Un Solvente PuroMaría de los Ángeles Moreno CoronadoBelum ada peringkat
- Laboratorio de Calorimetria.Dokumen3 halamanLaboratorio de Calorimetria.Luis MorenoBelum ada peringkat
- Informe N1 - Solubilidad Del Acido BenzoicoDokumen5 halamanInforme N1 - Solubilidad Del Acido BenzoicoJorge David MoraBelum ada peringkat
- Neutralizacion de 03Dokumen9 halamanNeutralizacion de 03Angel Esmit Roca LaurenteBelum ada peringkat
- Calor de NeutralizaciónDokumen8 halamanCalor de NeutralizaciónWilly SalcedoBelum ada peringkat
- Calor Diferencial de SolucionDokumen6 halamanCalor Diferencial de SolucionemerengiBelum ada peringkat
- Práctica y Reporte 6Dokumen10 halamanPráctica y Reporte 6Laura PerezBelum ada peringkat
- Practica 2 Calor de ReaccionDokumen8 halamanPractica 2 Calor de ReaccionAxel Moreno ModestoBelum ada peringkat
- Solubilidad en Función de TemperaturaDokumen9 halamanSolubilidad en Función de TemperaturaAndreita ArguelloBelum ada peringkat
- Determinación de La Estequiometría de Una ReacciónDokumen7 halamanDeterminación de La Estequiometría de Una ReacciónNICOLLE DAYANA MUÑOZ GALLEGOBelum ada peringkat
- Practica N°3. CONSTANTE UNIVERSAL DE LOS GASESDokumen11 halamanPractica N°3. CONSTANTE UNIVERSAL DE LOS GASESJUAN CAMILO GUIO HIGUERABelum ada peringkat
- Practica 3 Qumica Aplicada UpiicsaDokumen9 halamanPractica 3 Qumica Aplicada UpiicsaNne AmorosoBelum ada peringkat
- Práctica #7 SalesDokumen8 halamanPráctica #7 SalesCarolina MontenegroBelum ada peringkat
- Informe P2Dokumen10 halamanInforme P2veronica RodriguezBelum ada peringkat
- Conductividad Electrica Disoluciones PDFDokumen14 halamanConductividad Electrica Disoluciones PDFFerBelum ada peringkat
- Termodinámica Q.GeneralDokumen16 halamanTermodinámica Q.GeneralJorge Jesus Jeri JimenezBelum ada peringkat
- Fico 2 Informe 4Dokumen10 halamanFico 2 Informe 4Miguel AguilarBelum ada peringkat
- Ingeniería química. Soluciones a los problemas del tomo IDari EverandIngeniería química. Soluciones a los problemas del tomo IBelum ada peringkat
- Curso Práctico de Química GeneralDari EverandCurso Práctico de Química GeneralPenilaian: 4 dari 5 bintang4/5 (4)
- Linea Del Tiempo Historia de La ÓpticaDokumen45 halamanLinea Del Tiempo Historia de La ÓpticaMELANIE VANESSA PERALES ALCOCERBelum ada peringkat
- La Cultura y La Ciencia Hispano-ÁrabeDokumen38 halamanLa Cultura y La Ciencia Hispano-ÁrabeJose Antonio Moreno MorenoBelum ada peringkat
- 09 - Circuito Serie RLCDokumen11 halaman09 - Circuito Serie RLCIvanovBelum ada peringkat
- Memoria PFC Jokin AginagaDokumen89 halamanMemoria PFC Jokin AginagaLuis Fernando Coronel GonzalezBelum ada peringkat
- Requisitos para Pruebas de PESDokumen30 halamanRequisitos para Pruebas de PESOperaciones YJJBelum ada peringkat
- Nivel de FermiDokumen4 halamanNivel de FermiFerzz MontejoBelum ada peringkat
- Importancia de La Estructura de La Materia Responsabilidad SocialDokumen2 halamanImportancia de La Estructura de La Materia Responsabilidad SocialSebastian XAnder100% (3)
- Máquinas Simples: FísicaDokumen11 halamanMáquinas Simples: Física507profesorBelum ada peringkat
- Apuntes de Fisica II 2015Dokumen155 halamanApuntes de Fisica II 2015Manuel Lopez BañuelosBelum ada peringkat
- Puede Un Material Aislante Convertirse en Un ConductorDokumen4 halamanPuede Un Material Aislante Convertirse en Un ConductorJhonAlex GuarinBelum ada peringkat
- Eda 2023 - ModeloDokumen17 halamanEda 2023 - ModeloJorge Armando Quiroz CabadaBelum ada peringkat
- Cuadernillo Del 3er Periodo. FÍSICA. MIRIAMDokumen35 halamanCuadernillo Del 3er Periodo. FÍSICA. MIRIAMMìriam Alejandra Lázaro ChanBelum ada peringkat
- Parcial de Vectores 2019Dokumen9 halamanParcial de Vectores 2019Alejandra FernandezBelum ada peringkat
- Aplicaciones Movimiento AceleradoDokumen2 halamanAplicaciones Movimiento AceleradoLuis Eduardo Quintana RinconBelum ada peringkat
- Balance de Energía para Sistemas No ReaccionantesDokumen45 halamanBalance de Energía para Sistemas No ReaccionantesronaldBelum ada peringkat
- 2º ESO Act ExamenDokumen7 halaman2º ESO Act Examengolimo81100% (1)
- Manuel Bravo Tarea2 TermodinamicaDokumen7 halamanManuel Bravo Tarea2 TermodinamicaAgustínA.GalloMurga86% (7)
- Sensor Corriente PDFDokumen3 halamanSensor Corriente PDFFausto Wladimir Yanez ArevaloBelum ada peringkat
- ElectronegatividadDokumen2 halamanElectronegatividadMelissa HuertaBelum ada peringkat
- Martinez Galvan Nelida M19S2Al4Dokumen5 halamanMartinez Galvan Nelida M19S2Al4Javi Yanko100% (1)
- Unidad 1 Leyes Del Campo Electromagnético en El Espacio LibreDokumen43 halamanUnidad 1 Leyes Del Campo Electromagnético en El Espacio LibreJikary JimenezBelum ada peringkat
- PMYACIM Flujo de Fluidos Hacia PozosDokumen42 halamanPMYACIM Flujo de Fluidos Hacia PozosOrtizz OrtizBelum ada peringkat
- Agrotecnicahuaco Quintoaño Fisica Tec Guia3 PDFDokumen5 halamanAgrotecnicahuaco Quintoaño Fisica Tec Guia3 PDFYesenia Camargo morenoBelum ada peringkat
- Efecto Corana y SkinDokumen1 halamanEfecto Corana y SkinMemo Romero HernandezBelum ada peringkat
- Tarea No 2 de Presas de Tierra EXPLORACIONDokumen34 halamanTarea No 2 de Presas de Tierra EXPLORACIONJluis IpnBelum ada peringkat
- Solucionario Welty 4 Edicion PDFDokumen322 halamanSolucionario Welty 4 Edicion PDFCarmenAravenaGonzalezBelum ada peringkat
- James Clerk MaxwellDokumen3 halamanJames Clerk MaxwellHector CaryBelum ada peringkat
- Ejercicios Ley de FourierDokumen5 halamanEjercicios Ley de FourierJose Sarmiento50% (2)
- Actitud FilosóficaDokumen8 halamanActitud FilosóficaElizabeth ValladaresBelum ada peringkat
- Taller Sobre Las Leyes de Newton Fisica BasicaDokumen4 halamanTaller Sobre Las Leyes de Newton Fisica BasicaBIANCA LINETTE DE LA ROSA REYESBelum ada peringkat