Trabajo de Entrenamiento Practico Quimica
Diunggah oleh
dflcrHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Trabajo de Entrenamiento Practico Quimica
Diunggah oleh
dflcrHak Cipta:
Format Tersedia
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
ESCUELA DE CIENCIAS BASICAS TECNOLOGAS E INGENIERIAS
E.C.B.T.I.
Unidad de Ciencias Bsicas
201102 Qumica General
TRABAJO DE ENTRENAMIENTO PRACTICO UNIDAD 2
A. LEY DE BOYLE
B. SOLUCIONES
Francisco Javier Giraldo Rojas
Director
BOGOTA
JUNIO de 2015
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
Este trabajo est diseado para entregarse en este foro de forma
individual, para lo cual cada estudiante que entre al foro tomara
los tems de acuerdo al orden de aparicin en el foro.
Orden de aparicin en
el foro
Estudiante 1
tem a desarrollar
Estudiante 2
Estudiante 3
Estudiante 4
Estudiante 5
Ejemplo:
Entra el estudiante Juan primero y despus Alicia.
Entonces Juan desarrolla los tems 1A, 2A, 3A.....
Alicia desarrolla los tems 1B, 2B, 3B.....
A. LEY
DE
BOYLE
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
DESCRIPCIN DEL TRABAJO
Temticas
Intencionalidades
formativas
Ley de Boyle
PROPSITO
Comprobar leyes de los gases
OBJETIVO GENERAL
Observar la relacin que hay entre el volumen y la presin
a una temperatura constante.
METAS
Que el estudiante compruebe experimentalmente la
relacin de proporcionalidad directa entre el Volumen y la
presin.
COMPETENCIAS
Qu el estudiante adquiera habilidad de observacin,
anlisis y deduccin.
Fundamentacin Terica
A temperatura constante (T), el volumen (V) de una masa fija de un gas es
inversamente proporcional a la presin (P).
Para ver esta pelcula, debe
disponer de QuickTime y de
un descompresor .
Las ecuaciones anteriores significan que cuando la presin se duplica el volumen
se reduce a la mitad, si la presin se triplica el volumen se reduce a la tercera
parte; y si la presin, se reduce a la mitad el volumen se duplica, etc.
Descripcin de la practica
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
Se revisara pginas web donde se evidencie la relacin entre el volumen y la presin.
GENERALIDADES
Pasos generales para resolver problemas de gases:
Paso 1. Identificar las variables y tabularlas.
Paso 2. Convierta a las unidades apropiadas, ejemplo, para clculos de leyes de
los gases la temperatura debe expresarse en Kelvin.
Paso 3. Si una sola ecuacin relaciona las variables dadas por el problema,
despeje aquella cuyo valor se pide calcular.
Paso 4. Realice los clculos y siga las unidades durante todo el proceso, lo que
permite comprobar que se ha resuelto la ecuacin correctamente.
Si se opta por el mtodo analtico, 1. Se identifican las relaciones de
proporcionalidad entre las variables cuyo valor se pide calcular, con las dems del
sistema. 2. Se plantea la relacin de volumenes, presiones, o temperaturas
correspondientes 3. Se efectuan los clculos.
OBJETIVOS
1.
Observar el efecto del aumento de la presin sobre el
volumen de un gas confinado en un recipiente.
2.
Deducir la relacin grfica de la presin
partir de los datos obtenidos.
volumen a
PROCEDIMIENTO
Entrar al siguiente link y registrar en las siguientes tablas los
valores de presin y volumen para una temperatura
constante. (La temperatura se modifica en la parte de debajo
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
de la jeringa) Tabla No 1, 2 y 3 y luego representarlo en una
grafica Volumen vs. Presin.
http://www.iesalandalus.com/joomla3/images/stories/FisicayQuimica/flash/fq3es
o/mov_gas_tcm.swf
1A. Temperatura Kte:
1B. Temperatura Kte:
1C. Temperatura Kte:
1D. Temperatura Kte:
1E. Temperatura Kte:
245 C
250C
290 C
330 C
350 C
Tabla No 1.
3
Volumen(cm
)
Presin
(atmsferas)
Presin
(mmHg)
15,14
11506,4
10
5,27
4005,2
15
3,51
2667,6
20
2,62
1991,2
25
2,1
1596
30
1,75
1330
35
1,5
1440
40
1,31
995,6
Para una muestra de Helio registrar los cambios de presin
variando el volumen, como muestra la siguiente figura en el
link. Representarlo en una grafica Volumen vs. Presin.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
http://content.blackgold.ca/ict/Division4/Science/Div.%204/Boyles
%20Law/boyleslaw.htm
2A AIRE
2B OXIGENO
2C HIDROGENO
2D HELIO
2E GRAFICA AIRE (Volumen vs. Presin en atmsferas)
Tabla No 4.
Presin
(atmsferas)
Presin
(mmHg)
5,001378
3801,047
28
4,01471
3051,179
6
11
3,170942
2409,884
14
2,483678
1887,536
17
2,020965
1535,933
4
20
1,735172
1318,730
7
23
1,5140227
1150,65
Volumen(ml)
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
B. SOLUCIONES
DESCRIPCIN DEL TRABAJO
Temticas
Preparar soluciones de diferentes concentraciones
PROPSITO
Familiarizarse con la preparacin de soluciones de diferentes
concentraciones
OBJETIVO GENERAL
Aprender a calcular y preparar soluciones y diluciones de
diferentes concentraciones
METAS
Que el estudiante comprenda las diferentes formas de
expresar las concentraciones y cmo calcularlas.
COMPETENCIAS
Adquirir destreza en el manejo de materiales volumetricos
del laboratorio para la preparacin de diferentes soluciones.
Adquirir habilidad de deduccin para comprender la diferncia
entre las formas de expresar las concentraciones.
Fundamentacin Terica
Las soluciones son mezclas homogneas de dos o ms componentes. El ser
homogneas significa que las propiedades fsicas y qumicas son iguales en cualquier
parte de la solucin. Adems, cuando se observa una solucin a simple vista solo se
distingue una fase, sea lquida, slida o gaseosa.
Los componentes de la solucin se denominan soluto y solvente. Soluto es el
componente que se disuelve. Solvente es el componente en el cual el soluto se disuelve.
Distinguir en una solucin, cual es el soluto y el solvente, a veces se dificulta. Por regla
general, el solvente es el componente cuyo estado de la materia es igual al de la solucin
final. Por ejemplo, si mezclamos slidos y lquidos y la solucin resultante es slida,
entonces el solvente es el slido. Cuando los componentes se encuentran en el mismo
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
estado de la materia, el solvente ser el que se encuentra en mayor proporcin.
Las unidades de concentracin expresan la relacin de las cantidades de soluto y
solvente que se tomaron para preparar la solucin. Las principales unidades de
concentracin son: porcentaje en peso (o porcentaje en masa) % w/w; porcentaje en
volumen, % v/v; porcentaje peso volumen; % p/v; concentracin molar o molaridad (M);
concentracin molal o molalidad (m) y concentracin normal o normalidad (N).
OBJETIVOS
Identificar los componentes de una mezcla.
Preparar soluciones de diferentes concentraciones.
PROCEDIMIENTO
PARTE A.
Realizar los clculos para preparar las siguientes soluciones.
3A Preparar 500 mL de disolucin 0.4 M de cloruro de potasio (KCl) en agua.
3B Preparar 500 mL de disolucin de hidrxido de potasio (KOH) en agua al
9%m/v, suponiendo que la densidad de la disolucin es prcticamente la del
agua pura (1,0g/mL).
3C Preparar 400 mL de disolucin 2 N de carbonato de sodio (Na 2CO3) en agua.
3D Preparar 400 cm3 de disolucin 1 N de cido sulfurico (H 2SO4) a partir de cido
sulfurico comercial (98% p/p y densidad = 1,84g/mL)
3E Preparar 300 cm3 de una disolucin 0.3 M de cido clorhdrico (HCl) a partir de
cido clorhdrico comercial (36% p/p y densidad 1,18 g/mL).
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
ESCUELA DE CIENCIAS BASICAS TECNOLOGAS E INGENIERIAS
E.C.B.T.I.
Unidad de Ciencias Bsicas
201102 Qumica General
TRABAJO DE ENTRENAMIENTO PRACTICO UNIDAD 2
A. LEY DE BOYLE
B. SOLUCIONES
Francisco Javier Giraldo Rojas
Director
BOGOTA
JUNIO de 2015
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
Este trabajo est diseado para entregarse en este foro de forma
individual, para lo cual cada estudiante que entre al foro tomara
los tems de acuerdo al orden de aparicin en el foro.
Orden de aparicin en
el foro
Estudiante 1
tem a desarrollar
Estudiante 2
Estudiante 3
Estudiante 4
Estudiante 5
Ejemplo:
Entra el estudiante Juan primero y despus Alicia.
Entonces Juan desarrolla los tems 1A, 2A, 3A.....
Alicia desarrolla los tems 1B, 2B, 3B.....
A. LEY
DE
BOYLE
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
DESCRIPCIN DEL TRABAJO
Temticas
Intencionalidades
formativas
Ley de Boyle
PROPSITO
Comprobar leyes de los gases
OBJETIVO GENERAL
Observar la relacin que hay entre el volumen y la presin
a una temperatura constante.
METAS
Que el estudiante compruebe experimentalmente la
relacin de proporcionalidad directa entre el Volumen y la
presin.
COMPETENCIAS
Qu el estudiante adquiera habilidad de observacin,
anlisis y deduccin.
Fundamentacin Terica
A temperatura constante (T), el volumen (V) de una masa fija de un gas es
inversamente proporcional a la presin (P).
Para ver esta pelcula, debe
disponer de QuickTime y de
un descompresor .
Las ecuaciones anteriores significan que cuando la presin se duplica el volumen
se reduce a la mitad, si la presin se triplica el volumen se reduce a la tercera
parte; y si la presin, se reduce a la mitad el volumen se duplica, etc.
Descripcin de la practica
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
Se revisara pginas web donde se evidencie la relacin entre el volumen y la presin.
GENERALIDADES
Pasos generales para resolver problemas de gases:
Paso 1. Identificar las variables y tabularlas.
Paso 2. Convierta a las unidades apropiadas, ejemplo, para clculos de leyes de
los gases la temperatura debe expresarse en Kelvin.
Paso 3. Si una sola ecuacin relaciona las variables dadas por el problema,
despeje aquella cuyo valor se pide calcular.
Paso 4. Realice los clculos y siga las unidades durante todo el proceso, lo que
permite comprobar que se ha resuelto la ecuacin correctamente.
Si se opta por el mtodo analtico, 1. Se identifican las relaciones de
proporcionalidad entre las variables cuyo valor se pide calcular, con las dems del
sistema. 2. Se plantea la relacin de volumenes, presiones, o temperaturas
correspondientes 3. Se efectuan los clculos.
OBJETIVOS
3.
Observar el efecto del aumento de la presin sobre el
volumen de un gas confinado en un recipiente.
4.
Deducir la relacin grfica de la presin
partir de los datos obtenidos.
volumen a
PROCEDIMIENTO
Entrar al siguiente link y registrar en las siguientes tablas los
valores de presin y volumen para una temperatura
constante. (La temperatura se modifica en la parte de debajo
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
de la jeringa) Tabla No 1, 2 y 3 y luego representarlo en una
grafica Volumen vs. Presin.
http://www.iesalandalus.com/joomla3/images/stories/FisicayQuimica/flash/fq3es
o/mov_gas_tcm.swf
1A. Temperatura Kte:
1B. Temperatura Kte:
1C. Temperatura Kte:
1D. Temperatura Kte:
1E. Temperatura Kte:
245 C
250C
290 C
330 C
350 C
Tabla No 1.
3
Volumen(cm
)
Presin
(atmsferas)
Presin
(mmHg)
15,14
11506,4
10
5,27
4005,2
15
3,51
2667,6
20
2,62
1991,2
25
2,1
1596
30
1,75
1330
35
1,5
1440
40
1,31
995,6
Para una muestra de Helio registrar los cambios de presin
variando el volumen, como muestra la siguiente figura en el
link. Representarlo en una grafica Volumen vs. Presin.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
http://content.blackgold.ca/ict/Division4/Science/Div.%204/Boyles
%20Law/boyleslaw.htm
2A AIRE
2B OXIGENO
2C HIDROGENO
2D HELIO
2E GRAFICA AIRE (Volumen vs. Presin en atmsferas)
Tabla No 4.
Presin
(atmsferas)
Presin
(mmHg)
5,001378
3801,047
28
4,01471
3051,179
6
11
3,170942
2409,884
14
2,483678
1887,536
17
2,020965
1535,933
4
20
1,735172
1318,730
7
23
1,5140227
1150,65
Volumen(ml)
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
B. SOLUCIONES
DESCRIPCIN DEL TRABAJO
Temticas
Preparar soluciones de diferentes concentraciones
PROPSITO
Familiarizarse con la preparacin de soluciones de diferentes
concentraciones
OBJETIVO GENERAL
Aprender a calcular y preparar soluciones y diluciones de
diferentes concentraciones
METAS
Que el estudiante comprenda las diferentes formas de
expresar las concentraciones y cmo calcularlas.
COMPETENCIAS
Adquirir destreza en el manejo de materiales volumetricos
del laboratorio para la preparacin de diferentes soluciones.
Adquirir habilidad de deduccin para comprender la diferncia
entre las formas de expresar las concentraciones.
Fundamentacin Terica
Las soluciones son mezclas homogneas de dos o ms componentes. El ser
homogneas significa que las propiedades fsicas y qumicas son iguales en cualquier
parte de la solucin. Adems, cuando se observa una solucin a simple vista solo se
distingue una fase, sea lquida, slida o gaseosa.
Los componentes de la solucin se denominan soluto y solvente. Soluto es el
componente que se disuelve. Solvente es el componente en el cual el soluto se disuelve.
Distinguir en una solucin, cual es el soluto y el solvente, a veces se dificulta. Por regla
general, el solvente es el componente cuyo estado de la materia es igual al de la solucin
final. Por ejemplo, si mezclamos slidos y lquidos y la solucin resultante es slida,
entonces el solvente es el slido. Cuando los componentes se encuentran en el mismo
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
ESCUELA DE CIENCIAS BASICAS TECNOLOGIAS E INGENIERIAS
Trabajo Entrenamiento Practico Unidad 2. 201102 Qumica General
estado de la materia, el solvente ser el que se encuentra en mayor proporcin.
Las unidades de concentracin expresan la relacin de las cantidades de soluto y
solvente que se tomaron para preparar la solucin. Las principales unidades de
concentracin son: porcentaje en peso (o porcentaje en masa) % w/w; porcentaje en
volumen, % v/v; porcentaje peso volumen; % p/v; concentracin molar o molaridad (M);
concentracin molal o molalidad (m) y concentracin normal o normalidad (N).
OBJETIVOS
Identificar los componentes de una mezcla.
Preparar soluciones de diferentes concentraciones.
PROCEDIMIENTO
PARTE A.
Realizar los clculos para preparar las siguientes soluciones.
3A Preparar 500 mL de disolucin 0.4 M de cloruro de potasio (KCl) en agua.
3B Preparar 500 mL de disolucin de hidrxido de potasio (KOH) en agua al
9%m/v, suponiendo que la densidad de la disolucin es prcticamente la del
agua pura (1,0g/mL).
3C Preparar 400 mL de disolucin 2 N de carbonato de sodio (Na 2CO3) en agua.
3D Preparar 400 cm3 de disolucin 1 N de cido sulfurico (H 2SO4) a partir de cido
sulfurico comercial (98% p/p y densidad = 1,84g/mL)
3E Preparar 300 cm3 de una disolucin 0.3 M de cido clorhdrico (HCl) a partir de
cido clorhdrico comercial (36% p/p y densidad 1,18 g/mL).
Anda mungkin juga menyukai
- Caracterizacion Subproceso Colocar TiraDokumen7 halamanCaracterizacion Subproceso Colocar TiradflcrBelum ada peringkat
- Turbin ADokumen78 halamanTurbin AdflcrBelum ada peringkat
- Caracterizacion Subproceso Colocar TiraDokumen7 halamanCaracterizacion Subproceso Colocar TiradflcrBelum ada peringkat
- Caracterizacion Subproceso Colocar VarillasDokumen8 halamanCaracterizacion Subproceso Colocar VarillasdflcrBelum ada peringkat
- D 2ggfhgDokumen19 halamanD 2ggfhgdflcrBelum ada peringkat
- Turb 4654Dokumen61 halamanTurb 4654dflcrBelum ada peringkat
- Trabajo Colaborativ564654Dokumen22 halamanTrabajo Colaborativ564654dflcrBelum ada peringkat
- Trabajo Colaborativ564654Dokumen22 halamanTrabajo Colaborativ564654dflcrBelum ada peringkat
- Trabajo Colaborativ564654Dokumen22 halamanTrabajo Colaborativ564654dflcrBelum ada peringkat
- Turb I 89745645Dokumen54 halamanTurb I 89745645dflcrBelum ada peringkat
- Aporte Individual Termodinamica CALDERADokumen21 halamanAporte Individual Termodinamica CALDERAdflcrBelum ada peringkat
- Decreto-Ley 1295 de 1994Dokumen17 halamanDecreto-Ley 1295 de 1994dflcrBelum ada peringkat
- Trabajo Colaborativ564654Dokumen22 halamanTrabajo Colaborativ564654dflcrBelum ada peringkat
- Aporte Individual Termodinamica CALDERADokumen21 halamanAporte Individual Termodinamica CALDERAdflcrBelum ada peringkat
- Turb 4654Dokumen61 halamanTurb 4654dflcrBelum ada peringkat
- Turbina 4654654Dokumen70 halamanTurbina 4654654dflcrBelum ada peringkat
- PQ1Dokumen42 halamanPQ1dflcrBelum ada peringkat
- Decreto-Ley 1295 de 1994Dokumen17 halamanDecreto-Ley 1295 de 1994dflcrBelum ada peringkat
- Metoinve 1Dokumen25 halamanMetoinve 1dflcrBelum ada peringkat
- Definición Del Problema - 89Dokumen29 halamanDefinición Del Problema - 89dflcrBelum ada peringkat
- KHJKJHKJDokumen15 halamanKHJKJHKJdflcrBelum ada peringkat
- D 2140 00Dokumen21 halamanD 2140 00dflcrBelum ada peringkat
- Guia 8 Modulo 1 To HaveDokumen15 halamanGuia 8 Modulo 1 To HavedflcrBelum ada peringkat
- Guia 20 - 892545Dokumen9 halamanGuia 20 - 892545dflcrBelum ada peringkat
- 49 Trabajo Fase 2Dokumen14 halaman49 Trabajo Fase 2dflcrBelum ada peringkat
- Tracol 1 Proc de ManufacturaDokumen11 halamanTracol 1 Proc de ManufacturadflcrBelum ada peringkat
- Aporte Actividad 2 UnadDokumen20 halamanAporte Actividad 2 UnaddflcrBelum ada peringkat
- TC2 Dise TC2 DiseDokumen19 halamanTC2 Dise TC2 DisedflcrBelum ada peringkat
- Aporte Actividad 2 UnadDokumen20 halamanAporte Actividad 2 UnaddflcrBelum ada peringkat
- Modelo Plan - ContigenciaDokumen14 halamanModelo Plan - ContigenciaGiselBelum ada peringkat
- Reporte 2Dokumen18 halamanReporte 2braaaaaaanBelum ada peringkat
- 1 3 1 Semana 3 y 4 Manejo Seguro y Manipulacion Del Sistema de Alta TensionDokumen42 halaman1 3 1 Semana 3 y 4 Manejo Seguro y Manipulacion Del Sistema de Alta TensionGonzalo ContrerasBelum ada peringkat
- Campo TacoboDokumen5 halamanCampo TacoboJavier AquinoBelum ada peringkat
- HDS Primacore MW-71Dokumen24 halamanHDS Primacore MW-71JoseBelum ada peringkat
- Atencion Integral Al Individuo y FamiliaDokumen12 halamanAtencion Integral Al Individuo y FamiliaMarycela OsorioBelum ada peringkat
- El OlfatoDokumen2 halamanEl Olfatoyurainis Diaz AldanaBelum ada peringkat
- Nomeclatura TradicionalDokumen13 halamanNomeclatura TradicionalWilma CandelarioBelum ada peringkat
- PDF Estabilidad de Cuerpos SumergidosDokumen17 halamanPDF Estabilidad de Cuerpos SumergidosJuan Carlos Chuquilin Zamora100% (1)
- Monitoreo Fetal PresentacionDokumen18 halamanMonitoreo Fetal PresentacionClaudia Mercedes Alonso CuevasBelum ada peringkat
- 10 posiciones sexuales para el orgasmo femeninoDokumen7 halaman10 posiciones sexuales para el orgasmo femeninoHeriberto Mercedes0% (1)
- Inventario sustancias químicasDokumen49 halamanInventario sustancias químicasNicolas MonteroBelum ada peringkat
- Funcion de ReproduccionDokumen3 halamanFuncion de ReproduccionYosuni RamosBelum ada peringkat
- E.Coli (NMP)Dokumen1 halamanE.Coli (NMP)Carlos FerrufinoBelum ada peringkat
- 2 Bases-Acetatos Balanceo Raciones-Dr TrujilloDokumen126 halaman2 Bases-Acetatos Balanceo Raciones-Dr TrujilloWendy Machado100% (1)
- Endulzamiento de GasDokumen10 halamanEndulzamiento de GasJobita JMBelum ada peringkat
- Evaluación Tec. en Parvulo Bases Biológicas.Dokumen3 halamanEvaluación Tec. en Parvulo Bases Biológicas.Héctor Morales PonceBelum ada peringkat
- Tamizaje Terapia y FonologíaDokumen27 halamanTamizaje Terapia y FonologíaStef Paez100% (1)
- Esofagitis CausticasDokumen9 halamanEsofagitis CausticasmeryBelum ada peringkat
- Contactos Lesbianas Masajistas en MadridDokumen2 halamanContactos Lesbianas Masajistas en MadridEroticoBelum ada peringkat
- Diagnostico AmbientalDokumen10 halamanDiagnostico AmbientalRolando MorenteBelum ada peringkat
- Plan de Contingencia y Respuesta A EmergenciasDokumen13 halamanPlan de Contingencia y Respuesta A EmergenciasCarlos Alberto Cordova HerrnandezBelum ada peringkat
- Análisis de Los Aspectos Socioculturales y Familiares de La Violencia Contra La Persona Mayor en El Barrio Macunaima de VillavicencioDokumen53 halamanAnálisis de Los Aspectos Socioculturales y Familiares de La Violencia Contra La Persona Mayor en El Barrio Macunaima de VillavicencioKARLA JOHANA CHAVEZ ROJASBelum ada peringkat
- Gestión de Riesgos en Seguridad y Salud OcupacionalDokumen5 halamanGestión de Riesgos en Seguridad y Salud OcupacionalDani Novoa VegaBelum ada peringkat
- NTON 03 091 - 11 Norma Tecnica. Fortificación Del ArrozDokumen7 halamanNTON 03 091 - 11 Norma Tecnica. Fortificación Del ArrozSintia Elizabeth Saldaña CuzcoBelum ada peringkat
- Protocolo de Prevencion de Las Presiones AtmosfericasDokumen15 halamanProtocolo de Prevencion de Las Presiones AtmosfericasBeLLanira Trujillo ScarpettaBelum ada peringkat
- Valoracion MuscularDokumen3 halamanValoracion MuscularAngel Guerra GuzmanBelum ada peringkat
- PLAN DE RESIDUOS SOLIDOS - SUCCHA - 2020 - vr3Dokumen28 halamanPLAN DE RESIDUOS SOLIDOS - SUCCHA - 2020 - vr3Billy Chamana Aylas50% (2)
- Instructivo Ficha Notificación SivimDokumen10 halamanInstructivo Ficha Notificación SivimLeonardo SuarezBelum ada peringkat
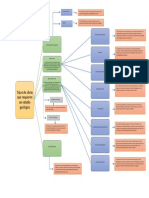
- Obras que requieren estudio geológicoDokumen1 halamanObras que requieren estudio geológicorodrigo0% (1)