Sumur X-1
Diunggah oleh
Dhana Jaya WardanaDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Sumur X-1
Diunggah oleh
Dhana Jaya WardanaHak Cipta:
Format Tersedia
23
Bab III
TINJAUAN PUSTAKA
Penurunan produksi pada Sumur X-1 diakibatkan karena adanya kerusakan
pada lubang sumur. Kerusakan pada lubang sumur tersebut umumnya ditunjukkan
oleh adanya penurunan laju produksi. Penyebab terjadinya kerusakan pada lubang
sumur ini diakibatkan terbentuknya scale. Scaling yang terbentuk pada sumur uap
diakibatkan karena terjadi penurunan tekanan. Sehingga fasa uap mengalami
kondensasi dan terbentuk scaling.
Salah satu cara yang dapat digunakan untuk memperbaiki kerusakan pada
lubang sumur tersebut yaitu dengan melakukan pengasaman. Ada tiga metode
penggunaan pengasaman yaitu matrix acidizing, acid fraturing, dan acid wash. Pada
skripsi ini metode acid wash yang digunakan.
3.1. Dasar Dilakukan Acid Wash
Pada lapangan Wayang Windu scaling yang terbentuk terdapat pada sumur
dominasi uap. Hal tersebut terjadi dikarenakan besarnya penurunan tekanan pada
sumur tersebut. Di daerah MBA penurunan tekanan mencapai 3.7% per tahunnya
yang ditunjukkan pada Gambar 3.1.
Untuk melakukan acidizing diperlukan suatu parameter untuk menentukan
pemilihan atau kandidat sumur. Adapun parameter yang menjadikan suatu sumur
bermasalah :
Penurunan tekanan yang besar ditunjukkan pada
Penurunan produksi lebih dari 17%
Pembuktian terjadinya scaling
Adanya pendangkalan pada lubang sumur ketikan melakukan uji kuster (PTS)
24
Gambar 3.1. Tekanan Reservoir di MBA-Pad6
3.2. Identifikasi Masalah
3.2.1. Kerusakan Pada Lubang Bor
Kerusakan pada lubang bor diakibatkan karena terbentuknya scaling pada
Sumur X-1. Dampak dari terbentuknya scaling ini yang menyebabkan berkurangnya
suplai aliran fluida panas bumi dari dasar sumur menuju permukaan yang
mengakibatkan berkurangya pasokan produksi uap ke turbin sehingga menyebabkan
penurunan produksi. Untuk mengetahui jenis sacling yang terbentuk pada lubang
sumur diperlukan penanganan sepert analisa fluida kimia untuk mengetahui
menentukan jenis anion dan kation. Pada umumnya ada 3 jenis air pada panas bumi
yaitu chloride (Cl), sulfat (SO4), dan bikarbonat (HCO3). Pada Gambar 3.2 diagram
segitiga Giggenbach menunjukkan jenis air fluida panas bumi.
25
Gambar 3.2. Diagram Segitiga Cl-SO4-HCO3
(Giggenbach, 1988 dalam Keith Nicholson, 1993)14
Scale terbentuk dari endapan mineral pada bidang permukaan yang
bersentuhan dengan air formasi yang memiliki tingkat pengendapan yang tinggi.
Scale terbentuk jika air mengandung ion-ion membentuk komponen yang tingkat
kelarutannya terbatas dan jika ada perubahan fisis maupun kimia akan menurunkan
kelarutannya dibawah konsentrasi. Adapun faktor penyebab terbentuknya endapan
scale antara lain adalah :
1. Komposisi Kimia Batuan Reservoir
Kebanyakan batuan reservoir (batuan beku) terdiri dari mineral, atau sedikit
sekali gelass yang biasa ada, tersusun dari Si, Al, Fe, Mg, Ca, Na, dan K bersama
sejumlah kecil Ti, Mn dan P. Elemen-elemen tersebut didampingi oleh oksigen dan
sekumpulan analisa batuan dinyatakan dalam bentuk komponen oksida (SiO2. Al2O3,
dan lain-lain). SiO2 merupakan komponen yang banyak sekali pada batuan beku,
berkisar antara 35 75 %.
26
2. Komposisi Kimia Fluida Reservoir
Kalsium karbonat dan silika adalah kandungan yang dominan dari scale yang
merupakan endapan dari fluida reservoir panasbumi. Kalsium karbonat biasanya
ditemukan sebagai endapan dari kalsit, disamping material lainnya, seperti silika dan
hidroksida yang mungkin terendapkan bersama. Karena kation-kation yang terbentuk
dari hidroksida tidak mudah diuraikan seperti besi atau magnesium, sehingga bisa
terendapkan bersama kalsium karbonat. Silika merupakan endapan tersendiri
berbentuk silika amorf, atau dengan kation-kation lain dalam bentuk kationik silika
seperti besi atau aluminium silika.
3. Kondisi Tekanan
Dalam reaksi kesetimbangan suatu larutan kimia, tekanan sedikit banyak
berpengaruh didalamnya. Kelarutan unsur kimia fluida panasbumi akan semakin
besar dengan kenaikan tekanan, sehingga semakin kecil kecenderungan untuk
terbentuknya scale.
Kondisi tekanan yang diasumsikan sebagai fungsi kecepatan dalam pipa, akan
didapatkan bahwa semakin kecil kecepatan aliran didalam pipa maka proses
terjadinya scale akan semakin meningkat, tetapi tidak sebaliknya. Kondisi tekanan
yang diasumsikan sebagai fungsi kecepatan dalam pipa dipengaruhi oleh pola aliran
fluida dalam pipa. Pembentukan scale cenderung lebih besar pada aliran turbulen
daripada aliran laminer.
4. Kondisi Temperatur
Kecenderungan terbentuknya scale meningkat dengan kanaikan temperatur
karena menaikkan kelarutan senyawa dalam air. Tetapi pada kenyataannya kondisi
temperatur tidak mutlak berbanding lurus dengan laju pembentukan scale. Sebagai
contoh dua macam scale yang umumnya terdapat pada fasilitas peralatan panasbumi
yaitu kalsium karbonat dan silika kalsium karbonat, yang terendapkan pada
permukaan yang panas, sebab kelarutan menurun dengan meningkatnya temperatur.
27
Dilain pihak, silika akan terendapkan pada peremukaan yang dingin karena kelarutan
silika menurun sesuai penurunan temperatur.
3.2.2. Jenis Scaling Yang Terbentuk
Untuk mengetahui jenis scaling yang terbentuk maka diperlukan analisa fluida
kimia pada sumur. Analisa fluida kimia sangat dibutuhkan karena dari analisa
tersebut dapat diketahui unsur anion dan kation. Pada Tabel 3.1 dan diagram
Gambar 3.3 menunjukkan jenis anion dan kation serta jenis air yang dominan dalam
pembentukan scaling calsite pada sumur uap. Unsur kation HCO3 lah yang lebih
dominan.
Tabel 3.1. Jenis Anion dan Kation
Pada Sumur X-16
Anion
Konsentrasi
Kation
Konsentrasi
Cl-
31.04
Na+
14700
HCO3-
227.62
K+
3370
Sio2-
172
Ca++
1200
SO4-
171.2
Mg++
0.549
NH4-
939
F-
As+++
Li+
Fe++ (Besi Total)
0.57
Unsur pembentuk scaling
Unsur berbahaya
28
Gambar 3.3. Diagram Bar Dari Nilai Bikarbonat
Pada Sumur Uap6
Pada Gambar 3.3 diagram bar menunjukkan bahwa pada sumur X-1 jenis air
bikarbonatlah yang paling dominan. Pada Bab II telah menjelaskan bawah Sumur uap
bagian utara Wayang Windu berada pada zona altrasi calsite Sehingga
memungkinkan untuk terbentuknya scaling berjenis calsite.
3.2.2.1. Scale Kalsium Karbonat (CaCO3)
Kalsium karbonat ini terdiri dari 2 unsur kalsium dan 1 unsur karbon dan 3
unsur oksigen. Setiap unsur karbon terikat kuat dengan 3 oksigen, dan ikatan ini
ikatannya lebih longgar dari ikatan antara karbon dengan kalsium pada satu senyawa.
Scale kalsium karbonat ini terbentuk dari reaksi antara ion Ca2+ dan CO32- atau HCO3, seperti terlihat pada Gambar 3.4 menunjukkan proses reaksi kimia terbentuknya
scaling pada sumur uap.
29
Gambar 3.4. Proses Reaksi Kimia Terbentuknya
Scaling Pada Sumur Uap X-16
Selama konsentrasi CO2 dalam larutan bertambah, reaksi bergeser ke kiri,
sehingga endapan CaCO3 lebih sedikit. Sebaliknya jika CO2 keluar dari larutan atau
tekanan partial CO2 berkurang dan pH air meningkat reaksi bergerak ke kanan yang
menyebabkan pengendapan CaCO3. Air akan semakan asam dengan bertambahnya
CO2 didalam air.
Gambar 3.5. Pengaruh Tekanan Partial CO2 Pada
Kelarutan CaCO39
30
Gambar 3.5 menunjukkan pengaruh tekanan partial CO2 dalam air murni.
Data ini menggambarkan bahwa kelarutan CaCO3 bertambah akibat dari
bertambahnya tekanan partial CO2. Pengaruhnya akan berkurang dengan naiknya
temperatur. Jumlah CO2 yang ada didalam air mempengaruhi kelarutan CaCO3. Tidak
adanya CO2 menyebabkan air makin basa, jika pH semakin besar, maka makin
banyak kemungkinan CaCO3 mengendap. Sebaliknya semakin rendah pH, semakin
sedikit kemungkinan pengendapan scale terjadi.
Pada Gambar 3.6 menunjukkan diagram niali pH pada Sumur X-1 memiliki
nilai pH diatas 5. Karena sumur-sumur dominasi uap yang berada di Wayang Windu
mayoritas nilia pH nya masih menunjukkan nilai dibawah 5 sehingga diambil batasan
bahwa untuk nilai pH diatas 5.
Gambar 3.6. Diagram Bar Dari Nilai pH
Pada Sumur Uap6
31
Kelarutan CaCO3 akan berkurang dengan bertambahnya temperatur, sehingga
semakin tinggi temperatur air, maka scale CaCO3 akan terbentuk ditunjukkan pada
Gambar 3.7.
Gambar 3.7. Pengaruh Temperatur Terhadap Kelarutan
CaCO3 Dalam Air Murni Pada Tekanan Partial CO2 Satu Bar9
3.2.3. Metode Perhitungan Kelarutan Stiff and Davis
Larsen-Bushwell dan Stiff-Davis telah mengembangkan metode Langier
sehingga dapat digunakan untuk air garam, yaitu dengan cara memasukkan parameter
kekuatan ion (ionic strength,), sebagai koreksi terhadap total konsentrasi garam dan
temperatur. Adapun
persamaan yang digunakan untuk menentukan harga ionic
strength adalah sebagai berikut :
= 0.5 (1 12 + 2 22 + 3 32 + + 1 ).....(3-1)
Keterangan :
C = konsentrasi ion, mol/1000 gram air.
32
Z = valensi ion
Untuk mempermudah perhitungan ionic strength, dapat dibuat tabel faktor
konversi untuk mengkonversikan hasil dari analisis contoh air formasi ke ionic
strength, yang merupakan jumlah dari hasil perkalian antara masing-masing
konsentrasi ion dengan faktor konversi. Besarnya faktor konversi masing-masing
komponen ion dapat dilihat pada Tabel 3.2.
Tabel 3.2. Faktor Konversi Perhitungan Ionic Strength10
Ion
Kosentrasi
PPM
Faktor Koreksi
Me/L
PPM
Me/L
Ion Strenght
Me/L X
Koreksi
Cl-
118.3
2.4 x 10-5
6.0 x 10-4
70.986 x 10-3
SO4-
3.125
2.1 x 10-5
1.0x 10-4
3.125 x 10-3
HCO3-
0.47
0.8 x 10-5
5.0x 10-4
0.235 x 10-3
Ca2+
0.7
3.0 x 10-5
2.0x 10-4
1.4 x 10-3
Mg2+
8.2 x 10-5
1.2x 10-4
8.1 x 10-5
1.5x 10-4
53.565 x 10-3
2.2 x 10-5
2.0 x 10-4
171.1634 x 10-3
Fe2+
1000
35.71
Ba2+
Negatif
Negatif
Na
85.5817
Tenaga ion keseluruhan dari (K) pada temperatur :
0 0C
20 0C = 2.76
40 0C = 1.84
80 0C = 1.32
100 0C = 0.72
= 3.16
33
Diantara pengembangan metode Larshon-Bushwel dan Stiff-Davis tersebut,
metode yang digunakan adalah metode Stiff and Davis. Untuk memperkirakan
kecenderungan pembentukan scale CaCO3, Stiff dan Davis menggunakan harga
indeks stabilitas sistem (stability index,SI), yang besarnya dapat ditentukan dengan
menggunakan LSI. Adapun persamaan sebagai berikut :
LSI = pH pHs....(3-2)
Keterangan :
LSI = Langelier Saturation Index
pH = derajat keasaman sistem
pHs = pH sistem yang terjenuhi dengan CaCO3.
Dengan penentuan pHs berdasarkan persamaan sebagai berikut :
pHs = K pCa pAlk.....(3-3)
sehingga
SI = pH (K pCa pAlk).....(3-4)
Keterangan :
SI = stability index
pH = pH air sebenarnya
K = konstanta yang merupakan fungsi dari komposisi, salinitas dan temperature air.
Harga K ini diperoleh dari Gambar 3.8, yang merupakan grafik antara hubungan
ionic strength dengan temperatur.
34
Sedangkan harga pCa dan pAlk dapat ditentukan dengan persamaan sebagai
berikut :
1
pCa = log (2+/)....(3-5)
atau,
pCa = 4.5977 0.4327 Ln(2+ ).......(3-6)
dan,
1
pAlk = log( /)...(3-7)
atau,
pAlk = 4.8139 0.4375 Ln (32 + 3 )..(3-8)
Besarnya harga K tergantung pada temperatur dan konsentrasi total garam dan
air. Pada kondisi dimana air dalam keadaan setimbang dengan kalsium karbonat,
maka harga K dapat diketahui dengan menentukan pH kalsium dan alkalinitasnya.
Adanya kandungan garam terlarut yang berbeda akan mempengaruhi harga K. Pada
air tawar, pengaruh ini dapat diabaikan, akan tetapi dalam air garam, khususnya air
formasi, pengaruh ini harus diperhitungkan, yaitu dengan memasukkan parameter
ionic strength sebagai koreksi terhadap total konsentrasi garam dan temperatur.
Penentuan harga pCa dan pAlk dapat ditentunkan pada Gambar 3.8.
35
Gambar 3.8. Harga K Pada Berbagai Ionic Strength10
Perkiraan kecenderungan pembentukan scale kalsium carbonat ditentukan
berdasarkan harga SI dengan ketentuan sebagai berikut :
Jika SI < 0 (negatif), maka sistem tidak terjenuhi CaCO3 dan scale cenderung
tidak terbentuk.
Jika SI > 0, maka sistem telah terjenuhi oleh CaCO3 dan terdapat
kecenderungan pengendapan scale.
Jika SI = 0, maka sistem berada pada titik jenuh (saturation point), dan scale
tidak akan terbentuk. Pada kondisi ini adapun persamaan yang digunakan :
pH pCa pAlk K = 0 ....(3-9)
36
sehingga,
K = pH pCa pAlk ........(3-10)
3.2.4. Konstanta Hasil Kelarutan (Ksp)
Jika reaksi asam telah mencapai kesetimbangan, proses pelarutan mineral oleh
asam akan berhenti meskipun masih terdapat molekul asam. Kesetimbangan tercapai
bila aktivitas kimia dari hasil reaksi mengimbangi aktivitas kimia reaktan atau
pereaksi. Definisi umum dari kesetimbangan reaksi dapat diambil dari argumen
thermodinamika, yaitu kesetimbangan akan terjadi bila aktivitas reaksi seimbang
dengan aktivitas reaktannya. Jika terdapat koefesien stoikiometri yang sama maka
terjadi kesetimbangan reaksi yang disebut dengan konstanta kesetimbangan seperti
pada contoh berikut Ksp senyawa Calsium Carbonate:
A+B
C+D
Ca++ + 2HCO3Ksp =
CaCO3 + CO2 + H2O
[ ][]
[][]
...(3-11)
Nilai Ksp berguna untuk menentukan keadaan senyawa ion dalam larutan
yang belum jenuh, tepat jenuh, atau lewat jenuh, yaitu dengan membandingkan hasil
kali ion dengan hasil kali kelarutan (Ksp). Kriterianya adalah :
IAP = Ksp, fluida dalam kondisi saturated (jenuh)
IAP > Ksp, fluida dalam kondisi supersaturated dan pengendapan scaling
kemungkinan terjadi.
IAP < Ksp, fluida dalam kondisi tidak jenuh (undersaturated), maka tidak ada
kemungkinan terjadi pengendapan scaling
37
3.2.5. Terjadinya Pendangkalan Pada Lubang Sumur
Salah satu indikasi terjadinya scaling dibuktikan ketika melakukan uji kuster
(PTS). Dimana saat dilakukan uji kuster (PTS) hanya mampu menembus hingga
kedalaman yang terukur 1167 m dari kedalman sebenarnya 1512 m ditunjukkan pada
Gambar 3.9 dan Gambar 3.10.
Kedalaman (m)
Pressure (bara)
5
25
125
0
200
400
600
800
1000
1200
1400
LD 1 P
LU 1 P
Gambar 3.9. Profil Tekanan Sumur X-1
Kedalaman (meter)
Temperatur (0C)
10
100
1000
0
200
400
600
800
1000
1200
1400
LD 1 T
LU 1 T
Gambar 3.10. Profil Temperatur Sumur X-1
38
3.3. Penanggulangan Scaling Dengan Acid Wash
3.3.1. Acid Wash
Acid Wash merupakan suatu operasi pengasaman yang didesain untuk
mengurangi dan menghilangkan endapan scaling yang terbentuk pada pada lubang
bor. Dampak dari terbentuknya scaling ini menyebabkan berkurangnya suplai aliran
fluida panas bumi dari dasar sumur menuju permukaan yang mengakibatkan
berkurangya pasokan produksi uap ke turbin sehingga menyebabkan
turunnya
produksi. Maka dari itu dilakukan pengasaman dengan cara mengsirkulasikan asam
untuk mempercepat proses pelarutan sehingga mampu melarutkan endapan scale
tersebut.
3.4. Pemilihan Jenis Asam dan Additive
Pemilihan jenis asam dalam operasi pengasaman perlu diketahui karakteristik
dan additifnya. Hal ini perlu diperhatikan agar pemilihan dapat dilakukan dengan
tepat, dan kerusakan atau pengaruh sampingan yang ditimbulkan dapat dihindari.
3.4.1. Karakteristik Asam
Asam yang dipakai di industri minyak adalah inorganic acid (mineral),
organic acid, powdered Acid, acid Mixture dan retarded Acid.
3.4.1.1. Inorganik Acid ( Mineral )
Mineral acid terbagi menjadi dua jenis asam, yaitu asam hydrochloric (HCl)
dan asam hydrochloric-hydrofluoric (HCl-HF) atau yang biasa disebut dengan mud
acid.
39
3.4.1.2. Asam Hydrocloric ( HCl )
Asam hydrochloric (HCl) merupakan jenis asam yang paling banyak
digunakan dalam operasi pengasaman di lapangan. Asam ini merupakan larutan
hydrogen chloride yang berupa gas di dalam air dengan berbagai konsentrasi.
Konsentrasi asam ini bervariasi antara 535 %. Secara umum yang biasa digunakan
di lapangan adalah konsentrasi 15 % HCl. Asam jenis ini akan melarutkan batu
gamping, dolomite dan karbonat lainnya. Sedangkan untuk pengasaman batupasir
digunakan 5-7 % HCl.
Keuntungan penggunaan asam HCl antara lain memiliki daya reaksi yang
cukup tinggi terhadap batugamping dan dolomite, serta harganya relatif lebih murah
dibandingkan dengan asam jenis lainnya. Sedangkan kerugiannya, asam memiliki
sifat korosifitas paling tinggi, terutama pada temperatur tinggi diatas 250oF. Oleh
karena itu agar temperatur tidak melebihi tingkat korosifitasnya, maka pada
penggunaan asam HCl biasanya ditambahkan additif yaitu corrosion inhibitor sebagai
pencegah korosi. Reaksi yang terjadi antara asam HCl dengan beberapa mineral
batuan dapat dilihat pada Tabel 3.3. Pada sumur X-1 HCl 20 % yang digunakan.
Tabel 3.3.
Reaksi Antara HCl Dengan Beberapa Mineral Batuan
(Doherty, Henry L., Acidizing Fundamentals, Society of Petroleum
Engineering, New York, 1979)
40
3.4.1.3. Asam Hydrofluoric ( HF )
Asam Hydrofluoric digunakan untuk stimulasi pada batu pasir karena dapat
melarutkan silikat. Tidak semua produk reaksi dengan HF akan larut dalam air. HF
dapat bereaksi dengan bermacam macam mineral seperti Ca dan Mg tetapi akan
terbentuk endapan. Pada batu pasir sering terdapat semen dari bahan Ca, maka
umumnya HF dicampur dengan HCl dalam penggunaannya.
Asam HF bukan merupakan mineral asam yang sudah tersedia namun
didapatkan dengan cara mencampur dengan mineral lain. Campuran HCl-HF dengan
konsentrasi tertentu didapatkan dengan cara mencampurkan padatan ammoniumbifluoride (NH4F-HF) dengan larutan HCl. Tabel 3.4 menunjukkan reaksi HF dengan
beberapa mineral batuan.
Tabel 3.4.
Reaksi Antara HF Dengan Beberapa Mineral Batuan
(Doherty, Henry L., Acidizing Fundamentals, Society of Petroleum
Engineering, New York, 1979)
41
3.4.2. Jenis dan Fungsi Bahan Kimia Tambahan (Additive)
Pada program pengasaman ditambahkan pula zatzat kimia lain untuk
memperbaiki sifat asam yang diinjeksikan. Keuntungan pemakaian additive adalah :
Memperpanjang waktu reaksi asam (spending time).
Menghindari terbentuknya pengendapan material yang tidak dapt larut dalam
asam.
Mengurangi korosi pada peralatan logam akibat reaksi kimia.
Mengubah kondisi kebasahan pada formasi tertentu untuk memperbaiki
pengasaman.
Menghindari terbentuknya sludge.
Mengurangi gesekan di sepanjang pipa / tubing pada laju reaksi asam yang
besar.
Menghindari aliran asam yang tidak merata akibat tidak seragamnya
permeabilitas formasi.
Adapun beberapa jenis additive yang sering digunakan untuk projek
pengasaman yaitu antara lain :
a. Corrosion Inhibitor
Corrosion inhibitor merupakan additif yang selalu digunakan dalam setiap
operasi pengasaman, dengan mengingat kondisi asam yang korosif terhadap peralatan
logam.
Dengan
adanya
corrosion
inhibitor,
walaupun
tidak
bisa
100%
menghilangkan korosi, tetapi dapat mengurangi laju korosi hingga batas yang dapat
ditolerir. Korosi yang terjadi tergantung dari konsentrasi asam, jenis logam,
temperatur dan konsentrasi inhibitor sendiri.
Corrosion inhibitor adalah campuran dari beberapa persenyawaan termasuk
quarternary amines, acetylenic, alcohols, methanol, dan surfactant. Corrosion
inhibitor mudah terpisah dari asam, jadi sistem asam harus diaduk sebelum dipompa.
42
Terpisahnya corrosion inhibitor dari asam terlihat dengan terbentuknya lapisan tipis
hitam seperti minyak di permukaan asam. Lapisan ini dapat terlihat dalam waktu 15
menit setelah sistem asam didiamkan. Corrosion inhibitor yang digunakan pada
sumur X-1 adalah CI-25. Berdasarkan komposisi kimia, inhibitor terbagi menjadi :
1. Inhibitor inorganik
Contoh inhibitor inorganik adalah chromat, phospat, nitrit dan arsenic. Namun
yang banyak digunakan adalah arsenic. Kelebihan inhibitor inorganik adalah dapat
digunakan pada temperatur tinggi dengan waktu kontak yang lama, dan dari segi
keekonomian lebih murah daripada inhibitor organik. Kelemahan inhibitor inorganik
adalah membentuk racun arsine sebagai hasil korosi serta tingkat keamanan
pengangkutan dan pencampuran yang sulit.
2. Inhibitor Organik
Inhibitor organik banyak digunakan pada sumur gas kondensat dan sumur
minyak yang mengandung gas H2S. Kelebihan inhibitor organik adalah tidak
membentuk racun katalis serta efektif digunakan pada berbagai konsentrasi asam.
Kelemahan inhibitor organik adalah kurang efektif dalam waktu yang relatif lama
pada temperatur diatas 200oF.
b. Iron Control Additives
Iron Control Additives bereaksi dengan besi yang terlarut dan ionion logam
yang terlarut lainnya untuk menghambat pengendapan padatan ketika asam bereaksi
dan pH meningkat. Iron control agent tidak mengurangi sejumlah besi yang terlarut,
tidak juga mengurangi atau mencegah reaksi asam dengan senyawa besi. Iron control
agent mencegah pengendapan senyawa besi dengan menjaga kation besi pada larutan.
Manfaat lainnya adalah mencegah pembentukan sludge. Pembentukan sludge
sering bertambah karena pengendapan besi. Maka iron control agent yang efektif
juga mengendalikan atau paling tidak mengurangi pembentukan sludge. Iron
43
reducing agent seperti asam eryhorbic, efektif dalam mengendalikan iron sludge.
Iron control agent yang digunakan pada sumur X-1 Ferrotrol 210, ferrotrol 300 dan
ferrotrol 810.
1. Acid Generator
Acid generator diinjeksi sebelum asam HF yang berguna untuk meningkatkan
keefektifan kerja asam tersebut. Pada sumur X-1 acid generator yang digunakan
adalah AF (Ammonium Flouride).
2. Friction Reducer
Umumnya berupa polimer sintetis, berfungsi untuk mengurangi friksi fluida
(gel atau non gel) terhadap media yang dilaluinya sehingga akan mengurangi daya
pompa yang diperlukan dan dapat meningkatkan laju injeksi. Banyak friction reducer
yang dapat bekerja baik dengan air, tetapi tidak stabil dengan beberapa jenis asam,
oleh sebab itu penggunaannya harus disesuaikan dengan jenis asamnya.
Friction reducer digunakan untuk mengurangi terjadinya gesekan selama
proses pengasaman. Bisa mengurangi hingga 85% dibandingkan hanya menggunakan
air. Pada sumur X-1 friction reducer yang digunakan adalah FRW-14.
3. pH Control Agent
pH control agent digunakan untuk memelihara kerendahan pH sehingga
bisa memperlambat terjadinya presipitasi senyawa besi yang tak terlarut. Ferrofree
merupakan pH control agent yang digunakan pada Sumur X-1.
4. Citric Acid
Citric acid adalah sequestering atau chelating agent yang bereaksi mengikat
ion ferric dan mencegah pengendapan sebagai ferric oxide. Biasanya Citric Acid
digunakan untuk melarutkan unsure Ca sehingga ditambahkan denga Ethylne
Diamine Tetracetic Acid (EDTA).
44
5. Corrosion Inhibitor Intensifier
Corrosion inhibitor intensifier digunakan untuk meningkatkan kemampuan
corrosion inhibitor di temperatur yang tinggi. HY Temp O merupakan corrosion
inhibitor yang digunakan pada sumur X-1.
6. Retarded Agent
Berguna memberikan waktu reaksi (spending time) yang lebih lama. Ini
diperlukan, terutama untuk reaksi asam terhadap batuan dimana volume asam yang
diinjeksikan dalam jumlah besar. Karena waktu reaksi asam akan lama untuk
bereaksi, sehingga diadakan penetrasi asamnya lebih jauh (dalam). Additive yang
digunakan HV acid yang berfungsi memperpanjang kerja dari HF.
3.5. Faktor yang Mempengaruhi Pengasaman
Keberhasilan suatu operasi stimulasi pengasaman dipengaruhi oleh tiga faktor
kimia pokok, yaitu stoichiometry asam dengan batuan, laju reaksi asam,
kesetimbangan kimia, dan waktu reaksi asam.
3.5.1. Stoichiometry Reaksi Asam Dengan Batuan
a. Batuan Karbonat
Stoikiometry
menunjukkan proporsi berbagai reaktan yang terjadi dalam
suatu reaksi kimia, baik yang menjadi zat reaktan maupun zat hasil reaksinya.
Perbaikan yang terjadi pada stimulasi pengasaman ini adalah adanya pelarutan batuan
atau material/matrik penyumbat oleh asam yang diinjeksikan ke formasi. Walaupun
proporsi ini mudah untuk dikenali antara limestone atau dolomite dengan HCl, namun
secara alami reaksinya sangat kompleks karena pengaruh kandungan mineral-mineral
lain yang juga bereaksi dengan asam hydrochloric (HCl), asam formic (CHOOH)
dan asam asetic (CH3COOH). Asamasam tersebut akan bereaksi dengan batuan
45
karbonat membentuk CO2, air dan garam magnesium atau kalsium. Sedangkan reaksi
yang terjadi adalah sebagai berikut :
2HCl + CaCO3
CaCl2 + H2O + CO2
4HCl + CaMg(CO3)2
CaCl2 + MgCl2 + 2H2O + 2CO2
2CH3COOH + CaCO3
Ca(CH3COOH)2 + H2O + CO2
2CHOOH + CaCO3
Ca(CHOOH)2 + H2O + CO2
Sedangkan asam hydrofluoric dapat bereaksi dengan batuan karbonat, tetapi
menghasilkan endapan CaF2, sehingga tidak pernah digunakan dalam pengasaman
batuan karbonat dan reaksi kimianya adalah sebagai berikut :
2HF + CaCO3
CaF2 + H2O + CO2
Kelima persamaan reaksi tersebut merupakan stoichiometry dari reaksi yang
menunjukkan perbandingan molekul antara reaktan dengan hasil reaksinya. Sebagai
contoh, pada persamaan rumus kimia diatas menunjukkan adanya 2 mol asam
hydrochloric (HCl) bereaksi dengan 1 mol karbonat (CaCO3) dan membentuk 1 mol
calsium clorida (CaCl2), 1 mole air (H2O) dan 1 mol karbon dioksida (CO2). Jumlah
komponen yang diperlukan dalam reaksi (misalakan 2 mol HCl) disebut dengan
koefisien stoichiometry, dengan diketahuinya berat molekul masing masing reaktan,
maka besarnya jumlah asam yang digunakan untuk melarutkan batuan karbonat dapat
diperkirakan. Berat molekul masingmasing reaktan dari beberapa reaksi diatas dapat
dilihat pada Tabel 3.5.
46
Tabel 3.5.
Berat Molekul dalam Reaksi Asam dengan Mineral Batuan12
KOMPONEN
SENYAWA KIMIA BERAT MOLEKUL (MW)
Hydrogen
H
1
Carbon
C
12
Oxygen
O
16
Fluoride
F
19
Sodium
Na
23
Magnesium
Mg
24,3
Aluminium
Al
27
Silicon
Si
28,1
Chlorine
Cl
35,5
Pottasium
K
39,1
Calcium
Ca
40,1
Iron
Fe
55,8
Hydrochloric Acid
HCl
36,5
Hydrofluoric Acid
HF
20,0
Calcite
CaCO3
100,1
Dolomite
CaMg(CO3)2
184,4
Siderite
FeCO3
115,8
Quartz
SiO2
60,1
Albine
NaAlSi3O8
262,3
Orthoclase
KAlSi3O8
278,4
Koalinite
Al4Si4O10(OH)8
516,4
Montmorillonite
Al4Si8O20(OH)4
720,8
3.5.2. Laju Reaksi Pengasaman
Laju kecepatan reaksi asam adalah perubahan konsentrasi reaktan (zat yang
direaksikan) ataupun produk reaksi dalam suatu satuan waktu. Atau dapat dinyatakan
sebagai laju berkurangnya konsentrasi suatu reaktan atau bertambahnya konsentrasi
suatu produk. Faktorfaktor yang mempengaruhi laju reaksi asam dengan batuan
yaitu :
3.5.2.1. Perbandingan LuasVolume
Perbandingan luasvolume (spesifik surface area) merupakan perbandingan
antara luas permukaan batuan yang kontak dengan asam persatuan volume.
47
Perbandingan luasvolume berbanding terbalik dengan jarijari batuan atau lebar
rekahan.
3.5.2.2. Temperatur
Temperatur mempunyai pengaruh langsung yang berbanding lurus terhadap
laju reaksi asam dengan batuan. Pada temperatur 140 oF, dan 150 oF laju reaksi
sekitar 2 kali lebih cepat dibandingkan dengan temperatur 80 oF, dengan kata lain
dengan bertambahnya temperatur maka laju reaksi akan semakin lebih cepat.
3.5.2.3. Tekanan
Laju reaksi pengasaman relatif tidak begitu dipengaruhi oleh perubahan
tekanan. Pengaruh tersebut dapat terjadi pada berbagai konsentrasi asam. Pada
tekanan diatas 750 psi, akan sedikit pengaruhnya terhadap laju reaksi asam. CO2 yang
terlarut dalam fluida meningkat sehingga konsentrasi CO2 sebagai hasil reaksi akan
menggerakkan reaksi kearah tercapainya kesetimbangan. Hal inilah yang dapat
memperlambat laju reaksi. Tekanan yang kurang dari 750 psi, CO2 yang terlarut
mulai terbebaskan sehingga laju reaksi meningkat. Proses pelepasan gas CO2
menimbulkan efek turbulensi dan agitasi sehingga dapat membantu mempercepat laju
reaksi.
3.5.2.4. Konsentrasi Asam
Konsentrasi merupakan jumlah mol zat yang terdapat dalam tiap liter larutan
atau ruangan (gas). Dengan bertambahnya konsentrasi larutan maka, kecepatan reaksi
akan semakin cepat. Laju reaksi asam naik sebanding dengan naiknya konsentrasi
HCl antara 15 sampai 20 % dan pada konsentrasi 20-24 %, laju reaksi mencapai titik
maksimum.
Peningkatan konsentrasi HCl melebihi 24 % akan menyebabkan penurunan
terhadap laju reaksi. Hal ini disebabkan karena konsentrasi yang tinggi (maksimum
24 %) akan melarutkan volume yang besar, sehingga hasil reaksi yang dihasilkan juga
48
banyak. Hasil reaksi seperti CaCl2 dan CO2 inilah yang dapat mengurangi laju reaksi,
karena bersifat retarded.
3.6. Tahapan Pelaksanaan Acid Wash
Didalam melaksanakan acid wash, perlu diperhatikan beberapa hal yang
mendasari keberhasilan pekerjaan. Penempatan diatur dengan urutan pickling stage,
pre-flush, main acid dan after-flush atau over-flush. Meskipun fluida lain dapat
dipompakan baik sebagai preflush maupun setelah overflush tetapi tidak ada
perubahan terhadap tiga tahap dari fluida yang dipompakan tersebut selama pekerjaan
berjalan. Adapun tahap pelaksanaan acid wash :
1. Pickling Stage
String untuk injeksi seperti drill pipe dan coil tubing dibersihkan (pickling)
sebelum memompa asam. Pickling biasanya menggunakan 5% HCl atau larutan
khusus untuk membersihkannya. Tahap ini bisa memberikan dampak yang signifikan
terhadap keberhasilan treatment. Konsentrasi 5% HCl yang digunakan mengandung
iron-control agent dan corrosion inhibitor. Tujuan dari tubing pickling adalah :
Menghilangkan korosi, oksida besi dan scale pada string.
Membatasi sejumlah unsur besi yang masuk ke formasi.
2. Preflush
Tujuan dilakukan preflush adalah untuk melarutkan mineral-mineral
carbonate yang terbentuk didalam casing sebelum menginjeksikan campuran HF.
Asam HF bereaksi dengan carbonate seperti calcium carbonate untuk membantu
calcium fluoride dan magnesium fluoride dimana keduanya tak dapat larut oleh HF.
49
Standar dari pre-flush adalah asam hydrochloric (HCl), biasanya konsentrasi 5-15%.
Asam organic seperti acetic dan formic, dapat juga digunakan sendiri atau saling
dikombinasikan dengan HCl. Asam organic khusus digunakan untuk temperatur
tinggi, karena tingkat korosifitasnya tidak setinggi HCl. Campuran formic dan acetic
sangat baik pada kasus tersebut.
3. Main Flush
Pada main treatment ini fluida didesain untuk mengatasi kerusakan-kerusakan
yang ada pada lubang sumur. Fluida treatment yang digunakan tergantung pada jenis
batuan fluida reservoir yang akan di acidizing
4. Post-Flush
Fluida post-flush digunakan untuk mendorong treatment fluida yang masih
ada di dalam tubing agar seluruh asam masuk ke dalam formasi dan untuk
mengurangi waktu kontak dengan tubing, disamping itu juga untuk menjauhkan asam
dari lubang sumur sehingga presiptasi yang dapat terbentuk tidak akan banyak
merusak. Pada Sumur X-1 jenis cairan yang digunakan adalah HCl.
3.6.1. Perencanaan Operasional Acid Wash
Dalam stimulasi pengasaman hal-hal yang perlu diperhitungkan adalah :
tekanan rekah formasi, penentuan laju injeksi dan tekanan maksimum dipermukaan
serta volume asam (fluida treatment) yang diperlukan.
50
1. Menentukan Gradien Rekah Formasi
Dengan menggunakan metode Hubber, Willis, dan Eaton persamaan
matematis yang digunakan untuk menentukan gradient rekah formasi yaitu :
1
= 3 (( )/) + ((2 )/)........(3-12)
Keterangan :
Gf
= gradien rekah formasi, psi/ft
Gob
= gradien overburden, psi/ft (0.91 psi/ft)
Pres
= tekanan reservoir, psi
= kedalaman, ft
2. Menentukan Besarnya Harga Tekanan Rekah Formasi
Dengan diketahuinya harga tekanan rekah formasi, maka dapat diatur berapa
besar tekanan yang diperlukan untuk menginjeksikan asam agar tidak terjadi rekahan
pada formasi. Adapun persamaan yang digunakan untuk menentukan tekanan rekah
formasi sebagai berikut :
= .....(3-13)
Keterangan :
Pf
= tekanan rekah formasi, psi
Gf
= gradient rekah formasi, psi/ft
= kedalaman sumur, ft
3. Penentuan Tekanan Injeksi Maksimum Asam di Permukaan
Persamaan yang digunakan untuk menghitung besarnya tekanan injeksi
maksimum pompa yang diperlukan di permukaan adalah sebagai berikut :
= ( ) ...(3-14)
Keterangan :
Pmax = tekanan injeksi maksimum di permukaan
Gf
= gradient rekah formasi, psi/ft
51
4. Efektif Wellbore Radius
= .........................................................................................................(3-15)
Keterangan :
rs
= radius efektif wellbor, ft
rw
= jari-jari sumur, ft
= Skin faktor
5. Penentuan Laju Injeksi Asam Maksimum di Permukaan
Untuk menghitung besarnya laju injeksi larutan asam dapat digunakan persamaan
berikut :
Q max =
4.917 106 (PrekahPres)
( )
.............................................................(3-16).
Keterangan :
Qmax = laju injeksi maksimum dipermukaan, bbl/menit
kh
= permeabilitas thickness, mD
Gf
= gradient rekah formasi, psi/ft
= kedalaman sumur, ft
Pr
= tekanan reservoir, psi
= viskositas asam, cp
rs
= radius efektif wellbor, ft
rw
= jari-jari sumur, ft
6. Penentuan Volume Injeksi Asam Pada Casing
Adapun persamaan yang diugnakan untuk menentukan berapa volume asam
yang harus diinjeksi, berikut persamaannya :
52
2
1029.4
.......(3-17)
Keterangan :
V = Volume Injeksi Acid (barel)
h = ketinggian (ftMD)
ID = Inside Diameter Casing (inch)
3.7. Penurunan Tekanan Model Homogenous
Model yang dibuat adalah dengan menggunakan homogeneous. Pemilihan
model homogeneous dikarenakan Sumur X-1 merupakan sumur uap dan model
homogenous memiliki tingkat akurasi yang cukup baik dalam memperkirakan
kehilangan tekanan. Untuk membuat model data yang dibutuhkan :
Kedalaman feedzone
Mass rate feedzone (inflow/outflow)
Enthalpy feedzone
Geometry Sumur :
Diameter
Angle
Measured Depth/Vertical Depth
Roughness
Berikut proses perhitunga model homogenous :
1. Tentukan Temperatur Fluida
= (0 0 )..(3-18)
2. Hitung Dryness ( X )
= (0 0 )........(3-19)
3. Hitung Densitas Campuran ( rho )
53
= +
........(3-20)
= (0 0 ).....(3-21)
4. Hitung area (m2)
= 0.25 2 ........(3-22)
5. Hitung velocity (m/s)
V (m/s) = ()...(3-23)
6. Hitung viscosity ( miu) oleh Hasan & Kabir = +() ( Chicitti )
( . ) = (0 0 )..(3-24)
7. Hitung Reynold Number
= ......(3-25)
8. Hitung Moody friction factor ( f ) f = 4*Fanning friction factor
=4
.(3-26)
5.0452
[4[
log ] ]
3.7065
()
1.1098
7.149 0.8981
+(
2.8257
....(3-27)
9. Hitung dP total
=
( + )
(1 )
2
2
2
1
....(3-28)
..(3-29)
10. Hitung tekanan di titik berikutnya ( P1 )
1 = 0 .....(3-30)
54
11. Hitung densitas campuran ( rho1 )
rho1(kg/m3) = (1 , 0 )...(3-31)
12. Hitung kecepatan fluida v1 (m/s) = M/(rho*A)
v1( m/s) =
()
....(3-32)
13. Hitung h1 dengan persamaan h1 = h0 + (ek0 ek1) + (ep0-ep1)
1 = 0 + (0 1 ) + (0 1 ).....(3-33)
14. Ulangi langkah 1-13 hingga surface.
3.8. Evaluasi Keberhasilan Berdasarkan Laju Produksi
Salah satu
parameter yang dapat diketahui langsung setelah
pekerjaan
acidizing adalah dengan melihat kenaikan laju produksi harian caranya denga
menggunakan analisa decline. Analisa decline yang baik dihasilkan dari penyiapan
data produksi yang baik. Analisa decline menjadi sulit dilakukan apabila terdapat
kesalahan pada data produksi (sifat erratic). Arps (1945) yang dikenal sebagai bapak
decline curve membuat persamaan untuk tiga jenis penurunan produksi yang disebut
eksponensial, hiperbolik, dan harmonik. Arps telah melakukan analisa decline rate
dengan menggunakan metode empirik atau berdasar pada data produksi. Arps
menyatakan bahwa semua penurunan produksi pada periode depletion dapat
dinyatakan oleh persamaan empirik berikut :
1
= (1 + )() ....(3-34)
dimana qi adalah laju produksi awal (dengan mengabaikan periode transient), q
adalah laju produksi pada waktu t, D adalah konstanta rate decline, dan n adalah
eksponen rate decline.
55
Harga n membedakan jenis decline sebagai berikut :
Decline eksponensial : n = 0
Decline hiperbolik : 0 < n < 1
Decline harmonic : n = 1
Sehingga untuk decline eksponensial:
= ....(3-35)
Dan untuk decline harmonik :
= (1+)
..(3-36)
Decline rate menunjukkan seberapa besar perubahan laju produksi setelah
suatu periode waktu tertentu dibandingkan dengan laju produksi sebelum periode
waktu tersebut. Sumur-sumur yang berproduksi rendah sebagai akibat dioperasikan
pada tekanan kepala sumur rendah akan menghasilkan tren decline yang
eksponensial. Hal ini salah satunya disebabkan oleh terjadinya scalling pada sumur.
Anda mungkin juga menyukai
- Manajemen TeknologiDokumen74 halamanManajemen TeknologiDhana Jaya Wardana100% (2)
- Kimia MineralDokumen31 halamanKimia MineralAlex Dino Matri100% (1)
- Klas Sistem PabumDokumen12 halamanKlas Sistem PabumDhana Jaya WardanaBelum ada peringkat
- Manajemen TeknologiDokumen219 halamanManajemen TeknologiDhana Jaya Wardana100% (1)
- Reaksi Reaksi KimiaDokumen16 halamanReaksi Reaksi KimiaGaby SenolinggiBelum ada peringkat
- Kesadahan AirDokumen13 halamanKesadahan AirRachmat SaputraBelum ada peringkat
- Eksplorasi Panasbumi & RekonaisanDokumen16 halamanEksplorasi Panasbumi & RekonaisanDhana Jaya WardanaBelum ada peringkat
- Scale in Oil FieldDokumen66 halamanScale in Oil FieldReva Astra Dipta100% (2)
- ANALISA KIMIAWI AIR FORMASIDokumen11 halamanANALISA KIMIAWI AIR FORMASIArii WAhyudiiBelum ada peringkat
- TEORI SCALEDokumen21 halamanTEORI SCALEBimo PamungkasBelum ada peringkat
- Materi Analisa Kimia Air FormasiDokumen18 halamanMateri Analisa Kimia Air FormasiGhiffari Paramanta ElbeesBelum ada peringkat
- ZETA POTENSIDokumen14 halamanZETA POTENSIMeyda PutriBelum ada peringkat
- Materi 6-7 GeokimiaDokumen43 halamanMateri 6-7 GeokimiaYusuf Apriansyah singgasana100% (1)
- Problema ProduksiDokumen6 halamanProblema ProduksiMuhammad Galih Eko SaputroBelum ada peringkat
- GEOKIMIA PANASBUMIDokumen30 halamanGEOKIMIA PANASBUMIWarung BucuBelum ada peringkat
- STT MIGAS BALIKPAPANDokumen19 halamanSTT MIGAS BALIKPAPANDella SeptianiBelum ada peringkat
- Transfer GasDokumen18 halamanTransfer GasDITA PUTRI PURWANINGSIH Teknik LingkunganBelum ada peringkat
- (Modul 6 - Senin 1 - 10111072) PDFDokumen18 halaman(Modul 6 - Senin 1 - 10111072) PDF10111072Belum ada peringkat
- Bab 8 Analisa Kimia Air FormasiDokumen25 halamanBab 8 Analisa Kimia Air Formasisuci wulandariBelum ada peringkat
- Air Laut Sebagai Larutan Kimia 3.8 - 3.14Dokumen30 halamanAir Laut Sebagai Larutan Kimia 3.8 - 3.14Endang SulandriBelum ada peringkat
- Sri R - SCALE REMOVAL BY INHIBITORDokumen11 halamanSri R - SCALE REMOVAL BY INHIBITORsri ramadhaniBelum ada peringkat
- BAB9SADAHDokumen56 halamanBAB9SADAHAgung SukendarBelum ada peringkat
- Scale AcidizingDokumen25 halamanScale AcidizingBarqun DzulqurnainBelum ada peringkat
- Koordinasi KimiaDokumen5 halamanKoordinasi KimiaOKTAVIABelum ada peringkat
- Rangkuman Pencegahan Pencemaran - Kelompok 3 - Bagas Zaki Muhammad, Muhammad Faturrohman, Naufal HafizhDokumen10 halamanRangkuman Pencegahan Pencemaran - Kelompok 3 - Bagas Zaki Muhammad, Muhammad Faturrohman, Naufal HafizhNaufalBelum ada peringkat
- Analisa Air FormasiDokumen24 halamanAnalisa Air FormasiRahmatBelum ada peringkat
- Tugas NitratDokumen2 halamanTugas NitratYemima ThorchiBelum ada peringkat
- Acara IiiDokumen10 halamanAcara IiiRatna PermatasariBelum ada peringkat
- ANALISA KIMIAWIDokumen27 halamanANALISA KIMIAWIPratama ZetoBelum ada peringkat
- Pi Ww5 Yuli Astuti 15303065Dokumen8 halamanPi Ww5 Yuli Astuti 15303065Novalina Annisa YudistiraBelum ada peringkat
- Modul 6 - 12218035Dokumen16 halamanModul 6 - 12218035Micheal LimBelum ada peringkat
- KESADAHAN AIRDokumen19 halamanKESADAHAN AIRSyamsul RizalBelum ada peringkat
- Analisa Air FormasiDokumen3 halamanAnalisa Air FormasiRizkyIslamedBelum ada peringkat
- Soal Latihan Dan Jawaban Pra UsDokumen8 halamanSoal Latihan Dan Jawaban Pra UsPratiwi Az-ZahraBelum ada peringkat
- Kesetimbangan Kimia - Kelompok 5Dokumen68 halamanKesetimbangan Kimia - Kelompok 5catherine nastasyaBelum ada peringkat
- Laporan Resmi Kimia Lingkungan (Kesadahan)Dokumen15 halamanLaporan Resmi Kimia Lingkungan (Kesadahan)Aufar Za'imBelum ada peringkat
- Kesetimbangan Kimia FixDokumen13 halamanKesetimbangan Kimia FixAmeliaLia AmeliaBelum ada peringkat
- PANAS BUMI MARIBAYADokumen16 halamanPANAS BUMI MARIBAYAReza FebriBelum ada peringkat
- Laporan ResmiDokumen9 halamanLaporan ResmiNur FitrianiBelum ada peringkat
- DasarDokumen61 halamanDasarTaufik NovandaBelum ada peringkat
- Buku Petunuk Praktikum Kimia Fisik 2013-1Dokumen54 halamanBuku Petunuk Praktikum Kimia Fisik 2013-1BayuimadeBelum ada peringkat
- JURNALDokumen5 halamanJURNALPutra Master HackerBelum ada peringkat
- Geokimia Panas BumiDokumen7 halamanGeokimia Panas Bumimilna sianturiBelum ada peringkat
- Hidrasi SemenDokumen3 halamanHidrasi SemenLukman HakimzBelum ada peringkat
- Geo IndicatorDokumen16 halamanGeo IndicatorBayu Cahyana PutraBelum ada peringkat
- Makalah GaramDokumen19 halamanMakalah GaramQarinaBelum ada peringkat
- Perbandingan Laju Korosi Retak Tegangan Pada Pipa Baja Karbon Dalam Larutan Asam Asetat Dan Air Laut Dengan Adanya Sweet GasDokumen9 halamanPerbandingan Laju Korosi Retak Tegangan Pada Pipa Baja Karbon Dalam Larutan Asam Asetat Dan Air Laut Dengan Adanya Sweet GasAldy Bagus PratamaBelum ada peringkat
- Laporan Penetapan Kadar Kesadahan Total Dalam Sampel AirDokumen7 halamanLaporan Penetapan Kadar Kesadahan Total Dalam Sampel AirFatimah Ayu0% (1)
- Kompleks Co(III)-aminaDokumen5 halamanKompleks Co(III)-aminaAnsori MuchtarBelum ada peringkat
- Membaca Diagram Fasa Sistem Dua Komponen CairDokumen22 halamanMembaca Diagram Fasa Sistem Dua Komponen Cairsarahriana75% (4)
- Kerak ScaleDokumen11 halamanKerak ScaleFety FaradiLah100% (1)
- Laju Reaksi Dan Kecepatan ReaksiDokumen10 halamanLaju Reaksi Dan Kecepatan ReaksiFirdaus Er DsBelum ada peringkat
- Tugas Kajian Tentang Gas Metana BatubaraDokumen11 halamanTugas Kajian Tentang Gas Metana BatubaraNadiaAisyahBelum ada peringkat
- Oilfield Scale Prediction ModelDokumen29 halamanOilfield Scale Prediction ModelRay NaldiBelum ada peringkat
- Titrasi Kompleksometri MerkuriDokumen15 halamanTitrasi Kompleksometri MerkuriDiylla W100% (1)
- BAB IV Stimulasi Acidizing Baru Revisi (v-4)Dokumen18 halamanBAB IV Stimulasi Acidizing Baru Revisi (v-4)Dhana Jaya WardanaBelum ada peringkat
- BAB IV Stimulasi Acidizing Baru Revisi (v-4)Dokumen18 halamanBAB IV Stimulasi Acidizing Baru Revisi (v-4)Dhana Jaya WardanaBelum ada peringkat
- PADI DIAGNOSADokumen8 halamanPADI DIAGNOSAArinie Haqqo0% (1)
- MatriksDokumen16 halamanMatriksDhana Jaya WardanaBelum ada peringkat
- PADI DIAGNOSADokumen8 halamanPADI DIAGNOSAArinie Haqqo0% (1)
- VOLCANODokumen11 halamanVOLCANOJayawardana IBBelum ada peringkat
- MEKANIKA FLUIDADokumen101 halamanMEKANIKA FLUIDAPopo ScairyBelum ada peringkat
- KL - Survei Heat LossDokumen4 halamanKL - Survei Heat LossDhana Jaya WardanaBelum ada peringkat
- VOLCANODokumen11 halamanVOLCANOJayawardana IBBelum ada peringkat
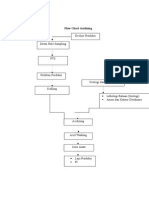
- Flow Chart Acid WashingDokumen1 halamanFlow Chart Acid WashingDhana Jaya WardanaBelum ada peringkat
- Perhitungan Anion Dan KationDokumen2 halamanPerhitungan Anion Dan KationDhana Jaya WardanaBelum ada peringkat