Teoría Del Enlace de Valencia
Diunggah oleh
mariana0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
57 tayangan3 halamanJudul Asli
Teoría del enlace de valencia.docx
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
57 tayangan3 halamanTeoría Del Enlace de Valencia
Diunggah oleh
marianaHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 3
Teora del enlace de valencia
En qumica, la teora del enlace de valencia explica la naturaleza de un enlace
qumico en una molcula, en trminos de las valencias atmicas.1 La teora del
enlace de valencia resume la regla que el tomo central en una molcula
tiende a formar pares de electrones, en concordancia con restricciones
geomtricas, segn est definido por la regla del octeto. La teora del enlace de
valencia est cercanamente relacionada con la teora de los orbitales
moleculares.
Una estructura de enlace de valencia es similar a una estructura de Lewis, sin
embargo, pueden escribirse varias estructuras de enlace de valencia donde no
puede escribirse slo una estructura de Lewis. Cada una de estas estructuras
de EV representa a una estructura de Lewis especfica. La combinacin de las
estructuras de enlace de valencia es el punto principal de la teora
de resonancia. La teora del enlace de valencia considera que
el solapamiento de orbitales atmicos de los tomos participantes formando
un enlace qumico. Debido al traslape, es ms probable que los electrones
estn en la regin del enlace. La teora del enlace de valencia considera a los
enlaces como orbitales dbilmente apareados (traslape pequeo). Tpicamente,
la teora del enlace de valencia es ms fcil de emplear en molculas en
el estado basal.
Teora de los orbitales moleculares
En qumica, la teora de los orbitales moleculares (TOM), es un mtodo para
determinar el enlace qumico en el que los electrones no estn asignados a
enlaces individuales entre tomos, sino que se mueven bajo la influencia de los
ncleos de toda la molcula.1
En esta teora, cada molcula tiene un grupo de orbitales moleculares, y se
asume que la funcin de onda f del orbital molecular est escrita de manera
aproximada como una simple combinacin lineal de los n orbitales atmicos
constituyentes i, de acuerdo con la siguiente ecuacin: 1
Los coeficientes cij pueden ser determinados numricamente por sustitucin de
esta ecuacin por la de Schrdinger y la aplicacin del principio variacional.
Este mtodo se llama combinacin lineal de orbitales atmicos y se utiliza en
la qumica computacional. Una transformacin unitaria adicional puede ser
aplicada en el sistema para acelerar la convergencia en algunos combinaciones
computacionales. La teora de los orbitales moleculares ha sido vista como
competidora de la teora del enlace de valencia en los aos 1930, pero se
descubri despus que los dos mtodos estn ntimamente relacionados y que
cuando son extendidos son equivalentes.
De acuerdo con la teora de los orbitales moleculares, los enlaces
covalentes de las molculas se forman por solapamiento de orbitales atmicos,
de manera que los nuevos orbitales moleculares pertenecen a la molcula
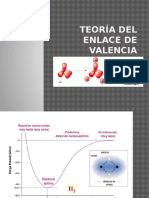
entera y no a un solo tomo. Durante la formacin de un enlace, los orbitales
atmicos se acercan y comienzan a solaparse, liberando energa a medida que
el electrn de cada tomo es atrado por la carga positiva del ncleo del otro
tomo. Cuanto mayor sea el solapamiento, mayor ser el desprendimiento de
energa y, por lo tanto, menor ser la energa del orbital molecular. Si el
proceso de aproximacin de los tomos contina, los ncleos atmicos pueden
llegar a repelerse mutuamente, lo que hace que la energa del sistema
aumente. Esto significa que la mxima estabilidad (mnima energa) se alcanza
cuando los ncleos se encuentran a una distancia determinada que se conoce
como longitud de enlace.2
Segn la teora de los orbitales moleculares, el nmero de orbitales
moleculares es igual al nmero de orbitales atmicos que se solapan. El orbital
molecular de menor energa se forma cuando se solapan dos orbitales
atmicos que estn en fase. Este orbital contiene a los dos electrones y
mantiene a los dos tomos unidos, por lo que se denomina orbital molecular
enlazante. Sin embargo, se forma otro orbital molecular, que posee una
energa mayor que la suma de las energas de los dos orbitales atmicos
separados. Este orbital molecular se denomina antienlazante y es destructivo,
es decir, si los electrones se encontraran en este orbital, los dos tomos se
repeleran.3 El orbital antienlazante, corresponde en la teora de Lewis al orbital
ocupado por aquellos electrones que no se comparten (llamados "pares no
enlazantes" en dicha teora). Por ejemplo, en el caso de la molcula de
oxgeno, existen dos pares enlazantes y cuatro pares no enlazantes. Los pares
enlazantes ocupan los orbitales sigma gerade y pi ungerade (en el nivel 2 de
energa), los cuales son orbitales enlazantes, y los pares no enlazantes ocupan
los orbitales 2s (que no se comparten) y los orbitales pi gerade, dado que
tienen menor energa (son ms estables) que los sigma gerade.
Anda mungkin juga menyukai
- Teoria Del Orbital MolecularDokumen9 halamanTeoria Del Orbital MolecularOmitowa Mendelew KioyaBelum ada peringkat
- Teoría Del Enlace de Valencia XDDokumen12 halamanTeoría Del Enlace de Valencia XDEmanuelBelum ada peringkat
- Enlace QuímicoDokumen19 halamanEnlace QuímicoAlexandra LunaBelum ada peringkat
- Teoría Del Enlace de ValenciaDokumen3 halamanTeoría Del Enlace de Valencia02-AS-LI-ROSSANJHELA JHOSELINE MANDUJANO OREBelum ada peringkat
- Op Sec Fisqui T 42 Orbitales MolecularesDokumen16 halamanOp Sec Fisqui T 42 Orbitales MolecularesCristina Martinez GonzalezBelum ada peringkat
- Enlaces Sigma y Enlaces PiDokumen2 halamanEnlaces Sigma y Enlaces PiIsrael Cortes100% (3)
- Teoria Del Enlace de ValenciaDokumen2 halamanTeoria Del Enlace de ValenciaMarina AquinoBelum ada peringkat
- Elance y Valencia y CovalenteDokumen6 halamanElance y Valencia y CovalenteAriel CQBelum ada peringkat
- Teoría de Orbitales MolecularesDokumen2 halamanTeoría de Orbitales MolecularesFrey MeloBelum ada peringkat
- Hibridación de Orbitales AtómicosDokumen30 halamanHibridación de Orbitales AtómicosMonica BortBelum ada peringkat
- Enlaces QuímicosDokumen5 halamanEnlaces QuímicosMelisa DlBelum ada peringkat
- 1.1.3. - Modelo de Orbitales MolecularesDokumen5 halaman1.1.3. - Modelo de Orbitales MolecularesALANBelum ada peringkat
- Prueba Cuatro QuimicaDokumen23 halamanPrueba Cuatro QuimicamariaBelum ada peringkat
- Teoría Del Enlace de ValenciaDokumen6 halamanTeoría Del Enlace de ValenciaErik Ortiz BlancoBelum ada peringkat
- Consulta N°2 Quimica General 1. Angamarca Angulo Brayan Alexander.Dokumen10 halamanConsulta N°2 Quimica General 1. Angamarca Angulo Brayan Alexander.BryanAngamarcaBelum ada peringkat
- Hibridación Orbital y Teoría de Orbitales MolecularesDokumen4 halamanHibridación Orbital y Teoría de Orbitales MolecularesazulcathalinagBelum ada peringkat
- Enlace (Química) - Wikipedia, La Enciclopedia LibreDokumen18 halamanEnlace (Química) - Wikipedia, La Enciclopedia LibreAnlli SanchezBelum ada peringkat
- Unidad 3 QuimicaDokumen18 halamanUnidad 3 QuimicaAlberto JimenezBelum ada peringkat
- N QuímicaDokumen4 halamanN QuímicaRomelin de jesusBelum ada peringkat
- Geometria Electronica QuimicaDokumen10 halamanGeometria Electronica QuimicaBryanAngamarcaBelum ada peringkat
- Reporte - Teoría de Enlace de ValenciaDokumen10 halamanReporte - Teoría de Enlace de ValenciaGuadalupeBelum ada peringkat
- Enlace QuimicoDokumen8 halamanEnlace QuimicoMaria yolimaBelum ada peringkat
- Teorías de Enlaces CovalentesDokumen23 halamanTeorías de Enlaces CovalentesUrquiza Luis Jesus AlexisBelum ada peringkat
- Aplicaciones y Limitaciones de La Regla Del OctetoDokumen4 halamanAplicaciones y Limitaciones de La Regla Del OctetoJuan Carlos Gonzalez0% (3)
- Inorganica 1Dokumen3 halamanInorganica 1Julio CesarBelum ada peringkat
- Ensayo Enlace CovalenteDokumen3 halamanEnsayo Enlace CovalenteCamilo Andres ZabaletaBelum ada peringkat
- Teoria de Orbitales AtomicosDokumen7 halamanTeoria de Orbitales AtomicosDark HikaruBelum ada peringkat
- Orbital MolecularDokumen2 halamanOrbital Molecularap22020071Belum ada peringkat
- Enlace QuímicoDokumen37 halamanEnlace Químicoelides bastardoBelum ada peringkat
- Investigacion EnlacesDokumen12 halamanInvestigacion EnlacesEmmanuel Rivas RamírezBelum ada peringkat
- Teoria de Enlace ValenciaDokumen10 halamanTeoria de Enlace ValenciaANDREWBelum ada peringkat
- Enlace Quimico y Fuerzas IntermolecularesDokumen7 halamanEnlace Quimico y Fuerzas IntermolecularesDanteJaraEspinozaBelum ada peringkat
- Tema 2 Enlace QuimicoDokumen5 halamanTema 2 Enlace QuimicoSilvano Salvador ondo ndong100% (1)
- UiouikjkjklDokumen10 halamanUiouikjkjklRaymi CampoBelum ada peringkat
- Enlace (Química)Dokumen15 halamanEnlace (Química)AnaBelum ada peringkat
- Taller Sobre Teoria Del Orbital MolecularDokumen6 halamanTaller Sobre Teoria Del Orbital MolecularLeidy RamirezBelum ada peringkat
- Enlace QuímicoDokumen16 halamanEnlace Químicoaguirre sergio danielBelum ada peringkat
- "Modelo de Enlace Valencia" Equipo - 5 Grupo1256Dokumen19 halaman"Modelo de Enlace Valencia" Equipo - 5 Grupo1256Lisbeth JimenezBelum ada peringkat
- Teorias Que Comprueban Los Enlaces CovalentesDokumen6 halamanTeorias Que Comprueban Los Enlaces Covalentesja431598Belum ada peringkat
- ENLACES MÚLTIPLEs TRABAJODokumen8 halamanENLACES MÚLTIPLEs TRABAJOJonathan Agudelo33% (3)
- Teorias Que Comprueban Los Enlaces CovalentesDokumen5 halamanTeorias Que Comprueban Los Enlaces Covalentesja431598Belum ada peringkat
- Estructura de LewisDokumen14 halamanEstructura de LewisEdwin Roberto Molina RamirezBelum ada peringkat
- En Lace Co ValenteDokumen31 halamanEn Lace Co Valenteceo_quercusBelum ada peringkat
- Enlace Químico TeoríaDokumen15 halamanEnlace Químico TeoríaDara AguilaBelum ada peringkat
- Combinación Lineal de Orbitales Atómicos, o Método CLOA, Que Considera Que El OrbitalDokumen5 halamanCombinación Lineal de Orbitales Atómicos, o Método CLOA, Que Considera Que El Orbitallitul888Belum ada peringkat
- $RW07N9HDokumen15 halaman$RW07N9Hedson chavezBelum ada peringkat
- Investigacion TrpecvDokumen4 halamanInvestigacion TrpecvMario Castilla RgBelum ada peringkat
- Exposicion de InorganicaDokumen4 halamanExposicion de InorganicaRocio Diaz TrujanoBelum ada peringkat
- Teoria de Enlace de ValenciaDokumen4 halamanTeoria de Enlace de ValenciaRicardo AlmarzaBelum ada peringkat
- Enlace QuímicoDokumen9 halamanEnlace QuímicoEva Soto cobosBelum ada peringkat
- Anexo 2 - Tarea 3Dokumen20 halamanAnexo 2 - Tarea 3Edgar PerezBelum ada peringkat
- Hibridación de OrbitalesDokumen1 halamanHibridación de OrbitalesoctavioBelum ada peringkat
- R.A 2.3Dokumen2 halamanR.A 2.3Jesus SanchezBelum ada peringkat
- Aportaciones de Gilbert Newton Lewis A La QuimicaDokumen5 halamanAportaciones de Gilbert Newton Lewis A La QuimicaMiraldelly BautistaBelum ada peringkat
- Tema 4 Teoría Del Orbital MolecularDokumen15 halamanTema 4 Teoría Del Orbital MolecularVale ITreBelum ada peringkat
- Actividad1 - U3 InvestigacionDokumen9 halamanActividad1 - U3 Investigacionmara alvarezBelum ada peringkat
- Práctica 1 - Química InorgánicaDokumen12 halamanPráctica 1 - Química InorgánicaJUAN RODRIGO BASTIDAS VILLAMILBelum ada peringkat
- Enlaces QuimicosDokumen50 halamanEnlaces QuimicosMario BlasBelum ada peringkat
- Trabajo de Estructuras de Lewis (Contenido)Dokumen12 halamanTrabajo de Estructuras de Lewis (Contenido)Marcell BriceñoBelum ada peringkat
- Monografia Puntos Cuanticos SignificadoDokumen9 halamanMonografia Puntos Cuanticos SignificadoDIEGO SantosBelum ada peringkat
- Guia 6 de QuimicaDokumen5 halamanGuia 6 de QuimicaLuis MartinezBelum ada peringkat
- Espectrofotometría UltravioletaDokumen4 halamanEspectrofotometría UltravioletaSantiago Castro RengifoBelum ada peringkat
- CLASE 2 - Recursos Técnicos y ExpresivosDokumen23 halamanCLASE 2 - Recursos Técnicos y ExpresivosRunciman1992Belum ada peringkat
- Marco Teorico de Espectros de CobreDokumen2 halamanMarco Teorico de Espectros de CobreJhonatan Mallqui QuispeBelum ada peringkat
- Diagrama de FlujoDokumen1 halamanDiagrama de FlujoAlex David Roldan CevallosBelum ada peringkat
- Informe (Lab 10) Espectroscopía ÓpticaDokumen8 halamanInforme (Lab 10) Espectroscopía ÓpticaAndres Fernando Silvestre SuarezBelum ada peringkat
- Guía de Aprendizaje Reflexión de La LuzDokumen18 halamanGuía de Aprendizaje Reflexión de La LuzAngel VásquezBelum ada peringkat
- Guía II Parcial QQ - 103Dokumen2 halamanGuía II Parcial QQ - 103Rubius MacrausBelum ada peringkat
- La EspectrometríaDokumen2 halamanLa Espectrometríaheidys tatiana cantillo mendozaBelum ada peringkat
- Teorias, Modelos Atomicos y Cálculo de SubparDokumen3 halamanTeorias, Modelos Atomicos y Cálculo de SubparAngie CarolinaBelum ada peringkat
- Actividad 06Dokumen5 halamanActividad 06Erika Dayana LECCA ALMÉSTARBelum ada peringkat
- Unidad I. Teoría AtómicaDokumen24 halamanUnidad I. Teoría Atómicaluis zavala (luisito)Belum ada peringkat
- Bio Cuestionario 1Dokumen2 halamanBio Cuestionario 1Lemon TeaBelum ada peringkat
- Enlaces QuimicosDokumen76 halamanEnlaces QuimicosGrc MrthBelum ada peringkat
- El Instrumento ÓpticoDokumen2 halamanEl Instrumento Ópticomagdalena alcaraz moralesBelum ada peringkat
- Fisica 4Dokumen21 halamanFisica 4FiorelaBelum ada peringkat
- Diferencia de Fase OpticaDokumen10 halamanDiferencia de Fase OpticaCarlitos TapiaBelum ada peringkat
- Espectroscopia de Absorción AtómicaDokumen7 halamanEspectroscopia de Absorción AtómicaRuberney CarrilloBelum ada peringkat
- Evolucion Del AtomoDokumen13 halamanEvolucion Del AtomoJhonatan RoldanBelum ada peringkat
- Actividad Experimental 4Dokumen1 halamanActividad Experimental 4fernanda13Belum ada peringkat
- Eespectrofotometria UV VisibleDokumen29 halamanEespectrofotometria UV VisiblePablo AlvarezBelum ada peringkat
- EXAMEN QUIMICA - 6to COMUNICACIONDokumen2 halamanEXAMEN QUIMICA - 6to COMUNICACIONEzekch PivaBelum ada peringkat
- Quimica Academia 2023Dokumen71 halamanQuimica Academia 2023Lisbeth Ramos IdmeBelum ada peringkat
- Tema 03 Nube ElectronicaDokumen13 halamanTema 03 Nube ElectronicaAlex Sebastian Olgado NuñezBelum ada peringkat
- 3,2 COMPUESTOS DE COORDINACION. Parte 2 Enlace Metal LigandoDokumen23 halaman3,2 COMPUESTOS DE COORDINACION. Parte 2 Enlace Metal LigandoLUVINCA DANIELA PLATA ALCONBelum ada peringkat
- Estructura Atómica y MolecularDokumen59 halamanEstructura Atómica y MolecularTomás MartinezBelum ada peringkat
- SESION SEM-11 1ro CyT AtomoDokumen1 halamanSESION SEM-11 1ro CyT AtomoFabiola100% (1)
- Tarea 3 - G299003 - 13Dokumen25 halamanTarea 3 - G299003 - 13Frank HerreraBelum ada peringkat
- PDF 2 1 CompressDokumen139 halamanPDF 2 1 CompressJhon SalcedoBelum ada peringkat