Laporan Sintesis Iodoform
Diunggah oleh
Rafika Firda Umamy HatibieHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Laporan Sintesis Iodoform
Diunggah oleh
Rafika Firda Umamy HatibieHak Cipta:
Format Tersedia
SINTESIS IODOFORM
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Sintesis adalah istilah yang mempunyai arti luas dan dapat
digunakan ke fisika, ideologi, dan fenomenologi. Sintesis juga dapat
diartikan sebagai hasil akhir dari percobaan untuk menggabungkan 2
senyawa kimia atau lebih. Sintesis juga dapat diartikan sebagai
proses pembentukan sebuah molekul tertentu dari prekursor kimia.
Iod merupakan senyawa halogen yang mempunyai rumus
kimia I2. Iodium sangat diperlukan dalam dunia farmasi. Dalam tubuh,
iod banyak dijumpai sebagai pembentukan hormon tiroksin. Umumnya
iod banyak dijumpai pada tumbuh-tumbuhan sekitar pinggir laut dan
pada garam dapur. Iod dikenal sebagai obat penyakit gondok, anti
tumor dan anti tiroid
Dalam mensintesis Iodoform harus memerlukan suatu tingkat
ketelitian yang tinggi sehingga hasil yang didapatkan sesuai dengan
yang diharapkan. Iod selain mempunyai efek positif juga memiliki
efek negatif terutama dalam penggunaannya pada wanita hamil yang
akan menyebabkan penyakit hipodesmi pada bayi. Juga bila
dikonsumsi, iodium harus sesuai dengan yang dibutuhkan. Hal inilah
yang membuktikan bahwa iodium merupakan senyawa yang sangat
bermanfaat bagi tubuh kita
Karena kegunaannya yang cukup luas itulah maka setiap
mahasiswa farmasi dituntun untuk mengetahui dan memahami
reaksi pembentukan iodoform tersebut. Pada percobaan ini
dilakukan sintesis iodoform untuk menghasilkan iodoform murni.
1.2 Maksud Praktikum
Untuk mengetahui dan memahami cara mensintesis iodoform
dan mekanisme reaksi.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
1.3 Tujuan Praktikum
Untuk mensintesis iodoform dengan reaksi iod dengan aseton
pada suasana basa dengan prinsip reaksi halogenasi.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
BAB 2 TINJAUAN PUSTAKA
2.1 Teori Umum
Iodoform adalah senyawa yang dibentuk dari reaksi antara iodine
dengan etanol/aseton dan asetaldehida dalam suasana basa.
Iodoform dapat digunakan sebagai desinfektan dan antiseptic luar.
Reaksi iodoform adalah reaksi haloform dimana dalam reaksi tersebut
digunakan iodide dari larutan alkali hidroksida (NaOH dan KOH)
sehingga menghasilkan iodoform (Cairns 2008, hal. 122).
Sintesis merupakan bentuk lain dari kegiatan atau metode
berpikir. Secara sederhana, Russel menyatakan bahwa sintesa logik
berarti menentukan makna pernyataan atas dasar empirik. Meskipun
demikian, kebenaran proposisi Russel perlu dianalisis dengan
membedah pengertian yang dikemukakan (Cairns 2008, hal. 120).
Halogenasi alfa merupakan dasar suatu uji kimia, yang
disebut uji iodoform, untuk metil keton. Gugus metil dari suatu metil
keton diiodinasi bertahap sampai terbentuk iodoform (CHI 3) padat
berwarna kuning (Moore 2003, 266).
Dalam tahap pertama dalam reaksi bersuasana basa adalah
pembentukan ion enolat. Anion suatu keton dengan gugus karbonil
merupakan basa yang jauh lebih kuat daripada ion hidrosida. Oleh
karena itu kesetimbangan asam-basa lebih menyukai ion hidroksida
daripada ion enolat. Meskipun begitu, terdapat juga sedikit ion enolat
dalam larutan basa. Segera setelah anion ini habis terpakai, akan
terbentuk lagi yang baru, untuk menuju ke tahap 2. Dalam tahap 2, ion
enolat secara cepat bereaksi dengan halogen, menghasilkan keton
terhalogenasi alfa dan ion halida. Halogenasi alfa dalam suasana
asam biasanya memberikan rendemen yang lebih baik daripada
reaksi dalam suasana basa. Reaksi berkatalis asam berlangsung
lewat enol, yang pembentukannya merupakan tahap penentu laju.
Ikatan rangkap karbon-karbon dari enol itu mengalami adisi
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
elektrofilik, sama seperti setiap ikatan rangkap karbon-karbon apa
saja, untuk membentuk karbonkation yang lebih stabil (Cairns 2008,
hal. 130).
Dalam sintesis Iodoform, dipilih menggunakan labu alas datar
agar bias berdiri sendiri yang dipegang karena akan dikerjakan seperti
titrasi hanya lebih kasar. Pemakaian labu alas bulat disini tidak
dibenarkan karena dalam prosedur tidak dilakukan pemanasan.
Dalam mensintesis iodoform harus memerlukan suatu tingkat
ketelitian yang tinggi sehingga hasil yang didapatkan sesuai dengan
yang diharapkan (Raharjo 2007, hal. 199).
Adapun maksud dari penambahan segera dengan banyak air
setelah terjadi kristal Iodoform adalah untuk mengencerkan NaOH
yang mungkin berlebih. Filtrat yang terbentuk tidak boleh bersifat
alkalis lagi sebab dengan adanya suasana alkalis maka pada
rekristalisasi dengan alkohol maka Iodoform akan terurai dan
kemungkinan akan dibebaskan Iodium yang terlihat dengan berwarna
coklatnya larutan (Raharjo 2007, hal. 201).
Dalam proses sintesis iodoform ini dilakukan penambahan air
yang banyak setelah terjadi kristal Iodoform dengan maksud
mengencerkan NaOH yang mungkin berlebihan. Jadi mengurangi
kecepatan terhidrolisisnya Iodoform yang terjadi kecepatan
terhidrolisirnya Iodoform yang terjadi dengan adanya NaOH (Raharjo
2007, hal. 201).
Iodum mengandung tidak kurang dari 99,8 % dan tidak lebih dari
100,5 % I. Pemerian keping atau granul, berat, hitam keabu-abuan,
bau khas, berkilau seperti metal. Kelarutan sangat sukar larut dalam
air, mudah larut dalam karbon disulfida, dalam kloroform, dalam
karbon tetraklorida dan dalam eter, larut dalam 13 bagian etanol
(95%)P dan dalam larutan iodida, agak sukar larut dalam gliserin.
Khasiat dan penggunaan Antiseptikum ekstern dan antijamur (Moore
2003, hal. 267).
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Iodoform bila kontak dengan tubuh melepaskan iodium secara
berangsur dan iodium inilah yang diharapkan bersifat bakterisid.
Iodium adalah suatu zat yang bersifat bakteriostatik non selektif .
sediaan yang mengandung zat ialah iodium tinktur dan lugol. Iodium
tinktur berwarna coklat, dapat menyebabkan iritasi, vesikulasi kulit,
kadang-kadang kulit dapat mengelupas. Karena toksik dan mudah
diperoleh, zat ini sering dipakai untuk percobaan bunuh diri. Bila
terjadi intoksikasi, akan timbul iritasi saluran cerna terdapat banyak
karbohidrat (Sunaryo 2010, 100).
Iodroform merupakan senyawa organik yang dalam bidang
kedokteran gigi masih kadang-kadang digunakan sebagai antiseptik
dan desinfektan. Desinfektan adalah zat-zat yang bekerja bakterisid
yang digunakan untuk membebaskan ruang dan pakaian dari mikroba,
tetapi juga dipakai pada produk eksresi orang sakit. Zat ini juga
bekerja mematikan pada hampir semua sel hidup lainnya. Sedangkan
antiseptik umumnya bekerja bakteriostatik. Biasanya dipakai pada
infeksi bakteri pada kulit, mukosa dan melawan infeksi pada luka
(Sunaryo 2010, hal. 101).
Brom dan klor juga bereaksi dengan metil keton, menghasilkan
masing-masing bromoform (CHBr3) dan kloroform (CHCl3). Istilah
umum untuk menyebut CHX3 ialah haloform maka reaksi ini sering
disebut sebagai reaksi haloform. Karena bromoform dan kloroform
merupakan cairan yang tidak mencolok, maka pembentukannya tak
berguna untuk maksud uji. Namun, reaksi antara suatu metil keton
dengan setiap halogen tersebut memberikan suatu metode
pengubahan metol keton ini menjadi asam karboksilat. Ikatan karbon-
hidrogen biasanya stabil, nonpolar, dan pasti tidak bersifat asam.
Tetapi dengan adanya suatu gugus karbonil terjadilah hidrogen alfa
yang bersifat asam (Fessenden 1982, hal. 201).
Reaksi dapat dipercepat dengan penambahan asam atau basa.
Telah ditemukan bahwa kecepatan halogenasi suatu keton berbanding
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
langsung dengan konsentrasi asam yang ditambahkan, tetapi tidak
bergantung pada konsentrasi atau jenis halogen yang digunakan (klor,
brom, atau iod). Halogenasi terhadap keton asimetris seperti metil
propil keton memperlihatkan bahwa orientasi halogenasi terjadi lebih
dominan terhadap karbon yang lebih tersubstitusi. Di dalam
halogenasi terkataliss basa terhadap keton, ditemukan juga bahwa
kecepatan reaksi sama sekali tidak tergantung pada konsentrasi dan
identitas halogen (Sunaryo 2010, hal. 103).
2.2 Uraian Bahan
1. Air suling ( Ditjen POM,1979)
Nama resmi : AQUA DESTILLATA
Nama lain : Aquades, air suling
RM/BM : H2O / 18,02
Rumus struktur : HOH
Pemerian : Cairan jernih, tidak berwarna, tidak berbau,
tidak.
Penyimpanan : Dalam wadah tertutup rapat.
Kegunaan :Mengencerkan NaOH
2. Aseton ( Ditjen POM,1979)
Nama resmi : ASETON
Nama lain : Aseton
RM/BM :(CH3)2CO/ 58,08
Rumus struktur :
Pemerian : Cairan jernih tidak berwarna mudah menguap
bau khas, mudah terbakar
Kelarutan : Dapat bercampur dengan air, dengan etanol
95 % P, dengan eter P dan dengan
kloroform P, membentuk larutan jernih.
Penyimpanan : Dalam wadah tertutup rapat.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Kegunaan :Sebagai bahan dasar pembuatan iodoform.
3. Iodium ( Ditjen POM, 1979)
Nama resmi :IODIDUM
Nama lain :Iodium
RM/BM :I2/ 126,1
Pemerian :Keping atau butir, berat, mengkilat, seperti
logam; hitam kelabu; bau khas.
Kelarutan :Larut dalam lebih kurang 3500 bagian air,13
Bagian dalam etanol 95 % P, dalam lebih
kurang 80 bagian gliserol P, dan dalam lebih
kurang 4 bagian karbondisulfida P; larut
kloroform P dan karbontetraklorida P.
Penyimpanan :Dalam wadah tertutup rapat
Kegunaan :Sebagai bahan utama pembuatan iodoform
4. Iodoform (Ditjen POM, 1979)
Nama resmi :IODOFORM
Nama lain :Iodoform
RM/BM :CHI3/ 394
Pemerian :Kepingan kuning hijau atau serbuk mikro
halus; bau khas dan sangat melekat.
Kelarutan :Hampir apa larut dalam air, melarut dalam 67
bagian spritus, dalam 6,1 bagian eter, dalam
20 bagian oleum olivarum dan dalam 1000
bagian gliserol.
Penyimpanan :Dalam wadah tertutup rapat
Kegunaan :Sebagai bahan yang disintesis
5. Natrium Hidroksida ( Ditjen POM, 1979)
Nama resmi :NATRII HYDROXIDUM
Nama lain :Natrium hidroksida
RM/BM :NaOH/ 40,00
Rumus struktur :
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Pemerian :Putih, bentuk batang, butiran, massa hablur,
kertas sraput, mudah meleleh, basa dan
alkalis.
Kelarutan :Mudah larut dalam air dan etanol.
Penyimpanan :Dalam wadah tertutup rapat
Kegunaan :Sebagai katalisator
2.3 Prosedur Kerja (Anonim, 2017)
1. Dalam labu alas bulat 500 mL diatruh 10 gram iodium, tambahkan
10 gram aseton.
2. Tambahkan sedikit demi sedikit dari corong pisah larutan NaOH
sebanyak 20 mL.(Bila terjadi panas dinginkan dibawah kran atau
bungkus dengan lap basah).
3. Segera setelah terjadi Kristal kuning diberi air yang banyak ( 300
mL).
4. Segera saring dengan corong Buchner
5. Cuci Kristal tersebut sampai filtrate tidak bereaksi alkalis lagi baru
boleh direkristalisasi dengan alcohol
6. Tentukan titik leburnya.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
BAB 3 METODE KERJA
3.1 Alat praktikum
Dalam praktikum ini, adapun alat yang digunakan yaitu corong
pisah, corong Buchner, labu alas bulat, dan statif.
3.2 Bahan praktikum
Adapun bahan yang digunakan dalam praktikum ini yakni 5 mL
aseton, alkohol, 5 gram iodium, aquades, dan NaOH.
3.3 Cara kerja
Disiapkan alat dan bahan. Ditimbang 5 gr iod lalu dimasukkan ke
dalam labu alas bulat (yang telah dibungkus aluminium foil) dan
dilarutkan dengan 5 mL aseton. Kemudian dihomogenkan. Pada
tempat yang lain, dimasukkan 10 mL NaOH ke dalam corong pisah.
Lalu ditambahkan sedikit demi sedikit NaOH ke dalam labu alas bulat,
hingga terbentuk Kristal kuning. Kemudian ditambahkan aquades
sebanyak 150 mL. Selanjutnya disaring dengan corong Buchner, dan
setelah itu Kristal yang tersaring dikeringkan di dalam oven.
BAB 4 HASIL DAN PEMBAHASAN
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
4.1 Hasil
4.1.1 Tabel Pengamatan
Berat
Berat kertas Berat kertas Berat
Sampel iodoform
saring saring + iod iodium
praktikum
Iodium 0,82 gram 2,543 gram 1,723 gram 5 gram
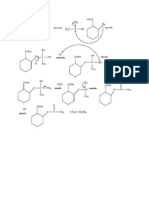
4.1.2 Reaksi
CH3-CO-CH3 + 3I2 CH3-CO-CI3 + 3HI
CH3-CO-CI3 + NaOH CHI3 + CH3-COONa
3NaOH + 3HI 3NaI + 3H2O
CH3-CO-CH3+3I2+4NaOH CHI3 + CH3COONa + 3NaI +
3H2O
4.1.3 Perhitungan
Dit : % rendamen
3 mol I2 setara dengan 1 mol CHI3
g iodium 5g
Mol I2 = =0,0196 m o l
BM iodium 254 ml
Mol CHI3 = 1/3 x mol I2
= 1/3 x 0,0196 mol
= 0,0065 mol
Berat teoritis = mol CHI3 x BM CHI3
= 0,0065 mol 393,78
= 2,56 gram
berat praktek
% rendamen = x 100
berat teori
1,723 gram
x 100
2,56 gram
= 67,304 %
4.4 Pembahasan
Iodoform merupakan senyawa yang dibentuk dari reaksi antara
iodin dengan etanol/aseton dan asetildehida dalam suasana basa.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Pada percobaan ini, bertujuan untuk mengetahui dan memahami cara
mensintesis iodoform dan mekanisme reaksi. Iodoform adalah
senyawa kimia yang dapat disintesis berdasarkan reaksi halogenasi.
Reaksi halogenasi ini adalah reaksi subtitusi atau pergantian 3 atom
hidrogen oleh atom iod pada bahan dasar dengan bantuan natrium
hidroksida sebagai katalisator.
Aadapun metode kerjanya yaitu disiapkan alat dan bahan,
Ditimbang 5 gr iod lalu dimasukkan ke dalam labu alas bulat (yang
telah dibungkus aluminium foil) dan dilarutkan dengan 5 mL aseton.
Kemudian dihomogenkan. Pada tempat yang lain, dimasukkan 10 mL
NaOH ke dalam corong pisah. Lalu ditambahkan sedikit demi sedikit
NaOH ke dalam labu alas bulat, hingga terbentuk Kristal kuning.
Kemudian ditambahkan aquades sebanyak 150 mL. Selanjutnya
disaring dengan corong Buchner, dan setelah itu Kristal yang tersaring
dikeringkan di dalam oven.
Adapun maksud dari penambahan segera dengan banyak air
setelah terjadibkrista iododform adalah untuk mengencerkan NaOH
yang mungkin berlebih, Filtrat yang terbentuk tidak boleh bersifat
alkalis maka pada rekristalisasi dengan alkohol maka iodoform akan
terurai dan kemungkinan akan dibebaskan iodium yang terlihat dengan
berwarna coklatnya larutan.
Penambahan NaOH sebaiknya menggunakan larutan pekat
tetapi tidak boleh berlebih. Untuk menghilangkan kelebihan asam pada
larutan. Dilakukan penambahan air banyak dengan segera setelah
terjadi Kristal iodoform dengan maksud mengencerkan NaOH yang
mungkin berlebih. Jadi mengurangi kecepatan hidrolisisnya iodoform
yang terjadi dengan NaOH. Kristal segera disaring agar filtrat tidak
bereaksi alkalis lagi, karena dengan adanya suasana alkalis maka
pada rekristalisasi dengan alcohol maka iodoform akan terurai dan
kemungkinan akan dibebaskan iodium yang terlihat dengan berwarna
coklatnya larut.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Dari hasil praktikum yang telah dilakukan diperoleh berat
%rendamen yaitu 67,304 %. Adapun kesalahan-kesalahan yang terjadi
yang menyebabkan hasil yang diperoleh tidak sempurna dan tidak
sesuai dengan teori karena pada saat pencampuran aseton dengan
iodium yang tidak merata, sehingga tidak terbentuk kristal kuning yang
sempurna.
BAB 5 PENUTUP
5.1 Kesimpulan
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Berdasarkan percobaan yang telah dilakukan, diperoleh
%rendamen yaitu 67,304 %
5.2 Saran
Agar memperoleh hasil yang maksimal dalam praktikum,
diharapkan kepada praktikum agar lebih teliti serta mengetahui
posedur kerja dalam percobaan , agar tidak terjadi kesalahan.
DAFTAR PUSTAKA
Anonim. 2017. Penuntun Praktikum Kimia Organik Sintesis. Makassar:
Universitas Muslim Indonesia.
Cairns, Donald. 2008. Intisari Kimia Farmasi.Jakarta : Penerbit Buku EGC.
Ditjen POM. 1979. Farmakope Indonesia Edisi ke-III. Jakarta:
Departemen Kesehatan RI.
Fessenden & Fessenden, 1982. Kimia Organik Jilid 2 Edisi III.
Erlangga :
Jakarta.
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Moore, John T. 2003. Kimia For Dummies. Indonesia : Pakar Raya.
Raharjo, Sentot B.2007. Kimia Berbasis Eksperimen. Solo : Yrama Widya.
Sunarya, Yayan. 2010. Kimia Dasar 1 Berdasarkan Prinsip-prinsip Kimia
Terkini.Bandung:Yrama Widya.
LAMPIRAN
a. Skema Kerja
Disiapkan alat dan bahan
Ditimbang 5 gr iod
Lalu dimasukkan ke dalam labu alas bulat (yang telah dibungkus
aluminium foil)
Dilarutkan dengan 5 mL aseton
Kemudian dihomogenkan
Pada wadah yang lain, dimasukkan NaOH 8 M ke dalam corong pisah
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
SINTESIS IODOFORM
Lalu ditambahkan sedikit demi sedikit NaOH 8 M ke dalam labu alas bulat,
hingga terbentuk Kristal kuning
Ditambahkan aquades sebanyak 150 mL
Selanjutnya disaring dengan corong Buchner
Setelah itu, Kristal yang tersaring dikeringkan di dalam oven
b. Foto Hasil Pengamatan
(Kristal Iodoform)
RAFIKA FIRDA U.HATIBIE. YSRAFIL
15020150028
Anda mungkin juga menyukai
- Laporan AspirinDokumen22 halamanLaporan Aspirinshella1680% (3)
- Tanaman Pepohonan Untuk Menjernihkan & Menetralisir Air Limbah Beracun Berbahaya Dari Kawasan Perairan Laut Sungai DanauDari EverandTanaman Pepohonan Untuk Menjernihkan & Menetralisir Air Limbah Beracun Berbahaya Dari Kawasan Perairan Laut Sungai DanauBelum ada peringkat
- Pembuatan AsetaldehidDokumen24 halamanPembuatan AsetaldehidIka Fajrin KurniaBelum ada peringkat
- Praktikum AspirinDokumen26 halamanPraktikum AspirinArbhy Indera I100% (3)
- Sintesis P NitroasetanilidaDokumen15 halamanSintesis P NitroasetanilidaFarida UtamiBelum ada peringkat
- Sintesis IodoformDokumen12 halamanSintesis IodoformPutri Pramita100% (2)
- IODOTESTDokumen15 halamanIODOTESTSepthya Nurul Nissa100% (3)
- Laporan Ko-Iodoform - VeroDokumen7 halamanLaporan Ko-Iodoform - VeroVeronika Purba100% (2)
- Sifat Kimia Dan Fisika IodoformDokumen1 halamanSifat Kimia Dan Fisika IodoformMikapinBelum ada peringkat
- OPTIMASI ASETALDEHIDDokumen23 halamanOPTIMASI ASETALDEHIDArief Wibisana100% (1)
- Laporan IodoformDokumen20 halamanLaporan IodoformAndi Sri MutmainnaBelum ada peringkat
- IodoformPembuatanDokumen11 halamanIodoformPembuatanKim Hye Nie100% (2)
- Etil AsetatDokumen16 halamanEtil AsetatShabila LintangBelum ada peringkat
- IODOFORMDokumen11 halamanIODOFORMSerli WahyunBelum ada peringkat
- Sintesis DibenzalasetonDokumen13 halamanSintesis DibenzalasetonMashiro Hikari100% (1)
- REAKSI IODOFORMDokumen7 halamanREAKSI IODOFORMDewi WulandhariBelum ada peringkat
- Percobaan Sintesis IodoformDokumen11 halamanPercobaan Sintesis IodoformVakhot SantikaBelum ada peringkat
- Percobaan I OrsinDokumen18 halamanPercobaan I OrsinFaradisa AninditaBelum ada peringkat
- Sintesis Asam BenzoatDokumen15 halamanSintesis Asam BenzoatAnii Voierfflichh67% (9)
- Sintesis AspirinDokumen14 halamanSintesis AspirinNUR RAHMADANI S1 FARMASI REGULER100% (2)
- Sintesis IodoformDokumen13 halamanSintesis IodoformYusuf Nur Cahyo100% (1)
- Reaksi Cannizzaro - Sintesis Benzil Alkohol Dan Asam Benzoat - FerrariskiDokumen9 halamanReaksi Cannizzaro - Sintesis Benzil Alkohol Dan Asam Benzoat - FerrariskiferrariskiBelum ada peringkat
- Halogenasi Oleh IodoformDokumen22 halamanHalogenasi Oleh Iodoformishm50% (2)
- IodoformDokumen13 halamanIodoformEdlia Fadilah MumtazahBelum ada peringkat
- Dasar TeoriDokumen8 halamanDasar TeoriRiska SeptiyaniBelum ada peringkat
- Laporan Rekristalisasi IodoformDokumen10 halamanLaporan Rekristalisasi IodoformMinny DevganBelum ada peringkat
- Laporan Lengkap Kos Sintesis IodoformDokumen15 halamanLaporan Lengkap Kos Sintesis IodoformWahyunial JansiskaBelum ada peringkat
- Laporan Sintesis IodoformDokumen14 halamanLaporan Sintesis IodoformFasalim RiadiBelum ada peringkat
- Sintesis IodoformDokumen19 halamanSintesis IodoformEllen NathaniaBelum ada peringkat
- Pembuatan Aspirin DapDokumen11 halamanPembuatan Aspirin DapDitoAPrasetyoBelum ada peringkat
- Laporan Farkin IntravnaDokumen21 halamanLaporan Farkin IntravnaRafika Firda Umamy HatibieBelum ada peringkat
- IodoformDokumen23 halamanIodoformpujiBelum ada peringkat
- Laporan Lengkap IodoformDokumen16 halamanLaporan Lengkap IodoformBeexy GamingBelum ada peringkat
- IodoformDokumen12 halamanIodoformknurulrBelum ada peringkat
- Laporan IodoformDokumen10 halamanLaporan IodoformBintoro Wisnu AdiBelum ada peringkat
- Iodoform 1Dokumen18 halamanIodoform 1Agus SalimBelum ada peringkat
- Makalah IodoformDokumen9 halamanMakalah IodoformRaga Dirgantara AnugrahBelum ada peringkat
- SINTESIS IODOFORMDokumen15 halamanSINTESIS IODOFORManricoBelum ada peringkat
- Percobaan 1 Iodoform-DikonversiDokumen17 halamanPercobaan 1 Iodoform-DikonversiFitri NurkhalizaBelum ada peringkat
- SINTESA IODOFORMDokumen17 halamanSINTESA IODOFORMIzkieflianiBelum ada peringkat
- IODOFORM REAKSIDokumen11 halamanIODOFORM REAKSIMelani JunaediBelum ada peringkat
- DAFTAR PUSTAKA DAN TEORI KIMIA ORGANIKDokumen24 halamanDAFTAR PUSTAKA DAN TEORI KIMIA ORGANIKCristiano Ebry100% (1)
- IodoformDokumen7 halamanIodoformSa'dur RifkiBelum ada peringkat
- IodoformDokumen2 halamanIodoformLusia DriktiBelum ada peringkat
- Sintesis Asam Salisilat Dari Minyak Gandapura Dan Uji Titik LelehDokumen6 halamanSintesis Asam Salisilat Dari Minyak Gandapura Dan Uji Titik LelehChristopher HermanBelum ada peringkat
- IODOFORMDokumen5 halamanIODOFORMRizky Dayu UtamiBelum ada peringkat
- Mekanisme Reaksi AspirinDokumen3 halamanMekanisme Reaksi AspirinTaufik Rahman100% (2)
- Laporan Kimia Organik Sintesis DibenzalasetonDokumen9 halamanLaporan Kimia Organik Sintesis DibenzalasetonRika MargarethaBelum ada peringkat
- IodoformPembahasanDokumen2 halamanIodoformPembahasanWidya AyuBelum ada peringkat
- Pembahasan Praktikum Pembuatan IodoformDokumen5 halamanPembahasan Praktikum Pembuatan IodoformnurfinaBelum ada peringkat
- Sintesis IodoformDokumen11 halamanSintesis IodoformrestiBelum ada peringkat
- PTL Dan IodoformDokumen21 halamanPTL Dan IodoformNur AlfiahBelum ada peringkat
- Laporan Kimorsin Asam SalisilatDokumen15 halamanLaporan Kimorsin Asam SalisilatAZima Hakim ATBelum ada peringkat
- IODOFORM SINTESISDokumen13 halamanIODOFORM SINTESISzulfa mahmudahBelum ada peringkat
- Kelompok 3 - IodoformDokumen16 halamanKelompok 3 - Iodoformcut puspitaBelum ada peringkat
- Laporan 6Dokumen10 halamanLaporan 6amani muflihahBelum ada peringkat
- Landasan Teori Iodoform KOSDokumen10 halamanLandasan Teori Iodoform KOSHalida SyahrahBelum ada peringkat
- PEMBENTUKAN IODOFORMDokumen7 halamanPEMBENTUKAN IODOFORMGraha Ditha Pratilajathi SiswamarganaBelum ada peringkat
- Contoh Sintesis IodoformDokumen9 halamanContoh Sintesis Iodoformeristya wardanaBelum ada peringkat
- 2 IodoformDokumen14 halaman2 IodoformWiri Resky Amalia0% (1)
- Laporan Lengkap Iodoform.Dokumen22 halamanLaporan Lengkap Iodoform.adrinianingsi Linggi'Belum ada peringkat
- Tugas FitoterapiDokumen9 halamanTugas FitoterapiRafika Firda Umamy HatibieBelum ada peringkat
- Makalah Asam Urat FikaDokumen11 halamanMakalah Asam Urat FikaRafika Firda Umamy HatibieBelum ada peringkat
- KIMEEEEDDokumen6 halamanKIMEEEEDRafika Firda Umamy HatibieBelum ada peringkat
- Novia Herawati Labudu 15020150043Dokumen4 halamanNovia Herawati Labudu 15020150043Rafika Firda Umamy HatibieBelum ada peringkat
- Makalah DindaDokumen1 halamanMakalah DindaRafika Firda Umamy HatibieBelum ada peringkat
- Isolasi dan Identifikasi Senyawa Kimia dari Ekstrak n-Heksan Batang Benalu Tanaman Jeruk (Dendrophtoe pentandra (L.)MiqDokumen6 halamanIsolasi dan Identifikasi Senyawa Kimia dari Ekstrak n-Heksan Batang Benalu Tanaman Jeruk (Dendrophtoe pentandra (L.)MiqVivin MarscellaBelum ada peringkat
- Salinan Terjemahan AJP 2 169Dokumen18 halamanSalinan Terjemahan AJP 2 169Rafika Firda Umamy HatibieBelum ada peringkat
- Novia Herawati Labudu 15020150043Dokumen3 halamanNovia Herawati Labudu 15020150043Rafika Firda Umamy HatibieBelum ada peringkat
- RANCANGAN OBAT BARUDokumen6 halamanRANCANGAN OBAT BARURafika Firda Umamy HatibieBelum ada peringkat
- Latar Belakang Kelompok 2 TemulawakDokumen4 halamanLatar Belakang Kelompok 2 TemulawakRafika Firda Umamy HatibieBelum ada peringkat
- Kandungan Flavonoid PDFDokumen10 halamanKandungan Flavonoid PDFRafika Firda Umamy HatibieBelum ada peringkat
- Laporan Farkin IntravnaDokumen21 halamanLaporan Farkin IntravnaRafika Firda Umamy HatibieBelum ada peringkat
- Fitriani Tamu PDFDokumen81 halamanFitriani Tamu PDFAzka TralalaBelum ada peringkat
- 06 Merah Ungu Antosianin PDFDokumen21 halaman06 Merah Ungu Antosianin PDFWildaYuniarBelum ada peringkat
- Teori ProduksiDokumen6 halamanTeori ProduksiRafika Firda Umamy HatibieBelum ada peringkat
- JENIS PENGENDALIANDokumen12 halamanJENIS PENGENDALIANRafika Firda Umamy HatibieBelum ada peringkat
- Sgot & SGPTDokumen16 halamanSgot & SGPTRafika Firda Umamy HatibieBelum ada peringkat
- KLTPDokumen17 halamanKLTPRafika Firda Umamy HatibieBelum ada peringkat
- KKKDokumen15 halamanKKKRafika Firda Umamy HatibieBelum ada peringkat
- Ekstraksi SampelDokumen8 halamanEkstraksi SampelRafika Firda Umamy HatibieBelum ada peringkat
- Makalah DindaDokumen1 halamanMakalah DindaRafika Firda Umamy HatibieBelum ada peringkat
- FRUKTOSA8Dokumen16 halamanFRUKTOSA8Natalia RevoanzBelum ada peringkat
- KKKDokumen15 halamanKKKRafika Firda Umamy HatibieBelum ada peringkat
- 9 Kromatografi Gas (KG)Dokumen18 halaman9 Kromatografi Gas (KG)Rafika Firda Umamy HatibieBelum ada peringkat
- KKKDokumen15 halamanKKKRafika Firda Umamy HatibieBelum ada peringkat
- Spektrometer MassaDokumen42 halamanSpektrometer MassaRafika Firda Umamy HatibieBelum ada peringkat
- Metode DPPH untuk Mengukur Aktivitas AntioksidanDokumen1 halamanMetode DPPH untuk Mengukur Aktivitas AntioksidanRafika Firda Umamy HatibieBelum ada peringkat
- 7 TLC DensitoDokumen88 halaman7 TLC DensitorioBelum ada peringkat
- POTENSI EKSTRAK DAUN PINUS SEBAGAI BIOHERBISIDA PENGHAMBAT PERKECAMBAHAN Echinochloa Colonum L. Dan Amaranthus Viridis.Dokumen5 halamanPOTENSI EKSTRAK DAUN PINUS SEBAGAI BIOHERBISIDA PENGHAMBAT PERKECAMBAHAN Echinochloa Colonum L. Dan Amaranthus Viridis.Latifatul FajriyahBelum ada peringkat