Informe Determinación de Fe en Un Jarabe
Diunggah oleh
Sebastian ViverosHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Informe Determinación de Fe en Un Jarabe
Diunggah oleh
Sebastian ViverosHak Cipta:
Format Tersedia
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
DETERMINACIN ESPECTROFOTOMETRICA DE Fe (II) EN UN PRODUCTO
FARMACEUTICO: CURVA DE ERROR
Lina Liseth Sandoval Yate (1538967), Kelly Johana Rojas Ortiz (1524798).
sandoval.lina@correounivalle.edu.co, kelly.rojas@correounivalle.edu.co
Programa: Tecnologa qumica (2131)
Fecha laboratorio: 01 de Septiembre de 2107
Fecha entrega: 08 de Septiembre de 2017
Docente: Harold Daz Segura
Palabras clave: absortividad molar, espectrofotmetro, curva de calibracin.
Resumen. En la prctica se determin por espectrofotometra la concentracin de hierro en un producto
farmacutico, se utiliz en este caso un jarabe. Para ello fue necesario la preparacin previa de una
solucin acetato de sodio 10% p/v, cloruro de hidroxilamina 10% p/v, 1-10 fenantrolina, HCl1%v/v y
soluciones estndar de hierro a partir de una solucin de 50ppm preparada previamente. Finalmente en el
espectrofotmetro se procedi a realizar un barrido espectral con una solucin de hierro de 2.0 ppm en un
intervalo de longitud de onda de 400 a 600 nm encontrando as un mximo de absorbancia de 512 nm, se
realiz la curva de error para mirar los intervalos donde el error relativo se hace menor y con base en esto
se pudo realizar una curva de calibracin. Obtenindose de la muestra problema una concentracin de
hierro 7782,2 ppm con un porcentaje de error de 3,13, con una absortividad molar de 10404,8 L/ mol x cm
con un error de 6,26%.
Clculos y resultados necesarios para obtener la solucin requerida y se
consignaron en la tabla 1.
Preparacin de soluciones
Se prepararon 25 mL de una solucin 2,0 ppm de Fe 25 [ ]
tomando como base una de 50 ppm, se realiz el [ ]
siguiente clculo para hallar los mL que se necesitaban. =
2,0 1000 Ec.1
50 = 2 50
1000 50 Concentracin Volumen de sln Volumen de sln
Luego se prepar una solucin de cloruro de 2,0 ppm (mL) 50 ppm (mL})
hidroxilamina al 10% p/v de la que se necesitaban 25 mL, 0,04 0,5 0
adicionalmente se elabor una solucin 10% p/v de 0,08 1,0 0
acetato de sodio (CH3COONa), a continuacin se 0,16 2,0 0
encuentran los respectivos clculos. 0,24 3,0 0
0,40 5,0 0
10 1,0 0 0,5
25 = 2,5
100 2,0 0 1,0
CHA: hidroxilamina 4,0 0 2,0
10
200 = 20 3 8,0 0 4,0
100 10,0 0 5,0
16,0 0 8,0
Posteriormente para realizar la solucin de 1-10
Tabla 1. Volumen de soluciones patrn
fenantrolina se utilizaron 0,05 g de monohidrato de 1-10
fenantrolina a la cual se le agreg 1 mL de etanol
A cada solucin patrn se le adicionaron 1 mL de cloruro
diluyendo en 10 mL de agua tibia y enrasando a 50mL y
de hidroxilamina, 2,5 mL de solucin de 1-10
para realizar los 200 mL de HCl al 1% v/v se
fenantrolina, 8,0 mL de solucin de acetato de sodio y se
cuantificaron los mL necesarios as:
enras con agua. Se llev acabo el mismo procedimiento
1 1,18 100 para la preparacin del blanco, teniendo en cuenta que
200 = 6,37 no se le adicionaba el analto en cuestin.
100 1 37
Consecutivamente se realiz un barrido espectral usando
Soluciones patrn la solucin que contena 2,0 ppm de Fe para visualizar la
Para preparar las soluciones estndar con las que se longitud de onda con mayor absorcin usando el blanco
trabajaron, se realiz una ecuacin general [Ec 1] en la como referencia, los resultados se encuentran en la tabla
que utilizando el anlisis dimensional se hallan los mL de 2.
la solucin patrn (ya sea de 2 o 50 ppm de Fe)
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
(nm) Abs Para realizar la curva de Crawford con el fin de
establecer el intervalo en el cual el error cometido
400 0,108
experimental es mnimo, para esto es necesario utilizar
420 0,177 los datos de absorbancia de las soluciones estndar, se
440 0,232 puede calcular la transmitancia usando la Ecuacin 3,
ahora con ese resultado se puede obtener la curva de
460 0,281
error usando la Ecuacin 4, considerando un error
480 0,330 fotomtrico constante de = 0,05%. Los datos
500 0,345 resultantes de la aplicacin de las ecuaciones se
encuentran en la tabla 3.
502 0,348
504 0,350 Solucin A T %T C/C
506 0,353 patrn
508 0,356 (ppm)
510 0,537 0,04 -0,09 1,230 123,026 0,195
512 0,358 0,08 -0,04 1,096 109,647 0,494
514 0,357 0,16 0,012 0,972 97,274 -1,858
516 0,355 0,24 0,020 0,954 95,499 -1,136
518 0,350 0,40 0,048 0,895 89,536 -0,504
520 0,343
1,00 0,177 0,665 66,527 -0,184
540 0,196
2,00 0,348 0,448 44,874 -0,138
560 0,063
580 0,018 4,00 0,723 0,189 18,923 -0,158
600 0,002 8,00 1,480 0,033 3,311 -0,442
10,00 1,818 0,015 1,520 -0,784
Tabla 2. Datos de barrido espectral con solucin de 2,0
ppm de Fe 16,00 1,889 0,012 1,291 -0,889
Tabla 3. Datos curva de Crawford
Espectro de absorcin de Fe % = 10 100 [. 3]
0,434
0.4 = [. 4]
log
0.35
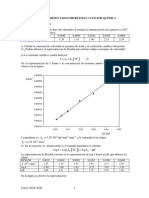
Con la tabla 3 se realiza la curva de Crawford (C/C vs
0.3
%T)
Absorcin
0.25
0.2
0.15
Curva de error relativo
0.1 1
0.05
0.5
0
350 400 450 500 550 600 650 0
(C/C)
Longitud de onda () -20 30 80 130
-0.5
Grfica 1. Espectro de absorcin del Fe (Absorcin vs -1
Longitud de onda)
En la grfica se evidencia que la longitud de onda con -1.5
mayor absorcin se encontr en 510 nm. -2
%T
Curva de error
Se midi la absorbancia emitida por las soluciones que Grfica 2.Curva de error relativo de las concentraciones
estaban a diferente concentracin, usando el blanco vs % de transmitancia.
como referencia y ajustando la longitud de onda de
mayor absorcin obtenida en el barrido espectral.
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
Segn la grfica 2, la curva de error nos indica cuales Tabla 5. Datos usados para la curva de calibracin luego
son las concentraciones que tienen mejor linealidad y por de analizar la curva de error.
lo tanto menor error relativo posible, el rango oscila entre
las concentraciones de 0,24 a 4,0 ppm. Curva de calibracin
Para obtener un mejor intervalo ptimo de 0.800
concentraciones que la curva de Crawford se procede a 0.700
y = 0.1863x - 0.0215
construir la curva de Ringbom (grfica 3), que consiste en 0.600
R = 0.9994
Absorbancia
construir una grfica de absorbancia (100- %T) vs. Log 0.500
[Concentracin], Para realizar esta curva se consigna los
0.400
datos en la tabla 4.
0.300
Log 100-%T 0.200
[Concentracin] 0.100
-1,398 -23,027 0.000
0 1 2 3 4 5
-1,097 -9,648
Concentracin (ppm)
-0,796 2,725
-0,620 4,501 Grfica 4. Curva de calibracin
-0,398 10,464
Determinacin de concentracin de Fe
0 33,473
En el tratamiento de la muestra se utiliza un jarabe con
0,301 55,125 803,33 mg Fe por 100 mL de jarabe, inicialmente se
0,602 81,077 adicionan 0,5 mL de este y 4,0 mL de HCl concentrado,
se procede a digestar calentndolo en una plancha hasta
0,903 96,689
que el volumen se disminuy a la mitad, luego de que se
1,000 98,479 enfri se adicionaron 10 mL de agua y se filtr, se
1,204 98,709 realizaron lavados con HCl 1% v/v hasta que completo
Tabla 4.Datos para curva de Ringbom los 100 mL del matraz, simultneamente se prepar un
blanco llevando a cabo el mismo procedimiento pero sin
adicionar el analito.
Curva de Ringbom Se hall la concentracin de Fe en el jarabe realizando el
siguiente clculo.
150.000 8033,3 1
0,5 = 40,16
1000 0,1
100.000
Para realizar la solucin 2,0 ppm de Fe a partir de la
100-%T
50.000 solucin preparada anteriormente se hallan los mL
necesarios as:
0.000 2 1000
25 = 1,24
-2.000 -1.500 -1.000 -0.500 0.000 0.500 1.000 1.500 1000 40,167
-50.000 Luego de mezclar los mL de solucin necesaria con agua
Log [Fe] se adicionan los mismos reactivos utilizados en las
soluciones patrn del primer punto.
Grfica 3.Curva de Ringbom
La muestra se deja reposar normalmente 15 minutos y se
Teniendo en cuenta la curva de error se decide tomar los toman las respectivas absorbancias en el
puntos de mejor linealidad y representarlos en una tabla. espectrofotmetro, el trabajo se realiza por duplicado y
(Tabla 5) para proceder a realizar la curva de se obtienen las absorbancias correspondientes a una
calibracin.(Grfica 4) longitud de onda de 512 nm.
Concentracin (ppm) Absorbancia Absorbancia muestra 1: 0,338
0,24 0,02 Absorbancia muestra 2:0,258
0,40 0,048
1,0 0,177 Con la grfica 4 (Curva de Beer o de calibracin) se
2,0 0,348 determin el comportamiento del sistema siendo ste
4,0 0,723 lineal y obedece a la siguiente ecuacin:
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
= 0.1863 0,0215
A partir de sta ecuacin podemos determinar la Anlisis de resultados
concentracin de la muestra siempre y cuando su La base de la espectroscopia Visible y Ultravioleta
absorbancia est en el intervalo de la curva. consiste en medir la intensidad del color (o de la
radiacin absorbida en UV) a una longitud de onda
+ 0.0215
= especfica comparndola con otras soluciones de
0,1863 concentracin conocida (soluciones estndar) que
0.338 + 0.0215
contengan la misma especie absorbente. Para tener
= esta relacin se emplea la Ley de Beer, que
0.1863
establece que para una misma especie absorbente
= 1,93 en una celda de espesor constante, la absorbancia
es directamente proporcional a la concentracin.
Concentracin de Fe en la muestra
Uno de los instrumentos utilizados en esta tcnica
1,93 25 100 1000 es el espectrofotmetro, para la determinacin de
1000 1,24 0.5 1 hierro en la prctica se utiliz uno de un solo haz, en
= 7782,2 el cual el haz de luz sigue una nica trayectoria entre
la fuente y el detector, normalmente se debe saber
Concentracin de Fe en la muestra expresada en en qu rango aproximado de longitud de onda
ppm de FeSO4 presenta seales significativas de absorbancia, es
necesario para poder programarlo. A continuacin en
7782,2 1 1 4 la imagen 1 se puede apreciar el tipo de
1000 55.85 1 espectrofotmetro que se us.
151.91 4
1 4
= 21,16 4
| .|
% = 100 [Ec. 5]
|8033,3 7782,2|
% = 100
8033,3
% = 3,13%
Absortividad molar del complejo Fe-(Fenantrolina)
Con la pendiente de grfica 4, podemos determinar el
coeficiente de absorcin molar de la siguiente manera:
0.1863 1 Imagen 1. Espectrofotmetro Genesys 20
=
1.00
Componentes
1000 55,85
= 0.1863 1 1. Interruptor de encendido/apagado
1 1 2. Pantalla digital
3. Tapa de compartimiento de muestras
= 10404,81 1 4. Teclado
5. Impresora interna opcional
|1110010404,8|
% = 100 6. Puerta del compartimiento de la lmpara
11100
% = 6,26% En este espectrofotmetro se trabaja en el rango visible
ya que el complejo del 1,10-fenantrolina con el hierro
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
crea un complejo fuerte de color rojo cuya forma los reactivos no reaccionen completamente y haya una
correspondiente oxidada da lugar a un color azul, el prdida de analito.
complejo (Imagen 2) obedece la ley de Beer para
concentraciones de Fe (II) inferiores a 9ppm, ya que para Conclusiones.
concentraciones superiores a esta pierde su linealidad. Se puede atribuir el porcentaje de error calculado en la
Por esto al trabajar en concentraciones de 2ppm el determinacin del hierro al no identificar las limitaciones
porcentaje de error es muy bajo. Se puede comprobar de la ley de Lamber-Beer. Para una aplicacin
con la longitud de onda de mxima intensidad obtenida espectrofotomtrica es necesario conocer las limitaciones
en este laboratorio que fue de 512nm y en la literatura la de la ley minimizando las desviaciones de la misma y
longitud de onda mxima para el complejo que se form poder obtener resultados ms exactos, seleccionar la
esta reportada con un intervalo de 510nm-512nm longitud de onda mxima es una prioridad ya que la
Absorbancia (A) y la Absortividad Molar () varan con
respecto a esta. Otra limitacin real de dicha ley es el
caso de que las soluciones utilizadas deben estar en
concentraciones inferiores a 0.01M. A concentraciones
ms altas, la distancia entre las molculas absorbentes
disminuye ocasionando que cada una de ellas afecte la
distribucin de carga de las dems. Esta interaccin
altera la cantidad de radiacin de determinada longitud
de onda que puede absorber ocasionando que algunas
necesiten ms radiacin que otras que no fueron afectas
Imagen 2.Reaccin hierro-fenatrolina su distribucin de carga.
En la grfica 2 en la que se observa la curva de error o Preguntas
curva de Crawford, se puede apreciar que en 1) Suponiendo un error fotomtrico del 1%,
disoluciones concentradas y diluidas existe un error ms demuestre matemticamente que el error en la medicin
grande, en el caso de las altas concentraciones hay un de la transmitancia es mnimo cuando el valor es
mayor error debido a que las molculas de soluto alrededor del 37%.
interaccionan entre s debido a su proximidad. Cuando El error absoluto cometido en la determinacin de la
las molculas del soluto se aproximan entre s, sus concentracin, para un cierto error de lectura de
propiedades cambian en algo. A concentraciones muy transmitancia es pequeo, pero al ser pequea la
altas, los solutos se convierten prcticamente en concentracin, el error relativo puede ser grande.
disolvente, para concentraciones de soluto
suficientemente altas el ndice de refraccin cambia y la Como se indica a continuacin se puede demostrar
variacin de la absorbancia parece no obedecer la ley de que el mnimo error relativo se obtiene para una
Beer.[1] Al igual en las concentraciones bajas la deteccin absorbancia de 0.434.
en la absorcin va a ser muy pequea y arrojar que no
La primera derivada de la ley de Beer es:
hay cantidad significativa de soluto.
Cuando se analiza la curva de error, es necesario =
descartar las absorbancias tomadas de las =
concentraciones tanto bajas como altas debido a lo que =
se explic anteriormente, finalmente se escogi un rango
entre 0,24 y 4,0 ppm de Fe para no tener la tendencia Donde dT representa el error indeterminado en la
de desviarse de la ley de Beer . lectura de la escala de transmitancia y dC indica la
incertidumbre en la concentracin.
Posteriormente en la grfica 3 se realiz la curva de Se tiene que = 0,434
Ringbom que puede ser usada para obtener el intervalo
ptimo de concentraciones en la cual la absorbancia se
=
comporta de forma lineal, esta se elabora mediante la
magnitud de 100-%T en el eje Y y en el eje x se =
representan la funcin Log de la concentracin en ppm. Se obtiene:
= 0,434 ()
Se puede decir que el porcentaje de error en las
muestras aunque es relativamente bajo puede deberse a
las diluciones y a no dejar una de las muestras reposar Derivando esta ecuacin de nuevo e igualando a
los 15 minutos requeridos, esto provoca que al enrasar cero, se obtiene que la transmitancia ptima
LABORATORIO DE ANLISIS ISNTRUMENTAL - UNIVERSIDAD DEL VALLE
corresponde a 36.8 % o 37% que equivale a una
absorbancia de 0.434.[y] Bibliografa.
Reemplazando T y T respectivamente como 1% y [1] Harris, D; Espectrofotometra. En Anlisis qumico
cuantitativo; Paniagua R; Grupo editorial Iberoamrica.
37% en la ecuacin (Ec.2) se tiene:
C 0.434 (1%) Mxico. ( pg. 499- 500).
= 0.37 log(0.37) [Ec 2]
C
[Y] Espectrofotometra de absorcin ultravioleta-visible
= 2.716% mnimo error pg. 8- pg. 9 http://ocw.usal.es/ciencias-
experimentales/analisis-aplicado-a-la-ingenieria-
quimica/contenidos/course_files/Tema_3.pdf (Revisado el
2) Explique porque hay perdida de la linealidad a 06 de Septiembre del 2017)
concentraciones altas del analito
La prdida de linealidad a concentraciones altas de
analto se puede atribuir a cambios en las especies
absorbentes o en las propiedades de la solucin. 2. Apellido, Inicial del nombre; Apellido, Inicial del nombre
Conforme una solucin se vuelve ms concentrada las (Ao). Ttulo del capitulo. En: ttulo del libro en letra cursiva.
molculas de soluto interactan entre si debido a su Apellido del Editor e Inicial del nombre. Editorial, Pas de
proximidad. Cuando una molcula interacta con otra, es edicin. pg-pg.
probable que cambien las propiedades elctricas de
ambas (incluyendo la absorcin de luz). En el caso
excepcional de una solucin muy concentrada el soluto Autores,direccin web, fecha de revision
se convierte en solvente.
Debido a esto se puede decir que no se espera que las
propiedades elctricas de la molcula sean las mismas
en diferentes solventes. En algunos casos, solutos que
no absorben pueden interactuar con las especies
absorbentes y modificar la absortividad aparente.
Para concentraciones de soluto suficientemente altas el
ndice de refraccin cambia y la variacin de la
absorbancia parece no obedecer la ley de Beer.[1]
3) Explique claramente como realizara la
especiacin del Fe (Fe3+ y Fe2+) en la muestra mediante
un mtodo espectrofotomtrico.
La dificultad en la especiacin del hierro es que se
requiere medir las diferentes especies en las que se
puede encontrar, la forma cambiante Fe2+ al igual que
Fe3+, cuya interconversin depende fuertemente del valor
de pH, por esto para hacer la especiacin de Fe3+ y Fe2+,
se debe tratar con un agente reductor como el cloruro de
hidroxilamina y mantenerla sellada hasta el momento de
realizar el anlisis para evitar la oxidacin a Fe+3, a esta
muestra es conveniente agregar fenantrolina utilizndolo
como ligando ya que forma complejos fuertes, se
adiciona en exceso para obtener una solucin coloreada,
adicionalmente agregar acetato de sodio que acta para
formar la correspondiente base conjugada y as regular el
pH, posteriormente se lleva a 25 ml con agua destilada y
finalmente se realizan las lecturas de absorbancia a 512
nm. En estos mtodos normalmente se determina el
contenido de Fe2+, y el Fe3+ se calcula por diferencia,
con respecto al hierro total
Anda mungkin juga menyukai
- HPLC Kevin Maru PDFDokumen11 halamanHPLC Kevin Maru PDFFoxy4DBelum ada peringkat
- Informe 04 Analisis InstrumentalDokumen5 halamanInforme 04 Analisis InstrumentalJorge Luis CastilloBelum ada peringkat
- Centrum 11Dokumen3 halamanCentrum 11Roberto Andres Delgado MillanBelum ada peringkat
- Taller EstadisticaDokumen10 halamanTaller EstadisticaMICHEL ADOLFO ANGEL OSPINABelum ada peringkat
- Informe #2Dokumen4 halamanInforme #2María Liliana Vargas TabordaBelum ada peringkat
- Solucion Leccion 6Dokumen15 halamanSolucion Leccion 6DanielBelum ada peringkat
- Volumetria Oxido Reducciòn PermanganometriaDokumen6 halamanVolumetria Oxido Reducciòn PermanganometriaAndres MorenoBelum ada peringkat
- Análisis de Una Mezcla de Carbonato y BicarbonatoDokumen4 halamanAnálisis de Una Mezcla de Carbonato y BicarbonatoValentina CardenasBelum ada peringkat
- Análisis de carbonatos y fosfatosDokumen8 halamanAnálisis de carbonatos y fosfatosJUAN CAMILO GONZALEZ NAVARRETEBelum ada peringkat
- Determinación de la acidez de vinagre y vinoDokumen5 halamanDeterminación de la acidez de vinagre y vinoAlexander VivasBelum ada peringkat
- Determinación Del Contenido de Hipoclorito Sódico en Un Producto Comercial y El Contenido de Yodo en Un Antiséptico BucalDokumen9 halamanDeterminación Del Contenido de Hipoclorito Sódico en Un Producto Comercial y El Contenido de Yodo en Un Antiséptico BucalGabriela CoyBelum ada peringkat
- Análisis de cloruros por métodos argentométricosDokumen7 halamanAnálisis de cloruros por métodos argentométricosAngie AyalaBelum ada peringkat
- Carbonato y FosfatoDokumen7 halamanCarbonato y FosfatoJuanka GonzalezBelum ada peringkat
- Determinación de etanol por CGDokumen6 halamanDeterminación de etanol por CGharold diazBelum ada peringkat
- CL en Orina y SueroDokumen15 halamanCL en Orina y SueroAngelo MolinaBelum ada peringkat
- Validacion de Etanol Por Cromotografia de GasesDokumen19 halamanValidacion de Etanol Por Cromotografia de GasesNash MoralesBelum ada peringkat
- PRÁCTICA 6 Aspirina PREVIASDokumen7 halamanPRÁCTICA 6 Aspirina PREVIASFernanda100% (1)
- Determinacion Del Contenido de Nitrog No Por El M Todo de MicroKjeldahlDokumen5 halamanDeterminacion Del Contenido de Nitrog No Por El M Todo de MicroKjeldahlLeonel Luna NawnesterBelum ada peringkat
- Orina y SueroDokumen9 halamanOrina y SueroMARTHA LORENA ZAMBRANO NAVAS100% (2)
- INFORME 3 Alfa AmilasaDokumen9 halamanINFORME 3 Alfa AmilasalauraBelum ada peringkat
- PRÁCTICA N 6 María Paula Carvajal NaviaDokumen9 halamanPRÁCTICA N 6 María Paula Carvajal NaviaMaría Paula Carvajal NaviaBelum ada peringkat
- Informe 1 Lab BioquimicaDokumen8 halamanInforme 1 Lab BioquimicalauraBelum ada peringkat
- Informe 3. Determinación de Nitrogeno Por El Metodo de MicrokjhdalDokumen5 halamanInforme 3. Determinación de Nitrogeno Por El Metodo de MicrokjhdalCarolina LemusBelum ada peringkat
- Informe Determinación de Nitrogeno en Alimentos (Definitivo)Dokumen4 halamanInforme Determinación de Nitrogeno en Alimentos (Definitivo)anon_315528371Belum ada peringkat
- Prácticas de Analítica II VoltamperometríaDokumen6 halamanPrácticas de Analítica II VoltamperometríaAlberto Romero GraciaBelum ada peringkat
- Taller Disoluciones y DilucionesDokumen1 halamanTaller Disoluciones y DilucionesYenifer Alejandra Diaz Chala0% (1)
- Determinación de Calcio en Leche Por Espectrometría de Absorción AtómicaDokumen4 halamanDeterminación de Calcio en Leche Por Espectrometría de Absorción AtómicaChiran AlexisBelum ada peringkat
- Práctica 6Dokumen39 halamanPráctica 6Ernesto OlguínBelum ada peringkat
- INFORME DE LABORATORIO No 5.1Dokumen6 halamanINFORME DE LABORATORIO No 5.1haroldoBelum ada peringkat
- Informe ViscosidadDokumen6 halamanInforme ViscosidadAntony possoBelum ada peringkat
- CROMATOGRAFIA DE CAPA FINA Y DE COLUMNA (Informe)Dokumen11 halamanCROMATOGRAFIA DE CAPA FINA Y DE COLUMNA (Informe)Anthony Carhuaz AncheliaBelum ada peringkat
- Electrogravimetria y ColumbimetríaDokumen5 halamanElectrogravimetria y Columbimetría05-FB-HU-EDISON PEREZ PAUCARBelum ada peringkat
- Cuantificación de etanol en bebidas alcohólicas mediante refractometríaDokumen4 halamanCuantificación de etanol en bebidas alcohólicas mediante refractometríaDavid Valencia CarreñoBelum ada peringkat
- Determinación de La Concentración de Calcio y Cobre Por Una Titulación FotométricaDokumen13 halamanDeterminación de La Concentración de Calcio y Cobre Por Una Titulación Fotométricavanessa lopezBelum ada peringkat
- Analisis de Minerales Por Absorcion Atomica en Una Muestra de CabelloDokumen6 halamanAnalisis de Minerales Por Absorcion Atomica en Una Muestra de CabelloLorena ZambranoBelum ada peringkat
- Determinación Potenciométrica de Cloruros 2123Dokumen13 halamanDeterminación Potenciométrica de Cloruros 2123wendyBelum ada peringkat
- PRACTICA 2. Estandarización de HCL y NaOH.Dokumen4 halamanPRACTICA 2. Estandarización de HCL y NaOH.Sofia Paredes OrtizBelum ada peringkat
- Análisis de FármacosDokumen4 halamanAnálisis de FármacossamantaBelum ada peringkat
- Informe de Lab Oratorio de Analisis Instrumental Cromatografia de Gases 2Dokumen5 halamanInforme de Lab Oratorio de Analisis Instrumental Cromatografia de Gases 2Oscar Armando Perez BenitezBelum ada peringkat
- Informe Sal de Mohr JeffersonDokumen5 halamanInforme Sal de Mohr JeffersonJeffer ZuñiigaBelum ada peringkat
- Determinación del benzoato de metilo mediante espectroscopía IRDokumen8 halamanDeterminación del benzoato de metilo mediante espectroscopía IRwendyBelum ada peringkat
- 10 Yodometría - YodimetríaDokumen3 halaman10 Yodometría - YodimetríaJeins SalazarBelum ada peringkat
- Preparacin de Anhdrido 9,10-DihidroantracenoDokumen15 halamanPreparacin de Anhdrido 9,10-DihidroantracenoMaribel Urrea Pelayo50% (2)
- Determinación de nitrógeno y proteína por MicroKjeldahlDokumen2 halamanDeterminación de nitrógeno y proteína por MicroKjeldahlLEONARDO CRUZ ELEJALDEBelum ada peringkat
- Determinacion Potenciometrica de Cloruros 1Dokumen10 halamanDeterminacion Potenciometrica de Cloruros 1Amarië FelagundBelum ada peringkat
- Determinación Espectrofotométrica de HierroDokumen6 halamanDeterminación Espectrofotométrica de HierroValentina LunaBelum ada peringkat
- Informe 4-Análisis Instrumental - Becerra y Montoya PDFDokumen9 halamanInforme 4-Análisis Instrumental - Becerra y Montoya PDFandres felipe montoya bolañosBelum ada peringkat
- Deberes 3 - Contraste Hipótesis-Y Anova (Recuperado)Dokumen16 halamanDeberes 3 - Contraste Hipótesis-Y Anova (Recuperado)SthefiiEnriquezBelum ada peringkat
- Informe 3-Espectroscopia de Absorcion AtomicaDokumen4 halamanInforme 3-Espectroscopia de Absorcion Atomicaleidy carolina peña ardilaBelum ada peringkat
- Cinética de La Oxidación Del Ácido Ascórbico Por El IonDokumen16 halamanCinética de La Oxidación Del Ácido Ascórbico Por El IonOscar Ramirez BermeoBelum ada peringkat
- EQUILIBRIO DE SOLUBILIDAD Info Largo Fisico2Dokumen5 halamanEQUILIBRIO DE SOLUBILIDAD Info Largo Fisico2David Colorado VegaBelum ada peringkat
- 1.manejo de La Balanza Analítica y Análisis Estadístico de DatosDokumen5 halaman1.manejo de La Balanza Analítica y Análisis Estadístico de DatosAndres Joaqui100% (1)
- Cuantificación de cafeína en productosDokumen3 halamanCuantificación de cafeína en productosrame ameBelum ada peringkat
- Identificación y Cuantificación de Vitamina Cpor Cromatografía Líquida de Alta ResoluciónDokumen6 halamanIdentificación y Cuantificación de Vitamina Cpor Cromatografía Líquida de Alta ResoluciónsamantaBelum ada peringkat
- Granulación húmeda APIDokumen14 halamanGranulación húmeda APIIveth Patricia Betacourth OrobioBelum ada peringkat
- Reporte 3. - ConductimetríaDokumen10 halamanReporte 3. - ConductimetríaJorge Adrian Pérez Trejo100% (1)
- Determinacion de Fe en Un JarabeDokumen6 halamanDeterminacion de Fe en Un JarabenataBelum ada peringkat
- Determinación de Fe en jarabeDokumen8 halamanDeterminación de Fe en jarabeKoko BeautyBelum ada peringkat
- HPLCDokumen7 halamanHPLCharold diazBelum ada peringkat
- Problemas resueltos de Hidráulica de CanalesDari EverandProblemas resueltos de Hidráulica de CanalesPenilaian: 4.5 dari 5 bintang4.5/5 (7)
- Taller 1 de BioquímicaDokumen4 halamanTaller 1 de BioquímicaSebastian ViverosBelum ada peringkat
- Taller CogeneracionDokumen5 halamanTaller CogeneracionSebastian ViverosBelum ada peringkat
- Trigeneración- Gerencia de plantasDokumen4 halamanTrigeneración- Gerencia de plantasSebastian ViverosBelum ada peringkat
- Taller CogeneracionDokumen5 halamanTaller CogeneracionSebastian ViverosBelum ada peringkat
- Cálculos y Resultados ZINC Y COBREDokumen2 halamanCálculos y Resultados ZINC Y COBRESebastian ViverosBelum ada peringkat
- Tarea 1Dokumen1 halamanTarea 1Sebastian ViverosBelum ada peringkat
- Materiales BioinspiradosDokumen1 halamanMateriales BioinspiradosSebastian ViverosBelum ada peringkat
- Trabajo FinalDokumen17 halamanTrabajo FinalSebastian ViverosBelum ada peringkat
- Qué Es La Biodigestión PDFDokumen2 halamanQué Es La Biodigestión PDFSteve Freddy Santivañez OrellanaBelum ada peringkat
- Clase 4 Cogeneración 2019 PDFDokumen103 halamanClase 4 Cogeneración 2019 PDFSebastian ViverosBelum ada peringkat
- Lab1 - Titulacion Acido-BaseDokumen11 halamanLab1 - Titulacion Acido-BaseSebastian ViverosBelum ada peringkat
- Dqo Informe FinalDokumen3 halamanDqo Informe FinalSebastian ViverosBelum ada peringkat
- Tarea 1Dokumen2 halamanTarea 1Sebastian ViverosBelum ada peringkat
- Cloruros InformeDokumen8 halamanCloruros InformeSebastian ViverosBelum ada peringkat
- Cálculos y ResultadosDokumen1 halamanCálculos y ResultadosSebastian ViverosBelum ada peringkat
- Relación O2-absorbancia mediante calibraciónDokumen2 halamanRelación O2-absorbancia mediante calibraciónSebastian ViverosBelum ada peringkat
- CómoFuncionaCámaraReflexDokumen2 halamanCómoFuncionaCámaraReflexSebastian ViverosBelum ada peringkat
- Cálculos y Resultados (Refractometria y Polarimetria)Dokumen5 halamanCálculos y Resultados (Refractometria y Polarimetria)Sebastian ViverosBelum ada peringkat
- Vitamina C CineticaDokumen1 halamanVitamina C CineticaSebastian ViverosBelum ada peringkat
- Fichjas BiliograficasDokumen4 halamanFichjas BiliograficasSebastian ViverosBelum ada peringkat
- Ley de OhmDokumen11 halamanLey de OhmSebastian ViverosBelum ada peringkat
- AstronomiaDokumen2 halamanAstronomiaSebastian ViverosBelum ada peringkat
- Parte Infrome LipidosDokumen3 halamanParte Infrome LipidosSebastian ViverosBelum ada peringkat
- IntroDokumen1 halamanIntroSebastian ViverosBelum ada peringkat
- DETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolDokumen4 halamanDETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolSebastian ViverosBelum ada peringkat
- DETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolDokumen4 halamanDETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolSebastian ViverosBelum ada peringkat
- Qué Son Los TricomasDokumen2 halamanQué Son Los TricomasSebastian ViverosBelum ada peringkat
- Determinación viscosidad glicerolDokumen4 halamanDeterminación viscosidad glicerolSebastian ViverosBelum ada peringkat
- Determinacion Del Coeficiente de Difusion en Un Gel de Azul de BromofenolDokumen5 halamanDeterminacion Del Coeficiente de Difusion en Un Gel de Azul de BromofenolSebastian ViverosBelum ada peringkat
- Resueltos ElasticidadDokumen7 halamanResueltos ElasticidadLuis Brayan Alejo100% (1)
- Las Capas de La TierraDokumen4 halamanLas Capas de La TierraCamila QuinteroBelum ada peringkat
- FlamaDokumen1 halamanFlamaDiego VegaBelum ada peringkat
- Algebra I BimDokumen24 halamanAlgebra I BimantonioBelum ada peringkat
- Examen DecimalesDokumen1 halamanExamen DecimalessitemironoteveoBelum ada peringkat
- Resolucion de Ecuaciones Mediante El Uso de Integrados 741Dokumen13 halamanResolucion de Ecuaciones Mediante El Uso de Integrados 741Luis SanchezBelum ada peringkat
- ACE6000 - User Guide ESP PDFDokumen142 halamanACE6000 - User Guide ESP PDF945288090% (3)
- Diseño mezcla ACI método cantera El GavilánDokumen3 halamanDiseño mezcla ACI método cantera El GavilánMardelin Raquel Flores LlanosBelum ada peringkat
- Contenidos Minimos de Un Proyecto de Instalaciones ElectricasDokumen37 halamanContenidos Minimos de Un Proyecto de Instalaciones ElectricasBrrt LuisBelum ada peringkat
- Tarea 2 - Andres ArizaDokumen3 halamanTarea 2 - Andres ArizaMauricio Herrera AnturiBelum ada peringkat
- Drivadas Parciales (Trabajo Escrito)Dokumen5 halamanDrivadas Parciales (Trabajo Escrito)Carlos CansecoBelum ada peringkat
- Redvit ProyectoDokumen14 halamanRedvit ProyectoYarinia MontesinosBelum ada peringkat
- Tema N°2 Lenguaje C WordDokumen27 halamanTema N°2 Lenguaje C WordLuis MurilloBelum ada peringkat
- Actividad 7 Medición de CaudalDokumen5 halamanActividad 7 Medición de Caudalalberto martinezBelum ada peringkat
- Mate 3Dokumen11 halamanMate 3María OgliastreBelum ada peringkat
- ProbabilidadesDokumen46 halamanProbabilidadesMauricio San Martín SalinasBelum ada peringkat
- Anc3a1lisis y Sintesis de Mecanismos 14 Junio2011Dokumen12 halamanAnc3a1lisis y Sintesis de Mecanismos 14 Junio2011Anonymous K2Lz2QljcJBelum ada peringkat
- Informe de LipidosDokumen5 halamanInforme de LipidosFabiana TorresBelum ada peringkat
- Spinoza y El Psicoanálisis - Nora Trosman - Página - 12 - Psicología - "Resistir A Toda Ilusión"Dokumen1 halamanSpinoza y El Psicoanálisis - Nora Trosman - Página - 12 - Psicología - "Resistir A Toda Ilusión"Lucas GrinsteinBelum ada peringkat
- Tarea 2Dokumen4 halamanTarea 2DANTE QUIJOTEBelum ada peringkat
- Tema 20FUERZA ELECTRICADokumen2 halamanTema 20FUERZA ELECTRICAPercy Torres Avalos KeplerBelum ada peringkat
- Respiración de semillas germinadasDokumen6 halamanRespiración de semillas germinadasMishell B. Caballero ErazoBelum ada peringkat
- Paralaje Estelar, BesselDokumen3 halamanParalaje Estelar, BesselDaniel MirandaBelum ada peringkat
- Turbinas y CompresoresDokumen3 halamanTurbinas y CompresoresLizanyeli Gonzalez0% (1)
- Tema 24Dokumen7 halamanTema 24AnaFerLyl100% (1)
- PRACTICA N°04 y #05Dokumen5 halamanPRACTICA N°04 y #05Jeanfrank CallaBelum ada peringkat
- Goma de PoliisoprenoDokumen2 halamanGoma de PoliisoprenoCarlos LopezBelum ada peringkat
- Doblar varilla corrugada: cálculo y característicasDokumen7 halamanDoblar varilla corrugada: cálculo y característicasSara AguilarBelum ada peringkat
- Regulador de Fluido GracoDokumen22 halamanRegulador de Fluido GracoCristian MenesesBelum ada peringkat