Tarea de Carlin
Diunggah oleh
Tania Karina Acero Valdes0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
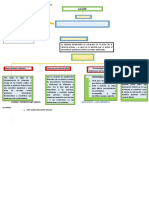
44 tayangan2 halamanEste documento compara las normas de buenas prácticas de fabricación de medicamentos de México y Perú. Ambas normas establecen requisitos para garantizar la calidad, seguridad y eficacia de los medicamentos fabricados y distribuidos en sus respectivos países. Si bien comparten campos como definiciones, gestión de calidad, personal y validación, la norma peruana incluye más detalles en algunas áreas.
Deskripsi Asli:
comparación NOM 059 con marco regulatorio de Peru
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniEste documento compara las normas de buenas prácticas de fabricación de medicamentos de México y Perú. Ambas normas establecen requisitos para garantizar la calidad, seguridad y eficacia de los medicamentos fabricados y distribuidos en sus respectivos países. Si bien comparten campos como definiciones, gestión de calidad, personal y validación, la norma peruana incluye más detalles en algunas áreas.
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
44 tayangan2 halamanTarea de Carlin
Diunggah oleh
Tania Karina Acero ValdesEste documento compara las normas de buenas prácticas de fabricación de medicamentos de México y Perú. Ambas normas establecen requisitos para garantizar la calidad, seguridad y eficacia de los medicamentos fabricados y distribuidos en sus respectivos países. Si bien comparten campos como definiciones, gestión de calidad, personal y validación, la norma peruana incluye más detalles en algunas áreas.
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 2
GEORGE ANTES HERNÀNDEZ
PAÍS MÉXICO PERU
NORMA/LEY NOM-059-SSA1-2015 LEY No. 29459
Dirección General de
ORGANISMO
Secretaría de Salud. Medicamentos, Insumos y
REGULADOR
Drogas
Ley de los productos
Buenas prácticas de fabricación
NOMBRE de medicamentos
farmacéuticos, dispositivos
médicos y productos sanitarios
Requisitos mínimos necesarios Define y establece los principios,
para el proceso de fabricación de normas, criterios y exigencias
los medicamentos para uso básicas sobre los productos
OBJETIVO humano comercializados en el farmacéuticos, dispositivos
país y/o con fines de médicos y productos sanitarios de
investigación. uso en seres humanos.
Comprende productos
farmacéuticos, dispositivos
Es de observancia obligatoria
médicos y productos sanitarios de
para todos los establecimientos
uso humano con finalidad
dedicados a la fabricación
preventiva, diagnostica, de
y/o importación de medicamentos
tratamiento y otros. Regula
para uso humano
también la actuación de las
comercializados en el país y/o
personas naturales o jurídicas
CAMPO DE APLICACIÓN con fines de investigación,
que intervienen en la fabricación,
así como los laboratorios de
importación, exportación,
control de calidad, almacenes de
almacenamiento, distribución,
acondicionamiento, depósito y
comercialización, promoción,
distribución de medicamentos y
publicidad, prescripción, atención
materias primas para su
farmacéutica, expendio, uso y
elaboración.
destino final de los productos
antes mencionados.
DEFINICIONES Si comprende Si comprende
Si comprende pero lo que en
SISTEMA DE GESTIÓN NOM se engloba en un solo
Si comprende
DE CALIDAD numeral en la guía de BPF de
Perú equivale a varios numerales.
GESTIÓN DE RIESGOS
Si comprende Si comprende
DE CALIDAD
Generalidades, gestión de
recursos, responsable de unidad Generalidades, personal clave,
PERSONAL de fabricación, responsable de capacitación, higiene del
unidad de calidad, consultores e personal.
higiene y seguridad.
Generalidades, consideraciones,
Generalidades, áreas auxiliares,
áreas de producción, auxiliares,
INSTALACIONES Y de pesadas, almacenamiento,
control de calidad y
EQUIPOS producción, control de calidad,
almacenamiento; equipos y
etc.
sistemas críticos.
Generalidades, impacto de la
validación, calificación y Comprende el numeral de
validación, PMV, protocolo de Validación, productos
CALIFICACIÓN Y validación y calificación, farmacéuticos estériles, buenas
VALIDACIÓN calificación, validación de prácticas de manufactura para
procesos asépticos, validación de ingredientes farmacéuticos
limpieza, sistemas activos.
computacionales, etc.
Generalidades, control de Generalidades, prevención de la
insumos, control de operaciones contaminación cruzada y
SISTEMAS DE
de fabricación, sistemas de bacteriana en la producción,
FABRICACIÓN producción de productos no operaciones de proceso,
estériles y estériles, biológicos y productos intermedios y a granel
GEORGE ANTES HERNÀNDEZ
biotecnológicos, gases y operaciones de empaquetado.
medicinales, medicamentos en
aerosol, medicamentos
homeopáticos, medicamentos
para uso de estudios clínicos y
compatibilidad de giros.
Control de materias primas, de
producto intermedio, en granel y
LABORATORIO DE terminados; requisitos exigidos en
Generalidades, etc.
CONTROL DE CALIDAD las pruebas; revisión de registros
de producción y estudios de
estabilidad.
Se encuentra dentro del numeral
sobre materiales donde además
de incluir este punto incluye
LIBERACIÓN DE Si cumple y es un numeral muy
generalidades, materia prima,
PRODUCTO TERMINADO grande.
materiales de empaque,
materiales intermedias y de
empaque, etc.
RETIRO DE PRODUCTO
Si comprende Si comprende
DEL MERCADO
Generalidades, agente
contratante, agente contratado,
contrato, servicios
ACTIVIDADES Generalidades, el contratante, el
subcontratados, maquilas,
SUBCONTROLADAS contratista y el contrato.
servicios de laboratorios de
análisis, servicios de sistemas
críticos y equipos.
DESTINO FINAL DE
Si comprende No comprende
RESIDUOS
BUENAS PRACTICAS DE Se encuentra dentro del numeral
de buenas prácticas de
ALMACENAMIENTO Y Si comprende
manufactura para ingredientes
DISTRIBUCIÓN farmacéuticos activos.
CONCORDANCIA DE
NORMAS NACIONALES E Si comprende No comprende
INTERNACIONALES
BIBLIOGRAFIA Si comprende Si comprende
OBSERVANCIA Si comprende Si comprende
En tanto no se apruebe y entre en
Entra en vigor a los 180 días vigencia el o los reglamentos de
naturales posteriores a su la presente Ley, mantienense en
VIGENCIA publicación en el Diario Oficial vigencia las disposiciones
de la Federación. contenidas, en lo que resulte
aplicable
PRIMERA. Del reglamento
SEGUNDA. de la vigencia de
ÚNICO. La presente Norma normas reglamentarias
cancela la Norma Oficial TERCERA. Del plazo de
Mexicana NOM-059-SSA1-2013, adecuación
TRANSITORIOS Buenas prácticas de fabricación CUARTA. De la obligación de las
de medicamentos, publicada en municipalidades
el Diario Oficial de la Federación QUINTA. De la tasa de registro
el 22 de julio de 2013. sanitario
SEXTA. Modificación de los art.
26° y 92°
Anda mungkin juga menyukai
- Farmacoctenia Fase 4 Construcion de La PropuestaDokumen13 halamanFarmacoctenia Fase 4 Construcion de La PropuestaGloria Cecilia Florez GonzalezBelum ada peringkat
- Matriz de Comparación de Los Requerimientos Normativos de Buenas Prácticas de Manufactura para La Industria Farmacéutica, Cosmética y de AlimentosDokumen36 halamanMatriz de Comparación de Los Requerimientos Normativos de Buenas Prácticas de Manufactura para La Industria Farmacéutica, Cosmética y de AlimentosCandell Nalvarez100% (1)
- Clase 12 Escala de Infracciones y Sanciones de Establecimientos FarmacéuticosDokumen21 halamanClase 12 Escala de Infracciones y Sanciones de Establecimientos FarmacéuticosMartinAlbis20130% (1)
- Sistemas de Calidad - Establecimientos FarmacéuticosDokumen38 halamanSistemas de Calidad - Establecimientos FarmacéuticosKatherine OjedaBelum ada peringkat
- Formulación MagistralDokumen13 halamanFormulación MagistralLucī LuBelum ada peringkat
- Mapa Conceptual BPM ... Jadier Navarro AraujoDokumen2 halamanMapa Conceptual BPM ... Jadier Navarro AraujoJimy jadier Navarro AraujoBelum ada peringkat
- Tema # 8 Buenas Practicas de Manufactura 01Dokumen7 halamanTema # 8 Buenas Practicas de Manufactura 01emilio peñaBelum ada peringkat
- Weebly Subir MapaDokumen2 halamanWeebly Subir Mapaluisa fernandaBelum ada peringkat
- Reforma Salud PERUDokumen37 halamanReforma Salud PERUOPPF DIREMID LORETO100% (1)
- DECRETOnRESOLIONnLEYnPOLITICAnnDELnSERVICIOnFARMACEUTICO 386359ac1311c7fDokumen8 halamanDECRETOnRESOLIONnLEYnPOLITICAnnDELnSERVICIOnFARMACEUTICO 386359ac1311c7fjhonatan german luna peñarandaBelum ada peringkat
- Resolución 1403 Del 2007.Dokumen27 halamanResolución 1403 Del 2007.angie ramirezBelum ada peringkat
- D.S 016Dokumen25 halamanD.S 016Yessica Acruta ArapaBelum ada peringkat
- Caso 2 - Aplicación de La Normatividad FarmacéuticaDokumen12 halamanCaso 2 - Aplicación de La Normatividad Farmacéuticalaura prietooBelum ada peringkat
- Ilovepdf MergedDokumen114 halamanIlovepdf Mergedemerson jesusBelum ada peringkat
- Buenas Practicas de Dispensacion en Establecimientos Farmaceuticos deDokumen36 halamanBuenas Practicas de Dispensacion en Establecimientos Farmaceuticos deemerson jesusBelum ada peringkat
- Nom VS FdaDokumen8 halamanNom VS FdaNenitamoxa Ventura Lugo50% (2)
- Regulacion y Calidad de MedicamentosDokumen2 halamanRegulacion y Calidad de MedicamentosRonald MelendezBelum ada peringkat
- FARMACIA HOSPITALARIA - Fase1Dokumen3 halamanFARMACIA HOSPITALARIA - Fase1Yuranii MonteroBelum ada peringkat
- MAPADokumen1 halamanMAPAFlor CastañedaBelum ada peringkat
- Reyes Zamudio Samantha Act3Dokumen3 halamanReyes Zamudio Samantha Act3Samantha Reyes ZamudioBelum ada peringkat
- Caso 3 Interpretación de Las Realidades en El Contexto Normativo ColombianoDokumen13 halamanCaso 3 Interpretación de Las Realidades en El Contexto Normativo ColombianoBLANCA TATIANA CELIS ALDANABelum ada peringkat
- Digemid y Sus FuncionesDokumen22 halamanDigemid y Sus FuncionesAlonso avellaneda lizanaBelum ada peringkat
- Buenas Practicas de AlmacenamientoDokumen18 halamanBuenas Practicas de AlmacenamientoCrystal NecaBelum ada peringkat
- INVIMADokumen2 halamanINVIMANataly BuitragoBelum ada peringkat
- Practica 1Dokumen10 halamanPractica 1Nathaniel PadillaBelum ada peringkat
- Regulatoria de Dispositivos Médicos - UCSM-2019 - 1Dokumen100 halamanRegulatoria de Dispositivos Médicos - UCSM-2019 - 1EstefaniIdaniaBelum ada peringkat
- Consultoria en Asuntos RegulatoriosDokumen18 halamanConsultoria en Asuntos RegulatoriosSANDRABelum ada peringkat
- Industria FarmacéuticaDokumen25 halamanIndustria FarmacéuticaErick Saul Garay Lazo100% (1)
- Legislacion FarmaceuticaDokumen5 halamanLegislacion Farmaceuticaandrea jimenezBelum ada peringkat
- Ley 29459Dokumen33 halamanLey 29459Ros CC100% (1)
- BPM F FinalDokumen39 halamanBPM F Finalkaren turpoBelum ada peringkat
- Farmacia HomeopaticaDokumen2 halamanFarmacia HomeopaticaYovany MillánBelum ada peringkat
- Elabore Una Infografia de Medicamento Generico y de MarcaDokumen8 halamanElabore Una Infografia de Medicamento Generico y de MarcaDelta Salome Tizon Checca0% (1)
- Semana 1 Farmacotecnia HospitalarioDokumen45 halamanSemana 1 Farmacotecnia HospitalarioPedro Jacinto Hervias100% (1)
- An Introduction To Regulation of Medical Devices in Australia (Esp)Dokumen53 halamanAn Introduction To Regulation of Medical Devices in Australia (Esp)LorenaBelum ada peringkat
- Clase 3 Bpadteeff 1Dokumen22 halamanClase 3 Bpadteeff 1Criss Fuster100% (1)
- II - BPM - Aseguramiento - de - La - Calidad (1) 87Dokumen97 halamanII - BPM - Aseguramiento - de - La - Calidad (1) 87Beatriz MarquezBelum ada peringkat
- Regulacion y Calidad de MedicamentosDokumen2 halamanRegulacion y Calidad de MedicamentosRonald MelendezBelum ada peringkat
- Mapa Regulacion y ArmonizacionDokumen2 halamanMapa Regulacion y ArmonizacionArturo LinaresBelum ada peringkat
- Ley 29459 Normas de Control de CalidadDokumen33 halamanLey 29459 Normas de Control de CalidadNilda judith rodrigo galvezBelum ada peringkat
- Ana - Vargas - Yuri - Hernandez Atencion Farmaceutica - Taller 3Dokumen19 halamanAna - Vargas - Yuri - Hernandez Atencion Farmaceutica - Taller 3Diego HernandezBelum ada peringkat
- Estandar de Medicamentos DispositivosDokumen64 halamanEstandar de Medicamentos DispositivosYURY MILEIDY SANTANA AVENDAÑOBelum ada peringkat
- Dispositivos MedicosDokumen22 halamanDispositivos MedicosCarmen HuaracayoBelum ada peringkat
- Xxx20082020matriz Farmacia HomeopaticaDokumen2 halamanXxx20082020matriz Farmacia HomeopaticaYovany MillánBelum ada peringkat
- Tecnovigilancia Farmacovigilancia y CosmetovigilanciaDokumen7 halamanTecnovigilancia Farmacovigilancia y Cosmetovigilanciaandy flores100% (1)
- Bpof ExposicionDokumen10 halamanBpof ExposicionMarilyn Sully Guzman MoralesBelum ada peringkat
- II BPM Aseguramiento de La CalidadDokumen89 halamanII BPM Aseguramiento de La CalidadCristian Dawing Perez Vasquez100% (1)
- Clase 4 Ley de Prod Farma, Dispositivos Médicos y Prod. SanitariosDokumen40 halamanClase 4 Ley de Prod Farma, Dispositivos Médicos y Prod. SanitariosAraceli VergarayBelum ada peringkat
- Módulo V - Clase 01 (Prof María de Los Ángeles Vi - 230925 - 103725Dokumen50 halamanMódulo V - Clase 01 (Prof María de Los Ángeles Vi - 230925 - 103725MacaRubioBelum ada peringkat
- ErewrweDokumen2 halamanErewrweScopy PrinterBelum ada peringkat
- Sílabo Dispensacion de Medicamentos en El Sistema de SaludDokumen7 halamanSílabo Dispensacion de Medicamentos en El Sistema de SaludAntonio TincopaBelum ada peringkat
- Autoridad Nacional de Medicamentos y Acceso A Productos Farmacéuticos, Dispositivos Médicos y Productos SanitariosDokumen19 halamanAutoridad Nacional de Medicamentos y Acceso A Productos Farmacéuticos, Dispositivos Médicos y Productos SanitarioslizdguevaraBelum ada peringkat
- Intro Ducci OnDokumen6 halamanIntro Ducci OnYale GarciaBelum ada peringkat
- Marco Normativo 1Dokumen8 halamanMarco Normativo 1Yudith Mirian Arellano EstradaBelum ada peringkat
- Regulacion Sanitaria Peruana y EvoluciónDokumen15 halamanRegulacion Sanitaria Peruana y EvoluciónDiana Beiseth Saavedra Torres0% (1)
- MD - IndMed - s3 - BPM Y BPLDokumen38 halamanMD - IndMed - s3 - BPM Y BPLBioquimica UplaBelum ada peringkat
- Manual de Gestion Droguerias y Tiendas Naturistas2012Dokumen37 halamanManual de Gestion Droguerias y Tiendas Naturistas2012Carlos Francisco Herrera GonzalezBelum ada peringkat
- UF0007 - Aplicación de métodos de control fitosanitarios en plantas, suelo e instalacionesDari EverandUF0007 - Aplicación de métodos de control fitosanitarios en plantas, suelo e instalacionesPenilaian: 5 dari 5 bintang5/5 (1)
- Ciencia regulatoria: Medicamentos bio y su relevancia para la saludDari EverandCiencia regulatoria: Medicamentos bio y su relevancia para la saludBelum ada peringkat
- Interacciones Entre Farmacos y NutrientesDokumen28 halamanInteracciones Entre Farmacos y NutrientesTania Karina Acero Valdes100% (1)
- Practica 2.1 Bloqueadores de La Placa Neuromuscular PolloDokumen1 halamanPractica 2.1 Bloqueadores de La Placa Neuromuscular PolloTania Karina Acero ValdesBelum ada peringkat
- Feum 11 Tomo IDokumen1.475 halamanFeum 11 Tomo ITania Karina Acero Valdes100% (8)
- Practica 4 AnticonvulsivosDokumen1 halamanPractica 4 AnticonvulsivosTania Karina Acero ValdesBelum ada peringkat
- Practica 1 V.E. AnalgesicoDokumen1 halamanPractica 1 V.E. AnalgesicoTania Karina Acero Valdes0% (1)
- Exposición FlavorDokumen52 halamanExposición FlavorTania Karina Acero Valdes100% (1)
- Practica 2 Bloqueadores de La Placa NeuromuscularDokumen1 halamanPractica 2 Bloqueadores de La Placa NeuromuscularTania Karina Acero ValdesBelum ada peringkat
- ARACNIDISMODokumen57 halamanARACNIDISMOTania Karina Acero ValdesBelum ada peringkat
- CUESTIONARIO 6 Morfologia ColonialDokumen4 halamanCUESTIONARIO 6 Morfologia ColonialTania Karina Acero Valdes78% (9)
- Analisis Quimico de Los AlimentosDokumen435 halamanAnalisis Quimico de Los AlimentosAlejandra Aragón Parra93% (14)
- Tabletas RecubiertasDokumen47 halamanTabletas RecubiertasTania Karina Acero ValdesBelum ada peringkat
- MicrocapsulasDokumen37 halamanMicrocapsulasTania Karina Acero Valdes100% (1)
- Sistema Nervioso AutónomoDokumen7 halamanSistema Nervioso AutónomoTania Karina Acero ValdesBelum ada peringkat
- Cuestionario de DistribucionDokumen6 halamanCuestionario de DistribucionTania Karina Acero Valdes100% (2)
- Insolvencia ProvocadaDokumen5 halamanInsolvencia ProvocadaHeydy MargioryBelum ada peringkat
- Clase Notariado w1Dokumen22 halamanClase Notariado w1Jacqueline Abigail Aroche PeñaBelum ada peringkat
- Acto Autentico de AdopcionDokumen4 halamanActo Autentico de AdopcionMaria Paredes Desprader57% (7)
- Cuadernillo Apunte Dr. Salgado Procesal Civil y ComercialDokumen189 halamanCuadernillo Apunte Dr. Salgado Procesal Civil y ComercialMaximiliano Javier NuñezBelum ada peringkat
- Principio de Causalidad, Percibido y DevengadoDokumen17 halamanPrincipio de Causalidad, Percibido y DevengadoGuadalupe Crisanto More75% (4)
- Cuadro ComparativoDokumen10 halamanCuadro ComparativoANDRES FABIAN PEREZ CHAVESBelum ada peringkat
- Fuero SindicalDokumen4 halamanFuero SindicalMarimar Agredo CruzBelum ada peringkat
- D. Civil (Reales) - AnticresisDokumen30 halamanD. Civil (Reales) - AnticresisRodrigo Toledo Tala100% (2)
- Apersonamiento AnDokumen2 halamanApersonamiento AnSheyla Del Carmen YQBelum ada peringkat
- Conceptos Fiscales PDFDokumen4 halamanConceptos Fiscales PDFErikaBeltránMartínezBelum ada peringkat
- Libro de ActasDokumen3 halamanLibro de ActasFRANCIA MARCELA BRICEÑO MATEUSBelum ada peringkat
- 1er Corte-Teoría General de La PruebaDokumen24 halaman1er Corte-Teoría General de La Pruebayubetzys tovarBelum ada peringkat
- Diagrama Ecuador - Alemania 15%Dokumen6 halamanDiagrama Ecuador - Alemania 15%Cltos FerroBelum ada peringkat
- Formulario Físico o Electrónico de Registro de Cuenta Corriente oDokumen1 halamanFormulario Físico o Electrónico de Registro de Cuenta Corriente okarinaBelum ada peringkat
- Contrato Lazo NievesDokumen1 halamanContrato Lazo NievesJessica Enit Coloma DelgadoBelum ada peringkat
- 1 Escritura Publica de Compraventa Con Representacion de Un MenorDokumen4 halaman1 Escritura Publica de Compraventa Con Representacion de Un MenorMaria ines Sosa luyaBelum ada peringkat
- Análisis Jurídico y Ético de Un Proceso Seguido en Contra de Un Profesional Del Derecho Por Actuaciones Ilegales en Los Diferentes Campos LaboralesDokumen18 halamanAnálisis Jurídico y Ético de Un Proceso Seguido en Contra de Un Profesional Del Derecho Por Actuaciones Ilegales en Los Diferentes Campos LaboralesGiselle Mjc100% (2)
- M5 Cuestionario M5Dokumen2 halamanM5 Cuestionario M5Miranda AlexBelum ada peringkat
- Mercedez CORRECTODokumen5 halamanMercedez CORRECTORiveraMariluBelum ada peringkat
- Conflicto de LeyesDokumen19 halamanConflicto de LeyesEmmanuel Bernal VargasBelum ada peringkat
- Manifestacion Bajo Gravedad de JuramentoDokumen1 halamanManifestacion Bajo Gravedad de JuramentoPaolo MedinaBelum ada peringkat
- Circuitos Electricos IDokumen15 halamanCircuitos Electricos IPablo PachecoBelum ada peringkat
- Narcotráfico en MéxicoDokumen1 halamanNarcotráfico en MéxicoAdrian Dominguez MoranBelum ada peringkat
- SentenciaDokumen11 halamanSentenciaCarmen Nilda Montalvo SanchezBelum ada peringkat
- A LegatoDokumen4 halamanA LegatoJorge Valenzuela AlvaradoBelum ada peringkat
- Carrion Eguiguren - Un Estudio Sobre Temas PosesoriosDokumen10 halamanCarrion Eguiguren - Un Estudio Sobre Temas PosesoriosJuan Sebastián BaqueroBelum ada peringkat
- Comparativo Ley de AlquileresDokumen15 halamanComparativo Ley de AlquileresLautaro LegunesBelum ada peringkat
- 1 Recurso de Revocatoria Al SereciDokumen4 halaman1 Recurso de Revocatoria Al SereciMarco Mero89% (9)
- Introd. A La Ing. Civil Semana 12-T 12 - 2020-2Dokumen55 halamanIntrod. A La Ing. Civil Semana 12-T 12 - 2020-2Edward Chacon MendozaBelum ada peringkat
- Contrato Expediente Nuevo TrujilloDokumen9 halamanContrato Expediente Nuevo TrujilloKir Torres RojasBelum ada peringkat