Redoks Dan Elektrokimia
Diunggah oleh
FitrianiParinduriHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Redoks Dan Elektrokimia
Diunggah oleh
FitrianiParinduriHak Cipta:
Format Tersedia
R.
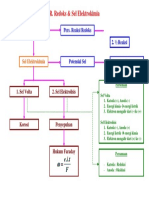
Redoks & Sel Elektrokimia
R. Redoks Pers. Reaksi Redoks
2. ½ Reaksi
Sel Elektrokimia Potensial Sel Potensial Elektroda
Perbedaan
1. Sel Volta 2. Sel Elektrolisis
Sel Volta
1. Katoda (+), Anoda (-)
2. Energi kimia energi listrik
3. Elektron mengalir dari (-) ke (+)
Sel Elektrolisis
Korosi Penyepuhan 1. Katoda (-), Anoda (+)
2. Energi listrik energi kimia
3. Elektron mengalir dari (+) ke (-)
Hukum Faraday Persamaan
e .i .t
- Katoda : Reduksi
F - Anoda : Oksidasi
Anda mungkin juga menyukai
- Kelompok 6 Kimia Dasar Farmasi: ElektrokimiaDokumen19 halamanKelompok 6 Kimia Dasar Farmasi: ElektrokimiaDr YurizalBelum ada peringkat
- Susunan Sel ElektrolisisDokumen4 halamanSusunan Sel ElektrolisisFaqih SultonfaqBelum ada peringkat
- Rangkuman ELEKTROKIMIA-unlockedDokumen4 halamanRangkuman ELEKTROKIMIA-unlockedDeti NurdiantiBelum ada peringkat
- Sel Volta TugasDokumen7 halamanSel Volta TugasMantabs JiwaBelum ada peringkat
- Marina Armayanti - 119270038 - Laporan - Praktikum - Kimia - Modul4 PDFDokumen19 halamanMarina Armayanti - 119270038 - Laporan - Praktikum - Kimia - Modul4 PDFRiyanto WidodoBelum ada peringkat
- Pertemuan 3-Pendahuluan ElektroanalitikDokumen38 halamanPertemuan 3-Pendahuluan ElektroanalitikZaqiaBelum ada peringkat
- Sel ElektrokimiaDokumen19 halamanSel ElektrokimiaDhiya SalsabilBelum ada peringkat
- ELEKTROLISADokumen36 halamanELEKTROLISAyanBelum ada peringkat
- TEORI SEL VOLTADokumen12 halamanTEORI SEL VOLTAagungahmad sultonsaputraBelum ada peringkat
- (PDF) Laporan Praktikum Sel Elektrokimia - CompressDokumen10 halaman(PDF) Laporan Praktikum Sel Elektrokimia - CompressAlfariz100% (1)
- Modul Pembelajaran KimiaDokumen10 halamanModul Pembelajaran KimiaNuryana Wahyuning SariBelum ada peringkat
- Materi PotensiometriDokumen10 halamanMateri PotensiometriThrowaway LohanBelum ada peringkat
- Industri ElektrokimiaDokumen13 halamanIndustri ElektrokimiaYuliBelum ada peringkat
- Bahan Ajar Sel VoltaDokumen5 halamanBahan Ajar Sel VoltaLuska ReniBelum ada peringkat
- Fitri ElektrokimiaDokumen8 halamanFitri ElektrokimiaFitria YunusBelum ada peringkat
- 4 ElektrolisisDokumen20 halaman4 ElektrolisisSherlyBelum ada peringkat
- Analisis Konsep 3.6&4.6-1Dokumen4 halamanAnalisis Konsep 3.6&4.6-1putty zindaBelum ada peringkat
- Volta Kim2 4 PDFDokumen5 halamanVolta Kim2 4 PDFClara PasmarangBelum ada peringkat
- Volta Kim2 4Dokumen5 halamanVolta Kim2 4Tri WahyudiBelum ada peringkat
- Makalah Sel EloktrokimiaDokumen13 halamanMakalah Sel EloktrokimiaFisal Soamole FadilahBelum ada peringkat
- KIMTEKDokumen17 halamanKIMTEKEci RahmanBelum ada peringkat
- ElektrokimiaDokumen37 halamanElektrokimiaIrmaWatiBelum ada peringkat
- Materi-1 (Sel Elektrokimia) - 1Dokumen6 halamanMateri-1 (Sel Elektrokimia) - 1nailasadah11Belum ada peringkat
- Lapres ElektrogravimetriDokumen36 halamanLapres Elektrogravimetri50Wahyu Aprilia RahmayantiBelum ada peringkat
- Sel VoltaDokumen5 halamanSel VoltaMa'rifatul Aulia Az-ZahraBelum ada peringkat
- BDT Kelompok 19Dokumen53 halamanBDT Kelompok 19raihan dzakyBelum ada peringkat
- Sel VoltaDokumen21 halamanSel VoltaYolandaBelum ada peringkat
- Sel Volta FixDokumen5 halamanSel Volta Fixwahyu pamungkasBelum ada peringkat
- MAKALAH ELEKTROKIMIADokumen19 halamanMAKALAH ELEKTROKIMIAadheBelum ada peringkat
- SELEKTROLISISDokumen32 halamanSELEKTROLISISAditya Meita NugrahaBelum ada peringkat
- Sel Elektrokimia 2Dokumen26 halamanSel Elektrokimia 2Aliya RahmaBelum ada peringkat
- Modul ElektrokimiaDokumen11 halamanModul Elektrokimiadicky_permana083091Belum ada peringkat
- ElektrokimiaDokumen27 halamanElektrokimiaSyamsir mursaliBelum ada peringkat
- Laporan Praktikum Sel ElektrokimiaDokumen22 halamanLaporan Praktikum Sel ElektrokimiaDesi Supiyanti100% (2)
- Materi Pembelajaran Sel ElektrolisisDokumen3 halamanMateri Pembelajaran Sel ElektrolisisLies LestariBelum ada peringkat
- ELEKTROKIMIADokumen83 halamanELEKTROKIMIAIamgrootBelum ada peringkat
- ELEKTROLISISDokumen4 halamanELEKTROLISISIan Alfian AminBelum ada peringkat
- ELEKTROKIMIADokumen20 halamanELEKTROKIMIAAzizah AzizahBelum ada peringkat
- POTENSIOMETRI Sel VoltaDokumen24 halamanPOTENSIOMETRI Sel Voltaalif ramdaniBelum ada peringkat
- P5 Aplikasi Elektrokimia 1Dokumen38 halamanP5 Aplikasi Elektrokimia 1Wella HijriyaniBelum ada peringkat
- Elektrokimia Kimia Fisika 2Dokumen35 halamanElektrokimia Kimia Fisika 2nurayniBelum ada peringkat
- Laporan Fisika 2 GabunganDokumen158 halamanLaporan Fisika 2 GabunganNabila Madya MandaBelum ada peringkat
- Acc KiDokumen14 halamanAcc KiNur AsmiBelum ada peringkat
- Sel ElektrokimiaDokumen9 halamanSel ElektrokimiaKelvin Octavianus DjohanBelum ada peringkat
- a) Esel yang dihasilkan oleh kedua elektroda tersebut adalah 0,799 - (-2,37) = 3,169 V b) Reaksi elektro: Mg → Mg2+ + 2e; Ag+ + 2e → AgDokumen30 halamana) Esel yang dihasilkan oleh kedua elektroda tersebut adalah 0,799 - (-2,37) = 3,169 V b) Reaksi elektro: Mg → Mg2+ + 2e; Ag+ + 2e → AgAriefa SalsabilaBelum ada peringkat
- Bab I Elektrokimia FixDokumen16 halamanBab I Elektrokimia FixAldi NelfrianBelum ada peringkat
- Resume Sel ElektrolisisDokumen10 halamanResume Sel ElektrolisisUlylhilmiBelum ada peringkat
- ELEKTROKIMIADokumen25 halamanELEKTROKIMIAnuraisyah aritonangBelum ada peringkat
- REAKSI REDOKS DAN ELEKTROLISISDokumen33 halamanREAKSI REDOKS DAN ELEKTROLISISNahya AndhiniBelum ada peringkat
- ElektrokimiaDokumen33 halamanElektrokimiaReihan FaizaldiBelum ada peringkat
- ElektrokimiaDokumen17 halamanElektrokimiaRonado LinggaBelum ada peringkat
- Bab Ii MipaDokumen13 halamanBab Ii MipaMus ThafaBelum ada peringkat
- 12 ElektrokimiaDokumen41 halaman12 ElektrokimiaIrwan ProssBelum ada peringkat
- Bab II Tinjauan PustakaDokumen15 halamanBab II Tinjauan PustakaJuminten SariBelum ada peringkat
- Bab II PembahasanDokumen15 halamanBab II PembahasantiaraBelum ada peringkat
- Voltameter TembagaDokumen27 halamanVoltameter TembagaAchda LazuardiBelum ada peringkat
- Elekt Kim2 5Dokumen2 halamanElekt Kim2 5anisyahfitriBelum ada peringkat
- Soal 1Dokumen27 halamanSoal 1FitrianiParinduriBelum ada peringkat
- Pertumbuhan Dan PerkembanganDokumen1 halamanPertumbuhan Dan PerkembanganFitrianiParinduriBelum ada peringkat
- Surat Pernyataan Mhs Baru 2019Dokumen1 halamanSurat Pernyataan Mhs Baru 2019FitrianiParinduriBelum ada peringkat
- Soal 2Dokumen27 halamanSoal 2FitrianiParinduriBelum ada peringkat
- Silabus-1Dokumen5 halamanSilabus-1Aulia Aurellya ArnoldhyBelum ada peringkat
- Polinasi Pada Tanaman Berumah Dua Dapat Terjadi Secara AutogamiDokumen1 halamanPolinasi Pada Tanaman Berumah Dua Dapat Terjadi Secara AutogamiFitrianiParinduriBelum ada peringkat
- Kalender Pendidikan 2018 - 2019Dokumen4 halamanKalender Pendidikan 2018 - 2019FitrianiParinduriBelum ada peringkat
- Fisika 12 Ipa Kur-13Dokumen9 halamanFisika 12 Ipa Kur-13FitrianiParinduriBelum ada peringkat
- Undangan BIMTEK HKI 2019Dokumen7 halamanUndangan BIMTEK HKI 2019FitrianiParinduriBelum ada peringkat
- Redoks Dan ElektrokimiaDokumen1 halamanRedoks Dan ElektrokimiaFitrianiParinduriBelum ada peringkat
- RPP RotistaDokumen14 halamanRPP RotistaFitrianiParinduriBelum ada peringkat
- New Format KKM ExcelDokumen9 halamanNew Format KKM ExcelFitrianiParinduriBelum ada peringkat
- Fisika 12 Ipa Kur-13Dokumen9 halamanFisika 12 Ipa Kur-13FitrianiParinduriBelum ada peringkat
- Soal - Soal RedoksDokumen1 halamanSoal - Soal RedoksFitrianiParinduriBelum ada peringkat
- STRUKTUR DAN FUNGSI KORMOPHYTADokumen1 halamanSTRUKTUR DAN FUNGSI KORMOPHYTAFitrianiParinduriBelum ada peringkat
- Soal Pertumbuhan Dan PerkembanganDokumen1 halamanSoal Pertumbuhan Dan PerkembanganFitrianiParinduriBelum ada peringkat
- Syllabus - ICHODokumen16 halamanSyllabus - ICHOPramudio PakertiBelum ada peringkat
- LPK PortofolioDokumen2 halamanLPK PortofolioFitrianiParinduriBelum ada peringkat
- Jadwal Penting Unbk 2018Dokumen2 halamanJadwal Penting Unbk 2018Yusrizal IzalBelum ada peringkat
- Cover-1Dokumen2 halamanCover-1FitrianiParinduriBelum ada peringkat
- Silabus-1Dokumen7 halamanSilabus-1FitrianiParinduri100% (1)
- PLPG SUMUT 2017Dokumen6 halamanPLPG SUMUT 2017FitrianiParinduriBelum ada peringkat
- CoverDokumen2 halamanCoverFitrianiParinduriBelum ada peringkat
- Peta Konsep RedoksDokumen1 halamanPeta Konsep RedoksFitrianiParinduriBelum ada peringkat
- Laporan Pembekalan Materi Peserta PLPG Tahun 2017Dokumen12 halamanLaporan Pembekalan Materi Peserta PLPG Tahun 2017Arip EthemBelum ada peringkat
- Ulangan HarianDokumen4 halamanUlangan HarianFitrianiParinduri0% (1)
- Peta Konsep StoikiometriDokumen1 halamanPeta Konsep StoikiometriFitrianiParinduriBelum ada peringkat
- Bagan Konsep MolDokumen1 halamanBagan Konsep MolFitrianiParinduriBelum ada peringkat
- RPP Bio Kelas X SMT 1 2Dokumen87 halamanRPP Bio Kelas X SMT 1 2Retno Wahyuningtyas100% (2)