Disolucion de Borax
Diunggah oleh
Ivan IvenianDeskripsi Asli:
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Disolucion de Borax
Diunggah oleh
Ivan IvenianHak Cipta:
Format Tersedia
Determinación de la entalpia, entropía y energía libre estándar
Objetivos
Determinar la energía libre estándar, la entalpía estándar y los cambios de entropía estándar para
una disolución del bórax en solución acuosa
Marco teórico
El cambio de la energía libre de un proceso químico es proporcional a su constante de equilibrio
de acuerdo a la siguiente ecuación
(1)
Donde R, la constante de los gases 8.314 x 10 -3 kJ/mol*K, y T es la temperatura en grados Kelvin.
La constante de equilibrio, K, se expresa para el sistema de equilibrio cuando los reactivos y
productos se encuentran en sus estados estándar.
Para una sal ligeramente soluble en un sistema acuoso, el precipitado y los iones en solución
corresponden a los estados estándar de los reactantes y los productos, respectivamente
(2)
El producto de solubilidad Kps, se establece como el producto de las concentraciones molares de
los iones, elevado a la potencia de sus respectivos coeficientes de la ecuación balanceada, la ley de
acción de masas para el sistema es
(3)
Y el cambio de la energía libre para el equilibrio es
(4)
Adicionalmente, el cambio de la energía libre para un proceso químico también es función del
cambio de la entalpia y cambio de entropía del proceso
(5)
Cuando las dos expresiones de energía libre son iguales para una sal ligeramente soluble, entonces
(6)
Reordenando y resolviendo para ln Kps
(7)
El cual es análogo a la ecuación de una recta y =mx+b
Procedimiento
Se pueden preparar cinco o seis muestras de bórax para el experimento. La sexta muestra (una
solución saturada en un baño de hielo) tendrá una muy baja solubilidad de bórax.
Con un matraz Erlenmeyer de 125 o 250 ml, agregue 30–35 g de bórax a 100 ml de agua destilada.
Tapar el matraz y agitar la mezcla durante varios minutos para preparar la solución saturada.
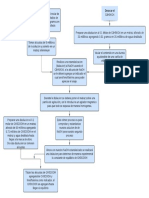
Llene los tubos de ensayo con 20 ml solución de bórax. Coloque los tubos de ensayo en los baños
respectivos que se muestran en la Figura. Se debe mantener la temperatura constante unos 15
minutos
Agite de vez en cuando los tubos de ensayo en los baños (para 10–15 minutos), asegurando la
formación de una solución saturada; el bórax sólido siempre debe estar presente: agregue más
bórax sólido si es necesario
Permita que el bórax se precipite hasta que la solución esté clara cuando se ha alcanzado el
equilibrio térmico. Espere de 10 a 15 minutos para que se establezca el equilibrio térmico.
Registrar la temperatura exacta de los respectivos baños de agua.
Transfiera rápida pero cuidadosamente 5 ml de las soluciones transparentes Retirar el calor de los
baños de agua.
Preparar para la transferencia de muestras. Configure y etiquete un conjunto de cinco, matraces
Erlenmeyer de 125. Al enfriar a temperatura ambiente en los tubos de ensayo, se puede cristalizar
algo de bórax. Regresar esas muestras a un baño de agua tibia (~ 55 ° C) hasta que todo el sólido
se disuelva
Diluir cada muestra a aproximadamente 25 ml con agua tibia y destilada. Agregue 2–3 gotas de
verde de bromocresol. Valorice cada una de las cinco muestras a un punto final amarillo con la
solución de HCl estandarizada preparada en la. Recuerde registrar las lecturas de bureta antes y
después de cada análisis de una muestra.
Anda mungkin juga menyukai
- Comic Del AguaDokumen9 halamanComic Del AguaIvan Ivenian91% (11)
- Practica Secado Introduccion EsiqieDokumen8 halamanPractica Secado Introduccion EsiqieEdwin Valadez100% (1)
- Tarea 2, Loor Intriago, Termodinámica, Paralelo B.Dokumen10 halamanTarea 2, Loor Intriago, Termodinámica, Paralelo B.Andres Saud100% (2)
- Planta de Acido Sulfurico en Eucaliptus EnviarDokumen3 halamanPlanta de Acido Sulfurico en Eucaliptus EnviarIvan IvenianBelum ada peringkat
- LA CREACION TrigueirinhoDokumen145 halamanLA CREACION TrigueirinhoGabriel Galetti100% (2)
- Termodinámica de Disolución de BoraxDokumen3 halamanTermodinámica de Disolución de BoraxIvan IvenianBelum ada peringkat
- Formulario FisicoquimicaDokumen4 halamanFormulario FisicoquimicaArturo Álvarez SilvaBelum ada peringkat
- Practica Analisis Funcional #4Dokumen22 halamanPractica Analisis Funcional #4Oscar Carias100% (1)
- Determinacion de Las Propiedades de Un FluidoDokumen11 halamanDeterminacion de Las Propiedades de Un FluidoCesar OrozcoBelum ada peringkat
- Tarea 2.5 ConversionesDokumen3 halamanTarea 2.5 ConversionesdavidBelum ada peringkat
- Microbiologia Práctica 9Dokumen17 halamanMicrobiologia Práctica 9Fatima ChaconBelum ada peringkat
- Tema1 - ProblemasDokumen4 halamanTema1 - ProblemasaaniitaaBelum ada peringkat
- Test Del or de Calor Miniatura HT 33 de Tubos y Coraza1Dokumen5 halamanTest Del or de Calor Miniatura HT 33 de Tubos y Coraza1Sebas Castilla MatallanaBelum ada peringkat
- BalanceDokumen8 halamanBalanceAlex Pascual ToapantaBelum ada peringkat
- Cuantificación de ProteínasDokumen14 halamanCuantificación de ProteínasCamila GPobleteBelum ada peringkat
- Ejercicios 08-1 Guia Cap. 9.1 9.2 DifusionDokumen4 halamanEjercicios 08-1 Guia Cap. 9.1 9.2 DifusionMike UlloaBelum ada peringkat
- Desalinizacion Del Agua de Mar InformeDokumen8 halamanDesalinizacion Del Agua de Mar InformePauly AndreaBelum ada peringkat
- Obtencion de BioanticorrosivoDokumen25 halamanObtencion de BioanticorrosivoMarcos ManciaBelum ada peringkat
- Problema Balance de Energía Con Reacción QuímicaDokumen11 halamanProblema Balance de Energía Con Reacción QuímicaFrancisco Javier Dominguez De Los SantosBelum ada peringkat
- MANUALDokumen44 halamanMANUALClaudia RTapiaBelum ada peringkat
- EtanolDokumen15 halamanEtanolReyna NolascoBelum ada peringkat
- Curva Característica de Bombas Conectadas en Serie, Con El Módulo HM 150.16.Dokumen11 halamanCurva Característica de Bombas Conectadas en Serie, Con El Módulo HM 150.16.Jorge Alonso Flores ChacollaBelum ada peringkat
- Problemas Practica 2 PDFDokumen3 halamanProblemas Practica 2 PDFAnderson GRBelum ada peringkat
- Informe Practica de Laboratorio Neutralizacion y TitulacionDokumen5 halamanInforme Practica de Laboratorio Neutralizacion y TitulacionRedison RiosBelum ada peringkat
- Cuantificacion de Mentol PDFDokumen8 halamanCuantificacion de Mentol PDFinvestigacion fabaBelum ada peringkat
- Taller. Soluciones.Dokumen2 halamanTaller. Soluciones.Ana María Muñoz JaramilloBelum ada peringkat
- 12 (Cromatografía Líquida de Alta Resolución, Determinación de Azúcares en Mieles)Dokumen2 halaman12 (Cromatografía Líquida de Alta Resolución, Determinación de Azúcares en Mieles)Diego A. RoblesBelum ada peringkat
- Mezclas Simples - FisicoquimicaDokumen17 halamanMezclas Simples - Fisicoquimicasergio castañedaBelum ada peringkat
- Determinación Experimental de La Constante de Equilibrio Del Ácido Acético.Dokumen1 halamanDeterminación Experimental de La Constante de Equilibrio Del Ácido Acético.ckireBelum ada peringkat
- Quimica # 3Dokumen19 halamanQuimica # 3melissBelum ada peringkat
- Ingenieria de Defectos de Nanomateriales para CatálisisDokumen4 halamanIngenieria de Defectos de Nanomateriales para CatálisisAlvaro Vargas RodriguezBelum ada peringkat
- Ejercicios de Balances de EnergíaDokumen2 halamanEjercicios de Balances de EnergíaAndreaBelum ada peringkat
- FisicoquimicaDokumen65 halamanFisicoquimicaAlfredo JbBelum ada peringkat
- Fuel OilDokumen5 halamanFuel OilWilians Churqui CondoriBelum ada peringkat
- Halogenuros de AlquiloDokumen15 halamanHalogenuros de AlquiloMarco Antonio Sierra100% (2)
- Problemario de Termodinamica 2Dokumen3 halamanProblemario de Termodinamica 2Esteban Reyes Ramos0% (1)
- Caracteristicas KPDokumen3 halamanCaracteristicas KPjcccp941016Belum ada peringkat
- Preparación de Solución de Coagulantes y Polielectrolitos para Los Ensayos de Pruebas de JarraDokumen4 halamanPreparación de Solución de Coagulantes y Polielectrolitos para Los Ensayos de Pruebas de JarraElizabethBarrantesBartraBelum ada peringkat
- Primera Ley de La TermodinámicaDokumen8 halamanPrimera Ley de La TermodinámicaAriana AlarcoBelum ada peringkat
- Composicion Quimica Del PinoDokumen4 halamanComposicion Quimica Del Pinomaru_tekero_4607223250% (2)
- Análisis de La Operación Unitaria Intercambio IónicoDokumen19 halamanAnálisis de La Operación Unitaria Intercambio IónicoRAFAEL LEONARDO LUGO PIRAQUIVEBelum ada peringkat
- Taller 1 - GasesDokumen2 halamanTaller 1 - GasesVerificadores calidadBelum ada peringkat
- Boletin Obtencion EtilenoDokumen2 halamanBoletin Obtencion EtilenoJ Gonzalo Chuquimia MuñozBelum ada peringkat
- INFORME QUIMICA 8listoDokumen13 halamanINFORME QUIMICA 8listojuan inocBelum ada peringkat
- Bomba CalorimetricaDokumen8 halamanBomba CalorimetricaJOSE ERAZO100% (2)
- Fuerza Ionica.Dokumen2 halamanFuerza Ionica.David0% (1)
- Clase 03 2017Dokumen31 halamanClase 03 2017Alexis RodriguezBelum ada peringkat
- MateriaDokumen26 halamanMateriaMARIA ELIZABETH GOMEZ ORTIZBelum ada peringkat
- 21.3 - Técnicas de Cristalización y SublimaciónDokumen8 halaman21.3 - Técnicas de Cristalización y SublimaciónAlejandra MorenoBelum ada peringkat
- Informe de Laboratorio Destilación FraccionadaDokumen11 halamanInforme de Laboratorio Destilación Fraccionadadanna gabriela pereira villanuevaBelum ada peringkat
- Deber N1-Diagrama de Flujo de Tratamiento de AguaDokumen8 halamanDeber N1-Diagrama de Flujo de Tratamiento de AguaMichelle Coello100% (1)
- Nomenclatura de Equipos Equipos para PFD PDFDokumen15 halamanNomenclatura de Equipos Equipos para PFD PDFKamilaRiquelmeVidalBelum ada peringkat
- Practica 5-Destilacion de Aceite de Naranja Por Arrastre de VaporDokumen7 halamanPractica 5-Destilacion de Aceite de Naranja Por Arrastre de Vaporandersson7750% (2)
- Parcial FisicoquímicaDokumen1 halamanParcial FisicoquímicaDaniela BarreraBelum ada peringkat
- Ejercicios Tercera EvaluacionDokumen8 halamanEjercicios Tercera EvaluacionFernando Luqui MartinezBelum ada peringkat
- Parametros TermodinámicosDokumen22 halamanParametros TermodinámicosMiguel BrionesBelum ada peringkat
- Reformacion Con Vapor de Agua PDFDokumen9 halamanReformacion Con Vapor de Agua PDFVictor Hugo FloresBelum ada peringkat
- Ejercicios Contaminacion AtmosfericaDokumen109 halamanEjercicios Contaminacion AtmosfericaÁngel Olazo67% (3)
- Práctica No. 4 Extracción de Fosfatasa Alcalina, Efecto de PH, Temperatura, Velocidad de Reacción-Actividad de SustratoDokumen7 halamanPráctica No. 4 Extracción de Fosfatasa Alcalina, Efecto de PH, Temperatura, Velocidad de Reacción-Actividad de SustratoLyseth GómezBelum ada peringkat
- Hoja de Problemas 12 (QGB 22-23)Dokumen5 halamanHoja de Problemas 12 (QGB 22-23)guesorrock 888Belum ada peringkat
- Termoquimica en SolucionDokumen20 halamanTermoquimica en SolucionIvanBelum ada peringkat
- Adsorción de Ácido Acético Con Carbón ActivadoDokumen26 halamanAdsorción de Ácido Acético Con Carbón ActivadoAndres Garcia OcampoBelum ada peringkat
- Tarea 2. Sistemas BinariosDokumen4 halamanTarea 2. Sistemas BinariosMontsZs G-oBelum ada peringkat
- ClaseN°4 2018 PDFDokumen53 halamanClaseN°4 2018 PDFAnonymous 9IwTTjHzBelum ada peringkat
- Camara de RefrigeracionDokumen10 halamanCamara de RefrigeracionIvan IvenianBelum ada peringkat
- INforme Cinetica QuimicaDokumen3 halamanINforme Cinetica QuimicaIvan IvenianBelum ada peringkat
- Informe CatalisisProcesos de Obtención de Ácido SulfúricoDokumen6 halamanInforme CatalisisProcesos de Obtención de Ácido SulfúricoIvan IvenianBelum ada peringkat
- Práctica de Operaciones de Separación Sol-Liq PDFDokumen8 halamanPráctica de Operaciones de Separación Sol-Liq PDFIvan IvenianBelum ada peringkat
- Produccion de Jugo de ToronjaDokumen2 halamanProduccion de Jugo de ToronjaIvan IvenianBelum ada peringkat
- Informe CatalisisProcesos de Obtención de Ácido SulfúricoDokumen6 halamanInforme CatalisisProcesos de Obtención de Ácido SulfúricoIvan IvenianBelum ada peringkat
- Celda de MercurioDokumen1 halamanCelda de MercurioIvan IvenianBelum ada peringkat
- Informe 5Dokumen5 halamanInforme 5Ivan Ivenian100% (1)
- Fosforo GasolinaDokumen3 halamanFosforo GasolinaIvan IvenianBelum ada peringkat
- CascadaDokumen1 halamanCascadaIvan IvenianBelum ada peringkat
- Indice de Neutralización Y Saponificación de Un Aceite LubricanteDokumen1 halamanIndice de Neutralización Y Saponificación de Un Aceite LubricanteIvan IvenianBelum ada peringkat
- Informe 6Dokumen6 halamanInforme 6Ivan Ivenian0% (1)
- Pilas GalvanicasDokumen2 halamanPilas GalvanicasIvan IvenianBelum ada peringkat
- Celda de DiafragmaDokumen2 halamanCelda de DiafragmaIvan IvenianBelum ada peringkat
- Obtención Del NaOHDokumen6 halamanObtención Del NaOHIvan Ivenian100% (1)
- Preparación de NaOH Medios No ElectroquimicosDokumen2 halamanPreparación de NaOH Medios No ElectroquimicosIvan IvenianBelum ada peringkat
- CUESTIONARIO ElectroquimicaDokumen2 halamanCUESTIONARIO ElectroquimicaIvan IvenianBelum ada peringkat
- Rendimiento BombaDokumen6 halamanRendimiento BombaIvan IvenianBelum ada peringkat
- Analisis Instrumental PolarimetriaDokumen1 halamanAnalisis Instrumental PolarimetriaIvan Ivenian100% (1)
- Ecuaciones Adimensionales y de SemejanzaDokumen2 halamanEcuaciones Adimensionales y de SemejanzaIvan IvenianBelum ada peringkat
- Factores Que Influyen en La VisionDokumen8 halamanFactores Que Influyen en La VisionFrank OliveraBelum ada peringkat
- Apuntes AntropometriaDokumen5 halamanApuntes AntropometriaIsrael RiveraBelum ada peringkat
- Reveladores de TensiónDokumen4 halamanReveladores de TensiónDeivith CondorpuzaBelum ada peringkat
- 2018-1 CB121 Trabajo EscalonadoDokumen36 halaman2018-1 CB121 Trabajo EscalonadoMack Bruno Manzano ChaucaBelum ada peringkat
- Cónicas. Circunferencia - 1 5TO AÑODokumen17 halamanCónicas. Circunferencia - 1 5TO AÑOMaite DelgadoBelum ada peringkat
- Parcial 5Dokumen4 halamanParcial 5SamjuelBelum ada peringkat
- Prueba Unida 1 La Luz 3°Dokumen3 halamanPrueba Unida 1 La Luz 3°Johana FuentesBelum ada peringkat
- Diseño de DisparoDokumen10 halamanDiseño de DisparoMoises Gonzalez SanguinoBelum ada peringkat
- Clase 6Dokumen24 halamanClase 6Geissler Bejarano CozBelum ada peringkat
- 4ta Guía Mat Ii Lapso-1Dokumen11 halaman4ta Guía Mat Ii Lapso-1JuanBelum ada peringkat
- Especificaciones Tecnicas To Cs Manco Capac OkDokumen11 halamanEspecificaciones Tecnicas To Cs Manco Capac OkCesar CcsBelum ada peringkat
- Manual Intelliscan 33 Zonas EspañolDokumen19 halamanManual Intelliscan 33 Zonas EspañolAlexanderBelum ada peringkat
- Interpretacion de La Herramienta de CaracterizacionDokumen135 halamanInterpretacion de La Herramienta de CaracterizacionWendy Herrera RodriguezBelum ada peringkat
- Taller Farmacia Magistral Forma Farmaceutica PolvosDokumen8 halamanTaller Farmacia Magistral Forma Farmaceutica PolvosStefany OspinaBelum ada peringkat
- Circuito ElevadorDokumen5 halamanCircuito ElevadorEddy PaulBelum ada peringkat
- Ecuacion de 2º Grado o Ecuacion CuadraticaDokumen5 halamanEcuacion de 2º Grado o Ecuacion Cuadraticajota354Belum ada peringkat
- Conexion Delta AbiertaDokumen15 halamanConexion Delta AbiertawilliamII0% (1)
- Memoria Descriptiva La LindaDokumen13 halamanMemoria Descriptiva La LindaCesar Laguna HuancaBelum ada peringkat
- Clase 2 Numeros RacionalesDokumen29 halamanClase 2 Numeros Racionalesffuentes_chacanaBelum ada peringkat
- CulvertsDokumen25 halamanCulvertsVictor PuglieseBelum ada peringkat
- Cuadro ComparativoDokumen4 halamanCuadro Comparativoanon_342918554100% (1)
- Catalogo de Aceros OteloDokumen64 halamanCatalogo de Aceros OteloLuis Anacari Tupel0% (1)
- Eln-356 Elect Analogica IDokumen2 halamanEln-356 Elect Analogica IRicardo Edilson M. FloresBelum ada peringkat
- 01-Manual MultimetroDokumen10 halaman01-Manual MultimetroJose RdrigoBelum ada peringkat
- Tiro ParabolicoDokumen8 halamanTiro ParabolicoMichael CastroBelum ada peringkat
- Evaluacion Practica Fisica Ruben MartinezDokumen8 halamanEvaluacion Practica Fisica Ruben MartinezrubenBelum ada peringkat
- FLEXIONDokumen5 halamanFLEXIONJavier MedinaBelum ada peringkat
- Historial Calificaciones 1193206866Dokumen2 halamanHistorial Calificaciones 1193206866David HernandezBelum ada peringkat