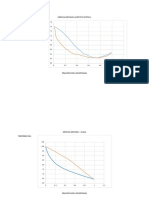
1, 2 y 3
Diunggah oleh
DavidDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
1, 2 y 3
Diunggah oleh
DavidHak Cipta:
Format Tersedia
1.- Una solución contiene 5g de urea por cada 100g de agua.
Si la solución obedece la Ley de
Raoult, ¿Cuál es la expresión total de burbuja a 25°C?, ¿Sería mayor o menor la presión de burbuja
si la urea fuese volátil?
𝑏
𝑎
𝑃1𝑠𝑎𝑡 = 𝑒 𝑇(°𝐶)+𝐶1
𝑃 = 𝑋𝐵 𝑃𝐵𝑠𝑎𝑡
𝐻20
100𝑔𝐻2𝑂
𝑃𝑀 =𝑀= = 5.55 𝑚𝑜𝑙𝑒𝑠
18𝑔/𝑚𝑜𝑙 𝑢𝑟𝑒𝑎
𝑈𝑟𝑒𝑎
5𝑔
𝑃𝑀 =𝑀= = 0.083 𝑚𝑜𝑙𝑒𝑠
60.06𝑔
𝑢𝑟𝑒𝑎
𝑚𝑜𝑙
𝑀𝑇 = 5.638 𝑚𝑜𝑙𝑒𝑠 𝑡𝑜𝑡𝑎𝑙𝑒𝑠
5.55 𝑚𝑜𝑙𝑒𝑠
𝑋𝐵 = = 0.985
5.638 𝑚𝑜𝑙𝑒𝑠 𝑡𝑜𝑡𝑎𝑙𝑒𝑠
0.083 𝑚𝑜𝑙𝑒𝑠
𝑋𝐴 = = 0.0147
5.638 𝑚𝑜𝑙𝑒𝑠 𝑡𝑜𝑡𝑎𝑙𝑒𝑠
CONSTANTE DE ANTOINE.
A = 16.3872 B= 3885.70 C = 230.170
3885.7
𝑃1𝑠𝑎𝑡 = 𝑒 16.3872−25+230.170 =3.1877𝐾𝑃𝑎
Temperatura baja = presión baja.
2.- Una solución formada de 10 g de un soluto orgánico no volátil y 100 g de éter dietílico ejerce
una presión de burbuja de 426 mmHg a 20°C. La presión de vapor del éter puro es 442.2 mmHg a
esa temperatura. ¿Cuál es el peso molecular del soluto?
PM = ¿SOLUTO?
PM ETER DIETÍLICO = 74.10 g/mol
10𝑔
= 𝑚𝑜𝑙. 𝑠𝑜𝑙𝑢𝑡𝑜
𝑃𝑀
𝑚 100𝑔 𝑒𝑡𝑒𝑟 𝑑𝑖𝑒𝑡í𝑙𝑖𝑐𝑜
𝑛= 𝑃𝑀
= 74.10𝑔/𝑚𝑜𝑙
= 1.35 moles de éter.
Fracc. Molar del éter.
𝑛𝑏
𝑋𝐵 =
𝑛𝑎 + 𝑛𝑏
1.3514 𝑚𝑜𝑙 𝑑𝑒 é𝑡𝑒𝑟 426 𝑚𝑚𝐻𝑔
𝑋𝐵 = =
10 442.2
𝑃𝑀 + 1.3514 𝑚𝑜𝑙𝑒𝑠 𝑒𝑡𝑒𝑟
1.3514𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 𝑒𝑡𝑒𝑟 426𝑚𝑚𝐻𝑔
= = 0.9633
10 442𝑚𝑚𝐻𝑔
+ 1.351 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 𝑒𝑡𝑒𝑟
𝑃𝑀
Resuelves ecuación para peso molecular.
10 1.3514 𝑚𝑜𝑙𝑒𝑠 𝑑𝑒 é𝑡𝑒𝑟
+ 1.3514 =
𝑃𝑀 0.9633
10
+ 1.3514 = 1.4028
𝑃𝑀
3.- Si 30 g de difenilo se disuelven en 250g de benceno, ¿Cuál será el punto de ebullición
resultante bajo la presión atmosférica?, ¿Cuál es el aumento del punto de ebullición del solvente?
P atm
𝑃𝑎𝑡𝑚 = 𝑋𝑐12𝐻10 ∗ 𝑃𝑐12𝐻2𝑂 + 𝑋𝐶6𝐻6 ∗ 𝑃𝐶6𝐻6
1 𝑚𝑜𝑙
30𝑔 154𝑔
= 0.1948 𝑚𝑜𝑙
1 𝑚𝑜𝑙
2.50 𝑔𝑟 70𝑔 = 3.21 𝑚𝑜𝑙
Moles totales= 3.40
𝑚𝑜𝑙𝑒𝑠
𝑋𝐴 =
𝑚𝑜𝑙. 𝑡𝑜𝑡𝑎𝑙𝑒𝑠
0.1948 3.21
𝑋𝐴 = = 0.057 𝑋𝐵 = = 0.94
3.40 3.40
𝐵𝑎 𝐵𝑏
𝑃 = 𝑋𝐴 𝑒 𝐴𝑎−𝑇+𝐶𝑎 + 𝑋𝐵 𝑒 𝐴𝑏−𝑇+𝐶𝑏
𝐵
𝑇 = 𝐴−𝑙𝑜𝑔10 𝑃𝑟𝑜𝑝. − 𝐶
1134.240
𝑇𝐵𝑒𝑛𝑐𝑒𝑛𝑜 = − 217.57 = 77.75°𝐶
3.98523 − 𝑙𝑜𝑔10(0.95)
1134.246
𝑇= − 185.15 = 155°𝐶
41887 − 𝑙𝑜𝑔10(0.06)
Anda mungkin juga menyukai
- 982 Tarea%2BSegundo%2BParcialDokumen2 halaman982 Tarea%2BSegundo%2BParcialCarlos Andres Perez50% (2)
- A4-EjerciciosDokumen7 halamanA4-EjerciciosRsfwfdjhhhBelum ada peringkat
- Determinacion de La Razón CP-CV Practica 2Dokumen4 halamanDeterminacion de La Razón CP-CV Practica 2hellmasterBelum ada peringkat
- Parcial FinalDokumen3 halamanParcial FinalSebastian OcampoBelum ada peringkat
- SISTEMAS_ABIERTOS_SEGUNDO_CORTEDokumen5 halamanSISTEMAS_ABIERTOS_SEGUNDO_CORTEJohn Nicolás Garzón HerránBelum ada peringkat
- Sistemas que requieren la solución simultánea del balance de materia y energíaDokumen2 halamanSistemas que requieren la solución simultánea del balance de materia y energíaJocelyn Grisel García GonzálezBelum ada peringkat
- TALLER 3 BalanceDokumen5 halamanTALLER 3 BalanceJhonatan SalazarBelum ada peringkat
- Sistemas abiertos a régimen permanenteDokumen21 halamanSistemas abiertos a régimen permanenteHarry Vara MarceloBelum ada peringkat
- Ejer Cici OsDokumen10 halamanEjer Cici OsagussbaBelum ada peringkat
- Determinación de hidratos de carbono en harina de trigoDokumen8 halamanDeterminación de hidratos de carbono en harina de trigoCelina GoffredoBelum ada peringkat
- Calorimetría de CombustiónDokumen4 halamanCalorimetría de CombustiónDeyaniraBelum ada peringkat
- Problemario 3Dokumen7 halamanProblemario 3Melisa Marquez Gomez0% (1)
- Sistema Benceno ExposiciónDokumen5 halamanSistema Benceno ExposiciónPablo Vargas100% (1)
- PDF Traducido de Termo 1 DDDokumen26 halamanPDF Traducido de Termo 1 DDJosé Castañeda100% (1)
- Problema 4 de Destilacion Benceno-ToluenoDokumen5 halamanProblema 4 de Destilacion Benceno-ToluenoRaymundo Salinas RamirezBelum ada peringkat
- Estructura Académica Ingeniería de Alimentos ReformaDokumen1 halamanEstructura Académica Ingeniería de Alimentos ReformaAlejandro PalominoBelum ada peringkat
- Examen 2 Cinética.Dokumen6 halamanExamen 2 Cinética.María Fernanda López Díaz100% (1)
- Ejercicios Desarrollados Semana 13.Dokumen9 halamanEjercicios Desarrollados Semana 13.Harollk Timkopa VemthuraBelum ada peringkat
- Termoquímica: Bomba CalorimétricaDokumen9 halamanTermoquímica: Bomba CalorimétricaMarisolBelum ada peringkat
- Taller 3Dokumen1 halamanTaller 3hitayosara fernandezBelum ada peringkat
- Ejercicios PropuestosDokumen22 halamanEjercicios PropuestosAlexander Gutierrez ChirinosBelum ada peringkat
- Gravedad APIDokumen4 halamanGravedad APICristian VallejoBelum ada peringkat
- Informe Componente PracticoDokumen21 halamanInforme Componente PracticoAnonymous CBGXUu5Belum ada peringkat
- Metodo de MerkelDokumen9 halamanMetodo de MerkelOSCAR ORTEGA REGALADOBelum ada peringkat
- Evaluar T, v, u, a y g a partir de h(s,PDokumen4 halamanEvaluar T, v, u, a y g a partir de h(s,PAyrton Jimenez InfantesBelum ada peringkat
- Gases reales: Propano a 320 K y 16 barDokumen8 halamanGases reales: Propano a 320 K y 16 barAngela tmBelum ada peringkat
- Problemario fq2Dokumen6 halamanProblemario fq2JorgeBelum ada peringkat
- Propiedades sólidos laboratorioDokumen9 halamanPropiedades sólidos laboratoriopaulaBelum ada peringkat
- IsotermasDokumen6 halamanIsotermasSamu Benito100% (1)
- Serie Ciclos. 21-IIDokumen8 halamanSerie Ciclos. 21-IIAbigail AndreaBelum ada peringkat
- Asignación #2 Valor 10Dokumen3 halamanAsignación #2 Valor 10AlejandroBorjasBelum ada peringkat
- Problemariouni3 IAFR 20310350Dokumen9 halamanProblemariouni3 IAFR 20310350Ivan FloresBelum ada peringkat
- Datos Termodinámicos de Acetato de Etilo y Sosa CáusticaDokumen5 halamanDatos Termodinámicos de Acetato de Etilo y Sosa CáusticaSamantha Elizabeth Borjón CastroBelum ada peringkat
- Probl Res IADokumen46 halamanProbl Res IArobertoam15100% (2)
- Actividad 5. Ej 1Dokumen6 halamanActividad 5. Ej 1DULCE GARCIA100% (1)
- 06-Principio de PascalDokumen3 halaman06-Principio de PascalSANTAMARIA ÑIQUEN ADRIANA BRIGITTEBelum ada peringkat
- UNIDAD3Dokumen118 halamanUNIDAD3Jorge KrischBelum ada peringkat
- Practica 6Dokumen3 halamanPractica 6EdiMiguelHernandezHernandezBelum ada peringkat
- Faiia Seminario X FinalDokumen1 halamanFaiia Seminario X Finaldany condori crispinBelum ada peringkat
- Asignación Balances Materia Sistemas Reactivos PDFDokumen1 halamanAsignación Balances Materia Sistemas Reactivos PDFAlexander Mera0% (1)
- Práctica 3Dokumen13 halamanPráctica 3Itzel Daniela Solis Tinoco100% (1)
- Tarea 2. Torres MendozaDokumen4 halamanTarea 2. Torres MendozaLisensiado LlovisBelum ada peringkat
- Termodinámica: Ejercicios de propiedades de sustancias purasDokumen9 halamanTermodinámica: Ejercicios de propiedades de sustancias purasitzelBelum ada peringkat
- Taller de Eficiencia Tamizado 2Dokumen1 halamanTaller de Eficiencia Tamizado 2javier orlando Delgado100% (1)
- INCROPERA - Transferencia de CalorDokumen23 halamanINCROPERA - Transferencia de CalorMiguel Montero Alonso100% (1)
- 3.1-3.3 Tamizado.Dokumen4 halaman3.1-3.3 Tamizado.VALERIA SUSANA REYNAGA RUBIOBelum ada peringkat
- Balance de MateriaDokumen6 halamanBalance de MateriaKathyCortezNuñezBelum ada peringkat
- Propiedades sustancias puras PVT T2Dokumen2 halamanPropiedades sustancias puras PVT T2dead canoBelum ada peringkat
- Universidad Nacional José Faustino Sanchez CarriónDokumen11 halamanUniversidad Nacional José Faustino Sanchez CarriónKevin DominguezchavezBelum ada peringkat
- PackDokumen7 halamanPackManolo BeniqueBelum ada peringkat
- Ejercicios 01 (Métodos Númericos) PDFDokumen9 halamanEjercicios 01 (Métodos Númericos) PDFLaura Yuliana Archila GonzalezBelum ada peringkat
- Fenomenos de TransporteDokumen16 halamanFenomenos de TransporteMarco Antonio Cervantes SacachipanaBelum ada peringkat
- Lab 1 de TermodianmicaDokumen7 halamanLab 1 de TermodianmicaYara VargasBelum ada peringkat
- Deber 3 - Continuación Primera LeyDokumen2 halamanDeber 3 - Continuación Primera LeyAndrés CaicedoBelum ada peringkat
- ProblemasDokumen10 halamanProblemasclaudiaBelum ada peringkat
- Determinacion Presion de VaporDokumen8 halamanDeterminacion Presion de VaporJuliana Rojas OtaloraBelum ada peringkat
- Sanroman Patiño Actividad 4 PDFDokumen13 halamanSanroman Patiño Actividad 4 PDFKarlaSanroman50% (2)
- ADA1. Problemario Introducción A QADokumen7 halamanADA1. Problemario Introducción A QAAlejandrp Josue Cardeña BenitezBelum ada peringkat
- 1-7 MergedDokumen19 halaman1-7 MergedArturo González LinaresBelum ada peringkat
- DibujoDokumen1 halamanDibujoDavidBelum ada peringkat
- Diagrama de FlujoDokumen7 halamanDiagrama de FlujoDavidBelum ada peringkat
- Diagrama de FlujoDokumen7 halamanDiagrama de FlujoDavidBelum ada peringkat
- Práctica 1. Pregunta GeneradoraDokumen4 halamanPráctica 1. Pregunta GeneradoraDavidBelum ada peringkat
- Gráficas Metanol+acetato de Etilo y Metanol+agua PDFDokumen2 halamanGráficas Metanol+acetato de Etilo y Metanol+agua PDFDavidBelum ada peringkat
- Práctica 1. PGDokumen15 halamanPráctica 1. PGDavidBelum ada peringkat
- Práctica 1. Pregunta GeneradoraDokumen4 halamanPráctica 1. Pregunta GeneradoraDavidBelum ada peringkat
- ProblemarioDokumen2 halamanProblemarioDavidBelum ada peringkat
- Práctica 1. Pregunta GeneradoraDokumen4 halamanPráctica 1. Pregunta GeneradoraDavidBelum ada peringkat
- A Que Temperatura Se Congela La Sangre Del Cuerpo HumanoDokumen2 halamanA Que Temperatura Se Congela La Sangre Del Cuerpo HumanoDavidBelum ada peringkat
- Convocatoria PermanenciaDokumen1 halamanConvocatoria PermanenciaChino GomezBelum ada peringkat
- Fisicoqu Mica Tablas Metanol Benceno TerminadoDokumen6 halamanFisicoqu Mica Tablas Metanol Benceno TerminadoDavidBelum ada peringkat
- SSDCDVDokumen8 halamanSSDCDVDavidBelum ada peringkat
- FisicquimicaDokumen8 halamanFisicquimicaDavidBelum ada peringkat
- BIOQUIMICADokumen3 halamanBIOQUIMICADavidBelum ada peringkat
- Guia COREANO 2da Unidad 6to SemestreDokumen10 halamanGuia COREANO 2da Unidad 6to SemestreDavidBelum ada peringkat
- SimbiosisDokumen2 halamanSimbiosisDavidBelum ada peringkat
- PSEUDokumen44 halamanPSEUDavidBelum ada peringkat
- Título - Docx Equipos de Perforacion Petrolera en BoliviaDokumen36 halamanTítulo - Docx Equipos de Perforacion Petrolera en BoliviaAnonymous DxHNPl0IGBelum ada peringkat
- Transformadores TrihalDokumen2 halamanTransformadores TrihalJOSE GUILLERMOBelum ada peringkat
- Análisis Estático de La Capacidad de Carga de Un PiloteDokumen22 halamanAnálisis Estático de La Capacidad de Carga de Un PiloteAlejandro Poblete PalavecinoBelum ada peringkat
- Ley de Ampere y Biot-SavartDokumen3 halamanLey de Ampere y Biot-SavartJose Cruz MichagaBelum ada peringkat
- Act 14 Quiz FisicoquimicaDokumen6 halamanAct 14 Quiz FisicoquimicadacavelBelum ada peringkat
- Cálculo de TransformadorDokumen20 halamanCálculo de TransformadorRandyBelum ada peringkat
- Prevencion Riesgos ElectricosDokumen10 halamanPrevencion Riesgos ElectricosaysBelum ada peringkat
- Modelacion Flexion y Corte-RuaumokoDokumen67 halamanModelacion Flexion y Corte-RuaumokoAnonymous z1bnQM4Belum ada peringkat
- Inventario CompjNUEVO 06-04-17) FDokumen56 halamanInventario CompjNUEVO 06-04-17) FAlejandro Renato Rengifo LedesmaBelum ada peringkat
- Representacion Grafica de ConexionesDokumen19 halamanRepresentacion Grafica de ConexionesMilagros DanitzaBelum ada peringkat
- Entrenamiento A La Red - Electricidad BasicaDokumen107 halamanEntrenamiento A La Red - Electricidad BasicaEnriqueBelum ada peringkat
- NTC1332 Alambres y Cables Con Aislamiento TermoplásticoDokumen152 halamanNTC1332 Alambres y Cables Con Aislamiento TermoplásticoNicolas PeraltaBelum ada peringkat
- CAPITULO 7 TransicionesDokumen30 halamanCAPITULO 7 TransicionesMARIANOBelum ada peringkat
- Impr LC AlternaDokumen4 halamanImpr LC AlternaÁngeles Campaña OlmosBelum ada peringkat
- PRUEBA SABER 2018 resumenDokumen47 halamanPRUEBA SABER 2018 resumenmaye camargoBelum ada peringkat
- Grúas Giratorias Fijas.Dokumen60 halamanGrúas Giratorias Fijas.Anonymous PAd5e7LaXY100% (1)
- Arco TeoriaDokumen27 halamanArco TeoriaJosue LewandowskiBelum ada peringkat
- Foro 4Dokumen10 halamanForo 4elius213Belum ada peringkat
- La Porcelana DentalDokumen2 halamanLa Porcelana DentalDavidGym100% (1)
- Disoluciones Ideales TermodinámicaDokumen18 halamanDisoluciones Ideales TermodinámicaMonse GuerraBelum ada peringkat
- Estudio Del Efecto de La Temperatura Sobre La Velocidad de ReaccionDokumen13 halamanEstudio Del Efecto de La Temperatura Sobre La Velocidad de ReaccionJuanCarlosPeñaAyalaBelum ada peringkat
- Laboratorio de EnsayoDokumen12 halamanLaboratorio de EnsayoMarianita Eliz RobayoBelum ada peringkat
- Resumen de Precipitaciones-Grupo N°3Dokumen14 halamanResumen de Precipitaciones-Grupo N°3Luis DimasBelum ada peringkat
- Ernest RutherfordDokumen2 halamanErnest RutherfordafrowbyBelum ada peringkat
- Electrostatica Y Ley de CoulombDokumen8 halamanElectrostatica Y Ley de CoulomblindachickBelum ada peringkat
- Normas de CortesíaDokumen2 halamanNormas de CortesíaMarcos OrozcoBelum ada peringkat
- Cálculo de vigas y columnas: Fuerzas cortantes y momentos flexionantesDokumen19 halamanCálculo de vigas y columnas: Fuerzas cortantes y momentos flexionantesanon_707269376Belum ada peringkat
- Informe Lab Pendulo Simple Fisica IIDokumen11 halamanInforme Lab Pendulo Simple Fisica IIRafael A Cubillos R33% (3)
- Antenas 1 Capítulo 10 Tomasi IISemestre 09Dokumen61 halamanAntenas 1 Capítulo 10 Tomasi IISemestre 09Joseph AparicioBelum ada peringkat