Bab6 Detail Junction Fix
Diunggah oleh
Valenci MiyakeeJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Bab6 Detail Junction Fix
Diunggah oleh
Valenci MiyakeeHak Cipta:
Format Tersedia
INTERAKSI MANUSIA DAN LINGKUNGAN Hidrosfer: lapisan air di permukaan bumi
- Hukum termodinamika
HUKUM I TERMODINAMIKA
dQ = dU + dW
Ket:
dQ : Energy supplied to or extracted from a closed
system
dU : Change in the internal energy of the system
dW : work done by the system
Hukum I termodinamika adalah penggambaran dari prinsip
konservasi energi, yaitu energi tidak dapat diciptakan dan
dimusnahkan PERSEBARAN POLUSI AIR PERMUKAAN
Energi internal total energi kinetik (termasuk gerak tidak Difusi: Ukiran partikel terdispersi dan pendispersi sama besar
beraturan, rotasi, dan getaran) dari semua atom dan Gerak brown: Ukuran partikel terdispersi lebih besar daripada
- Energi transfer
molekul, meliputi gas dan energi potensialnya pendispersi
KONDUKSI
Entalpi: H = U + pV - Persamaan Difusi
Proses perpindahan energi antara dua titik pada benda 𝑀
Ket: padat yang berbeda temperatur 𝐶=
𝑉
H : Heat content of the energy system Proses konduksi dicapai melalui dua cara, yaitu getaran Ket:
Termodynamic state function molekul dan perpindahan elektron konduksi AIR DALAM ORGANISME DAN LINGKUNGAN C : Concentration
U : Internal Energy Rumus: - Water Vapor : Kondisi saturasi 𝐹 = −𝐷∇𝐶
P : Pressure 𝑑𝑄 −𝑘 ∙ 𝐴 ∙ Δ𝑇 Titik seimbang tekanan uap tercapai apabila jumlah partikel yang Ket:
V : Volume =
dilepas air sama dengan jumlah yang ditangkap kembali oleh F : Flux menunjukkan arah ke mana partikel terdispersi
𝑑𝑇 𝐿
dH(perubahan entalpi dari sebuah reaksi kimia) Ket: air mengalir
dalam sebuah keadaan di mana tidak ada gaya eksternal, k : Konduktivitas termal D : Tetapan diffusivity/diffusion/...
maka dW=0, maka dH=dU KOVEKSI - partikel fisis
HUKUM II TERMODINAMIKA Proses perpindahan energi pada fluida ???
=Hukum Carnot Proses konveksi dicapai melalui dua cara, yaitu konveksi Di mana A adalah ketinggian di atas air laut(m) - Dispersi dalam aliran air
”di dalam sebuah mesin carnot/mesin penghasil panas, gaya alami dan buatan(ada gaya buatan yang memengaruhi)
yang bekerja dalam suatu sistem didapat dari transfer Rumus: dengan u=0
energi antara temperatur yang tinggi ke yang rendah. Hal 𝑑𝑄 Titik seimbang tekanan uap dicapai dalam sistem air tertutup
tersebut tidak dapat dibalik kecuali ada energi luar yang = −ℎ ∙ 𝐴 ∙ Δ𝑇 - Water Potential and Water Content PERSEBARAN POLUSI DALAM TANAH
𝑑𝑇 - Definisi dasar
memengaruhi” Ket: Water Content: Perbandingan antara volume air dengan total
(T1 − T2) h : Koefisien konveksi volumenya, atau perbandingan antara massa air dengan a. Impervious layer: lapisan kedap air (contoh: tanah liat)
e= b. Akuuifer: water-carrying layer (cobtoh: pasir, batu)
T1 RADIASI massa basah/kering material di dalamnya
Ket: 𝑉 c. Confined aquifer: lapisan akuifer di antara 2 lapisan
Proses perpindahan energi dalam bentuk gelombang 𝜃= 𝑤
T1 : Temperatur lebih tinggi 𝑉𝑡 impervious
elektromagnetik yang dapat melalui ruang hampa 𝑚𝑤
T2 : Temperatur lebih rendah 𝑤= d. Unconfined aquifer: lapisan akuifer di atas lapisan impervious
Rumus: 𝑚𝑡
HUKUM III TERMODINAMIKA Ket: (berhubungan dengan atmosfer)
𝑃 = 𝑒 ∙ 𝜎 ∙ 𝐴 ∙ 𝑇4
Energi mengalir dari temperatur tinggi ke rendah, maka V : Volume - Tegangan permukaan dan tanah
Ket:
umumnya energi akan mengalir dari sistem ke e : emisivitas(0-1) m : Massa dengan p = rho.g.h
lingkungan. Proses tersebut bersifat ireversibel. 𝜎 : Konstanta Stefan 5,67 ∙ 10−8 𝑊/𝑚2 𝐾 4 w : water mass - Hukum darcy
Lingkungan akan mendapat energi pada akhirnya EVAPORASI t : total mass q = −k grad φ
dS = dQ/T Proses menguapnya cairan d : dry mass Menggambarkan aliran air tanah.
Ket: 𝑄 =𝑚∙𝐿 Water Potential: Energi potensial permol, perunit massa, perunit
dS : perubahan entropi, akan bernilai lebih dari 0 Ket: volume, atau perunit berat, dari air, dengan referensi bahwa air
dQ : energi yang diperoleh lingkungan murni memiliki water potential sebesar 0
L :kalor lebur/kalor laten air: 2,25 ∙ 106 𝐽/𝑚2 𝐾 4
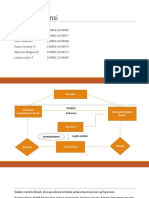
T : suhu akhir lingkungan - Biosfer Ψ = Ψ𝑔 + Ψ𝑚 + Ψ𝑝 + Ψ𝑜 vertical flow
Ludwig Boltzman mencetuskan adanya kemungkinan Skema hubungan energi dan massa dalam biosfer Ket:
entropi(W), yaitu Ψ : total water potential
𝑆 = 𝐾 ∙ 𝑙𝑛𝑊 g : gravitational component
Ket m : matric component horizontal flow
k : 1,38 ∙ 10−23 p : pressure component
W : kemungkinan energi yang didapat pengaruh o : osmotic component Permisalan dengan aliran stabil pada air tanah tanpa adanya
perbedaan distribusi partikel energi - Water Potentials in Organisms and their Surroundings perubahan jumlah air pada tanah.
- Transport masa dan momentum Pada MANUSIA: darah(-700J/kg), keringat(350J/kg), uriin(-400- - Simple flow in confined Aquifer
Mahluk hidup di alam bergantung pada perubahan(aliran) angin ishJ/kg) - Time Dependence in confined Aquifer
dan air yang bergantung pada trasnport massa, misalnya Pada TUMBUHAN, sel penghisap(-500-7000J/kg), Mesophytic(- - Adsoprtion dan desortion pollutan
pertukaran oksigen dan karbondioksida 1000-2000J/kg) Adsorpsi
Gaya yang terjadi secara natural di alam adalah bentuk trasnport Pada TANAH saat jenuh WP mendekati 0, namun terpengaruh
momentum gravitasi menjadi -10-30K/kg
Beberapa FUNGI dappat hidup dengan WP sebesr -5—70kJ/kg
- Relation of Liquid- to Gas-Phase Water
- Hidrosfer dan Siklus hidrologi
Radikal hidroperoksil dapat mengalami reaksi rantai terminasi
seperti berikut ini:
HOO• + HO•→ H2O + O2
HOO• + HOO• → H2O2 + O2
Hidrogen peroksida, H2O2 yang terbentuk dapat keluar dari
atmosfer dengan jalan pengendapan.. radikal hidroperoksil
dapat bereaksi lebih lanjut yang menghasilkan kembali radikal
HO. Ketika bereaksi dengan NO atau ozon, O3.
LISTRIK DAN PENGUKURANNYA HOO•+ NO → NO2 + HO•
- Hukum Coulomb HOO• + O2 → 2 O2 + HO•
Hukum yang menjelaskan hubungan antara gaya yang timbul Hydroperoxyl radikal yang dibuat oleh dua reaksi berikut,
antara dua titik muatan, yang terpisahkan jarak tertentu, dimulai dengan photolytic disosiasi formaldehida untuk
dengan nilai muatan dan jarak pisah keduanya. menghasilkan reaksi radikal formyl:
𝑞1∙𝑞2
𝐹=𝑘 2
𝑟
HCHO + hn → H + HCO
Ket: HCO + O2 → HOO • + CO
k : Konstanta (9 ∙ 109 ) Hydroperoxyl radikal bereaksi lebih lambat dengan spesies lain
q : Muatan daripada hidroksil radikal. Kinetika dan mekanisme dari reaksi
- medan lisrik radikal hydroperoxyl sulit untuk dipelajari karena ini sulit untuk
Efek yang ditimbulkan oleh keberadaan muatan listrik, mempertahankan radikal bebas dari radikal hidroksil.
seperti elektron, ion, atau proton, dalam ruangan yang ada di
sekitarnya - Produksi ozon dari corona discharge
𝐹 /𝑞/
𝐸= =𝑘 2
𝑄 𝑟
- potensial listrik
Usaha yang diperlukan untuk memindahkan muatan positif
sebesar 1 satuan dari tempat tak terhingga ke suatu titik
tertentu
𝑞
𝑉=𝑘
𝑟
Σ𝑉 = 𝑣1 + 𝑣2 + 𝑣𝑛 O2 + e ——> 2 O + e (1)
- daya listrik O + O2 + M ——> O3 + (M) (2)
laju hantaran energi listrik dalam rangkaian listrik
O3 + O ——> 2 O2 (3)
𝑃 =𝑉∙𝐼
O3 + e ——-> O + O2 + e (4)
𝑉 =𝐼∙𝑅
-
CORONA DISCHARGE
- Plasma dan Corona Dicharge
Plasma adalah gas yang terionisasi dan merupakan fase keempat
dari sebuah materi.
Dari hasil penelitian, plasma dapat membunuh kuman, bakteri atau
mikroorrganisme
Pembuatan ozon dari oksigen merupakan salah satu proses
plasma kimia.
Corona discharge merupakan salah satu contoh alat
pengaplikasian plasma, alat ini menghasilkan ozom yang dapat
membunuh bakteri/kuman dan memecah senyawa-senyawa
berbahaya
- Proses terbentuknya radikal hidroksil
Pada altitude lebih tinggi, reaksi pembentukan radikal hidroksil
yang umum adalah fotolisis dari air,
H2O + hv → NO. + H
Untuk tujuan eksperimen di laboratorium dengan jalan fotolisis
uap asam nitrat seperti reaksi berikut ini :
HONO + hv → HO. + NO
Radikal hidroksil sering dapat dihilangkan dari lapisan troposfer
melalui reaksi dengan gas metana atau karbon monoksida :
CH4 + HO• → H2C• + H2O
CO + HO• → CO2 + H.
Selanjutnya radikal metal yang mempunyai kereaktifan tingg, H3C,
bereaksi dengan oksigen.
H3C• + O2 → H3COO• + H2O
Untuk membentuk methylperoxyl radikal, H3COO• Atom hidrogen
bereaksi dengan O2 untuk menghasilkan radikal hydroperoxyl:
H + O2 → HOO•
Radikal hidroperoksil terbentuk ketika hydrogen atomic yang
dihasilkan dari reaksi.
CO + HO•→ CO2 + H•
Anda mungkin juga menyukai
- KimlingagainDokumen2 halamanKimlingagainValenci MiyakeeBelum ada peringkat
- Translate Kimling Chapter 6 Bukan MikrobioDokumen3 halamanTranslate Kimling Chapter 6 Bukan MikrobioValenci MiyakeeBelum ada peringkat
- Resume Tugas PTPA Part 1Dokumen3 halamanResume Tugas PTPA Part 1Valenci MiyakeeBelum ada peringkat
- Resume Tugas PTPA Part 1Dokumen3 halamanResume Tugas PTPA Part 1Valenci MiyakeeBelum ada peringkat
- BAB 1,2,3,4 LaporanDokumen30 halamanBAB 1,2,3,4 LaporanValenci MiyakeeBelum ada peringkat
- Peta Perpipaan PDFDokumen1 halamanPeta Perpipaan PDFValenci MiyakeeBelum ada peringkat
- Contoh Logbook Kerja PraktikDokumen2 halamanContoh Logbook Kerja PraktikValenci MiyakeeBelum ada peringkat
- PunyaKimling 7.9Dokumen1 halamanPunyaKimling 7.9Valenci MiyakeeBelum ada peringkat
- KorespondensiDokumen6 halamanKorespondensiValenci MiyakeeBelum ada peringkat
- Bab6 Detail Junction FixDokumen6 halamanBab6 Detail Junction FixValenci MiyakeeBelum ada peringkat
- Lembar PengesahanDokumen2 halamanLembar PengesahanValenci MiyakeeBelum ada peringkat
- Lembar PengesahanDokumen3 halamanLembar PengesahanValenci MiyakeeBelum ada peringkat
- DeduksiDokumen4 halamanDeduksiValenci MiyakeeBelum ada peringkat
- Metris Uji HipotesisDokumen7 halamanMetris Uji HipotesisValenci MiyakeeBelum ada peringkat
- PP Nomor 27 Tahun 2012 Tentang Izin LingkunganDokumen50 halamanPP Nomor 27 Tahun 2012 Tentang Izin LingkunganBang Ir100% (1)
- Bab 3 Pudr RevisiDokumen10 halamanBab 3 Pudr RevisiValenci MiyakeeBelum ada peringkat
- Lampiran Perda RTRWDokumen50 halamanLampiran Perda RTRWValenci MiyakeeBelum ada peringkat
- B NJHGSV NJCDokumen7 halamanB NJHGSV NJCValenci MiyakeeBelum ada peringkat
- Laporan Akhir Jakstranas Percepatan Pengelolaan SampahDokumen212 halamanLaporan Akhir Jakstranas Percepatan Pengelolaan SampahRia Sarah Sanitya50% (2)
- Lembar PengesahanDokumen2 halamanLembar PengesahanValenci MiyakeeBelum ada peringkat
- 5.4 Kelompok 7Dokumen6 halaman5.4 Kelompok 7Valenci MiyakeeBelum ada peringkat
- ETIKA LINGKUNGAN Kel4Dokumen3 halamanETIKA LINGKUNGAN Kel4Valenci MiyakeeBelum ada peringkat
- Analsisis KesehatanDokumen1 halamanAnalsisis KesehatanValenci MiyakeeBelum ada peringkat
- 4.4 Kelompok 7Dokumen4 halaman4.4 Kelompok 7sonia rahimaBelum ada peringkat
- Pemodelan LingkunganDokumen120 halamanPemodelan LingkunganValenci MiyakeeBelum ada peringkat
- ETIKA LINGKUNGAN Kel4Dokumen3 halamanETIKA LINGKUNGAN Kel4Valenci MiyakeeBelum ada peringkat
- Fasilitas Industri Kesehatan SoniaDokumen3 halamanFasilitas Industri Kesehatan SoniaValenci MiyakeeBelum ada peringkat
- KAIZENDokumen11 halamanKAIZENValenci MiyakeeBelum ada peringkat
- Penulisan Kutipan Dan ReferensiDokumen8 halamanPenulisan Kutipan Dan ReferensiValenci MiyakeeBelum ada peringkat