Angio Genesis
Diunggah oleh
jornescaHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Angio Genesis
Diunggah oleh
jornescaHak Cipta:
Format Tersedia
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Desarrollado por:
Lewis J. Kleinsmith, Ph.D.
Donna Kerrigan, M.S.
Jeanne Kelly
Brian Hollen
Traducido por:
Miguel Monroy
Una descripción ilustrada de la angiogénesis
y su importancia en la investigación del
cáncer.
Estas transparencias de PowerPoint no son archivos asegurados. Usted puede mezclar y combinar
transparencias de clases de tutor diferentes a medida que prepara sus propias presentaciones o
conferencias. En la sección de “Notas” usted encontrará explicaciones de los dibujos.
El arte en esta clase de tutor tiene derecho de propiedad literaria y no puede ser reutilizado para
obtener ganancia comercial.
Por favor, no remueva el logotipo del NCI ni la marca de derecho de propiedad literaria o R
“copyright” de ninguna transparencia.
Estas clases de tutor se pueden copiar solamente si se distribuyen gratis con propósitos educativos.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 1
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
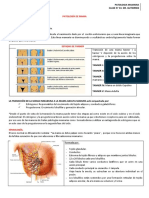
¿Qué son las Metástasis?
1. Las células
Vaso cancerosas invaden a
sanguíneo los tejidos y a los
vasos vecinos
2. Las células
cancerosas son
transportadas por el
sistema circulatorio a
sitios distantes
3. Las células cancerosas
reinvaden y crecen en un
nuevo lugar R
Cuando se diagnostica a los pacientes con cáncer, ellos desean saber si su enfermedad es local o
si se ha diseminado a otros lugares. El cáncer se disemina por metástasis, la habilidad de las
células cancerosas de penetrar dentro de los vasos linfáticos y sanguíneos, circular a través del
torrente sanguíneo y después invadir y crecer en los tejidos normales de otras partes del cuerpo.
En gran medida, es esta habilidad de diseminarse a otros tejidos y órganos lo que hace que el
cáncer sea una enfermedad que potencialmente pone en peligro la vida y es por esto que hay un
gran interés por entender lo que hace posible las metástasis de un tumor canceroso.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 2
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Las Metástasis Requieren la Angiogénesis
Angiogénesis
Los investigadores del cáncer que estudian las condiciones necesarias para que se desarrollen las
metástasis del cáncer han descubierto que uno de los eventos fundamentales requeridos es el
crecimiento de una nueva red de vasos sanguíneos. Este proceso de formación de nuevos vasos
sanguíneos se conoce como angiogénesis.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 3
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
¿Qué es la Angiogénesis Tumoral?
Tumor pequeño Tumor que puede crecer
localizado y diseminarse
Angiogénesis
Vaso sanguíneo
Molécula
señaladora
La angiogénesis tumoral es la proliferación de una red de vasos sanguíneos que penetra dentro de
crecimientos cancerosos, proporcionando nutrientes y oxígeno y removiendo productos de
desecho. La angiogénesis tumoral empieza en realidad cuando las células cancerosas del tumor
liberan moléculas que envían señales al tejido huésped normal vecino. Este señalamiento activa a
ciertos genes en el tejido huésped que, a su vez, producen proteínas para estimular el crecimiento
de nuevos vasos sanguíneos.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 4
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Angiogénesis Normal en los Niños
Además de su papel en los tumores, la angiogénesis ocurre normalmente en el cuerpo humano en
ocasiones específicas en el desarrollo y crecimiento. Por ejemplo, un bebé desarrollándose en la
matriz (útero) de la mamá debe crear la enorme red de arterias, venas y capilares que se
encuentran en el cuerpo humano. Un proceso conocido como vasculogénesis crea la red primaria
de las células vasculares endoteliales que se convertirán en vasos sanguíneos principales. Más
tarde, la angiogénesis remodela esta red y la convierte en los nuevos y pequeños vasos
sanguíneos o capilares que completan el sistema circulatorio del bebé.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 5
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Angiogénesis Normal en Adultos
Angiogénesis en
el revestimiento
uterino
Angiogénesis en el tejido
durante la curación de
una herida
La proliferación de nuevos vasos sanguíneos también se lleva a cabo en adultos, aunque es un
evento relativamente infrecuente. En las mujeres la angiogénesis es activa unos cuantos días
cada mes a medida que nuevos vasos sanguíneos se forman en el revestimiento del útero durante
el ciclo menstrual. También, la angiogénesis es necesaria para la reparación o regeneración de
tejido durante la curación de una herida.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 6
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
La Angiogénesis y las
Células Vasculares Endoteliales
Vaso sanguíneo
Células
vasculares
endoteliales
Las paredes de los vasos sanguíneos están formadas por células vasculares endoteliales. Estas
células raramente se dividen, haciéndolo así solamente alrededor de una vez cada 3 años en
promedio. Sin embargo, cuando la situación así lo requiere, la angiogénesis puede estimularlas
para que se dividan.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 7
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
La Angiogénesis y las Proteínas Reguladoras
Concentración de Inhibidoras de la Angiogénesis
Inhibidoras en Inhibidoras en
concentraciones altas concentraciones bajas
Activadoras en Activadoras en
concentraciones bajas concentraciones altas
Vaso sanguíneo
División celular rara División celular frecuente
R
La angiogénesis es regulada por ambas, moléculas activadoras e inhibidoras. Normalmente, las
inhibidoras predominan, bloqueando el crecimiento. Si surge la necesidad de desarrollar nuevos
vasos sanguíneos, las activadoras de la angiogénesis se incrementan en número y las inhibidoras
disminuyen. Esto provoca el crecimiento y la división de células vasculares endoteliales y,
finalmente, la formación de nuevos vasos sanguíneos.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 8
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
La Angiogénesis y el Cáncer
Teoría Anterior Nueva Teoría
Dilatación del vaso Angiogénesis
Antes de los años 1960s, los investigadores del cáncer creían que el suministro de sangre
alcanzaba a los tumores simplemente debido a que los vasos sanguíneos pre-existentes se
dilataban. Pero experimentos posteriores mostraron que la angiogénesis--el crecimiento de
nuevos vasos sanguíneos--es necesaria para que los tumores cancerosos continúen creciendo y
diseminándose.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 9
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Sin la Angiogénesis,
el Crecimiento del Tumor se Detiene
Se infunde solución
de nutrientes
Órgano aislado
(p.ej., la glándula tiroides)
Las células
cancerosas
inyectadas dejan de
crecer a medida que
la masa llega a un
tamaño de 1 a 2 mm.
de diámetro R
En experimentos anteriores, los investigadores se preguntaron si el crecimiento canceroso
requería a la angiogénesis. Los científicos removieron un tumor canceroso de un animal de
laboratorio e inyectaron algunas de las células cancerosas en un órgano normal removido de la
misma variedad de animal. El órgano entonces se colocó en una cámara de vidrio y una solución
de nutrientes se administró en el órgano para mantenerlo vivo por una semana o dos. Los
científicos encontraron que las células cancerosas se convirtieron en tumores pequeños pero no
pudieron unirse a los vasos sanguíneos del órgano. Como resultado, el crecimiento del tumor se
detuvo en un diámetro de alrededor de 1 ó 2 mm. Sin la angiogénesis, el crecimiento del tumor
se detuvo.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 10
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Con la Angiogénesis,
el Crecimiento del Tumor Procede
Tumor
suspendido
en la cámara
anterior Tumor
creciendo
Tamaño del tumor
en el iris
Tumor
Córnea creciendo
en el iris
Tumor
suspendido
en la cámara
Iris anterior
Cristalino
2 4 6 8 10
Días R
En otro experimento diseñado para encontrar si el crecimiento del cáncer puede continuar
cuando la angiogénesis ocurre, los investigadores compararon la conducta de las células
cancerosas en dos regiones del mismo órgano. Ambos lugares en el ojo tenían nutrientes
disponibles, pero sólo uno pudo mantener la angiogénesis. Los científicos encontraron que la
misma inyección de inicio de células cancerosas creció de 1 a 2 mm. de diámetro y después se
detuvo en la región sin vasos sanguíneos cercanos, pero creció más allá de 2 mm. cuando se
colocó en el área en donde la angiogénesis era posible. Con la angiogénesis, el crecimiento del
tumor continuó.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 11
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
¿Qué Provoca la Angiogénesis?
Cámara
Célula cancerosa Molécula señaladora
Se coloca la cámara debajo de la piel del animal
Angiogénesis
En un experimento diseñado para determinar si las moléculas de las células cancerosas o de los
tejidos huéspedes circundantes son responsables de empezar la angiogénesis, los científicos
implantaron células cancerosas en una cámara rodeada de una membrana con poros demasiado
pequeños para que las células pudieran salir. Bajo estas condiciones, la angiogénesis aún empezó
en la región vecina al implante. Las moléculas activadoras pequeñas producidas por las células
cancerosas deben haberse transferido fuera de la cámara y señalado la angiogénesis en el tejido
vecino.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 12
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Activadores de la Angiogénesis
Una vez que los investigadores supieron que las células cancerosas podían liberar moléculas para
activar el proceso de angiogénesis, el reto se convirtió en encontrar y estudiar a estas moléculas
estimuladoras de la angiogénesis en los tumores de animales y humanos.
De estos estudios, más de una docena de proteínas diferentes, así como también varias moléculas
más pequeñas, han sido identificadas como angiogénicas, lo que significa que ellas son liberadas
por tumores como señales para la angiogénesis. Entre estas moléculas, dos proteínas parecen ser
las más importantes para sustentar el crecimiento de tumor: factor de crecimiento vascular
endotelial (FCVE) (vascular endothelial growth factor o VEGF, en inglés) y factor básico de
crecimiento de fibroblastos (FBCF) (basic fibroblast growth factor o bFGF, en inglés). El factor
FCVE y el factor FBCF son producidos por muchos tipos de células cancerosas y por ciertos
tipos de células normales también.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 13
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
La Cascada Señalizadora de la Angiogénesis
Célula cancerosa
FCVE (o FBCF)
Proteína receptora Superficie
Proteínas celular
de relevo endotelial
Los genes son
activados en el
núcleo celular
Las proteínas estimulan
nuevo crecimiento
celular endotelial R
Los factores de crecimiento FCVE y FBCF son sintetizados primero dentro de las células
tumorales y después secretadas en el tejido vecino. Cuando encuentran a células endoteliales,
ellos se unen a proteínas específicas, conocidas como receptoras, localizadas en la superficie
exterior de las células. La unión de alguno de los dos factores de crecimiento FCVE o FBCF a su
receptor apropiado activa una serie de proteínas de relevo que transmiten una señal dentro del
núcleo de las células endoteliales. La señal nuclear finalmente provoca que un grupo de genes
produzcan los productos necesarios para el nuevo crecimiento celular endotelial.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 14
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Activación Endotelial Celular
Secreta Célula
MPMs que endotelial
digieren la activada
matriz vecina
Matriz
La célula
migra y se
divide
La activación de células endoteliales por los juegos de factores FCVE o FBCF pone en marcha
una serie de pasos hacia la creación de nuevos vasos sanguíneos. Primero, las células
endoteliales activadas producen metaloproteinasas de la matriz o MPMs (matrix
metalloproteinases o MMPs, en inglés), una clase especial de enzimas degradadoras. Estas
enzimas entonces se liberan de las células endoteliales al tejido vecino. Las MPMs degradan la
matriz extracelular--el material de apoyo que llena los espacios entre las células y que está
compuesto de proteínas y polisacáridos. La degradación de esta matriz permite la migración de
las células endoteliales. A medida que ellas migran a los tejidos vecinos, las células endoteliales
activadas empiezan a dividirse. Pronto ellas se organizan en tubos huecos que evolucionan
gradualmente y se convierten en una red madura de vasos sanguíneos.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 15
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Inhibidores de la Angiogénesis
Aunque muchos tumores producen moléculas angiogénicas tales como los factores FCVE y
FBCF, su presencia no es suficiente para iniciar el crecimiento de vasos sanguíneos. Para que la
angiogénesis empiece, estas moléculas activadoras deben superar una variedad de inhibidores de
la angiogénesis que normalmente reprimen el crecimiento de los vasos sanguíneos.
Casi una docena de proteínas que existen naturalmente pueden inhibir la angiogénesis. Entre este
grupo de moléculas, las proteínas conocidas como angiostatina, endostatina y trombospondina
parecen ser especialmente importantes. Un balance finamente armonizado entre las
concentraciones de inhibidores y de activadores de la angiogénesis tales como los factores de
crecimiento FCVE y FBCF determina si un tumor puede inducir el crecimiento de nuevos vasos
sanguíneos. Para activar la angiogénesis, la producción de activadores se debe incrementar a
medida que la producción de inhibidores disminuye.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 16
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Los Inhibidores de la Angiogénesis y los
Tumores Primarios
Tamaño
del tumor
en ratones
0 40 80 120 160 200 240
Días
Iniciar Iniciar
Parar Parar
Tratamiento con Endostatina
R
El descubrimiento de los inhibidores de la angiogénesis plantea la pregunta de si tales moléculas
podrían terapéuticamente detener o contener el crecimiento del cáncer. Los investigadores han
tomado en consideración esta pregunta en numerosos experimentos involucrando a animales. En
un estudio destacado, ratones con varios tipos diferentes de cánceres se trataron con inyecciones
de endostatina. Después de varios ciclos de tratamiento, el tumor inicial (primario) formado en el
sitio de las células cancerosas inyectadas casi desapareció y los animales no desarrollaron
resistencia a los efectos de la endostatina después de su uso repetido.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 17
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Inhibidores de la Angiogénesis y Metástasis
Se inyectan las
células
cancerosas
Se le permite crecer
al tumor inicial por
varias semanas
Se remueve
el tumor inicial
Se da tiempo para que
las metástasis aparezcan
Inyecciones de No se proporciona
angiostatina tratamiento
Una cuantas metástasis Muchas metástasis
R
El descubrimiento de que los inhibidores de la angiogénesis tales como la endostatina pueden
reprimir el crecimiento de los tumores primarios plantea la posibilidad de que dichos inhibidores
probablemente puedan también retardar las metástasis de tumores.
Para probar esta hipótesis, los investigadores inyectaron varios tipos de células cancerosas de
ratón debajo de la piel de varios ratones y permitieron que las células crecieran por alrededor de
dos semanas. Los tumores primarios entonces fueron removidos y los animales se examinaron
durante varias semanas. Los ratones que no recibieron ningún tratamiento adicional desarrollaron
alrededor de 50 tumores visibles que se habían diseminado a los pulmones antes de la remoción
de sus tumores primarios. Sin embargo, los ratones tratados con angiostatina desarrollaron un
promedio de sólo 2 ó 3 tumores en sus pulmones. La inhibición de la angiogénesis por la
angiostatina había reducido la tasa de diseminación (metástasis) en alrededor de 20 veces.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 18
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
La Angiogénesis y el Estado
Tumoral Latente
La angiostatina inhibe
Tumor primario grande
Masas tumorales en estado latente muy pequeñas
Se ha sabido por muchos años que las células cancerosas que se originan en un tumor primario
pueden diseminarse a otro órgano y formar masas tumorales muy pequeñas, microscópicas
(metástasis), que pueden permanecer en estado latente por muchos años. Una probable
explicación de este estado de latencia tumoral es que no ocurrió la angiogénesis, por lo que los
tumores pequeños carecieron de los nuevos vasos sanguíneos necesarios para el crecimiento
continuado.
Una posible razón del estado de latencia tumoral puede ser que algunos tumores primarios
secretan el inhibidor angiostatina dentro del torrente sanguíneo, el cual entonces circula por todo
el cuerpo e inhibe el crecimiento de vasos sanguíneos en otros sitios. Esto podría prevenir que las
metástasis microscópicas crezcan y se desarrollen en tumores visibles.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 19
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Cáncer en Ratones Deficientes en la Angiogénesis
Ratón normal Ratón mutante deficiente en
la angiogénesis
Se inyectan
células
cancerosas del
seno
Cáncer Sin cáncer R
Un apoyo adicional para la idea de que el interferir con el proceso de la angiogénesis puede
reprimir el crecimiento del tumor ha provenido de estudios genéticos con ratones. Los científicos
han creado recientemente variedades de ratones que carecen de dos genes, conocidos como Id1 e
Id3, cuya ausencia dificulta la angiogénesis. Cuando se inyectan células cancerosas del seno de
ratones en dichos ratones mutantes deficientes en la angiogénesis, hay un periodo pequeño de
crecimiento del tumor, pero los tumores regresionan completamente después de unas cuantas
semanas y los ratones permanecen saludables sin señales de cáncer. En contraste, los ratones
normales inyectados con las mismas células cancerosas del seno mueren de cáncer en unas
cuantas semanas.
Cuando se inyectan células cancerosas del pulmón en la misma variedad de ratones mutantes
deficientes en la angiogénesis, los resultados son levemente diferentes. Las células cancerosas
del pulmón sí se desarrollan en tumores en los ratones mutantes, pero los tumores crecen más
lentamente que en los ratones normales y fallan en diseminarse (metastatizarse) a otros órganos.
Como resultado de ello, los ratones mutantes viven mucho más tiempo que los ratones normales
inyectados con los mismos tipos de células cancerosas del pulmón.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 20
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Los Inhibidores de la Angiogénesis en el
Tratamiento del Cáncer Humano
Célula
cancerosa
FCVE (o FBCF)
Proteína
receptora
Célula Inhibidores de la
endotelial angiogénesis
MPMs
Matriz
Los investigadores ahora se están preguntando si el inhibir la angiogénesis puede retardar o
prevenir el crecimiento y la diseminación de las células cancerosas en los seres humanos.
Para contestar esta pregunta, casi dos docenas de inhibidores de la angiogénesis están
actualmente siendo evaluados en los pacientes con cáncer. Estos inhibidores caen dentro de
varias categorías diferentes dependiendo de su mecanismo de acción. Algunos inhiben a las
células endoteliales directamente, mientras que otros inhiben la cascada señalizadora de la
angiogénesis o bloquean la habilidad de las células endoteliales para degradar la matriz
extracelular.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 21
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Farmacos (Medicamentos) Que Inhiben la
Angiogénesis Directamente
Células
cancerosas
Endostatina
FCVE EMD121974
(o FBCF) TNP-470
Escualamina
Proteína
receptora Apoptosis
Célula
endotelial
Combretastatina A4
MPMs Matriz
Molécula del
Integrina fármaco
(medicamento)
La integrina interactúa con los medicamentos para R
destruir las células endoteliales que están proliferando
Una clase de inhibidores de la angiogénesis que están siendo evaluados en los pacientes con
cáncer son las moléculas que directamente inhiben el crecimiento de las células endoteliales.
Incluida en esta categoría está la endostatina, la proteína que está presente naturalmente y que se
sabe que inhibe el crecimiento de tumores en los animales. Otro fármaco (medicamento), la
combretastatina A4, causa que las células endoteliales que están creciendo se suiciden
(apoptosis). Otros fármacos (medicamentos), que interactúan con una molécula conocida como
integrina, también pueden promover la destrucción de células endoteliales que están
proliferando.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 22
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Fármaco (Medicamento) Antiguo Con Un
Nuevo Uso
Célula
cancerosa
FCVE (o FBCF)
Proteína
receptora
Célula
endotelial Talidomida
MPMs
Matriz
Otro fármaco (medicamento) interesante es la talidomida, un sedante utilizado en los años 1950s
que fue subsecuentemente retirado del mercado debido a que causaba defectos de nacimiento
cuando era tomado por mujeres embarazadas. Aunque este fármaco (medicamento) claramente
no sería apropiado para las mujeres embarazadas, su habilidad de prevenir que las células
endoteliales formen nuevos vasos sanguíneos podría hacerlo útil para tratar a pacientes con
cáncer que no están embarazadas.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 23
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Fármacos (Medicamentos) Que Bloquean a
la Cascada Señalizadora de la Angiogénesis
Célula
cancerosa Interferón alfa
FCVE (o FBCF)
Proteína
receptora
Anticuerpo anti-
FCVE
SU5416
SU6668
Célula PTK787/ZK 22584
endotelial
No hay
MPMs crecimiento
de células
Matriz endoteliales
Un segundo grupo de inhibidores de la angiogénesis que se está evaluando en estudios clínicos
en seres humanos son las moléculas que interfieren con los pasos en la cascada señalizadora de la
angiogénesis. Incluidos en esta categoría se encuentran los anticuerpos anti-FCVE que bloquean
al receptor del FCVE y evitan que se una al factor de crecimiento. Otro agente, el interferón alfa,
es una proteína que existe naturalmente y que inhibe la producción de los factores de crecimiento
FBCF y FCVE evitando que estos factores de crecimiento inicien la cascada señalizadora.
También, varios fármacos (medicamentos) sintéticos capaces de interferir con los receptores
celulares endoteliales se están evaluando en los pacientes con cáncer.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 24
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Fármacos (Medicamentos) Que Bloquean
La Degradación de la Matriz Extracelular
Célula
cancerosa
FCVE (o FBCF)
Proteína
receptora Marimistat
AG3340
COL-3
Neovastat
Célula BMS-275291
endotelial
No migración
MPMs celular
endotelial
Matriz
Un tercer grupo de inhibidores de la angiogénesis está dirigido en contra de uno de los productos
iniciales elaborados por las células endoteliales que están creciendo, principalmente las MPMs,
enzimas que catalizan la degradación de la matriz extracelular. Debido a que la degradación de la
matriz es requerida antes de que las células endoteliales puedan migrar a los tejidos vecinos y
proliferar en nuevos vasos sanguíneos, los fármacos (medicamentos) que ponen como blanco a
las MPMs también pueden inhibir la angiogénesis.
Varias moléculas sintéticas y otras moléculas que existen naturalmente que inhiben la actividad
de las MPMs actualmente se están evaluando para ver si el interferir con esta etapa de la
angiogénesis prolongará la supervivencia de los pacientes con cáncer.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 25
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Fármacos (Medicamentos) Con Otros
Mecanismos de Acción
También se está evaluando en pacientes con cáncer un grupo misceláneo de fármacos
(medicamentos), cuya habilidad para inhibir la angiogénesis involucra a mecanismos que, o bien
no son específicos o no son entendidos claramente. Un ejemplo es un fármaco (medicamento)
conocido como CAI, el cual ejerce sus efectos inhibiendo el flujo de los iones de calcio hacia el
interior de las células. Aunque esta inhibición de la absorción de calcio suprime el crecimiento
de células endoteliales, dicho mecanismo general puede afectar muchos otros procesos celulares.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 26
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Hacia los Estudios Clínicos
Los investigadores han contestado muchas preguntas acerca de la angiogénesis, pero muchas
preguntas aún permanecen sin contestar. Los científicos no saben si el utilizar los inhibidores de
la angiogénesis para tratar el cáncer activará efectos secundarios desconocidos, cuánto tiempo
necesitará durar el tratamiento o si las células tumorales encontrarán rutas alternativas para la
vascularización. Para contestar dichas preguntas, estudios clínicos en seres humanos se están
realizando en este momento.
Para obtener una lista actualizada de estudios clínicos actualmente en curso y actualmente
planeados que involucren a los inhibidores de la angiogénesis, incluyendo números de teléfono
para obtener información adicional, refiérase al sitio Web de Estudios Clínicos del Cáncer del
Instituto Nacional del Cáncer (National Cancer Institute CancerTrial™, en inglés), el cual tiene
una sección dedicada a los Inhibidores de la Angiogénesis en los Estudios Clínicos.
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 27
Instituto Nacional del Cáncer
Entendiendo al Cáncer y Temas Relacionados
Entendiendo la Angiogénesis
Nos gustaría escuchar de usted . . .
Si tiene alguna pregunta acerca del contenido de esta clase de tutor, sugerencias
para nuevos temas u otra información de retroalimentación sobre el sitio Web,
por favor, envíe un correo electrónico (e-mail) a kerrigad@mail.nih.gov.
Si tiene alguna pregunta acerca del arte o ilustraciones de esta clase de tutor o si
desea permiso para utilizarlos, por favor, envíe correo electrónico (e-mail) a
beankelly@verizon.net.
R
Sitio Web del NCI: http://cancer.gov/cancertopics/understandingcancer 28
Anda mungkin juga menyukai
- DICCIONARIO BiodescodificacionDokumen751 halamanDICCIONARIO BiodescodificacionPablo Sánchez Pozzi98% (88)
- Los 120 Puntos Más Importantes de La AcupunturaDokumen12 halamanLos 120 Puntos Más Importantes de La Acupunturanogerbo92% (52)
- Las Frecuencias de Royal RifeDokumen75 halamanLas Frecuencias de Royal RifeSimon Peralta100% (4)
- Dispositivo Radionico para Hacer RemediorsDokumen1 halamanDispositivo Radionico para Hacer Remediorsjornesca100% (3)
- Así Fue Universo 25 - El Paraíso Artificial para RatonesDokumen2 halamanAsí Fue Universo 25 - El Paraíso Artificial para Ratonesjornesca67% (3)
- El Toque Cuantico - El Poder de Curar - Richard GordonDokumen216 halamanEl Toque Cuantico - El Poder de Curar - Richard GordonAna María50% (2)
- Manejo Del DermatronDokumen25 halamanManejo Del Dermatronjornesca83% (6)
- Sanmarcos PatologiaDokumen6 halamanSanmarcos Patologiaanon-737622Belum ada peringkat
- Mente, Energía y Máquinas Construcción de Máquina Radiónica Tipo HDRDokumen3 halamanMente, Energía y Máquinas Construcción de Máquina Radiónica Tipo HDRjornesca100% (2)
- Como Pueden Ayudarlo Las Bio FrecuenciasDokumen12 halamanComo Pueden Ayudarlo Las Bio Frecuenciasjornesca100% (1)
- Mente, Energía y Máquinas Construcción de Máquina Radiónica de Tres Diales Con Amplificador y Oscilador VariableDokumen2 halamanMente, Energía y Máquinas Construcción de Máquina Radiónica de Tres Diales Con Amplificador y Oscilador VariablejornescaBelum ada peringkat
- Cancer de BocaDokumen3 halamanCancer de BocagcalitoBelum ada peringkat
- Colores RadiestesiaDokumen4 halamanColores Radiestesiamarco_p2014100% (3)
- Mente, Energía y Máquinas Amplificador de Audio Sencillo para Proyectos RadiónicosDokumen2 halamanMente, Energía y Máquinas Amplificador de Audio Sencillo para Proyectos RadiónicosjornescaBelum ada peringkat
- Ginecología y Obstetricia Coment - WDokumen22 halamanGinecología y Obstetricia Coment - Wjrlol2Belum ada peringkat
- Collareta 2 y 3 ChinaDokumen18 halamanCollareta 2 y 3 ChinajornescaBelum ada peringkat
- Mente, Energía y Máquinas Zapper RegulableDokumen1 halamanMente, Energía y Máquinas Zapper RegulablejornescaBelum ada peringkat
- Back SterDokumen8 halamanBack SterjornescaBelum ada peringkat
- Mente, Energía y Máquinas Zapper SencilloDokumen1 halamanMente, Energía y Máquinas Zapper SencillojornescaBelum ada peringkat
- Elaboración Casera de Algunas HarinasDokumen26 halamanElaboración Casera de Algunas HarinasjornescaBelum ada peringkat
- Conocer Los Condensadores de Seguridad - FidestecDokumen9 halamanConocer Los Condensadores de Seguridad - FidestecjornescaBelum ada peringkat
- Mente, Energía y Máquinas Doctor PapelDokumen42 halamanMente, Energía y Máquinas Doctor Papeljornesca50% (2)
- Taller Aiepi Diagnostico Temprano de Cancer en La NiñezDokumen7 halamanTaller Aiepi Diagnostico Temprano de Cancer en La NiñezlauraBelum ada peringkat
- 4-Imagenologia de Los Tumores RenalesDokumen7 halaman4-Imagenologia de Los Tumores RenalesAileen RicaldeeBelum ada peringkat
- Eq3. Entregable 1 Reto BasesDokumen32 halamanEq3. Entregable 1 Reto BasesDavid PaniaguaBelum ada peringkat
- 11 Cristina PouDokumen29 halaman11 Cristina PouLuis ParisBelum ada peringkat
- Goji - La Baya de La FelicidadDokumen198 halamanGoji - La Baya de La FelicidadJose Mendez MaciasBelum ada peringkat
- CATALOGO MULTIALOE 2019 Especial CompletoDokumen51 halamanCATALOGO MULTIALOE 2019 Especial CompletoCarlos Alberto CortesBelum ada peringkat
- Corrientes de Baja Frecuencia - 20181031083704Dokumen33 halamanCorrientes de Baja Frecuencia - 20181031083704Brayan CZ100% (1)
- Algas Contra La RadiaciónDokumen3 halamanAlgas Contra La RadiaciónJJBelum ada peringkat
- Ejemplo de ChocolateDokumen186 halamanEjemplo de ChocolateRafael Jesus AyanomaBelum ada peringkat
- Prestadores DesaludDokumen135 halamanPrestadores DesaludGabrielaBelum ada peringkat
- Ensayo CelularesDokumen1 halamanEnsayo CelularesLiz AstudilloBelum ada peringkat
- Revista 43 Suplemento TecnicoDokumen27 halamanRevista 43 Suplemento TecnicoKollinz ZfBelum ada peringkat
- Adiss2017 944Dokumen108 halamanAdiss2017 944Limber Galef Tunque ToribioBelum ada peringkat
- El Citoesqueleto en La Glandula MamariaDokumen29 halamanEl Citoesqueleto en La Glandula MamariaLaura Jimena HernandezBelum ada peringkat
- Guia Medica 2014 - FinalDokumen36 halamanGuia Medica 2014 - FinalCesar SanchezBelum ada peringkat
- Cromosoma 3 y 4Dokumen2 halamanCromosoma 3 y 4Laura Criollo FloresBelum ada peringkat
- Cancers-12-02796 en EsDokumen23 halamanCancers-12-02796 en EsCRISTHIAN CASTILLO JIBAJABelum ada peringkat
- Practica Calif Encarg 1Dokumen4 halamanPractica Calif Encarg 1Denis PozoBelum ada peringkat
- Cancer de ProstataDokumen21 halamanCancer de Prostatalisette espidioBelum ada peringkat
- 14.-Patologia MamariaDokumen22 halaman14.-Patologia MamariaMarlon RojasBelum ada peringkat
- Emociones y AdaptaciónDokumen3 halamanEmociones y AdaptaciónLis AcevedoBelum ada peringkat
- Vitamina B17Dokumen3 halamanVitamina B17virissierraBelum ada peringkat
- Ayuda Memoria Cancer CervicouteroinoDokumen3 halamanAyuda Memoria Cancer CervicouteroinoGonza LopezBelum ada peringkat
- Daños Ambientales Que Ocasiono La Segunda Guerra MundialDokumen2 halamanDaños Ambientales Que Ocasiono La Segunda Guerra MundialKristel MedinɑBelum ada peringkat
- 2011Dokumen61 halaman2011Ronaldo LópezBelum ada peringkat
- HALLMARK3Dokumen16 halamanHALLMARK3ROGER JOSEQUIROZ MARTINEZ EstudianteBelum ada peringkat