Anhídridos
Diunggah oleh
Willy Saquic0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
386 tayangan2 halamanLos anhídridos son compuestos formados por un elemento no metálico y oxígeno. Su fórmula general es X2On, donde X es el elemento no metálico. Existen varias nomenclaturas para nombrar los anhídridos, incluyendo la tradicional, de stock y sistemática, cada una con sus propias convenciones para indicar la valencia del elemento no metálico.
Deskripsi Asli:
anhibridos
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniLos anhídridos son compuestos formados por un elemento no metálico y oxígeno. Su fórmula general es X2On, donde X es el elemento no metálico. Existen varias nomenclaturas para nombrar los anhídridos, incluyendo la tradicional, de stock y sistemática, cada una con sus propias convenciones para indicar la valencia del elemento no metálico.
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
386 tayangan2 halamanAnhídridos
Diunggah oleh
Willy SaquicLos anhídridos son compuestos formados por un elemento no metálico y oxígeno. Su fórmula general es X2On, donde X es el elemento no metálico. Existen varias nomenclaturas para nombrar los anhídridos, incluyendo la tradicional, de stock y sistemática, cada una con sus propias convenciones para indicar la valencia del elemento no metálico.
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 2
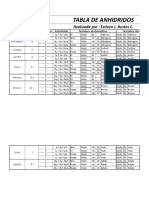
Anhídridos (no metal + oxígeno)
Compartir
Los anhídridos son compuestos formados por un elemento no metálico más
oxígeno. Este grupo de compuestos son también llamados óxidos
ácidos u óxidos no metálicos.
Formulación de los anhídridos (óxidos ácidos o
no metálicos)
Los anhídridos son formulados utilizando el símbolo del elemento no metálico
junto a la valencia del oxígeno más el oxígeno junto a la valencia del
elemento no metálico.
La fórmula de los anhídridos es del tipo X2On (donde X es un elemento no
metálico y O es oxígeno). Entre los numerosos ejemplos de los anhídridos se
encuentran: CO2, SO3, SeO, etc.
Nomenclatura de los anhídridos (óxidos ácidos o
no metálicos)
Nomenclatura tradicional: la nomenclatura tradicional de los anhídridos
se realiza nombrando la palabra anhídrido seguido del elemento no
metálico. Para ello se debe de tener en cuenta la valencia del elemento no
metálico siguiendo los siguientes criterios:
Una valencia: Anhídrido ... ico
o Si+4 + O-2 » Si2O4 » SiO2: anhídrido silícico
Dos valencias:
o Menor valencia: Anhídrido ... oso
C+2 + O-2 » C2O2 » CO: anhídrido carbonoso
o Mayor valencia: Anhídrido ... ico
C+4 + O-2 » C2O4 » CO2: anhídrido carbónico
Tres valencias:
o Menor valencia: Anhídrido hipo ... oso
S+2 + O-2 » S2O2 » SO: anhídrido hiposulfuroso
o Valencia intermedia: Anhídrido ... oso
S+4 + O-2 » S2O4 » SO2: anhídrido sulfuroso
o Mayor valencia: Anhídrido ... ico
S+6 + O-2 » S2O6 » SO3: anhídrido sulfúrico
Cuatro valencias:
o Primera valencia (baja): Anhídrido hipo ... oso
I+1 + O-2 » I2O: anhídrido hipoyodoso
o Segunda valencia: Anhídrido ... oso
I+3 + O-2 » I2O3: anhídrido yodoso
o Tercera valencia: Anhídrido ... ico
I+5 + O-2 » I2O5: anhídrido yódico
o Cuarta valencia (alta): Anhídrido per ... ico
I+7 + O-2 » I2O7: anhídrido peryódico
Nomenclatura de stock: la nomenclatura de stock consiste en escribir la
palabra "óxido" + elemento no metálico y a continuación el número de
valencia del elemento no metálico en números romanos y entre paréntesis.
Ejemplos:
CO2: óxido de carbono (IV)
Br2O3: óxido de bromo (III)
Nomenclatura sistemática: la nomenclatura sistemática consiste en la
utilización de un prefijo que depende del número de átomos de cada
elemento seguido de la expresión "óxido" + el elemento no metálico
precedido de la valencia del elemento no metálico.
Los prefijos utilizados dependiendo del número de átomos en esta
nomenclatura son:
1 átomo: Mono
2 átomos: Di
3 átomos: Tri
4 átomos: Tetra
5 átomos: Penta
6 átomos: Hexa
7 átomos: Hepta
...
Ejemplos:
P2O5: pentaóxido de difósforo
Cl2O: monóxido de dicloro
Anda mungkin juga menyukai
- Nomenclatura de OxidosDokumen3 halamanNomenclatura de OxidosJorge GonzalezBelum ada peringkat
- Nomenclatura y Notación Química 10-11Dokumen10 halamanNomenclatura y Notación Química 10-11AndersonRoseroBelum ada peringkat
- Tarea de Anhidridos Pry 3Dokumen14 halamanTarea de Anhidridos Pry 3Mateo M TeofiloBelum ada peringkat
- Formulacion Inorganica 29412Dokumen17 halamanFormulacion Inorganica 29412AlexGallegoCubillosBelum ada peringkat
- 65.sales HaloideasDokumen2 halaman65.sales HaloideasmarianoquiBelum ada peringkat
- Oxidos No MetalicosDokumen1 halamanOxidos No MetalicoslinetteBelum ada peringkat
- Acidos OxácidosDokumen9 halamanAcidos OxácidosRicardo VillavicencioBelum ada peringkat
- Tabla de Valencias No Metales y MetalsDokumen1 halamanTabla de Valencias No Metales y MetalsEdison CepedaBelum ada peringkat
- E3ro Notación de Los Óxidos BásicosDokumen13 halamanE3ro Notación de Los Óxidos Básicosrufino sarmiento100% (1)
- HIDROXIDOS (Quimica Inorganica Principios)Dokumen11 halamanHIDROXIDOS (Quimica Inorganica Principios)Kevin Rojas CalizayaBelum ada peringkat
- Presidete Adolfo BalliviánDokumen5 halamanPresidete Adolfo BalliviánRubén VillarroelBelum ada peringkat
- TIOACIDOSDokumen4 halamanTIOACIDOScesarBelum ada peringkat
- Radical EsDokumen1 halamanRadical EsSkynetBelum ada peringkat
- Sustancias Simples y CompuestasDokumen3 halamanSustancias Simples y CompuestasPablo Mamani TarquiBelum ada peringkat
- ObraDokumen3 halamanObraGM Kru Alvaro OvandoBelum ada peringkat
- Anhídridos TemaDokumen6 halamanAnhídridos TemaMonzerrat Arroyo VelásquezBelum ada peringkat
- Informe Sobre Medidor de PH Casero-1Dokumen20 halamanInforme Sobre Medidor de PH Casero-1Kaneki CoilloBelum ada peringkat
- 027 - Nuevas Normas Ortográficas de La RaeDokumen35 halaman027 - Nuevas Normas Ortográficas de La Raetrm915572Belum ada peringkat
- Ejercicios de Nomenclatura Oxisales Neutras.: #Fórmula Sistemática Stock TradicionalDokumen2 halamanEjercicios de Nomenclatura Oxisales Neutras.: #Fórmula Sistemática Stock TradicionalGraciela Vinogradoff100% (1)
- Ejercicios Sobre Peroxidos y SuperoxidosDokumen1 halamanEjercicios Sobre Peroxidos y SuperoxidosSofia González MüllerBelum ada peringkat
- S5 HT Función Hidruro y Ácidos TeoríaDokumen6 halamanS5 HT Función Hidruro y Ácidos TeoríaKelion Tadeo SantosBelum ada peringkat
- Alejo CarpentierDokumen2 halamanAlejo CarpentierViviana Cruz SotoBelum ada peringkat
- Taller Óxidos y BasesDokumen4 halamanTaller Óxidos y BasesMariana VargasBelum ada peringkat
- TABLA Valencia CorregidoDokumen1 halamanTABLA Valencia CorregidoRoberto Marin RuizBelum ada peringkat
- Cultura LambayequeDokumen4 halamanCultura LambayequeMilagros MilyBelum ada peringkat
- Taller de Nomenclatura 2021-QG1Dokumen7 halamanTaller de Nomenclatura 2021-QG1jeanet ramosBelum ada peringkat
- SalesDokumen4 halamanSalesLuis R Ticona100% (1)
- NomenclaturaDokumen3 halamanNomenclaturalaura hernandezBelum ada peringkat
- HidruroDokumen7 halamanHidruroMaikel CanalesBelum ada peringkat
- Taller de NomenclaturaDokumen3 halamanTaller de NomenclaturaPaula Restrepo100% (1)
- Tabla Acidos y Sus AnionesDokumen3 halamanTabla Acidos y Sus Anionesjuan manuel bernal tarazona100% (1)
- Practica de QuimicaDokumen2 halamanPractica de QuimicaMiriam MendozaBelum ada peringkat
- Tabla de Numeros de OxidacionDokumen1 halamanTabla de Numeros de OxidacionAlfredo Sánchez100% (1)
- 14 AnhidridosDokumen1 halaman14 AnhidridosHS1-Ximena Orea Gomez IbarraBelum ada peringkat
- Tablas de ValenciasDokumen2 halamanTablas de ValenciasPaco67% (3)
- FormulacionDokumen4 halamanFormulacionKikalucasBelum ada peringkat
- OXIDOSDokumen8 halamanOXIDOSEstiven BustosBelum ada peringkat
- Funciones OxigenadasDokumen3 halamanFunciones OxigenadasMichell LazaroBelum ada peringkat
- Ácidos OxácidosDokumen3 halamanÁcidos OxácidosPill Salas0% (1)
- AnalogiasDokumen17 halamanAnalogiasWilson Patiño RoqueBelum ada peringkat
- Sales OxisalesDokumen3 halamanSales OxisalesMilagros Rodríguez100% (1)
- Hidroxidos-Quimica 10°Dokumen1 halamanHidroxidos-Quimica 10°Valentina Lee Perneth100% (2)
- La EtopeyaDokumen12 halamanLa EtopeyaGabriela Correa Peña0% (1)
- Sales OxisalesDokumen3 halamanSales OxisalesAri Arandi RodríguezBelum ada peringkat
- Laboratorios BagoDokumen10 halamanLaboratorios BagoMariela Ivonne VelardeBelum ada peringkat
- SERIES VERBALES. CAMPO SEMÁNTICO - Tarea de Razonamiento VervalDokumen9 halamanSERIES VERBALES. CAMPO SEMÁNTICO - Tarea de Razonamiento VervalEnso MaldonadoBelum ada peringkat
- Don DimasDokumen2 halamanDon DimasValeria Vasquez RiveroBelum ada peringkat
- Sopaybingo LOSHUESOSDokumen1 halamanSopaybingo LOSHUESOSMagdalena Andrea Vasquez Lepe100% (1)
- Compuestos Inorgánicos en La Vida Cotidiana. CarolinaDokumen11 halamanCompuestos Inorgánicos en La Vida Cotidiana. CarolinaDiana86% (7)
- Los Ácidos Oxácidos U Oxoácidos Son Compuestos Ternarios Formados Por Un Óxido No Metálico y Una Molécula de AguaDokumen8 halamanLos Ácidos Oxácidos U Oxoácidos Son Compuestos Ternarios Formados Por Un Óxido No Metálico y Una Molécula de AguaTeban Quispe Garcia50% (2)
- Texto ArgumentativoDokumen9 halamanTexto ArgumentativoAura Medina100% (1)
- Quimica EspecialDokumen36 halamanQuimica EspecialBeat CarBelum ada peringkat
- Elaboración de Bobina de TeslaDokumen6 halamanElaboración de Bobina de TeslaJose Luis BallesterosBelum ada peringkat
- Tabla de Matales y No MetalesDokumen2 halamanTabla de Matales y No MetalesBryanyMaria100% (1)
- Prefijos LatinosDokumen3 halamanPrefijos LatinosbegogilrBelum ada peringkat
- Cuadro de Simbolos y Valencias de Los Principales Elementos QuimicosDokumen1 halamanCuadro de Simbolos y Valencias de Los Principales Elementos QuimicosSantiago Daniel Murillo Espinosa0% (1)
- AnhídridosDokumen5 halamanAnhídridosnorbertoBelum ada peringkat
- 6nomenclatura Química.Dokumen18 halaman6nomenclatura Química.Hugo AlexanderBelum ada peringkat
- Formulación QUIMICADokumen2 halamanFormulación QUIMICABeat CarBelum ada peringkat
- AnhídridosDokumen3 halamanAnhídridosarmando yarupayta de la cruzBelum ada peringkat
- Informe de Aminoacidos y ProteinasDokumen19 halamanInforme de Aminoacidos y ProteinasMacyory GutierrezBelum ada peringkat
- Obturaciones de Composite ESQUEMADokumen42 halamanObturaciones de Composite ESQUEMAYasmine BenazzouzBelum ada peringkat
- Diagrama de FlujoDokumen5 halamanDiagrama de FlujoJose galindez cruzBelum ada peringkat
- Practica de RedoxDokumen3 halamanPractica de RedoxLuca RiosBelum ada peringkat
- Informe Lab6 Zeballos BrayanDokumen7 halamanInforme Lab6 Zeballos BrayanArmando Brayan Zeballos RiosBelum ada peringkat
- Acidificacion Areniscas CarbonatosDokumen50 halamanAcidificacion Areniscas CarbonatosAlex Sanca Ponce100% (1)
- Informe de Práctica 8Dokumen12 halamanInforme de Práctica 8kristelita2811Belum ada peringkat
- Reporte de Análisis y Tendencias: #Lab Normal Precaución Alerta Toma de Muestra Equipo Horas/Kms Lubricante Horas/KmsDokumen2 halamanReporte de Análisis y Tendencias: #Lab Normal Precaución Alerta Toma de Muestra Equipo Horas/Kms Lubricante Horas/KmswilmerBelum ada peringkat
- 21 0 6ta Participación - NiqueladoDokumen10 halaman21 0 6ta Participación - NiqueladoJhon WilliamsBelum ada peringkat
- Practica 1 - Acetilación de Anilina - CatherineCaná1065419Dokumen9 halamanPractica 1 - Acetilación de Anilina - CatherineCaná1065419CatherineBelum ada peringkat
- Determinación de La Dureza Del AguaDokumen9 halamanDeterminación de La Dureza Del AguaRJosueBoadaBelum ada peringkat
- ActividadesderepasoquimicaDokumen9 halamanActividadesderepasoquimicaAnonymous GruLUfBelum ada peringkat
- Taller Segunda Semana 11 NomenclaturaDokumen6 halamanTaller Segunda Semana 11 NomenclaturaDilan ManriqueBelum ada peringkat
- GUIA 2019-LaboratorioDokumen62 halamanGUIA 2019-LaboratorioAndrea PilataxiBelum ada peringkat
- 2-Cuestionario de Quimica AmbientalDokumen11 halaman2-Cuestionario de Quimica AmbientalVictor LanderoBelum ada peringkat
- Metabolismo CelularDokumen11 halamanMetabolismo CelularLudem Villca BonifacioBelum ada peringkat
- Práctica 9. Preparación y Valoración de SolucionesDokumen2 halamanPráctica 9. Preparación y Valoración de SolucionesTania Sofia Torres RomeroBelum ada peringkat
- Laboratorio 1 ElementosDokumen3 halamanLaboratorio 1 ElementosAnonymous eFepy8O8SYBelum ada peringkat
- Sintesis de Acido CinamicoDokumen4 halamanSintesis de Acido CinamicoSHARON OSSA CABALLEROBelum ada peringkat
- AMINASDokumen6 halamanAMINASGuadalupe GarciaBelum ada peringkat
- 3.8.1.2 AlquinosDokumen4 halaman3.8.1.2 AlquinosjlgzBelum ada peringkat
- Lípidos Clasificación y FuncionesDokumen78 halamanLípidos Clasificación y FuncionesHeidi Maggalí GarleppBelum ada peringkat
- Taller NomenclaturaDokumen2 halamanTaller NomenclaturaLuis Guillermo Torres EllesBelum ada peringkat
- 9 Nutrición Microbiana y Medios de CultivoDokumen34 halaman9 Nutrición Microbiana y Medios de CultivoCarla VillaverdeBelum ada peringkat
- DiagenesisDokumen8 halamanDiagenesisSANDRA ELIZABETH CANCINO PÉREZBelum ada peringkat
- Tarea Cerro VerdeDokumen24 halamanTarea Cerro VerdeFrank YauriBelum ada peringkat
- Guía de Estudio para El Primer Parcial de Química IDokumen6 halamanGuía de Estudio para El Primer Parcial de Química Iaxeladriel gtzhdzBelum ada peringkat
- Problemas de Calorimetria-TermoquimicaDokumen3 halamanProblemas de Calorimetria-TermoquimicaKaren RivasplataBelum ada peringkat
- BoratosDokumen13 halamanBoratosNathalyy Nicole Serricueta MondacaBelum ada peringkat
- Laboratorio Aldehídos y CetonasDokumen2 halamanLaboratorio Aldehídos y CetonasandresBelum ada peringkat