Gases
Diunggah oleh
paolagoHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Gases
Diunggah oleh
paolagoHak Cipta:
Format Tersedia
GASES
INTRODUCCIN El estado gaseoso es un estado disperso de la materia, es decir , que las molculas del gas estn separadas unas de otras por distancias mucho mayores del tamao del dimetro real de las molculas. Resuelta entonces, que el volumen ocupado por el gas ( V) depende de la presin (P), la temperatura (T) y de la cantidad o numero de moles
( n).
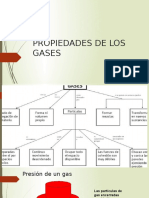
PROPIEDADES DE LOS GASES Las propiedades de la materia en estado gaseoso son :
1. Se adaptan a la forma y el volumen del recipiente que los contiene.
Un gas, al cambiar de recipiente, se expande o se comprime, de manera que ocupa todo el volumen y toma la forma de su nuevo recipiente.
2. Se dejan comprimir fcilmente. Al existir espacios intermoleculares,
las molculas se pueden acercar unas a otras reduciendo su volumen, cuando aplicamos una presin.
3. Se difunden fcilmente. Al no existir fuerza de atraccin
intermolecular entre sus partculas, los gases se esparcen en forma espontnea.
4. Se dilatan, la energa cintica promedio de sus molculas es
directamente proporcional a la temperatura aplicada.
VARIABLES QUE AFECTAN EL COMPORTAMIENTO DE LOS GASES
1. PRESIN :
Es la fuerza ejercida por unidad de rea. En los gases esta fuerza acta en forma uniforme sobre todas las partes del recipiente.
Pasc al
(fuerza perpendicul Presin ar a la superficie)
(rea donde se = N/m2 distribu ye la fuerza )
F
( dinas )
A
( cm2 ) = dinas / cm2
Presin
Otras unidades usadas para la presin : gramos fuerza / cm2, libras / pulgadas2. La presin atmosfrica es la fuerza ejercida por la atmsfera sobre los cuerpos que estn en la superficie terrestre. Se origina del peso del aire que la forma. Mientras ms alto se halle un cuerpo menos aire hay por encima de l, por consiguiente la presin sobre l ser menor.
Presin atmosfrica =
2. TEMPERATURA
76 cm Hg
1 760 = atmsfer = mm Hg a.
Es una medida de la intensidad del calor, y el calor a su vez es una forma de energa que podemos medir en unidades de caloras. Cuando un cuerpo caliente se coloca en contacto con uno fro, el calor fluye del cuerpo caliente al cuerpo fro. La temperatura de un gas es proporcional a la energa cintica media de las molculas del gas. A mayor energa cintica mayor temperatura y viceversa. La temperatura de los gases se expresa en grados kelvin. K= C +
273 3. CANTIDAD La cantidad de un gas se puede medir en unidades de masa, usualmente en gramos. De acuerdo con el sistema de unidades SI, la cantidad tambin se expresa mediante el numero de moles de sustancia, esta puede calcularse dividiendo el peso del gas por su peso molecular. 4. VOLUMEN Es el espacio ocupado por un cuerpo. Unidades de volumen:
m3
1000 = litros litro
1000 centmetros cbicos (c.c) 1c.c
1 mililitro
En una gas ideal ( es decir, el gas cuyo comportamiento queda descrito exactamente mediante las leyes que plantearemos mas adelante), el producto PV dividido por nT es una constante, la constante universal de los gases, R . EL valor de R depende de las unidades utilizadas para P, V, n y T. A presiones suficientemente bajas y a temperaturas suficientemente altas se ha demostrado que todos los gases obedecen las leyes de Boyle, Charles y Gay-Lussac, las cuales relacionan el volumen de un gas con la presin y la temperatura. 5. DENSIDAD Es la relacin que se establece entre el peso molecular en gramos de un gas y su volumen molar en litros. Se da en gr/L.
LEYES DE LOS GASES
EXPRESI N MATEM TICA
LEYE S
POSTU LADO
EJEMPLO
REPRESENTACIN GRAFICA
* Se tiene un
Ley de Boyle Mario tte
A temper atura consta nte, el volum en de cualqui er gas, es invers ament e propor cional a la presi na que se somet e.
volumen de 400 cm3 de oxgeno a una presin de 380 mm de Hg. Qu volumen ocupar a una presin de 760 mm de Hg, si la temperatura permanece constante ? Segn la expresin matemtica: 38 76 0 400 0 m x cm3 =m x V1 m m Hg Hg Despejando V1 :
Ley de Charl es :
A presi n consta nte, el volum en de una masa dada de gas varia directa mente con la temper atura absolu ta
* Se tiene 3
moles de un gas ideal en un recipiente de 700 cm3 a 12C y calentamos el gas hasta 27C. Cul ser el nuevo volumen del gas ? Volumen inicial = 700 cm3 Temperatura inicial = 12 + 273 = 285 K Temperatura final = 27 + 273 = 300 K De acuerdo con la Ley de Charles, al aumentar la temperatura del gas debe aumentar el volumen: Segn la expresin matemtica: 70 0 285 V 300 x = x cm K 2 K
3
Despejando V2
* Se calienta
Ley de gayLussa c
A volum en consta nte , la presi n de un gas es directa mente propor cional a la temper atura
aire en un cilindro de acero de 20 C a 42C. Si la presin inicial es de 4.0 atmsferas Cual es su presin final? Condiciones iniciales: T1 = 273 + 20 = 293 K; P1= 40 atm Condiciones finales: T2 = 273 + 42 = 315K ;P2=? Sustituyendo en la ecuacin de GayLussac:
Ley combi nada de los gases
A partir de la ley combi nada podem os calcula r la forma como cambi a el volum en o presi no temper atura si se conoce n las condici ones iniciale s (Pi,Vi,Ti ) y se conoce n dos de las condici ones finales (es decir, dos de las tres cantid ades Pt, Vt, Tf)
* Qu volumen ocupar
una masa de gas a 150C y 200 mm Hg, sabiendo que a 50C y 1 atmsfera ocupa un volumen de 6 litros ? Condiciones iniciales: V1 = 6 litros P1 = 760 mm Hg T1 = 50 = 273 = 323 K Condiciones finales; V2 = ? P2 = 200 mm Hg T2 = 150 + 273 = 423 K
Remplazando:
P(total) =P1 + P2 + P3...
* Dos recipientes de un
ley de Dalto n
En una mezcla de gases, la presi n total es igual a la suma de las presio nes parcial es
litro se conectan por medio de una vlvula cerrada. Un recipiente contiene nitrgeno a una presin de 400 mm Hg y el segundo contiene oxgeno a una presin de 800 mm Hg. Ambos gases estn a la misma temperatura. Qu sucede cuando se habr la vlvula ? Suponiendo que no hay cambio de la temperatura del sistema cuando los gases se difunden y se mezclan uno con otro y que los gases no reaccionan, entonces la presin final total ser igual a la suma de las presiones parciales de los dos gases : P total = P [N2] + P [O2] P total = 400 mm Hg + 800 mm Hg P total = 1200 mm Hg
Hipt esis de Avoga dro
Volm enes iguales de cualqui er gas en las misma s condici ones de temper atura y presi
V (C.N)
6.02 x 10 23 molculas
V 22.4 L =
Vn
n, contie nen el mismo numer o de molc ulas Las velocid ades de difusi n de dos gases a la misma temper atura son invers ament e propor cional a raz cuadra da de sus densid ades
Leyes de Grah am
El peso molecular es proporcional a la densidad
ECUACIN DE ESTADO:
Si se combinan adecuadamente las leyes de Boyle y Charles con el principio de Avogadro, se llega a una expresin que relaciona simultneamente el volumen de determinada cantidad de un gas con la presin y la temperatura del mismo. Esta ecuacin recibe el nombre de ecuacin de estado o ley de los gases ideales :
PV = nRT
R se conoce como la constante universal de los gases ideales y su valor
depende de las unidades en que se expresen las diversas cantidades. Por convencin, el volumen de un gas se expresa en litros, el valor de n en moles, la temperatura en K y la presin en atmsferas. El valor de la constante R, para una mol de cualquier gas a condiciones normales se determina a partir de la ecuacin anterior as :
EJEMPLO: Calcular la presin ejercida por 0,35 moles de cloro, que se encuentran en un recipiente de 1,5 litros medidos a 27C.
TEORA CINTICA MOLECULAR
La teora cintica de los gases se enuncia en los siguientes postulados, teniendo en cuenta un gas ideal o perfecto:
1. Las sustancias estn constituidas por molculas pequesimas
ubicadas a gran distancia entre si; su volumen se considera despreciable en comparacin con los espacios vacos que hay entre ellas.
2. Las molculas de un gas son totalmente independientes unas de
otras, de modo que no existe atraccin intermolecular alguna.
3. Las molculas de un gas se encuentran en movimiento continuo, en
forma desordenada; chocan entre si y contra las paredes del recipiente, de modo que dan lugar a la presin del gas.
4. Los choques de las molculas son elsticas , no hay perdida ni
ganancia de energa cintica, aunque puede existir transferencia de energa entre las molculas que chocan.
5. La energa cintica media de las molculas , es directamente
proporcional a la temperatura absoluta del gas; se considera nula en el cero absoluto. Los gases reales existen, tienen volumen y fuerzas de atraccin entre sus molculas. Adems, pueden tener comportamiento de gases ideales en determinadas condiciones : temperatura altas y presiones muy bajas
LICUACIN DE GASES
Es el proceso mediante el cual un gas cambia su estado al de lquido. Los gases se pueden licuar por la aplicacin de suficiente enfriamiento y compresin. TEMPERATURA CRITICA: Es la mxima temperatura a la cual es posible licuar un gas sometido a cualquier cantidad de presin. PRESIN CRITICA: Es la presin requerida para licuar un gas estando en su temperatura crtica. VOLUMEN CRITICO: Es el volumen ocupado por una mol de gas estando en la temperatura y presin crticas.
REACCIONES CON INTERVENCIN DE GASES. ESTEQUIOMETRA
Una vez que se tiene la ecuacin qumica balanceada, se sabe directamente por medio de los coeficientes el nmero relativo de moles de cada sustancia que interviene en la reaccin. Si uno o varios de los reactivos o productos son gaseosos, entonces se puede hablar tambin de los volmenes de los reactivos o productos a travs de la ecuacin de estado.
El principio de Avogadro indica que los moles de todos los gases tienen el mismo volumen bajo las mismas condiciones de temperatura y presin. Por tanto, las relaciones molares en una ecuacin son tambin relaciones de volmenes de los gases. Por ejemplo:
H2(g)
1 molcula 1 mol 1 volumen 1 litro 1cm3 22.4 litros
Cl2(g)
1 molcula 1 mol 1 volumen 1 litro 1cm3 22.4 litros
2HCl(g)
2 molcula 2 mol 2 volumen 2 litro 2cm3 2 x 22.4 litros = 44.8 litros
DENSIDAD Y PESO MOLECULAR DE LOS GASES
La densidad de un gas est dada por la relacin de su masa, g, a su volumen:
Pero el volumen de un gas depende de su temperatura y presin. Utilizando la ley de los gases ideales.
(1)
Por tanto, en condiciones normales la densidad de un gas es directamente proporcional a su peso molecular M. En consecuencia, si conocemos la densidad de un gas a una determinada presin y temperatura, podemos calcular su peso molecular. la siguiente ecuacin permite obtener pesos moleculares por comparacin de las densidades de dos gases medidos a la misma temperatura y presin. Si d1 se refiere al gas 1 y d2 al gas 2, se tiene que;
Dividiendo entre s las dos ecuaciones ( P, T y R se cancelan);
Se puede emplear la ecuacin (1) para obtener la densidad de un gas a cualquier temperatura y presin, si conocemos su densidad a una determinada temperatura y presin. Sea d1, la densidad medida para un gas a T1 y P1 y d2 la densidad a diferentes T2 y P2. se pueden escribir las ecuaciones;
M es el mismo, ya que el gas ideal es el mismo. Dividiendo estas dos cantidades:
Esta ecuacin da el cambio en la densidad de un gas con la temperatura y presin.
SOLUCIONES INTRODUCCIN Una solucin es una mezcla homognea de dos o mas sustancias. La sustancia disuelta se denomina soluto y esta presente generalmente en pequea cantidad en pequea cantidad en comparacin con la sustancia donde se disuelve denominada solvente. en cualquier discusin de soluciones, el primer requisito consiste en poder especificar sus composiciones, esto es, las cantidades relativas de los diversos componentes. La concentracin de una solucin expresa la relacin de la cantidad de soluto a la cantidad de solvente. Las soluciones poseen una serie de propiedades que las caracterizan :
1. 2.
Su composicin qumica es variable. Las propiedades qumicas de los componentes de una solucin no se alteran. Las propiedades fsicas de la solucin son diferentes a las del solvente puro : la adicin de un soluto a un solvente aumenta su punto de ebullicin y disminuye su punto de congelacin; la adicin de un soluto a un solvente disminuye la presin de vapor de ste.
3.
PRINCIPALES CLASES DE SOLUCIONES
SOLUCI DISOLVE SOLUT EJEMPL N NTE O OS
Gaseosa Liquida Liquida Liquida
Gas Liquido Liquido Liquido
Gas Liquido Gas Slido
Aire Alcohol en agua O2 en H2O NaCl en H 2O
SOLUBILIDAD
La solubilidad es la cantidad mxima de un soluto que puede disolverse en una cantidad dada de solvente a una determinada temperatura. Factores que afectan la solubilidad: Los factores que afectan la solubilidad son:
a) Superficie de contacto: La interaccin soluto-solvente aumenta cuando
hay mayor superficie de contacto y el cuerpo se disuelve con ms rapidez ( pulverizando el soluto).
b) Agitacin: Al agitar la solucin se van separando las capas de
disolucin que se forman del soluto y nuevas molculas del solvente continan la disolucin
c) Temperatura: Al aument6ar la temperatura se favorece el movimiento
de las molculas y hace que la energa de las partculas del slido sea alta y puedan abandonar su superficie disolvindose.
d) Presin: Esta influye en la solubilidad de gases y es directamente
proporcional
MODO DE EXPRESAR LAS CONCENTRACIONES
La concentracin de las soluciones es la cantidad de soluto contenido en una cantidad determinada de solvente o solucin. Los trminos diluida o concentrada expresan concentraciones relativas. Para expresar con exactitud la concentracin de las soluciones se usan sistemas como los siguientes:
a) Porcentaje peso a peso (% P/P): indica el peso de soluto por cada
100 unidades de peso de la solucin.
b) Porcentaje volumen a volumen (% V/V): se refiere al volumen
de soluto por cada 100 unidades de volumen de la solucin.
c) Porcentaje peso a volumen (% P/V): indica el nmero de gramos
de soluto que hay en cada 100 ml de solucin.
d) Fraccin molar (Xi): se define como la relacin entre las moles de
un componente y las moles totales presentes en la solucin.
Xsto + Xste = 1
e) Molaridad ( M ): Es el nmero de moles de soluto contenido en un
litro de solucin. Una solucin 3 molar ( 3 M ) es aquella que contiene tres moles de soluto por litro de solucin.
EJEMPLO:
* Cuntos gramos de AgNO3 , se necesitan para preparar 100 cm3 de
solucin 1M? Previamente sabemos que:
El peso molecular de AgNO3 es: 100 de H20 cm3 170 g =masa de 1 mol AgNO3
y qu e
equival a 100 ml. H20 en
Usando la definicin de molalidad , se tiene que en una solucin 1M hay 1 mol de AgNO3 por cada Litro (1000 ml ) de H2O (solvente) es decir:
Utilizando este factor de conversin y los datos anteriores tenemos que:
Se necesitan 17 g de AgNO3 para preparar una solucin 1 M
f) Molalidad (m): Es el nmero de moles de soluto contenidos en un
kilogramo de solvente. Una solucin formada por 36.5 g de cido clorhdrico, HCl , y 1000 g de agua es una solucin 1 molal (1 m)
EJEMPLO:
* Cuntos gramos de AgNO3 , se necesitan para preparar 100 cm3 de
solucin 1m?
Previamente sabemos que:
El peso molecular de AgNO3 es: 100 de H20 cm3 170 g =masa de 1 mol AgNO3
y qu e
equival a 100 gr. H20 en
Usando la definicin de molalidad , se tiene que en una solucin 1m hay 1 mol de AgNO3 por cada kg (1000 g ) de H2O (solvente) es decir:
Utilizando este factor de conversin y los datos anteriores tenemos que:
Se necesitan 17 g de AgNO3 para preparar una solucin 1 m, observe que debido a que la densidad del agua es 1.0 g/ml la molaridad y la molalidad del AgNO3 es la misma
g) Normalidad (N): Es el nmero de equivalentes gramo de soluto
contenidos en un litro de solucin.
EJEMPLO:
* Cuntos gramos de AgNO3 , se necesitan para preparar 100 cm3 de
solucin 1N? Previamente sabemos que:
El peso molecular 170 g =masa de 1
de AgNO3 es: 100 de H20 cm3
mol AgNO3 equival a 100 gr. H20 en
qu e
Usando la definicin de molalidad , se tiene que en una solucin 1N hay 1 mol de AgNO3 por cada kg (1000 g ) de H2O (solvente) es decir: Utilizando este factor de conversin y los datos anteriores tenemos que:
El peso equivalente de un compuesto se calcula dividiendo el peso molecular del compuesto por su carga total positiva o negativa.
h) Formalidad (F): Es el cociente entre el nmero de pesos frmula
gramo (pfg) de soluto que hay por cada litro de solucin. Peso frmula gramo es sinnimo de peso molecular. La molaridad (M) y la formalidad (F) de una solucin son numricamente iguales, pero la unidad formalidad suele preferirse cuando el soluto no tiene un peso molecular definido, ejemplo: en los slidos inicos.
SOLUCIONES DE ELECTROLITOS
Electrolitos: Son sustancias que confieren a una solucin la capacidad de conducir la corriente elctrica. Las sustancias buenas conductoras de la electricidad se llaman electrolitos fuertes y las que conducen la electricidad en mnima cantidad son electrolitos dbiles. Electrolisis:
Son las transformaciones qumicas que producen la corriente elctrica a su paso por las soluciones de electrolitos. Al pasar la corriente elctrica, las sales, los cidos y las bases se ionizan. EJEMPLOS:
NaCl CaSO4 HCl AgNO
3
Na+ Ca+2 H+ Ag+ Na+
+ + + + +
ClSO4-2 ClNO3OH-
NaOH
Los iones positivos van al polo negativo o ctodo y los negativos al polo positivo o nodo.
PRODUCTO INICO DEL H2O
El H2O es un electrolito dbil. Se disocia as:
H2O
H+
OH-
La constante de equilibrio para la disociacin del H2O es :
El smbolo [ ] indica la concentracin molar
Keq [H2O]
[H + ]
[OH-].
La concentracin del agua sin disociar es elevada y se puede considerar constante.
Valor del producto inico del H2O( 10-14 moles/litro).
En el agua pura el nmero de iones H+ y OH- es igual. Experimentalmente se ha demostrado que un litro de agua contiene una diez millonsima del numero H+ e igual de OH-; esto se expresa como 107 por tanto, la concentracin molar de H+ se expresa asi [H + ]= 10-7 moles/litro y [OH-] = 10-7; entonces; [H2O] = 10-7 moles / litro [H2O] = 10-14 moles/litro. Si se conoce la concentracin de uno de los iones del H2O se puede calcular la del otro. EJEMPLO:
Si se agrega un cido al agua hasta que la concentracin del H+ sea de 1 x 104 moles / litro, podemos determinar la concentracin de los iones OH-; la presencia del cido no modifica el producto inico de H2O: [H2O]
[H + [OH-] ] =
10-14 de donde
Si se aade una base (NaOH) al H2O hasta que la concentracin de iones OH- sea 0.00001 moles/ litro ( 1 X 10-5); se puede calcular la concentracin de iones H+. [H2O] [H + ]10-5
= =
[H + [OH-] ] =
10-14; entonces;
10-14 de donde;
POTENCIAL DE HIDROGENACIN O pH
El pH de una solucin acuosa es igual al logaritmo negativo de la concentracin de iones H+ expresado en moles por litro
Escala de pH;
El pOH es igual al logaritmo negativo de la concentracin molar de iones OH. Calcular el pH del agua pura
Log 1.0 x 107
el pH del agua es 7 EJEMPLO:
Log 1.0
+log =7
107
0 + =
Cul es el pH de una solucin de 0.0020 M de HCl?
Log 5 + log 102 = 0.7 + 2 = 2.7 Respuesta: el pH de la solucin es de 2.7
INDICADORES
Son sustancias que pueden utilizarse en formas de solucin o impregnadas en papeles especiales y que cambian de color segn el grado del pH
INDICADOR
Fenoftaleina Tornasol Rojo congo
MEDIO CIDO MEDIO BSICO
incoloro rojo azul rojo azul rojo
Alizarina
amarillo
rojo naranja
COLOIDES
los coloides son mezclas intermedias entre las soluciones y las mezclas propiamente dichas; sus partculas son de tamao mayor que el de las soluciones ( 10 a 10.000 A se llaman micelas). Los componentes de un coloide se denominan fase dispersa y medio dispersante. Segn la afinidad de los coloides por la fase dispersante se clasifican en lifilos si tienen afinidad y lifobos si no hay afinidad entre la sustancia y el medio.
Clase de coloides segn el estado fsico
NOMBRE Aerosol slido Geles Aerosol liquido Emulsin Emulsin slida Espuma Espuma slida
EJEMPLOS Polvo en el aire Gelatinas, tinta, clara de huevo Niebla leche, mayonesa Pinturas, queso Nubes, esquemas Piedra pmez
FASE MEDIO DISPERS DISPERSAN A TE Slido Slido Liquido Liquido Liquido Gas Gas Gas Liquido Gas Liquido Slido Liquido Slido
PROPIEDADES DE LOS COLOIDES
Las propiedades de los coloides son :
Movimiento browniano: Se observa en un coloide al
ultramicroscopio, y se caracteriza por un movimiento de partculas rpido, catico y continuo; esto se debe al choque de las partculas dispersas con las del medio. Efecto de Tyndall Es una propiedad ptica de los coloides y consiste en la difraccin de los rayos de luz que pasan a travs de un coloide. Esto no ocurre en otras sustancias.
Adsorcin : Los coloides son excelentes adsorbentes debido al
tamao pequeo de las partculas y a la superficie grande. EJEMPLO: el carbn activado tiene gran adsorcin, por tanto, se usa en los extractores de olores; esta propiedad se usa tambin en cromatografa. Carga elctrica : Las partculas presentan cargas elctricas positivas o negativas. Si se trasladan al mismo tiempo hacia el polo positivo se denomina anaforesis; si ocurre el movimiento hacia el polo negativo, cataforesis.
Anda mungkin juga menyukai
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDari EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesBelum ada peringkat
- Fundamentos Teoricos Tema de Los GasesDokumen18 halamanFundamentos Teoricos Tema de Los GasesMantrazBelum ada peringkat
- 5 GasesDokumen45 halaman5 GasesConstructora InsajBelum ada peringkat
- 8 GasesDokumen10 halaman8 GasesJUANS HIDALDOBelum ada peringkat
- Gases 11Dokumen7 halamanGases 11yapimaBelum ada peringkat
- Gases Química PDFDokumen8 halamanGases Química PDFMax ChazzBelum ada peringkat
- Semana 13 - GasesDokumen26 halamanSemana 13 - GasesNadia AlfaroBelum ada peringkat
- Gases Ideales y Sus LeyesDokumen30 halamanGases Ideales y Sus LeyesSofi AntinoriBelum ada peringkat
- 02-28-16 Gases P1Dokumen4 halaman02-28-16 Gases P1Diego Fernando Ardila ArizaBelum ada peringkat
- CAPITULO IV. TermodinamicaDokumen29 halamanCAPITULO IV. TermodinamicaKeyt Nicold Ocas NuñezBelum ada peringkat
- Guia Nº1 de Los Gases Grado UndecimoDokumen3 halamanGuia Nº1 de Los Gases Grado UndecimoNatali Sanabria VasquezBelum ada peringkat
- Resumen Los GasesDokumen5 halamanResumen Los Gasesppeinado00Belum ada peringkat
- Difusion GaseosaDokumen19 halamanDifusion GaseosaCarlos GarciaBelum ada peringkat
- Tarea 1 - Gases IdealesDokumen7 halamanTarea 1 - Gases IdealesNancy Olivia VentoleroBelum ada peringkat
- CONOCIMIENTOS PREVIOS. Flores Zaragoza D. Janet, MTZ García S. Paola, Morales Reséndiz K. EvelynDokumen7 halamanCONOCIMIENTOS PREVIOS. Flores Zaragoza D. Janet, MTZ García S. Paola, Morales Reséndiz K. EvelynKarina Evelyn Morales ReséndizBelum ada peringkat
- Guia-de-GasesDokumen27 halamanGuia-de-GasesjimminBelum ada peringkat
- Gases IdealesDokumen29 halamanGases IdealesPerorina ellieBelum ada peringkat
- GasDokumen6 halamanGasPame LxuBelum ada peringkat
- Ley de Gases IdealesDokumen18 halamanLey de Gases IdealesJear ArenasBelum ada peringkat
- Gases QuimicaDokumen6 halamanGases QuimicaEvelin P. Uyuquipa F.Belum ada peringkat
- GASES FinDokumen32 halamanGASES FinAntony Merino QuinchullaBelum ada peringkat
- U 6 Gases PDFDokumen7 halamanU 6 Gases PDFWa WaiiBelum ada peringkat
- 2.4 Comportamiento de Gases Reales DJVMDokumen11 halaman2.4 Comportamiento de Gases Reales DJVMalondraBelum ada peringkat
- Informe de Labortatorio GasesDokumen11 halamanInforme de Labortatorio GasesYacqui Adeli OblitasBelum ada peringkat
- Guía Quimica 11 2PDokumen14 halamanGuía Quimica 11 2PLINAFLAKBelum ada peringkat
- Leyes de Los Gases Ideales 2020Dokumen8 halamanLeyes de Los Gases Ideales 2020Lino AndresBelum ada peringkat
- 3 CalculoscomunesDokumen16 halaman3 CalculoscomunesAlexander Perez PerezBelum ada peringkat
- Gases Ideales - MonografiaDokumen7 halamanGases Ideales - MonografiaAlexis Pacheco CastilloBelum ada peringkat
- Los GasesDokumen7 halamanLos Gasesdaniel alejandro castroBelum ada peringkat
- Informe 5Dokumen23 halamanInforme 5Eva Caballero0% (1)
- 4 - GasesDokumen4 halaman4 - GasesLautaro CastilloBelum ada peringkat
- GasesDokumen9 halamanGasesJUAN CAMILO ACUÑA ENDOBelum ada peringkat
- Unidad 1 PDFDokumen29 halamanUnidad 1 PDFbertha angamarcaBelum ada peringkat
- Lab 2 QMC 1206Dokumen16 halamanLab 2 QMC 1206Andrea Flores MedranoBelum ada peringkat
- Teoria de GasesDokumen6 halamanTeoria de GasesClaudia Mabel FloresBelum ada peringkat
- Guía Teórica de GasesDokumen15 halamanGuía Teórica de GasesYomairis RodriguezBelum ada peringkat
- Gas IdealDokumen8 halamanGas IdealGustavo Armando López DíazBelum ada peringkat
- Estado Gaseoso - Estequiometría - Problemas ResueltosDokumen25 halamanEstado Gaseoso - Estequiometría - Problemas ResueltosCane AbacaBelum ada peringkat
- Universidad Central Del EcuadorDokumen11 halamanUniversidad Central Del Ecuadorrick0ctsBelum ada peringkat
- Los GasesDokumen19 halamanLos GasesTami Di DinoBelum ada peringkat
- Estado Gaseoso UnmsmDokumen31 halamanEstado Gaseoso UnmsmWilber Milla Trujillo0% (1)
- Laboratorio N 4 de QuimicaDokumen17 halamanLaboratorio N 4 de QuimicaCristhianNeyraKunkel100% (1)
- CaratulaDokumen21 halamanCaratulaJose VilelaBelum ada peringkat
- Diapositivas Unidad # 4 Leyes de Los GasesDokumen46 halamanDiapositivas Unidad # 4 Leyes de Los GasesMellkyo -.-100% (1)
- Quimica Capitulo 11Dokumen9 halamanQuimica Capitulo 11Sergio moralesBelum ada peringkat
- GasesDokumen22 halamanGasesMiguel André Salinas RevillaBelum ada peringkat
- GasesDokumen4 halamanGasesJesúsEnriqueGarciaBelum ada peringkat
- Unidad 1Dokumen34 halamanUnidad 1ej pf0% (1)
- Aplico Mi Saber Quimica 2021Dokumen29 halamanAplico Mi Saber Quimica 2021ani lorenaBelum ada peringkat
- Propiedades de Los GasesDokumen30 halamanPropiedades de Los GasesyennyBelum ada peringkat
- Informe Quimica 5Dokumen17 halamanInforme Quimica 5Valeria DuharteBelum ada peringkat
- Estado Gaseoso de La MateriaDokumen17 halamanEstado Gaseoso de La MateriaJosé Manuel Lombardero MejiasBelum ada peringkat
- Clase 9. Estado Gaseoso-Leyes de Los GasesDokumen33 halamanClase 9. Estado Gaseoso-Leyes de Los Gasesgeomara pures100% (1)
- Presentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaDokumen17 halamanPresentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde TurquesaBRAYAN LEONEL SANCHEZ CHABLEBelum ada peringkat
- Termodinamica 4 D Medio Guía Semana 7...Dokumen10 halamanTermodinamica 4 D Medio Guía Semana 7...Fernando Gonzalez BlancoBelum ada peringkat
- Gases IdealesDokumen9 halamanGases IdealesJuan Alberto Mondaca FuentesBelum ada peringkat
- Ley de Los Gases Del Grado 11Dokumen2 halamanLey de Los Gases Del Grado 11jorge ortizBelum ada peringkat
- 02 - GasesDokumen6 halaman02 - GasesAnita Elizabeth Layza MendiolaBelum ada peringkat
- Gases, Ley de Los GasesDokumen29 halamanGases, Ley de Los GasesJavier AlvarezBelum ada peringkat
- Tema 12 Gases Ideales y Reales$Dokumen11 halamanTema 12 Gases Ideales y Reales$JuanLoredoBelum ada peringkat
- Liquidación de Obra Por ContrataDokumen67 halamanLiquidación de Obra Por ContrataAlberth SCBelum ada peringkat
- ReporteadorDokumen2 halamanReporteadorRoxana AlbertiBelum ada peringkat
- Ep Edd A1Dokumen3 halamanEp Edd A1CHRISTOPHER ISRAEL COSIO MARTINEZBelum ada peringkat
- Manual de PsicomagiaDokumen3 halamanManual de Psicomagiaanon_853017717Belum ada peringkat
- Taller Semana 3Dokumen2 halamanTaller Semana 3Nicolas Alias0% (1)
- Parcial GERENCIA ESTRATEGICA #1Dokumen7 halamanParcial GERENCIA ESTRATEGICA #1Angel MiguelBelum ada peringkat
- Prueba 1 II Parcial (IEEE802.11) - Revisión Del IntentoDokumen5 halamanPrueba 1 II Parcial (IEEE802.11) - Revisión Del IntentoJomaira MaribelBelum ada peringkat
- Informe Psicológico Test Del ÁrbolDokumen9 halamanInforme Psicológico Test Del ÁrbolRuth ChacónBelum ada peringkat
- Modalidades Curriculares en La Educacià N ParvulariaDokumen9 halamanModalidades Curriculares en La Educacià N ParvulariaJosette Gyubel AvilÉs OlivosBelum ada peringkat
- Principios de Instrumentacion IndustrialDokumen8 halamanPrincipios de Instrumentacion IndustrialFelipe ApazaBelum ada peringkat
- Instrumento DSM 5 Adultos 2 Hojas cDERS Con Tablas de CalificaciónDokumen4 halamanInstrumento DSM 5 Adultos 2 Hojas cDERS Con Tablas de CalificaciónIsayah Cuevas Coronel100% (1)
- Clases de Contratos Civles Comerciales Administrativos y LaboralesDokumen6 halamanClases de Contratos Civles Comerciales Administrativos y LaboralesElsa Janeth Acuña CamargoBelum ada peringkat
- PLÁTANODokumen6 halamanPLÁTANODante Luis Cayahuallpa EspinozaBelum ada peringkat
- Ficha Técnica ANTICORROSIVO CROMATO BLER®Dokumen2 halamanFicha Técnica ANTICORROSIVO CROMATO BLER®YUDY SILVABelum ada peringkat
- Consumidor Capitulo 3Dokumen15 halamanConsumidor Capitulo 3Denise CABelum ada peringkat
- Fuzzy Logic - En.españolDokumen24 halamanFuzzy Logic - En.españolSaul CamposBelum ada peringkat
- Juguemos A Master Chef JuniorDokumen24 halamanJuguemos A Master Chef JuniorRocio MendozaBelum ada peringkat
- C Sharp ProgramasDokumen8 halamanC Sharp ProgramasManeNenu100% (1)
- Estudios Previos CHIPAQUEDokumen13 halamanEstudios Previos CHIPAQUEAlvaro Stiven MORENO SALINASBelum ada peringkat
- Diapositivas Proyecto de GradoDokumen12 halamanDiapositivas Proyecto de GradokekekekeBelum ada peringkat
- 03-Perfiles ComercialesDokumen32 halaman03-Perfiles ComercialesGuido ZuccarelliBelum ada peringkat
- Formato Prescripcion Personas MoralesDokumen2 halamanFormato Prescripcion Personas MoralesGerko ManriqueBelum ada peringkat
- Revista Andalucía Subterránea 29Dokumen104 halamanRevista Andalucía Subterránea 29Federación Andaluza de EspeleologíaBelum ada peringkat
- Entre Windows 10 y Win 11Dokumen1 halamanEntre Windows 10 y Win 11Jerson CabezasBelum ada peringkat
- Cuadernillo de Los NumerosDokumen85 halamanCuadernillo de Los NumeroscristianBelum ada peringkat
- Guia Espina de PescadoDokumen13 halamanGuia Espina de Pescadowilliam castañedaBelum ada peringkat
- Fci Pionero FFDokumen1 halamanFci Pionero FFJhonny GiulianoBelum ada peringkat
- Tecnoquímicas S.A.Dokumen30 halamanTecnoquímicas S.A.emersonBelum ada peringkat
- LitografiaDokumen8 halamanLitografiaJavier Arancibia MartinezBelum ada peringkat
- Parque Canino - Roberto Romahn DiezDokumen98 halamanParque Canino - Roberto Romahn DiezJulio César Ark'sBelum ada peringkat