Acidosis Respiratoria Listo
Diunggah oleh
Diane Troncoso AlegriaHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Acidosis Respiratoria Listo
Diunggah oleh
Diane Troncoso AlegriaHak Cipta:
Format Tersedia
Araya
Procesos Biolgicos I CBI 120 Instituto de ciencias naturales Facultad de educacin
Unidad II: Trabajo Voluntario Evaluado
Por qu el cuerpo debe regular el pH?
Nombre: Nicolle Estrella Valenzuela Briones Seccin: 401 Sede: Santiago Centro Msc: Sylvia Araya
3) Mencione algunas causas de acidosis respiratoria y la forma que tiene nuestro organismo de compensar.
Acidosis Respiratoria
Acidosis respiratoria elevacin de pCO2 - elevacin de HCO3
Definicin:
Hipercapnia usualmente debida a una excrecin pulmonar inadecuada
de CO2, esto quiere decir que la acidosis respiratoria se caracteriza por la incapacidad de los pulmones para eliminar todo el CO2 producido por el organismo, por lo que la pCO2 aumenta y la existencia de un nivel normal de Bicarbonato produce una disminucin en la relacin bicarbonato /cido carbnico.
Puede ser aguda o crnica
Acidosis respiratoria Aguda
Patrones en el anlisis de gases arteriales:
pH menor a 7.35
PCO2 mayor a 45 mmHg
Exceso de base estndar 0+/-5
Acidosis Respiratoria Aguda (Fisiopatologa)
La disminucin de la excrecin pulmonar de CO2 usualmente debida a la Hipoventilacin alveolar, origina un incremento en la PCO2
La Hipercapnia produce Acidosis, con incremento en el H+ plasmtico de aprox. 0.75mEq/L por c/mmHg de incremento en PCO2.
El intercambio resulta en hipoxemia
Se producen cambios adaptativos, en minutos
Algunas causas de esta alteracin son:
enfermedad broncopulmonar intoxicacin por barbitricos respiracin asistida mal estimada asfixia
Depresin del SNC: anestesia, sedantes, TEC, ACV, apnea del sueo,
edema cerebral, tumores cerebrales, encefalitis.
Desrdenes Neuromusculares: lesin de la mdula espinal, sndrome
de Guillain Barre, status epilptico, botulismo, ttanos, crisis de miastenia gravis, miopata hipokalmica, drogas o toxinas.
Restriccin de la ventilacin: fractura costal, neumotrax Defecto en la perfusin pulmonar: colapso circulatorio, TEP.
La compensacin: Se producir porque el rin eliminar una mayor cantidad de H+
causando, de este modo, un incremento del bicarbonato.
Bicarbonato: El sistema cido Carbnico-Bicarbonato es el buffer ms importante de nuestro organismo. Existen mltiples caractersticas que hacen de este sistema un regulador de pH el ms eficaz en el hombre. En primer lugar se trata de un sistema que est presente en todos los medios tanto intracelulares como extracelulares. A primera vista su pKa parecera corresponder a un buffer poco til para nuestro organismo ya que su valor es de 6,10.Sin embargo este hecho se ve compensado por la posibilidad de regular independientemente las concentraciones tanto de la especie aceptora de protones como la dadora de protones. Es importante tener en cuenta que todos los sistemas buffer estn interrelacionados y que se amortiguan unos a otros, de modo que todos los buffer de un mismo compartimiento van a variar conjuntamente ante un cambio en el pH. Esto nos va a permitir conocer los cambios de cada sistema si conocemos los que ha experimentado uno de ellos
(aportes) http://www.slideshare.net/jorgis82/acidosis-respiratoria http://es.scribd.com/doc/6657395/Acidosis-Respiratoria Fisiologa Humana STUART IRA FOX
Bibliografa:
Anda mungkin juga menyukai
- Tesis Rodrigo Cornejo Nuevos Sentidos Del Trabajo Docente (Biblioteca)Dokumen557 halamanTesis Rodrigo Cornejo Nuevos Sentidos Del Trabajo Docente (Biblioteca)Rodrigo Cornejo ChavezBelum ada peringkat
- Acta Colombiana de Psicología 0123-9155: Issn: Revistaacta@ucatolica - Edu.coDokumen10 halamanActa Colombiana de Psicología 0123-9155: Issn: Revistaacta@ucatolica - Edu.coDiane Troncoso AlegriaBelum ada peringkat
- Atención PrimariaDokumen8 halamanAtención PrimariaDiane Troncoso AlegriaBelum ada peringkat
- Burnout en ProfesoresDokumen25 halamanBurnout en Profesoresjack staffBelum ada peringkat
- Revista de Especialidades Médico-Quirúrgicas 1665-7330: Issn: Revespmedquir@issste - Gob.mxDokumen11 halamanRevista de Especialidades Médico-Quirúrgicas 1665-7330: Issn: Revespmedquir@issste - Gob.mxDiane Troncoso AlegriaBelum ada peringkat
- Salud Laboral DocenteDokumen9 halamanSalud Laboral DocenteAngel SotoBelum ada peringkat
- Fondo de Investigación Y Desarrollo en Educación Fonide: Informe FinalDokumen123 halamanFondo de Investigación Y Desarrollo en Educación Fonide: Informe FinalDiane Troncoso AlegriaBelum ada peringkat
- Sı Ndrome de Tako-Tsubo e Insuficiencia Cardiaca: Seguimiento A Largo PlazoDokumen7 halamanSı Ndrome de Tako-Tsubo e Insuficiencia Cardiaca: Seguimiento A Largo PlazoDiane Troncoso AlegriaBelum ada peringkat
- Del Trabajo: Medicina SeguridadDokumen6 halamanDel Trabajo: Medicina SeguridadDiane Troncoso AlegriaBelum ada peringkat
- ¿Estrés o Burnout?: PresentaciónDokumen8 halaman¿Estrés o Burnout?: PresentaciónDiane Troncoso AlegriaBelum ada peringkat
- Salud Laboral DocenteDokumen9 halamanSalud Laboral DocenteAngel SotoBelum ada peringkat
- 1 - Condiciones Trabajo Salud Docente INVESTIGACIONDokumen212 halaman1 - Condiciones Trabajo Salud Docente INVESTIGACIONLucia Frones CarreñoBelum ada peringkat
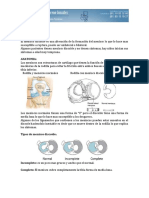
- Articulacion Femoro PatelarDokumen15 halamanArticulacion Femoro PatelarJulio Cesar Vera VasquezBelum ada peringkat
- Menisco DiscoideDokumen4 halamanMenisco DiscoideDiane Troncoso AlegriaBelum ada peringkat
- Bournout en Teachers de Cali PDFDokumen12 halamanBournout en Teachers de Cali PDFChristian MolinaBelum ada peringkat
- Fundamentos de Fisiologia de La Actividad Fisica y El DeporteDokumen146 halamanFundamentos de Fisiologia de La Actividad Fisica y El Deportekarencita1986Belum ada peringkat
- El Burnout o Sindrome de Estar Quemado en Profesionales..Dokumen24 halamanEl Burnout o Sindrome de Estar Quemado en Profesionales..C'ristián RAmoneBelum ada peringkat
- Fuentes de Estrés, Burnout y Estrategias de Coping en Profesores PortuguesesDokumen20 halamanFuentes de Estrés, Burnout y Estrategias de Coping en Profesores PortuguesesDiane Troncoso AlegriaBelum ada peringkat
- Paper Cervicales MiofacialDokumen9 halamanPaper Cervicales MiofacialDiane Troncoso AlegriaBelum ada peringkat
- Salud laboral de profesores en ChileDokumen109 halamanSalud laboral de profesores en Chilefeliponcho2008Belum ada peringkat
- ManualDokumen9 halamanManualDiane Troncoso AlegriaBelum ada peringkat
- Niveles de Desgaste Profesional (Burnout) en Docentes y Estrategias de Prevención.Dokumen245 halamanNiveles de Desgaste Profesional (Burnout) en Docentes y Estrategias de Prevención.Diane Troncoso AlegriaBelum ada peringkat
- Hipertension Fisiopatologia Servicio de Cardiologia. Hospital Virgen de La Salud. Toledo.2003Dokumen19 halamanHipertension Fisiopatologia Servicio de Cardiologia. Hospital Virgen de La Salud. Toledo.2003Adrian Estrada GarciaBelum ada peringkat
- Dialnet FuentesDeEstresSindromeDeBurnoutYActitudesDisfunci 1494Dokumen404 halamanDialnet FuentesDeEstresSindromeDeBurnoutYActitudesDisfunci 1494Amanda BaldwinBelum ada peringkat
- Listado de Papers Transición Sd-Bp. 2.Dokumen2 halamanListado de Papers Transición Sd-Bp. 2.Diane Troncoso AlegriaBelum ada peringkat
- Ine Adulto MayorDokumen4 halamanIne Adulto Mayorhowarda09Belum ada peringkat
- Listado de Papers Transición Sd-Bp. 1.Dokumen3 halamanListado de Papers Transición Sd-Bp. 1.Diane Troncoso AlegriaBelum ada peringkat
- Caídas en El Adulto Mayor y Su Relación Con La Capacidad Funcional.Dokumen9 halamanCaídas en El Adulto Mayor y Su Relación Con La Capacidad Funcional.Diane Troncoso AlegriaBelum ada peringkat
- Hemorragia PospartoDokumen63 halamanHemorragia PospartoJose BrionesBelum ada peringkat
- Liverfine PorcinobDokumen2 halamanLiverfine PorcinobAna Luisa GilBelum ada peringkat
- EquinodermosDokumen5 halamanEquinodermosMarielinsimianBelum ada peringkat
- Adquirida IIDokumen5 halamanAdquirida IIAlejandra UrrutiaBelum ada peringkat
- Tema1 - Problemas - Estatica de FluidosDokumen2 halamanTema1 - Problemas - Estatica de FluidosJavierBelum ada peringkat
- Aparato Reproductor de Las AvesDokumen2 halamanAparato Reproductor de Las AvesEnrique TorreiroBelum ada peringkat
- Glosario EgoDokumen6 halamanGlosario EgoCarlos ArguetaBelum ada peringkat
- Dieta Rica en HierroDokumen3 halamanDieta Rica en HierroPamela CastilloBelum ada peringkat
- Guia Practica Autonomo RevisadoDokumen16 halamanGuia Practica Autonomo RevisadoTaty GueledelBelum ada peringkat
- APOPTOSi SDokumen3 halamanAPOPTOSi SFernanda Comba100% (1)
- Monitoreo Del Pulso.Dokumen12 halamanMonitoreo Del Pulso.Noemi100% (1)
- Distribución de Los MicroorganismosDokumen6 halamanDistribución de Los MicroorganismosEduardo Perez100% (3)
- Guía Cvemp y OvempDokumen2 halamanGuía Cvemp y OvempCarolina OjedaBelum ada peringkat
- El efecto de la insulina y glibenclamida en ratas con diabetes experimentalDokumen4 halamanEl efecto de la insulina y glibenclamida en ratas con diabetes experimentalGrace Mirella0% (1)
- Catergorias y Test para CardioDokumen5 halamanCatergorias y Test para CardioJuan OsorioBelum ada peringkat
- Fisioterapia parálisis facialDokumen14 halamanFisioterapia parálisis facialRicardo Chuan GarciaBelum ada peringkat
- Características de Las Células (Erica)Dokumen2 halamanCaracterísticas de Las Células (Erica)xpress111100% (4)
- Apuntes Unidad IVDokumen30 halamanApuntes Unidad IVcarmen carballo camposBelum ada peringkat
- Estres de SobrevivenciaDokumen10 halamanEstres de Sobrevivenciaana beatrizBelum ada peringkat
- 3 Año Biologia Guia No2 II LapsoDokumen3 halaman3 Año Biologia Guia No2 II LapsoyadilkaBelum ada peringkat
- MANUCLASES62 Guia Glucogenosis Actualizada Mayo 2017 PDFDokumen20 halamanMANUCLASES62 Guia Glucogenosis Actualizada Mayo 2017 PDFDanny Heras GonzalezBelum ada peringkat
- Super Detox CelularDokumen27 halamanSuper Detox CelularJose Brunello100% (2)
- Tema El BrocoliDokumen8 halamanTema El BrocoliKenyi Fabian BernalBelum ada peringkat
- AparatologiaDokumen30 halamanAparatologiaDaniel Muñoz Castillo89% (9)
- Enfermeria V (Extremidad Superior)Dokumen34 halamanEnfermeria V (Extremidad Superior)davidplay313Belum ada peringkat
- Fisiologia Humana Sistema LimbicoDokumen21 halamanFisiologia Humana Sistema LimbicoEnrique M. GonzalezBelum ada peringkat
- 27 Hacks Mente EmocionesDokumen12 halaman27 Hacks Mente EmocionesAnonymous GjeL2x9kIi100% (3)
- Curso de ElectrocardiografíaDokumen134 halamanCurso de ElectrocardiografíaDavud PortugalBelum ada peringkat
- Cuentoconociendo El Aparato Reproductor MasculinoDokumen2 halamanCuentoconociendo El Aparato Reproductor Masculinodiboty23378% (9)
- PatrickDokumen4 halamanPatrickeliherBelum ada peringkat