Química RG PPT - Propriedades Coligativas
Diunggah oleh
Química PPT100%(2)100% menganggap dokumen ini bermanfaat (2 suara)
799 tayangan10 halaman1) O documento discute propriedades coligativas, que são variações nas propriedades físicas de um solvente quando um soluto não volátil é adicionado.
2) Propriedades coligativas incluem pressão de vapor, temperatura de ebulição, crioscopia e pressão osmótica.
3) A magnitude dos efeitos coligativos depende da quantidade e tipo de partículas dissolvidas (iônicas ou moleculares).
Deskripsi Asli:
Hak Cipta
© Attribution Non-Commercial (BY-NC)
Format Tersedia
PPT, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Ini1) O documento discute propriedades coligativas, que são variações nas propriedades físicas de um solvente quando um soluto não volátil é adicionado.
2) Propriedades coligativas incluem pressão de vapor, temperatura de ebulição, crioscopia e pressão osmótica.
3) A magnitude dos efeitos coligativos depende da quantidade e tipo de partículas dissolvidas (iônicas ou moleculares).
Hak Cipta:
Attribution Non-Commercial (BY-NC)
Format Tersedia
Unduh sebagai PPT, PDF, TXT atau baca online dari Scribd
100%(2)100% menganggap dokumen ini bermanfaat (2 suara)
799 tayangan10 halamanQuímica RG PPT - Propriedades Coligativas
Diunggah oleh
Química PPT1) O documento discute propriedades coligativas, que são variações nas propriedades físicas de um solvente quando um soluto não volátil é adicionado.
2) Propriedades coligativas incluem pressão de vapor, temperatura de ebulição, crioscopia e pressão osmótica.
3) A magnitude dos efeitos coligativos depende da quantidade e tipo de partículas dissolvidas (iônicas ou moleculares).
Hak Cipta:
Attribution Non-Commercial (BY-NC)
Format Tersedia
Unduh sebagai PPT, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 10
PROPRIEDADES COLIGATIVAS
PROF.: ROBERTO GOIS
PROPRIEDADES COLIGATIVAS
É o estudo da variação nas propriedades físicas do
solvente quando adicionado um soluto não volátil. As
propriedades coligativas dependem da quantidade de
partículas dissolvidas.
PRESSÃO MÁXIMA DE VAPOR
Pressão que o
vapor do líquido
saturado
exerce sobre o
líquido.
Prof. Roberto Gois
Prof. Roberto Gois
PRESSÃO DE VAPOR E TEMPERATURA DE EBULIÇÃO
* Um líquido entra em ebulição quando a sua pressão
de vapor se iguala a pressão externa (atmosférica).
Prof. Roberto Gois
DIAGRAMA DE FASES
Prof. Roberto Gois
TONOSCOPIA
É o abaixamento da pressão de vapor de um
líquido quando adicionado um soluto não volátil.
Prof. Roberto Gois
CRIOSCOPIA E EBULIOSCOPIA
Prof. Roberto Gois
PRESSÃO OSMÓTICA
OSMOSE
PRESSÃO OSMÓTICA: A mínima pressão exercida para
impedir a osmose.
Prof. Roberto Gois
SOLUÇÕES IÔNICAS X SOLUÇÕES MOLECULARES
SOLUÇÕES MOLECULARES : O número de partículas
dissolvida é igual ao número de não dissolvida.
SOLUÇÕES IÔNICAS: O número de partículas
dissolvidas é maior que o número de partículas não
dissolvidas. ( dissociação e ionização)
Prof. Roberto Gois
CÁLCULO DOS EFEITOS COLIGATIVOS
EFEITO SOLUÇÃO SOLUÇÃO
COLIGATIVO IÔNICA MOLECULAR
TONOSCÓPIA ∆p/po = Kt.M.i ∆p/po = Kt.M.i
= x1 = x1
EBULIOSCÓPIA ∆Te = Ke.M ∆Te = Ke.M. i
CRIOSCÓPIA ∆Tc = Kc.M ∆Tc = Kc.M.i
PRESSÃO π = M.R.T π = M.R.T.i
OSMÓTICA
Prof. Roberto Gois
Anda mungkin juga menyukai
- Propriedades Coligativas ResumoDokumen18 halamanPropriedades Coligativas ResumomarsjommBelum ada peringkat
- Química PPT - Dispersões IDokumen14 halamanQuímica PPT - Dispersões IQuímica PPT100% (3)
- Química PPT - SoluçõesDokumen15 halamanQuímica PPT - SoluçõesQuímica PPT100% (1)
- Aula 2 - Propriedades ColigativasDokumen44 halamanAula 2 - Propriedades ColigativasBeatriz NunesBelum ada peringkat
- Estudo Dos Gases - Parte IDokumen12 halamanEstudo Dos Gases - Parte IjulianosmaBelum ada peringkat
- PRIMEBOOK - Capítulo 05 - Leis PonderaisDokumen7 halamanPRIMEBOOK - Capítulo 05 - Leis PonderaisGleidiane FerreiraBelum ada peringkat
- Cinetica QuimicaDokumen25 halamanCinetica QuimicaSaulo Luis CapimBelum ada peringkat
- Resumão Química P1B1Dokumen17 halamanResumão Química P1B1Soteldo100% (1)
- Sobre o (Não) Domínio da Linguagem Química e sua Influência na AprendizagemDari EverandSobre o (Não) Domínio da Linguagem Química e sua Influência na AprendizagemBelum ada peringkat
- Reacoes OrganicasDokumen62 halamanReacoes OrganicasLarissa SantosBelum ada peringkat
- Química PPT - Tabela Periódica - HistóricoDokumen10 halamanQuímica PPT - Tabela Periódica - HistóricoQuímica PPT100% (3)
- 2017 08 17 Propriedades Coligativas SerDokumen33 halaman2017 08 17 Propriedades Coligativas SerEugenio ManuelBelum ada peringkat
- Balanceamento de Equações QuímicasDokumen6 halamanBalanceamento de Equações Químicasalanlima92Belum ada peringkat
- Cinetica QuimicaDokumen24 halamanCinetica QuimicaAdriana Bemstar100% (1)
- Separação de MisturasDokumen26 halamanSeparação de MisturasJoabe AraújoBelum ada peringkat
- Extrator de Óleo Essencial: Um Experimento de Baixo Custo para o Ensino de Química Orgânica No Ensino MédioDokumen1 halamanExtrator de Óleo Essencial: Um Experimento de Baixo Custo para o Ensino de Química Orgânica No Ensino MédioWilliam Sousa100% (1)
- Cinética Química 2015Dokumen52 halamanCinética Química 2015RomeuComastriAbdalaBelum ada peringkat
- Química PPT - Teoria Atômica MolecularDokumen21 halamanQuímica PPT - Teoria Atômica MolecularQuímica PPT100% (3)
- (Apostila) Química Orgânica - CETEBDokumen110 halaman(Apostila) Química Orgânica - CETEBEduardo Bandeira50% (2)
- Propriedades ColigativasDokumen9 halamanPropriedades ColigativascjtmidiaBelum ada peringkat
- Aula 4 - Fundamentos Da EspectrofotometriaDokumen41 halamanAula 4 - Fundamentos Da Espectrofotometriaricardosm23Belum ada peringkat
- Introdução À Química Orgânica - 2022Dokumen6 halamanIntrodução À Química Orgânica - 2022Maria FabíulaBelum ada peringkat
- Eletroquímica - Cap 20 Parte 1Dokumen62 halamanEletroquímica - Cap 20 Parte 1Ana Clara CastroBelum ada peringkat
- Relatorio Lab Aula 2Dokumen18 halamanRelatorio Lab Aula 2Fernanda SoaresBelum ada peringkat
- Química PPT - Introdução A QuímicaDokumen61 halamanQuímica PPT - Introdução A QuímicaQuímica PPT83% (6)
- Apostila 1 de Química X - Prof Zila - UERJ PDFDokumen58 halamanApostila 1 de Química X - Prof Zila - UERJ PDFIsabelle ChristineBelum ada peringkat
- Apostila Concentração Das Soluções 1Dokumen8 halamanApostila Concentração Das Soluções 1wesley NETUBERBelum ada peringkat
- Química PPT - Aula Métodos Separação MisturasDokumen42 halamanQuímica PPT - Aula Métodos Separação MisturasQuímica PPT100% (10)
- Propriedades Coligativas - Roteiro para Os EstudantesDokumen7 halamanPropriedades Coligativas - Roteiro para Os EstudantesNicele PaixãoBelum ada peringkat
- Estudo Das Soluções PDFDokumen47 halamanEstudo Das Soluções PDFRenanEQBelum ada peringkat
- Propriedades ColigativasDokumen22 halamanPropriedades Coligativasskull41Belum ada peringkat
- Soluções (Slide)Dokumen58 halamanSoluções (Slide)Felipe QueirozBelum ada peringkat
- Propriedades Coligativas - Exercícios Cola Da WebDokumen5 halamanPropriedades Coligativas - Exercícios Cola Da WebGildásio JúniorBelum ada peringkat
- Pratica 5 - Cinetica QuimicaDokumen4 halamanPratica 5 - Cinetica QuimicaDébora Costa ReisBelum ada peringkat
- Relatório 9 FQ - Equilíbrio Químico em SoluçõesDokumen10 halamanRelatório 9 FQ - Equilíbrio Químico em SoluçõesSérgio GuimarãesBelum ada peringkat
- Aula 9 - Teoria Do Orbital MolecularDokumen32 halamanAula 9 - Teoria Do Orbital Molecularmax_patricioBelum ada peringkat
- Noções Gerais de RedoxDokumen14 halamanNoções Gerais de RedoxAna Paula Oliveira MartinsBelum ada peringkat
- c6 Curso A Prof QuimicaDokumen20 halamanc6 Curso A Prof QuimicaTiago RodriguesBelum ada peringkat
- Cap 6 EstequiometriaDokumen23 halamanCap 6 EstequiometriaLuana Ribeiro GarciaBelum ada peringkat
- 2 Propriedades - ColigativasDokumen37 halaman2 Propriedades - ColigativasGleison Paulino GonçalvesBelum ada peringkat
- Lei de Hess - Exercícios de Revisão PDFDokumen7 halamanLei de Hess - Exercícios de Revisão PDFGeliane RochaBelum ada peringkat
- Elementos Do Bloco DDokumen8 halamanElementos Do Bloco DNatália CataniBelum ada peringkat
- Aula 8 EstereoquímicaDokumen58 halamanAula 8 EstereoquímicaThiago TakeoBelum ada peringkat
- APOSTILA 01 - Introdução QO e Hibridização Do CarbonoDokumen19 halamanAPOSTILA 01 - Introdução QO e Hibridização Do CarbonoAlinne GirlaineBelum ada peringkat
- Relatorio Pratica COLOIDESDokumen17 halamanRelatorio Pratica COLOIDESLivia Dantas0% (1)
- Aula Quimica Inorganica Sais e OxidosDokumen26 halamanAula Quimica Inorganica Sais e OxidosEloiza GonçalvesBelum ada peringkat
- Soluções - Profº Agamenon RobertoDokumen15 halamanSoluções - Profº Agamenon Robertocb_penatrujilloBelum ada peringkat
- 3-Reações de Eliminação de Haletos de AlquilaDokumen64 halaman3-Reações de Eliminação de Haletos de AlquilaMateus Ramos0% (1)
- Aula 11transposição Didático-Digital e Avaliação Da Aprendizagem Nas Modalidades de Ensino Remoto e HíbridoDokumen35 halamanAula 11transposição Didático-Digital e Avaliação Da Aprendizagem Nas Modalidades de Ensino Remoto e HíbridoRaimundo Nonato de SousaBelum ada peringkat
- Apostila FQIIDokumen44 halamanApostila FQIIIzaias AiresBelum ada peringkat
- Apostila Tabela e Propriedades PeriodicasDokumen10 halamanApostila Tabela e Propriedades PeriodicasSandra QBelum ada peringkat
- Relatório 1 - Tensão SuperficialDokumen6 halamanRelatório 1 - Tensão SuperficialNatália CataniBelum ada peringkat
- Fundamentação TeóricaDokumen2 halamanFundamentação TeóricaLucas Sousa TintiBelum ada peringkat
- Compostos ComplexosDokumen14 halamanCompostos ComplexosAlbino José JoaquimBelum ada peringkat
- Estrutura Do CarbonoDokumen21 halamanEstrutura Do CarbonofernandoalvesjrBelum ada peringkat
- Lista Funcoes InorganicasDokumen7 halamanLista Funcoes InorganicasAmanda LouresBelum ada peringkat
- Texto LuckesiDokumen6 halamanTexto LuckesiMarlapbBelum ada peringkat
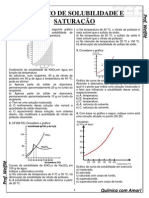
- Coeficiente de Solubilidade e Tipos de SaturaçãoDokumen5 halamanCoeficiente de Solubilidade e Tipos de SaturaçãoWelff Junior100% (2)
- Apostila Do 2 Ano Noturno QuimicaDokumen34 halamanApostila Do 2 Ano Noturno QuimicacatilioBelum ada peringkat
- Métodos de Separação PDFDokumen31 halamanMétodos de Separação PDFDébora GuimarãesBelum ada peringkat
- Operacoes Unitarias - PETROBRASDokumen78 halamanOperacoes Unitarias - PETROBRASEduardo CastroBelum ada peringkat
- Propriedade QuímicasDokumen13 halamanPropriedade QuímicasEder Cezano GonçalvesBelum ada peringkat
- Propriedades ColigativasDokumen20 halamanPropriedades ColigativasAlessandra CarolinaBelum ada peringkat
- TonosDokumen8 halamanTonosCYNARA MAIRA JERONIMO DE PAULABelum ada peringkat
- Química PPT - Reações de SubstituiçãoDokumen26 halamanQuímica PPT - Reações de SubstituiçãoQuímica PPT100% (2)
- Química PPT - Origem Da VidaDokumen17 halamanQuímica PPT - Origem Da VidaQuímica PPT100% (1)
- Química PPT - SaisDokumen35 halamanQuímica PPT - SaisQuímica PPT100% (4)
- Química PPT - CASD - Moleculas - Geometria MolecularDokumen10 halamanQuímica PPT - CASD - Moleculas - Geometria MolecularQuímica PPT100% (1)
- Química PPT - Origem Do UniversoDokumen13 halamanQuímica PPT - Origem Do UniversoQuímica PPT100% (1)
- Química RG PPT - Substancias Puras e MisturasDokumen18 halamanQuímica RG PPT - Substancias Puras e MisturasQuímica PPT100% (4)
- Química RG PPT - Cinética QuímicaDokumen6 halamanQuímica RG PPT - Cinética QuímicaQuimica Passei100% (1)
- Química PPT - Teorema de Energia CinéticaDokumen12 halamanQuímica PPT - Teorema de Energia CinéticaQuímica PPT100% (1)
- Química PPT - Soluções - TampãoDokumen16 halamanQuímica PPT - Soluções - TampãoQuímica PPT100% (3)
- Quimica Tabela Distribuicao EletronicaDokumen4 halamanQuimica Tabela Distribuicao EletronicaluklinkinBelum ada peringkat
- Química PPT - Reações Orgânicas IIDokumen58 halamanQuímica PPT - Reações Orgânicas IIQuímica PPT100% (2)
- Química PPT - Propriedades ColigativasDokumen18 halamanQuímica PPT - Propriedades ColigativasQuímica PPT100% (2)
- Química PPT - Solução Aquosa - PH e POH 02Dokumen10 halamanQuímica PPT - Solução Aquosa - PH e POH 02Química PPTBelum ada peringkat
- Química PPT - Modelos AtômicosDokumen20 halamanQuímica PPT - Modelos AtômicosQuímica PPT100% (3)
- Química PPT - Geometria Das MoléculasDokumen10 halamanQuímica PPT - Geometria Das MoléculasQuímica PPTBelum ada peringkat
- Química PPT - Polaridade Da Ligação CovalenteDokumen19 halamanQuímica PPT - Polaridade Da Ligação CovalenteQuímica PPTBelum ada peringkat
- Reações OrganicasDokumen55 halamanReações OrganicasEraclitoSL100% (11)
- Química PPT - Reações Orgânicas - ClassificaçãoDokumen54 halamanQuímica PPT - Reações Orgânicas - ClassificaçãoQuímica PPT100% (4)
- Química PPT - HidrocarbonetosDokumen8 halamanQuímica PPT - HidrocarbonetosQuímica PPTBelum ada peringkat
- Química PPT - Isomeria GeométricaDokumen14 halamanQuímica PPT - Isomeria GeométricaQuímica PPTBelum ada peringkat
- Química PPT - Orgânica - IsomeriaDokumen21 halamanQuímica PPT - Orgânica - IsomeriaQuímica PPT100% (4)
- Química PPT - Polaridade Da Ligação CovalenteDokumen19 halamanQuímica PPT - Polaridade Da Ligação CovalenteQuímica PPTBelum ada peringkat
- Química PPT - Gases PerfeitosDokumen13 halamanQuímica PPT - Gases PerfeitosQuímica PPT100% (1)