Preparasi Fisik-Kimia - PBG II
Diunggah oleh
Brian ThomasJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Preparasi Fisik-Kimia - PBG II
Diunggah oleh
Brian ThomasHak Cipta:
Format Tersedia
PREPARASI
FISIK (AGGLOMERASI)
KIMIA
OLEH
UNTUNG SUKAMTO
SUDARYANTO
AGGLOMERASI
PRINSIP AGGLOMERATION ADALAH
MATERIAL YANG HALUS , DITAMBAH
BINDER (PEREKAT), DIPANASKAN
SAMPAI PERMUKAAN MELELEH,
AKHIRNYA MENGGUMPAL.
SINTERING
PELLETIZING
BRIQUETING
NODULIZING
SINTERING
UNTUK MEMPRODUKSI SPONGY COKE
(CAMPURAN BESI DENGAN COKE)
MATERIAL, BAHAN BAKAR DAN AIR
DICAMPUR, KEMUDIAN DIPANASKAN DI
BAWAH TITIK LELEH NYA
APABILA DIDINGINKANAKAN SALING
MENGIKAT
JIKA AIRNYA MENGUAP , MENYEBABKAN
BAHAN MENJADI POROUS
ALAT YANG DIGUNAKAN ADALAH
SINTERING GRATE
SINTERING GRATE
5 % COKE, 5-10 % AIR, LAINNYA BESI
PEMANASAN DILAKUKAN DI ATAS
PEMANAS
SINTER MIX
GRATE
DIHISAP
SETELAH DICETAK , DIREMUK, DIAYAK YANG
TIDAK MEMENUHI UKURAN DICETAK KEMBALI
5 % COKE, 5-10 % AIR, LAINNYA BESI
PEMANASAN DILAKUKAN DI ATAS
PEMANAS
SINTER MIX
GRATE
DIHISAP
SETELAH DICETAK , DIREMUK, DIAYAK YANG TIDAK
MEMENUHI UKURAN DICETAK KEMBALI
5 % COKE, 5-10 % AIR, LAINNYA BESI
PEMANASAN DILAKUKAN DI ATAS
PEMANAS
SINTER MIX
GRATE
DIHISAP
SETELAH DICETAK , DIREMUK, DIAYAK YANG TIDAK
MEMENUHI UKURAN DICETAK KEMBALI
5 % COKE, 5-10 % AIR, LAINNYA BESI
PEMANASAN DILAKUKAN DI ATAS
PEMANAS
SINTER MIX
GRATE
DIHISAP
SETELAH DICETAK , DIREMUK, DIAYAK YANG TIDAK
MEMENUHI UKURAN DICETAK KEMBALI
BRIQUETING
MATERIAL HALUS DICAMPUR BINDER
(TER, COKE, LIME , CLAY)
DICETAK DALAM BENTUK KUBUS,
TANPA PEMANASAN
DAPAT DILAKUKAN PEMANASAN,
DENGAN REAKSI :
2 ZnS + C + 4 O
2
2 ZnO + CO
2
+ 2SO
2
PELLETIZING
MATERIAL HALUS 200 #, DIGUMPALKAN
MENJADI 10-30 MM, PALING KECIL 3 MM
MATERIAL DITAMBAH AIR, DAN CLAY
DIMASUKKAN KE ALAT ROTARY DISC
ATAU PAN PELLETIZING
DIBAKAR SAMPAI 1200 1300
O
C.
AIR MENGUAP, MATERIAL POROUS
BERBENTUK PELLET ( GULING)
NODULIZING
SEPERTI PEMBUATAN KLINKER SEMEN
DENGAN CARA DIPANASKAN SAMBIL
DIPUTAR (TANUR PUTAR)
2 Zn (OH)
2
(halus) ZnO (kasar) + H
2
O
ZnO MENGGUMPAL DAN KEADAANNYA
POROUS
PREPARASI KIMIA
ADALAH PEKERJAAN PERSIAPAN
UMPAN AGAR DAPAT DENGAN MUDAH
MEMBANTU PROSES SELANJUTNYA
YANG BERKAITAN DENGAN PROSES
KIMIA
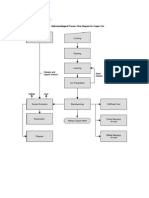
PREPARASI KIMIA MELIPUTI :
PENGERINGAN (DRYING), KALSINASI
( CALCINING), PEMANGGANGAN
(ROASTING)
PENGERINGAN
BERTUJUAN MENGHILANGKAN
KANDUNGAN AIR BEBAS (MOISTURE)
SAMPAI TEMPERATUR 110
O
C
BERMAKSUD MENGHINDARI PENGUAPAN
DALAM JUMLAH BESAR YANG
KEMUNGKINANNYA MEMBAWA LOGAM
BERHARGA, DAN SEBAGIAN KALOR PASTI
DIGUNAKAN UTK MENGUAP KAN AIR.
PENGERINGAN DPT DENGAN GAS BUANG
PANAS, DAN DILAKUKAN DALAM ROTARY
KILN
KALSINASI
PROSES PEMANASAN TANPA TERJADI
PELEBURAN DAN TANPA PENAMBAH AN
REAGENT
TUJUAN : MENGUBAH SENYAWA KIMIA
(KARBONAT, AIR KRISTAL, HIDROKSIDA,
DESAGREGASI BIJIH KOMPAK)
PENGURAIAN KARBONAT
MCO
3
(p) MO (p) + CO
2
(g)
CaCO
3
CaO + CO
2
( 900 1100
O
C )
FeCO
3
FeO + CO
2
( 200
O
C)
PENGHILANGAN AIR KRISTAL DAN
PENGURAIAN HIDROKSIDA (PADA
KALSINASI)
AIR KRISTAL ADALAH MOLEKUL H
2
O
TERIKAT SECARA KIMIA DENGAN
SENYAWA OKSIDA TERTENTU
REAKSI PENGHILANGAN AIR KRISTAL
M(OH)
2
MO + H
2
O
Mg(OH)
2
MgO + H
2
O (200
O
C)
2 Al(OH)
3
Al
2
O
3
+ 3 H
2
O (1000 1100
O
C)
PEMANGGANGAN
PROSES PEMANASAN BIJIH TANPA
PELELEHAN YANG DISERTAI PENAMBAHAN
REAGENT (GAS) DENGAN TUJUAN
MENGUBAH SENYAWA SULFIDA MENJADI
SENYAWA LAIN ( OKSIDA, SULFAT, METAL)
DLL.
PEMANGGANGAN TERMASUK PREPARASI
KIMIA, TAPI DAPAT JUGA SEBAGAI PROSES
EKSTRAKSI, MAUPUN SEBAGAI PROSES
PEMURNIAN
PEMANGGANGAN
(Roasting)
Oksidasi Reduksi Khloridisasi Khusus
Oksida Sulfatisasi Metalisasi
Parsial Sempurna
PEMANGGANGAN OKSIDASI
SECARA TERMODINAMIKA PEMANGGANGAN
OKSIDASI TERHADAP LOGAM SULFIDE
DAPAT DIATUR SEHINGGA DIDAPAT : LOGAM
OKSIDA, LOGAM SULFAT, LOGAM
UNTUK MENENTUKAN KONDISI YANG TEPAT
BAGI PEMBENTUK PRODUK, PERLU DITINJAU
HUBUNGAN KESETIMBANGAN SYSTEM :
LOGAM, BELERANG, OKSIGEN.
HUBUNGAN KESETIMBANGAN SYSTEM :
LOGAM, BELERANG DAN OKSIGEN
DIPENGARUHI OLEH TEKANAN O
2
DAN SO
2
SEHINGGA UNTUK MENENTUKAN PRODUK
DARI PEMANGGANGAN OKSIDASI DAPAT
DILIHAT PADA SUATU DIAGRAM KELLOG
DIAGRAM KELLOG
(5)
(6)
(2)
(4)
(1)
(3)
(8)
MO
M
MO.SO
4
MSO
4
MS
+
0
-
0
+
-
CATATAN : P.S
2
= 1 Atm (Pers.4)
P.SO
3
= 1 Atm (Pers.5)
Log P.SO
2
Log P.O
2
(7)
2 MS + 3 O
2
2 MO + 2 SO
2
.. (1)
MS + 2 O
2
MSO
4
(2)
MS + O
2
M + SO
2
(3)
2 S + 2O
2
2 SO
2
. (4)
2 SO
2
+ O
2
2 SO
3
. (5)
4 MSO
4
2 MO.MSO
4
+ 2 SO
2
+ O
2
(6)
2 MO.MSO
4
4 MO + 2 SO
2
+ O
2
.. (7)
2 MO 2 M + O
2
(8)
PEMANGGANGAN OKSIDASI
MENGHASILKAN LOGAM OKSIDA
PEMANGGANGAN OKSIDA, MENGUBAH
SENYAWA SULFIDA MENJADI OKSIDA.
2 ZnS + 3 O
2
2 ZnO + 2 SO
3
2 FeS
2
+ 5,5 O
2
Fe
2
O
3
+ 4 SO
2
PEMANGGANGAN MENGHASILKAN
OKSIDA ADA DUA MACAM, YAITU :
OKSIDA SEMPURNA DAN SEBAGIAN
PEMANGGANGAN OKSIDA
SEMPURNA
MENGHILANGKAN SEMUA KANDUNG AN
BELERANG (S) DAN DIUBAH MENJADI
OKSIDA, DENGAN TUJUAN :
ZnS, PbS DIUBAH ZnO dan PbO KARENA AKAN
MUDAH BILA DIREDUKSI
ADA LOGAM JIKA BERBENTUK SENYAWA
OKSIDA AKAN MUDAH MENGUAP ( As
2
O
3
,
Sb
2
O
3
), dijaga jangan membentuk oksida yang lebih
tinggi, sebab akan stabil dan wujudnya padat
PEMANGGANGAN OKSIDA
SEBAGIAN
DIUSAHAKAN LOGAM UTAMANYA TETAP
SENYAWA SULFIDA, SEDANG
PENGOTORNYA DIUBAH MENJADI OKSIDA,
PROSES OKSIDASI BERSIFAT SELEKTIF.
DALAM PROSES TEMBAGA, CuS
DIUSAHAKAN TETAP, FeS SEBAGIAN DIUBAH
MENJADI FeO LARI KE SLAG
BILA SEMUA FeS FeO, ADA KEMUNGKINAN
CuS ADA YANG MENJADI CuO SLAG
CuO + FeS CuS + FeO
PEMANGGANGAN SULFATISASI
MENGUBAH SENYAWA SULFIDA
MENJADI SENYAWA SULFAT DENGAN
TUJUAN AGAR MUDAH DILARUTKAN
DENGAN AIR (DALAM HYDRO
METALLURGY)
TEMPERATUR PENGURAIAN SULFAT
BERBAGAI LOGAM : FeSO
4
(550
O
C),
CuSO
4
(700
O
C), ZnSO
4
(750
O
C),
PbSO
4
( > 1000
O
C )
PEMANGGANGAN METALISASI
PEMANGGANGAN TERHADAP SULFIDA AGAR
DIDAPAT LOGAM DENGAN CARA OKSIDASI PADA
TEMPERATUR TINGGI
SYARAT PEMANGGANGAN METALISASI ADALAH:
LOGAM YANG AKAN DIPANGGANG HRS LEBIH
STABIL DARI LOGAM OKSIDA MAUPUN LOGAM
SULFAT
HgS + O
2
Hg + SO
2
Hg LEBIH STABIL DARIPADA HgO MAUPUN HgSO
4
TEKANAN UAP LOGAM CUKUP TINGGI (Hg = 500
800
O
C) BERUPA UAP
PEMANGGANGAN REDUKSI
PEMANGGANGAN DENGAN PENAMBAHAN
REDUKTOR SEPERTI C, H
2
, CH
4
, DENGAN TUJUAN
MENURUNKAN DERAJAT OKSIDA, MEREDUKSI BIJIH
/ KONSENTRAT, ROASTING MAGNETISASI (DALAM
KONSENTRAT TIMAH)
DALAM PROSES HYL, YANG MENGGUNAKAN
REDUKTOR GAS CH
4
GAS CH4 DIREFORMASI DAHULU :
CH
4
+ H
2
) CO + 3 H
2
CO + H
2
O CO
2
+ H
2
Fe
2
O
3
+ 3 H
2
2 Fe + 3 H
2
O
Fe
2
O
3
+ 3 CO 2 Fe + 3 CO
2
PEMANGGANGAN KLORIDISASI
MENGUBAH SENYAWA LOGAM MENJADI
SENYAWA KLORIDA, DENGAN TUJUAN AGAR
MUDAH LARUT DALAM AIR (PREPARASI
HYDROMETALLURGY), DISAMPING ITU AGAR
LOGAM MUDAH MENGUAP, DAPAT
DIPISAHKAN DENGAN KOTORANNYA.
MS + 2 NaCl + 2O
2
Na
2
SO
4
+ MCl
2
REAKSI PEMANGGANGAN KLODISASI
MENGHASILKAN UAP :
MO + CaCl
2
MCl
2
+ CaO
Tahap 1 : MS + CaCl
2
+ 0,5 O
2
MCl
2
+ CaO + SO
2
.
Tahap 2 : MO + Cl
2
MCl
2
+ 0,5 O
2
MS + Cl
2
+ O
2
MCl
2
+ SO
2
PEMANGGANGAN KHUSUS
PEMANGGANGAN NIKEL PADA MOND
PROCESS SEHINGGA MENGHASILKAN
GAS YANG DISEBUT NIKEL CARBONIL.
PEMANGGANGAN TERJADI PADA
TEMPERATUR 43
O
C
Ni + 4 CO Ni ( CO)
4
(nikel carbonil dalam
bentuk uap)
Anda mungkin juga menyukai
- Temperatur EfektifDokumen2 halamanTemperatur EfektifBrian ThomasBelum ada peringkat
- Hidrometalurgi TembagaDokumen3 halamanHidrometalurgi TembagaBrian Thomas100% (1)
- Trigonometri SubstitusiDokumen10 halamanTrigonometri SubstitusiBrian ThomasBelum ada peringkat
- Mekanisme JigDokumen10 halamanMekanisme JigBrian ThomasBelum ada peringkat
- Istilah Dalam Pertambangan 1Dokumen3 halamanIstilah Dalam Pertambangan 1Brian ThomasBelum ada peringkat
- Gambar Jaw Crusher Dan BagianDokumen2 halamanGambar Jaw Crusher Dan BagianBrian Thomas0% (1)
- Gas MetanaDokumen3 halamanGas MetanaBrian ThomasBelum ada peringkat
- Proses Pembentukan BatubaraDokumen30 halamanProses Pembentukan BatubaraBrian ThomasBelum ada peringkat