Hidrolisa Polisakarida
Hidrolisa Polisakarida
Diunggah oleh
andriadistiaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Hidrolisa Polisakarida
Hidrolisa Polisakarida
Diunggah oleh
andriadistiaHak Cipta:
Format Tersedia
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
I PENDAHULUAN
Bab ini akan menguraikan mengenai : (1) Latar Belakang
Percobaan, (2) Tujuan Percobaan, (3) Prinsip Percobaan, dan
(4) Reaksi Percobaan.
1.1. Latar Belakang Percobaan
Pati merupakan cadangan makanan yang terdapat di
dalam biji-bijian atau umbi-umbian. Pati merupakan
homopolimer glukosa dengan ikatan -glikosidik. Berbagai
macam pati tidak sama sifatnya, tergantung dari panjang
rantai C-nya, serta apakah lurus atau bercabang rantai
molekulnya. Pati terdiri dari dua fraksi yang dapat dipisahkan
dengan air panas, yaitu:
A. Amilosa, merupakan fraksi yang terlarut dalam air panas
yang mempunyai struktur lurus dengan ikatan -1,4-Dglukosa.
B. Amilopektin, merupakan fraksi yang tidak larut dalam air
panas dan mempunyai struktur bercabang dengan ikatan 1,6-D-glukosa. (Winarno, 2004)
1.2. Tujuan Percobaan
Untuk membuktikan susunan polisakarida terdiri dari
beberapa monosakarida.
1.3.
Prinsip Percobaan
Berdasarkan polisakarida yang dihidrolisa oleh asam
akan terurai menjadi monosakarida.
Laboratorium Biokimia Pangan
1.4.
Karbohidrat II (Hidrolisa Suatu Polisakarida)
Reaksi Percobaan
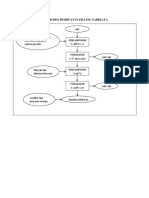
Gambar 4. Reaksi Percobaan Hidrolisa Suatu Polisakarida
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
II METODE PERCOBAAN
Bab ini akan menguraikan mengenai : (1) Bahan yang
Digunakan, (2) Pereaksi yang Digunakan, (3) Alat yang
Digunakan, dan (4) Metode Percobaan.
2.1. Bahan yang digunakan
Bahan yang digunakan
Polisakaridaadalah Amilum.
dalam
Hidrolisa
Suatu
2.2. Pereaksi yang digunakan
Pereaksi yang digunakan dalam Hidrolisa
Polisakarida adalah larutan HCl 3M dan larutan I2.
Suatu
2.3. Alat yang digunakan
Alat yang digunakan dalam Hidrolisa Suatu Polisakarida
adalah tabung reaksi, pipet, plat tetes dan penangas air.
2.4. Metode Percobaan
KI/I
2
Gambar 5. Metode Percobaan Hidrolisa Suatu Polisakarida
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
III HASIL PENGAMATAN
Bab ini akan menguraikan mengenai : (1) Hasil
Pengamatan dan (2) Pembahasan.
3.1. Hasil Pengamatan
Tabel 3. Hasil Pengamatan Hidrolisa Suatu Polisakarida
Sampel Pereaksi Waktu Warna Hasil Keteranga
n
0
Ungu
+++
5
Ungu
+++
Amilodext
10
Ungu
+++
rin
15
Ungu
+++
20
Ungu
+++
HCl 3M +
25
Merah
++
Amilum
Erythodex
30
Merah
++
I2
35
Merah
++
trin
40
Merah
++
45
Kuning
+
Erythodex
50
Kuning
+
trin
55
Kuning
+
Sumber : Andri Adistia dan Wina Yesica, Kelompok D, Meja 1,
2015.
Keterangan :
(+++) Amilodekstrin
(++) Erythrodekstrin
(+) Achrodekstrin
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
Gambar 6. Hasil Pengamatan Hidrolisa Suatu Polisakarida
3.2. Pembahasan
Berdasarkan hasil pengamatan pada uji hidrolisa suatu
polisakarida didapatkan hasil dari waktu 020 membentuk
amilodekstrin, 2540 membentuk eritrodekstrin dan 4555
membentuk akrodekstrin.
Fungsi larutan HCl dalam percobaan ini yaitu untuk
membentuk suasana asam pada sampel amylum karena
dalam keadaan asam amylum akan mudah terhidrolisis
menjadi senyawa-senyawa sederhana. Sedangkan fungsi
pemanasan yaitu untuk mempercepat proses jalannya reaksi.
Fungsi penambahan KI/I2 adalah sebagai indikator yang
spesifik untuk mengetahui apakah amylum sudah terhidrolisis
atau belum.
Fungsi perlakuan pada percobaan ini salah satunya yaitu,
pemanasan yang berfungsi menghidrolisis larutan pati.
Larutan pati sendiri merupakan amilum yang termasuk
golongan polisakarida. Polisakarida ini akan terhidrolisis
menjadi monosakarida.
Pati yang berikatan dengan iodin (I 2) akan menghasilkan
warna biru. Sifat ini dapat digunakan untuk menganalisis
adanya pati. Hal ini disebabkan oleh struktur molekul pati yang
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
berbentuk spiral, sehingga akan mengikat molekul iodin dan
terbentuklah warna biru. Bila pati dipanaskan, spiral
merenggang, molekul-molekul iodin terlepas sehingga warna
biru menghilang. Dari percobaan-percobaan didapat bahwa
pati akan merefleksikan warna biru bila berupa polimer
glukosa yang lebih besar dari dua puluh, misalnya molekul
amilosa (Winarno, 1992)
Hidrolisis adalah jenis reaksi kimia yang terjadi antara air
dan senyawa lain. Selama reaksi, ikatan kimia akan rusak di
kedua molekul, menyebabkan mereka menjadi pecah. Molekul
air terpecah untuk membentuk ion hidrogen bermuatan positif
(H +) dan hidroksida bermuatan negatif (OH-), dan molekul
lainnya terbagi menjadi dua bagian sederhana, juga dengan
muatan positif dan negatif. Ion H + dan OH- melekat pada
masing-masing bagian ini (wikipedia,2015).
Amilum terdiri dari dua macam polisakarida yang keduaduanya adalah polimer dari glukosa, yaitu amilosa (kira-kira
20-28%) dan sisanya amilopektin. Amilosa terikat dengan
ikatan alpa-1,4-glikosidik, jadi molekulnya merupakan rantai
terbuka. Amilopektin terikat dengan ikatan yang sebagian
besar 1,4-glikosidik dan sebagian lagi 1,6-glikosidik. Adanya
ikatan 1,6-glikosidik ini menyebabkan terjadinya cabang,
sehingga amilopektin berbentuk terbuka dan bercabang.
Molekul amilopektin lebih besar daripada molekul amilosa
karena terdiri atas lebih dari 1000 unit glukosa. Butir-butir pati
tidak larut dalam air dingin tetapi apanila suspensi dalam air
dipanaskan, akan terjadi suatu larutan koloid yang kental.
Larutan koloid ini apabila diberi larutan iodium akan berwarna
biru. Warna biru tersebut disebabkan oleh molekul amilosa
yang membentuk senyawa. Amilopektin dengan iodium akan
memberikan warna ungu atau merah lembayung (Poedjiadi,
1996).
Dekstrin adalah hasil antara pada proses hidrolisis
amilum sebelum terbentuk maltosa. Tahaptahap dalam
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
proses hidrolisis amilum serta warna yang terjadi pada reaksi
dengan iodium adalah sebagai berikut :
(Poedjiadi, 1996).
Sifat dari I2 yaitu menguap pada suhu kamar menjadi gas
ungu biru dengan bau menyengat. Iod membentuk senyawa
dengan banyak unsur, tapi tidak sereaktif halogen lainnya,
yang kemudian menggeser iodida. Iod menunjukkan sifat-sifat
menyerupai logam. Iod mudah larut dalam kloroform, karbon
tetraklorida, atau karbon disulfida yang kemudian membentuk
larutan berwarna ungu yang indah. Iod hanya sedikit larut
dalam air (Risma,2014).
Penambahan I2 terlebih dulu sebelum amilum dapat
berpengaruh karena sifat dari I 2 sendiri yang mudah menguap
sehingga jika I2 ditambahkan terlebih dulu hasilnya tidak akan
efektif.
Faktor kesalahan yang dapat terjadi pada percobaan ini
yaitu kesalahan pengamatan warna, penambahan I 2 yang
terlebih dahulu sehingga I2 sudah menguap dan kontaminasi
dari alat yang kurang bersih.
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
IV KESIMPULAN DAN SARAN
Bab ini akan menguraikan mengenai : (1) Kesimpulan
dan (2) Saran.
4.1. Kesimpulan
Berdasarkan hasil pengamatan pada uji hidrolisa suatu
polisakarida didapat dari waktu 0 20 membentuk
amilodextrin, 25 40 membentuk erythodextrindan 45 55
membentuk achrodextrin.
4.2. Saran
Saran dalam uji hidrolisa polisakarida harusnya ada
penangas air tambah karena penangas air yang ada
digunakan juga pada uji lain sehingga menumpuk.
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
DAFTAR PUSTAKA
Anonim. 2015. Hidrollisis. id.wikipedia.org. Diakses 16 Maret
2015.
Poedjiadi, Anna. 2005. Dasar-dasar Biokimia. Penerbit
Universitas Indonesia : Jakarta
Risma.
2014.
Uji
http://rismasriayu.blogspot.com.
2015.
Phenylhidrazine.
Diakses 16 Maret
Winarno, F.G. 1992. Kimia Pangan dan Gizi. Percetakan PT
Gramedia : Jakarta
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
LAMPIRAN 1
Hasil Laboratorium Biokimia Pangan
Sam
pel
Tabel 4. Uji Hidrolisa Polisakarida
Pereak Wakt
Has Keterang
Warna
si
u
il
an
0
Ungu
+++
5
Ungu
+++
10
Ungu
+++
15
Ungu
+++
20
Merah
++
Amilu HCl 3m
25
Merah
++
m
+ I2
30
Merah
++
35
Merah
++
40
Merah
++
45
Kuning
+
50
Kuning
+
55
Kuning
+
Sumber : Laboratorium Biokimia Pangan, 2015.
Amilodext
rin
Erythodex
trin
Achrodext
rin
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
LAMPIRAN 2
Soal modul praktikum Uji Hidrolisa Polisakarida.
1. Tuliskan reaksi hidrolisis dari gula disakarida !
2. Peristiwa hidrolisa juga disebut peristiwa?
Hidrolisis adalah jenis reaksi kimia yang terjadi antara air
dan senyawa lain. Selama reaksi, ikatan kimia akan rusak di
kedua molekul, menyebabkan mereka menjadi pecah.
Molekul air terpecah untuk membentuk ion hidrogen
bermuatan positif (H +) dan hidroksida bermuatan negatif
(OH-), dan molekul lainnya terbagi menjadi dua bagian
sederhana, juga dengan muatan positif dan negatif. Ion H +
dan OH- melekat pada masing-masing bagian ini.
3. Jelaskan faktor-faktor yang mempengaruhi hidrolisis !
Proses hidrolisis ini dipengaruhi oleh beberapa faktor,
diantaranya :
pH (derajat keasaman)
pH mempengaruhi proses hidrolisis sehingga dapat
dihasilkan hidrolisis yang sesuai dengan yang diinginkan. pH
yang
baik
untuk
proses
hidrolisis
adalah
2,3.
(Soebijanto,1986).
Suhu
Laboratorium Biokimia Pangan
Suhu juga
hidrolisis. Suhu
sekitar 21 oC
Konsentrasi
Konsentrasi
hidrolisis asam
H2SO4 pekat.
Karbohidrat II (Hidrolisa Suatu Polisakarida)
mempengaruhi proses kecepatan reaksi
yang baik untuk hidrolisis selulosa adalah
mempengaruhi laju reaksi hidrolisis. Untuk
digunakan konsentrasi HCl pekat atau
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
LAMPIRAN 3
Quis
1. Jelaskan tujuan dan prinsip Uji Phenylhidrazine !
Tujuan Percobaan
Untuk mengetahui adanya gula aldosa atau ketosa pada
bahan pangan.
Prinsip Percobaan
Berdasarkan reaksi antara gugus karbonil dari aldehid
atau gugus keton bebas bersama phenylhidrazine berlebih
dalam suasana panas akan membentuk senyawa osazon.
2. Jelaskan tujuan dan prinsip Uji Moore !
Tujuan Percobaan
Untuk mengetahui terjadinya sifat karamelisasiyang
ditandai dengan bau dan warna yang khas.
Prinsip Percobaan
Berdasarkan oksidasi dan pemanasan senyawa
karbohidrat yang menghasilkan senyawa kompleks berwarna
coklat dengan bau yang khas (bau karamel).
3. Jelaskan tujuan dan prinsip Uji Hidrolisa suatu
polisakarida !
Tujuan Percobaan
Untuk membuktikan susunan polisakarida terdiri dari
beberapa monosakarida.
Prinsip Percobaan
Berdasarkan polisakarida yang dihidrolisa oleh asam
akan terurai menjadi monosakarida.
4. Jelaskan perbedaan hidrazin dan osazon!
Perbedaan hidrazon dengan osazon yaitu hidrazon dapat
larut dalam air karena hidrazon merupakan substansi yang
Laboratorium Biokimia Pangan
Karbohidrat II (Hidrolisa Suatu Polisakarida)
mudah larut dalam air (soluble) dan sulit diisolasi. Sedangkan
pada osazon rekatif tidak larut dan membentuk kristal yang
berbentuk spesifik untuk setiap jenis sakarida.
5. Jelaskan kenapa sukrosa hasilnya negatif !
Sukrosa memberikan hasil negatif karena pada molekul
sukrosa terdapat ikatan antara molekul glukosa dan fruktosa,
yaitu antara atom karbon nomor 1 pada glukosa dengan atom
karbon nomor 2 pada fruktosa melalui atom oksigen. Kedua
atom tersebut adalah tom karbon yang mempunyai gugus
OH glikosidik, atau atom karbon yang merupakan gugus
aldehida pada glukosa dan gugus keton pada fruktosa. Oleh
karena itu molekul sukrosa tidak mempunyai gugus aldehida
atau keton bebas, atau tidak mempunyai gugus OH
glikosidik.
Anda mungkin juga menyukai
- Sop Proses Pembuatan Selai SarikayaDokumen6 halamanSop Proses Pembuatan Selai SarikayaandriadistiaBelum ada peringkat
- II Tinjauan Umum RecDokumen15 halamanII Tinjauan Umum RecandriadistiaBelum ada peringkat
- I PendahuluanDokumen17 halamanI PendahuluanandriadistiaBelum ada peringkat
- Laporan Cuka ApelDokumen17 halamanLaporan Cuka ApelandriadistiaBelum ada peringkat
- Produk YoghurtDokumen14 halamanProduk YoghurtandriadistiaBelum ada peringkat
- Produk Makanan Dalam NegeriDokumen5 halamanProduk Makanan Dalam Negeriandriadistia100% (1)
- Laporan Kiman Uji NyalaDokumen6 halamanLaporan Kiman Uji NyalaandriadistiaBelum ada peringkat
- Laporan TPP Minyak KelapaDokumen10 halamanLaporan TPP Minyak KelapaandriadistiaBelum ada peringkat
- Uji Konsentrasi Substrat SILDokumen16 halamanUji Konsentrasi Substrat SILandriadistiaBelum ada peringkat
- Prinsip-Prinsip Cara Penentuan Batasan Maksimu BTMDokumen21 halamanPrinsip-Prinsip Cara Penentuan Batasan Maksimu BTMandriadistiaBelum ada peringkat
- Sterilisasi GammaDokumen2 halamanSterilisasi Gammaandriadistia100% (1)
- Ion ExchangeDokumen45 halamanIon ExchangeandriadistiaBelum ada peringkat
- Manajemen ProduksiDokumen12 halamanManajemen ProduksiandriadistiaBelum ada peringkat
- BAB III FixDokumen11 halamanBAB III FixandriadistiaBelum ada peringkat