Patofisiologi Gagal
Diunggah oleh
rafie odong-odong0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
13 tayangan3 halamanchf
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOC, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Inichf
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
13 tayangan3 halamanPatofisiologi Gagal
Diunggah oleh
rafie odong-odongchf
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 3
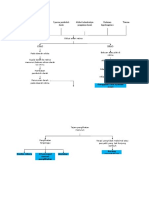
Patofisiologi Gagal jantung
Patofisiologi CHF terjadi karena in
teraksi kompleks antara faktor-faktor
yang memengaruhi kontraktilitas, after load, preload, atau fungsi lusitropik (fungsi
relaksasi) jantung, dan respons neurohormonal dan hemodinamik yang diperlukan
untuk menciptakan kompensasi sirkulasi. Meskipun konsekuensi hemodinamik gagal
jantung berespons terhadap intervensi farmakologis standar, terdapat interaksi
neurohormonal kritis yang efek gabungannya memperberat dan memperlama sindrom
yang ada.
Sistem reniniangiotensinfaldosteron (RAA): Selain untuk meningkatkan tahanan
perifer dan volume darah sirkulasi, angiotensin dan aldosteron berimplikasi pada
perubahan struktural miokardium yang terlihat pada cedera iskemik dan
kardiomiopati hipertropik hipertensif. Perubahan ini meliputi remodeling miokard
dan kematian sarkomer, kehilangan matriks kolagen normal, dan fibrosis interstisial.
Terjadinya miosit dan sarkomer yang tidak dapat mentransmisikan kekuatannya,
dilatasi jantung, dan pembentukan jaringan parut dengan kehilangan komplians
miokard normal turut memberikan gambaran hemodinamik dan simtomatik pada
CHF.
Sistem saraf simpatis (SNS): Epinefrin dan norepinefrin menyebabkan peningkatan
tahanan perifer dengan peningkatan kerja jantung, takikardia, peningkatan konsumsi
oksigen oleh miokardium, dan peningkatan risiko aritmia. Katekolamin juga turut
menyebabkan remodeling ventrikel melalui toksisitas langsung terhadap miosit,
induksi apoptosis miosit, dan peningkatan respons autoimun.
Vasodilator endogen, seperti endotelin dan oksida nitrat, peptida jantung, dan peptida
natriuretik: Perannya dalam CHF sedang diselidiki dan intervensinya sedang diuji.
- Sitokin imun dan inflamasi: Faktor nekrosis tumor alfa (TNFa) dan interleukin 6
(IL-6) menyebabkan remodeling ventrikel dengan apoptosis miosit, dilatasi ventrikel,
dan penurunan kontraktilitas. Lebih lanjut, mereka juga berperan dalam efek sistemik
seperti penurunan berat badan dan kelemahan yang terlihat pada CHF brat (kakheksia
jantung).
Kejadian etiologi awal memengaruhi respons awal miokardium, tetapi seiring
dengan perkembangan sindrom, mekanisme umum mulai muncul sehingga pasien
CHF lanjut memperlihatkan gejala dan respons yang sama terhadap intervensi
farmakologis yang sama apapun penyebab awal CHF-nya.
Meskipun banyak pasien mengalami disfungsi ventrikel kiri sistolik dan diastolik,
kategori ini sebaiknya dianggap sebagai hal yang berbeda untuk dapat memahami
efeknya terhadap homeostasis sirkulasi dan responsnya terhadap berbagai intervensi.
Disfungsi ventrikel kiri sistolik
1) Penurunan curah jantung akibat penurunan kontraktilitas, peningkatan afterload,
atau peningkatan preload yang mengakibatkan penurunan fraksi ejeksi dan
peningkatan volume akhir diastolik ventrikel kiri (LVEDV). Ini meningkatkan
tekanan akhir diastolik pada ventrikel kiri (I-VEDP) dan menyebabkan kongesti vena
pulmonal dan edema paru.
2) Penurunan kontraktilitas (inotropi) terjadi akibat fungsi miokard yang tidak
adekuat atau tidak terkoordinasi schingga ventrikel kiri tidak dapat melakukan ejeksi
lebih dari 60% dari volume akhir diastoliknya (LVEDV). lni menyebabkan
peningkatan bertahap LVEDV (juga dinamakan preload) mengakibatkan peningkatan
LVEDP dan kongesti vena pulmonalis. Penyebab penurunan kontraktilitas yang
tersering adalah penyakit jantung iskemik, yang tidak hanya mengakibatkan nekrosis
jaringan miokard sesungguhnya, tetapi juga menyebabkan remodeling ventrikel
iskemik. Remodeling iskemik adalah sebuah proses yang sebagian dimediasi oleh
angiotensin II (ANG II) yang menyebabkan jaringan parut dan disfungsi sarkomer di
jantung sekitar daerah cedera iskemik. Aritmia jantung dan kardiomiopati primer
seperti yang disebabkan olch alkohol, infeksi, hemakromatosis, hipertiroidisme,
toksisitas obat dan amiloidosis juga menyebabkan penurunan kontraktilitas.
Penurunan curah jantung mengakibatkan kekurangan perfusi pada sirkulasi sistemik
dan aktivasi sistem saraf simpatis dan sistem RAA, menyebabkan peningkatan
tahanan perifer dan peningkatan afterload.
3) Peningkatan afterload berarti terdapat peningkatan tahanan terhadap ejeksi LV.
Biasanya disebabkan oleh peningkatan tahanan vaskular perifer yang umum terlihat
pada hipertensi. Bisa juga diakibatkan oleh stenosis katup aorta. Ventrikel kiri
berespon terhadap peningkatan beban kerja ini dengan hipertrofi miokard, suatu
respons yang meningkatkan massa otot ventrikel kiri tetapi pada saat yang sama
meningkatkan kebutuhan perfusi koroner pada ventrikel kiri. Suatu keadaan
kelaparan energi tercipta sehingga berpadu dengan ANG II dan respons
neuroendokrin lain, menyebabkan perubahan buruk dalam miosit seperti semakin
sedikitnya mitokondria untuk produksi energi, perubahan ekspresi gen dengan
produksi protein kontraktil yang abnormal (aktin, miosin, dan tropomiosin), fibrosis
interstisial, dan penurunan daya tahan hidup miosit. Dengan berjalannya waktu,
kontraktilitas mulai menurun dengan penurunan curah jantung dan fraksi ejeksi,
peningkatan LVEDV, dan kongesti paru.
4) Peningkatan preload berarti peningkatan LVEDV, yang dapat disebabkan langsung
oleh kelebihan volume intravaskular sama seperti yang terlihat pada infus cairan intra
vena atau gagal ginjal. Selain itu, penurunan fraksi ejeksi yang disebabkan oleh
perubahan kontraktilitas atau afterload menyebabkan peningkatan LVEDV sehingga
meningkatkan preload. Pada saat LVEDV meningkat, ia akan meregangkan jantung,
menjadikansarkomer berada pada posisi mekanis yang tidak menguntungkan
sehingga terjadi penurunan kontraktilitas. Penurunan kontraktilitas ini, yang
menyebabkan penurunan fraksi ejeksi, menyebabkan peningkatan LVEDV yang lebih
lanjut, sehingga menciptakan lingkaran setan perburukan gagal jantung.
5) Jadi, pasien dapat memasuki lingkaran penurunan kontraktilitas,
peningkatanafterload, dan peningkatan preload akibat berbagai macam alasan (mis.,
infark miokard [MI], hipertensi, kelebihan cairan) dan kemudian akhimya mengalami
semua keadaan hemodinamik dan neuro-hormonal CHF sebagai sebuah mekanisme
yang menuju mekanisme lainnya.
Disfungsi ventrikel kiri diastolik
1) Penyebab dari 90% kasus
2) Didefinisikan sebagai kondisi dengan temuan klasik gagal kongestif dengan fungsi
diastolik abnormal tetapi fungsi sistolik normal; disfungsi diastolik mumi akan
dicirikan dengan tahanan terhadap pengisian ventrikel dengan peningkatan LVEDP
tanpa peningkatan LVEDV atau penurunan curah jantung.
3) Tahanan terhadap pengisian ventrikel kiri terjadi akibat relaksasi abnormal
(lusitropik) ventrikel kiri dan dapat disebabkan oleh setiap kondisi yang membuat
kaku miokard ventrikel seperti penyakit jantung iskemik yang menyebabkan jaringan
parut, hipertensi yang mengakibatkan kardiomiopati hipertrofi, kardiomiopati
restriktif, penyakit katup atau penyakit perikardium.
4) Peningkatan denyut jantung menyebabkan waktu pengisian diastolik menjadi
berkurang dan memperberat gejala disfungsi diastolik. Oleh karena itu, intoleransi
terhadap olahraga sudah menjadi umum.
5) Karena penanganan biasanya memerlukan perubahan komplians miokard yang
sesungguhnya, efektivitas obat yang kini tersedia masih sangat terbatas.
Penatalaksanaan terkini paling berhasil dengan penyekat beta yang meningkatkan
fungsi lusitropik, menurunkan denyut jantung, dan mengatasi gejala. Inhibitor ACE
dapat membantu memperbaiki hipertrofi dan membantu perubahan struktural di
tingkat jaringan pada pasien dengan remodeling iskemik atau hipertensi.
Anda mungkin juga menyukai
- LP DMDokumen18 halamanLP DMrafie odong-odongBelum ada peringkat
- Format Pengkajian KeluargaDokumen19 halamanFormat Pengkajian Keluargarafie odong-odongBelum ada peringkat
- Patofisiologi DMDokumen2 halamanPatofisiologi DMrafie odong-odongBelum ada peringkat
- Format Pengkajian GerontikDokumen13 halamanFormat Pengkajian Gerontikrafie odong-odongBelum ada peringkat
- CrurisDokumen11 halamanCrurisrafie odong-odongBelum ada peringkat
- Undangan MMDDokumen2 halamanUndangan MMDrafie odong-odongBelum ada peringkat
- Kata PengantarDokumen2 halamanKata Pengantarrafie odong-odongBelum ada peringkat
- Print 1x Format Asqep Non Trauma IGDDokumen4 halamanPrint 1x Format Asqep Non Trauma IGDrafie odong-odongBelum ada peringkat
- LP VSDDokumen10 halamanLP VSDrafie odong-odong100% (2)
- Hernia Inguinalis EditNDokumen29 halamanHernia Inguinalis EditNrafie odong-odongBelum ada peringkat
- WOCDokumen3 halamanWOCrestygustina_8881806Belum ada peringkat
- Leaflet TBC Paru A 4Dokumen2 halamanLeaflet TBC Paru A 4rafie odong-odongBelum ada peringkat
- WOCDokumen3 halamanWOCrestygustina_8881806Belum ada peringkat
- AnalisaDokumen1 halamanAnalisarafie odong-odongBelum ada peringkat
- Patofisiologi Persalinan Kala IIDokumen1 halamanPatofisiologi Persalinan Kala IIrafie odong-odongBelum ada peringkat
- Bab Ii SDHDokumen23 halamanBab Ii SDHrafie odong-odongBelum ada peringkat
- Askep KasusDokumen7 halamanAskep Kasusrafie odong-odongBelum ada peringkat
- Patofis CA LaringDokumen1 halamanPatofis CA Laringrafie odong-odongBelum ada peringkat
- Aplikasi Teori Orlando Dalam Asuhan KeperawatanDokumen18 halamanAplikasi Teori Orlando Dalam Asuhan Keperawatanpanzhl6689100% (1)
- Ggn. Kes. Cairan&ElektrolitDokumen15 halamanGgn. Kes. Cairan&Elektrolitrafie odong-odongBelum ada peringkat
- Metode Hukum Dan Praktek KedokteranDokumen55 halamanMetode Hukum Dan Praktek Kedokteranrafie odong-odongBelum ada peringkat
- LP SAHprintDokumen19 halamanLP SAHprintrafie odong-odongBelum ada peringkat
- Patofisiologi Oklusi Arteri RetinaDokumen2 halamanPatofisiologi Oklusi Arteri Retinarafie odong-odongBelum ada peringkat
- Anatomi Dan Fisiologi Sistem Endokrin 2003Dokumen7 halamanAnatomi Dan Fisiologi Sistem Endokrin 2003rafie odong-odongBelum ada peringkat
- Laporan Pendahuluan SDH 1Dokumen25 halamanLaporan Pendahuluan SDH 1rafie odong-odongBelum ada peringkat
- Laporan Pendahuluan SDH 1Dokumen25 halamanLaporan Pendahuluan SDH 1rafie odong-odongBelum ada peringkat
- Laporan Pendahuluan SDH 1Dokumen25 halamanLaporan Pendahuluan SDH 1rafie odong-odongBelum ada peringkat
- Laporan Pendahuluan SDH 1Dokumen25 halamanLaporan Pendahuluan SDH 1rafie odong-odongBelum ada peringkat
- LP Nadif-1Dokumen16 halamanLP Nadif-1rafie odong-odongBelum ada peringkat