File PDF
Diunggah oleh
Andi SulfianaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
File PDF
Diunggah oleh
Andi SulfianaHak Cipta:
Format Tersedia
UNIVERSITAS INDONESIA
LAPORAN PRAKTIK KERJA PROFESI APOTEKER
DI PT. KIMIA FARMA TRADING AND DISTRIBUTION
JL. BUDI UTOMO NO. 1 JAKARTA PUSAT
PERIODE 23 SEPTEMBER – 01 NOVEMBER 2013
LAPORAN PRAKTIK KERJA PROFESI
ENNIE RIBEN SIHTE, S.Farm.
1206329575
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
Uni
Laporan praktek….., Ennie Riben, FFar UI, 2014
UNIVERSITAS INDONESIA
LAPORAN PRAKTIK KERJA PROFESI APOTEKER
DI PT. KIMIA FARMA TRADING AND DISTRIBUTION
JL. BUDI UTOMO NO. 1 JAKARTA PUSAT
PERIODE 23 SEPTEMBER – 01 NOVEMBER 2013
LAPORAN PRAKTIK KERJA PROFESI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Apoteker
ENNIE RIBEN SIHITE, S.Farm.
1206329575
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
Uni
Laporan praktek….., Ennie Riben, FFar UI, 2014
TIALAMAII PERIYYATAA}T ORISINALITAS
Laporan Praktek Kerja Profesi Apoteker ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk telah
saya nyatakan dengan benar.
Nama Ennie Riben Sihite, S.Farm
NPM 1206329575
Tanda Tangan
Tanggal 17 lanLtari20l4
Laporan praktek….., Ennie Riben, FFar UI, 2014
Laporan praktek….., Ennie Riben, FFar UI, 2014
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, karena
berkat rahmat dan anugerah-Nya, penulis dapat menyusun dan menyelesaikan
Laporan Praktik Kerja Profesi Apoteker (PKPA) di PT. Kimia Farma Trading and
Distribution Jakarta yang telah dilaksanakan pada tanggal 23 September – 01
November 2013.
Pelaksanaan Praktik Kerja Profesi Apoteker merupakan salah satu sarana
untuk mengembangkan wawasan kefarmasian di Pedagang Besar Farmasi
sebelum melakukan pengabdian sebagai Apoteker, dan merupakan salah satu
syarat yang harus dipenuhi untuk menyelesaikan Program Profesi Apoteker di
Fakultas Farmasi Universitas Indonesia.
Pada kesempatan ini penulis ingin menyampaikan rasa hormat dan terima
kasih kepada:
1. Dr. Mahdi Jufri, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas
Indonesia.
2. Prof. Dr. Yahdiana Harahap MS., sebagai Pejabat Sementara Dekan Fakultas
Farmasi Universitas Indonesia sampai dengan tanggal 20 Desember 2013.
3. Dr. Harmita, Apt., selaku Ketua Program Pendidikan Profesi Apoteker
Fakultas Farmasi Universitas Indonesia dan pembimbing dari Fakultas
Farmasi Universitas Indonesia yang telah memberikan bimbingan dan
pengarahan.
4. Drs. Ignatius Muryanta, Apt., selaku Direktur Utama PT. Kimia Farma
Trading and Distribution.
5. Drs. M. Umar Said, Apt., MM., selaku Direktur Bidang Keuangan dan
Sumber Daya Manusia PT. Kimia Farma Trading and Distribution atas
waktu, pikiran dan ijin yang diberikan untuk pelaksanaan kegiatan PKPA di
PT. Kimia Farma Trading and Distribution.
6. Drs. Taufik Hidayat, Apt., selaku Manajer Bidang Sumber Daya Manusia dan
Pembimbing di PT. Kimia Farma Trading and Distribution Jakarta atas
waktu, tenaga dan pikiran yang telah diberikan kepada penulis.
iv Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
7. Bapak Syafrial selaku pembimbing lapangan di Pedagang Besar Farmasi PT.
Kimia Farma Trading and Distribution Jakarta atas ijin dan bimbingan selama
penulis melakukan PKPA di KFTD cabang Bogor.
8. Seluruh staf dan karyawan KFTD cabang Bogor yang telah membantu dalam
pelaksanaan Praktik Kerja Profesi Apoteker.
9. Bapak dan Ibu staf pengajar beserta segenap karyawan Fakultas Farmasi
Universitas Indonesia.
10. Rekan-rekan Program Profesi Apoteker Universitas Indonesia angkatan
LXXVII atas kebersamaan dan dukungan selama menempuh pendidikan.
11. Semua pihak yang tidak dapat disebutkan satu persatu yang telah membantu
secara langsung maupun tidak langsung dalam penulisan laporan ini.
Demikian laporan PKPA ini disusun, dengan harapan tulisan ini
bermanfaat bagi rekan-rekan sejawat khususnya dan pembaca pada umumnya.
Penulis sangat mengharapkan masukan, kritik dan saran yang membangun guna
perbaikan dan penyempurnaan laporan ini. Semoga laporan ini memberikan
manfaat bagi berbagai pihak. Terima kasih.
Penulis
2013
v Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
HALAMAN PER}I-YATAAI\T PERSETUJUAN PTIBLIKASI
TUGAS AKIIIR UNTUK KEPENTINGAII AKADEMIS
Sebagai sivitas akademik Universitas Indonesia, saya yang bertanda tangan
dibawah ini:
Nama Ennie Riben Sihite, S.Farm
NPM 120632957s
Program Studi Apoteker
Fakultas Farmasi
Jenis karya Laporan Praktek Kerja Profesi Apoteker
demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada
Universitas Indonesia Hak Bebas Royalti Noneksklusif (Non-exclusive Royalg
Free Right'1atas karya ilmiah saya yang berjudul:
LAPORAN PRAKTIK KERJA PROFESI APOTEKER
DI PT. KIMIA FARMA TRADING AND DISTRIBUTION
PERIODE 23 SEPTEMBER - 01 NOYEMBER 2013
beserta perangkat yang ada(bila diperlukan) dengan Hak Bebas Royalti
Noneksklusif ini Universitas Indonesia berhak menyimpan, mengalih
media/formatkan, mengelola dalam bentuk basis data, merawat, dan
mempublikasikan tugas akhir saya selama tetap mencantumkan nama saya sebagai
penulis/pencipta dan sebagai pemilik Hak Cipta.
Demikian pemyataan ini saya buat dengan sebenarnya.
Dibuat di : Depok
Pada Tanggal : 17 Januan2}l4
Yang menyatakan
(Ennie Riben Sihite, S.Farm.)
Laporan praktek….., Ennie Riben, FFar UI, 2014
ABSTRAK
Nama : Ennie Riben Sihite, S. Farm
NPM : 1206329575
Program Studi : Profesi Apoteker
Judul : Laporan Praktik Kerja Profesi Apoteker di PT. Kimia
Farma Trading and Distribution Periode 23 September – 01
November 2013
Praktek Kerja Profesi Apoteker di PT. Kimia Farma Trading and Distribution
bertujuan untuk memahami tugas dan fungsi apoteker di PBF dan memahami
kegiatan di PBF baik secara teknis kefarmasian maupun non teknis kefarmasian.
Tugas khusus yang diberikan berjudul Kepatuhan Melaksanakan Cara Distribusi
Obat yang Baik (CDOB) untuk Sediaan Narkotika dan Psikotropika di PT. Kimia
Farma Trading and Distribution cabang Bogor. Tujuan dari tugas khusus ini
adalah untuk mengamati sejauh mana kepatuhan KFTD cabang Bogor
menerapkan Cara Distribusi Obat yang Baik (CDOB) dalam untuk sediaan
narkotika dan psikotropika.
Kata kunci : Pedagang Besar Farmasi, KFTD Kimia Farma
Tugas umum : x + 63 halaman; 19 lampiran
Tugas khusus : iii + 26 halaman; 19 lampiran
Daftar Acuan Tugas Umum : 12 (1997-2012)
Daftar Acuan Tugas Khusus : 6 (1997-2012)
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
ABSTRACT
Name : Ennie Riben Sihite, S.Farm
NPM : 1206329575
Program Study : Apothecary profession
Title : Pharmacist Internship Program at PT. Kimia Farma
Trading and Distribution Period Sept 23th - Nov 1st 2013
Practice Pharmacist at PT. Kimia Farma Trading and Distribution aims to
understand the duties and functions of pharmacists in PBF and PBF understand
the activities in both technical and non-technical pharmacy pharmacy. Given a
special task entitled Implementing Compliance of Good Distribution Practices
(CDOB) for the preparation of Narcotics and Psychotropic PT. Kimia Farma
Trading and Distribution Bogor branch. The purpose of this special task is to
observe the extent to which compliance KFTD implement the Bogor branch of
Good Distribution Practices (CDOB) in preparation for narcotics and
psychotropic substances.
Keywords : Pharmaceutical wholesalers, KFTD Kimia Farma
General Assignment : x + 63 pages; 19 appendices
Specific Assignment : iii + 26 pages; 19 appendices
Bibliography of General Assignment: 12 (1997-2012)
Bibliography of Specific Assignment: 6 (1997-2012)
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR ISI
HALAMAN SAMPUL .................................................................................... i
HALAMAN JUDUL ........................................................................................ ii
HALAMAN PENGESAHAN .......................................................................... iii
KATA PENGANTAR ...................................................................................... iv
DAFTAR ISI .................................................................................................... vi
DAFTAR GAMBAR ....................................................................................... ix
DAFTAR LAMPIRAN .................................................................................... x
BAB 1 PENDAHULUAN ............................................................................... 1
1.1 Latar Belakang ............................................................................... 1
1.2 Tujuan ............................................................................................ 2
BAB 2 TINJAUAN UMUM ........................................................................... 3
2.1 Pedagang Besar Farmasi (PBF) ..................................................... 3
2.1.1 Definisi .............................................................................. 3
2.1.2 Landasan Hukum PBF ....................................................... 3
2.1.3 Tugas dan Fungsi PBF ....................................................... 3
2.1.4 Persyaratan PBF ................................................................ 4
2.1.4.1 Tempat atau Lokasi ................................................ 4
2.1.4.2 Bangunan ............................................................... 4
2.1.4.3 Perlengkapan PBF ................................................. 5
2.1.5 Apoteker Penanggung jawab untuk PBF ........................... 5
2.1.6 Tata Cara Perizinan PBF ................................................... 8
2.1.7 Pencabutan Ijin PBF .......................................................... 11
2.1.8 Penyelenggaraan PBF ........................................................ 11
2.1.8.1 Pengadaan .............................................................. 12
2.1.8.2 Penyaluran ............................................................. 12
2.1.9 Pelaporan Kegiatan PBF .................................................... 14
2.1.10 Larangan PBF .................................................................... 14
2.2 Cara Distribusi Obat yang Baik (CDOB) ...................................... 14
2.2.1 Manajemen Mutu ............................................................... 14
2.2.2 Organisasi, Managemen, Personalia .................................. 16
2.2.3 Bangunan dan Peralatan .................................................... 16
2.2.4 Operasional ........................................................................ 18
2.2.5 Inspeksi Diri ...................................................................... 21
2.2.6 Keluhan, Obat dan/atau Bahan Obat Kembalian, Diduga
Palsu, dan Penarikan Kembali ........................................... 22
2.2.7 Transportasi ....................................................................... 23
2.2.8 Fasilitas Distribusi Berdasarkan Kontrak .......................... 24
2.2.9 Dokumentasi ...................................................................... 24
2.2.9.1 Pelaporan Kegiatan di PBF ke Institusi Terkait ..... 26
2.2.9.2 Pelaporan Narkotika dan Psikotropika .................. 26
BAB 3 TINJAUAN KHUSUS ........................................................................ 28
3.1 PT. Kimia Farma Trading And Distribution ................................. 28
vi Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
3.1.1 Sejarah Pendirian Perusahaan ............................................ 28
3.1.2 Visi dan Misi ..................................................................... 30
3.1.2.1 Visi ......................................................................... 30
3.1.2.2 Misi ........................................................................ 31
3.1.3 Strategi ............................................................................... 31
3.1.4 Sistem Pengadaan dan Pendistribusian Barang ................. 31
3.1.5 Jenis Pelanggan PT. KFTD (Channel Distribution) .......... 31
3.2 Manajemen Operational ................................................................ 32
3.2.1 Manajemen Pengadaan ...................................................... 33
3.2.1.1 Definisi .................................................................. 33
3.2.1.2 Tujuan .................................................................... 33
3.2.1.3 Tugas dan Tanggung Jawab ................................... 33
3.2.1.4 Standar Operational and Procedure Pengadaan
Barang .................................................................... 33
3.2.1.5 Sasaran ................................................................... 35
3.2.1.6 Indikator ................................................................. 35
3.2.2 Manajemen Penyimpanan .................................................. 35
3.2.2.1 Definisi .................................................................. 35
3.2.2.2 Tujuan .................................................................... 35
3.2.2.3 Tugas dan Tanggung Jawab ................................... 35
3.2.2.4 Sistem Penyimpanan Barang di Gudang ............... 36
3.2.2.5 Penataan Alokasi Ruang Penyimpanan di Gudang . 37
3.2.2.6 Kelengkapan Peralatan Gudang ............................. 38
3.2.2.7 Standar Operational and Procedure Penerimaan,
Penyimpanan, dan Pengeluaran Barang ................. 38
3.2.2.8 Sasaran ................................................................... 40
3.2.2.9 Indikator ................................................................. 40
3.2.3 Manajemen Penjualan dan Pelayanan ............................... 40
3.2.3.1 Definisi .................................................................. 40
3.2.3.2 Tujuan .................................................................... 40
3.2.3.3 Standar Operational and Procedure Penjualan
dan Pelayanan ........................................................ 40
3.2.3.4 Sasaran ................................................................... 43
3.2.3.5 Indikator ................................................................. 43
3.2.4 Manajemen Piutang ........................................................... 43
3.2.4.1 Definisi .................................................................. 43
3.2.4.2 Standar Operational and Procedure Piutang ........ 44
3.2.4.3 Sasaran ................................................................... 45
3.2.4.4 Indikator ................................................................. 45
3.2.5 Manajemen Pembukuan .................................................... 46
3.2.5.1 Definisi .................................................................. 46
3.2.5.2 Tujuan .................................................................... 47
3.2.5.3 Standar Operational and Procedure Pembukuan . 47
3.2.5.4 Sasaran ................................................................... 47
3.2.5.5 Indikator ................................................................. 48
3.3 Pajak .............................................................................................. 48
3.3.1 Pajak Pertambahan Nilai (PPN) ........................................ 48
3.3.2 Pajak Penghasilan (PPh) .................................................... 49
vii Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 4 HASIL DAN PEMBAHASAN .......................................................... 51
BAB 5 KESIMPULAN DAN SARAN .......................................................... 60
5.1 Kesimpulan .................................................................................... 60
5.2 Saran .............................................................................................. 61
DAFTAR ACUAN ....................................................................................... 62
LAMPIRAN .................................................................................................... 63
......................................................................................................................
viii Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR GAMBAR
Gambar 3.1. Diagram pengadaan barang ...................................................... 34
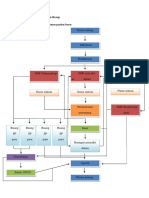
Gambar 3.2. Diagram Penerimaan, Penyimpanan, dan Pengeluaran Barang 39
Gambar 3.3. Alur Penerimaan, Penyimpanan, dan Pengeluaran Barang ...... 38
Gambar 3.4. Contoh Alat Kontrol Penjualan ............................................ ... 41
Gambar 3.5. Diagram Penjualan ................................................................... 43
Gambar 3.6. Diagram Piutang ....................................................................... 46
Gambar 3.7. Diagram Pembukuan ................................................................ 47
ix Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR LAMPIRAN
Lampiran 1. Surat pesanan pembelian ke pihak III ...................................... 64
Lampiran 2. Surat pesanan ke Unit Bisnis Logistik (UBL) .......................... 65
Lampiran 3. Faktur pembelian dari pihak III ................................................ 66
Lampiran 4. Surat Kirim Barang (SKB) dari UBL ke KFTD cabang .......... 67
Lampiran 5. Surat pesanan sementara........................................................... 68
Lampiran 6. Surat pesanan yang di faksimile ............................................... 69
Lampiran 7. Delivery order atau SKB penjualan ......................................... 70
Lampiran 8. Faktur penjualan ....................................................................... 71
Lampiran 9. Faktur pajak penjualan ............................................................. 72
Lampiran 10. Kartu stok ................................................................................. 73
Lampiran 11. Buku ekspedisi tunai................................................................. 74
Lampiran 12. Buku ekspedisi kredit ............................................................... 75
Lampiran 13. Tanda terima tukar faktur ......................................................... 76
Lampiran 14. Konfirmasi piutang per pelanggan ........................................... 77
Lampiran 15. Nota inkaso ............................................................................... 78
Lampiran 16. Laporan harian kunjungan salesman ........................................ 79
Lampiran 17. Daftar kunjungan salesman ...................................................... 80
Lampiran 18. Kunjungan penagih ................................................................... 81
Lampiran 19. Customer record card............................................................... 82
x Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Upaya kesehatan merupakan setiap kegiatan dan/atau serangkaian kegiatan
yang dilakukan secara terpadu, terintegrasi dan berkesinambungan untuk
memelihara dan meningkatkan derajat kesehatan masyarakat dalam bentuk
pencegahan penyakit, peningkatan kesehatan, pengobatan penyakit, dan
pemulihan keseharan oleh pemerintah dan/atau masyarakat (Presiden Republik
Indonesia, 2009).
Dalam rangka menyelenggarakan upaya kesehatan masyarakat diperlukan
suatu sumber daya kesehatan. Sediaan farmasi merupakan salah satu sumber daya
kesehatan yang dimanfaatkan untuk menyelenggarakan upaya kesehatan yang
dilakukan oleh pemerintah, pemerintah daerah, dan/atau masyarakat (Menteri
Kesehatan Republik Indonesia, 2010). Untuk menjamin ketersediaan sediaan
farmasi di masyarakat maka pemerintah menetapkan peraturan tentang
pendistribusian obat. Menurut peraturan pemerintah nomor 51 tahun 2009,
penyimpanan, pendistribusian atau penyaluran obat, dan pengelolaan obat
merupakan salah satu pekerjaan kefarmasian dan fasilitas distribusi atau
penyaluran sediaan farmasi yang digunakan untuk mendistribusikan atau
menyalurkan sediaan farmasi disebut instalasi sediaan farmasi dan pedagang besar
farmasi (Presiden Republik Indonesia, 2009).
Pedagang Besar Farmasi (PBF) adalah perusahaan berbentuk badan hukum
yang memiliki izin untuk pengadaan, penyimpanan, penyaluran obat dan/atau
bahan obat dalam jumlah besar sesuai ketentuan peraturan perundang-undangan.
Adapun penanggung jawab PBF wajib seorang Apoteker yang memenuhi
kualifikasi dan kompetensi sesuai peraturan perundang-undangan. Di samping itu,
PBF dalam menyelenggarakan kegiatannya wajib menggunakan Pedoman Teknis
Cara Distribusi Obat yang Baik (CDOB). CDOB adalah cara distribusi atau
penyaluran obat dan atau bahan obat yang bertujuan memastikan mutu sepanjang
1 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
2
jalur distribusi atau penyaluran sesuai persyaratan dan tujuan penggunaannya
(BPOM RI, 2012).
Semua pihak yang terlibat dalam distribusi obat dan atau bahan obat
bertanggung jawab untuk memastikan mutu obat dan atau bahan obat dan
mempertahankan integritas rantai distribusi selama proses distribusi.
Sebagai mahasiswa program profesi apoteker, perlu adanya pemahaman
tentang peran apoteker di PBF. Oleh karena itu, Universitas Indonesia bekerja
sama dengan PT. Kimia Farma Trading and Distribution yang bergerak dalam
bidang distribusi dan penyaluran sediaan farmasi melaksanakan praktik kerja
profesi apoteker pada tanggal 23 September–01 November 2013. Melalui kegiatan
ini diharapkan mahasiswa yang merupakan calon apoteker dapat mendapatkan
ilmu dan pengalaman kerja agar nantinya dapat diterapkan secara nyata dalam
menjalankan perannya sebagai apoteker.
1.2 Tujuan
Praktik Kerja Profesi Apoteker (PKPA) di PT. Kimia Farma Trading and
Distribution bertujuan untuk :
a. Mengetahui dan memahami cara distribusi obat yang baik di PT. Kimia Farma
Trading and Distribution.
b. Memahami peran dan tanggung jawab apoteker di pedagang besar farmasi.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 2
TINJAUAN UMUM
2.1 Pedagang Besar Farmasi (PBF)
2.1.1 Definisi PBF
Menurut Pedoman Cara Distribusi Obat yang Baik (CDOB) dan Peraturan
Menteri Kesehatan Republik Indonesia Nomor 1148/MENKES/PER/VI/2011,
pedagang besar farmasi adalah perusahaan berbentuk badan hukum yang memiliki
izin untuk pengadaan, penyimpanan, penyaluran obat dan/ atau bahan obat dalam
jumlah besar sesuai ketentuan peraturan perundang-undangan. PBF dan PBF
Cabang dalam menyelenggarakan pengadaan, penyimpanan, dan penyaluran obat
dan/ atau bahan obat wajib menerapkan Pedoman Teknis Cara Distribusi Obat
yang Baik (CDOB). CDOB adalah cara distribusi atau penyaluran obat dan/ atau
bahan obat yang bertujuan untuk memastikan mutu sepanjang jalur distribusi
sesuai persyaratan dan tujuan penggunaannya (Badan Pengawas Obat dan
Makanan Republik Indonesia, 2012).
2.1.2 Landasan Hukum PBF
PBF memiliki landasan hukum yang diatur dalam:
a. Peraturan Menteri Kesehatan RI Nomor 1148/MENKES/PER/VI/2011 tentang
Pedagang Besar Farmasi.
b. Peraturan Menteri Kesehatan RI Nomor 889/MENKES/PER/V/2011 tentang
Registrasi, Izin Praktik, dan Izin Kerja Tenaga Kefarmasian.
c. Peraturan Pemerintah Nomor 51 Tahun 2009 tentang Pekerjaan Kefarmasian.
d. Undang-Undang Nomor 35 Tahun 2009 tentang Narkotika.
e. Undang-Undang Nomor 5 Tahun 1997 tentang Psikotropika.
2.1.3 Tugas dan Fungsi PBF
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
1148/MENKES/PER/VI/2011 tentang PBF, tugas dan fungsi PBF yaitu:
a. Menyelenggarakan pengadaan, penyimpanan dan penyaluran obat.
b. Sebagai tempat pendidikan dan pelatihan.
3 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
4
2.1.4 Persyaratan PBF
Suatu PBF beroperasi setelah mendapat surat izin. Selama PBF tersebut
masih aktif melakukan kegiatan pengelolaan obat, maka seluruh kegiatan yang
dilaksanakan di PBF tersebut wajib berdasarkan kepada CDOB.
2.1.4.1 Tempat atau Lokasi
Lokasi PBF dapat dipilih dengan mempertimbangkan segi efisiensi dan
efektivitas dalam pengadaan dan penyaluran obat ke sarana pelayanan kesehatan
dan faktor-faktor lainnya.
2.1.4.2 Bangunan
Suatu PBF harus mempunyai luas bangunan yang cukup dan memenuhi
persyaratan teknis, sehingga dapat menjamin kelancaran pelaksanaan tugas dan
fungsi PBF. Suatu PBF paling sedikit memiliki ruang tunggu, ruang penerimaan
obat, ruang penyiapan obat, ruang administrasi, ruang kerja apoteker, gudang obat
jadi, ruang makan dan kamar kecil. Bangunan PBF dilengkapi dengan sumber air
yang memenuhi syarat kesehatan, pencahayaan yang memadai, alat pemadam
kebakaran, ventilasi dan sanitasi yang baik.
Bangunan harus dirancang dan disesuaikan untuk memastikan bahwa
kondisi penyimpanan yang baik dapat dipertahankan, mempunyai keamanan yang
memadai, kapasitas yang cukup untuk memungkinkan penyimpanan dan
penanganan obat yang baik, dan area penyimpanan dilengkapi dengan
pencahayaan yang memadai untuk memungkinkan semua kegiatan dilaksanakan
secara akurat dan aman.
Area penerimaan, penyimpanan dan pengiriman harus terpisah, terlindung
dari kondisi cuaca, dan harus didesain dengan baik serta dilengkapi dengan
peralatan yang memadai. Akses masuk ke area penerimaan, penyimpanan dan
pengiriman hanya diberikan kepada personil yang berwenang, yakni dengan
adanya sistem alarm dan kontrol akses yang memadai (Badan Pengawas Obat dan
Makanan Republik Indonesia, 2012).
Bangunan dan fasilitas penyimpanan harus bersih, bebas dari sampah dan
debu serta harus dirancang dan dilengkapi, sehingga memberikan perlindungan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
5
terhadap masuknya serangga, hewan pengerat atau hewan lain. Ruang istirahat,
toilet dan kantin untuk personil harus terpisah dari area penyimpanan. Selain itu
harus disediakan area khusussepertipenyimpananobat-obatnarkotikaseperti yang
telahditetapkandalam CDOB (Badan Pengawas Obat dan Makanan Republik
Indonesia, 2012).
2.1.4.3 Perlengkapan PBF
Suatu PBF yang ingin beroperasi harus memiliki perlengkapan yang
memadai agar dapat mendukung pendistribusian obat jadi. Perlengkapan yang
harus dimiliki yaitu peralatan penyimpanan obat dan perlengkapan administrasi.
Peralatan dan tempat penyimpanan obat seperti lemari obat jadi, lemari
pendingin (kulkas), lemari untuk menyimpan produk kembalian, kontainer untuk
pengiriman barang dan box es untuk pengiriman obat dengan suhu penyimpanan
rendah.
Perlengkapan administrasi terkait dokumen penjualan, pembelian dan
penyimpanan, seperti blanko pesanan, blanko faktur, blanko tukar faktur, bilyet
giro, blanko faktur pajak, blanko surat jalan, kartu stok obat, bukti penerimaan
pembayaran, form retur, blanko faktur pajak dan stempel PBF. Buku-buku dan
literatur standar yang diwajibkan, serta kumpulan perundang-undangan yang
berhubungan dengan kegiatan di PBF.
2.1.5 Apoteker Penanggung Jawab untuk PBF
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
889/MENKES/PER/V/2011 tentang Registrasi, Izin Praktik, dan Izin Kerja
Tenaga Kefarmasian menjelaskan bahwa apoteker adalah Sarjana Farmasi yang
telah lulus sebagai apoteker dan telah mengucapkan sumpah jabatan apoteker.
Sedangkan Tenaga Teknis Kefarmasian adalah tenaga yang membantu apoteker
dalam menjalankan pekerjaan kefarmasian, yang terdiri atas Sarjana Farmasi, Ahli
Madya Farmasi, Analis Farmasi dan Tenaga Menengah Farmasi/ Asisten
Apoteker.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
6
Apoteker yang akan menjalankan pekerjaan kefarmasian harus memenuhi
persyaratan yang tertera dalam Peraturan Pemerintah Nomor 51 Tahun 2009 Pasal
35, 37, 52, 54, yaitu sebagai berikut:
a. Memiliki keahlian dan kewenangan.
b. Menerapkan Standar Profesi.
c. Didasarkan pada Standar Kefarmasian dan Standar Operasional.
d. Memiliki sertifikat kompetensi profesi.
e. Memiliki Surat Tanda Registrasi Apoteker (STRA).
Surat Tanda Registrasi (STRA) merupakan bukti tertulis yang diberikan
oleh Menteri kepada apoteker yang telah diregistrasi. STRA berlaku 5 (lima)
tahun dan dapat diperpanjang untuk jangka waktu lima tahun selama masih
memenuhi persyaratan. Untuk memperoleh STRA, apoteker harus memenuhi
persyaratan (Pemerintah Republik Indonesia, 2009):
a. Memiliki ijazah apoteker.
b. Memiliki sertifikat kompetensi profesi.
c. Mempunyai surat pernyataan telah mengucapkan sumpah/ janji apoteker.
d. Mempunyai surat keterangan sehat fisik dan mental dari dokter yang memiliki
surat izin praktek.
e. Membuat pernyataan akan mematuhi dan melaksanakan ketentuan etika
profesi.
f. Pas foto terbaru berwama ukuran 4 x 6 cm sebanyak 2 (dua) lembar dan
ukuran 2 x 3 cm sebanyak 2 (dua) lembar.
Setelah memenuhi persyaratan di atas, seorang apoteker yang akan bekerja
sebagai apoteker penanggungjawab di PBF wajib memiliki Surat Izin Kerja
Apoteker (SIKA). SIKA adalah surat izin praktek yang diberikan kepada apoteker
untuk dapat melaksanakan pekerjaan kefarmasian pada fasilitas produksi atau
fasilitas distribusi atau penyaluran. SIKA hanya diberikan untuk 1 (satu) tempat
fasilitas kefarmasian. Untuk memperoleh SIKA, apoteker mengajukan
permohonan kepada Kepala Dinas Kesehatan Kabupaten/ Kota tempat pekerjaan
kefarmasian dilaksanakan serta harus menerbitkan SIKA paling lama 20 (dua
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
7
puluh) hari kerja sejak surat permohonan diterima dan dinyatakan lengkap.
Berkas-berkas yang harus dilampirkan untuk permohonan SIKA yaitu:
a. Fotokopi STRA yang dilegalisir oleh Komite Farmasi Nasional (KFN).
b. Surat penyataan mempunyai tempat praktik profesi atau surat keterangan dari
pimpinan fasilitas pelayanan kefarmasian atau dari pimpinan fasilitas produksi
atau distribusi/ penyaluran.
c. Surat rekomendasi dari organisasi profesi.
d. Pas foto berwarna ukuran 4 x 6 sebanyak 2 (dua) lembar dan 3 x 4 sebanyak 2
(dua) lembar.
Pencabutan SIKA oleh Kepala Dinas Kesehatan Kabupaten/ Kota dapat
dilakukan apabila:
a. Atas permintaan yang bersangkutan.
b. STRA tidak berlaku lagi.
c. Yang bersangkutan tidak bekerja pada tempat yang tercantum dalam surat
izin.
d. Yang bersangkutan tidak lagi memenuhi persyaratan fisik dan mental untuk
menjalankan pekerjaan kefarmasian berdasarkan pembinaan dan pengawasan
dan ditetapkan dengan surat keterangan dokter.
e. Melakukan pelanggaran disiplin tenaga kefarmasian berdasarkan rekomendasi
KFN.
f. Melakukan pelanggaran hukum di bidang kefarmasian yang dibuktikan
dengan putusan pengadilan.
Menurut Pedoman Teknis CDOB (2012), tugas dan kewajiban apoteker di
PBF adalah sebagai berikut:
a. Menyusun, memastikan dan mempertahankan penerapan sistem manajemen
mutu.
b. Fokus pada pengelolaan kegiatan yang menjadi kewenangannya serta menjaga
akurasi dan mutu dokumentasi.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
8
c. Menyusun dan/ atau menyetujui program pelatihan dasar dan pelatihan
lanjutan mengenai CDOB untuk semua personil yang terkait dalam kegiatan
distribusi.
d. Mengkoordinasikan dan melakukan dengan segera setiap kegiatan penarikan
obat.
e. Memastikan bahwa keluhan pelanggan ditangani dengan efektif.
f. Melakukan kualifikasi dan persetujuan terhadap pemasok dan pelanggan.
g. Meluluskan obat kembalian untuk dikembalikan ke dalam stok obat yang
memenuhi syarat jual.
h. Turut serta dalam pembuatan perjanjian antara pemberi kontrak dan penerima
kontrak yang menjelaskan mengenai tanggung jawab masing-masing pihak
yang berkaitan dengan distribusi dan/ atau transportasi obat.
i. Memastikan inspeksi diri dilakukan secara berkala sesuai program dan
tersedia tindakan perbaikan yang diperlukan.
j. Mendelegasikan tugasnya kepada apoteker/ tenaga teknis kefarmasian yang
telah mendapatkan persetujuan dari instansi berwenang ketika sedang tidak
berada di tempat dalam jangka waktu tertentu dan menyimpan dokumen yang
terkait dengan setiap pendelegasian yang dilakukan.
k. Turut serta dalam setiap pengambilan keputusan untuk mengkarantina atau
memusnahkan obat.
2.1.6 Tata Cara Perizinan PBF
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
1148/MENKES/PER/VI/2011 tentang PBF, setiap pendirian PBF wajib memiliki
izin dari Direktur Jenderal yang dapat diperoleh apabila pemohon mengajukan
permohonan kepada Direktur Jenderal dengan tembusan kepada Kepala Badan,
Kepala Dinas Kesehatan Provinsi dan Kepala Balai POM dengan menggunakan
Formulir 1. Izin PBF berlaku selama 5 (lima) tahun dan dapat diperpanjang
selama memenuhi persyaratan. Untuk memperoleh izin PBF, pemohon harus
memenuhi persyaratan sebagai berikut:
a. Berbadan hukum berupa perseroan terbatas atau koperasi.
b. Memiliki Nomor Pokok Wajib Pajak (NPWP).
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
9
c. Memiliki secara tetap apoteker Warga Negara Indonesia sebagai penanggung
jawab.
d. Komisaris/ dewan pengawas dan direksi/ pengurus tidak pernah terlibat, baik
langsung atau tidak langsung dalam pelanggaran peraturan perundang-
undangan di bidang farmasi.
e. Menguasai bangunan dan sarana yang memadai untuk dapat melaksanakan
pengadaan, penyimpanan, dan penyaluran obat serta dapat menjamin
kelancaran pelaksanaan tugas dan fungsi PBF.
f. Menguasai gudang sebagai tempat penyimpanan dengan perlengkapan yang
dapat menjamin mutu serta keamanan obat yang disimpan.
g. Memiliki ruang penyimpanan obat yang terpisah dari ruangan lain sesuai
CDOB.
Permohonan harus ditandatangani oleh direktur/ ketua dan apoteker calon
penanggung jawab disertai dengan kelengkapan administratif sebagai berikut:
a. Fotokopi Kartu Tanda Penduduk (KTP)/ identitas direktur/ ketua.
b. Susunan direksi/ pengurus.
c. Pernyataan komisaris/ dewan pengawas dan direksi/ pengurus tidak pernah
terlibat pelanggaran peraturan perundang-undangan di bidang farmasi.
d. Akta pendirian badan hukum yang sah sesuai ketentuan peraturan perundang-
undangan.
e. Surat Tanda Daftar Perusahaan.
f. Fotokopi Surat Izin Usaha Perdagangan.
g. Fotokopi Nomor Pokok Wajib Pajak.
h. Surat bukti penguasaan bangunan dan gudang.
i. Peta lokasi dan denah bangunan.
j. Surat penyataan kesediaan bekerja penuh apoteker penanggung jawab.
k. Fotokopi Surat Tanda Registrasi Apoteker penanggung jawab.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
10
Berikut ini merupakan alur dari pengajuan izin PBF, yaitu:
a. Paling lama dalam waktu 6 (enam) hari kerja sejak diterimanya tembusan
permohonan, Kepala Dinas Kesehatan Provinsi melakukan verifikasi
kelengkapan administratif.
b. Paling lama dalam waktu 6 (enam) hari kerja sejak diterimanya tembusan
permohonan, Kepala Balai POM melakukan audit pemenuhan persyaratan
CDOB.
c. Paling lama dalam waktu 6 (enam) hari kerja sejak dinyatakan memenuhi
kelengkapan administratif, Kepala Dinas Kesehatan Provinsi mengeluarkan
rekomendasi pemenuhan kelengkapan administratif kepada Direktur Jenderal
dengan tembusan kepada Kepala Balai POM dan pemohon dengan
menggunakan Formulir 2.
d. Paling lama dalam waktu 6 (enam) hari kerja sejak dinyatakan memenuhi
persyaratan CDOB, Kepala Balai POM mengeluarkan rekomendasi hasil
analisis pemenuhan persyaratan CDOB kepada Direktur Jenderal dengan
tembusan kepada Kepala Badan, Kepala Dinas Kesehatan Provinsi dan
pemohon dengan menggunakan Formulir 3.
e. Paling lama dalam waktu 6 (enam) hari kerja sejak menerima rekomendasi
serta persyaratan lainnya yang ditetapkan, Direktur Jenderal menerbitkan izin
PBF dengan menggunakan Formulir 4.
f. Dalam hal ketentuan sebagaimana dimaksud pada poin (c), (d), (e) tidak
dilaksanakan pada waktunya, pemohon dapat membuat surat pernyataan siap
melakukan kegiatan kepada Direktur Jenderal dengan tembusan kepada
Kepala Badan, Kepala Balai POM dan Kepala Dinas Kesehatan Provinsi
dengan menggunakan Formulir 5.
g. Paling lama 12 (dua belas) hari kerja sejak diterimanya surat pernyataan
sebagaimana dimaksud pada poin (f), Direktur Jenderal menerbitkan izin PBF
dengan tembusan kepada Kepala Badan, Kepala Dinas Kesehatan Provinsi,
Kepala Dinas Kesehatan Kabupaten/ Kota dan Kepala Balai POM.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
11
2.1.7 Pencabutan Ijin PBF
Izin PBF dinyatakan tidak berlaku apabila:
a. Masa berlakunya habis dan tidak diperpanjang;
b. Dikenai sanksi berupa penghentian sementara kegiatan; atau
c. Izin PBF dicabut.
2.1.8 Penyelenggaraan PBF
Penyelenggaraan PBF diatur dalam Peraturan Menteri Kesehatan Republik
Indonesia Nomor 1148/MENKES/PER/VI/2011 tentang PBF yang menyebutkan
bahwa PBF hanya dapat mengadakan, menyimpan dan menyalurkan obat yang
memenuhi persyaratan mutu yang ditetapkan oleh Menteri. Untuk pengadaan obat
di PBF, PBF hanya dapat melaksanakan pengadaan obat dari industri farmasi dan/
atau sesama PBF. Sedangkan PBF cabang hanya dapat melaksanakan pengadaan
obat dan/ bahan obt dari PBF pusat.
Setiap PBF harus memiliki apoteker penanggung jawab yang telah
memiliki izin yang bertanggung jawab terhadap pelaksanaan ketentuan
pengadaan, penyimpanan, dan penyaluran obat. Selain itu, apoteker penanggung
jawab dilarang merangkap jabatan sebagai direksi/ pengurus PBF. Jika terjadi
pergantian apoteker penanggung jawab, direksi/ pengurus PBF wajib melaporkan
kepada Direktur Jenderal atau Kepala Dinas Kesehatan Provinsi selambat-
lambatnya dalam jangka waktu 6 (enam) hari kerja.
PBF dalam menyelenggarakan pengadaan, penyimpanan, dan penyaluran
obat wajib menerapkan Pedoman Teknis CDOB (Badan Pengawas Obat dan
Makanan Republik Indonesia, 2012). Sertifikat CDOB akan diberikan pada PBF
yang telah menerapkan CDOB.
Setiap PBF wajib melaksanakan dokumentasi pengadaan, penyimpanan,
dan penyaluran di tempat usahanya dengan mengikuti pedoman CDOB.
Dokumentasi tersebut dapat dilakukan secara elektronik. Dokumentasi tersebut
dapat digunakan sebagai penelusuran kegiatan yang dilakukan oleh PBF dan
untuk keperluan pemeriksaan petugas yang berwenang.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
12
2.1.8.1 Pengadaan
Sebelum melakukan pengadaan obat di PBF harus dilakukan kualifikasi
yang tepat sebelum pengadaan dilaksanakan. Pemilihan pemasok, termasuk
kualifikasi dan persetujuan penunjukannya, merupakan hal operasional yang
penting. Pemilihan pemasok harus dikendalikan dengan prosedur tertulis dan
hasilnya didokumentasikan serta diperiksa ulang secara berkala. Jika obat dan/
atau bahan obat diperoleh dari industri farmasi, maka fasilitas distribusi wajib
memastikan bahwa pemasok tersebut mempunyai izin serta menerapkan prinsip
dan Pedoman CPOB sedangkan jika bahan obat diperoleh dari industri non-
farmasi yang memproduksi bahan obat dengan standar mutu farmasi, maka
fasilitas distribusi wajib memastikan bahwa pemasok tersebut mempunyai izin
serta menerapkan prinsip CPOB. Pengadaan obat dan/ atau bahan obat harus
dikendalikan dengan prosedur tertulis dan rantai pasokan harus diidentifikasi serta
didokumentasikan (Badan Pengawas Obat dan Makanan Republik Indonesia,
2012).
2.1.8.2 Penyaluran
Menurut Peraturan Menteri Kesehatan Republik Indonesia Nomor
1148/MENKES/PER/VI/2011 tentang PBF, PBF hanya dapat menyalurkan obat
kepada PBF lain, dan fasilitas pelayanan kefarmasian sesuai ketentuan peraturan
perundang-undangan, meliputi apotek, instalasi farmasi rumah sakit, puskesmas,
klinik dan toko obat (selain obat keras).
Dalam pelaksanaan penyaluran sediaan farmasi di PBF terdapat beberapa
ketentuan, yakni meliputi:
a. Penyaluran Obat
1) Untuk memenuhi kebutuhan pemerintah, PBF dapat menyalurkan obat
kepada instansi pemerintah yang dilakukan sesuai dengan ketentuan
peraturan perundang-undangan. Namun, PBF tidak dapat menyalurkan
obat keras kepada toko obat.
2) PBF hanya melaksanakan penyaluran obat berupa obat keras berdasarkan
surat pesanan yang ditandatangani apoteker pengelola apotek atau
apoteker penanggung jawab.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
13
b. Penyaluran Narkotika
Setiap PBF yang melakukan pengadaan, penyimpanan, dan penyaluran
narkotika wajib memiliki izin khusus sesuai ketentuan peraturan perundang-
undangan.
c. Penyaluran Psikotropika
Berdasarkan Undang-Undang Nomor 5 Tahun 1997 tentang Psikotropika,
penyaluran psikotropika dalam rangka peredaran dilakukan oleh pabrik obat,
pedagang besar farmasi, dan sarana penyimpanan sediaan farmasi Pemerintah.
Penyaluran psikotropika salah satunya dapat dilakukan oleh:
1) Pabrik obat kepada pedagang besar farmasi, apotek, sarana penyimpanan
sediaan farmasi pemerintah, rumah sakit, dan lembaga penelitian dan/ atau
lembaga pendidikan.
2) Pedagang besar farmasi kepada pedagang besar farmasi lain-nya, apotek,
sarana penyimpanan sediaan farmasi pemerintah, rumah sakit, dan lembaga
penelitian dan/ atau lembaga pendidikan.
Psikotropika golongan I hanya dapat disalurkan oleh pabrik obat dan
pedagang besar farmasi kepada lembaga penelitian dan/ atau lembaga pendidikan
guna kepentingan ilmu pengetahuan. Sedangkan psikotropika yang digunakan
untuk kepentingan ilmu pengetahuan hanya dapat disalurkan oleh pabrik obat dan
pedagang besar farmasi kepada lembaga penelitian dan/ atau lembaga pendidikan
atau diimpor secara langsung oleh lembaga penelitian dan/ atau lembaga
pendidikan yang bersangkutan.
Ekspor psikotropika hanya dapat dilakukan oleh pabrik obat atau
pedagang besar farmasi yang telah memiliki izin sebagai eksportir sesuai dengan
ketentuan peraturan perundang-undangan yang berlaku. Sedangkan impor
psikotropika hanya dapat dilakukan oleh pabrik obat atau pedagang besar farmasi
yang telah memiliki izin sebagai importir sesuai denganketentuan peraturan
perundang-undangan yang berlaku, serta lembaga penelitian atau lembaga
pendidikan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
14
2.1.9 Pelaporan Kegiatan PBF
Setiap PBF wajib menyampaikan laporan kegiatan setiap 3 (tiga) bulan
sekali namun dapat diminta setiap saat, meliputi kegiatan penerimaan dan
penyaluran obat kepada Direktur Jenderal dengan tembusan kepada Kepala
Badan, Kepala Dinas Kesehatan Provinsi dan Kepala Balai POM.
Setiap PBF yang menyalurkan narkotika dan psikotropika wajib
menyampaikan laporan bulanan penyaluran narkotika dan psikotropika sesuai
ketentuan peraturan perundang-undangan. Laporan tersebut dapat dilakukan
secara elektronik dengan menggunakan teknologi informasi dan komunikasi.
Selain itu, laporan tersebut harus dapat diperiksa oleh petugas yang berwenang.
2.1.10 Larangan PBF
Berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor
1148/MENKES/PER/VI/2011 tentang PBF, terdapat beberapa hal yang dilarang
untuk dilakukan di PBF, yaitu:
a. Setiap PBF dilarang menjual obat secara eceran.
b. Setiap PBF dilarang menerima dan/ atau melayani resep dokter.
2.2 Cara Distribusi Obat yang Baik (CDOB)
2.2.1 Manajemen Mutu
Fasilitas distribusi harus mempertahankan sistem mutu yang mencakup
tanggung jawab, proses dan langkah manajemen risiko terkait dengan kegiatan
yang dilaksanakan. Fasilitas distribusi harus memastikan bahwa mutu obat dan/
atau bahan obat dan integritas rantai distribusi dipertahankan selama proses
distribusi. Seluruh kegiatan distribusi harus ditetapkan dengan jelas, dikaji secara
sistematis dan semua tahapan kritis proses distribusi dan perubahan yang
bermakna harus divalidasi dan didokumentasikan. Sistem mutu harus mencakup
prinsip manajemen risiko mutu. Pencapaian sasaran mutu merupakan tanggung
jawab dari penanggung jawab fasilitas distribusi, membutuhkan kepemimpinan
dan partisipasi aktif serta harus didukung oleh komitmen manajemen puncak.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
15
Manajemen Mutu yang diuraikan dalam CDOB (2012), meliputi sistem
mutu, pengelolaan kegiatan berdasarkan kontrak, kajian dan pemantuan
manjamen, dan manajemen risiko mutu.
Dalam suatu organisasi, pemastian mutu berfungsi sebagai alat
manajemen. Harus ada kebijakan mutu terdokumentasi yang menguraikan maksud
keseluruhan dan persyaratan fasilitas distribusi yang berkaitan dengan mutu,
sebagaimana dinyatakan dan disahkan secara resmi oleh manajemen. Sistem mutu
harus memastikan bahwa:
a. Obat dan/ atau bahan obat diperoleh, disimpan, disediakan, dikirimkan atau
diekspor dengan cara yang sesuai dengan persyaratan CDOB;
b. Tanggung jawab manajemen ditetapkan secara jelas;
c. Obat dan/ atau bahan obat dikirimkan ke penerima yang tepat dalam jangka
waktu yang sesuai;
d. Kegiatan yang terkait dengan mutu dicatat pada saat kegiatan tersebut
dilakukan;
e. Penyimpangan terhadap prosedur yang sudah ditetapkan didokumentasikan
dan diselidiki;
f. Tindakan perbaikan dan pencegahan (Corrective Action Preventive Action/
CAPA) yang tepat diambil untuk memperbaiki dan mencegah terjadinya
penyimpangan sesuai dengan prinsip manajemen risiko mutu.
Sistem manajemen mutu harus mencakup pengendalian dan pengkajian
berbagai kegiatan berdasarkan kontrak. Proses ini harus mencakup manajemen
risiko mutu yang meliputi penilaian terhadap pihak yang ditunjuk, penetapan
tanggung jawab dan proses komunikasi, dan pemantauan dan pengkajian secara
teratur.
Manajemen puncak harus memiliki proses formal untuk mengkaji sistem
manajemen mutu secara periodik. Kajian tersebut mencakup
pengukuranpencapaian sasaran, penilaian indikator kinerja, peraturan, pedoman
dan hal baru yang berkaitan dengan mutu, inovasi, perubahan iklim usaha dan
bisnis.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
16
Bagian terakhir dalam manajemen mutu adalah manajemen risiko mutu
yang merupakan suatu proses sistematis untuk menilai, mengendalikan,
mengkomunikasikan dan mengkaji risiko terhadap mutu obat dan/ atau bahan
obat. Hal ini dapat dilaksanakan baik secara proaktif maupun retrospektif.
2.2.2 Organisasi, Manajemen, Personalia
Pelaksanaan dan pengelolaan sistem manajemen mutu yang baik serta
distribusi obat dan/ atau bahan obat yang benar sangat bergantung pada personil
yang menjalankannya. Harus ada personil yang cukup dan kompeten untuk
melaksanakan semua tugas yang menjadi tanggung jawab fasilitas distribusi.
Tanggung jawab masing-masing personil harus dipahami dengan jelas dan dicatat.
Semua personil harus memahami prinsip CDOB dan harus menerima pelatihan
dasar maupun pelatihan lanjutan yang sesuai dengan tanggung jawabnya.
Di dalam perusahaan harus ada struktur organisasi untuk tiap bagian yang
dilengkapi dengan bagan organisasi yang jelas. Tanggung jawab, wewenang dan
hubungan antar semua personil harus ditetapkan dengan jelas. Manajemen puncak
di fasilitas distribusi harus menunjuk seorang penanggung jawab. Penanggung
jawab harus seorang Apoteker yang memenuhi kualifikasi dan kompetensi sesuai
peraturan perundang-undangan. Selain itu setiap personil lainnya harus kompeten
dan dalam jumlah yang memadai. Perlu dilakukan pelatihan terhadap personil
secara berkala untuk meningkatkan kompetensinya. Untuk mendukung kegiatan
yang dilakukan perlu diterapkan higiene personil. Harus tersedia prosedur tertulis
berkaitan dengan higiene personil yang relevan dengan kegiatannya mencakup
kesehatan, higiene dan pakaian kerja.
2.2.3 Bangunan dan Peralatan
Fasilitas distribusi harus memiliki bangunan dan peralatan untuk menjamin
perlindungan dan distribusi obat dan/ atau bahan obat meliputi gedung,gudang
dan penyimpanan. Menurut Badan Pengawas Obat dan Makanan Republik
Indonesia (2012), persyaratan Bangunan dan Peralatan sesuai CDOB antara lain:
a. Bangunan harus dirancang dan disesuaikan untuk memastikan bahwa kondisi
penyimpanan yang baik dapat dipertahankan, mempunyai keamanan yang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
17
memadai dan kapasitas yang cukup untuk memungkinkan penyimpanan dan
penanganan obat yang baik, dan area penyimpanan dilengkapi dengan
pencahayaan yang memadai untuk memungkinkan semua kegiatan
dilaksanakan secara akurat.
b. Jika bangunan (termasuk sarana penunjang) bukan milik sendiri, maka harus
tersedia kontrak tertulis dan pengelolaan bangunan tersebut.
c. Harus ada area terpisah dan terkunci antara obat dan/ atau bahan obat yang
menunggu keputusan lebih lanjut mengenai statusnya, meliputi obat dan/ atau
bahan obat yang diduga palsu, yang dikembalikan, yang ditolak, yang akan
dimusnahkan, yang ditarik, dan yang kedaluwarsa dari obat dan/ atau bahan
obat yang dapat disalurkan.
d. Jika diperlukan area penyimpanan dengan kondisi khusus, harus dilakukan
pengendalian yang memadai untuk menjaga agar semua bagian terkait dengan
area penyimpanan berada dalam parameter suhu, kelembaban dan
pencahayaan yang dipersyaratkan.
e. Harus tersedia kondisi penyimpanan khusus untuk obat dan/ atau bahan obat
yang membutuhkan penanganan dan kewenangan khusus sesuai dengan
peraturan perundang-undangan (misalnya narkotika).
f. Harus tersedia area khusus untuk penyimpanan obat dan/ atau bahan obat yang
mengandung bahan radioaktif dan bahan berbahaya lain yang dapat
menimbulkan risiko kebakaran atau ledakan (misalnya gas bertekanan, mudah
terbakar, cairan dan padatan mudah menyala) sesuai persyaratan keselamatan
dan keamanan.
g. Area penerimaan, penyimpanan dan pengiriman harus terpisah, terlindung dari
kondisi cuaca, dan harus didesain dengan baik serta dilengkapi dengan
peralatan yang memadai.
h. Akses masuk ke area penerimaan, penyimpanan dan pengiriman hanya
diberikan kepada personil yang berwenang. Langkah pencegahan dapat berupa
sistem alarm dan kontrol akses yang memadai.
i. Harus tersedia prosedur tertulis yang mengatur personil termasuk personil
kontrak yang memiliki akses terhadap obat dan/ atau bahan obat di area
penerimaan, penyimpanan dan pengiriman, untuk meminimalkan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
18
kemungkinan obat dan/ atau bahan obat diberikan kepada pihak yang tidak
berhak.
j. Bangunan dan fasilitas penyimpanan harus bersih dan bebas dari sampah dan
debu. Harus tersedia prosedur tertulis, program pembersihan dan dokumentasi
pelaksanaan pembersihan.
k. Ruang istirahat, toilet dan kantin untuk personil harus terpisah dari area
penyimpanan.
Menurut Badan Pengawas Obat dan Makanan Republik Indonesia (2012),
persyaratan peralatan sesuai CDOB antara lain:
a. Semua peralatan untuk penyimpanan dan penyaluran obat dan/ atau bahan
obat harus didesain, diletakkan dan dipelihara sesuai dengan standar yang
ditetapkan. Harus tersedia program perawatan untuk peralatan vital, seperti
termometer, genset, dan chiller.
b. Peralatan yang digunakan untuk mengendalikan atau memonitor lingkungan
penyimpanan obat dan/ atau bahan obat harus di kalibrasi, serta kebenaran dan
kesesuaian tujuan penggunaan diverifikasi secara berkala dengan metodologi
yang tepat.
c. Kegiatan perbaikan, pemeliharaan, dan kalibrasi peralatan harus dilakukan
sedemikian rupa sehingga tidak mempengaruhi mutu obat dan/ atau bahan
obat.
d. Dokumentasi yang memadai untuk kegiatan perbaikan, pemeliharaan dan
kalibrasi peralatan utama harus dibuat dan disimpan. Peralatan tersebut
misalnya tempat penyimpanan suhu dingin, termohigrometer, atau alat lain
pencatat suhu dan kelembaban, unit pengendali udara dan peralatan lain yang
digunakan pada rantai distribusi.
2.2.4 Operasional
Semua tindakan yang dilakukan oleh fasilitas distribusi harus dapat
memastikan bahwa identitas obat dan/ atau bahan obat tidak hilang dan
distribusinya ditangani sesuai dengan spesifikasi yang tercantum pada kemasan.
Bagian operasional terdiri dari proses penerimaan, penyimpanan, pemisahan,
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
19
pemusnahan, pengambilan, pengemasan, dan pengiriman obat dan/ atau bahan
obat.
Proses penerimaan obat dan/ atau bahan obat ditujukan untuk memastikan
bahwa kiriman obat dan/ atau bahan obat yang diterima benar, berasal dari
pemasok yang disetujui, tidak rusak atau tidak mengalami perubahan selama
transportasi. Obat dan/ atau bahan obat tidak boleh diterima jika kedaluwarsa,
atau mendekati tanggal kedaluwarsa sehingga kemungkinan besar obat dan/ atau
bahan obat telah kedaluwarsa sebelum digunakan oleh konsumen. Selain itu,
nomor batch dan tanggal kedaluwarsa obat dan/ atau bahan obat harus dicatat
pada saat penerimaan, untuk mempermudah penelusuran. Jika ditemukan obat
dan/ atau bahan obat diduga palsu, batch tersebut harus segera dipisahkan dan
dilaporkan ke instansi berwenang, dan ke pemegang izin edar. Pengiriman obat
dan/ atau bahan obat yang diterima dari sarana transportasi harus diperiksa
sebagai bentuk verifikasi terhadap keutuhan kontainer/ sistem penutup, fisik dan
fitur kemasan serta label kemasan.
Proses penyimpanan dan penanganan obat dan/ atau bahan obat harus
mematuhi peraturan perundang-undangan. Kondisi penyimpanan untuk obat dan/
atau bahan obat harus sesuai dengan rekomendasi dari industri farmasi atau non-
farmasi yang memproduksi bahan obat standar mutu farmasi. Obat dan/ atau
bahan obat harus disimpan terpisah dari produk selain obat dan/ atau bahan obat
dan terlindung dari dampak yang tidak diinginkan akibat paparan cahaya
matahari, suhu, kelembaban atau faktor eksternal lain. Perhatian khusus harus
diberikan untuk obat dan/ atau bahan obat yang membutuhkan kondisi
penyimpanan khusus.
Kegiatan yang terkait dengan penyimpanan obat dan/ atau bahan obat
harus memastikan terpenuhinya kondisi penyimpanan yang dipersyaratkan
danmemungkinkan penyimpanan secara teratur sesuai kategorinya; obat dan/ atau
bahan obat dalam status karantina, diluluskan, ditolak, dikembalikan, ditarik atau
diduga palsu.
Harus diambil langkah-langkah untuk memastikan rotasi stok sesuai
dengan tanggal kedaluwarsa obat dan/ atau bahan obat mengikuti kaidah First
Expired First Out (FEFO). Obat dan/ atau bahan obat harus ditangani dan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
20
disimpan sedemikian rupa untuk mencegah tumpahan, kerusakan, kontaminasi
dan campur-baur. Obat dan/ atau bahan obat tidak boleh langsung diletakkan di
lantai. Obat dan/ atau bahan obat yang kedaluwarsa harus segera ditarik,
dipisahkan secara fisik dan diblokir secara elektronik. Penarikan secara fisik
untuk obat dan/ atau bahan obat kedaluwarsa harus dilakukan secara berkala.
Untuk menjaga akurasi persediaan stok, harus dilakukan stock opname
secara berkala berdasarkan pendekatan risiko. Perbedaan stok harus diselidiki
sesuai dengan prosedur tertulis yang ditentukan untuk memeriksa ada tidaknya
campur-baur, kesalahan keluar-masuk, pencurian, penyalahgunaan obat dan/ atau
bahan obat. Dokumentasi yang berkaitan dengan penyelidikan harus disimpan
untuk jangka waktu yang telah ditentukan.
Pemusnahan obat dan/ atau bahan obat dilaksanakan terhadap obat dan/
atau bahan obat yang tidak memenuhi syarat untuk didistribusikan. Obat dan/ atau
bahan obat yang akan dimusnahkan harus diidentifikasi secara tepat, diberi label
yang jelas, disimpan secara terpisah dan terkunci serta ditangani sesuai dengan
prosedur tertulis. Prosedur tertulis tersebut harus memperhatikan dampak terhadap
kesehatan, pencegahan pencemaran lingkungan dan kebocoran/ penyimpangan
obat dan/ atau bahan obat kepada pihak yang tidak berwenang.
Proses pengambilan obat dan/ atau bahan obat harus dilakukan dengan
tepat sesuai dengan dokumen yang tersedia untuk memastikan obat dan/ atau
bahan obat yang diambil benar. Obat dan/ atau bahan obat yang diambil harus
memiliki masa simpan yang cukup sebelum kedaluwarsa dan berdasarkan sistem
FEFO. Nomor batch obat dan/ atau bahan obat harus dicatat. Pengecualian dapat
diizinkan jika ada kontrol yang memadai untuk mencegah pendistribusian obat
dan/ atau bahan obat kedaluwarsa.
Obat dan/ atau bahan obat harus dikemas sedemikian rupa sehingga
kerusakan, kontaminasi dan pencurian dapat dihindari. Kemasan harus memadai
untuk mempertahankan kondisi penyimpanan obat dan/ atau bahan obat selama
transportasi. Kontainer obat dan/ atau bahan obat yang akan dikirimkan harus
disegel.
Pengiriman obat dan/ atau bahan obat harus ditujukan kepada pelanggan
yang mempunyai izin sesuai dengan peraturan perundang-undangan. Untuk
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
21
penyaluran obat dan/ atau bahan obat ke pihak yang berwenang atau berhak untuk
keperluan khusus, seperti penelitian, special access dan uji klinik, harus
dilengkapi dengan dokumen yang mencakup tanggal, nama obat dan/ atau bahan
obat, bentuk sediaan, nomor batch, jumlah, nama dan alamat pemasok, nama dan
alamat pemesan atau penerima. Proses pengiriman dan kondisi penyimpanan
harus sesuai dengan persyaratan obat dan/ atau bahan obat dari industri farmasi.
Dokumentasi harus disimpan dan mampu tertelusur. Dokumen untuk pengiriman
obat dan/ atau bahan obat harus disiapkan dan harus mencakup sekurang-
kurangnya informasi berikut:
a. Tanggal pengiriman;
b. Nama lengkap, alamat (tanpa akronim), nomor telepon dan status dari
penerima (misalnya Apotek, rumah sakit atau klinik);
c. Deskripsi obat dan/ atau bahan obat, misalnya nama, bentuk sediaan dan
kekuatan (jika perlu);
d. Nomor batch dan tanggal kedaluwarsa;
e. Kuantitas obat dan/ atau bahan obat, yaitu jumlah kontainer dan kuantitas per
kontainer (jika perlu);
f. Nomor dokumen untuk identifikasi order pengiriman;
g. Transportasi yang digunakan mencakup nama dan alamat perusahaan
ekspedisi serta tanda tangan dan nama jelas personil ekspedisi yang menerima
(jika menggunakan jasa ekspedisi) dan kondisi penyimpanan.
2.2.5 Inspeksi Diri
Inspeksi diri adalah inspeksi yang dilakukan oleh diri sendiri terhadap
sistem. Inspeksi diri dilakukan untuk mengukur kinerja dan mengetahui
apakahsistem yang direncanakan dan dijalankan sudah memenuhi standar.
Inspeksi diri dilembaga distribusi obat dilakukan secara periodik. Inspeksi diri
harus dilakukan dalam rangka memantau pelaksanaan dan kepatuhan terhadap
pemenuhan CDOB dan untuk bahan tindak lanjut langkah-langkah perbaikan
yang diperlukan.
Program inspeksi diri harus dilaksanakan dalam jangka waktu yang
ditetapkan dan mencakup semua aspek CDOB serta kepatuhan terhadap peraturan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
22
perundang-undangan, pedoman dan prosedur tertulis. Inspeksi diri tidak hanya
dilakukan pada bagian tertentu saja.
Inspeksi diri harus dilakukan dengan cara yang independen dan rinci oleh
personil yang kompeten dan ditunjuk oleh perusahaan. Audit eksternal yang
dilakukan oleh ahli independen dapat membantu, namun tidak bisa dijadikan
sebagai satu-satunya cara untuk memastikan kepatuhan terhadap penerapan
CDOB.
Audit terhadap kegiatan yang disubkontrakkan harus menjadi bagian dari
program inspeksi diri. Semua pelaksanaan inspeksi diri harus dicatat. Laporan
harus berisi semua pengamatan yang dilakukan selama inspeksi. Salinan laporan
tersebut harus disampaikan kepada manajemen dan pihak terkait lainnya. Jika
dalam pengamatan ditemukan adanya penyimpangan dan/ atau kekurangan, maka
penyebabnya harus diidentifikasi dan dibuat CAPA. CAPA harus
didokumentasikan dan ditindaklanjuti.
2.2.6 Keluhan, Obat dan/ atau Bahan Obat Kembalian, Diduga Palsu, dan
Penarikan Kembali
Jika terjadi keluhan maka semua keluhan dan informasi lain tentang obat
dan/ atau bahan obat berpotensi rusak harus dikumpulkan, dikaji dan diselidiki
sesuai dengan prosedur tertulis serta harus tersedia dokumentasi untuk setiap
proses penanganan keluhan termasuk pengembalian dan penarikan kembali serta
dilaporkan kepada pihak yang berwenang. Jika obat ternyata dapat dijual kembali
maka harus melalui persetujuan dari personil yang bertanggung jawab sesuai
dengan kewenangannya. Adapun persyaratan obat dan/ atau bahan obat yang
layak dijual kembali, antara lain jika:
a. Obat dan/ atau bahan obat dalam kemasan asli dan kondisi yang memenuhi
syarat serta memenuhi ketentuan;
b. Obat dan/ atau bahan obat kembalian selama pengiriman dan penyimpanan
ditangani sesuai dengan kondisi yang dipersyaratkan;
c. Obat dan/ atau bahan obat kembalian diperiksa dan dinilai oleh penanggung
jawab atau personil yang terlatih, kompeten dan berwenang;
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
23
d. Fasilitas distribusi mempunyai bukti dokumentasi tentang kebenaran asal-usul
obat dan/ atau bahan obat termasuk identitas obat dan/ atau bahan obat untuk
memastikan bahwa obat dan/ atau bahan obat kembalian tersebut bukan obat
dan/ atau bahan obat palsu.
Sedangkan untuk obat dan/ atau bahan obat diduga palsu, penyalurannya
harus dihentikan, segera dilaporkan ke instansi terkait dan menunggu tindak lanjut
dari instansi yang berwenang. Setelah ada pemastian bahwa obat dan/ atau bahan
obat tersebut palsu, maka harus segera ditindaklanjuti sesuai dengan instruksi dari
instansi yang berwenang.
2.2.7 Transportasi
Selama proses transportasi, harus diterapkan metode transportasi yang
memadai. Obat dan/ atau bahan obat harus diangkut dengan kondisi penyimpanan
sesuai dengan informasi pada kemasan. Metode transportasi yang tepat harus
digunakan mencakup transportasi melalui darat, laut, udara atau kombinasi di
atas. Apapun moda transportasi yang dipilih, harus dapat menjamin bahwa obat
dan/ atau bahan obat tidak mengalami perubahan kondisi selama transportasi yang
dapat mengurangi mutu. Pendekatan berbasis risiko harus digunakan ketika
merencanakan rute transportasi.
Obat dan/ atau bahan obat dan kontainer pengiriman harus aman untuk
mencegah akses yang tidak sah. Kendaraan dan personil yang terlibat dalam
pengiriman harus dilengkapi dengan peralatan keamanan tambahan yang sesuai
untuk mencegah pencurian obat dan/ atau bahan obat dan penyelewengan lainnya
selama transportasi. Kondisi penyimpanan yang dipersyaratkan untuk obat dan/
atau bahan obat harus dipertahankan selama transportasi sesuai dengan
yangditetapkan pada informasi kemasan. Jika menggunakan kendaraan
berpendingin, alat pemantau suhu selama transportasi harus dipelihara dan
dikalibrasi secara berkala atau minimal sekali setahun. Persyaratan ini meliputi
pemetaan suhu pada kondisi yang representatif dan harus mempertimbangkan
variasi musim. Jika diperlukan, pelanggan dapat memperoleh dokumen data suhu
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
24
untuk menunjukkan bahwa obat dan/ atau bahan obat tetap dalam kondisi suhu
penyimpanan yang dipersyaratkan selama transportasi.
2.2.8 Fasilitas Distribusi Berdasarkan Kontrak
Cakupan kegiatan kontrak terutama yang terkait dengan keamanan, khasiat
dan mutu obat dan/ atau bahan obat meliputi kontrak antar fasilitas distribusi dan
kontrak antara fasilitas distribusi dengan pihak penyedia jasa antara lain
transportasi, pengendalian hama, pergudangan, kebersihan dan sebagainya. Semua
kegiatan kontrak harus tertulis antara pemberi kontrak dan penerima kontrak serta
setiap kegiatan harus sesuai dengan persyaratan CDOB.
Pemberi kontrak bertanggung jawab untuk menilai kompetensi yang
diperlukan oleh penerima kontrak. Pemberi kontrak harus melakukan pengawasan
terhadap penerima kontrak dalam melaksanakan tugas yang dikontrakkan sesuai
dengan prinsip dan pedoman CDOB. Penerima kontrak harus memiliki tempat,
personil yang kompeten, peralatan, pengetahuan dan pengalaman dalam
melaksanakan tugas yang dikontrakkan oleh pemberi kontrak. Penerima kontrak
tidak diperbolehkan untuk mengalihkan pekerjaan yang dipercayakan oleh
pemberi kontrak kepada pihak ketiga sebelum dilakukannya evaluasi, dan
mendapatkan persetujuan dari pemberi kontrak serta dilakukannya audit ke pihak
ketiga tersebut.
2.2.9 Dokumentasi
Dokumentasi merupakan dokumen tertulis terkait dengan distribusi
(pengadaan, penyimpanan, penyaluran dan pelaporan), prosedur tertulis dan
dokumen lain yang terkait dengan pemastian mutu. Menurut Cara Distribusi Obat
yang Baik (CDOB), dokumentasi yang baik merupakan bagian penting dari sistem
manajemen mutu.Dokumentasi dilakukan dengan tujuan sebagai berikut :
a. Menjamin semua pelaksanaan distribusi berjalan sesuai dengan panduan mutu
dan ketentuan perundang-undangan yang berlaku.
b. Apabila terjadi penyelewengan sistem, maka dapat ditelusuri dengan sistem
dokumentasi perjalanan distribusi.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
25
c. Untuk mencegah kesalahan dari komunikasi lisan dan untuk memudahkan
penelusuran, antara lain sejarah batch, instruksi dan prosedur, maka
dokumentasi harus tertulis jelas.
Dokumentasi terdiri dari semua prosedur tertulis, petunjuk, kontrak,
catatan dan data, dalam bentuk kertas maupun elektronik. Dicatat dengan jelas dan
rinci merupakan dasar untuk memastikan bahwa setiap personil melaksanakan
kegiatan, sesuai uraian tugas sehingga memperkecil risiko kesalahan.
Dokumentasi distribusi harus mencakup informasi berikut:
a. Tanggal;
b. Nama obat dan/ atau bahan obat;
c. Nomor batch;
d. Tanggal kedaluwarsa;
e. Jumlah yang diterima/ disalurkan;
f. Nama dan alamat pemasok/ pelanggan.
Dokumentasi harus dibuat pada saat kegiatan berlangsung, sehingga
mudah untuk ditelusuri. Dokumentasi harus komprehensif mencakup ruang
lingkup kegiatan fasilitas distribusi dan ditulis dalam bahasa yang jelas,
dimengerti oleh personil dan tidak berarti ganda. Prosedur tertulis harus disetujui,
ditandatangani dan diberi tanggal oleh personil yang berwenang. Prosedur tertulis
tidak ditulis tangan dan harus tercetak.
Setiap perubahan yang dibuat dalam dokumentasi harus ditandatangani,
diberi tanggal dan memungkinkan pembacaan informasi yang asli. Jika
diperlukan, alasan perubahan harus dicatat dan seluruh dokumentasi harus tersedia
sebagaimana mestinya. Semua dokumentasi harus mudah didapat kembali,
disimpan dan dipelihara pada tempat yang aman untuk mencegah dari perubahan
yang tidak sah, kerusakan dan/ atau kehilangan dokumen. Dokumen yang
dibuatharus disimpan dalam waktu sekurang-kurangnya 3 tahun dari tanggal
pembuatan dokumen.
Dokumentasi permanen, tertulis atau dengan elektronik, untuk setiap obat
dan atau bahan obat yang disimpan harus menunjukkan kondisi penyimpanan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
26
yang direkomendasikan, tindakan pencegahan dan tanggal uji ulang khusus untuk
bahan obat (jika ada) harus diperhatikan. Persyaratan farmakope dan peraturan
nasional terkini tentang label dan wadah harus dipatuhi.
Dokumen yang dibuat harus dikaji ulang secara berkala dan dijaga agar
selalu up to date. Jika suatu dokumen direvisi, harus dijalankan suatu sistem untuk
menghindarkan penggunaan dokumen yang sudah tidak berlaku.
2.2.9.1 Pelaporan Kegiatan di PBF ke Institusi Terkait
Menurut pasal 8 Peraturan Menteri Kesehatan Republik Indonesia Nomor
1148/MENKES/Per/VI/2011 tentang pedagang besar farmasi :
a. Setiap PBF dan cabangnya wajib menyampaikan laporan kegiatan setiap 3
(tiga) bulan sekali meliputi kegiatan penerimaan dan penyaluran obat dan/
atau bahan obat kepada Direktur Jenderal dengan tembusan kepada Kepala
Badan, Kepala Dinas Kesehatan Provinsi dan Kepala Balai POM.
b. Selain laporan kegiatan sebagaimana dimaksud pada ayat (1), Direktur
Jenderal setiap saat dapat meminta laporan kegiatan penerimaan dan
penyaluran obat dan/ atau bahan obat.
c. Setiap PBF dan PBF cabang yang menyalurkan narkotika dan psikotropika
wajib menyampaikan laporan bulanan penyaluran narkotika dan psikotropika
sesuai ketentuan peraturan perundang-undangan.
d. Laporan sebagaimana dimaksud pada ayat (1) dan ayat (2) dapat dilakukan
secara elektronik dengan menggunakan teknologi informasi dan komunikasi.
e. Laporan sebagaimana dimaksud pada ayat (4) setiap saat harus dapat diperiksa
oleh petugas yang berwenang.
2.2.9.2 Pelaporan Narkotika dan Psikotropika
Menurut Undang-Undang Republik Indonesia Nomor 35 Tahun 2009
tentang narkotika, Pasal 14 ayat 2 industri farmasi, pedagang besar farmasi,
saranapenyimpanan sediaan farmasi pemerintah, apotek, rumah sakit, pusat
kesehatan masyarakat, balai pengobatan, dokter, dan lembaga ilmu pengetahuan
wajib membuat, menyampaikan, dan menyimpan laporan berkala mengenai
pemasukan dan/ atau pengeluaran narkotika yang berada dalam penguasaannya.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
27
Dokumen pelaporan mengenai narkotika yang berada di bawah
kewenangan Badan Pengawas Obat dan Makanan, disimpan dengan ketentuan
sekurang-kurangnya dalam waktu 3 (tiga) tahun. Maksud adanya kewajiban untuk
membuat, menyimpan, dan menyampaikan laporan adalah agar pemerintah setiap
waktu dapat mengetahui tentang persediaan narkotika yang ada di dalam
peredaran dan sekaligus sebagai bahan dalam penyusunan rencana kebutuhan
tahunan narkotika.
Menurut Peraturan Menteri Kesehatan Republik Indonesia Nomor
912/MENKES/PER/VIII/1997 tentang kebutuhan dan pelaporan psikotropika.
Pasal 7 ayat 1 pabrik obat dan pedagang besar farmasi yang menyalurkan
psikotropika wajib mencatat dan melaporkan psikotropika setiap bulan dengan
menggunakan formulir laporan penyaluran psikotropika.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 3
TINJAUAN KHUSUS
3.1 PT. KIMIA FARMA TRADING AND DISTRIBUTION
3.1.1 Sejarah Pendirian Perusahaan
Kimia Farma merupakan pioneer dalam industri farmasi di Indonesia. Asal
mula berdirinya perusahaan dapat dirunut balik ke tahun 1997, ketika NV
Chemicalien Handle Rathkamp and Co, perusahaan farmasi pertama di Hindia
Timur didirikan pada tahun 1871. Sejalan dengan kebijakan nasional bekas
perusahaan-perusahaan Belanda, pada tahun 1958 pemerintah melebur sejumlah
perusahaan farmasi menjadi Bhineka Kimia Farma (PNF). Selanjutnya pada
tanggal 16 Agustus 1971, bentuk badan hukumnya diubah menjadi PT. Kimia
Farma (Persero).
Sejak tanggal 4 Juli 2001, Kimia Farma tercatat sebagai perusahaan publik
di Bursa Efek Jakarta dan Surabaya. Pada tanggal 28 Juni 2001, PT. Kimia Farma
(Persero) menjadi Perusahaan Terbuka (Tbk.) dengan nama PT. Kimia Farma
Tbk., dimana untuk privatisasi tahap I saham yang lepas adalah sebanyak 9%
dengan rincian 3% untuk program Kepemilikan Saham Karyawan dan
Manajemen (KSKM) PT. Kimia Farma, dan sebanyak 6% untuk masyarakat
umum.
Berbekal atas tradisi industri yang panjang selama lebih dari 195 tahun dan
nama yang identik dengan mutu, saat ini Kimia Farma telah berkembang menjadi
sebuah perusahaan pelayanan kesehatan utama di Indonesia yang kian memainkan
peranan penting dalam pengembangan, pembangunan bangsa dan masyarakat.
Bisnis Kimia Farma meliputi antara lain:
a. PT. Kimia Farma Tbk. (Holding)
PT. Kimia Farma Tbk. dibentuk pada tanggal 16 Agustus 1971 dengan
jalur usaha pelayanan kesehatan. Sebagai perusahaan publik sekaligus Badan
Usaha Milik Negara (BUMN), Kimia Farma berkomitmen penuh untuk
melaksanakan tata kelola perusahaan yang baik sebagai suatu kebutuhan sekaligus
kewajiban sebagaimana diamanatkan Undang-Undang Nomor 19 tahun 2003
tentang BUMN. PT. Kimia Farma Tbk., merupakan sebuah perusahaan pelayanan
28 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
29
kesehatan yang terintegrasi, bergerak dari hulu ke hilir yaitu industri, marketing,
retail, laboratorium klinik dan klinik kesehatan. Pada tanggal 4 januari 2003 PT.
Kimia Farma Tbk. membentuk 2 anak perusahaan yaitu: PT. Kimia Farma Health
and Care dan PT. Kimia Farma Trading and Distribution.
b. Anak Perusahaan (Subsidiaries)
1) PT. Kimia Farma Apotek
Perusahaan ini dibentuk pada tanggal 4 Januari 2003 dengan jalur usaha
Farmasi. Pada akhir tahun 2012 PT. Kimia Farma Apotek (KFA) mengelola
sebanyak 412 apotek, 64 klinik kesehatan dan 33 laboraturium klinik. KFA
menyediakan layanan kesehatan yang terintegrasi meliputi layanan farmasi
(apotek), klinik kesehatan, laboraturium klinik dan optik, dengan konsep One Stop
Health Care Solution (OSHcS) sehingga memudahkan masyarakat mendapatkan
layanan berkualitas. Pelayanan farmasi menggunakan standar Good Pharmacy
Practice (GPP) yaitu standar internasional yang diterbitkan oleh The International
Pharmaceutical Federation serta standar yang ditetapkan oleh Kementrian
Kesehatan Republik Indonesia tentang Standar Pelayanan Kefarmasiaan di
Apotek.
Pada tahun 2012, jumlah tenaga kerja KFA adalah 2.535 orang, yang
sebagian besar tenaga apoteker yang memiliki sertifikat kompetensi dari
organisasi Ikatan Apoteker Indonesia (IAI) dan didukung oleh Asisten Apoteker
yang terlatih.
2) PT. Kimia Farma Trading and Distribution
Perusahaan ini dibentuk pada tanggal 4 Januari 2003, dengan jalur usaha
distribusi obat dan alat kesehatan. PT. Kimia Farma (Persero) Tbk. PT. Kimia
Farma Trading and Distribution (KFTD) sebelumnya merupakan divisi yang
bergerak dibidang yang sama, yaitu perdagangan dan distribusi. Oleh karena itu
pengalamannya bukan baru sepuluh tahun, tetapi sama dengan umur PT. Kimia
Farma Tbk. sendiri.
Sebelum menjadi perusahaan tersendiri, PT. Kimia Farma Trading and
Distribution (KFTD) dahulu merupakan divisi Pedagang Besar Farmasi (PBF)
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
30
dari PT Kimia Farma Tbk. yang memiliki tugas utama mendistribusikan produk-
produk farmasi yang diproduksi PT. Kimia Farma Tbk. ke channel-channel yang
tersebar di seluruh nusantara.
Berbekal kemampuan serta pengalaman menangani pendistribusian
produk-produk PT Kimia Farma Tbk. sejak tahun 1917, pada tanggal 4 Januari
2003 divisi Pedagang Besar Farmasi ini kemudian berkembang menjadi anak
perusahaan dengan nama PT. Kimia Farma Trading and Distribution, yang
berbasis Jasa Layanan Perdagangan dan Distribusi.
PT. Kimia Farma Trading and Distribution (KFTD) adalah anak
perusahaan PT. Kimia Farma Tbk. yang didirikan berdasarkan akta pendirian No.
07 tanggal 4 Januari 2003 yang dibuat di hadapan Notaris Ny. Imas Fatimah, S.H
di Jakarta dan telah diubah dengan akta No.42 tanggal 22 April 2003 yang dibuat
di hadapan Notaris Nila Noordjasmani Soeyasa Besar, S.H. Akta ini telah
mendapat persetujuan dari Menteri Kehakiman dan Hak Manusia Republik
Indonesia dengan surat keputusan No: C-09648 HT.01.01 TH 2003 tanggal 1 Mei
2003.
Untuk memudahkan operasionalnya, KFTD juga didukung oleh 44 kantor
cabang (6 cabang kelas 1, 32 cabang kelas 2 dan 7 cabang kelas 3) dengan
wilayah operasinya mulai dari Aceh sampai dengan Jayapura, jumlah salesman
450 orang dan armada pengantar roda 4 (mobil box) 477 unit dan pengantar roda 2
(motor box) 292 unit. Jaringan distribusi ini melayani lebih dari 31 rekanan
principal, memenuhi kebutuhan sekitar 13.963 apotek, 1.527 Pedagang Besar
Farmasi (PBF), 3.691 toko obat, 106 horeka (hotel restoran karaoke), 1.975 rumah
sakit, 6.572 pasar tradisional dan 2.074 pasar modern.
3.1.2 Visi dan Misi
3.1.2.1 Visi
Menjadi perusahaan terkemuka dibidang distribusi dan perdagangan
produk kesehatan (to be the greatest trading and distribution company).
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
31
3.1.2.2 Misi
Misi PT. Kimia Farma Tbk. ialah sebagai berikut:
a. Meningkatkan jumlah jaringan distribusi produk kesehatan baik produk sendiri
maupun principal pihak ketiga.
b. Meningkatkan perdagangan dan pengadaan produk kesehatan di pasar institusi.
c. Meningkatkan perdagangan alat kesehatan dan diagnostik keagenan atau
private label.
3.1.3 Strategi
Dalam menjalankan kegiatannya, strategi yang diterapkan antara lain
sebagai berikut:
a. Cost leadership guna menciptakan comparative advantages.
b. Product differentiation jenis produk unggulan guna meningkatkan competitive
advantages.
3.1.4 Sistem Pengadaan dan Pendistribusian Barang
Sesuai dengan anggaran dasarnya, perusahaan melakukan usaha dalam
bidang Distribusi dan Perdagangan, yang produknya meliputi produk farmasi dan
alat kesehatan. Principal meliputi principal perusahaan induk (PT. Kimia Farma
Tbk) sebesar 60% dan principal pihak ketiga 40%, seperti Biofarma, Janssen,
Otsuka, Daria Varia, Rohto, Novartis, dan lain-lain.
Sebagai penyedia Jasa Layanan Distribusi, KFTD menyalurkan aneka
produk dari perusahaan induk, produk dari principal lainnya, serta produk-produk
non-principal. Di bidang jasa perdagangan atau trading, KFTD menangani
kontrak-kontrak bisnis yang didapat melalui sistem tender.
3.1.5 Jenis Pelanggan KFTD (Channel Distribution)
Sesuai dengan jenis penjualannya, Pelanggan KFTD terdiri dari :
a. Pelanggan reguler adalah pelanggan yang membeli produk secara rutin, tanpa
melalui pelelangan (tender). Sesuai dengan Permenkes Nomor
1148/Menkes/Per/VI/2011 tentang PBF, pelanggan reguler terdiri dari:
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
32
1) Pedagang Besar Farmasi (PBF)
2) Instalasi Farmasi Rumah Sakit
3) Puskesmas
4) Klinik
5) Apotek
6) Toko obat
b. Pelanggan Institusi adalah pelanggan yang membeli produk secara paket
melalui pelelangan terbuka (tender) atau penunjukan langsung. Sesuai dengan
Perpres No. 70 Tahun 2012 tentang Pengadaan Barang dan Jasa oleh
Pemerintah, pelanggan institusi terdiri dari :
1) Kementerian (Kementerian Kesehatan, Kementerian Agama, Kementerian
Tenaga Kerja, dan sebagainya)
2) Lembaga (BKKBN, BPOM, Universitas, dan sebagainya)
3) Satuan kerja perangkat daerah (Dinas kesehatan)
4) Institusi (Rumah Sakit)
3.2 Manajemen Operasional
Manajemen operasional adalah suatu cara pengelolaan fungsi-fungsi
kegiatan (fungsi-fungsi manajemen) yang terdapat dalam suatu perusahaan, untuk
mencapai tujuan. Cara pengelolaan pada setiap fungsi kegiatan berbeda antara
fungsi kegiatan yang dengan yang lainnya, karena pada setiap fungsi kegiatan
tersebut memiliki tujuan yang berbeda.
a. Fungsi kegiatan pembelian, yaitu memperoleh harga beli barang yang efisien
dan menjaga ketersediaan (availability) barang.
b. Fungsi kegiatan pengelolaan barang di gudang (warehousing), yaitu menjaga
kondisi kualitas barang sesuai persyaratan Farmakope, tidak rusak dan tidak
hilang.
c. Fungsi kegiatan penjualan dan pelayanan, yaitu memperoleh pertumbuhan
penjualan (sales growth) dan jumlah pelanggan (customer growth) serta untuk
mempertahankan pelanggan yang loyal (customer rate retention).
d. Fungsi kegiatan pengelolaan piutang (accounting), untuk menjaga likuiditas
keuangan dan aliran kas (cash flow) yang sehat.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
33
e. Fungsi kegiatan pembukuan atau tata usaha, yaitu menyajikan laporan yang
tepat waktu, isi dan guna agar dapat mengambil keputusan dengan cepat dan
tepat.
3.2.1 Manajemen Pengadaan
3.2.1.1 Definisi
Pengadaan merupakan proses penyediaan obat yang dibutuhkan, yang
diperoleh dari pemasok eksternal melalui pembelian dari manufaktur, distributor,
atau pedagang besar farmasi.
3.2.1.2 Tujuan
Manajemen pengadaan dilakukan untuk menyediakan obat atau bahan obat
untuk memenuhi kebutuhan stok di gudang.
3.2.1.3 Tugas dan Tanggung Jawab
Tugas dan Tanggung jawab seorang supervisor pembelian di KFTD yaitu:
a. Bertugas dan bertanggung jawab membuat rencana pembelian.
b. Bertugas dan bertanggung jawab memantau hasil pembelian dengan cara
memeriksa copy faktur yang diterima terhadap kelengkapan barang, dan
kebenaran harga.
c. Bertugas dan bertanggung jawab mengevaluasi hasil pembelian.
d. Bertugas dan bertanggung jawab terhadap kelancaran penyediaan barang
dagangan.
e. Bertugas dan bertanggung jawab atas pilihannya dalam menentukan supplier.
3.2.1.4 Standard Operational and Procedure Pengadaan Barang
Tahapan dalam melakukan pengadaan barang di KFTD adalah sebagai berikut:
a. Membuat daftar rencana pembelian barang
Petugas logistik (kepala gudang) bersama petugas penjualan menghitung
buffer stock dan kebutuhan level stock per item barang setiap bulan berdasarkan
data historis, lalu data tersebut dikirim ke petugas pembelian untuk membuat
daftar rencana pembelian barang setiap bulannya.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
34
b. Membuat kontrak pembelian barang
Petugas pembelian melakukan perjanjian kontrak pembelian barang
dengan pemasok atau principal untuk memperoleh margin yang lebih besar dan
masa tenggang pembayaran relatif lebih panjang.
c. Mengeksekusi pembelian barang
Petugas pembelian menyiapkan Surat Pesanan (SP), ditandatangani oleh
penanggung jawab logistik atau penanggung jawab PBF, lalu mengirimkan SP ke
principal atau pemasok.
d. Menerima dan memeriksa barang
Petugas logistik memeriksa dan menerima fisik barang dari pemasok
sesuai dengan SP dan faktur barang, lalu membuat tanda terima barang di faktur
(stempel dan tanda tangan) petugas gudang.
e. Memeriksa kebenaran faktur pembelian barang
Petugas pembelian faktur mengenai jumlah, jenis, harga barang dan diskon
serta masa tenggang pembayaran, lalu memberikan paraf dan mengirimkan faktur
pembelian ke fungsi tata usaha (TU).
f. Membukukan faktur pembelian sebagai pembelian dan hutang
Petugas TU membukukan faktur tersebut sebagai pembelian barang dan
hutang di kartu hutang lalu membuat laporan pembelian dan hutang setiap
bulannya.
Gambar 3.1. Diagram pengadaan barang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
35
3.2.1.5 Sasaran
Sasaran mutu dari manajemen pengadaan yaitu memperoleh harga barang
yang lebih murah (lebih efisien) serta dapat melayani seluruh kebutuhan barang
pelanggan (service level) 100%.
3.2.1.6 Indikator
Indikator yang digunakan untuk mencapai sasaran diatas adalah sebagai berikut:
a. Harga pokok penjualan (HPP)
1) Jika HPP yang diperoleh < dari HPP tahun lalu (PBF pesaing), maka fungsi
pembelian berfungsi dengan baik.
2) Jika HPP yang diperoleh > dari HPP tahun lalu (PBF pesaing), maka fungsi
pembelian tidak berfungsi dengan baik.
b. Service level
1) Jika service level > dari service level tahun lalu, maka fungsi pembelian
berfungsi dengan baik.
2) Jika service level < dari service level tahun lalu, maka fungsi pembelian
tidak berfungsi dengan baik.
3.2.2 Manajemen Penyimpanan
3.2.2.1 Definisi
Penyimpanan adalah suatu kegiatan menyimpan dan memelihara dengan
cara menempatkan perbekalan farmasi yang diterima pada tempat yang dinilai
aman dari pencurian serta gangguan fisik yang dapat merusak mutu obat.
3.2.2.2 Tujuan
Tujuan adanya manajemen penyimpanan ialah untuk memastikan bahwa
obat atau bahan obat yang disimpan sesuai dengan rekomendasi dari industri
farmasi atau non farmasi.
3.2.2.3 Tugas dan Tanggung Jawab
a. Bertugas dan bertanggung jawab memeriksa kebenaran produk (fisik item,
bets) di gudang pengeluaran barang yang akan didistribusikan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
36
b. Bertugas dan bertanggung jawab memvalidasi administrasi atas kebenaran
mutasi pengeluaran dalam sistem informasi logistik sentral.
c. Bertugas dan bertanggung jawab menyerahkan produk yang telah divalidasi ke
masing-masing gudang tujuan hantaran.
d. Bertugas dan bertanggung jawab meningkatkan ketepatan dan kecepatan proses
pengeluaran barang.
e. Bertugas dan bertanggung jawab melaksanakan dokumentasi pengeluaran
barang yang sistematis, tertib, rapi, bersih, dan mudah dicari.
f. Bertugas dan bertanggung jawab membina SDM dalam jajaran fungsi kerjanya
agar memiliki kemampuan dalam melaksanakan business process di
pengeluaran barang yang efektif dan efisien sesuai fungsinya.
3.2.2.4 Sistem Penyimpanan Barang di Gudang
Sesuai dengan SK Kepala BPOM No. HK 00.05.3.252 tahun 2003, bangunan dan
peralatan harus memenuhi beberapa persyaratan.
a. Sistem penyimpanan obat di gudang dalam kegiatan distribusi berdasarkan
sistem first expired first out (FEFO) atau sistem first in first out (FIFO).
b. Kondisi fisik bangunan :
1) Memiliki sirkulasi udara yang baik
2) Tidak boleh banjir
3) Tidak boleh ada rembesan air tanah
4) Tidak boleh ada binatang, serangga dan tikus serta binatang lain yang dapat
mempengaruhi kualitas obat dan bahan obat
5) Selalu dalam keadaan bersih dan rapih
c. Suhu dan kelembaban udara harus sesuai dengan sifat obat dan bahan obatnya
yang ditetapkan Farmakope Indonesia Indonesia, seperti:
1) Disimpan pada suhu kamar (pada suhu 15-30 oC), untuk obat tablet, kaplet,
sirup, infus atau ditentukan lain.
2) Disimpan pada tempat sejuk (pada suhu 5-15 oC), untuk minyak atsiri, salep
mata, krim, ovula, suppositoria, tingtur.
3) Disimpan ditempat dingin (pada suhu 0–5oC), untuk vaksin atau ditentukan
lain.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
37
d. Layout ruangan meliputi:
1) Ruang penerimaan dan pemeriksaan barang masuk (transito in)
2) Ruang penyimpanan barang
3) Ruang pengeluaran dan pemeriksaan barang keluar (transito out)
e. Alokasi ruangan meliputi:
1) Ruang barang tidak kedaluwarsa
2) Ruang narkotika
3) Ruang psikotropika
4) Ruang barang–barang kedaluwarsa
f. Persyaratan peralatan
1) Alat penyimpanan barang, seperti rak dan paletnya
2) Alat pengukur suhu ruangan serta dokumen data kalibrasinya
3) Alat pengangkut barang di gudang, sepeti forklift, trolley dan tangga
4) Alat pengirim barang bersuhu 5-15oC, seperti cooler box
3.2.2.5 Penataan Alokasi Ruang Penyimpanan di Gudang
Sesuai dengan ketentuan peraturan yang ditetapkan Pemerintah tersebut
diatas dan berdasarkan sifat obatnya sendiri, maka ruang penyimpanan obat dibagi
menjadi 6 yaitu:
a. Ruang penyimpanan obat bersuhu 15-30oC, seperti untuk obat tablet, kaplet,
sirup atau ditentukan lain.
b. Ruang penyimpanan obat bersuhu 5–15oC, seperti untuk minyak atsiri, salep,
krim, ovula, suppositoria, tingtur, eter, floatane, halotane.
c. Ruang penyimpanan obat bersuhu 0-5oC, seperti untuk obat vaksin dan serum
atau ditentukan lain.
d. Ruang penyimpanan narkotika sesuai dengan peraturan yang berlaku.
e. Ruang penyimpanan psikotropika sesuai dengan peraturan yang berlaku.
f. Ruang penyimpanan obat kedaluwarsa.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
38
3.2.2.6 Kelengkapan Peralatan Gudang
Kelengkapan peralatan gudang sesuai kebijakan KFTD yaitu:
a. Alat pemeliharaan gedung: generator, alat pemadam kebakaran, alat kebersihan
dan tempat sampah.
b. Alat pemeriksaan dan penerimaan barang: komputer, barcode scanner, trolley
dan stempel.
c. Kelengkapan alat penyimpan barang: AC, lemari narkotika, rak besi dan palet,
trolley, tangga dan forklift
d. Kelengkapan alat pengeluaran barang: komputer, barcode scanner, trolley,
forklift dan buku ekspedisi pengeluaran barang.
e. Kelengkapan alat K3 (Kesehatan dan Keselamatan Kerja): helm, sepatu dan
rompi.
f. Kelengkapan alat pengiriman barang: mobil box dan sepeda motor box.
3.2.2.7 Standard Operational and Procedure Penerimaan, Penyimpanan, dan
Pengeluaran Barang
a. Menerima barang di transito in
1) Petugas logistik memeriksa dan menerima fisik barang dari pemasok sesuai
dengan SP dan faktur barang, di ruang transito in.
2) Membuat tanda terima barang (stempel atau paraf) di faktur pembelian.
3) Menyimpan dan memasukkan data barang pada sistem informasi.
b. Menyimpan barang
1) Petugas logistik memasukkan barang dari ruang transito in ke ruang
penyimpanan sesuai dengan lokasinya masing–masing barang.
2) Mencatat barang masuk di sistem informasi dan masing–masing kartu
barangnya.
3) Melaporkan penerimaan barang ke TU sebagai pembelian dan hutang.
c. Mengeluarkan barang dari gudang
1) Petugas logistik berdasarkan SP dan faktur penjualan dari fakturis,
mengeluarkan barang dari gudang ke transito out.
2) Mencatat mutasi barang di kartu barang dan sistem informasi.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
39
3) Mencatat penyerahan barang dari gudang ke pengantar barang di buku
ekspedisi hantaran barang dan meminta paraf pengantar barang.
4) Memeriksa kembali penyerahan barang dari pengantar barang ke pelanggan
melalui faktur yang ada tanda terima dari pelanggan.
d. Membuat laporan mutasi barang di gudang
1) Petugas gudang membuat laporan mutasi barang.
2) Petugas gudang menghitung saldo barang setiap periode tertentu (1 bulan, 3
bulan), lalu membuat berita acara stock opname barang kemudian mengirim
laporan tersebut ke fungsi TU.
Gambar 3.2. Diagram penerimaan, penyimpanan, dan pengeluaran barang
Gambar 3.3. Alur penerimaan, penyimpanan, dan pengeluaran barang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
40
3.2.2.8 Sasaran
Sasaran dari manajemen penyimpanan ialah mencegah kehilangan dan
kerusakan barang atau kedaluwarsa.
3.2.2.9 Indikator
a. Jika jumlah barang hilang dan rusak > dari angka kebijakannya, maka fungsi
pergudangan berfungsi dengan baik.
b. Jika jumlah barang hilang dan rusak < dari angka kebijakannya, maka fungsi
pergudangan tidak berfungsi dengan baik.
3.2.3 Manajemen Penjualan dan Pelayanan
3.2.3.1 Definisi
The American Marketing Association mendefinisikan marketing
(management) sebagai “the process of planning and executing the conception,
pricing, promotion,and distribution of ideas, goods, and services to create
exchanges that satisfy individual and organizational objectives.
Philip Kotler mendefinisikan marketing management sebagai “the art and
science of choosingtarget markets and getting, keeping, and growing customers
through creating, delivering, and communicating superior customer values”.
3.2.3.2 Tujuan
Tujuan dari manajemen penjualan ialah untuk memperoleh pertumbuhan
penjualan (sales growth) dan pertumbuhan jumlah pelanggan (costumer growth)
serta untuk mempertahankan pelanggan yang loyal (costumer rate retention).
3.2.3.3 Standard Operational and Procedure Penjualan dan Pelayanan
a. Mengecek SP terhadap status umur hutang pelanggan yang lebih dari 2 bulan
1) Salesman mengunjungi pelanggan yang tidak bermasalah (tidak memiliki
hutang > 2 bulan), secara rutin.
2) Salesman menawarkan produk ke pelanggan (jumlah item dan SKU’s)
melalui program–program dari principalnya, seperti program diskon dan
bonus.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
41
3) Salesman mengambil SP dari pelanggan dan memeriksa status umur hutang
yang > 2 bulan, mencatat statusnya (ok atau tidak ok).
4) Salesman menyerahkan SP ke fakturis untuk dibuatkan fakturnya.
Gambar 3.4. Contoh alat kontrol penjualan
b. Pembuatan faktur atas SP pelanggan
1) Fakturis mengecek kebenaran data dan alamat pelanggan melalui sistem
informasi dan mencatat statusnya (ok atau tidak ok).
2) Fakturis membuatkan faktur penjualan barangnya.
3) Fakturis menyerahkan faktur dan SP pelanggan ke fungsi logistik.
c. Menyiapkan barang pesanan pelanggan
1) Petugas logistik mengeluarkan barang atas pesanan pelanggan berdasarkan
faktur dan SP, dan mencatat mutasi barang di kartu barang.
2) Petugas mengecek kesesuaian barang dengan faktur dan SP kemudian
mencatat statusnya (ok atau tidak ok).
3) Petugas mencatat jumlah barang yang dikeluarkannya sesuai dengan nama
pelanggan di sistem informasi.
4) Petugas memindahkan barang yang siap dikirim ke ruang transito out dan
mencatat di buku ekspedisi pengeluaran barang gudang.
5) Petugas membuat tanda terima penyerahan barang ke pengantar barang di
buku ekspedisi pengeluaran barang.
d. Memindahkan barang pesanan ke transito out
1) Petugas gudang memindahkan barang yang siap dikirim ke ruang transito
out dan mencatat di buku ekspedisi pengeluaran barang gudang.
2) Petugas membuat tanda terima penyerahan barang ke pengantar barang di
buku ekspedisi pengeluaran barang.
e. Menyerahkan barang ke petugas hantaran
1) Petugas gudang menyerahkan barang yang siap antar kepada petugas
hantaran.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
42
2) Petugas hantaran mencatat seluruh barang pesanan di buku ekspedisinya.
f. Mengirim barang ke pelanggan
1) Petugas hantaran barang mengirim barang ke pelanggan.
2) Petugas hantaran barang meminta tanda terima barang dari pelanggan dan
mencatat status penerimaannya (ok atau tidak ok).
3) Petugas hantaran barang menyerahkan tanda terima barang ke fungsi
logistik.
g. Memvalidasi pengeluaran barang
1) Petugas logistik memvalidasi pengiriman barang ke pelanggan di sistem
informasi sebagai barang keluar.
2) Petugas logistik menyerahkan faktur penjualan yang telah ada tanda terima
dari pelanggan dan SP ke fungsi TU.
h. Mencatat hasil penjualan barang ke pelanggan
1) Petugas administrasi penjualan TU memasukkan data pengiriman barang di
sistem informasi sebagai penjualan berdasarkan faktur dan SP yang telah
ada TT nya dari pelanggan.
2) Petugas administrasi penjualan TU juga memasukkan ke sistem informasi
hasil penjualan tersebut.
3) Petugas administrasi penjualan menyerahkan SP dan faktur penjualan ke
administrasi inkaso.
i. Menyimpan faktur dan penyerahan faktur yang telah jatuh tempo ke juru tagih
1) Petugas administrasi inkaso memasukkan data penjualan di kartu piutang
berdasarkan faktur dan SP yang telah ada tanda terimanya dari pelanggan ke
dalam sistem informasi.
2) Petugas administrasi inkaso menyimpan faktur penjualan dan membuat
daftar tanggal jatuh temponya ke sistem informasi.
3) Petugas administrasi inkaso akan menyerahkan faktur tagihan ke juru tagih
sesuai dengan daftar tagihan yang telah jatuh tempo untuk ditagihkan ke
pelanggan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
43
Gambar 3.5. Diagram penjualan
3.2.3.4 Sasaran
Sasaran yang ingin dicapai pada penjualan ialah mencapai target penjualan dan
service level yang ditentukan.
3.2.3.5 Indikator
a. Jika penjualannya > target atau dari tahun lalu, maka fungsi pelayanannya
berfungsi dengan baik
b. Jika penjualannya < target atau dari tahun lalu, maka fungsi pelayanannya tidak
berfungsi dengan baik
c. Jika service levelnya = 100 % atau > baik dari tahun lalu, maka fungsi
pelayanannya berfungsi dengan baik
d. Jika service levelnya < 100 %, maka fungsi pelayanannya tidak berfungsi
dengan baik
3.2.4 Manajemen Piutang
3.2.4.1 Definisi
Menurut Nurjannah (2012), piutang adalah hak klaim terhadap seseorang
atau perusahaan lain, menuntut pembayaran dalam bentuk uang atau penyerahan
aktiva atau jasa kepada pihak terhutang. Piutang merupakan semua tuntutan
terhadap langganan baik berbentuk perkiraan uang, barang maupun jasa dan
segala bentuk perkiraan seperti transaksi. Penjualan secara kredit menimbulkan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
44
hak bagi perusahaan yang melakukan penagihan pada langganannya sesuai
persyaratan yang telah disepakati bersama pada saat melakukan transaksi. Piutang
dapat diartikan sebagai jumlah nominal yang harus dibayarkan oleh pelanggan
kepada pihak penyedia setelah dilakukan proses transaksi jual beli pada waktu
jatuh tempo pembayarannya.
3.2.4.2 Standard Operational and Procedure Piutang
SOP Piutang menurut Said (2013) yaitu:
a. Penyerahan faktur tagihan dari fungsi TU ke administrasi Inkaso
1) Administrasi penjualan menerima dokumen penjualan kredit (faktur yang
sudah ada tanda terima dari pelanggan beserta SP) dari fungsi gudang.
2) Administrasi penjualan mengelompokkan dokumen penjualan kredit sesuai
dengan nama-nama pelanggannya dan mencatat di kartu piutang per
pelanggan.
3) Administrasi penjualan membukukan penjualan kredit per pelanggan di
sistem informasi (komputer).
4) Administrasi penjualan pada awal bulan merekap hasil penjualan kredit dan
membuatkan rekap tagihan per pelanggan lalu menyerahkan ke administrasi
inkaso.
b. Penyerahan faktur tagihan dari administrasi inkaso ke juru tagih
1) Adminsitrasi inkaso memeriksa dan menerima penyerahan fisik faktur
tagihan dan membuat tanda terima di buku ekspedisi penyerahan faktur dari
administrasi penjualan.
2) Administrasi inkaso mencatat piutang masuk di sistem informasi (kartu
piutang) per pelanggan.
3) Adminsitrasi inkaso membuat rencana penagihan berdasarkan tanggal jatuh
temponya.
4) Administrasi inkaso menyerahkan sejumlah faktur yang telah jatuh tempo
ke juru tagih disertai dengan nota inkaso (dokumen tanda penyerahan faktur
tagihan ke juru tagih).
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
45
c. Penyerahan faktur tagihan dari juru tagih ke pelanggan
1) Juru tagih menerima faktur tagihan dari administrasi inkaso disertai tanda
terima di nota inkaso.
2) Juru tagih menyerahkan faktur yang telah jatuh tempo ke pelanggan.
3) Pelanggan menerima faktur dan membayar hutangnya dengan 3
kemungkinan yaitu:
a) Dibayar lunas (100 %)
b) Dibayar sebagian
c) Hanya membuat tanda terima faktur dan pembayaran pada tanggal
berikutnya
d. Penyetoran dan pelaporan uang hasil tagihan
1) Juru tagih menyetorkan uang hasil tagihan pada hari yang sama (sore hari)
ke fungsi keuangan dengan meminta tanda terima setortan uang tagihan di
nota inkaso, jika pelanggan membayar 100 % lunas atau sebagian lunas.
2) Juru tagih melaporkan dan menyerahkan kembali hasil dokumen alat tagih
ke administrasi inkaso dengan tiga keterangan:
a) Dibayar lunas (100 %) oleh pelanggan.
b) Dibayar sebagian oleh pelanggan dengan melampirkan bukti sebagian
pembayarannya di balik faktur aslinya.
3) Ditunda oleh pelanggan dengan melampirkan bukti tanda terima faktur dari
pelanggan dan keterangan tanggal akan dibayar oleh pelanggan.
4) Administrasi inkaso menerima laporan dari juru tagih dan menyimpan
kembali faktur–faktur tagihan atau tanda terima faktur yang belum lunas
dibrankas.
5) Administrasi inkaso menyerahkan kembali faktur tagihan atau tanda terima
faktur yang belum lunas ke juru tagih untuk ditagihkan kembali ke
pelanggan sesuai janji.
e. Konfirmasi piutang ke pelanggan
1) Administrasi inkaso membuat data mutasi piutang per pelanggan pada setiap
awal bulan.
2) Administrasi inkaso membuat surat konfirmasi setiap bulan tentang jumlah
hutang kepada setiap pelanggan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
46
3) Bagi pelanggan yang tidak menjawab surat konfirmasi tersebut, maka angka
hutang pelanggan yang dibuat apotek yang dianggap benar.
Gambar 3.6. Diagram piutang
3.2.4.3 Sasaran
Sasaran yang ingin dicapai ialah mencegah kehilangan faktur dan pencurian uang
hasil tagihan.
3.2.4.4 Indikator
a. Jika tingkat kehilangan faktur atau pencurian uang hasil tagihan = 0 %, maka
administrasi inkaso berfungsi dengan baik.
b. Jika tingkat kehilangan atau pencurian uang hasil tagihan > 0, maka
administrasi inkaso tidak berfungsi dengan baik.
3.2.5 Manajemen Pembukuan
3.2.5.1 Definisi
Manajemen pembukuan adalah cara mengelola pembukuan atau
pencatatan (accounting) dan pengikhtisaran seluruh transaksi dagang dan
keuangan serta penganalisaan, pembuktian dan pembuatan laporan. Di Indonesia
istilah (bagian) pembukuan yang terdapat di suatu perusahaan juga dikenal dengan
nama tata usaha yaitu fungsi kegiatan yang bertugas melakukan pencatatan,
pemeriksaan, pembuatan laporan dan pengarsipan (Said, 2013).
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
47
3.2.5.2 Tujuan
Pembukuan dibutuhkan untuk menyimpan seluruh kegiatan perusahaan
dan transaksi-transaksi yang telah dilaksanakan Tujuan utama kegiatan
pembukuan di PBF adalah agar seluruh transaksi keuangan dapat
didokumentasikan sesuai dengan urutan peristiwa atau kejadian dan besarannya,
sehingga dapat disajikan dalam laporan keuangan dengan benar dan berguna bagi
pihak-pihak yang membutuhkan (Menteri Pekerjaan Umum, 2013).
3.2.5.3 Standard Operational and Procedure Pembukuan
Adapun proses pembuatan laporan akuntansi keuangan terdiri:
a. Mengumpulkan seluruh dokumen transaksi
b. Mencatat seluruh data transaksi ke buku jurnal
c. Memindahkan dari buku jurnal ke buku besar (posting)
d. Mencocokkan (judgment) terhadap informasi terakhir
e. Menyususun (reporting) laporan dari data buku besar
f. Menutup buku besar dan membuat laporannya
g. Mengirimkan laporan ke pihak yang membutuhkan
h. Mengarsipkan (filing)
Gambar 3.7. Diagram pembukuan
3.2.5.4 Sasaran
Sasaran yang ingin dicapai ialah menyajikan laporan keuangan tepat isi
dan tepat waktu.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
48
3.2.5.5 Indikator
a. Jika laporan keuangan dapat dibuat dan disajikan tepat isi dan waktu sesuai
tanggal yang ditetapkan, maka TU berfungsi dengan baik.
b. Jika laporan keuangan tidak dapat dibuat dan disajikan tepat isi dan waktu
sesuai tanggal yang ditetapkan, maka TU tidak berfungsi dengan baik.
3.3 Pajak
Jenis pajak yang dikelola di bagian tata usaha PT. Kimia Farma Trading
and Distribution antara lain pajak pertambahan nilai (PPN) dan Pajak Penghasilan
(PPh).
3.1.1 Pajak Pertambahan Nilai (PPN)
Menurut Undang-Undang Nomor 18 tahun 2000 tentang Perubahan Kedua
atas Undang-Undang Nomor 8 tahun 1983 tentang Pajak Pertambahan Nilai
Barang dan Jasa dan Pajak dan Pajak Penjualan Atas Barang Mewah, Pajak
Pertambahan Nilai adalah pajak yang dikenakan atas :
a. Penyerahan barang kena pajak di dalam Daerah Pabean yang dilakukan oleh
pengusaha
b. Impor barang kena pajak
c. Penyerahan jasa kena pajak di dalam Daerah Pabean yang dilakukan oleh
pengusaha
d. Pemanfaatan barang kena pajak tidak berwujud dari luar Daerah Pabean
e. Pemanfaatan jasa kena pajak dari luar Daerah Pabean, di dalam Daerah Pabean
atau ekspor barang kena pajak oleh pengusaha kena pajak.
Daerah Pabean adalah wilayah Republik Indonesia yg meliputi wilayah
darat, perairan dan ruang udara diatasnya serta tempat-tempat tertentu di Zona
Ekonomi Ekslusif dan Landas Kontinen. Barang kena pajak adalah barang yang
dikenakan pajak. Dalam PPN dikenal pula istilah diantaranya yaitu :
a. Pajak keluaran yaitu, PPN terutang yang wajib dipungut oleh pengusaha kena
pajak yang melakukan penyerahan barang kena pajak. Dalam hal ini Pajak
keluaran merupakan pajak yang dikeluarkan oleh KFTD kepada pelanggan
terhadap transaksi jual beli yang dilakukan, dibuktikan dengan adanya faktur
pajak.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
49
b. Pajak masukan yaitu, PPN yang seharusnya sudah dibayar oleh pengusaha
kena pajak karena perolehan barang kena pajak. Pajak masukan dalam hal ini
merupakan pajak yang telah dibayarkan oleh KFTD pada saat proses
pembelian barang kepada pihak principal pihak III, dibuktikan dengan adanya
Surat Setoran Pajak (SSP).
Faktur pajak yaitu, bukti pemungutan pajak yang dibuat oleh pengusaha
kena pajak yang melakukan penyerahan barang kena pajak. Faktur pajak dalam
hal ini dibundel menjadi satu bersama dengan faktur penjualan. Faktur pajak
pelanggan akan dikelola oleh pihak KFTD pusat.
3.1.2 Pajak Penghasilan (PPh)
Menurut Undang-Undang Republik Indonesia Nomor 7 tahun 1983
tentang Pajak Penghasilan, pajak penghasilan merupakan pajak yang dikenakan
terhadap orang pribadi atau perseorangan dan badan berkenaan dengan
penghasilan yang diterima atau diperolehnya selama satu tahun pajak. Badan yang
terdiri dari Perseroan Terbatas, Perseroan Komanditer, Badan Usaha Milik Negara
dan daerah dengan nama dan dalam bentuk apapun, persekutuan, perseroan atau
perkumpulan lainnya dan bentuk usaha tetap.
Orang pribadi yang dimaksud yaitu pegawai yang dikenakan pajak
meliputi pegawai tetap dan tidak tetap yang jumlah nominal kena pajaknya
disesuaikan dengan statusnya antara kawin, kawin dengan memiliki anak dan
memiliki tanggungan terhadap anak serta status tidak kawin. Berdasarkan PMK
No. 162/PMK.011/2012 besarnya pajak yang dibayarkan dalam satu tahun yaitu
Rp. 24.300.000,- untuk pegawai dengan status tidak kawin, Rp. 2.025.000,- untuk
pegawai dengan status kawin dan untuk status kawin dengan tanggungan anggota
keluarga berupa anak, jumlah anak yang ditanggung maksimal tiga orang.
Sedangkan Badan Usaha Milik Negara dalam hal ini yaitu KFTD, dikenakan
pajak pula atas badan usaha dengan penghasilan yang diterima atau diterimanya
selama satu tahun pajak. Jumlah nominal pajak yang dikenakan berdasarkan dari
jumlah pemasukan yang didapat selama satu tahun.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
50
Dalam hal pengelolaan pajak diambil alih oleh KFTD pusat, sedangkan
besarnya nominal pajak penghasilan yang harus dibayarkan ke Direktorat Jenderal
Pajak dihitung oleh KFTD di cabang masing-masing di bagian tata usaha.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 4
HASIL DAN PEMBAHASAN
Praktik Kerja Profesi Apoteker di PT. Kimia Farma Trading and
Distribution (KFTD) dilaksanakan di tiga cabang, yaitu KFTD cabang Bogor
yang merupakan KFTD cabang kelas 2 dan terletak di Jl. Tentara Pelajar No. 2
Bogor, KFTD cabang Jakarta-1 yang merupakan KFTD cabang kelas 3 terletak di
Jl. Majapahit No. 20 Jakarta Pusat, serta KTFD cabang Serpong yang merupakan
KFTD cabang kelas 1 dan terletak di Komplek Multiguna nomor A12 Serpong
Tangerang Selatan. Perbedaan kelas cabang didasarkan pada besarnya omset
penjualan.
KFTD melakukan tugasnya sebagai distributor sediaan farmasi dan
perbekalan kesehatan ke berbagai tempat diantaranya yaitu institusi pemerintahan,
rumah sakit, apotek, toko obat, pedagang besar farmasi lainnya, horeka (hotel,
restoran, karaoke atau kafe) dan lain-lain. Diantara produk yang di distribusikan
yaitu, obat-obat keras dengan resep dokter, obat Over The Counter (OTC),
narkotika, Obat Generik Berlogo (OGB), kosmetika, bahan baku dan alat
kesehatan. KFTD cabang Bogor melakukan pendistribusian sediaan farmasi dan
perbekalan kesehatan ke wilayah Bogor, Depok, Cileungsi, dan Cibubur. KFTD
cabang Jakarta-1 melakukan pendistribusian ke wilayah Cengkareng, Pluit, Muara
Karang, Grogol, Tomang, Slipi, Mangga Besar, Tanjung Duren, Tanah Abang,
Asemka. KFTD cabang Serpong melakukan pendistribusian ke wilayah Kota
Tangerang, Tangerang Selatan, beberapa daerah di Jakarta Selatan seperti
Fatmawati hingga Blok M, dan beberapa wilayah di pinggiran Jakarta Barat
seperti Pos Pengumben.
Penanggung jawab diketiga cabang KFTD adalah seorang apoteker yang
bekerja purna waktu sesuai dengan peraturan dan persyaratan CDOB. Apoteker
bertanggung jawab menyusun, memastikan dan mempertahankan penerapan
sistem manajeman mutu di fasilitas distribusi. Apabila apoteker penanggung
jawab (APJ) tidak dapat melakukan tugasnya dalam kurun waktu tertentu yang
ditetapkan, maka perlu ada pendelegasian tugas ke tenaga teknis kefarmasian.
Namun, SOP pendelegasian tugas ini di ketiga cabang belum ada.
51 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
52
Pengadaan barang di ketiga cabang didasarkan pada kondisi stok barang di
gudang dengan mengacu kepada kondisi level stock, buffer stock dan minimal
stock di gudang. Hal lain yang menjadi dasar pengadaan barang yaitu dilihat dari
laporan penjualan bulan sebelumnya. Untuk barang yang dinilai laku (fast
moving) maka dapat dilakukan pengadaan kembali, namun untuk barang yang
kurang laku atau tidak laku tidak akan dilakukan pengadaan.
Pengadaan barang dilakukan oleh petugas logistik ke pihak-pihak yang
telah disetujui oleh KFTD pusat sebagai pemasok yang sah dalam melakukan
pembelian, yaitu Principal Perusahaan Induk (PT. Kimia Farma Tbk.) yang
memasok Obat Generik Berlogo (OGB), Over The Counter Drugs (OTC), dan
narkotika-psikotropika, Principal Pihak III (Industri Farmasi atau PBF lain yang
telah bekerja sama dengan KFTD pusat) seperti Biofarma, dan Principal Lokal
(Industri Farmasi atau PBF lain yang telah bekerja sama dengan KFTD cabang
dengan persetujuan KFTD pusat). Pengadaan ke principal perusahaan induk
melalui Unit Bisnis Logistik (UBL) dilakukan seminggu sekali. KFTD cabang
Bogor dan Serpong melakukan pengadaan pada hari senin, sedangkan KFTD
cabang Jakarta-1 pada hari rabu. Pengadaan ke principal pihak III dan principal
lokal di ketiga cabang dilakukan sesuai kebutuhan.
Pemesanan barang dilakukan menggunakan surat pesanan (SP) (Lampiran
1 dan Lampiran 2). Untuk pemesanan narkotika wajib menggunakan SP khusus
model N-9 dan untuk psikotropika menggunakan SP khusus psikotropika.
Pemesanan yang telah dibuat oleh bagian pembelian ditandatangani oleh
supervisor logistik dan kepala cabang sebagai persetujuan pengadaan barang. SP
yang telah disetujui, di faksimile untuk dipesan, lalu diarsipkan. Untuk SP
nakotika yang telah di faksimile seharusnya segera dikirimkan ke UBL melalui
pos, namun pengiriman SP asli tidak segera dilakukan. Seperti di KFTD cabang
Jakarta-1 pengiriman SP asli narkotika-psikotropika oleh apoteker dilakukan
sebulan kemudian. KFTD cabang Serpong pengiriman SP asli narkotika-
psikotropika dilakukan seminggu kemudian. Namun di cabang Bogor pengiriman
SP asli narkotika-psikotropika dilakukan saat penerimaan barang dari UBL.
Setelah pemesanan dilakukan, maka proses selanjutnya adalah penerimaan
dan penyimpanan. Kegiatan penerimaan dilakukan di ruang penerimaan (transito
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
53
in). Penerimaan barang dilakukan dengan pengecekan kesesuaian antara surat
pesanan dengan faktur pembelian (Lampiran 3) atau SKB (Surat Kirim Barang)
(Lampiran 4) meliputi item barang, jumlah barang, diskon, dan harga. Kemudian
dilakukan pengecekan kembali antara faktur atau SKB dengan fisik barang
meliputi item barang, jumlah barang, nomor batch, tanggal kedaluwarsa, dan
kondisi fisik barang.
Seluruh kegiatan penggadaan obat reguler diketiga cabang telah sesuai
dengan standard operational procedure (SOP) dan mengacu pada CDOB.
Sedangkan penggadaan narkotika-psikotropika belum mengacu pada CDOB.
Barang yang telah diterima selajutnya disimpan di gudang dan dokumen
barang atau faktur pembelian (Lampiran 3) ditandatangani oleh bagian
penerimaan dan APJ PBF. Kemudian dilakukan entry data barang masuk di sistem
informasi oleh bagian logistik. Faktur pembelian (Lampiran 3) kemudian
ditandatangani kembali oleh supervisor tata usaha (TU) dan dijadikan sebagai
hutang dagang.
Sistem penyimpanan di gudang KFTD cabang Bogor, Serpong, Jakarta-1
menggunakan sistem First Expired First Out (FEFO). Khusus penyimpanan
narkotika-psikotropika di cabang Bogor menggunakan sistem First In First Out
(FIFO).
Penyimpanannya di ketiga cabang berbeda-beda. Penyimpanan di KFTD
cabang Bogor berdasarkan obat reguler dan obat narkotika-psikotropika. Gudang
obat regular dipisahkan berdasarkan obat dari Kimia Farma dan dari pihak III.
Penyimpanannya di KFTD cabang Jakarta-1 dipisahkan berdasarkan obat reguler
dan obat narkotika-psikotropika. Obat reguler dipisahkan kembali berdasarkan
obat yang berasal dari Kimia Farma dan pihak III menggunakan rak-rak yang
berbeda. Gudang terbagi menjadi gudang produk eceran atau box serta gudang
produk dalam bentuk dus. Penyimpanannya di KFTD cabang Serpong
berdasarkan obat reguler dan obat narkotika-psikotropika. Gudang obat regular
dipisahkan kembali berdasarkan: 1) Rak 1, obat generik Kimia Farma, 2) Rak 2,
OTC dan ethical Kimia Farma, 3) Rak 3, Pihak III dan Kosmetik, 4) Rak 4, Pihak
III.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
54
Kelengkapan alat penyimpanan obat regular di ketiga cabang dilengkapi
dengan pallet, tangga, exhaust fan, dan alat pengendali suhu (AC) namun tidak
terkalibrasi. Di KFTD cabang Jakarta-1 dan Serpong terdapat APAR dan
generator tetapi belum memadai, sedangkan di KFTD cabang Bogor tidak
tersedia. KFTD cabang Serpong telah dilengkapi dengan forklift untuk
memudahkan pemindahan barang, sedangkan di KFTD cabang Bogor dan Jakarta-
1 belum tersedia. Ketidaktersediaan forklift di KFTD cabang Jakarta-1, dapat
diatasi dengan adanya lift gedung.
Gudang narkotika-psikotropika di KFTD cabang Bogor dan Serpong
ditempatkan diruang terpisah dengan dua lapis pintu yang terkunci. Namun di
cabang Jakarta-1 hanya satu lapis pintu. Kunci gudang narkotika-psikotropika
dipegang oleh APJ PBF sekaligus sebagai penanggung jawab narkotika-
psikotropika. Persyaratan untuk menyimpan narkotika-psikotropika telah sesuai
dengan CDOB.
Untuk penyimpanan vaksin dan obat yang memerlukan suhu rendah di
KFTD cabang Bogor dan Jakarta-1 terdapat 1 chiller dan 1 refrigerator rumah
tangga. Refrigerator tidak dilengkapi dengan termometer. Chiller maupun
refrigerator di KFTD cabang Bogor belum terkalibrasi namun di KFTD cabang
Jakarta-1 telah dikalibrasi. KFTD cabang Serpong memiliki 1 chiller dan 2
refrigerator dan belum dikalibrasi. Pemantauan suhu chiller dan refrigerator di
ketiga cabang belum dilakukan secara teratur setiap pagi, siang, dan sore.
Layout bangunan di KFTD cabang Bogor dan Jakarta-1 belum memenuhi
syarat peta dan ruang karena belum adanya ruang transito in dan transito out. Di
KFTD cabang Serpong telah memiliki ruangan transito in dan transito out namun
pintu transito out tidak memadai barang-barang yang teralu besar (karton) tidak
dapat melewati ruangan transito out. Cabang yang tidak memiliki ruangan transito
in dan transito out dilakukan proses penerimaan dan pengeluaran barang pada
waktu yang terpisah. Ketika proses penerimaan barang dilakukan maka tidak ada
proses pengeluaran barang dan begitu pula sebaliknya.
Untuk obat yang rusak dan kedaluwarsa di ketiga cabang telah dilakukan
pemisahan dan ditempatkan di ruang yang terpisah, Ruangan obat rusak dan
kedaluwarsa di KFTD cabang Serpong dan Bogor tidak terkunci, namun di
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
55
cabang Jakarta-1 sudah terkunci dengan baik. Obat yang diduga palsu belum
pernah ditemukan diketiga cabang. Untuk obat kembalian di cabang Bogor dan
Jakarta-1 dilakukan pemisahan dari obat-obat reguler, namun di cabang Serpong
tidak dipisahkan. Pemusnahan obat di cabang Jakarta-1 belum pernah dilakukan
karena pemusnahan dilakukan oleh UBL. Pemusnahan obat di cabang Bogor
pernah dilakukan tahun 2011, begitu juga dengan cabang Serpong. Pemusnahan
obat disertai dengan berita acara pemusnahan yang dibuat oleh APJ dengan
disaksikan oleh BPOM, Dinas Kesehatan dan APJ. Pemusnahan dilakukan dengan
cara dibakar atau diencerkan sesuai dengan sifat barang yang akan dimusnahkan
setelah itu ditimbun di dalam tanah.
Kegiatan penjualan dan pelayanan di ketiga cabang KFTD terdiri dari
penjualan regular dan penjualan narkotika-psikotropika. Untuk penjualan yang
bersifat regular maka pelanggan dapat langsung melakukan pemesanan melalui
telepon (Lampiran 5), menggunakan Surat pesanan (SP) yang di faksimile
(Lampiran 6) atau menggunakan SP yang dititipkan kepada salesman. Pada
pemesanan narkotika-psikotropika, wajib menggunakan SP Narkotika (Form N-9)
asli atau SP Psikotropika asli yang ditandatangani oleh APJ sesuai dengan
ketentuan CDOB. Pada KFTD cabang Bogor dan Jakarta-1, pemesanan narkotika-
psikotropika telah sesuai dengan ketetapan CDOB, namun di KFTD cabang
Serpong masih ditemukan adanya pemesanan via telepon/ faksimile oleh APJ dan
tidak menggunakan SP asli. SP asli diterima sesaat sebelum dilakukan penyerahan
narkotika oleh petugas hantaran. Hal ini merupakan kebijakan yang diberikan oleh
KFTD cabang Serpong atas pertimbangan pemenuhan kebutuhan pelanggan yang
mungkin mendesak.
Setelah SP diterima, selanjutnya dibuat sales order (SO) di sistem
informasi untuk mengecek ketersediaan barang dalam memenuhi pesanan,
kemudian dibuat surat kirim barang (SKB) (Lampiran 7) dan faktur penjualan
(Lampiran 8) serta faktur pajak (Lampiran 9) jika pembayaran secara COD. Jika
pembayaran secara kredit maka faktur pajak akan dibuat saat tukar faktur atau saat
penagihan. SKB akan dicetak oleh petugas logistik untuk kemudian dilakukan
penyiapan pesanan. Proses penyiapan diawali dengan pengambilan barang sesuai
dengan SKB, mulai dari nama sediaan, jumlah, jenis atau bentuk sediaan, nomor
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
56
batch sampai dengan pengecekan tanggal kedaluwarsa. Untuk meminimalkan
kesalahan pengambilan barang (error) maka petugas penyiapan dan petugas
pengemasan merupakan orang yang berbeda, dimana kedua orang tersebut
melakukan pemeriksaan saat penyiapan dan saat pengemasan (double check).
Pengambilan barang dari rak penyimpanan berdasarkan sistem FEFO.
Pengambilan barang reguler dan CCP belum terdokumentasi dengan baik, dimana
telah dilakukan pencatatan jumlah sediaan yang diambil, nomor faktur dan nama
pelanggan, namun belum dicatat nomor batch dan sisa stok di kartu stok barang
(Lampiran 10). Sedangkan untuk sediaan narkotika dan psikotropika, dokumentasi
pengambilan barang telah dilakukan dengan baik.
Setelah kegiatan pengambilan dilaksanakan, barang dikemas dan disegel
untuk menjaga mutu selama transportasi pengiriman, kemudian diberi label.
Kegiatan ini dilakukan untuk menghindari kemungkinan kerusakan, kontaminasi,
pencurian dan tertukarnya barang hantaran. Selanjutnya, petugas logistik akan
mengeluarkan barang yang sudah dikemas ke ruang transito out dan barang
selanjutnya diberikan kepada petugas penghantar barang. Penghantar barang
kemudian menuliskan tanggal penghantaran, nomor faktur, nama pelanggan dan
total harga barang yang harus dibayarkan di dalam buku ekspedisi penjualan
(Lampiran 11). Buku ekspedisi ini merupakan dokumentasi penghantaran barang
ke pelanggan. Setelah diisi, buku selanjutnya diperiksa kebenarannya oleh
penanggung jawab logistik. Selain buku ekspedisi penjualan, penghantaran juga
disertai dengan faktur penjualan (Lampiran 8) dan SP dari pelanggan (Lampiran 5
dan Lampiran 6).
Pengiriman barang di ketiga cabang KFTD berbeda, dimana KFTD cabang
Bogor mengirim barang melalui pihak ketiga (out sourching), KFTD cabang
Jakarta-1 pengiriman barang dilakukan sendiri dan KFTD cabang Serpong
dilakukan melaui pihak ketiga (out sourching) dan dilakukan sendiri.
Penghantaran barang dilakukan setiap pagi dan sore hari. Penghantaran dilakukan
menggunakan motor dan mobil box. Mobil box telah dilengkapi dengan kunci
gembok guna menjaga keamanan dan mencegah pencurian obat dan
penyelewengan lainnya selama transportasi. Namun, penghantaran dengan
menggunakan motor belum dilengkapi dengan box melainkan menggunakan tas
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
57
ransel. Hal ini tidak sesuai dengan ketentuan CDOB yang menyatakan bahwa
kendaraan yang digunakan harus dapat menjamin bahwa obat tidak mengalami
perubahan kondisi selama penghantaran yang dapat mengurangi mutu, seperti
penyok, basah karena hujan atau rusak karena jatuh. Selain itu, hal tersebut juga
berbahaya bagi petugas penghantar. Untuk sediaan dengan suhu tertentu seperti
vaksin, dalam penghantarannya digunakan cool box berisi ice pack untuk
menjaga kondisi mutu sediaan sesuai dengan anjuran CDOB. Namun, belum
tersedia termometer untuk memastikan bahwa barang yang dihantarkan tidak
berubah suhunya selama proses penghantaran. Petugas penghantar barang belum
dibekali dengan pengetahuan CDOB, dimana pada KFTD cabang ini memang
belum pernah diberikan pelatihan mengenai CDOB pada personil.
Selanjutnya, barang diserahkan kepada pelanggan dan faktur penjualan
(Lampiran 8) ditandatangani oleh tim penerima barang. Faktur penjualan yang
telah ditandatangani diserahkan ke PJ logistik kemudian dibuatkan faktur
pajaknya (Lampiran 9). Faktur ini akan menjadi dokumen yang sah untuk
dilakukan penagihan kepada pelanggan. Pada penjualan regular, pembayaran
dapat dilakukan secara tunai maupun non tunai (kredit) dengan tenggang waktu 30
hari. Sedangkan untuk sediaan narkotika dan psikotropika, pembayaran dilakukan
secara tunai atau cash on delivery (COD) pada saat barang dihantarkan. Hal ini
diberlakukan agar sediaan narkotika setelah dihantarkan secara sah telah menjadi
tanggung jawab pelanggan dan bukan tanggung jawab KFTD lagi, serta
menghindari penyalahgunaan narkotika oleh pihak yang tidak berwenang. Namun,
untuk penjualan narkotika dan psikotropika ke rumah sakit, pembayaran dapat
dilakukan secara kredit dengan batas pembayaran maksimal 14 hari setelah
pemesanan karena proses dokumen di rumah sakit yang rumit, sehingga untuk
melakukan pembayaran secara COD. Pemilihan pelanggan dalam proses
penjualan juga menjadi perhatian, dimana penyaluran sediaan farmasi dan alat
kesehatan hanya disalurkan kepada pihak yang berhak dan berwenang untuk
menyerahkan obat ke masyarakat yang dibuktikan dengan adanya Surat Izin
Apotek, toko obat dan PBF, Surat Izin Penanggung Jawab dan NPWP (Nomor
Pokok Wajib Pajak) atau SIUP (Surat Izin Usaha Pengusaha). Pada penjualan
non-tunai, penagihan dilakukan ketika pembayaran telah jatuh tempo. Sebelum
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
58
waktu jatuh tempo, petugas penagih mendatangi pelanggan membawa faktur
penjualan (Lampiran 8) untuk melakukan tukar faktur dengan pelanggan yang
tujuannya untuk mengingatkan pelanggan bahwa pembayaran telah mendekati
jatuh tempo. Ketika telah tiba tanggal jatuh tempo, penagih datang membawa
tanda terima tukar faktur yang kemudian akan dijadikan alat penagihan kepada
pelanggan. Batas pembayaran bagi pelanggan adalah 45 hari, jika lebih dari 45
hari maka pelanggan tidak boleh melakukan transaksi pembelian dengan PBF
sampai piutang dibayar. Penagihan piutang kepada pelanggan yang telat
membayar setelah 45 hari maka akan disertakan surat konfirmasi piutang per
pelanggan (Lampiran 14) saat melakukan penagihan. Hal ini dilakukan sebagai
alat kontrol dalam penagihan.
Bagian terakhir dalam seluruh rangkaian proses kegiatan yang dilakukan
di KFTD yaitu pengarsipan dokumentasi. Hal ini sangat penting untuk menelusuri
seluruh aspek kegiatan jikalau terjadi suatu hal yang tidak dinginkan di masa yang
akan datang. Pengarsipan dokumentasi yang dilakukan oleh ketiga cabang KFTD
telah memenuhi ketentuan CDOB yaitu adanya dokumentasi tertulis yang berupa
prosedur (SOP), kontrak, dan data berbentuk kertas dan elektronik pada kegiatan
pembelian, penerimaan, penyimpanan, penyaluran dan pelaporan. Seluruh
dokumen seperti laporan keuangan, laporan penjualan, laporan pembelian dan
lain-lain dicetak dan ditandatangani oleh masing-masing petugas dengan
persetujuan kepala cabang. Dokumen disimpan di rak arsip secara teratur dan
belum pernah dimusnahkan. Pelaporan dilakukan secara bulanan, triwulan dan
tahunan ke KFTD pusat sebagai bahan pertimbangan untuk kegiatan selanjutnya
di waktu mendatang.
Berdasarkan dari seluruh rangkaian kegiatan tersebut maka kegiatan di
ketiga cabang KFTD dapat dikelompokkan menjadi tiga bagian utama yaitu
kegiatan pembelian dan penyimpanan (Unit Logistik), kegiatan penjualan dan
pelayanan (Unit Penjualan) dan kegiatan penagihan serta pengarsipan
dokumentasi (Unit Tata Usaha). Seluruh rangkaian kegiatan memiliki indikator
apakah kegiatan berjalan dengan baik atau tidak serta sasaran kegiatan sebagai
tolak ukur pencapaian tujuan. Dari seluruh rangkaian kegiatan tersebut maka unit
logistik di ketiga cabang KFTD dalam hal pembelian telah mencapai sasaran
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
59
memperoleh harga barang yang lebih murah dengan adanya diskon yang diberikan
oleh pihak principal terutama principal pihak III pusat. Namun, service level
pembelian belum 100%, karena UBL belum mampu memenuhi seluruh
permintaan di ketiga cabang KFTD dan sering terjadinya keterlambatan dalam
pengiriman barang. Manajemen pergudangan bertujuan untuk mencegah
kehilangan, kerusakan, dan kedaluarsa barang. Dalam hal penyimpanan, jumlah
barang rusak di KFTD cabang Serpong lebih kecil dari angka kebijakannya
(0,4%), yaitu 0,07%. Hal ini menandakan bahwa manajemen pergudangan telah
berfungsi dengan baik.
Pada unit penjualan di KFTD cabang Serpong, sasaran penjualan untuk
bulan september tahun 2013 telah tercapai. Pencapaian penjualan bulan tersebut
lebih besar dari yang ditargetkan, dimana capaian di bulan tersebut ialah 3,9
milyar dan target capaian di bulan tersebut ialah 3,7 milayar. Dapat dilihat bahwa
fungsi penjualan di bulan tersebut berjalan dengan baik. Pencapaian penjualan di
KFTD cabang Jakarta-1 untuk bulan September 2013 ialah 2,5 milyar dari target
awal 2,7 milyar. Bila dibandingkan dengan target pencapaian pada bulan
September 2012, maka pencapaian di bulan September tahun ini lebih besar,
begitu pula dengan pencapaian penjualan di KFTD Bogor. Dapat dilihat bahwa
fungsi penjualan di kedua cabang KFTD tersebut berjalan dengan baik. Namun,
service level di ketiga cabang KFTD belum 100%, dikarenakan masih adanya
pesanan yang tidak dapat dilayani karena barang tidak tersedia.
Pada unit tata usaha di ketiga cabang KFTD, pencapaian sasaran sudah
tercapai dengan tidak adanya kehilangan faktur. Di sisi lain, unit tata usaha juga
telah mencapai sasaran kegiatan dengan menyajikan laporan keuangan yang tepat
isi dan tepat waktu.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil Praktik Kerja Profesi Apoteker di PT. Kimia Farma
Trading and Distribution, dapat disimpulkan bahwa:
a. Cara Distribusi Obat yang Baik di PT. Kimia Farma Trading and Distribution
meliputi aspek manajemen mutu, organisasi, manajemen dan personalia,
bangunan dan peralatan, operasional, inspeksi diri, transportasi, fasilitas
distribusi berdasar kontrak dan dokumentasi. Sebagai Pedagang Besar
Farmasi, KFTD cabang Bogor, KFTD cabang Jakarta 1, dan KFTD cabang
Serpong telah berusaha berpedoman pada CDOB yang dikeluarkan oleh
BPOM RI pada semua lini kegiatannya, namun masih terdapat kekurangan
yang harus diperbaiki.
b. Dalam melakukan kegiatannya PT. Kimia Farma Trading and Distribution
(KFTD) telah menunjuk apoteker sebagai penanggung jawab fasilitas
distribusi, dimana tanggung jawab apoteker yaitu menyusun, memastikan dan
mempertahankan penerapan sistem manajeman mutu di fasilitas distribusi.
5.2 Saran
a. Sebaiknya dibuat SOP pendelegasian tugas ke tenaga teknis kefarmasian lain
apabila APJ tidak dapat melaksanakan tugasnya dalam waktu yang ditentukan.
b. Perlu dilakukannya inspeksi diri secara berkala dan berkesinambungan di
ketiga KFTD cabang untuk mengetahui kelebihan dan kekurangan masing-
masing lini kegiatan agar mampu menjadi bahan evaluasi untuk kegiatan di
masa yang akan datang serta mempertahankan kinerja baik yang telah ada.
c. Sebaiknya ruang transito out dan transito in di KFTD Jakarta-1 dan KFTD
Bogor dipisah dan tidak dijadikan tempat penyimpanan barang untuk
mencegah kesalahan saat pengiriman barang, penerimaan barang dan
kehilangan barang.
d. Sebaiknya SP asli pengadaan narkotika-psikotropika di ketiga KFTD cabang
segera dikirimkan ke UBL setelah dibuat oleh APJ.
60 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
61
e. Sebaiknya pemeriksaan pada penerimaan barang didokumentasikan secara
rutin oleh ketiga KFTD cabang.
f. Sebaiknya alat pengukur suhu ruangan di gudang ketiga KFTD cabang Bogor
dipelihara, dikalibrasi, dimonitoring dan didokumentasikan secara rutin oleh
petugas logistik.
g. Sebaiknya dibuat jadwal pembersihan gudang yang rutin di ketiga KFTD
cabang.
h. Sebaiknya barang kembalian, rusak, dan kedaluarsa yang ada di KFTD cabang
Serpong dan KFTD cabang Bogor disimpan di ruang terpisah dan terkunci.
i. Sebaiknya pengadaan AC untuk gudang reguler di ketiga KFTD cabang segera
direalisasikan demi menjaga mutu sediaan farmasi tetap terjaga.
j. Sebaiknya penjualan narkotika-psikotropika di KFTD cabang Jakarta-1 dan
KFTD cabang Serpong hanya melayani pesanan dengan SP asli.
k. Sebaiknya pencatatan pengambilan barang ke dalam kartu stok untuk barang
reguler dilakukan dengan lengkap oleh ketiga KFTD cabang (tanggal, nomor
faktur, nama pelanggan, nomor batch, tanggal kedaluwarsa, jumlah barang
yang diambil, dan sisa stok) sesuai SOP.
l. Sebaiknya motor penghantar barang di KFTD cabang Jakarta-1 dan KFTD
cabang Serpong dilengkapi dengan box demi menjaga mutu sediaan dan
keselamatan penghantar.
m. Sebaiknya dilakukan pelatihan kepada petugas di ketiga KFTD cabang
mengenai penggunaan APAR, pengelolaan CCP, pengelolaan narkotika-
psikotropika, CDOB dan perundang-undangan yang terkait.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR ACUAN
Badan Pengawasan Obat dan Makanan Republik Indonesia. (2012). Peraturan
Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor
HK.03.1.34.11.12.7542 Tahun 2012 tentang Pedoman Teknis Cara
Distribusi Obat yang Baik. Jakarta.
Kimia Farma. (2012). Laporan Tahunan Annual Report Tahun 2012. Jakarta:
Kimia Farma.
Kementerian Kesehatan. (2011). Peraturan Menteri Kesehatan No. 1148 Tahun
2011 tentang Pedagang Besar Farmasi. Jakarta.
Kementerian Keuangan. (2012). Peraturan Menteri Keuangan Nomor
162/PMK.011/2012. Jakarta.
Kementrian Pekerjaan Umum. (2013). Pembukuan Unit Pengelola Keuangan.
Jakarta: Direktorat Jenderal Cipta Karya.
Nurjannah. (2012). Analisis Tingkat Perputaran Piutang Pada PT Adira Finance
Makassar. Skripsi. Universitas Hasanuddin. Makassar.
Pemerintah Republik Indonesia. (2009). Peraturan Pemerintah Republik
Indonesia No. 51 Tahun 2009 tentang Pekerjaan Kefarmasian. Jakarta.
Presiden Republik Indonesia. (1983). Undang-Undang Republik Indonesia No. 7
Tahun1983 tentang Pajak Penghasilan. Jakarta.
Presiden Republik Indonesia. (2000). Undang-Undang Republik Indonesia No. 18
Tahun 2000 tentang Perubahan Kedua Atas Undang-Undang Nomor 8
Tahun 1983 tentang Pajak Pertambahan Nilai Barang dan Jasa dan Pajak
dan Pajak Penjualan Atas Barang Mewah. Jakarta.
Presiden Republik Indonesia. (2009). Undang-Undang Republik Indonesia No. 35
Tahun 2009 tentang Narkotika. Jakarta.
Presiden Republik Indonesia. (1997). Undang-Undang Republik Indonesia Nomor
5 Tahun 1997 tentang Psikotropika. Jakarta.
Said, Muhammad Umar. (2013). Manajemen Pedagang Besar Farmasi Praktis.
Solo: CV. Ar-Rahman.
62 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
62
LAMPIRAN
Laporan praktek….., Ennie Riben, FFar UI, 2014
63
Lampiran 1. Surat pesanan pembelian ke pihak III
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
64
Lampiran 2. Surat pesanan ke unit bisnis logistic (UBL)
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
65
Lampiran 3. Faktur pembelian dari pihak III
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
66
Lampiran 4. Surat kirim barang (SKB) dari UBL ke KFTD cabang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
67
Lampiran 5. Surat pesanan sementara
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
68
Lampiran 6. Surat pesanan yang di faksimile
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
69
Lampiran 7. Delivery order atau SKB penjualan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
70
Lampiran 8. Faktur penjualan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
71
Lampiran 9. Faktur pajak penjualan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
72
Lampiran 10. Kartu stok
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
73
Lampiran 11. Buku ekspedisi tunai
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
74
Lampiran 12. Buku ekspedisi kredit
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
75
Lampiran 13. Tanda terima tukar faktur
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
76
Lampiran 14. Konfirmasi piutang per pelanggan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
77
Lampiran 15. Nota inkaso
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
78
Lampiran 16. Laporan harian kunjungan salesman
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
79
Lampiran 17. Daftar kunjungan salesman
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
80
Lampiran 18. Kunjungan penagih
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
81
Lampiran 19. Customer record card
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
UNIVERSITAS INDONESIA
KEPATUHAN MELAKSANAKAN CARA DISTRIBUSI OBAT
YANG BAIK (CDOB) UNTUK SEDIAAN NARKOTIKA DAN
PSIKOTROPIKA DI PT. KIMIA FARMA TRADING AND
DISTRIBUTION CABANG BOGOR
TUGAS KHUSUS PRAKTIK KERJA PROFESI APOTEKER
ENNIE RIBEN SIHITE, S.Farm.
1206329575
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
Uni
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR ISI
DAFTAR ISI ........................................................................................................ ii
DAFTAR LAMPIRAN ....................................................................................... iii
BAB 1 PENDAHULUAN ................................................................................... 1
1.1 Latar Belakang ................................................................................... 1
1.2 Tujuan ................................................................................................ 2
BAB 2 TINJAUAN PUSTAKA .......................................................................... 3
2.1 Narkotika dan Psikotropika ................................................................ 3
2.1.1 Narkotika .................................................................................. 3
2.1.2 Psikotropika .............................................................................. 4
2.2 PT. Kimia Farma Tranding and Distribution (KFTD) Cabang Bogor 5
2.2.1 Gambaran Umum...................................................................... 5
2.2.2 Struktur Organisasi ................................................................... 5
2.3 Cara Distribusi Obat yang Baik (CDOB)........................................... 6
2.3.1 Definisi ..................................................................................... 6
2.3.2 Tujuan ....................................................................................... 6
2.4 Pengelolaan Narkotika dan Psikotropika menurut Cara Distribusi Obat
yang Baik (CDOB) ............................................................................. 6
2.4.1 Prinsip ....................................................................................... 6
2.4.2 Umum ....................................................................................... 6
2.4.3 Penanggung Jawab.................................................................... 6
2.4.4 Bangunan dan Peralatan ........................................................... 7
2.4.5 Operasional ............................................................................... 7
2.4.5.1 Kualifikasi Pemasok ................................................... 7
2.4.5.2 Kualifikasi Pelanggan ................................................. 7
2.4.5.3 Pengadaan ................................................................... 8
2.4.5.4 Penerimaan ................................................................. 8
2.4.5.5 Penyimpanan .............................................................. 9
2.4.5.6 Penyaluran .................................................................. 10
2.4.5.7 Ekspor dan Impor ....................................................... 12
2.4.5.8 Pemusnahan ................................................................ 12
2.4.6 Narkotika dan Psikotropika Kembalian .................................... 13
2.4.7 Dokumentasi ............................................................................. 13
2.5 Pelaporan Narkotika dan Psikotropika ............................................... 14
2.5.1 Narkotika .................................................................................. 14
2.5.2 Psikotropika .............................................................................. 15
BAB 3 PEMBAHASAN ...................................................................................... 16
BAB 4 KESIMPULAN DAN SARAN ............................................................... 23
4.1 Kesimpulan......................................................................................... 23
4.2 Saran ................................................................................................... 24
DAFTAR ACUAN............................................................................................... 25
LAMPIRAN ......................................................................................................... 26
ii
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR LAMPIRAN
Lampiran 1. Struktur Organisasi .......................................................................... 27
Lampiran 2. Produk Narkotika di KFTD cabang Bogor ...................................... 28
Lampiran 3. Produk Psikotropika di KFTD cabang Bogor .................................. 29
Lampiran 4. Surat Pesanan Narkotika ke KFTD Pusat ........................................ 30
Lampiran 5. Surat Pesanan Psikotropika ke KFTD Pusat .................................... 31
Lampiran 6. Gudang Narkotika dan Psikotropika ................................................ 32
Lampiran 7. Lemari Besi Penyimpanan Narkotika .............................................. 33
Lampiran 8. Langit-langit Ruang Narkotika ........................................................ 34
Lampiran 9. Tempat Penyimpanan Psikotropika ................................................. 35
Lampiran 10. Air Conditioner (AC) di ruang Narkotika dan Psikotropika ......... 36
Lampiran 11. Surat Pesanan Narkotika dari Pelanggan ....................................... 37
Lampiran 12. Surat Pesanan Psikotropika dari Pelanggan ................................... 38
Lampiran 13. Faktur Penjualan Narkotika ........................................................... 39
Lampiran 14. Faktur Penjualan Psikotropika ....................................................... 40
Lampiran 15. Kartu Stok Narkotika ..................................................................... 41
Lampiran 16. Kartu Stok Psikotropika ................................................................ 42
Lampiran 17. Pengemasan Narkotika .................................................................. 43
Lampiran 18. Pengemasan Psikotropika .............................................................. 44
Lampiran 19. Laporan Bulanan Narkotika, Psikotropika dan Prekursor ............. 45
iii
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Pembangunan nasional bertujuan untuk mewujudkan masyarakat
Indonesia yang sejahtera, adil dan makmur yang merata materiil dan spiritual
berdasarkan Pancasila dan Undang-Undang Dasar Negara Republik Indonesia
Tahun 1945. Kualitas sumber daya manusia Indonesia sebagai salah satu modal
pembangunan nasional perlu dipelihara dan ditingkatkan secara terus-menerus,
termasuk derajat kesehatannya. Salah satu upaya untuk meningkatkan derajat
kesehatan sumber daya manusia Indonesia dalam rangka mewujudkan
kesejahteraan rakyat perlu dilakukan upaya peningkatan di bidang pengobatan dan
pelayanan kesehatan, salah satunya dengan mengusahakan ketersediaan narkotika
dan psikotropika jenis tertentu yang sangat dibutuhkan sebagai obat serta
melakukan pencegahan dan pemberantasan bahaya penyalahgunaan dan peredaran
gelap narkotika dan psikotropika (Presiden Republik Indonesia, 2009).
Narkotika dan psikotropika di satu sisi merupakan obat atau bahan yang
bermanfaat di bidang pengobatan atau pelayanan kesehatan dan pengembangan
ilmu pengetahuan dan di sisi lain dapat pula menimbulkan ketergantungan yang
sangat merugikan kehidupan manusia dan kehidupan bangsa sehingga pada
gilirannya dapat mengancam ketahanan nasional apabila disalahgunakan atau
digunakan tanpa pengendalian dan pengawasan yang ketat dan saksama.
Sehubungan dengan pertimbangan tersebut di atas, untuk menghadapi
penyalahgunaan narkotika dan psikotropika yang berkecenderungan terus
meningkat, Pemerintah dan Dewan Perwakilan Rakyat Republik Indonesia
mengesahkan Undang-Undang Nomor 5 Tahun 1997 tentang Psikotropika dan
Undang-Undang Nomor 35 tahun 2009 tentang Narkotika.
Selain mengesahkan undang-undang tersebut, untuk mempermudah
pengawasan maka Menteri Kesehatan membuat keputusan dengan memberikan
izin importasi narkotika kepada satu Perusahaan Milik Negara yaitu PT. Kimia
Farma (Persero) Tbk. berdasarkan Keputusan Menteri Kesehatan No.
199/Menkes/SK/III/1996 tentang Penunjukan pedagang besar farmasi PT.
1 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
2
(Persero) Kimia Farma Depot Sentral sebagai Importir Tunggal Narkotik di
Indonesia.
Sebagai importir tunggal narkotika PT. Kimia Farma Tbk., harus dapat
menjamin keabsahan mutu produk narkotika ataupun psikotropika yang sampai ke
konsumen adalah produk yang aman, efektif dan dapat digunakan sesuai
indikasinya; dan menjamin penyimpanan obat aman dan sesuai kondisi yang
dipersyaratkan, termasuk pada sistem transportasinya. Salah satu usaha
perusahaan ini adalah dengan melakukan penyaluran narkotika dan psikotropika
hanya melalui PT. Kimia Farma Tranding and Distibution (KFTD). KFTD
merupakan anak perusahaan dari PT. Kimia Farma Tbk., yang bergerak dalam
bidang distribusi atau yang biasa disebut pedagang besar farmasi (PBF). Menurut
Menurut Peraturan Kepala Badan Pengawas Obat dan Makanan Republik
indonesia Nomor HK.03.1.34.11.12.7542 tahun 2012, setiap PBF atau PBF
cabang wajib memenuhi ketentuan Cara Distribusi Obat yang Baik (CDOB).
Oleh karena itu, mahasiswa Praktik Kerja Profesi Apoteker (PKPA)
Universitas Indonesia diberikan tugas khusus mengenai Kepatuhan dalam
Melaksanakan Cara Distribusi Obat yang Baik untuk sediaan narkotika dan
psikotropika di PT. Kimia Farma Trading and Distribution cabang Bogor.
1.2 Tujuan
Praktek Kerja Profesi Apoteker (PKPA) di PT. Kimia Farma Tranding and
Distribution (KFTD) cabang Bogor, bertujuan agar para calon Apoteker dapat
mengamati sejauh mana kepatuhan KFTD cabang Bogor menerapkan Cara
Distribusi Obat yang Baik (CDOB) dalam untuk sediaan narkotika dan
psikotropika.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 2
TINJAUAN PUSTAKA
2.1 Narkotika dan Psikotropika
2.1.1 Narkotika
Berdasarkan Undang-Undang Republik Indonesia Nomor 35 Tahun 2009,
narkotika adalah zat atau obat yang berasal dari tanaman atau bukan tanaman,
baik sintetis maupun semisintetis, yang dapat menyebabkan penurunan atau
perubahan kesadaran, hilangnya rasa, mengurangi sampai menghilangkan rasa
nyeri, dan dapat menimbulkan ketergantungan. Narkotika dibagi menjadi tiga
golongan, yaitu:
a. Narkotika golongan I
Narkotika yang hanya dapat digunakan untuk tujuan pengembangan ilmu
pengetahuan dan tidak digunakan dalam terapi, serta mempunyai potensi sangat
tinggi mengakibatkan ketergantungan. Contohnya: opium, candu, kokaina, ganja,
MDMA, meskalina, heroina.
b. Narkotika golongan II
Narkotika berkhasiat pengobatan digunakan sebagai pilihan terakhir dan
dapat digunakan dalam terapi dan/ atau untuk tujuan pengembangan ilmu
pengetahuan serta mempunyai potensi tinggi mengakibatkan ketergantungan.
Contohnya: fentanil, metadona, morfina.
c. Narkotika golongan III
Narkotika berkhasiat pengobatan dan banyak digunakan dalam terapi
dan/atau untuk tujuan pengembangan ilmu pengetahuan serta mempunyai potensi
ringan mengakibatkan ketergantungan. Contoh narkotika golongan ini adalah
kodein.
Pengaturan narkotika dalam Undang-Undang nomor 35 tahun 2009 meliputi
segala bentuk kegiatan dan/atau perbuatan yang berhubungan dengan narkotika
dan prekursor narkotika. Peraturan ini perlu dilakukan dengan tujuan untuk:
a. Menjamin ketersediaan narkotika untuk kepentingan pelayanan kesehatan
dan/atau pengembangan ilmu pengetahuan dan teknologi;
3 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
4
b. Mencegah, melindungi, dan menyelamatkan Bangsa Indonesia dari
penyalahgunaan narkotika;
c. Memberantas peredaran gelap narkotika dan prekursor narkotika; dan
d. Menjamin pengaturan upaya rehabilitasi medis dan sosial bagi penyalah guna
dan pecandu narkotika.
2.1.2 Psikotropika
Berdasarkan Undang-Undang Republik Indonesia Nomor 5 Tahun 1997,
psikotropika adalah zat atau obat, baik alamiah maupun sintetis bukan narkotika,
yang berkhasiat psikoaktif melalui pengaruh selektif pada susunan saraf pusat
yang menyebabkan perubahan khas pada aktivitas mental dan perilaku.
Psikotropika yang digolongkan menjadi:
a. Psikotropika golongan I
Psikotropika yang hanya dapat digunakan untuk tujuan ilmu pengetahuan
dan tidak digunakan dalam terapi serta mempunyai potensi amat kuat
mengakibatkan sindroma ketergantungan. Contoh dari obat psikotropika golongan
I adalah ecstasy (MDMA), psilosin, LSD (lisergik deitilamid), dan meskalin
(kaktus amerika).
b. Psikotropika golongan II
Psikotropika yang berkhasiat pengobatan dan dapat digunakan dalam
terapi dan/ atau untuk tujuan ilmu pengetahuan serta mempunyai potensi kuat
mengakibatkan sindroma ketergantungan. Contoh obat golongan psikotropika
golongan II adalah amfetamin, metamfetamina, sekobarbital, metakualon, dan
metilfenidat.
c. Psikotropika golongan III
Psikotropika yang berkhasiat pengobatan dan banyak digunakan dalam
terapi dan/ atau untuk tujuan ilmu pengetahuan serta mempunyai potensi sedang
mengakibatkan sindroma ketergantungan. Contoh obat psikotropika golongan III
adalah amorbarbital, flunitrazepam, dan kastina.
d. Psikotropika golongan IV
Psikotropika yang berkhasiat pengobatan dan sangat luas digunakan dalam
terapi dan/ atau untuk tujuan ilmu pengetahuan serta mempunyai potensi ringan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
5
mengakibatkan sindroma ketergantungan. Contoh obat psikotropika golongan IV
adalah barbital, bromasepam, diazepam, estazolam, fenorbarbital, klobazam, dan
klorazepam.
2.2 PT. Kimia Farma Trading and Distribution (KFTD) Cabang Bogor
2.2.1 Gambaran Umum
PT. Kimia Farma Trading and Distribution (KFTD) cabang Bogor
merupakan salah satu cabang kelas 2 dari PT. Kimia Farma Trading and
Distribution, yang terletak di di Jl. Tentara Pelajar No. 2 Bogor. Bangunan yang
digunakan KFTD cabang Bogor untuk melaksanakan kegiatan operasional bukan
milik pribadi (sewa) dari KFTD Pusat, oleh sebab itu KFTD cabang Bogor
memiliki kontrak tertulis sehingga pengelolaan bangunan sepenuhnya tanggung
jawab KFTD cabang Bogor. KFTD cabang Bogor melakukan distribusi sediaan
farmasi ke berbagai tempat seperti rumah sakit, apotek, toko obat, dan toko
kosmetik yang berada di wilayah Kota Bogor, Cileungsi, Cibubur dan Depok.
Sediaan Farmasi yang didistribusikan oleh KFTD Cabang Bogor meliputi obat
reguler (obat bebas, obat bebas terbatas, dan obat keras), obat tradisional,
kosmetika, obat narkotika dan psikotropika, serta beberapa alat kesehatan habis
pakai seperti kasa hidrofil.
2.2.2 Struktur Organisasi
Struktur organisasi PT. Kimia Farma Trading and Distribution (KFTD)
cabang Bogor dapat dilihat pada Lampiran 1. PT. Kimia Farma Trading and
Distribution (KFTD) cabang Bogor dipimpin oleh Branch Manager yang
berpengalaman. Kepala cabang membawahi 4 supervisor, yaitu :
a. Supervisor Tata Usaha dan Keuangan
b. Supervisor Pembelian
c. Supervisor Penjualan
d. Supervisor Logistik
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
6
2.3 Cara Distribusi Obat yang Baik (CDOB)
2.3.1 Definisi
Menurut Peraturan Kepala Badan Pengawas Obat dan Makanan Republik
indonesia Nomor HK.03.1.34.11.12.7542 tahun 2012, Cara Distribusi Obat yang
Baik, yang selanjutnya disingkat CDOB adalah cara distribusi/ penyaluran obat
dan/atau bahan obat yang bertujuan untuk memastikan mutu sepanjang jalur
distribusi/penyaluran sesuai persyaratan dan tujuan penggunaannya.
2.3.2 Tujuan
CDOB dimaksudkan untuk memastikan bahwa keamanan, manfaat dan
mutu produk obat di sepanjang jalur distribusi tetap dipertahankan sesuai dengan
karakteristik pada saat obat dimaksud disetujui untuk beredar, yaitu sejak dari
industri farmasi hingga fasilitas pelayanan kefarmasian meliputi apotek, rumah
sakit, klinik, pusat kesehatan masyarakat dan toko obat (Badan Pengawas Obat
dan Makanan, 2012).
2.4 Pengelolaan Narkotika dan Psikotropika menurut Cara Distribusi Obat
yang Baik (CDOB)
2.4.1 Prinsip
Cara distribusi narkotika dan psikotropika harus dilakukan dalam rangka
pemenuhan CDOB termasuk untuk mencegah terjadinya penyimpangan dan/atau
kehilangan narkotika dan psikotropika dari jalur distribusi resmi
2.4.2 Umum
Distribusi narkotika dan psikotropika wajib memenuhi ketentuan peraturan
perundang-undangan dan CDOB.
2.4.3 Penanggung jawab
Sesuai dengan peraturan perundang undangan penanggung jawab narkotika
dan psikotropika di pedagang besar farmasi (PBF) adalah seorang Apoteker.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
7
2.4.4 Bangunan dan Peralatan
Persyaratan bangunan dan peralatan yang digunakan untuk mengelola
narkotika wajib memenuhi ketentuan peraturan perundang-undangan. Gudang
atau lemari penyimpanan narkotika dan psikotropika harus aman dan terkunci.
Kunci lemari atau gudang penyimpanan narkotika dan psikotropika dipegang oleh
penanggung jawab fasilitas distribusi atau personil lain yang dikuasakan sesuai
dengan uraian pekerjaan.
Kapasitas lemari atau gudang khusus penyimpanan narkotika atau
psikotropika harus sesuai dengan yang dipersyaratkan. Gudang khusus
penyimpanan narkotika dan psikotropika tidak boleh dimasuki orang lain tanpa
izin penanggung jawab fasilitas distribusi
2.4.5 Operasional
2.4.5.1 Kualifikasi Pemasok
Pemasok yang menyalurkan narkotika wajib memiliki ijin khusus sebagai
fasilitas distribusi atau industri farmasi yang memproduksi narkotika. Izin khusus
menyalurkan atau memproduksi narkotika diterbitkan oleh Menteri Kesehatan.
Menteri Kesehatan memberikan izin importasi narkotika kepada satu Perusahaan
Milik Negara yaitu PT. Kimia Farma (Persero) Tbk., berdasarkan Kepmenkes No.
199/Menkes/SK/III/1996 tentang Penunjukan Pedagang Besar Farmasi PT
(Persero) Kimia Farma Depot Sentral sebagai Importir Tunggal Narkotika di
Indonesia.
2.4.5.2 Kualifikasi Pelanggan
Fasilitas distribusi harus memastikan penyaluran narkotika ke fasilitas
distribusi lain yang memiliki ijin khusus penyalur narkotika, instalasi sediaan
farmasi, apotek dan rumah sakit yang memiliki kewenangan menyalurkan atau
menyerahkan narkotika sesuai dengan peraturan perundang-undangan. Fasilitas
distribusi harus memastikan penyaluran psikotropika ke fasilitas distribusi lain,
instalasi sediaan farmasi, apotek dan rumah sakit yang memiliki kewenangan
menyerahkan psikotropika sesuai dengan peraturan perundang-undangan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
8
2.4.5.3 Pengadaan
Perencanaan kebutuhan tahunan harus dibuat dalam pengadaan narkotika
atau psikotropika. Pengadaan narkotika atau psikotropika harus berdasarkan surat
pesanan dengan format khusus sesuai dengan peraturan perundang-undangan.
Surat Pesanan wajib:
a. Asli dan dibuat paling sedikit dalam rangkap 2 (dua) serta tidak dibenarkan
dalam bentuk faksimili dan fotokopi.
b. Ditandatangani oleh penanggung jawab fasilitas distribusi dan dilengkapi
dengan nama jelas dan nomor Surat Izin Kerja (SIK)/ Surat Tanda Registrasi
Apoteker (STRA).
c. Mencantumkan nama dan alamat lengkap, nomor telepon/ faksimili, nomor
izin dan stempel fasilitas distribusi.
d. Mencantumkan nama industri farmasi atau fasilitas distribusi pemasok beserta
alamat lengkap.
e. Mencantumkan nama narkotika atau psikotropika, jenis dan kekuatan sediaan,
isi kemasan dan jumlah dalam bentuk angka dan huruf.
f. Diberi nomor urut dan tanggal dengan penulisan yang jelas.
g. Dibuat terpisah dari surat pesanan obat lain.
2.4.5.4 Penerimaan
Pada saat penerimaan harus dilakukan pemeriksaan terhadap:
a. Kebenaran nama, jenis, nomor bets, tanggal kedaluwarsa, jumlah dan kemasan
harus sesuai dengan surat pengantar/ pengiriman barang dan/ atau faktur
penjualan.
b. Kondisi kontainer pengiriman dan/ atau kemasan termasuk segel, label dan/
atau penandaan dalam kondisi baik.
c. Kebenaran nama, jenis, jumlah dan kemasan dalam surat pengantar/
pengiriman barang dan/ atau faktur penjualan harus sesuai dengan arsip surat
pesanan.
Setelah dilakukan pemeriksaan dan dinyatakan telah sesuai, penanggung
jawab fasilitas distribusi harus menandatangani surat pengantar/ pengiriman
barang dan/atau faktur penjualan dan dibubuhi stempel fasilitas distribusi. Jika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
9
setelah dilakukan pemeriksaan terdapat item obat yang tidak sesuai dengan surat
pesanan atau kondisi kemasan tidak baik, maka obat tersebut harus dikembalikan
dengan disertai bukti retur dan surat pesanan asli, dan segera meminta bukti
terima pengembalian dari pemasok.
Jika terdapat ketidaksesuaian nomor bets, tanggal kedaluwarsa dan jumlah
antara fisik dengan dokumen pengadaan harus dibuat dokumentasi untuk
mengklarifikasi ketidak sesuaian dimaksud ke pihak pemasok.
2.4.5.5 Penyimpanan
a. Narkotika
Penyimpanan narkotika wajib memenuhi ketentuan peraturan perundang-
undangan. Menurut Peraturan Menteri Kesehatan RI No. 28/Menkes/Per/I/1978
Pedagang besar farmasi harus mempunyai gudang khusus untuk menyimpan
narkotika dan dikunci dengan baik. Gudang yang dimaksudkan harus memenuhi
persyaratan sebagai berikut :
1) Dinding dibuat dari tembok dan hanya mempunyai satu pintu dengan 2 (dua)
buah kunci yang kuat dengan merk yang berlainan.
2) Langit-langit dan jendela dilengkapi dengan jeruji besi.
3) Dilengkapi dengan lemari besi yang tidak kurang dari 150 kilogram dan
mempunyai kunci yang kuat.
4) Gudang dan lemari tidak boleh digunakan untuk menyimpan barang selain
narkotika, kecuali ditentukan oleh Menteri Kesehatan.
5) Gudang tidak boleh dimasuki oleh orang lain tanpa ijin penanggung jawab.
6) Anak kunci gudang dan anak kunci lemari besi dipegang oleh penanggung
jawab atau pegawai lain yang dikuasakan
b. Psikotropika
Psikotropika harus disimpan dalam lemari atau gudang terkunci serta tidak
boleh digunakan menyimpan barang selain psikotropika untuk menjamin
keamanan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
10
2.4.5.6 Penyaluran
Dalam penyaluran harus memperhatikan tahap-tahap penerimaan
pesanan, pengemasan dan pengiriman.
a. Penerimaan pesanan
1) Pada saat penerimaan pesanan, penanggung jawab fasilitas distribusi wajib
memeriksa hal-hal sebagai berikut:
a) surat pesanan menggunakan format khusus yang telah ditentukan dan
terpisah dari produk lain
b) keaslian surat pesanan, tidak dalam bentuk faksimile, fotokopi maupun
email
c) memeriksa kebenaran surat pesanan, meliputi: nama dan alamat
penanggung jawab sarana pemesan; nama narkotika atau psikotropika,
jenis dan kekuatan sediaan, isi kemasan dan jumlah dalam bentuk
angka dan huruf; nomor surat pesanan; nama, alamat dan izin sarana
pemesan.
d) keabsahan surat pesanan, meliputi: tanda tangan dan nama jelas
penanggung jawab, nomor Surat Izin Kerja (SIK) penanggung jawab,
stempel fasilitas distribusi atau sarana pelayanan kefarmasian
2) Penanggung jawab fasilitas distribusi harus memperhatikan kewajaran
jumlah dan frekuensi pesanan.
3) Pesanan yang ditolak atau yang tidak dapat dilayani harus segera
diberitahukan kepada pemesan dengan menerbitkan Surat Penolakan
Pesanan paling lama 7 (tujuh) hari kerja.
4) Surat pesanan narkotika atau psikotropika yang dapat dilayani, disahkan
oleh penanggung jawab fasilitas distribusi dengan membubuhkan tanda
tangan atau paraf atau sistem lain yang dapat dipertanggungjawabkan.
b. Pengemasan
1) Pengemasan untuk tujuan pengiriman narkotika atau psikotropika harus
dilaksanakan setelah menerima surat pesanan
2) Setiap pengeluaran narkotika atau psikotropika untuk dilakukan
pengemasan harus dicatat dalam kartu stok dan disahkan dengan paraf
Kepala Gudang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
11
3) Sebelum dilakukan pengemasan narkotika atau psikotropika yang akan
dikirim harus dilakukan pemeriksaan terhadap:
a) kebenaran nama narkotika atau psikotropika, jenis dan kekuatan
sediaan, isi kemasan dan jumlah
b) nomor bets, tanggal kedaluwarsa dan nama industri farmasi
c) kondisi kemasan termasuk penandaan dan segel dari narkotika atau
psikotropika
d) kelengkapan dan keabsahan dokumen serta kebenaran tujuan
pengiriman.
c. Pengiriman
1) Setiap pengiriman narkotika atau psikotropika harus disertai dan
dilengkapi dengan dokumen pengiriman narkotika atau psikotropika yang
sah, antara lain surat jalan dan/ atau surat pengantar/ pengiriman barang
dan/ atau faktur penjualan yang dikeluarkan oleh fasilitas distribusi yang
ditandatangani oleh kepala gudang dan penanggung jawab fasilitas
distribusi.
2) Dokumen pengiriman harus terpisah dari dokumen lain.
3) Fasilitas distribusi wajib bertanggung jawab terhadap pengiriman
narkotika atau psikotropika sampai diterima di tempat pemesan oleh
penanggung jawab sarana atau penanggung jawab produksi, dibuktikan
dengan telah ditandatanganinya surat pengantar/ pengiriman barang
(nama, nomor SIK/ SIPA, tanda tangan penanggung jawab, tanggal
penerimaan, dan stempel sarana)
4) Pengiriman narkotika atau psikotropika wajib sesuai dengan alamat yang
tercantum pada surat pesanan dan faktur penjualan atau surat pengantar/
pengiriman barang.
5) Setiap narkotika atau psikotropika yang mengalami kerusakan dalam
pengiriman harus dicatat dalam bentuk berita acara dan dilaporkan segera
kepada penanggung jawab fasilitas distribusi pengirim. Selanjutnya hal
tersebut dilaporkan kepada Badan POM RI dengan tembusan Balai Besar/
Balai POM setempat.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
12
6) Setiap kehilangan narkotika atau psikotropika selama pengiriman wajib
dicatat dalam bentuk berita acara dan dilaporkan segera kepada
penanggung jawab fasilitas distribusi. Selanjutnya hal tersebut segera
dilaporkan kepada Badan POM RI dengan tembusan Balai Besar/ Balai
POM setempat dilengkapi dengan bukti lapor kepolisian.
2.4.5.7 Ekspor dan Impor
a. Setiap pengadaan narkotika atau psikotropika melalui impor harus memenuhi
peraturan perundang-undangan.
b. Setiap pengadaan narkotika dan psikotropika impor harus dilengkapi dengan
surat pesanan dan estimasi kebutuhan tahunan dari industri farmasi pengguna.
c. Setiap kegiatan ekspor narkotika atau psikotropika, harus memenuhi peraturan
perundang-undangan.
2.4.5.8 Pemusnahan
Pemusnahan dilakukan oleh penanggung jawab fasilitas distribusi dan
disaksikan oleh petugas Badan POM, serta dibuat berita acara pemusnahan yang
ditandatangani oleh penanggung jawab fasilitas distribusi dan saksi. Pelaksanaan
pemusnahan dilaporkan ke Badan POM dengan tembusan disampaikan ke Balai
Besar/ Balai POM dan Dinas Kesehatan Provinsi setempat dengan melampirkan
berita acara pemusnahan. Laporan pemusnahan sekurang-kurangnya memuat:
a. nama narkotika atau psikotropika, jenis dan kekuatan sediaan, isi kemasan,
jumlah, nomor bets dan tanggal kedaluwarsa;
b. tanggal, waktu dan tempat pelaksanaan pemusnahan;
c. cara dan alasan pemusnahan;
d. nama penanggung jawab fasilitas distribusi; dan
e. nama saksi-saksi.
Sesuai dengan Peraturan Menteri Kesehatan RI No. 28/Menkes/Per/I/1978
pasal 9 mengenai pemusnahan narkotika, pedagang besar farmasi dapat
memusnahkan narkotika yang rusak, kadaluarsa, dan tidak memenuhi syarat untuk
digunakan dalam pelayanan kesehatan dan/ atau untuk pengembangan ilmu
pengetahuan. Menurut undang-undang RI No. 5 tahun 1997 pemusnahan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
13
psikotropika dilaksanakan dalam hal : berhubungan dengan tindak pidana,
diproduksi tanpa memenuhi standar dan persyaratan yang berlaku dan/atau tidak
dapat digunakan dalam proses produksi psikotropika, kadaluwarsa, tidak
memenuhi syarat untuk digunakan pada pelayanan kesehatan dan/atau untuk
kepentingan ilmu pengetahuan.
2.4.6 Narkotika dan Psikotropika Kembalian
Ketentuan tentang narkotika dan psikotropika kembalian, dengan ketentuan
tambahan sebagai berikut:
a. Narkotika atau psikotropika kembalian harus disimpan terpisah dari obat
dan/atau bahan obat kembalian lain, terkunci dan aman untuk mencegah
pendistribusian kembali.
b. Penanganan produk kembalian dan tindak lanjutnya harus didokumentasikan.
Untuk produk kembalian yang akan dimusnahkan harus dilaporkan ke Badan
POM RI.
2.4.7 Dokumentasi
Pencatatan mutasi narkotika atau psikotropika wajib dilakukan dengan tertib
dan akurat. Melakukan stock opname secara berkala sekurang-kurangnya 1 (satu)
bulan sekali. Melakukan investigasi adanya selisih stok dengan fisik saat stock
opname dan mendokumentasikan hasil investigasi dalam bentuk berita acara hasil
investigasi selisih stock serta melaporkan ke Badan POM RI dengan tembusan
Balai Besar/Balai POM setempat.
Dokumen pengadaan meliputi arsip surat pesanan, faktur penjualan dan/atau
surat pengantar/ pengiriman barang/ dari industri farmasi atau fasilitas distribusi
lain, bukti retur dan/ atau nota kredit, wajib diarsipkan menjadi satu berdasarkan
nomor urut atau tanggal penerimaan barang dan terpisah dari dokumen lain.
Dokumen penyaluran meliputi surat pesanan, faktur penjualan dan/atau
surat penyerahan/ pengiriman barang, bukti retur dan/ atau nota kredit, wajib
diarsipkan menjadi satu berdasarkan nomor urut atau tanggal penyaluran barang
dan terpisah dari dokumen produk lain. Surat pesanan yang tidak dapat dilayani
tetap diarsipkan dengan diberi tanda pembatalan yang jelas
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
14
Dokumen berita acara pemusnahan, berita acara kerusakan, berita acara
kehilangan dan berita acara hasil investigasi selisih stok, wajib didokumentasikan,
dipisahkan dari dokumen obat dan/atau bahan obat lain dan disusun berdasarkan
urutan tanggal berita acara.
Arsip kartu stok manual wajib disimpan secara terpisah dari kartu stok
produk lain dan disusun berdasarkan tanggal sehingga mudah ditampilkan dan
dapat ditelusuri pada saat diperlukan.
Fasilitas distribusi wajib menyampaikan laporan bulanan penyaluran
narkotika dan atau psikotropika sesuai dengan ketentuan peraturan perundang-
undangan. Fasilitas distribusi yang melakukan importasi narkotika dan/atau
psikotropika wajib menyampaikan laporan realisasi impor sesuai dengan
peraturan perundang-undangan. Fasilitas distribusi yang melakukan eksportasi
narkotika dan/atau psikotropika wajib menyampaikan laporan realisasi ekspor
sesuai dengan peraturan perundang-undangan.
2.5 Pelaporan Narkotika dan Psikotropika
2.5.1 Narkotika
Menurut Undang-undang Republik Indonesia Nomor 35 tahun 2009
tentang narkotika Pasal 14 ayat 2 industri farmasi, pedagang besar farmasi, sarana
penyimpanan sediaan farmasi pemerintah, apotek, rumah sakit, pusat kesehatan
masyarakat, balai pengobatan, dokter, dan lembaga ilmu pengetahuan wajib
membuat, menyampaikan, dan menyimpan laporan berkala mengenai pemasukan
dan/atau pengeluaran narkotika yang berada dalam penguasaannya.
Dokumen pelaporan mengenai narkotika yang berada di bawah
kewenangan Badan Pengawas Obat dan Makanan, disimpan dengan ketentuan
sekurang-kurangnya dalam waktu 3 (tiga) tahun. Maksud adanya kewajiban untuk
membuat, menyimpan, dan menyampaikan laporan adalah agar pemerintah setiap
waktu dapat mengetahui tentang persediaan narkotika yang ada di dalam
peredaran dan sekaligus sebagai bahan dalam penyusunan rencana kebutuhan
tahunan narkotika.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
15
2.5.2 Psikotropika
Menurut Peraturan Menteri Kesehatan Republik Indonesia Nomor
912/Menkes/Per/VIII/1997 tentang kebutuhan dan pelaporan psikotropika, pasal 7
ayat 1 Pabrik obat dan pedagang besar farmasi yang menyalurkan psikotropika
wajib mencatat dan melaporkan psikotropika setiap bulan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 3
PEMBAHASAN
PT. Kimia Farma Tranding and Distribution (KFTD) cabang Bogor
merupakan Pedagang Besar Farmasi yang melakukan tugasnya sebagai distributor
sediaan farmasi dan perbekalan kesehatan ke berbagai tempat diantaranya yaitu
institusi pemerintahan, rumah sakit, apotek, toko obat, horeka (hotel, restoran,
karaoke atau kafe) dan lain-lain. Produk yang di distribusikan yaitu, obat keras
dengan resep dokter, Over The Counter (OTC), narkotika, psikotropika, Obat
Generik Berlogo (OGB), kosmetika dan alat kesehatan. Sebagai penyalur
narkotika, KFTD cabang Bogor telah memiliki izin khusus penyaluran narkotika
dengan nomor izin khusus HK.07.01/I/307/09. Penanggung jawab di KFTD
cabang Bogor sudah sesuai dengan peraturan perundang-undangan yaitu seorang
Apoteker yang bekerja purna waktu dan telah mempunyai SIKA serta tidak
merangkap jabatan sebagai direksi/pengurus PBF atau PBF Cabang lain. Di
KFTD cabang Bogor Apoteker penanggung jawab PBF juga berfungsi sebagai
Supervisor Logistik/penanggung jawab gudang dan penanggung jawab narkotika.
Dalam kegiatan operasional narkotika dan psikotropika, KFTD cabang
Bogor telah memiliki SOP khusus penyaluran narkotika dan psikotropika mulai
dari pengadaan, penerimaan, penyimpanan, penyaluran dan pemusnahan.
Pemasok narkotika dan psikotropika di KFTD cabang Bogor ialah UBL
(Unit Bisnis Logistik) yang merupakan principal perusahaan induk (PT. Kimia
Farma Tbk.). KFTD cabang Bogor memasok 24 produk narkotika (Lampiran 2)
dan 12 produk psikotropika (Lampiran 3) dari UBL. Pengadaan narkotika atau
psikotropika di KFTD cabang Bogor dimulai dari Supervisor Logistik yang juga
sebagai apoteker penanggung jawab membuat perencanaan kebutuhan narkotika
dan psikotropika sesuai dengan sisa stok, historis penjualan, dan permintaan
penjualan. Untuk pemesanan narkotika wajib menggunakan SP khusus model N-9
(Lampiran 4) dan untuk psikotropika menggunakan SP khusus psikotropika
(Lampiran 5). Supervisor Logistik membuat surat pesanan (SP) yang
mencantumkan nama pemesan, jabatan pemesan, alamat, nama narkotika atau
psikotropika, jenis dan kekuatan sediaan, isi kemasan dan jumlah dalam bentuk
16 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
17
angka dan huruf, tanggal, nomor urut SP dan tujuan pemesanan dengan penulisan
yang jelas. Dalam satu SP narkotika hanya boleh digunakan untuk menuliskan
satu jenis narkotika segangkan dalam satu SP psikotropika boleh digunakan untuk
beberapa jenis obat. Surat pesanan yang telah dibuat ditandatangani oleh
penanggung jawab narkotika dan kepala cabang, sebagai persetujuan pengadaan
barang, dan dilengkapi dengan nama penanggung jawab narkotika, stempel dan
nomor Surat Izin Kerja (SIK) di kirim ke UBL dalam bentuk faksimile, lalu
diarsipkan. Pengiriman SP narkotika dan psikotropika dalam bentuk faksimile
sebenarnya tidak dibenarkan sesuai Pedoman Teknis Cara Distribusi Obat yang
Baik (CDOB) walapun surat pesanan asli akan diserahkan pada saat barang
dikirim.
Setelah pemesanan dilakukan, maka proses selanjutnya adalah penerimaan
dan penyimpanan. Kegiatan penerimaan dilakukan di ruang penerimaan (transito
in). Penerimaan barang dilakukan dengan pengecekan kesesuaian antara surat
pesanan dengan faktur atau surat kirim barang (SKB) meliputi item barang,
jumlah barang, diskon, dan harga. Kemudian dilakukan pengecekan kembali
antara faktur atau SKB dengan fisik barang meliputi item barang, jumlah barang,
nomor batch, tanggal kedaluwarsa, dan kondisi fisik barang.
Setelah dilakukan pemeriksaan dan dinyatakan telah sesuai, supervisor
logistik akan menandatangani faktur atau SKB pembelian dan dibubuhi stempel
serta menyerahkan surat pesanan asli yang sesuai dengan yang telah di kirim
dalam bentuk faksimili sebelumnya. Jika setelah dilakukan pemeriksaan terdapat
item obat yang tidak sesuai dengan surat pesanan atau kondisi kemasan tidak baik,
maka obat tersebut dikembalikan dengan disertai bukti retur dan surat pesanan
asli, dan segera meminta bukti terima pengembalian dari UBL.
Kemudian dilakukan entry data barang masuk di sistem informasi oleh
bagian logistik. Faktur pembelian kemudian ditandatangani kembali oleh
supervisor tata usaha (TU) dan dijadikan sebagai hutang dagang.
Di KFTD cabang Bogor sudah mempunyai gudang khusus yang terbuat dari
tembok untuk penyimpanan narkotika dan psikotropika dan telah dikunci dengan
baik. Narkotika dan psiktropika disimpan dalam satu ruangan yang hanya
mempunyai satu pintu dengan dua buah kunci yang kuat dengan merk yang
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
18
berlainan (Lampiran 6). Gudang penyimpanan telah dilengkapi dengan
pencahayaan yang memadai untuk memungkinkan semua kegiatan dilaksanakan
dengan akurat. Narkotika di simpan di dalam lemari besi terkunci (Lampiran 7)
dan di lengkapi dengan jeruji besi di bagian langit-langit dan jendela (Lampiran 8)
yang terkunci untuk menjamin keamanan narkotika. Sedangkan untuk
psikotropika di simpan di bagian luar jeruji besi. Penyimpanan psikotropika masih
dalam dus asli dari pabrik sehingga penyimpanan psikotropika belum tersusun
rapi seperti narkotika (Lampiran 9). Sistem penyimpanan narkotika dan
psikotropika di gudang KFTD cabang Bogor menggunakan sistem First In First
Out (FIFO).
Gudang penyimpanan narkotika dan psikotropika dilengkapin air
conditioner (Lampiran 10) sebagai alat pengendali suhu namun belum dilengkapi
alat pengukur suhu dan kelembaban. Untuk dapat menjaga mutu narkotika dan
psikotropika seharusnya dilakukan pengontrolan suhu ruangan dengan mengecek
suhu pada alat pengukur suhu dan mencatatnya. Kunci gudang narkotika dan
psikotropika dipegang oleh apoteker penanggung jawab gudang sekaligus sebagai
penanggung jawab narkotika dan psikotropika. Jika apoteker penanggung jawab
berhalangan hadir, kunci lemari dan gudang dipegang oleh pegawai lain yang
dikuasakan sesuai dengan Standard Operational Procedure (SOP). Gudang khusus
penyimpanan narkotika dan psikotropika tidak boleh dimasuki orang lain tanpa
izin penanggung jawab gudang.
KFTD cabang Bogor hanya melakukan penyaluran narkotika dan
psikotropika ke apotek dan rumah sakit yang telah memiliki kewenangan
menyalurkan atau menyerahkan narkotika atau psikotropika sesuai dengan
peraturan perundang-undangan dan telah melakukan registrasi sebagai pelanggan
dari KFTD cabang Bogor.
Kegiatan penjualan atau pelayanan narkotika atau psikotropika dilakukan
hanya jika ada pemesanan narkotika atau psikotropika dengan menggunakan SP
Narkotika asli (Lampiran 11) atau SP Psikotropika asli (Lampiran 12) yang telah
ditandatangani oleh Apoteker Penanggung jawab apotik atau rumah sakit, jika SP
asli belum di terima oleh bagian fakturis atau pemesanan hanya via
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
19
telepon/faksimile maka pesanan tidak dapat dilayani walaupun untuk keperluan
mendesak.
Pada saat penerimaan pesanan, penanggung jawab akan memeriksa keaslian
dan kebenaran surat pesanan, meliputi: nama dan alamat penanggung jawab
sarana pemesan, nama narkotika atau psikotropika, jenis dan kekuatan sediaan, isi
kemasan dan jumlah dalam bentuk angka dan huruf, no surat pesanan, tanda
tangan, nama jelas, no SIPA penanggung jawab dan stempel apotek/rumah sakit.
Selain itu penanggung jawab akan memperhatikan kewajaran jumlah dan
frekuensi pesanan. Surat pesanan yang tidak memenuhi syarat akan ditolak dan
akan segera diberitahukan kepada pemesan melalui telepon.
Setelah SP asli memenuhi syarat dan diterima, selanjutnya dibuat sales order
(SO) di sistem informasi untuk mengecek ketersediaan barang dalam memenuhi
pesanan, kemudian dibuat faktur penjualan (Lampiran 13 dan Lampiran 14).
Proses penyiapan diawali dengan pengambilan narkotika atau psikotropika oleh
penanggung jawab sesuai dengan faktur, mulai dari nama sediaan, jumlah, jenis
atau bentuk sediaan, nomor batch sampai dengan pengecekan tanggal
kedaluwarsa. Setiap pengeluaran narkotika atau psikotropika untuk dilakukan
pengemasan harus dicatat dalam kartu stok (Lampiran 15 dan Lampiran 16) dan
disahkan dengan paraf Penanggung jawab gudang yang merupakan Penanggung
jawab narkotika dan psikotropika. Pengeluaran narkotika atau psikotropika belum
terdokumentasi sepenuhnya, dimana nomor batch dan tanggal kedaluwarsa tidak
dicatat di kartu. Sedangkan menurut SOP, setiap pengeluaran barang wajib
mengisi kolom di kartu stok dengan lengkap yaitu: tanggal pengambilan, nomor
faktur, nama pelanggan, nomor batch, tanggal kedaluwarsa, jumlah barang yang
diambil, sisa stok, dan paraf petugas. Dalam CDOB juga ditetapkan bahwa setiap
pengeluaran produk harus dicatat pada lembar catatan pengiriman yang isinya
meliputi tujuan pengiriman, jenis barang, jumlah, nomor batch dan tanggal
kedaluwarsanya (Badan POM RI, 2012). Pengemasan narkotika atau psikotropika
hanya menggunakan plastik atau dus (Lampiran 17 dan Lampiran 18).
Setiap pengiriman narkotika atau psikotropika disertai dan dilengkapi
dengan surat pesanan asli dan faktur penjualan yang ditandatangani oleh
penanggung jawab gudang. Pengiriman narkotika atau psikotropika dilakukan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
20
melalui pihak ketiga yang telah melakukan kerjasama dengan KFTD cabang
Bogor sehingga pihak fasilitas distribusi wajib bertanggung jawab terhadap
pengiriman narkotika atau psikotropika sampai diterima di tempat pemesan oleh
penanggung jawab sarana. Pengiriman narkotika atau psikotropika wajib sesuai
dengan alamat yang tercantum pada surat pesanan dan faktur penjualan. Barang
yang telah diterima oleh pemesan dibuktikan dengan faktur penjualan yang telah
diberi tanda tangan penanggung jawab, serta diberi nama, nomor SIPA, tanggal
penerimaan, dan stempel sarana. Untuk sediaan narkotika dan psikotropika,
pembayaran dilakukan secara cash pada saat barang dihantarkan (Cash On
Delivery/ COD) sehingga pada saat pengiriman telah disertai dengan faktur pajak.
Faktur penjualan yang telah ditandatangani oleh penerima diserahkan ke
supervisor logistik.
Pemusnahan dilakukan jika terdapat barang yang kedaluwarsa dan rusak.
Penanggung jawab gudang akan membuat daftar narkotika dan psikotropika yang
akan dimusnahkan mencangkup nama barang, nomor batch, tanggal kedaluwarsa
dan jumlah. Setiap akan melakukan pemusnahan, KFTD cabang Bogor harus
mengajukan ijin prinsip pemusnahan barang kepada Direksi. Setelah mendapat
persetujuan, pemusnahan dilakukan oleh penanggung jawab gudang dan
disaksikan oleh petugas Balai Pengawasan Obat dan Makanan (POM), serta
dibuat berita acara pemusnahan yang ditandatangani oleh penanggung jawab
gudang. Balai POM dan saksi. Pemusnahan dilakukan dengan cara dibakar atau
diencerkan sesuai dengan sifat barang yang akan dimusnahkan setelah itu
ditimbun di dalam tanah. Pelaksanaan pemusnahan dilaporkan ke Badan POM
dengan tembusan disampaikan ke Balai Besar/Balai POM dan Dinas Kesehatan
Provinsi setempat dengan melampirkan berita acara pemusnahan. Laporan
pemusnahan memuat: nama narkotika atau psikotropika, jenis dan kekuatan
sediaan, isi kemasan, jumlah, nomor bets dan tanggal kedaluwarsa; tanggal, waktu
dan tempat pelaksanaan pemusnahan; cara dan alasan pemusnahan; nama
penanggung jawab gudang dan nama saksi-saksi. KFTD cabang Bogor pernah
melakukan pemusnahan pada Tahun 2011.
Pengarsipan dokumentasi yang dilakukan oleh KFTD cabang Bogor telah
memenuhi ketentuan CDOB yaitu adanya dokumentasi tertulis yang berupa
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
21
prosedur (SOP) dan data berbentuk kertas dan elektronik pada kegiatan
pembelian, penerimaan, penyimpanan, penyaluran dan pelaporan narkotika atau
psikotropika yang dilakukan dengan tertib. Hal ini sangat penting untuk
menelusuri seluruh aspek kegiatan jikalau terjadi suatu hal yang tidak dinginkan
di masa yang akan datang.
Dokumentasi yang telah dilakukan untuk narkotika dan psikotropika, yaitu
dokumen pengadaan meliputi arsip surat pesanan dan faktur pembelian narkotika
atau psikotropika dari UBL, bukti retur dan/atau nota kredit, diarsipkan menjadi
satu berdasarkan nomor urut atau tanggal penerimaan barang dan terpisah dari
dokumen lain.
Dokumen penyaluran meliputi surat pesanan, faktur penjualan, dan bukti
retur telah diarsipkan menjadi satu. Dokumen berita acara retur barang kembalian,
rusak dan kedaluwarsa ke UBL yang disusun berdasarkan tanggal dan dipisahkan
dari berita acara retur barang reguler.
Seluruh dokumen seperti laporan keuangan, laporan penjualan, laporan
pembelian dan lain-lain dicetak dan ditandatangani oleh masing-masing petugas
dengan persetujuan kepala cabang. Dokumen disimpan di rak arsip secara teratur
dan belum pernah dimusnahkan. Pelaporan dilakukan secara bulanan, triwulan
dan tahunan ke UBL sebagai bahan pertimbangan untuk kegiatan selanjutnya di
waktu mendatang.
Kegiatan stock opname dilakukan secara berkala setiap 3 (tiga) bulan sekali
sesuai kebijakan UBL, namun hal ini tidak sesuai dengan ketentuan dalam CDOB
dimana stok opname narkotika dan psikotropika seharusnya dilakukan secara
berkala sekurang-kurangnya 1 (satu) bulan sekali. Jika terjadi selisih stok dengan
fisik saat stock opname, maka penanggung jawab gudang akan melakukan
investigasi adanya dan mendokumentasikan hasil investigasi dalam bentuk berita
acara hasil investigasi selisih stok serta melaporkan ke UBL, Badan POM dengan
tembusan Balai Besar/Balai POM setempat.
Arsip kartu stok manual telah disimpan secara terpisah dari kartu stok
produk lain dan disusun berdasarkan tanggal sehingga mudah ditampilkan dan
dapat ditelusuri pada saat diperlukan.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
22
Laporan bulanan pendistribusian narkotika dan psikotropika di KFTD
cabang Bogor dibuat setiap bulan oleh penanggung jawab narkotika dan
psikotropika berdasarkan transaksi pembelian dan penjualan narkotika dan
psikotropika selama 1 bulan dan dikirimkan ke Badan Pengawasan Obat dan
Makanan (BPOM) melalui email wasnapza@pom.go.id paling lambat setiap
tanggal 10 setiap bulannya. dengan tembusan kepada balai Besar POM dan untuk
arsip (Lampiran 19).
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
BAB 4
KESIMPULAN DAN SARAN
5.1 Kesimpulan
PT. Kimia Farma Tranding and Distribution (KFTD) cabang Bogor dalam
rantai distribusi narkotika dan psikotropika telah memiliki ijin khusus penyaluran
narkotika dan penanggung jawab seorang apoteker yang mempunyai SIKA.
Pemasok narkotika dan psikotropika di KFTD cabang Bogor ialah UBL (Unit
Bisnis Logistik) yang merupakan principal perusahaan induk (PT. Kimia Farma
Tbk.), sedangkan pelanggan narkotika dan psikotropika KFTD cabang Bogor
ialah apotek dan rumah sakit yang telah memiliki kewenangan menyalurkan atau
menyerahkan narkotika atau psikotropika sesuai dengan peraturan perundang-
undangan dan telah melakukan registrasi sebagai pelanggan dari KFTD cabang
Bogor. Pengadaan narkotika telah menggunakan SP N-9 yang dicetak, namun
dikirimkan melalui faksimile. Standar bangunan dan peralatan yang digunakan
untuk penyimpanan narkotika dan psikotropika juga telah hampir memenuhi
standar yang ditetapkan dalam CDOB. Gudang dilengkapi dengan AC sebagai
pengatur suhu namun belum tersedia termometer yang terkalibrasi sebagai alat
pengukur suhu. Penjualan narkotika didasarkan atas SP N-9 asli dan SP khusus
psikotropika asli. Penghantaran narkotika dan psikotropika telah disertai dengan
dokumen-dokumen seperti faktur penjualan, faktur pajak dan SP asli. Pemusnahan
narkotika dan psikotropika telah sesuai dengan ketentuan CDOB. Dokumen
pengadaan, dokumen penyaluran, dokumen berita acara retur barang kembalian,
rusak dan kedaluwarsa, laporan keuangan, laporan penjualan dan laporan
pembelian telah diarsipkan dan terpisah dari dokumen obat reguler. Pelaporan
penyaluran narkotika dan psikotropika di KFTD cabang Bogor dibuat setiap bulan
oleh penanggung jawab narkotika dan psikotropika ke Badan Pengawasan Obat
dan Makanan (BPOM) melalui email wasnapza@pom.go.id.
23 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
24
5.2 Saran
a. Penerapan aspek-aspek CDOB di KFTD cabang Bogor perlu terus dipertahankan
dan ditingkatkan sehingga mutu narkotika dan psikotropika di KFTD cabang
Bogor tetap dipertahankan selama proses distribusi.
b. Pada saat KFTD cabang Bogor akan melakukan pemesanan narkotika dan
psikotropika, sebaiknya surat pesanan asli segera dikirimkan langsung ke UBL
bukan melalui faksimile, sesuai dengan ketentuan dalam CDOB.
c. Sebaiknya gudang penyimpanan narkotika dan psikotropika di KFTD cabang
Bogor dilengkapi dengan alat pengukur suhu (termometer) yang terkalibrasi.
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
DAFTAR ACUAN
Badan Pengawasan Obat dan Makanan Republik Indonesia. (2012). Cara
Distribusi Obat yang Baik. Jakarta: Badan Pengawasan Obat dan Makanan
RI.
PT. Kimia Farma Tranding and Distribution. (2011). Standard Operating
Procedures. Jakarta: PT. Kimia Farma Tranding and Distribution.
Pemerintah Republik Indonesia. (2009). Peraturan Pemerintah Republik
Indonesia No. 51 Tahun 2009 Tentang Pekerjaan Kefarmasian. Jakarta.
Presiden Republik Indonesia. (1997). Undang-Undang Republik Indonesia Nomor
5 Tahun 1997 Tentang Psikotropika. Jakarta.
Presiden Republik Indonesia. (2009). Undang-Undang Republik Indonesia No. 36
Tahun 2009 Tentang Kesehatan. Jakarta.
Presiden Republik Indonesia. (2009). Undang-Undang Republik Indonesia Nomor
35 Tahun 2009 Tentang Narkotika. Jakarta.
25 Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
LAMPIRAN
26
Laporan praktek….., Ennie Riben, FFar UI, 2014
27
Lampiran 1. Struktur organisasi
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
28
Lampiran 2. Produk narkotika di KFTD cabang Bogor
No Nama Produk Kemasan Besar Sediaan
1 Pethidin HCl 50 mg inj Dus 10 x 2 mL
2 Codein 10 mg tablet Botol 250 tablet
3 Codein 15 mg tablet Botol 250 tablet
4 Codein 20 mg tablet Botol 250 tablet
5 Coditam tablet Dus 100 tablet
6 Codikaf 20 mg tablet Dus 10 x 10 strip
7 Codikaf 10 mg tablet Dus 10 x 10 strip
8 Codipront caps Dus 1 x 10 strip
9 Codipront caps Botol 100 kapsul
10 Codipront cum expect caps Dus 1 x 10 strip
11 Codipront cum expect sirup Botol 60 mL
12 Codipront sirup Botol 60 mL
13 Morphine hcl 10 mg Dus 10x 1 mL
14 Clopedin injeksi 2 ml Dus 10 x 2 mL
15 Fentanil 0,05 mg/ml 10 ml inj Dus 5 ampul
16 Fentanil 0,05 mg/ml inj 2 ml Dus 5 ampul
17 Fentanil 0,05 mg/ml inj 10 ml Dus 10 mL
18 Fentanyl 0.05 mg/ml 2 ml Dus 2 mL
19 Durogesic 12,5 mu matrix Dus Set
20 Durogesic 25 mu matrix Dus Set
21 Durogesic 50 mu matrix Dus Set
22 Mst continus 10 mg Tablet 60 tablet
23 Mst continus 15 mg Tablet 60 tablet
24 Mst continus 30 mg Tablet 60 tablet
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
29
Lampiran 3. Produk psikotropika di KFTD cabang Bogor
No Nama Produk Kemasan Jumlah
1 Diazepam 2 mg Botol 1000 tablet
2 Phenobarbital 30 mg Botol 1000 tablet
3 Neurodial Dus 10 x 10
4 Clofritis 10 mg Dus 100 tablet
5 Prohipen Dus 30 tablet
6 Riklona 2 mg Dus 100 tablet
7 Sibital injeksi 2 ml Dus 10 ampul
8 Valdimex 5 mg Dus 100 tablet
9 Merlopam 2 mg Dus 100 tablet
10 Merlopam 0.5 mg Dus 100 tablet
11 Atarax 0,5 mg Dus 100 tablet
12 Valdimex 10mg/2mL Dus 5 ampul
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
30
Lampiran 4. Surat pesanan narkotika ke KFTD Pusat
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
31
Lampiran 5. Surat pesanan psikotropika ke KFTD Pusat
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
32
Lampiran 6. Gudang narkotika dan psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
33
Lampiran 7. Lemari besi penyimpanan narkotika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
34
Lampiran 8. Langit-langit ruang narkotika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
35
Lampiran 9. Tempat penyimpanan psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
36
Lampiran 10. Air conditioner (AC) di ruang narkotika dan psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
37
Lampiran 11. Surat pesanan narkotika dari pelanggan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
38
Lampiran 12. Surat pesanan psikotropika dari pelanggan
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
39
Lampiran 13. Faktur penjualan narkotika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
40
Lampiran 14. Faktur penjualan psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
41
Lampiran 15. Kartu stok narkotika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
42
Lampiran16. Kartu stok psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
43
Lampiran 17. Pengemasan narkotik
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
44
Lampiran 18. Pengemasan psikotropika
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
45
Lampiran 19. Laporan bulanan narkotika, psikotropika dan prekursor
Universitas Indonesia
Laporan praktek….., Ennie Riben, FFar UI, 2014
Anda mungkin juga menyukai
- Perkembangan Islam Pada Masa Moder2Dokumen12 halamanPerkembangan Islam Pada Masa Moder2Andi SulfianaBelum ada peringkat
- SIPTTKDokumen4 halamanSIPTTKAndi SulfianaBelum ada peringkat
- Laporan Lengkap BBKPM RevisiDokumen91 halamanLaporan Lengkap BBKPM RevisiAndi Sulfiana0% (1)
- Laporan Lengkap BBKPM RevisiDokumen91 halamanLaporan Lengkap BBKPM RevisiAndi Sulfiana0% (1)
- Alur Palayanan Pasien Baru BBKPMDokumen2 halamanAlur Palayanan Pasien Baru BBKPMAndi SulfianaBelum ada peringkat
- PENYIMPANANDokumen5 halamanPENYIMPANANAndi SulfianaBelum ada peringkat
- HIPOTESISDokumen15 halamanHIPOTESISAndi SulfianaBelum ada peringkat
- File PDFDokumen144 halamanFile PDFAndi SulfianaBelum ada peringkat