Kimia-2 SKL 2
Diunggah oleh
Abil DarmaHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Kimia-2 SKL 2
Diunggah oleh
Abil DarmaHak Cipta:
Format Tersedia
KIMIA – II E.
0,026 0C
SIFAT KOLIGATIF LARUTAN 2
8. 21,4 gram basa bervalensi tiga dalam 200
1. SBMPTN 2013 Kode 131 gram air mendidih pada suhu 101,7 0C.
Larutan 5 g urea (Mr = 60) dalam 100 ml Jika derajat ionisasi = 0,8 dan Kb = 0,50
air mempunyai titik didih yang sama maka massa atom relatif logam basa
dengan larutan 8 g zat X nonelektrolit tersebut adalah....
dalam 200 ml air. Massa molekul relatif X A. 107 C. 83 E. 46
adalah… B. 90 D. 56
A. 24 C. 48 E. 96
B. 36 D. 60 9. 3 liter larutan CuSO4 (Mr = 160) pada suhu
27 0C menimbulkan tekanan osmosis
2. SIMAK UI 2013 KODE 139 sebesar 4,5 atm (R = 0,08). Massa CuSO4
A solution made of 5.4 gr M(OH)2 dissolved yang terlarut adalah....
in 500 gr water boils at 100.156◦C. If the A. 22,5 gram
ionization degree of the base is 0.75 and B. 30 gram
the value Kb for water is 0.52◦C/m, what is C. 45 gram
the atomic weight of its metal? D. 67,5 gram
A. 90 C. 52 E. 24 E. 90 gram
B. 56 D. 40
10.Pada suhu yang sama, larutan BaCl 2
3. Sebanyak 45 g senyawa dengan rumus isotonik dengan larutan FeCl 3. Bila
molekul (H2CO)x dilarutkan dalam 500 g air dianggap α=1, maka perbandingan
(Kf = 1,86 der/m) jika titik beku senyawa konsentrasi larutan BaCl2 : FeCl3 adalah....
ini -0,93oC dan Ar C=12, H=1, O= 16 maka A. 1 : 1 D. 3 : 2
harga x adalah.... B. 2 : 3 E. 4 : 3
A. 12 C. 8 E. 4 C. 3 : 4
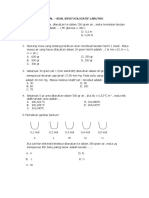
B. 10 D. 6 12. Perhatikan diagram PT berikut:
4. Diketahui Kf air = 1,86. Ar H=1, C= 12, dan
O=16. Titik beku air dalam radiator mobil
yang berisi cairan dengan perbandingan 62
g etilen glikol HOCH2CH2OH, dalam 500 g
air adalah....
A. – 0,93oC D. – 3,72oC
B. – 1,86 C
o
E. – 5,58oC
C. – 7,64 C
o
5. 100 gram asam oksalat, H2C2O4 (Mr = 90), Bagian yang merupakan perubahan wujud
dilarutkan ke dalam 500 mL air (Kb =0,5). dari cair ke gas suatu pelarut adalah...
Jika larutan tersebut mendidih pada suhu A. K – L D.T–M
102oC, maka derajat ionisasi (α) asam B. M – N E.R–N
oksalat adalah.... C. M – P
A. 0,80 C. 0,45 E. 0,30
B. 0,60 D. 0,40 13. Perhatikan diagram P - T berikut!
6. Diantara larutan-larutan dibawah ini yang
mendidih pada suhu tertinggi adalah....
A. CuSO4 0,05 m
B. FeCl3 0,02 m
C. Urea 0,12 m
D. Na3PO4 0,04 m
E. Ba(NO3)2 0,03 m
7. Suatu larutan urea dalam air mempunyai
penurunan titik beku 0,372 0C. Bila Kf air =
1,86 dan Kb = 0,52 maka kenaikan titik
didih larutan larutan urea tersebut Titik beku larutan ditunjukkan oleh....
adalah.... A. K B. L C. M D. N E. Q
A. 2,60 0C
B. 1,04 0C
C. 0,892 0C
D. 0,104 0C
14. Gambar berikut menyatakan diagram P – T larutan 5,0 g naftalena (C10H8) dalam 100 g
air, larutan urea 0,2 M. benzena? (Ar : C = 12 ; H = 1)
(SIMAK UI 2011 kode 511)
A. 81◦C D. 0,99 ◦C
B. 79 C
◦
E. 100,99 ◦C
C. 75 C
◦
21. Jika tekanan osmotik dari 500 ml larutan
glukosa, C6H12O6 (Mr = 180) pada suhu 32°C
sebesar 2 atm, massa glukosa yang terlarut
sebanyak (R = 0,082 L atm /mol K)….
Titik didih larutan urea 0,2 M dinyatakan oleh A. 7,2 gram
titik.... B. 9,0 gram
A. E C. H E. L C. 14,4 gram
B. F D. K D. 18,0 gram
E. 45,0 gram
15. Tekanan osmotik dari 500 ml larutan yang
mengandung 17,1 gram gula (Mr gula = 342) 22. Tetapan kenaikan titik didih molar air adalah
pada suhu 27°C adalah …. (R = 0,082 0,52. Larutan A dibuat dengan melarutkan 9,5
L.atm/mol.K) g MgCl2 (Mr = 95) kedalam 500 g air. Larutan
A. 3 atm B dibuat dengan melarutkan 5,05 g KNO3 (Mr
B. 2,76 atm = 101) ke dalam 500 g air. Kedua senyawa
C. 2,46 atm tersebut terionisasi sempurna di dalam air.
D. 1, 69 atm Perbandingan ∆Tb larutan A terhadap ∆Tb
E. 1 atm larutan B adalah ... (SBMPTN 2015 kode 534)
A. 3/1 D. 2/3
16. Sebanyak 9,5 g Benzofenon (Mr = 190) B. 2/1 E. 1/6
dilarutkan dalam 500 g benzena. Jika titik C. 4/3
didih benzena murni = 80,1 °C dan Kb
benzena = 2,52 °C kg mol -1. Larutan akan 23. Larutan A dibuat dengan mencampurkan 0,5
mendidih pada suhu ... g protein dengan 100 g air. Kenaikan titik
A. 80,35 °C D. 80,95°C didih larutan A adalah 5,0 x 10-3 oC. larutan B
B. 80,57 °C E. 81,33 °C dibuat dengan mencampurkan 0,1 g MgCl 2
C. 80,73 °C dan 100 g air dan memiliki kenaikan titik didih
1,5 x 10-1 oC. perbandingan massa molekul
17. Larutan asam lemah biner 2 m mendidih pada relatif protein terhadap massa molekul relatif
suhu 101,56 °C (Kb = 0,52°C kg mol-1) nilai MgCl2 adalah .... (SBMPTN 2016 kode 203)
derajat ionisasi asam tersebut adalah ... A. 16,7 D. 450
A. 0,1 D. 0,4 B. 50 E. 1500
B. 0,2 E. 0,5 C. 150
C. 0,3
24. Larutan A dibuat dengan mencampurkan
18. Larutan 5 g urea (Mr = 60) dalam 100 ml air 0,005 mol kalium klorida dan 0,03 mol
mempunyai titik didih yang sama dengan magnesium klorida dengan 1 kg air. Larutan B
larutan 8 g zat X nonelektrolit dalam 200 ml dibuat dengan melarutkan 0,01 mol glukosa
air. Massa molekul relatif X adalah… (SBMPTN dalam 500 g air. Bila garam klorida
2013 Kode 131) terdisosiasi sempurna dalam air, maka
A. 24 D. 60 perbandingan kenaikan titik didih larutan A
B. 36 E. 96 terhadap kenaikan titik didih larutan B adalah
C. 48 ... (SBMPTN 2016 kode 204)
A. 10 : 1 D. 1 : 2
19. Sebanyak 14 g elektrolit kuat A2X dilarutkan B. 5 : 1 E. 1 : 1
dalam 1 L air pada 27oC mempunyai tekanan C. 2 : 5
osmosis 7 atm (R = 0,082 L.atm.mol -1.K-1).
Mr A2X adalah (SBMPTN 2017 kode 102) 25.SBMPTN 2013 Kode 439
A. 49,2 D. 147,6 Senyawa antibeku nonelektrolit sebanyak
B. 70,0 E. 210,8 18,6 g dilarutkan dalam 1 L air. Titik beku
C. 140,0 larutan ini sama dengan titik beku larutan
15,15 g KNO3 (Mr = 101) dalam 1 L air. Massa
20. Konstanta kenaikan titik didih untuk benzena molekul relatif senyawa antibeku tersebut
adalah 2,53◦C/m. Jika titik didih benzena adalah…
murni adalah 80◦C, berapakah titik didih A. 15 C. 62 E. 124
B. 31 D. 93
Anda mungkin juga menyukai
- Ulangan Harian 1Dokumen3 halamanUlangan Harian 1YAYAN SUYANTA100% (4)
- KimiaDokumen49 halamanKimiaMANGIHUT PANDAPOTAN "PAKPAHAN"Belum ada peringkat
- Sifat Koligatif LarutanDokumen2 halamanSifat Koligatif Larutanchem1stry1991Belum ada peringkat
- KoligatifDokumen7 halamanKoligatifAndy PutraBelum ada peringkat
- KoligatifDokumen7 halamanKoligatifRio DarputraBelum ada peringkat
- Soal Sifat Koligatif Larutan (Lengkap)Dokumen2 halamanSoal Sifat Koligatif Larutan (Lengkap)Sherly Liana0% (1)
- PTN KoligatifDokumen3 halamanPTN KoligatifPb Nugroho M PjBelum ada peringkat
- Latihan Soal KimiaDokumen6 halamanLatihan Soal KimiaErwin TambaBelum ada peringkat
- Uh Sifat Koligatif Larutan Kode Soal ADokumen9 halamanUh Sifat Koligatif Larutan Kode Soal AatanageBelum ada peringkat
- 4c. Latihan Soal SKLDokumen2 halaman4c. Latihan Soal SKLJuwita Kemala Dewi GeaBelum ada peringkat
- Kunci Jawaban Soal Kimia Brutal 2023Dokumen43 halamanKunci Jawaban Soal Kimia Brutal 2023himmm himmmBelum ada peringkat
- Latihan Soal Sifat Koligatif LarutanDokumen2 halamanLatihan Soal Sifat Koligatif Larutansiti nuraeniBelum ada peringkat
- Latihan KoligatifDokumen3 halamanLatihan KoligatifAfriiqntiBelum ada peringkat
- Uh Sifat Koligatif LarutanDokumen1 halamanUh Sifat Koligatif LarutanSheline Hirfa HirfaBelum ada peringkat
- Soal Sifat Koligatif Larutan (Latihan)Dokumen1 halamanSoal Sifat Koligatif Larutan (Latihan)Ilhamsya Nurghaly AldrianBelum ada peringkat
- Kumpulan Soal Sifat Koligatif LarutanDokumen1 halamanKumpulan Soal Sifat Koligatif LarutanDedi WahyudinBelum ada peringkat
- Soal Sifat Koligatif LarutanDokumen3 halamanSoal Sifat Koligatif Larutanayu irsalinaBelum ada peringkat
- Soal Koligatif LarutanDokumen2 halamanSoal Koligatif LarutanAstuti RaufBelum ada peringkat
- Uh 2014Dokumen8 halamanUh 2014Maria JuanaBelum ada peringkat
- 12 Soal Persiapan Pas GanjilDokumen9 halaman12 Soal Persiapan Pas Ganjil19 Ni Kadek Dea PurnamiBelum ada peringkat
- Sifat KoligatifDokumen4 halamanSifat KoligatifismailfirmanBelum ada peringkat
- LATIHAN SOAL PTS SIFAT KOLIGATIF DAN REDOKS (VOLTA) 2018 RevisiDokumen5 halamanLATIHAN SOAL PTS SIFAT KOLIGATIF DAN REDOKS (VOLTA) 2018 RevisiArisanti MaulidinaBelum ada peringkat
- Kimia PH 1-1Dokumen10 halamanKimia PH 1-1Aura SyifaBelum ada peringkat
- Koligatif LarutanDokumen2 halamanKoligatif LarutanmirdaprismaBelum ada peringkat
- CHAPTER - 3 Kelas 12Dokumen5 halamanCHAPTER - 3 Kelas 12anggaBelum ada peringkat
- Sifat Koligatif LarutanDokumen81 halamanSifat Koligatif LarutanDevi permata sariBelum ada peringkat
- Kimia - Sifat Koligatif LarutanDokumen5 halamanKimia - Sifat Koligatif LarutanClouseizBelum ada peringkat
- Sifat Koligatif Larutan Part 2Dokumen2 halamanSifat Koligatif Larutan Part 2Ririn ArdiantoBelum ada peringkat
- Soal AjaDokumen5 halamanSoal AjaChadmelia Igga MustikaBelum ada peringkat
- Soal Handbook Mapel Kimia Sci 2019 PDFDokumen200 halamanSoal Handbook Mapel Kimia Sci 2019 PDFSusi Susanti100% (2)
- Soal Sifat KoligatifDokumen3 halamanSoal Sifat KoligatifKhalidBelum ada peringkat
- Tugas KimiaDokumen108 halamanTugas KimiaAl-Ihzan L.Belum ada peringkat
- Soal Sifat KoligatifDokumen3 halamanSoal Sifat KoligatifKhalidBelum ada peringkat
- Soal Sifat Koligatif (PG)Dokumen5 halamanSoal Sifat Koligatif (PG)Ryuo GamingBelum ada peringkat
- Sifat Koligatif LarutanDokumen6 halamanSifat Koligatif LarutanAprya Ningsih100% (1)
- Soal KoligatifDokumen3 halamanSoal KoligatifDwi Wahyunanti JohanBelum ada peringkat
- 03 Xii Mipa KimDokumen4 halaman03 Xii Mipa Kimesti rohimahBelum ada peringkat
- Soal Sifat Koligatif Larutan LengkapDokumen5 halamanSoal Sifat Koligatif Larutan Lengkapwiwin jayantiBelum ada peringkat
- Soal Sifat Koligatif LarutanDokumen2 halamanSoal Sifat Koligatif LarutanGito Sucipto100% (1)
- Booster KimiaDokumen7 halamanBooster KimiaAlison burgerBelum ada peringkat
- Soal Uh Sifat Koligatif 2022Dokumen2 halamanSoal Uh Sifat Koligatif 2022Sofi SalsaBelum ada peringkat
- Dokumen - Tips Soal Sifat Koligatif Larutan LengkapDokumen3 halamanDokumen - Tips Soal Sifat Koligatif Larutan LengkapekaemilianaBelum ada peringkat
- Soal Semester 1 Kelas Xii TP 2021-2022Dokumen4 halamanSoal Semester 1 Kelas Xii TP 2021-2022Mifha RhamadaniBelum ada peringkat
- Latihan Sifat Koligatif LarutanDokumen5 halamanLatihan Sifat Koligatif LarutanRens AlbinBelum ada peringkat
- Latihan Soal Sifat Koligatif LarutanDokumen2 halamanLatihan Soal Sifat Koligatif LarutanRaffi Putra NugrohoBelum ada peringkat
- Soal Kimia 12Dokumen5 halamanSoal Kimia 12Kha Ha JaBelum ada peringkat
- Soal Latihan Bab 1 - Sifat Koligatif LarutanDokumen3 halamanSoal Latihan Bab 1 - Sifat Koligatif LarutanIndrabenBelum ada peringkat
- PM Pas 1 Kimia Kelas 12 Sma BiDokumen3 halamanPM Pas 1 Kimia Kelas 12 Sma BiSoni HarsonoBelum ada peringkat
- Soal PDF Untuk SiswaDokumen8 halamanSoal PDF Untuk SiswaDA MaiBelum ada peringkat
- Soal Pas Kimia Kelas Xii 2018Dokumen19 halamanSoal Pas Kimia Kelas Xii 2018laila firda rahmawati100% (1)
- M.Kevin Yashman XII MIPA 3 TUGAS KIMIA REMEDIAL PTSDokumen5 halamanM.Kevin Yashman XII MIPA 3 TUGAS KIMIA REMEDIAL PTSBojez KevinBelum ada peringkat
- Lampiran 3 (Soal)Dokumen9 halamanLampiran 3 (Soal)havizhahBelum ada peringkat
- NN Kelas Xii BaruDokumen2 halamanNN Kelas Xii BaruAnonymous viipLHxyBelum ada peringkat
- US Kelas XII IPA KIMIADokumen3 halamanUS Kelas XII IPA KIMIAWidya AzariaBelum ada peringkat
- Soal Sifat Koligatif LarutanDokumen1 halamanSoal Sifat Koligatif LarutanDwi FitriyaniBelum ada peringkat
- Soal Sifat Koligatif LesDokumen8 halamanSoal Sifat Koligatif Lesnur syabaniawatiBelum ada peringkat
- Soal Pas Kimia Kelas Xii K13Dokumen5 halamanSoal Pas Kimia Kelas Xii K13kikiBelum ada peringkat
- Soal UAS Kelas XII-k13Dokumen5 halamanSoal UAS Kelas XII-k13sri astuti100% (1)
- Kimia UN OrganikDokumen4 halamanKimia UN OrganikAbil DarmaBelum ada peringkat
- Kimia-3 RedoksDokumen2 halamanKimia-3 RedoksAbil DarmaBelum ada peringkat
- Kimia-3 RedoksDokumen2 halamanKimia-3 RedoksAbil DarmaBelum ada peringkat
- Soal Sifat Koligatif LarutanDokumen2 halamanSoal Sifat Koligatif LarutanAbil DarmaBelum ada peringkat