Tipus
Diunggah oleh
rifa nabila0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
8 tayangan10 halamantipus
Judul Asli
tipus
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Initipus
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
8 tayangan10 halamanTipus
Diunggah oleh
rifa nabilatipus
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 10
II.
TINJAUAN PUSTAKA
2.1. Karakteristik Fisik Limbah
Wilgoso (1979) mendefinisikan air limbah sebagai wastewater is water
carriying waste from hames, business and industries that mixture and dissolved or
suspended solids. Yang artinya adalah limbah cair adalah limbah kotor yang
membawa sampah dari tempat tinggal, bangungan, perdagangan, dan industri
berupa campuran air dan bahan padat terlarut atau bahan evaporasi.
Menurut Environmental Protection Agency (1977), air limbah sebagai
wastewater is water carriying dissolvedor suspended solids from homes farms
business and industries. Yang artinya limbah cair adalah air yang membawa
bahan padat terlarut atau tersuspensi dari tempat tinggal, kebun,bangunan
perdagangan dan industri. Menurut Salvato 1982, air limbah adalah air bekas yang
berasal dari penyediaan air bersih sudah dicemari berbagai macam
penggunaannya.
Limbah adalah sampah cair dari suatu lingkungan masyarakat dan
terutama terdiri dari air yang telah digunakan dengan hampir 0,1% dari padatan
berupa benda-benda padat yang terdiri dari zat organik dan non-organik (Mahida,
1984), sedangkan menurut Gintings (2005), limbah adalah buangan yang
kehadirannya pada suatu saat dan tempat tertentu tidak dikehendaki di lingkungan
karena ternyata tidak mempunyai nilai ekonomi.
Perubahan fisik yang ditimbulkan dalam air limbah yaitu: padatan, bau,
temperatur, dan warna. Padatan terdiri dari bahan padat organik maupun
anorganik yang larut, mengendap maupun suspensi. Bahan ini akan mengendap
pada dasar air yang lama kelamaan menimbulkan pendangkalan pada dasar badan
penerima. Akibat lain dari padatan ini menimbulkan tumbuhnya tanaman air
tertentu dan dapat menjadi racun bagi makhluk lain. Banyak padatan
menunjukkan banyaknya lumpur terkandung dalam air.
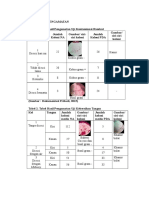
Gambar 1. Hubungan antara Sumber Limbah dan Karakteristik
Sumber: www.google.com
Bau timbul karena adanya kegiatan mikroorganik yang menguraikan zat
organik menghasilkan gas tertentu. Di samping itu bau juga timbul karena
terjadinya reaksi kimia yang menimbulkan gas. Kuat tidaknya bau yang
dihasilkan limbah tergantung pada jenis dan banyak gas yang ditimbulkan.
Temperatur air limbah mempengaruhi badan penerima bila terdapat perbedaan
suhu yang cukup besar. Temperatur air limbah akan mempengaruhi kecepatan
reaksi kimia serta tata kehidupan dalam air. Perubahan suhu memperlihatkan
aktivitas kimiawi biologis pada benda padat dan gas dalam air. Pembusukan
terjadi pada suhu yang tinggi dan tingkatan oksidasi zat organik jauh lebih besar
pada suhu yang tinggi.
Warna timbul akibat suatu bahan terlarut atau tersuspensi dalam air, di
samping adanya bahan pewarna tertentu yang kemungkinan mengandung logam
berat. Bau disebabkan karena adanya campuran dari nitrogen, fospor, protein,
sulfur, amoniak, hidrogen sulfida, carbon disulfida dan zat organik lain. Kecuali
bau yang disebabkan bahan beracun, jarang merusak kecepatan manusia tapi
mengganggu ketenangan bekerja.
Sifat fisik limbah cair yang miuda terlihat dapat menentukan derajat
pengotoran air limbah pertanian. Sifat-sifat fisik yang penting diantaranya adalah
kandungan zat-zat padat yang menunjukkan kejernihan air, bau, warna, suhu, dan
pH. Air sering digunakan sebagai medium pendingan dalam berbagai proses
produksi. Air tersebut selanjutnya dibuang ke tempat asalnya seperti sungai atau
sumber lainnya. Air buangan yang mempunyai suhu lebih tinggi dari tempat
asalnya, dapat menimbulkan berbagai akibat :jumlah oksigen terlarut (DO) dalam
air menurun, kecepatan reaksi meningkat, kehidupan biota air terganggu atau
mati. Nilai pH air terpopulasi berbeda-beda tergantung dari jenis buangannya.
Perubahan tajam keasaman air limbah ke arah alkali (pH>7) maupun ke arah asam
(pH<7) dapat mengganggu biota makhluk hidup disekitar tempat tersebut. Air
limbah dengan pH asam dapat bersifat korosif terhadap baja pipa-pipa besi.
Jumlah endapan pada contoh air merupakan sisa penguapan dari contoh air limbah
pada suhu 103-105 oC. Jumlah total endapan terdiri dari benda-benda yang
mengendap, terlarut, dan tercampur.
2.2 Pengujian COD
COD adalah jumlah oksigen yang dibutuhkan untuk mengoksidasi senyawa
organic dalam contoh. Parameter COD menunjukkan jumlah senyawa organik
dalam air yang dapat dioksidasi secara kimia. Oksidator yang umm digunakan
adalah Kalium Dikromat. Beberapa metode pengukuran COD diantaranya adalah
metode tanpa refluks untuk kadar air tinggi, metode refluks untuk kadar air
rendah, metode untuk air garam.
Analisis COD adalah menentukan banyaknya oksigen yang diperlukan
untuk mengoksidasi senyawa organik secara kimiawi. Hasil analisis COD
menunjukkan kandungan senyawa organik yang terdapat dalam limbah. Bahan
organik yang ada diurai secara kimia dengan menggunakan oksidator kuat kalium
bikromat pada kondisi asam dan panas dengan katalisator perak sulfat, sehingga
segala macam bahan organik akan teroksidasi. COD atau Chemical Oxygen
Demand adalah jumlah oksigen yang diperlukan untuk mengurai seluruh bahan
organik yang terkandung dalam air (Boyd, 1990). Hal ini karena bahan organik
yang ada sengaja diurai secara kimia dengan menggunakan oksidator kuat kalium
bikromat pada kondisi asam dan panas dengan katalisator perak sulfat sehingga
segala macam bahan organik, baik yang mudah urai maupun yang kompleks dan
sulit urai, akan teroksidasi. Nilai COD secara umum lebih tinggi dari nilai BOD
karena sebagian besar bahan organik lebih mudah dioksidasi secara kimiawi
daripada secara biologi (Aryani dan Widiyani, 2004).
Prinsip dari pengujian COD ini adalah jumlah oksidan Cr2O72- yang
bereaksi dengan contoh uji dan dinyatakan sebagai mg O2 untuk tiap 1000 ml
contoh uji. Senyawa organik dan anorganik, terutama organik dalam contoh uji
dioksidasi oleh Cr2O72- dalam refluks tertutup mengahsilkan Cr3+. Jumlah oksidan
yang dibutuhkan dinyatakan dalam ekuivalen oksigen (O2 mg/L).
2.3 Pengujian BOD dan DO
2.3.1 Pengujian BOD
Pada umumnya indikasi polusi air dapat ditunjukkan berdasarkan
peningkatan bahan-bahan terdekomposisi (organik) ke dalam air sungai atau
danau sebagai tempat pembuangan limbah. Masuknya bahan-bahan tesebur ke
dalam badan air akan mengubah sifat fisik, kima dan biologis air sehingga
kandungan oksigen terlarut dalam air akan menurun.
Ketersediaan oksigen dalam air dapat habis akibat pertumbuhan mikroba
pengurai, sehingga dapat terjadi kondisi anaeoribik yang menyebabkan kematian
biota air seperti ikan dan tanaman. Jumlah oksigen yang digunakan oleh mikroba
tergantung dari jumlah limbah yang terdekomposisi, sehingga untuk mencegah
peningkatan mikroba pembusuk harus dilakukan pemecahan limbah sesempurna
mungkin sebelum limbah tersebut dibuang ke pembuangan akhir.
Salah satu cara untuk mendeteksi kualitas air secara kimiawi adalah
dengan melakukan uji BOD (biochemical Oxygen Demand). BOD adalah
banyaknya oksigen yang dibutuhkan oleh bakteri selama penguraian senyawa
organik pada kondisi aerobik. Paramater BOD yang digunakan untuk menentukan
tingkat pencemaran oleh senyawa organik BOD kira kira 1 -10 ppm, sedangkan
untuk air tercemar mempunyai nilai BOD> 10 ppm. Beberapa metode untuk
mengukur BOD adalah metode sederhana (inkubasi), metode AOAC (1984),
metode standar, dan metode Manometrik (Jennie dan Fardiaz, 1989).
2.3.2 Pengujian DO
Oksigen terlarut dalam air berasal dari fotosintesa atau absorpsi dari udara.
Oksigen dari udara jumlahnya tidak tetap, sedangkan kecepatan absorpsi dari
udara sangat terbatas. Air limbah yang terpopulasi bahan-bahan organik akan
meningkatkan aktivitas aerobik, sehingga terjadi konsumsi oksigen terlarut dakam
jumlah besar. Akibatnya air akan kekurangan oksigen terlarut. Oleh karena itu,
untuk menganalisa jumlah bahan organik yang terdapat dalam air perlu diketahui
pula jumlah oksigen terlarut (DO).
Beberapa metode untuk mengukur oksigen terlarut diantaranya adalah
dengan metode Winkler, metode Azida, metode permanganat, metode Pomeroy-
Kirshman-Alsterberg, metode Chemtrix Oxygen, metode membran Elektroda (DO
meter), atau dengan metode titrasi lainnya. Pengukuran oksigen terlarut harus
dianalisa secepat mungkin, karena kelarutan oksigen dalam air sangat dipengaruhi
oleh temperatur dan tekanan udara. Senyawa reduktor atau oksidator (nitrit) dalam
air dapat mengganggu pengukuran oksigen dengen metode Winkler. Untuk
mencegah gangguan tersebut harus ditambahkan senyawa Natrium Azide (NAN3)
ke dalam oksigen.
2.4 Perhitungan Total Mikroorganisme Limbah
Penyebaran mikroorganisme yang tumbuh pada limbah terdiri dari bakteri,
jamur/kapang, virus dan disamping itu terdapat juga binatang satu sel.
Pertumbuhan dan perkembangan mikroorganisme akan menyebabkan perubahan-
perubahan tertentu yaitu : perubahan yang bersifat fisik dan dan kimiawi, sebagai
contoh yaitu: konsistensi bahan menjadi lunak, timbul gas atau aroma tertentu dan
zat racun yang membahayakan. Jumlah penyebaran bakteri/mikroorganisme pada
limbah yang sedang mengalami pembusukan sangat bervariasi jumlahnya dan
tidak sama jenis (species)-nya serta tergantung pada: varietas, habitat, susunan
kimia, cara penanganan, suhu penyimpanan dan lain-lain.
Pertumbuhan mikroorganisme yang membentuk koloni dapat dianggap
bahwa setiap koloni yang tumbuh berasal dari satu sel, maka dengan menghitung
jumlah koloni dapat diketahui penyebaran bakteri yang ada pada bahan. Jumlah
mikroba pada suatu bahan dapat dihitung dengan berbagai macam cara,
tergantung pada bahan dan jenis mikrobanya. Ada 2 macam cara perhitungan
jumlah mikroba/bakteri, yaitu perhitungan secara langsung dan tidak langsung.
Perhitungan secara tidak langsung dapat dilakukan dengan beberapa cara yaitu:
1. Penentuan volume total
Cara ini adalah semacam modifikasi penentuan hematokrit pada
pengukuran volume total butir-butir darah, misalnya 10 ml biakan dimasukkan ke
dalam tabung reaksi khusus (tabung hopklins) yang bagian bawahnya berupa
silinder dan bergaris ukuran.
2. Metode turbidometri
Teknik ini sudah dipakai sebagai cara mengukur keker han suspensi atas
dasar penyerapan dan pemencaran cahaya yang dilintaskan, sehingga yang
mengandung lebih dari 107 - 108 sel/ml, tampak lebih keruh oleh mata telanjang.
Suatu volume biakan yang telah ditakar ditempatkan dalam tabung khusus yang
jernih dengan diameter tertentu. Berbeda dengan hal di atas, perhitungan langsung
dapat dilakukan dengan cara sebagai berikut :
1. Perhitungan sel langsung
Cara ini menggunakan bilik hitung (hemoci tometer) yang menghasilkan
hitungan total, karena semua sel terhitung, baik sel yang hidup maupun sel yang
mati. Karena bakteri itu kecil, maka perhitungan yang dilakukan secara statistik
dapat diterima, namun harus dibuat suspensi sekurang-kurangnya 107/ ml.
2. Menghitung dengan alat penghitung elektronik
Dengan alat ini dapat dihitung beribu-ribu bakteri dalam beberapa detik.
Penggunaan alat ini banyak didasarkan atas kerja dengan lobang pengintai
elektronik (dapat disamakan dengan mata elektronik) kerjanya tergantung pada
interupsi dari berkas cahaya elektronik yang melintasi suatu ruang antara dua
ruang elektron yang berdekatan letaknya. Tiap partikel yang karena perbedaan
kkonduktivitas sel dan cairan. Interupsi ini dicetak oleh suatu alat secara elektris.
3. Menghitung dengan metode cawan
Metode perhitungan cawan didasarkan pada anggapan bahwa setiap sel
yang hidup dapat berkembang menjadi koloni. Jadi jumlah koloni yang muncul
pada cawan adalah indeks bagi jumlah mikroorganisme yang terkandung dalam
sampel. Teknik yang harus dikuasai dari metode ini adalah mengencerkan sampel
dan mencawankan hasil pengenceran tersebut. Setelah inkubasi, jumlah semua
koloni diamati untuk memenuhi persyaratan statistik. Cawan yang dipilih untuk
menghitung koloni adalah cawan yang mengandung antara 30 sampai 300 koloni.
Organisme yang terdapat dalam sampel asal ditentukan dengan mengalikan
jumlah koloni yang terbentuk dengan faktor pengenceran pada cawan yang
bersangkutan.
Metode hitungan cawan dibedakan atas dua cara, yaitu metode tuang (pour
plate) dan metode permukaan (surfacelspread plate). Pada metode tuang, sejumlah
sampel (1 ml atau 0,1 ml) dari pengenceran yang dikehendaki dimasukkan ke
dalam cawan petri, kemudian ditambhkan agar-agar cair yang steril yang telah
didinginkan (47-50oC) sebanyak 15-20 ml dan digoyangkan supaya sampelnya
menyebar. Metode ini merupakan cara yang paling sensitif untuk menentukan
jumlah jasad renik, dengan alasan :
Hanya sel mikroba yang hidup yang dapat dihitung
Beberapa jasad renik dapat dihitung sekaligus
Dapat digunakan untuk isolasi dan identifikasi mikroba, karena koloni
yang terbentuk mungkin berasal dari mikroba yang mempunyai
penampakan spesifik.
Selain keuntungan-keuntungan tersebut di atas, metode hitungan cawan
juga memiliki kelemahan sebagai berikut :
Hasil perhitungan tidak menunjukkan hasil yang sebenarnya, karena
beberapa sel yang berdekatan mungkin membentuk koloni.
Medium dan kondisi inkubasi yang berbeda mungkin menghasilkan
jumlah yang berbeda pula.
Mikroba yang ditumbuhkan harus dapat tumbuh pada medium padat dan
membentuk koloni yang kompak, jelas, dan tidak mnyebar.
Memerlukan persiapan dan waktu inkubasi relatif lama sehingga
pertumbuhan koloni dapat dihitung
2.5 Pengujian Bakteri Koliform
Bakteri koliform merupakan golongan mikroorganisme yang lazim
digunakan sebagai indikator, dimana bakteri ini dapat menjadi indikator untuk
menentukan suatu sumber air telah terkontaminasi oleh patogen atau
tidak. Berdasarkan penelitian, bakteri koliform ini menghasilkan zat etionin yang
dapat menyebabkan kanker. Selain itu, bakteri pembusuk ini juga memproduksi
bermacam-macam racun sepertin indol dan skatol yang dapat menimbulkan
penyakit bila jumlahnya berlebih di dalam tubuh. Bakteri koliform dapat
digunakan sebagai indikator karena densitasnya berbanding lurus dengan tingkat
pencemaran air. Bakteri ini dapat mendekteksi patogen pada air seperti virus,
protozoa, dan parasit. Selain itu, bakteri ini juga memiliki daya tahan yang lebih
tinggi daripada patogen serta lebih mudah diisolasi dan ditumbuhkan (Wikipedia,
2012).
Suatu metode telah dikembangkan untuk membedakan antara koliform
fekal (Eschericia coli) dan koliform nonfekal (Enterobacter aerogenes) (Fardiaz,
1992). Bakteri koliform fekal digunakan sebagai indikator pencemaran
dikarenakan jumlah koloninya pasti berkorelasi positif dengan keberadaan bakteri
patogen. Selain itu, mendeteksi koliform jauh lebih murah, cepat, dan sederhana
daripada mendeteksi bakteri patogenik lain. Beberapa metode untuk mengetahui
jumlah koliform pada sampel diantaranya adalah metode MPN, metode SPC,
metode Millipore Membran Filter (MF), dll.
E. coli disebut koliform fekal karena ditemukan dalam saluran usus hewan
dan manusia, sehingga sering terdapat di dalam feses. E. aerogenes disebut
koliform non fekal karena tidak merupakan flora normal di dalam saluran
pencernaan, melainkan ditemukan pada tanaman/hewan yang telah mati, dan
sering menimbulkan lendir pada makanan. Kedua bakteri ini merupakan bakteri
berbentuk basil, gram negatif, dan bersifat anaerobik fakultatif (Fardiaz, 1992).
Untuk mengetahui jumlah sel bakteri golongan coliform yang terdapat
dalam sampel air, dilakukan Metode Jumlah Perkiraan terdekat atau Most
Probable Number. Penggunaan media selektif dan diferensial sangat membantu
mempercepat usaha pemeriksaan air guna mendeteksi organism coliform.
Pemeriksaan tersebut terdiri dari 3 langkah berurutan:
1) Uji Pendugaan (Presumptive Test)
2) Uji Lanjutan (Confirmed Test)
3) Uji Pelengkap (Complete Test)
Kelompok bakteri coliform antara lain Eschericia coli, Enterrobacter
aerogenes, dan Citrobacter fruendii.Keberadaan bakteri ini dalam air minum juga
menunjukkan adanya bakteri patogen lain, misalnya Shigella, yang bisa
menyebabkan diare hingga muntaber (Kompas Cyber Media, 2003 dalam
Kompas.com).
2.6 Pengujian Bakteri Salmonella-Shigella
Salmonella adalah penyebab utama dari penyakit yang disebarkan melalui
makanan (foodborne diseases). Pada umumnya, serotipe Salmonella menyebabkan
penyakit pada organ pencernaan. Penyakit yang disebabkan oleh Salmonella
disebut Salmonellosis. Ciri-ciri orang yang mengalami salmonellosis adalah diare,
keram perut, dan demam dalam waktu 8-72 jam setelah memakan makanan yang
terkontaminasi oleh Salmonella. Gejala lainnya adalah demam, sakit kepala, mual
dan muntah-muntah. Tiga serotipe utama dari jenis S. enterica adalah S. typhi, S.
typhimurium, dan S. enteritidis. S. typhi menyebabkan penyakit demam tifus
(Typhoid fever), karena invasi bakteri ke dalam pembuluh darah dan
gastroenteritis, yang disebabkan oleh keracunan makanan/intoksikasi. Gejala
demam tifus meliputi demam, mual-mual, muntah dan kematian. S. typhi memiliki
keunikan hanya menyerang manusia, dan tidak ada inang lain. Infeksi Salmonella
dapat berakibat fatal kepada bayi, balita, ibu hamil dan kandungannya serta orang
lanjut usia. Hal ini disebabkan karena kekebalan tubuh mereka yang menurun.
Bakteri Shigella merupakan bakteri gram negatif, anaerobic fakultatif,
berbentuk bacillus (batang), famili Enterobakteriaceae, nonmotil, tidak dapat
menggunakan sitrat sebagai sumber karbon tunggal dan melakukan fermentasi
karbohidrat, mempunyai bentuk antigenik berupa plasmid yang kompleks
sehingga memberikan kemudahan dalam menembus sel inang. Genus Shigella
terdiri dari empat spesies penting yaitu, S. dysentriae, S. flexneri, S. boydii dan S.
sonnei.
Dilihat dari klasifikasi ilmiahnya, bakteri Salmonella dan Shigella
memiliki kekerabatan yang sangat dekat karena satu famili, yakni
Enterobakteriaceae. Famili ini memiliki bentuk basil gram negatif, bersifat
anaerobik fakultatif. Kebanyakan anggotanya mempunyai flagela monotrikat,
kecuali Shigella yang tidak mempunyai flagela. Hal inilah yang membedakan
antara bakteri Salmonella dan Shigella (Fardiaz,1992).
Anda mungkin juga menyukai
- Penda Hulu AnDokumen2 halamanPenda Hulu Anrifa nabilaBelum ada peringkat
- Laprak SayuranDokumen22 halamanLaprak Sayuranrifa nabilaBelum ada peringkat
- Komponen ToksikDokumen5 halamanKomponen Toksikrifa nabilaBelum ada peringkat
- ImprovementDokumen3 halamanImprovementrifa nabilaBelum ada peringkat
- DAPUS KeccDokumen1 halamanDAPUS Keccrifa nabilaBelum ada peringkat
- Design Project Material Transfer RMDokumen1 halamanDesign Project Material Transfer RMrifa nabilaBelum ada peringkat
- Hasil Pengamatan Sanitasi PekerjaDokumen2 halamanHasil Pengamatan Sanitasi Pekerjarifa nabilaBelum ada peringkat
- Makalah Evaluasi Biologis Ketersediaan Vs EfesiensiDokumen18 halamanMakalah Evaluasi Biologis Ketersediaan Vs Efesiensirifa nabilaBelum ada peringkat
- Makalah Evaluasi Biologis Ketersediaan Vs EfesiensiDokumen18 halamanMakalah Evaluasi Biologis Ketersediaan Vs Efesiensirifa nabilaBelum ada peringkat
- TipusDokumen3 halamanTipusrifa nabilaBelum ada peringkat
- Latar Belakang ShilaDokumen1 halamanLatar Belakang Shilarifa nabilaBelum ada peringkat
- HASPENG Sabu Karinnnnnnn2Dokumen4 halamanHASPENG Sabu Karinnnnnnn2rifa nabilaBelum ada peringkat
- Penda Hulu AnDokumen3 halamanPenda Hulu Anrifa nabilaBelum ada peringkat
- Haspeng SabuDokumen7 halamanHaspeng Saburifa nabilaBelum ada peringkat
- Contoh Dokumen 2Dokumen3 halamanContoh Dokumen 2rifa nabilaBelum ada peringkat
- HaspengmolimbahDokumen2 halamanHaspengmolimbahrifa nabilaBelum ada peringkat
- Sanitasi 02Dokumen8 halamanSanitasi 02rifa nabilaBelum ada peringkat
- Pembahasan MimaDokumen1 halamanPembahasan Mimarifa nabilaBelum ada peringkat
- Latbel TujuanDokumen1 halamanLatbel Tujuanrifa nabilaBelum ada peringkat
- Tabel Suhu TinggiDokumen1 halamanTabel Suhu Tinggirifa nabilaBelum ada peringkat
- Alba + TujuanDokumen3 halamanAlba + Tujuanrifa nabilaBelum ada peringkat
- Teori Dasar KemasanDokumen2 halamanTeori Dasar Kemasanrifa nabilaBelum ada peringkat
- Contoh Dokumen 2 Dan 3'isiDokumen4 halamanContoh Dokumen 2 Dan 3'isirifa nabilaBelum ada peringkat
- Has Peng OnlyDokumen4 halamanHas Peng Onlyrifa nabilaBelum ada peringkat
- Haspeng Sabu Gula TinggiDokumen2 halamanHaspeng Sabu Gula TinggiAgraBelum ada peringkat
- 25-2 Daftar PustakaDokumen2 halaman25-2 Daftar Pustakarifa nabilaBelum ada peringkat
- Dapus KonseparDokumen1 halamanDapus Konseparrifa nabilaBelum ada peringkat
- Prose DurDokumen2 halamanProse Durrifa nabilaBelum ada peringkat
- Studi Kasus Pengawasan Mi Instan Dengan HACCPDokumen9 halamanStudi Kasus Pengawasan Mi Instan Dengan HACCPrifa nabila100% (1)