Jawaban Asam Basah
Diunggah oleh
oktiana putrii0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
17 tayangan9 halamanJudul Asli
jawaban asam basah
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
17 tayangan9 halamanJawaban Asam Basah
Diunggah oleh
oktiana putriiHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 9
1.
Menurut Arhenius
Asam adalah zat yang dapat menghasilkan ion H+ di dalam air,
sedangkan basa adalah zat yang dapat menghasilkan ion OH- di
dalam air. Contohnya :
HCl -------> H+ + Cl-
CH3COOH -------> CH3COO- + H+
KOH ------> K+ + OH-
NH4OH ------> NH4+ + OH-
2. Asam
sifat senyawa adalah konduktor listrik
mengandung derajat keasaman pH < 7
mempunyai rasa asam
jika dilarutkan dalam air maka akan menghasilkan ion H+
dalam interaksi kimia : donatur proton
Basa
sifat senyawa adalah bukan konduktor listrik
mengandung derajat keasamana pH > 7
mempunyai rasa pahit
jika dilarutkan dalam air maka akan menghasilkan ion OH-
dalam interaksi kimia : akseptor proton
3. Contoh reaksi ionisasi larutan asam kuat
Asam klorida
Asam bromida
Asam iodida
Asam sulfat
Asam perklorat
Asam nitrat
4. Contoh reaksi ionisasi larutan basa kuat
Natrium hidroksida
Kalium hidroksida
Litium hidroksida
Kalsium hidroksida
Stronsium hidroksida
Barium hidroksida
5. -menggunakan kertas lakmus
.jika lakmus merah dicelupkan dalam suatu larutan warnanya tetap,
atau lakmus biru dicelupkan dalam suatu larutan warnanya berubah
merah, berarti larutan tersebut bersifat asam
.jika lakmus merah dicelupkan dalam suatu larutan warnanya
berubah biru, atau lakmus biru dicelupkan dalam suatu larutan
warnanya tetap, maka larutan tersebut bersifat basa
-menggunakan indikator universal
celupkan kertas indikator universal ke dalam suatu larutan, amati
perubahan warnanya dan cocokkan ke klasifikasi warna beserta
derajat pHnya di box kemasan.
(dan masih banyak lagi, seperti indikator alami, fenoftalein, metil
biru, metil merah, metil jingga dsb)
4.9
6. Contoh asam organik:
Asam askorbat atau vitamin C (C₆H₈O₆)
Asam sitrat (C₆H₈O₇)
Asam asetat atau asam cuka (CH₃COOH)
Asam propionat (CH₃CH₂CO₂H)
Asam butanoat (CH₃CH₂CH₂-COOH)
Contoh asam anorganik:
Asam sulfat (H₂SO₄)
Asam nitrat (HNO₃)
Asam klorida (HCl)
Asam iodida (HI)
Asam florida (HF)
7. Contoh asam kuat
Asam sulfat (H₂SO₄)
Asam Klorida (HCl)
Asam perklorat (HClO₄)
Asam nitrat (HNO₃)
Asam Iodida (HI)
Contoh asam lemah
Asam nitrit (HNO₂)
Asam formiat (HCOOH)
Asam florida (HF)
Asam fosfat (H₃PO₄)
Asam asetat (CH₃COOH)
8. Contoh Larutan Basa Kuat :
NaOH = natrium hidroksida
KOH = kalium hidroksida
Ba(OH)₂ = barium hidroksida
Ca(OH)₂ = kalsium hidroksida
Mg(OH)₂ = magnesium hidroksida
Contoh Larutan Basa Lemah :
NH₄OH = amonium hidroksida
Fe(OH)₂ = besi (II) hidroksida
Zn(OH)₂ = seng / zink hidroksida
Cu(OH)₂ = tembaga (II) hidroksida
Al(OH)₃ = aluminum hidroksida
9. Asam sulfat H₂SO₄ termasuk jenis asam kuat bervalensi 2, sesuai
jumlah ion H⁺
Diketahui H₂SO₄ 0,05 M yang akan ditentukan nilai pH.
a.⇔ [H⁺] = valensi x M
⇔ [H⁺] = 2 x 0,05
⇔ [H⁺] = 10⁻¹ molar
Selanjutnya,
⇔ pH = - log [H⁺]
⇔ pH = - log [10⁻¹]
Diperoleh pH sebesar 1
b. V KOH = 100 mL
M HCOOH = 0,04 M
V KOH = 100 mL
M KOH = 0,04 M
Ka HCOOH = 2 x 10⁻⁴
Kw = 1 x 10⁻¹⁴
10. asam asetat CH3COOH
asam sulfat H2SO4
natrium hidroksida NaOH
magnesium hidrosida Mg(OH)2
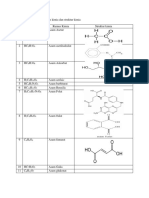
N Senyawa Rumus Kimia Reaksi Ionisasi
o
1 Asam Asetat CH3COOH CH3COOH → CH3COO- +
H+
2 Asam Arsenat H3AsO4 H3AsO4 → AsO4- + 3H+
3 Asam Benzoat C6H5COOH C6H5COOH → C6H5COO-
+ H+
4 Asam Borat H3BO3 H3BO3 → BO33- + 3H+
5 Asam Karbonat H2C03 H2C03 → CO33- + 2H
6 Asam Formiat HCOOH HCOOH → HCOO- + H+
7 Asam Iodida HI HI →I- + H+
8 Asam Bromida HBr HBr → Br- + H+
9 Asam Klorida HCl HCl → Cl- + H+
10 Asam Fluorida HF HF → F- + H+
11 Asam Sianida HCN HCN → CN- + H+
12 Asam Sulfida H2S H2S → S2- + 2H+
13 Asam Nitrat HNO3 HNO3 → NO3- + H+
14 Asam Nitrit HNO2 HNO2 → N02- + H+
15 Asam Oksalat H2C2O4 H2C2O4 → C2O42- + 2H+
16 Asam Fosfat H3PO4 H3PO4 → PO43- + 3H+
17 Asam Sulfat H2SO4 H2SO4 → SO42- +2H+
18 Asam Triosianat HSCN HSCN → SCN- + H+
19 Asam Klorat HClO3 HClO3 → ClO3- + H+
20 Asam Perklorat HClO4 HClO4 → ClO4- + H+
21 Asam Silikat H2SiO3 H2SiO3 → SiO32- + 2H+
22 Asam Stanat H2SNO3 H2SNO3 → SNO32- + 2H+
23 Asam Stanit H2SNO2 H2SNO2 → SNO22- + 2H+
24 Asam Plumbat H2PbO3 H2PbO3 → PbO32- + 2H+
25 Asam Plumbit H2PbO2 H2PbO2 → PbO22- + 2H+
26 Asam Arsenit H3ASO4
27 Asam Finol C6H5OH
28 Asam Fiosianat H5CN
29 Asam Hipoklorit HClO
30 Asam Sulfit H2SO3
31 Asam Askorbat C5H8O6
32 Asam Sitrat C6H8O7
33 Asam Laktat C3H5O3
34 Asam Rodat HIO3
35 Asam Hipobromit HBrO3
36 Asam Karboksilat ArCOOH
37 Asam Tioasetat CH5CO5H
38 Asam Propinat H7C3COOH
39 Asam Larutan CH3(CH2)10COO
H
40 Asam Palmiat CH3(CH2)14COO
H
41 Asam CH3(CH2)16COO
Oktadekanoat H
42 Asam Butirat CH3(CH2)2COOH
43 Asam Valerat CH3(CH2)3COOH
44 Asam Kaproat CH3(CH2)4COOH
45 Asam Enatoat CH3(CH2)5COOH
46 Asam Kaprilat CH3(CH2)6COOH
47 Asam Pelargonat CH3(CH2)7COOH
48 Asam Koprat CH3(CH2)8COOH
49 Asam Miristat CH3(CH2)12COO
H
50 Asam Araohidit CH3(CH2)18COO
H
51 Asam Adipat C6H12O4
52 Asam Aspartat C4H7NO4
53 Asam Asparagina C4H8N2O3
54 Asam Glutamia C5H10N2O3
55 Asam Lisina C6H14N2O3
56 Asam Arginia C6H14N4O2
57 Asam Histidina C6H9N8O2
58 Asam Sisteina C8H7NO2S
59 Asam Metionina C5H11NO2S
60 Asam Ontimonit H2SBO3
61 Asam Ontimonat H2SBO4
62 Asam Prolina C5H9NO2
63 Asam Triftotan C11H12N2O2
64 Asil Halida RCOX
65 Tria Zina C3H3N3
66 Aspartam C14H18
67 Arachidic Acid CH3(CH2)18COO
H
68 Oleic C18H34O2
69 Bohenic C22H44O2
70 Arachic C20H40O2
71 Steatik C18H36O2
72 Palmilik C16H32O2
73 Asam Amino C2H5NO2
Glisina
74 Asam Amino C3H7NO2
Alavina
75 Asam Amino C5H11NO2
Valina
76 Asam Amino C6H13NO3
Leusina
Anda mungkin juga menyukai
- 76 Macam Asam Dan ReaksinyaDokumen3 halaman76 Macam Asam Dan ReaksinyaHime_Chiaki100% (1)
- 76 Nama Senyawa AsamDokumen3 halaman76 Nama Senyawa AsamAnyndahBelum ada peringkat
- Asam & Basa Beserta IonisasinyaDokumen4 halamanAsam & Basa Beserta IonisasinyaNissa Rahma100% (2)
- Daftar Nama Larutan Asam Dan BasaDokumen15 halamanDaftar Nama Larutan Asam Dan Basamohamad erwin supuBelum ada peringkat
- 7 Asam KuatDokumen3 halaman7 Asam KuatFahrul SyawalBelum ada peringkat
- Asam BasaDokumen4 halamanAsam BasaRaraIsparaniRafifahPutri100% (1)
- Tata Nama AsamDokumen9 halamanTata Nama AsamIlham TobingBelum ada peringkat
- Asam BasaDokumen2 halamanAsam Basapratiwi rahmadantiBelum ada peringkat
- DokumenDokumen11 halamanDokumenPutri warisoBelum ada peringkat
- Asam KuatDokumen4 halamanAsam Kuatovan05Belum ada peringkat
- Tabel Nama Dan Rumus Asam AnorganikDokumen5 halamanTabel Nama Dan Rumus Asam AnorganikYahya Bachrun100% (1)
- Daftar Nama Larutan Asam Dan BasaDokumen4 halamanDaftar Nama Larutan Asam Dan BasaKhalilah SyawaBelum ada peringkat
- Daftar AsambasaDokumen3 halamanDaftar Asambasasri astutiBelum ada peringkat
- Asam Basa Kuat LemahDokumen8 halamanAsam Basa Kuat Lemahtaufiq bapiq100% (1)
- Asam Kuat Dan Lemah (Full)Dokumen4 halamanAsam Kuat Dan Lemah (Full)VaniaBelum ada peringkat
- Jenis AsamDokumen2 halamanJenis AsamIvan MaulanaBelum ada peringkat
- Daftar Asam Dan Basa Kuat DanDokumen6 halamanDaftar Asam Dan Basa Kuat DanRayhan Genos100% (3)
- Asam Lemah-KuatDokumen6 halamanAsam Lemah-KuatFitria Feb.Belum ada peringkat
- Asamkarboksilat Ester DiahDokumen29 halamanAsamkarboksilat Ester DiahwidiyaBelum ada peringkat
- Tabel Kimia Asam BasaDokumen1 halamanTabel Kimia Asam BasaNadira Erwanto100% (6)
- Asam & BasaDokumen4 halamanAsam & BasaDear Farah Sielma0% (1)
- Asam KuatDokumen2 halamanAsam KuatAlan Adiwijaya100% (1)
- Daftar Asam BasaDokumen3 halamanDaftar Asam BasaNurulita AyuningtyasBelum ada peringkat
- Daftar Asam & BasaDokumen5 halamanDaftar Asam & BasaYoga VirgozBelum ada peringkat
- Larutan Asam BasaDokumen18 halamanLarutan Asam BasaDamar DjatiBelum ada peringkat
- Rumus Kimia Sekitar KitaDokumen3 halamanRumus Kimia Sekitar KitamulyanaBelum ada peringkat
- MATERI KULIAH KIMDAS (ASAM & BASA) Copy (1) - 1Dokumen95 halamanMATERI KULIAH KIMDAS (ASAM & BASA) Copy (1) - 1Yusril Fikri AmrullahBelum ada peringkat
- Asam KuatDokumen3 halamanAsam KuatSeaGate IvyBridge MsiNvidiaBelum ada peringkat
- Tata Nama Asam Basa KimiaDokumen4 halamanTata Nama Asam Basa KimiaJames Burton100% (1)
- Rumus KimiaDokumen3 halamanRumus KimiaRendi Nak SepusatBelum ada peringkat
- Kunci Jawaban Latihan Soal Hidrolisis Garam 1Dokumen4 halamanKunci Jawaban Latihan Soal Hidrolisis Garam 1alfarisiBelum ada peringkat
- Daftar Asam Basa Kuat LemahDokumen2 halamanDaftar Asam Basa Kuat LemahRichard YaphanathaBelum ada peringkat
- LKMJKJNDokumen9 halamanLKMJKJNUmisabariyahBelum ada peringkat
- ASAM KARBS Dan TurunannyaDokumen52 halamanASAM KARBS Dan TurunannyaTiurma Debora SimatupangBelum ada peringkat
- Asam LemakDokumen2 halamanAsam LemakmusrinsalilaBelum ada peringkat
- Asam& SingkatanDokumen2 halamanAsam& Singkatanlutfi fitrianiBelum ada peringkat
- Daftar Nama Larutan Asam Dan BasaDokumen9 halamanDaftar Nama Larutan Asam Dan BasaPagi Tribute BonJoviBelum ada peringkat
- Daftar ASAM Dan BasaDokumen4 halamanDaftar ASAM Dan BasaIP ManBelum ada peringkat
- 51 - Widi Dwi Kuncoro PLMDokumen4 halaman51 - Widi Dwi Kuncoro PLMtyas.widiastuti09Belum ada peringkat
- GaramDokumen17 halamanGaramsusenaBelum ada peringkat
- Reaksi PenggaramanDokumen15 halamanReaksi PenggaramanFina ARika DJati100% (2)
- Daftar Asam Dan BasaDokumen1 halamanDaftar Asam Dan BasaPridana Ynwa0% (2)
- Asam Basa PrintDokumen2 halamanAsam Basa PrintAnggita SpBelum ada peringkat
- 4 Stoikiometri Larutan 1Dokumen10 halaman4 Stoikiometri Larutan 1hidayaniBelum ada peringkat
- Daftar Nama Larutan Asam Dan BasaDokumen3 halamanDaftar Nama Larutan Asam Dan BasaRudy CaemBelum ada peringkat
- Kimia Senyawa JadiDokumen5 halamanKimia Senyawa JadiHartanti WardaniBelum ada peringkat
- Kimia2 WDokumen2 halamanKimia2 WwendisantanaputraBelum ada peringkat
- Catatan Nama AsamDokumen1 halamanCatatan Nama AsamLouisa Ovelia Renata SetiawanBelum ada peringkat
- Bahan AjarDokumen17 halamanBahan AjarFita Candra SBelum ada peringkat
- Asam BasaDokumen4 halamanAsam BasailhamBelum ada peringkat
- Larutan Asam Dan BasaDokumen14 halamanLarutan Asam Dan BasaPutriBelum ada peringkat
- AsidialkalimetriDokumen69 halamanAsidialkalimetriSultan Guna Wibawa100% (1)
- Modul Kimia Asam Basa 1Dokumen11 halamanModul Kimia Asam Basa 1Rz:))Belum ada peringkat
- Asam Kuat Dan Asam LemahDokumen2 halamanAsam Kuat Dan Asam LemahIsmunandar CuhuyBelum ada peringkat
- Materi Asam BasaDokumen20 halamanMateri Asam BasaKholida HandayaniBelum ada peringkat
- Arifpenky - 76 Nama Senyawa Asam-Basa Beserta Reaksi IonisasinyaDokumen5 halamanArifpenky - 76 Nama Senyawa Asam-Basa Beserta Reaksi IonisasinyaSania HairahBelum ada peringkat
- Asam Organik Beserta Rumus Kimia Dan Struktur KimiaDokumen3 halamanAsam Organik Beserta Rumus Kimia Dan Struktur KimiaAbdulMalikFajarBelum ada peringkat
- Nama Senyawa & Rumus KimiaDokumen6 halamanNama Senyawa & Rumus KimiaNital AndekanBelum ada peringkat
- Senyawa Asam BasaDokumen3 halamanSenyawa Asam BasaAnni RahimaaBelum ada peringkat
- Sap DM PutriDokumen17 halamanSap DM Putrioktiana putriiBelum ada peringkat
- Tugas Individu KJDDokumen15 halamanTugas Individu KJDoktiana putriiBelum ada peringkat
- Tugas Agama Sehrli (Elearning 1)Dokumen5 halamanTugas Agama Sehrli (Elearning 1)oktiana putriiBelum ada peringkat
- Proposal Pengajuan Ukm CinemaDokumen7 halamanProposal Pengajuan Ukm Cinemaoktiana putriiBelum ada peringkat
- Tugas Jurnalis WritingDokumen2 halamanTugas Jurnalis Writingoktiana putriiBelum ada peringkat
- Tugas Jurnalistik RadioDokumen2 halamanTugas Jurnalistik Radiooktiana putriiBelum ada peringkat
- Tugas IndividuDokumen4 halamanTugas Individuoktiana putriiBelum ada peringkat
- Acara Seminar Perfilman Dalam Kegiatan Dies Natalis UnivedDokumen1 halamanAcara Seminar Perfilman Dalam Kegiatan Dies Natalis Univedoktiana putriiBelum ada peringkat
- Jawaban DGPDokumen13 halamanJawaban DGPoktiana putriiBelum ada peringkat
- Jawabn Modul pkk2Dokumen18 halamanJawabn Modul pkk2oktiana putriiBelum ada peringkat
- Jawaban KorosiDokumen3 halamanJawaban Korosioktiana putriiBelum ada peringkat
- Jawaban Modul Pkk-YuliaDokumen19 halamanJawaban Modul Pkk-Yuliaoktiana putriiBelum ada peringkat
- AlamatDokumen1 halamanAlamatoktiana putriiBelum ada peringkat
- Askep Anemia Nanda Noc NicDokumen28 halamanAskep Anemia Nanda Noc NicIyanBelum ada peringkat
- Templete Tugas MetlitDokumen13 halamanTemplete Tugas Metlitoktiana putriiBelum ada peringkat
- Pemeriksaan Ibu Hamil D3Dokumen3 halamanPemeriksaan Ibu Hamil D3oktiana putriiBelum ada peringkat
- BAB 2-DikonversiDokumen23 halamanBAB 2-Dikonversioktiana putriiBelum ada peringkat
- Templete Tugas MetlitDokumen12 halamanTemplete Tugas Metlitoktiana putriiBelum ada peringkat
- Jurnal KDK 2 Ica Proses Keperawatan-2019-10-04t07 - 08 - 35.000ZDokumen7 halamanJurnal KDK 2 Ica Proses Keperawatan-2019-10-04t07 - 08 - 35.000Zoktiana putriiBelum ada peringkat
- Leafleat OkeDokumen2 halamanLeafleat Okeoktiana putriiBelum ada peringkat
- Anggi PengkajianDokumen7 halamanAnggi PengkajianBudi PhuaBelum ada peringkat
- Pemeriksaan LeopoldDokumen2 halamanPemeriksaan LeopoldOktiana PutriiBelum ada peringkat
- Format Pengkajian PrenatalDokumen4 halamanFormat Pengkajian Prenataloktiana putriiBelum ada peringkat
- Plasenta Previa Totalis 1Dokumen3 halamanPlasenta Previa Totalis 1oktiana putriiBelum ada peringkat
- Sop Wash OutDokumen3 halamanSop Wash OutTita Siti NurhalaBelum ada peringkat