Adoc - Pub - Perhatikan Gambar Diagram P T Berikut
Diunggah oleh
Saka AdityaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Adoc - Pub - Perhatikan Gambar Diagram P T Berikut
Diunggah oleh
Saka AdityaHak Cipta:
Format Tersedia
SIFAT KOLIGATIF LARUTAN
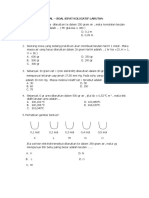
1. Yang bukan merupakan sifat koligatif larutan Perhatikan gambar diagram P-T berikut:
adalah….
A. Penurunan tekanan uap P
B. Penurunan titik beku A D F C
C. Penurunan titik didih
D. Kenaikan titik didih
E. Tekanan osmosis
E
2. Adanya zat terlarut mengakibatkan… B
A. Kenaikan titik beku
B. Penurunan titik beku T
C. Kenaikan tekanan uap jenuh Titik didih larutan ditunjukkan pada huruf…
D. Penurunan titik didih A. A
E. Kenaikan tekanan osmotik B. B
C. C
Perhatikan gambar P-T berikut ! D. D
1atm
E. F
P 3. Diketahui data titik didih beberapa larutan:
Pelarut
Larutan Konsentrasi Titik didih (0C)
Glukosa 0,1 m 100,052
Larutan
Urea 0,2 m 100,104
NaCl 0,1 m 100,104
0
C KOH 0,2 m 100,208
Pernyataan berikut yang tidak sesuai
dengan data pada grafik di atas ialah … Berdasarkan data tersebut pernyataan yang
A. makin tinggi P maka titik didih pelarut tepat yaitu…
makin tinggi A. Semakin besar konsentrasi semakin tinggi
B. makin rendah P maka titik beku pelarut titik didih
makin rendah B. Semakin besar konsentrasi semakin
C. makin rendah P maka titik beku larutan rendah titik didih
makin tinggi C. Titik didih larutan elektrolit = titik didih
D. makin rendah P maka titik didih larutan larutan non elektrolit dengan konsentrasi
makin rendah yang sama
E. makin tinggi P maka titik beku larutan D. Titik didih larutan elektrolit < titik didih
makin rendah larutan non elektrolit dengan konsentrasi
yang sama
E. Titik didih larutan non elektrolit > titik
didih larutan elektrolit dengan konsentrasi
yang sama
SIFAT KOLIGATIF LARUTAN 87
4. Data percobaan penurunan titik beku: 8. Sebanyak 10 gram asam oksalat H2C2O4
(Mr=90) dilarutkan dalam 100 gram air. Jika
Konsentrasi Titik Beku tekanan uap menurun dari 36 cmHg menjadi
Larutan
(molal (oC) 35,75 cmHg, maka derajad ionisasi asam
NaCl 0,1 – 0,372 oksalat adalah….
NaCl 0,2 – 0,744 A. 0,3
CO(NH2)2 0,1 – 0,186 B. 0,5
CO(NH2)2 0,2 – 0,372 C. 0,6
D. 0,75
C6H12O6 0,1 – 0,186
E. 0,8
Berdasarkan data tersebut dapat disimpulkan
bahwa penurunan titik beku tergantung pada 9. Suatu larutan terbentuk dari 9 gram zat non
… elektrolit dan 360 gram air. Tekanan uap
A. jenis zat terlarut jenuh larutan itu adalah 40 mmHg. Jika
B. konsentrasi molal larutan tekanan uap jenuh air pada suhu yang sama
C. jenispelarut adalah 40,1 mmHg, maka Mr zat itu adalah…
D. jenis partikel zat terlarut A. 360
E. jumlah partikel zat terlarut B. 342
C. 180
5. Sebanyak 18 gram glukosa (Mr= 180) D. 126
dilarutkan dalam 72 gram air. Jika tekanan E. 90
uap air murni 20,1 cmHg pada suhu tertentu,
besarnya Penurunan tekanan uap adalah.... 10. Dilarutkan 18 gram C6H12O6 ke dalam 500
A. 0,49 cmHg gram air. Jika Kfair = 1,8, Mr gula = 180,
B. 1,96 cmHg maka titik beku larutan tersebut adalah….0C
C. 4,9 cmHg A. -7,20
D. 9,8 cmHg B. -3,6
E. 19,60 cmHg C. -1,8
6. Tekanan uap jenuh air pada 300C adalah 31,8 D. -0,36
mmHg dan fraksi mol zat Y dalam air adalah E. -0,18
0,056. Pada suhu yang sama tekanan uap
jenuh larutan Y adalah...mmHg 11. Sebanyak 11,7 gram suatu zat elektrolit biner
A. 33,58 dilarutkan dalam 2000 g air mempunyai
B. 30,01 penurunan titik beku 0,372 oC jika Kf air =
C. 28,30 1,86 oC.m-1, maka Mr zat elektrolit biner
D. 17,80 tersebut adalah . . . .
E. 1,78 A. 314,5
B. 117
7. Di dalam air terlarut 10% massa urea (Mr= C. 58,5
60) . Diketahui tekanan uap air pada suhu D. 29,25
300C adalah 0,93 atm. Tekanan uap jenuh E. 11,7
larutan tersebut adalah…atm
A. 0,96 12. Dua gram suatu zat elektrolit biner dilarutkan
B. 0,90 dalam 500 gram air. Ternyata larutan tersebut
C. 0,87 membeku pada suhu -0,3720C, Jika Kf air =
D. 0,45 1,86 maka Mr senyawa tersebut adalah…
E. 0,03 A. 20
B. 30
C. 40
SIFAT KOLIGATIF LARUTAN 88
D. 60 D. 0,87
E. 90 E. 0,98
13. Titik beku larutan 0,1 m NaCl dalam air 18. Bila 3,1 gram glikol (C2H6O2) dilarutkan
adalah -0,360C. diharapkan titik beku larutan dalam 250 gram air dicampur dengan 17,1
kalsium klorida (CaCl2) 0,05 m dalam air gram sukrosa (C12H22O11) dalam 500 gram
adalah…0C air. Bila diketahui Kf air = 1,86o C (Ar : H =
A. -0,18 1, O = 16, C = 12). Titik beku campuran
B. -0,27 larutan adalah …
C. -0,36 A. +0,37C
D. -0,45 B . +0,24C
E. -0,54 C. +0,18C
14. Bila 10 gram dari masing masing zat berikut D. -248oC
ini di larutkan ke dalam 1 Kg air . zat E. -0,37C
manakah yang akan menghasilkan larutan
19. Suatu larutan glukosa dalam air mempunyai
dengan titik beku paling rendah…
penurunan titik beku 0,744oC , bila Kf air =
A. CH3OH
1,86 oC.m-1 dan Kb air = 0,52 oC.m-1 , maka
B. C2H5OH
titik didih larutan glukosa tersebut adalah . . .
C. C6H12O6
A. 100,208 oC
D. C3H8O3
B. 100,104 oC
E. CO(NH2)2
C. 100,052 oC
D. 0,208 oC
15. Di antara kelima macam larutan di bawah ini
E. 0,104 oC
yang membeku paling cepat adalah…
A. K2CO3 0,3M 20. Sebanyak 17,1 gram gula (Mr= 342)
B. Urea 0,8 M dilarutkan dalam 250mL air. Jika Kb= 0,5
C. CaSO4 0,2 M maka titik didih larutan sebesar…..0C
D. CH3COOH 0,2 M A. 100,1
E. Ba(NO3)2 0,3 B. 100,2
C. 100.4
16. Larutan 0,5 molal suatu larutan elektrolit
D. 100,6
biner membeku pada suhu -1,550C. jika Kf
E. 100,8
air = 1,86 0C/molal, maka derajad ionisasi
larutan elektrolit tersebut adalah….
21. Ke dalam 500 gram air dilarutkan 13,35 gram
A. 0,33
senyawa AlCl3. Jika Kb air = 0,52oC/mol,
B. 0,42
harga α = 0,8, kenaikan titik didih larutan
C. 0,66
tersebut adalah … (Ar : Al = 27, Cl = 35,5)
D. 0,83
A. 0,163oC
E. 0,99
B. 0,354 oC
C. 0,496 oC
17. Dalam 250 gram air dilarutkan 1,9 gram
D. 0,659 oC
MgCl2, ternyata larutan membeku pada
0 E. 0,839 oC
-0,372 C. Jika tetapan titik beku molal air =
1,86 C/m, derajad ionisasi garam MgCl2 22. Tiga gram zat X yang dilarutkan dalam 100
adalah … (Ar: Mg = 24, Cl = 35,5) gram bezena menghasilkan kenaikan titik
A. 0,40 didih sebesar 0,540C. bila diketahui kenaikan
B. 0,55
C. 0,75
SIFAT KOLIGATIF LARUTAN 89
titik didih molal benzene = 2,70C, berapakah 27. Larutan glukosa dalam air, mendidih pada
massa molekul relative (Mr) zat X? 100,26o C, Jika Kb = 0,52 dan Kf = 1,86
A. 15 maka larutan tersebut akan membeku pada
B. 30 suhu …
C. 60
D. 120 A. 1,80 oC
E. 150 B. 0,93 oC
C. –0,72o C
23. Ke dalam 500 gram air dilarutkan berturut
turut 12 gram magnesium sulfat (Mr = 120) D. –0,93 oC
dan 6 gram urea (Mr = 60). Jika Kb air = 0,5, E. –1,86 o C
maka larutan hasil campuran akan mendidih
pada suhu… 28. Suatu larutan glukosa dalam air mempunyai
A. 100 0C penurunan titik beku 0,744oC , bila Kf air =
B. 100,2 0C 1,86 oC.m-1 dan Kb air = 0,52 oC.m-1 , maka
C. 100,3 0C titik didih larutan urea tersebut adalah . . . .
D. 100,4 0C A. 100,208 oC
E. 100,5 0C B. 100,104 oC
C. 100,052 oC
24. Diantara larutan berikut yang memiliki titik D. 0,208 oC
didih paling rendah adalah …. E. 0,104 oC
A NaCl 0,01 M
B. CO(NH2)2 0,01 M 29. Sebanyak 11,7 gram suatu zat elektrolit biner
C. H2SO3 0,01 M dilarutkan dalam 2000 g air mempunyai
D. CaCl2 0,01M penurunan titik beku 0,372 oC jika Kf air =
E. AlCl3 0,01M 1,86 oC.m-1, maka Mr zat elektrolit biner
tersebut adalah . . . .
25. Suatu larutan zat non elektrolit dalam air A. 314,5
mendidih pada suhu 100,26°C. Jika Kb air = B. 117
0,52°C/m dan Kf air = l,86°C/m, maka C. 58,5
larutan tersebut akan membeku pada suhu .... D. 29,25
A. –1,86°C E. 11,7
B. –0,93°C
C. –0,52°C 30. Sebanyak 5,8 gram Mg(OH)2 (ArMg=24,
D. –0,260C O=16, H=1) dilarutkan dalam 500 gram air
E. –0,13°C jika Kb air = 0,52 oC.m-1, maka kenaikan titik
didih larutan tersebut adalah….
26. Ke dalam 600 gram air dilarutkan 27 gram A. 100,312oC
senyawa non elektrolit. Larutan tersebut B. 100,104oC
mendidih pada temperatur 100,13 C. Jika C. 0,104oC
diketahui Kb air = 0,520 C/m, maka massa D. 0,312oC
molekul relatif senyawa tersebut adalah … E. 0,52oC
A. 60
B. 90 31. Sebanyak 300 gram senyawa X (non
C. 120 elektrolit) dilarutkan dalam 1 Kg air
D. 180 memberikan perbedaan titik didih dan titik
E. 342 beku sebesar 111,90C. Jika Kb air = 0,52 dan
Kf air = 1,86, maka Mr senyawa X adalah…
SIFAT KOLIGATIF LARUTAN 90
A. 20 D. 96
B. 40 E. 144
C. 58
D. 60 36. Urea sebesar 2,4 gram dilarutkan ke dalam air
E. 98 sampai volume 250 cm3 pada suhu 270C. Mr
urea= 60, R= 0,082. Tekanan osmosis larutan
32. Sekelompok siswa melakukan percobaan tersebut adalah...
dengan data pada tabel berikut: A. 3,936 atm
larutan titik beku larutan 0C B. 4,418 atm
Urea 1 m -1,75 C. 7,872 atm
MgCl2 2 m - 9,22 D. 15,744 atm
Dari data tersebut didapatkan derajat ionisasi E. 39,36 atm
(α ) dari MgCl2 adalah... 37. Sebanyak 6 gram urea (Mr=60) dalam 1 liter
A. 0,74 larutan urea isotonis dengan
B. 0,76 A. 2 M KCl
C. 0,80 B. 1 M KCl
D. 0,82 C. 0,5 M KCl
E. 1.00 D. 0,1 M KCl
E. 0,05 M KCl
33. Jika tekanan osmotik dari 500mL larutan
fruktosa, C6H12O6 pada suhu 32o C sebesar 2 38. Untuk membuat 500 mL larutan glukosa yang
atm, massa fruktosa yang terlarut sebanyak isotonis dengan larutan KCl 0,1 M diperlukan
… glukosa (Mr = 180) sebanyak . . . .
A. 7,2 gram A. 180 gram
B. 9,0 gram B. 36 gram
C. 14,4 gram C. 18 gram
D. 18,0 gram D. 9 gram
E. 45,0 gram E. 4,5 gram
34. Sebanyak 500 ml larutan yang mengandung 39. Dalam konsentrasi yang sama, yang
17,1 gram zat non elektrolit pada suhu 27oC, mempunyai tekanan osmosis paling tinggi
mempunyai tekanan osmotik 2,46 atm. Mr adalah …
zat non elektrolit tersebut adalah … A. C6H12O6
(R = 0,082 L atm mol-1 K-1)
B. BaI2
A. 90
C. Al2(SO4)3
B. 150
C. 207 D. FeO
D. 278 E. KCl
E. 342
35. Suatu zat non elektrolit sebanyak 24 gram
dilarutkan dalam air hingga volumenya 250
mL dan mempunyai tekanan osmotik sebesar
32,8 atmosfer pada suhu 27°C. Jika R = 0,082
L atm/mol K, massa molekul relatif zat
tersebut adalah ...
A. 36
B. 48
C. 72
SIFAT KOLIGATIF LARUTAN 91
Anda mungkin juga menyukai
- LATIHAN SOAL PTS SIFAT KOLIGATIF DAN REDOKS (VOLTA) 2018 RevisiDokumen5 halamanLATIHAN SOAL PTS SIFAT KOLIGATIF DAN REDOKS (VOLTA) 2018 RevisiArisanti MaulidinaBelum ada peringkat
- Latihan Sifat Koligatif LarutanDokumen5 halamanLatihan Sifat Koligatif LarutanRens AlbinBelum ada peringkat
- Soal KoligatifDokumen3 halamanSoal KoligatifDwi Wahyunanti JohanBelum ada peringkat
- Kunci Jawaban Soal Kimia Brutal 2023Dokumen43 halamanKunci Jawaban Soal Kimia Brutal 2023himmm himmmBelum ada peringkat
- Booster KimiaDokumen7 halamanBooster KimiaAlison burgerBelum ada peringkat
- Soal Sifat Koligatif 1Dokumen3 halamanSoal Sifat Koligatif 1CaratbunnyBelum ada peringkat
- 03 Xii Mipa KimDokumen4 halaman03 Xii Mipa Kimesti rohimahBelum ada peringkat
- Soal Latihan Bab 1 - Sifat Koligatif LarutanDokumen3 halamanSoal Latihan Bab 1 - Sifat Koligatif LarutanIndrabenBelum ada peringkat
- SKL Dan ElektrokimiaDokumen2 halamanSKL Dan ElektrokimiaAnisa ArisantiBelum ada peringkat
- Soal Pas Kimia Kelas Xii 2018Dokumen19 halamanSoal Pas Kimia Kelas Xii 2018laila firda rahmawati100% (1)
- Kimia Xii Sem 1Dokumen25 halamanKimia Xii Sem 1Eli SuharlinaBelum ada peringkat
- Sifat Koligatif Larutan Elektrolit (KD 3.2)Dokumen4 halamanSifat Koligatif Larutan Elektrolit (KD 3.2)mirzaaa riskyyy.Belum ada peringkat
- Sifat Koligatiflarutan Elektrolit Dan NonelektrolitDokumen3 halamanSifat Koligatiflarutan Elektrolit Dan NonelektrolitAini Nur NahdiyahBelum ada peringkat
- Koligatif PilganDokumen3 halamanKoligatif PilganNovan AliBelum ada peringkat
- Soal Sifat Koligatif LarutanDokumen2 halamanSoal Sifat Koligatif LarutanGito Sucipto100% (1)
- Soal Sifat Koligatif (PG)Dokumen5 halamanSoal Sifat Koligatif (PG)Ryuo GamingBelum ada peringkat
- Soal Kimia 12Dokumen5 halamanSoal Kimia 12Kha Ha JaBelum ada peringkat
- Soal Latihan Skl-Kimia UnsurDokumen7 halamanSoal Latihan Skl-Kimia UnsurYanah NurjannahBelum ada peringkat
- Uh Sifat Koligatif LarutanDokumen1 halamanUh Sifat Koligatif LarutanSheline Hirfa HirfaBelum ada peringkat
- Remedial Uts Kelas XiiDokumen3 halamanRemedial Uts Kelas XiiMpinBelum ada peringkat
- SOAL - 2A Sifat - Koligatif - Larutan 2016Dokumen3 halamanSOAL - 2A Sifat - Koligatif - Larutan 2016Susy HarahapBelum ada peringkat
- Soal Handbook Mapel Kimia Sci 2019 PDFDokumen200 halamanSoal Handbook Mapel Kimia Sci 2019 PDFSusi Susanti100% (2)
- 12 Soal Persiapan Pas GanjilDokumen9 halaman12 Soal Persiapan Pas Ganjil19 Ni Kadek Dea PurnamiBelum ada peringkat
- Latihan Soal Sifat Koligatif LarutanDokumen3 halamanLatihan Soal Sifat Koligatif LarutanDarren EmilBelum ada peringkat
- Pretest Koligatif 21Dokumen3 halamanPretest Koligatif 21Aris SanwaniBelum ada peringkat
- Soal Semester 5Dokumen13 halamanSoal Semester 5Christin Natalia PBelum ada peringkat
- Soal Sifat Koligatif KimiaDokumen9 halamanSoal Sifat Koligatif KimiaroslainileniBelum ada peringkat
- Dilarutkan 18 Gram Glukosa C6H12O6 Ke Dalam 500 Gram AirDokumen13 halamanDilarutkan 18 Gram Glukosa C6H12O6 Ke Dalam 500 Gram Airb09a100% (1)
- LKPD Diagram PT Dan Perband LarDokumen3 halamanLKPD Diagram PT Dan Perband LarAnonymous fpUdSJOBelum ada peringkat
- Kimia Kelas 12 Ipa Sma LigaDokumen4 halamanKimia Kelas 12 Ipa Sma Ligasoegie_535867100% (2)
- Soal Latihan Pts Kim GasalDokumen3 halamanSoal Latihan Pts Kim GasalRinandaNosaBelum ada peringkat
- Latihan PAS Gasal Kelas XIIDokumen6 halamanLatihan PAS Gasal Kelas XIISuasti Ayu TBelum ada peringkat
- EvaluasiDokumen2 halamanEvaluasitu smalaBelum ada peringkat
- Latihan 2 Pas Kimia Xii 2023Dokumen4 halamanLatihan 2 Pas Kimia Xii 2023sidharta.sigmaBelum ada peringkat
- Koligatif LarutanDokumen2 halamanKoligatif LarutanmirdaprismaBelum ada peringkat
- Koligatif SiapDokumen4 halamanKoligatif SiapZettry SainsBelum ada peringkat
- Soal Kimia Kelas XIIDokumen3 halamanSoal Kimia Kelas XIIDeyaismaBelum ada peringkat
- Modul Kimia Jadi BSCDokumen17 halamanModul Kimia Jadi BSCbsc gondangBelum ada peringkat
- Soal Latihan Ulangan Sifat KoligatifDokumen4 halamanSoal Latihan Ulangan Sifat Koligatifsamuel.purbonegoroBelum ada peringkat
- Uji Kompetensi Kelas 12Dokumen2 halamanUji Kompetensi Kelas 12Dewi KamidaBelum ada peringkat
- Uji Kompetensi Kelas 12Dokumen2 halamanUji Kompetensi Kelas 12Dewi KamidaBelum ada peringkat
- 12 Kim EngDokumen7 halaman12 Kim EngDavid SyaifudinBelum ada peringkat
- Soal Ulangan Harian 1Dokumen15 halamanSoal Ulangan Harian 1DwianggraeniBelum ada peringkat
- Latihan Soal KimiaDokumen6 halamanLatihan Soal KimiaErwin TambaBelum ada peringkat
- Kesetimbangan KimiaDokumen10 halamanKesetimbangan KimiaRahmadani PutriBelum ada peringkat
- Template Soal Kimia Kelas XIIDokumen10 halamanTemplate Soal Kimia Kelas XIIariBelum ada peringkat
- Soal SKL 46Dokumen12 halamanSoal SKL 46195060501111027 RahmaTMBelum ada peringkat
- Soal Kimia Kelas XiiDokumen5 halamanSoal Kimia Kelas XiiZie ChanBelum ada peringkat
- C. Sifat Koligatif Larutan ElektrolitDokumen13 halamanC. Sifat Koligatif Larutan ElektrolitAnindya PuspitaxbBelum ada peringkat
- CHAPTER - 3 Kelas 12Dokumen5 halamanCHAPTER - 3 Kelas 12anggaBelum ada peringkat
- PTS Kelas XIIDokumen8 halamanPTS Kelas XIIahasti aldaBelum ada peringkat
- Soal Kimia - Xii MipaDokumen6 halamanSoal Kimia - Xii MipaDavaBelum ada peringkat
- Soal Latihan Kelas XIIDokumen5 halamanSoal Latihan Kelas XIIMonica Mia hestinaBelum ada peringkat
- Latihan UasDokumen3 halamanLatihan UasKucing GirangBelum ada peringkat
- KimiaDokumen49 halamanKimiaMANGIHUT PANDAPOTAN "PAKPAHAN"Belum ada peringkat
- Tugas Kimia Ke-2Dokumen25 halamanTugas Kimia Ke-2Olivia MargarethaBelum ada peringkat
- Kimia-2 SKL 2Dokumen3 halamanKimia-2 SKL 2Abil DarmaBelum ada peringkat
- KoligatifDokumen7 halamanKoligatifAndy PutraBelum ada peringkat
- Kisi2 Kimia XII UAS Ganjil 2023Dokumen6 halamanKisi2 Kimia XII UAS Ganjil 2023ebenezer.sinaga20Belum ada peringkat
- Jadwal Lomba Porseka Tahun 2022-3Dokumen2 halamanJadwal Lomba Porseka Tahun 2022-3Saka AdityaBelum ada peringkat
- LKPD 8 - KD 4.2 Indikator 4.2.2Dokumen1 halamanLKPD 8 - KD 4.2 Indikator 4.2.2Saka AdityaBelum ada peringkat
- LKPD Data KelompokDokumen2 halamanLKPD Data KelompokSaka AdityaBelum ada peringkat
- Juknas Juknis 2022Dokumen7 halamanJuknas Juknis 2022Saka AdityaBelum ada peringkat
- Fpip Biaya WebDokumen2 halamanFpip Biaya WebSaka AdityaBelum ada peringkat