Fi2208 2022 Uas
Diunggah oleh
Brigita SteffyJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Fi2208 2022 Uas
Diunggah oleh
Brigita SteffyHak Cipta:
Format Tersedia
FI2208 Termodinamika B Dosen: Dr.
Agus Suroso
Semester 2, 2021-2022
UJIAN AKHIR SEMESTER
(20 Mei 2021, pukul 07.00-10.00 WIB)
Kerjakan secara mandiri dan jujur.
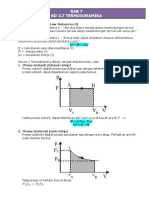
1. Sebuah mesin mengubah kalor menjadi kerja mekanik dengan menerapkan sebuah siklus yang terdiri atas tiga
proses terbalikkan: isobarik, isokhorik, dan adiabatik. Anggap zat kerja mesin tersebut adalah gas ideal.
a. Gambarkan siklus tersebut dalam diagram T-S.
b. Tentukan efisiensi mesin tersebut. Asumsikan mesin bekerja pada rentang temperatur [𝑇1 , 𝑇2 ] dan rentang
entropi [𝑆1 , 𝑆2 ].
2. Tinjau 𝑛 mol gas ideal yang terkurung dalam suatu wadah dengan volume 𝑉 dan temperatur 𝑇. Gas kemudian
mengalami ekspansi hingga volume akhirnya adalah 𝛼𝑉, dengan 𝛼 suatu konstanta, melalui dua cara (lihat
gambar):
(A) gas ditempatkan dalam piston, kemudian dilakukan proses ekspansi isotermal terbalikkan,
(B) gas ditempatkan pada wadah tertutup bervolume 𝛼𝑉 yang disekat. Mula-mula gas menempati ruangan
sebelah kiri dengan volume 𝑉, kemudian sekat dibuka sehingga gas menempati seluruh wadah.
𝑉 (𝛼 − 1)𝑉 𝑉 (𝛼 − 1)𝑉
(A) (B)
Tentukan:
a. perubahan entropi total pada masing-masing cara,
b. kerja yang diperlukan untuk mengembalikan sistem (B) ke keadaan sebelum ekspansi,
𝜕𝑇
c. besaran (𝜕𝑉) untuk ekspansi cara (B).
𝑈
3. Hukum I Termodinamika dapat dituliskan dalam bentuk 𝑑𝐴 = −𝑃𝑑𝑉 − 𝑇𝑑𝑆 dengan 𝐴 adalah fungsi Helmholtz.
a. Tuliskan hubungan Maxwell yang dapat diperoleh dari persamaan di atas.
b. Asumsikan entropi sebagai fungsi temperatur dan tekanan, 𝑆 = 𝑆(𝑇, 𝑃) dan gunakan hubungan Maxwell pada
𝜕𝑉
butir a untuk mendapatkan 𝑇𝑑𝑆 = −𝑇 (𝜕𝑇 ) 𝑑𝑃 + 𝐶𝑃 𝑑𝑇.
𝑃
c. Raksa (𝛽 = 1,81 × 10−4 K-1 dan 𝜅 = 4,01 × 10−11 Pa-1) dengan volume 15 cm3 dan suhu 20 C mengalami
kenaikan tekanan secara isothermal terbalikkan dari 1 atm menjadi 1000 atm. Tentukan kalor yang
masuk/keluar dari raksa dan kerja yang dilakukan oleh/pada raksa.
4. Entropi jenis dari suatu cairan pada tekanan atmosfer dan suhu 100 ◦C adalah 0,31 cal/g.◦C dan entropi uapnya
pada temperatur dan tekanan yang sama adalah 1,76 cal/g.◦C.
a. Tentukan kalor uap zat pada suhu tersebut.
b. Jika entalpi uap zat tersebut adalah 640 cal/g, tentukan entalpi zat cair pada keadaan tersebut.
c. Tentukan fungsi Gibbs dari tiap gram zat tersebut dalam fasa cair dan uap.
Selamat bekerja!
Anda mungkin juga menyukai
- Latihan SoalDokumen2 halamanLatihan SoalolipiaBelum ada peringkat
- Soal2 Termodinamika Untuk SMADokumen8 halamanSoal2 Termodinamika Untuk SMASamuel PolontaloBelum ada peringkat
- Soal2 TermodinamikaDokumen8 halamanSoal2 Termodinamikawahyu widiawatiBelum ada peringkat
- SoalDokumen3 halamanSoalsalmaBelum ada peringkat
- Soal TermoDokumen14 halamanSoal TermoBambang SabirinBelum ada peringkat
- Tugas Rutin IiiDokumen3 halamanTugas Rutin IiiAyulia AnnisaBelum ada peringkat
- FisikaDokumen14 halamanFisikaDara Agusti MaulidyaBelum ada peringkat
- SoalDokumen12 halamanSoalSri RahardjoBelum ada peringkat
- TermodinamikaDokumen21 halamanTermodinamikayehuda pramanaBelum ada peringkat
- Soal PTS Genap 2022 Fisika Paket ADokumen5 halamanSoal PTS Genap 2022 Fisika Paket AOctaVhyan RondonuwuBelum ada peringkat
- TermoDokumen29 halamanTermoAsra FebriadiBelum ada peringkat
- Tugas Rutin IiDokumen3 halamanTugas Rutin IiZahratul HasanahBelum ada peringkat
- Kisi-Kisi UAS Termodinamika Dasar - Des 2019 PDFDokumen3 halamanKisi-Kisi UAS Termodinamika Dasar - Des 2019 PDFAhmadJuliantoBelum ada peringkat
- ThermoDokumen18 halamanThermosavio Ximenes100% (1)
- Soal Esay FisikaDokumen3 halamanSoal Esay Fisikasefayi3279Belum ada peringkat
- Soal Latihan FisikaDokumen6 halamanSoal Latihan FisikaPutri Rani LestariBelum ada peringkat
- Tugasvii Fisikalanjut PDFDokumen1 halamanTugasvii Fisikalanjut PDFFajar PriyonoBelum ada peringkat
- 02 Latihan 1 - Teori Kinetik GasDokumen3 halaman02 Latihan 1 - Teori Kinetik GasJulham EfendiBelum ada peringkat
- Soal PTS Fisika XI Sem 2....Dokumen9 halamanSoal PTS Fisika XI Sem 2....aditya wahyuBelum ada peringkat
- T Kinetik & TermoDokumen22 halamanT Kinetik & TermodianBelum ada peringkat
- TermodinamikaDokumen3 halamanTermodinamikaKharis LiftyawanBelum ada peringkat
- Analisis Kadar AirDokumen55 halamanAnalisis Kadar AirTabitaKristina100% (2)
- BAB 9. TermodinamikaDokumen18 halamanBAB 9. TermodinamikaHerdimanBelum ada peringkat
- Tugas-1 TermodinamikaDokumen3 halamanTugas-1 TermodinamikaAnonymous iXl3xkBelum ada peringkat
- TermodinamikaDokumen17 halamanTermodinamikaNur SollikhahBelum ada peringkat
- Tugas Termodinamika RahmadiDokumen6 halamanTugas Termodinamika RahmadiagusBelum ada peringkat
- BAB07Dokumen24 halamanBAB07Marsha ChrissieBelum ada peringkat
- TermodinamikaDokumen17 halamanTermodinamikaAuliyaa Zahra SupriyatnaBelum ada peringkat
- BAB 7 TermodinamikaDokumen6 halamanBAB 7 TermodinamikaddewBelum ada peringkat
- BAB07Dokumen24 halamanBAB07ridhoprogsBelum ada peringkat
- TermodinamikaDokumen40 halamanTermodinamikaFia CubyBelum ada peringkat
- Hukum TermodinamikaDokumen8 halamanHukum TermodinamikaDavid steven TangkealloBelum ada peringkat
- TermodinamikaDokumen15 halamanTermodinamikaSyah AmilBelum ada peringkat
- Soal Teori Kinetik Gas Dan TermoDokumen2 halamanSoal Teori Kinetik Gas Dan TermoFirqieBelum ada peringkat
- (22-24) Laporan Praktikum TermodinamikaDokumen13 halaman(22-24) Laporan Praktikum TermodinamikawindamargarethaBelum ada peringkat
- Modul 9 Fidas IA - 2022 2023Dokumen6 halamanModul 9 Fidas IA - 2022 2023Nada G KhalisaBelum ada peringkat
- Tugas FINAL Termodinamika (Kisi-Kisi)Dokumen2 halamanTugas FINAL Termodinamika (Kisi-Kisi)Edysul IsdarBelum ada peringkat
- Bab 7 Marthen KanginanDokumen15 halamanBab 7 Marthen KanginanDedi WahyudinBelum ada peringkat
- PTS II Fisika XIDokumen5 halamanPTS II Fisika XIimam SutrisnoBelum ada peringkat
- Suhu Tinggi Reservoir Mesin Carnot 5 K Dan Efisiensinya 60Dokumen9 halamanSuhu Tinggi Reservoir Mesin Carnot 5 K Dan Efisiensinya 60Andy MarshaidBelum ada peringkat
- TermodinamikaDokumen3 halamanTermodinamikaAminullah HusnainiBelum ada peringkat
- Kuis Kimia IIDokumen1 halamanKuis Kimia IIYudha Agil Prasetya Effendi0% (1)
- 1 TermodinamikaDokumen16 halaman1 TermodinamikanugrahaaryaBelum ada peringkat
- Soal Kinetik Gas Dan Termodinamika KLS Xi, GenapDokumen8 halamanSoal Kinetik Gas Dan Termodinamika KLS Xi, GenapGregorius AraBelum ada peringkat
- Soal FormatifDokumen6 halamanSoal FormatifKasmi YantiBelum ada peringkat
- UAS TermodinamikaDokumen1 halamanUAS TermodinamikaFarchan Abdul KhafizBelum ada peringkat
- TERMODINAMIKADokumen8 halamanTERMODINAMIKA35. тαтα ιναηкαBelum ada peringkat
- Kelompok 3 - Analisis Exergy Siklus UapDokumen11 halamanKelompok 3 - Analisis Exergy Siklus UapKoko motohdBelum ada peringkat
- Oke 3Dokumen7 halamanOke 3asepblBelum ada peringkat
- Fisika: TermodinamikaDokumen43 halamanFisika: TermodinamikaNugroho PriatmojoBelum ada peringkat
- Tentang Diri - PowerPointDokumen22 halamanTentang Diri - PowerPointBrigita SteffyBelum ada peringkat
- Brigita Steffy - Makalah Manpes - No Space CoverDokumen22 halamanBrigita Steffy - Makalah Manpes - No Space CoverBrigita SteffyBelum ada peringkat
- OSBIO - 1 - 12921061 - Brigita SteffyDokumen21 halamanOSBIO - 1 - 12921061 - Brigita SteffyBrigita SteffyBelum ada peringkat
- Brigita Steffy - Makalah Manpes - No Space CoverDokumen22 halamanBrigita Steffy - Makalah Manpes - No Space CoverBrigita SteffyBelum ada peringkat
- Minggu 1, Agustus 2021 Toxic Social MediaDokumen22 halamanMinggu 1, Agustus 2021 Toxic Social MediaBrigita SteffyBelum ada peringkat
- Brigita Steffy M - Refleksi Karakter PDFDokumen2 halamanBrigita Steffy M - Refleksi Karakter PDFBrigita SteffyBelum ada peringkat
- Kegiatan JC Bulan AgustusDokumen1 halamanKegiatan JC Bulan AgustusBrigita SteffyBelum ada peringkat
- Contoh Puisi Tema IbuDokumen1 halamanContoh Puisi Tema IbuBrigita SteffyBelum ada peringkat
- Soal PAS Matematika Wajib Kelas XI Tahun 2018 2019Dokumen6 halamanSoal PAS Matematika Wajib Kelas XI Tahun 2018 2019Dianing WulanBelum ada peringkat