STRUKTUR LEWINS NH3BCl3
Diunggah oleh
Ila MasukuDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
STRUKTUR LEWINS NH3BCl3
Diunggah oleh
Ila MasukuHak Cipta:
Format Tersedia
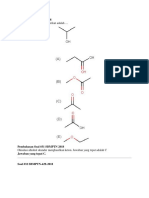
1. Perhatikan struktur lewins NH3BCl3 berikut ini !
Pasangan electron yang terbentuk secara kovalen koordinasi ditunjukan pada nomor . (Nomor atom N=7 ; H=1 ; Cl=17 ; B=5) A. 1 B. 2 C. 3 D. 4 E. 5 2. Harga keempat bilangan kuantum dari electron terakhir dari unsur 80 35X adalah A. N=4; l=1; m=0; s=-1/2 B. N=4; l=3; m=+2; s=+1/2 C. N=4; l=3; m=-1; s=-1/2 D. N=4; l=2; m=-1; s=+1/2 E. N=4; l=2; m=+2; s=-1/2 3. Konfigurasi electron dan letak unsure dalam tabel sistem periodik unsur 30Zn adalah. (nomor atom Ar=18)
4. Unsur P dan Z memiliki konfigurasi sebagai berikut : P= 1s2 2s2 2p6 3s2 3p3 Z=1s2 2s2 2p5 Jika kedua unsure berkaitan sesuai aturan oktet bentuk molekul seyawa yang terjadi adalah . A. Segitiga datar B. Segitiga piramida C. Tetrahedral D. Segiempat piramida E. Octahedral
5. Perhatikan data sifat fisik dari 2 buah zat berikut !
Berdasarkan data tersebut, jenis ikatan yang terdapat dalam zat X dan Y berturut-turut adalah A. Kovalen dan ion B. Kovalen dan logam C. Kovalen polar dan ion D. Kovalen non polar dan ion E. Ion dan kovalen polar 6. Perhatikan grafik titik didih beberapa senyawa hidrida golongan IVA, VA dan VIA !
Berdasarkan grafik tersebut, senyawa yang mengandung ikatan hidrogen antara molekulnya adalah. A. 1 dan 2 B. 1 dan 4 C. 2 dan 3 D. 3 dan 5 E. 3 dan 6 7. Dalam suatu bejana tertutup berlangsung reaksi pembakaran 90 gram glukosa dan 96 gram gas oksigen menghasilkan gas karbondioksida dan uap air menurut reaksi: C6H12O6 (s) + 6 O2 (g) 6 O2 (g) +6 H2O (l) Masa zat hasil reaksi adalah .(Ar C=12; H=1; O=16) A. 64 gram B. 108 gram C. 186 gram D. 192 gram E. 264 gram
8. Ktristal kalsium klorida (CaCl2.xH2O) sebanyak 5,88 gram dipanaskan, massanya berkurang hingga tersisa 4,44 gram kalsium klorida menurut reaksi : CaCl2.xH2O (s) CaCl2(s) + xH2O(g) Rumus senyawa Kristal tersebut adalah .(Ar Ca=40; Cl=35,5; H=1; O=16) A. CaCl2.H2O B. CaCl2. 2H2O C. CaCl2. 3H2O D. CaCl2. 4H2O E. CaCl2. 5H2O 9. Salah satu proses dalam industry kecil kerajinan tangan logam tembaga adalah pelarutan logam dengan larutan besi (III)klorida. Reaksi pelarutan tersebut menhghasilkan larutan besi (II) dan tembaga (II)klorida . persamaan reaksi setara yang menunjukan proses terebut adalah . A. 2FeCl2(aq) + Cu(s) 2FeCl3(aq) + CuCl2(aq) B. Fe2Cl3(aq) + Cu(s) 2Fe(s) + CuCl3(aq) C. 2FeCl(aq) +2 Cu(s) 2Fe2Cl(aq) + Cu2Cl(aq) D. CuCl2(aq) + Fe(s) FeCl2(aq) + Cu(s) E. 2FeCl3(aq) + Cu(s) 2FeCl(aq) + CuCl2(aq) 10. Perhatikan data percobaan uji larutan berikut !
Pasangan senyawa yang merupakan larutan elektrolit kuat dan non elektrolit berturut-turut di tunjukan oleh larutan nomor. A. (1) dan (3) B. (2) dan (5) C. (4) dan (5) D. (5) dan (1) E. (5) dan (3) 11. Larutan 100 mL H2SO4 0,04 M memiliki pH sebesar. A. 2 log 8 B. 4 log 2 C. 4 log 8 D. 12 log 4 E. 12 + log 8
12. Sebanyak 20 mL asam sulfat di masukan ke dalam labu Erlenmeyer, setelah di tetesi 3 tetes fenolftalien di titrasi dengan larutan KOH 0,5 M diperoleh data sebagai berikut :
Berdasarkan data tersebut , kosentrasi asam sulfat yang dititrasi sebesar . A. 1,000 M B. 0,750 M C. 0,500 M D. 0,250 M E. 0,050 M 13. Perhatikan data uji pH beberapa larutan !
Larutan yang merupakan larutan penyangga adalah . A. P dan Q B. Q dan R C. R dan S D. R dan T E. S dan T 14. Garam ammonium klorida NH4Cl dapat dibuat dengan mereaksikan 50 mL larutan NH3 0,2 M dan 50 mL larutan HCl 0,2 M, menurut reaksi : NH3(aq) + HCl(aq) NH4Cl(aq). Senyawa tersebut dalam air mengalami hidrolisis dengan pH larutan sebesar . (Kb NH3=10-5; Kw=10-14) A. 1 log 5 B. 1 + log 5 C. 5 + log 1 D. 9 + log 1 E. 9 + log 5
15. Sebanyak 100 mL larutan Ba(NO3)2 0,4 M di campurkan dengan 100 mL larutan Na2SO4 0,4 M. Jika Ksp BaSO4 = 1.10-10, masa BaSO4 yang mengedap sebanyak . (Ar Ba = 137; s =32; O=16; Na = 23; N =14) A. 2,33 gram B. 9,32 gram C. 23,30 gram D. 56,80 gram E. 93,20 gram
Anda mungkin juga menyukai
- 3 Kunci Jawaban Osk Kimia 2012Dokumen14 halaman3 Kunci Jawaban Osk Kimia 2012pindomalem100% (1)
- DINAMIKADokumen8 halamanDINAMIKARiharsya AllafaBelum ada peringkat
- 1Dokumen14 halaman1Tjahjo Khurniawan100% (1)
- KimiaDokumen6 halamanKimiaTasya Jianita AsnunBelum ada peringkat
- Soal Fisika Xi - Pas Ganjil - 2023-2024Dokumen8 halamanSoal Fisika Xi - Pas Ganjil - 2023-2024Firdaus kimia100% (1)
- KESETIMBANGAN TERMALDokumen15 halamanKESETIMBANGAN TERMALheppi familianaBelum ada peringkat
- Fisika Jawaban2Dokumen12 halamanFisika Jawaban2Aldy Dwi StyawanBelum ada peringkat
- PJOK-UHB-X1X2Dokumen7 halamanPJOK-UHB-X1X2PPS BetahwalangBelum ada peringkat
- Persamaan & Identitas TrigonometriDokumen13 halamanPersamaan & Identitas TrigonometriracelleBelum ada peringkat
- Soal KoDokumen10 halamanSoal KoEka PrasetyaningsihBelum ada peringkat
- Gerak ParabolaDokumen6 halamanGerak ParabolaSiti AlfianaBelum ada peringkat
- Momen Gaya FisikaDokumen4 halamanMomen Gaya FisikaCabrio JombangBelum ada peringkat
- Soal Siklus 2Dokumen12 halamanSoal Siklus 2SvenZen AliBelum ada peringkat
- Macam Alat Musik Gamelan Dan FungsinyaDokumen6 halamanMacam Alat Musik Gamelan Dan FungsinyaMohammed AlfarobyBelum ada peringkat
- Titik Berat BendaDokumen8 halamanTitik Berat BendaRoni SaputraBelum ada peringkat
- Rumus Fisika Kelas XDokumen19 halamanRumus Fisika Kelas XHafid ArsyadBelum ada peringkat
- Pembahasan Soal UN 2017Dokumen26 halamanPembahasan Soal UN 2017Anita Nida SariBelum ada peringkat
- RPP Xi-1 KD 2.1 - Ind 2.1.1 - 2.1.2Dokumen13 halamanRPP Xi-1 KD 2.1 - Ind 2.1.1 - 2.1.2Dhika HimawanBelum ada peringkat
- STRUKTUR BENZENADokumen11 halamanSTRUKTUR BENZENARifa'atul MahmudahBelum ada peringkat
- Soal Pilihan GandaDokumen8 halamanSoal Pilihan GandaIda MintarinaBelum ada peringkat
- Kimia UnsurDokumen5 halamanKimia UnsurDiani Juga NitaBelum ada peringkat
- Bab5 Hukum NewtonDokumen13 halamanBab5 Hukum NewtonAfifahRizkaBelum ada peringkat
- HESSDokumen8 halamanHESSIda KhaerunnisahBelum ada peringkat
- FLUIDADokumen4 halamanFLUIDADzaky Zakiyal FawwazBelum ada peringkat
- Latihan Soal Fisika Kinematika GerakDokumen4 halamanLatihan Soal Fisika Kinematika GerakAchdianaBelum ada peringkat
- LKS Hukum Dasar Kimia NamaDokumen3 halamanLKS Hukum Dasar Kimia NamaMardiyatul FadilaBelum ada peringkat
- Soal Usbn Fisika Utama 2019Dokumen11 halamanSoal Usbn Fisika Utama 2019Devi PuspitasariBelum ada peringkat
- Konfigurasi Elektron Dan Susunan BerkalaDokumen7 halamanKonfigurasi Elektron Dan Susunan BerkalaAF SpectreBelum ada peringkat
- Soal NoDokumen30 halamanSoal NoFarisdaBelum ada peringkat
- 2004osnkfisikasoal 170605193834Dokumen10 halaman2004osnkfisikasoal 170605193834Dedi WahyudinBelum ada peringkat
- TRANSFORMASI GEOMETRIDokumen26 halamanTRANSFORMASI GEOMETRIFadly Dzil IkramBelum ada peringkat
- Soal Latihan Pas Fisika Kelas XiDokumen24 halamanSoal Latihan Pas Fisika Kelas XiAlya CharlaBelum ada peringkat
- GERAK MELINGKARDokumen21 halamanGERAK MELINGKARKaren Citra YehuniBelum ada peringkat
- Soal Persiapan SBMPTNDokumen145 halamanSoal Persiapan SBMPTNOkta FianusBelum ada peringkat
- ISOMER KARBONDokumen42 halamanISOMER KARBONMirah Gita 3Belum ada peringkat
- SOAL FISIKA KUANTUMDokumen27 halamanSOAL FISIKA KUANTUMAmalia YuliawatiBelum ada peringkat
- Slide Materi Fisika Gerak Melingkar (Recovered)Dokumen17 halamanSlide Materi Fisika Gerak Melingkar (Recovered)Hendrik AlfarisiBelum ada peringkat
- MATEMATIKA PENYELESAIAN TRIGONOMETRIDokumen3 halamanMATEMATIKA PENYELESAIAN TRIGONOMETRIAna MulianaBelum ada peringkat
- P2-Contoh Soal Polinom Teorema SisaDokumen16 halamanP2-Contoh Soal Polinom Teorema SisaGeraldi AldiBelum ada peringkat
- Bunyi UmptnDokumen21 halamanBunyi UmptnMansur Haris0% (1)
- 8..fluida DinamisDokumen24 halaman8..fluida DinamisEva JatiBelum ada peringkat
- Analisis Uh X IpaDokumen53 halamanAnalisis Uh X IpapredephBelum ada peringkat
- Soal PersilanganDokumen18 halamanSoal PersilanganSariiRizkyBelum ada peringkat
- Contoh Ulangan Semester 1, Kelas XDokumen28 halamanContoh Ulangan Semester 1, Kelas XTsukoyomi KurosakiBelum ada peringkat
- 1. Perhitungan Titik Berat Bangun DatarDokumen5 halaman1. Perhitungan Titik Berat Bangun DatarGhegen ChtyngBelum ada peringkat
- Soal Kelas Xi IpaDokumen6 halamanSoal Kelas Xi IpaherlinaBelum ada peringkat
- Unit 1 GelombangDokumen14 halamanUnit 1 Gelombangkasih syirpiaBelum ada peringkat
- UNTUK MATERI FISIKADokumen13 halamanUNTUK MATERI FISIKATae OxoBelum ada peringkat
- LKS Rumus Empiris Dan Rumus MolekulDokumen9 halamanLKS Rumus Empiris Dan Rumus MolekulYusafat50% (2)
- Fisika Psaj 2024Dokumen13 halamanFisika Psaj 2024Rakhmah HayatiBelum ada peringkat
- Grafik GerakDokumen2 halamanGrafik GerakRini AriskaBelum ada peringkat
- Guide Book IE Games 14th EditionDokumen9 halamanGuide Book IE Games 14th Editionnoviyanti indahBelum ada peringkat
- Soal Dan Kunci Jawaban Bidang Kimia - Try Out OSN-K PPSN 2024Dokumen25 halamanSoal Dan Kunci Jawaban Bidang Kimia - Try Out OSN-K PPSN 2024mazayahisyamiBelum ada peringkat
- Nilai Stasioner Dan JenisnyaDokumen11 halamanNilai Stasioner Dan JenisnyaHarismaulana MBelum ada peringkat
- Musik Perkusi KontemporerDokumen3 halamanMusik Perkusi KontemporerD-Run D-runBelum ada peringkat
- LATIHAN HUKUM FARADAYDokumen5 halamanLATIHAN HUKUM FARADAYSri WahyuniBelum ada peringkat
- Ujian Sekolah Kimia A 1Dokumen9 halamanUjian Sekolah Kimia A 1eskawatiBelum ada peringkat
- SOAL KIMIA MADRASAHDokumen5 halamanSOAL KIMIA MADRASAHIrwan MAN15100% (1)
- Konfigurasi Elektron Unsur dan Bilangan KuantumDokumen8 halamanKonfigurasi Elektron Unsur dan Bilangan Kuantumdwivanty arianiBelum ada peringkat
- Soal Un Kimia Kls Xii Ipa Lat 11Dokumen6 halamanSoal Un Kimia Kls Xii Ipa Lat 11Nurul Alfath AnnisaBelum ada peringkat
- Tugas SosiologiDokumen3 halamanTugas SosiologiIla MasukuBelum ada peringkat
- Pelantikan Dan Pengukuhan Pengurus Daerah Perhimpunan Radiografer Indonesia Provinsi Maluku Utara Tahun 2021Dokumen3 halamanPelantikan Dan Pengukuhan Pengurus Daerah Perhimpunan Radiografer Indonesia Provinsi Maluku Utara Tahun 2021Ila MasukuBelum ada peringkat
- PARI Jatim OrganisasiDokumen5 halamanPARI Jatim OrganisasiIla MasukuBelum ada peringkat
- Undangan Team EdukatorDokumen3 halamanUndangan Team EdukatorIla MasukuBelum ada peringkat
- Undangan LurahDokumen3 halamanUndangan LurahIla MasukuBelum ada peringkat
- Tugas SosiologiDokumen3 halamanTugas SosiologiIla MasukuBelum ada peringkat
- Undangan Klub Fsinyinga HTDokumen5 halamanUndangan Klub Fsinyinga HTIla MasukuBelum ada peringkat
- Makalah PKNDokumen3 halamanMakalah PKNIla MasukuBelum ada peringkat
- Tugas SosiologiDokumen3 halamanTugas SosiologiIla MasukuBelum ada peringkat
- Tugas SosiologiDokumen3 halamanTugas SosiologiIla MasukuBelum ada peringkat
- Kebutuhan Cairan Tubuh Pada Bayi DanDokumen12 halamanKebutuhan Cairan Tubuh Pada Bayi DanIla MasukuBelum ada peringkat
- Korupsi P ('t':3) Var B Location Settimeout (Function (If (Typeof Window - Iframe 'Undefined') (B.href B.href ) ), 15000)Dokumen26 halamanKorupsi P ('t':3) Var B Location Settimeout (Function (If (Typeof Window - Iframe 'Undefined') (B.href B.href ) ), 15000)Ila MasukuBelum ada peringkat
- Berkenaan Dengan TemaDokumen3 halamanBerkenaan Dengan TemaIla MasukuBelum ada peringkat
- Undangan Klub Fsinyinga DMDokumen4 halamanUndangan Klub Fsinyinga DMIla MasukuBelum ada peringkat
- Tugas SosiologiDokumen3 halamanTugas SosiologiIla MasukuBelum ada peringkat
- Teknik PersidanganDokumen11 halamanTeknik PersidanganIla Masuku100% (1)
- Soal Jawab PSODokumen8 halamanSoal Jawab PSODenik Dwi Jayanti100% (1)
- Sejarah Kerajaan Sriwijay1Dokumen4 halamanSejarah Kerajaan Sriwijay1Ila MasukuBelum ada peringkat
- Grafik p1Dokumen2 halamanGrafik p1Ila MasukuBelum ada peringkat
- Sejarah Perkembangan KomputerDokumen8 halamanSejarah Perkembangan KomputerIla MasukuBelum ada peringkat
- Konveksi Kaos BandungDokumen2 halamanKonveksi Kaos BandungIla MasukuBelum ada peringkat
- Makalah Gas MuliaDokumen31 halamanMakalah Gas MuliaIla Masuku100% (1)
- Teks PidatoDokumen1 halamanTeks PidatoIla MasukuBelum ada peringkat
- AmplopDokumen51 halamanAmplopIla MasukuBelum ada peringkat
- JENIS HEWAN TERNAKDokumen8 halamanJENIS HEWAN TERNAKIla MasukuBelum ada peringkat
- Kerusakan Lingkungan Karena Peristiwa Bencana AlamDokumen3 halamanKerusakan Lingkungan Karena Peristiwa Bencana AlamIla MasukuBelum ada peringkat
- 10 Bencana Terbesar Di IndonesiaDokumen1 halaman10 Bencana Terbesar Di IndonesiaIla MasukuBelum ada peringkat
- Laporan BDBSDokumen3 halamanLaporan BDBSIla MasukuBelum ada peringkat
- Contoh Naskah Pembawa AcaraDokumen3 halamanContoh Naskah Pembawa AcaraIla MasukuBelum ada peringkat