Titrasi Asam Basa
Titrasi Asam Basa
Diunggah oleh
Linda Magfirah0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
21 tayangan5 halamanJudul Asli
TITRASI ASAM BASA
Hak Cipta
© © All Rights Reserved
Format Tersedia
PPTX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
21 tayangan5 halamanTitrasi Asam Basa
Titrasi Asam Basa
Diunggah oleh
Linda MagfirahHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 5
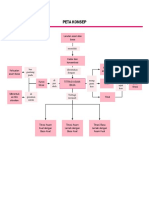
TITRASI ASAM BASA
Yang akan dipelajari pada materi ini:
1. Pengertian Titrasi
2. Membuat Larutan
3. Merancang Titrasi Asam Basa
4. Perhitungan Titrasi Asam Basa
5. Kurva Titrasi
TITRASI ASAM BASA
• Titrasi suatu metode kimia analisa yang
digunakan untuk menentukan kadar atau
konsentrasi suatu larutan.
• Dalam titrasi, larutan yang volumenya terukur
direaksikan secara bertahap dengan larutan
lain yang telah diketahui kadarnya atau
disebut juga dengan larutan standar.
• Proses terjadinya titrasi asam basa, terdapat
keterlibatan reaksi neutralisasi, yaitu reaksi
yang terjadi ketika larutan asam dan basa
berada dalam jumlah konsentrasi yang
ekuivalen.
• Zat dititrasi (titran) adalah larutan yang
ditempatkan di Erlenmeyer dan tidak
diketahui jumlah konsentrasinya.
• Zat peniter (titrat) adalah larutan baku yang
sudah diketahui jumlah konsentrasinya dan
dimasukkan ke dalam buret.
1. Prinsip Titrasi Asam Basa
• Titrasi asam basa melibatkan dua jenis larutan,
yaitu larutan basa dan larutan asam yang
dapat menempati dua peran, baik sebagai zat
dititrasi (titra) ataupun zat peniter (titrat).
• Untuk memaksimalkan proses titrasi asam
basa, maka ketika proses pemberian titran ke
dalam larutan titrat harus memiliki sebuah
indikator pengukuran. Hal tersebut bertujuan
untuk mendapatkan jumlah pemberian yang
cukup, sehingga dapat mencapai konsentrasi
dari larutan asam-basa yang ekivalen.
• Indikator yang digunakan dapat menggunakan
zat kimia dan terbuat dari asam atau basa
organik lemah. Zat tersebut nantinya akan
memberikan warna yang berubah bila
terdapat pemberian zat titran yang berlebihan
saat proses titrasi.
• Titik ekivalen dalam proses titrasi terjadi
ketika jumlah mol asam sama dengan jumlah
mol basa, atau tepat habis bereaksi.
• Titik akhir titrasi yaitu titik saat indikator asam
basa mengalami perubahan warna.
Anda mungkin juga menyukai
- UEU Kimia Analisis 3Dokumen12 halamanUEU Kimia Analisis 3Siti JuhanaBelum ada peringkat
- LP Kimia Titrasi Asam BasaDokumen11 halamanLP Kimia Titrasi Asam BasaRiskaBelum ada peringkat
- Laporan KImiaDokumen22 halamanLaporan KImiaAl MaBelum ada peringkat
- Volumetri Kel 2Dokumen24 halamanVolumetri Kel 2mayaBelum ada peringkat
- TitrasiDokumen2 halamanTitrasiAyu TBelum ada peringkat
- Definisi, Jenis Dan Prinsip TitrasiDokumen10 halamanDefinisi, Jenis Dan Prinsip TitrasiRizkaTaswiyatulAiniBelum ada peringkat
- Bahan Ajar TitrasiDokumen16 halamanBahan Ajar TitrasiafriliawsBelum ada peringkat
- Makalah Titrasi Asam Basa Kelompok 1Dokumen21 halamanMakalah Titrasi Asam Basa Kelompok 1Aisyah Agustina100% (1)
- 25Dokumen2 halaman25aretha aleeyaBelum ada peringkat
- Titrasi Tugas Kimia Dasar RemedialDokumen7 halamanTitrasi Tugas Kimia Dasar RemedialUzha Hilman HanafiBelum ada peringkat
- TitrasiDokumen6 halamanTitrasiRezky FadhilBelum ada peringkat
- Buku Kuning AlkalimetriDokumen6 halamanBuku Kuning AlkalimetrianitacahyaBelum ada peringkat
- TitrasiDokumen12 halamanTitrasiCut putri MuliandaBelum ada peringkat
- Titrasi KimiaDokumen5 halamanTitrasi KimiadeekayBelum ada peringkat
- Laporan Praktikum Asidi Alkalimetri 1Dokumen24 halamanLaporan Praktikum Asidi Alkalimetri 1Zuhrotul Fikri Ilma40% (5)
- Titrasi Asam Basa VolumetriDokumen11 halamanTitrasi Asam Basa VolumetriEdri KingryoBelum ada peringkat
- Titrasi Asam BasaDokumen8 halamanTitrasi Asam BasaAzrii AprisoniasaritaBelum ada peringkat
- VolumetriDokumen16 halamanVolumetriBrandon MarshallBelum ada peringkat
- Titrasi Asam Basa LisaDokumen15 halamanTitrasi Asam Basa LisanurhalisaBelum ada peringkat
- Laporan Kimia Titrasi Asam BasaDokumen10 halamanLaporan Kimia Titrasi Asam BasaFajar RamdanBelum ada peringkat
- Kegiaan Pembelajaran Titrasi Asam Basa - Imam-DikonversiDokumen8 halamanKegiaan Pembelajaran Titrasi Asam Basa - Imam-DikonversiIMAM FIRDAUSBelum ada peringkat
- Asidi Alkalimetri2014Dokumen36 halamanAsidi Alkalimetri2014Pocut NurulAlamBelum ada peringkat
- Pembahasan TitrasiDokumen12 halamanPembahasan TitrasialfikiakimtaBelum ada peringkat
- TitrasiDokumen2 halamanTitrasiRyo VolveBelum ada peringkat
- Materi TITRASI ASAM BASA PRESENTASIDokumen15 halamanMateri TITRASI ASAM BASA PRESENTASIyeny yulizahBelum ada peringkat
- Praktikum Titrasi Asam Basa Dan Contoh Bentuk LaporannyaDokumen1 halamanPraktikum Titrasi Asam Basa Dan Contoh Bentuk LaporannyaYoulan Theresia SugiartoBelum ada peringkat
- Jurnal VolumetriDokumen14 halamanJurnal Volumetribela67% (6)
- Gina Aprilia Xi Mipa 1 Titrasi Asam BasaDokumen7 halamanGina Aprilia Xi Mipa 1 Titrasi Asam BasaRiska AmaliaBelum ada peringkat
- Titrasi Asam BasaDokumen2 halamanTitrasi Asam BasaDilaFaradianBelum ada peringkat
- Aku - Titrasi Asam BasaDokumen40 halamanAku - Titrasi Asam BasaUtari Ika CahyaniBelum ada peringkat
- Titrasi Kelompok 20Dokumen10 halamanTitrasi Kelompok 20Sherina CarmeliaBelum ada peringkat
- Titrasi Alkali Dan AsidiDokumen18 halamanTitrasi Alkali Dan AsidiAbdul Aziz SetiawanBelum ada peringkat
- Tugas Kimsis - Eka Saputri-G70119105-BDokumen5 halamanTugas Kimsis - Eka Saputri-G70119105-BEkha SaputriBelum ada peringkat
- Asidi AlkalimetriDokumen6 halamanAsidi AlkalimetriAnisah SahrulBelum ada peringkat
- Kad 1Dokumen17 halamanKad 1Anonymous xh1gDv3PA9Belum ada peringkat
- Titrasi Asam BasaDokumen3 halamanTitrasi Asam BasaAsrianiBelum ada peringkat
- Lapres Pupuk ZADokumen25 halamanLapres Pupuk ZAMan ZilaBelum ada peringkat
- DDKA Titrasi Asam BasaDokumen12 halamanDDKA Titrasi Asam BasaKirani puspita sariBelum ada peringkat
- Makalah Titrimetri 1Dokumen18 halamanMakalah Titrimetri 1Anonymous kZFrCaBelum ada peringkat
- BAB I KebawahDokumen9 halamanBAB I KebawahShella DearisaBelum ada peringkat
- Laporan Kimia Titrasi BenarDokumen12 halamanLaporan Kimia Titrasi BenarAbdul LatifBelum ada peringkat
- Asidi AlkalimetriDokumen8 halamanAsidi Alkalimetrisri yunitaBelum ada peringkat
- Kesimpulan Dan Saran Laporan Titrasi Asam Dan BasaDokumen1 halamanKesimpulan Dan Saran Laporan Titrasi Asam Dan Basaaretha aleeya100% (1)
- VolumetriDokumen21 halamanVolumetriRenhardBelum ada peringkat
- Titrasi Asam Basa DNG Indikator PP Dan MODokumen19 halamanTitrasi Asam Basa DNG Indikator PP Dan MOahmad sukaryaBelum ada peringkat
- Lamtiarma Panjaitan 31S19001Dokumen21 halamanLamtiarma Panjaitan 31S19001Lamtiarma PanjaitanBelum ada peringkat
- Kad 1 HahahaDokumen10 halamanKad 1 HahahaDwi anisahBelum ada peringkat
- Cara Dan Proses Titrasi NetralisasiDokumen2 halamanCara Dan Proses Titrasi NetralisasiHumanBelum ada peringkat
- Titrasi ialah salah satu metode kimia untuk dapat menentukan konsentrasi suatu larutan dengan cara mereaksikan sejumlah volume larutan itu terhadap sejumlah volume larutan lain yang konsentrasinya itu sudah diketahuiDokumen3 halamanTitrasi ialah salah satu metode kimia untuk dapat menentukan konsentrasi suatu larutan dengan cara mereaksikan sejumlah volume larutan itu terhadap sejumlah volume larutan lain yang konsentrasinya itu sudah diketahuiRosna IstofainaBelum ada peringkat
- Volumetrik Asam BasaDokumen7 halamanVolumetrik Asam BasaIlma Inaroh AzizahBelum ada peringkat
- Lap KelompokDokumen3 halamanLap KelompokEvan OrlandoBelum ada peringkat
- 059-Gita Saraswati1Dokumen19 halaman059-Gita Saraswati1Inggried AudreyBelum ada peringkat
- NetralisasiDokumen14 halamanNetralisasiYogi Yogi0% (1)
- (PPT) Alkalimetri Kimia AnalisisDokumen16 halaman(PPT) Alkalimetri Kimia Analisisbaby jungkookBelum ada peringkat
- Makalah AsidimetriDokumen12 halamanMakalah AsidimetriHasanah50% (4)
- Titrasi Asam BasaDokumen8 halamanTitrasi Asam BasaWahyu ade dwi anugraBelum ada peringkat
- Titra SiDokumen16 halamanTitra SiAniBelum ada peringkat
- Literature Kimia Baru LagiDokumen4 halamanLiterature Kimia Baru Lagieka rizkiBelum ada peringkat
- Titrasi Asam Basa Dengan Pelarut AirDokumen12 halamanTitrasi Asam Basa Dengan Pelarut AirYustina100% (1)