NEW - Termokimia
Diunggah oleh
Lintang Punggi zahra 22Deskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
NEW - Termokimia
Diunggah oleh
Lintang Punggi zahra 22Hak Cipta:
Format Tersedia
Termokimia
Termokimia → Ilmu yang mempelajari tentang reaksi kimia dan [erubahan energi yang terlibat.
A. Sistem dan Lingkungan
Sistem → Segala sesuatu yang menjadi pusat perhatian atau
pengamatan.
Dibagi menjadi :
- Sistem Terbuka : adanya pertukaran energi dan materi
- Sistem Tertutup : adanya pertukaran energi dan tidak terjadi
pertukaran materi
- Sistem Terisolasi : tidak terjadi pertukaran
Lingkungan → Segala sesuatu yang berada diluar atau disekitar sistem.
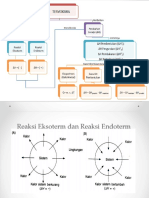
B. Reaksi Endoterm dan Reaksi Endoterm
1. Reaksi Endoterm (H = + )
“Reaksi yang memerlukan energi (menyerap kalor), kalor berpindah dari lingkungan ke system”. (suhu
turun)
Contoh : Melarutkan salmiak ( NH4Cl ) ke dalam air,
Reaksi Ba(OH)2 dengan NH4Cl,
Pemanasan CuCO3.
2. Reaksi Eksoterm (H = )
“Reaksi yang menghasilkan energi (melepaskan kalor), kalor berpindah dari sistem ke lingkungan”. (suhu
naik)
Contoh : Logam natrium dilarutkan ke dalam air,
Na(s) + H2O (ℓ) → NaOH(aq) + ½ H2 (g) + energi,
Reaksi Mg dengan HCl.
Perbedaan reaksi endoterm dan eksoterm
Perbedaan Reaksi endoterm Reaksi eksoterm
Dibebaskan/dilepaskan
Diserap/diterima sistem
Energi (H) sistem
H2 > H1
H2 < H1
Diagram tingkat energi
Turun/dingin Naik/panas
Suhu lingkungan (T)
Takhir < Tawal Takhir > Tawal
∆H reaksi (+) (-)
C. Entalpi (H) dan Perubahan Entalpi (∆H)
Entalpi standar adalah perubahan entalpi yang terjadi pada suhu 25° C (atau 298 K), tekanan 1 atm, pada 1 mol
suatu zat, dilambangkan dengan ΔH°.
1. Entalpi Pembentukan Standar (∆H0f)
“Kalor yang dibutuhkan/dilepaskan pada pembentukan 1 mol senyawa dari unsur-unsur nya yang paling
stabil”.
Contoh :
H2 + ½ O2 → H2O ∆H0f = -285,5 kJ
N2 + 4H2 + 2Cr + 7/2 O2 → (NH4)2Cr2O7 ΔH°f = -2780,08 kJ
2. Entalpi Penguraian Standar (∆H0d)
“Kalor yang dibutuhkan/dilepaskan pada penguraian 1 mol senyawa menjadi unsur-unsur nya yang paling
stabil”.
Contoh :
C2H6 → 2C + 3H2 ΔH°d = -285,5 kJ
NaCl → Na + ½ Cl2 ΔH°d = +410,9 kJ
3. Entalpi Pembakaran Standar (∆H0c)
“Kalor yang dibutuhkan/dilepaskan pada pembakaran 1 mol senyawa atau unsur menjadi CO2 (pembakaran
sempurna) / CO (pembakaran tidak sempurna) dan H2O”.
Contoh :
C3H6 + 9/2 O2 → 3CO2 + 3H2O ΔH° = -2377 kJ
D. Persamaan Termokimia
Perhitungan Persamaan Termokimia berlaku :
Jika reaksi dibalik → nilai ∆H berubah tanda + ke – atau sebaliknya
Jika reaksi dikali x → maka nilai ∆H dikali x
Jika reaksi dibagi x → maka nilai ∆H dibagi x
E.Menghitung nilai ∆H
Entalpi reaksi ditentukan dengan:
1) Menggunakan kalorimetri.
2) Menggunakan hukum Hess (penjumlahan).
3) Menggunakan data entalpi pembentukan.
4) Menggunakan data energi ikatan.
1. Kalorimetri
Kalorimetri adalah cara penentuan energi kalor reaksi dengan kalorimeter.
−qreaksi Keterangan :
∆ H= ∆ T : perubahan suhu (0C) C : kapasitas kalor (J/0C) q : kalor
mol m : massa air (gram) c : kalor jenis air (J/g0C) (4,2 J/g0C)
q sistem=mc ∆ T
q reaksi=qsistem + q kalorimeter
q kalorimeter =C ∆ T
2. Hukum Hess (Penjumlahan)
Tidak semua perubahan entalpi reaksi dapat ditentukan secara langsung dengan menggunakan kalorimeter .
G .Hess mengemukakan hukumnya : “Perubahan entalpi hanya bergantung pada keadaan awal dan
keadaan akhir reaksi”. Jadi penentuan perubahan entalpi dapat ditentukan dengan :
a. Siklus Energi
A (s) B (s) ∆H1 = ∆H2 + ∆H3
∆H1
∆H2 = ∆H3
= C (s) =
b. Penjumlahan aljabar beberapa persamaan termokimia
Tentukan perubahan entalpi penguapan air dari wujud padat (H2O(s) → H2O(g)), jika diketahui reaksi-
reaksi berikut:
- H2(g) + ½ O2(g) → H2O(g) ΔH = -241,8 kJ (reaksi tetap)
- H2O(l) → H2O(s) ΔH = -6,01 kJ (reaksi dibalik)
- H2(g) + ½ O2(g) → H2O(l) ΔH = -285,8 kJ (reaksi dibalik)
Penyelesaian :
H2(g)+ ½ O2(g) → H2O(g) ΔH =-241,8 kJ
H2O(s) → H2O(l) ΔH = 6,01 kJ
H2O(l) → H2(g) + ½ O2(g) ΔH = 285,8 kJ
+
H2O(s) → H2O(g) ΔH = 50,01 kJ
3. ∆H0f
=∑ ∆ H −¿ ∑ ∆ H
0 0 0
∆H reaksi f kanan f kiri ¿
0
∆H reaksi
Tentukan entalpi reaksi berikut!
BaCl2(aq) + H2SO4(aq) → BaSO4(s) + 2HCl(aq)
Jika diketahui entalpi pembentukan standar dari BaCl2, BaSO4, H2SO4 , dan HCl berturut-turut adalah −858,6
kJ/mol, −1473,3 kJ/mol, −909,27 kJ/mol, dan −167,1 kJ/mol
Penyelesaian :
ΔH0R = (ΔH°f produk) − (ΔH°f reaktan)
= (ΔH°f BaSO4 + 2ΔH°f HCl) − (ΔH°f BaCl2 + ΔH°f H2SO4)
= (−1473,3 − 2 x 167,1) − (−858,6 − 909,27)
= −39,63 kJ/mol
4. Energi Ikatan
∆H =∑ energi ikatan kiri – ∑ energi ikatan kanan
0
reaksi
Ikatan Energi Ikatan Ikatan Energi Ikatan
C−H 413 kJ/mol C=O 358 kJ/mol
O=O 146 kJ/mol O−H 463 kJ/mol
Tentukan perubahan entalpi reaksi dari pembakaran CH 2 berikut : CH2(g) + 3/2 O2(g) → CO2(g) + H2O(g)
ΔH = ?
Penyelesaian : ΔH = (H−C−H) + 3 /2(O=O) → (O=C=O) + (H−O−H)
= (2x413) + (3/2x146) – ((2x358) + (2x463)) = −743 kJ
Anda mungkin juga menyukai
- ThermokimiaDokumen35 halamanThermokimiaVicky raihan akbar 068Belum ada peringkat
- Termokimia Bahan AjarDokumen38 halamanTermokimia Bahan Ajarra_puspitaBelum ada peringkat
- TermokimiaDokumen30 halamanTermokimiaLailatul LuthfiyatiBelum ada peringkat
- Bab 5 TermokimiaDokumen5 halamanBab 5 TermokimiaHafidz SayyidBelum ada peringkat
- BAB II TermokimiaDokumen4 halamanBAB II TermokimiaTri FaturrBelum ada peringkat
- TERMOKIMIADokumen63 halamanTERMOKIMIAAri Sofyan SauriBelum ada peringkat
- Termokimia Kelas XiDokumen4 halamanTermokimia Kelas XidwiBelum ada peringkat
- Term Okimi ADokumen32 halamanTerm Okimi Amutiara tiaraBelum ada peringkat
- I - ThermokimiaDokumen111 halamanI - ThermokimiaTheresia AustinBelum ada peringkat
- Termokimia ZoomDokumen11 halamanTermokimia ZoomZakwan AlthofBelum ada peringkat
- (Kelas 11) BAB 4 TERMOKIMIADokumen13 halaman(Kelas 11) BAB 4 TERMOKIMIAMutia AgustinBelum ada peringkat
- Termokimia PPTXDokumen24 halamanTermokimia PPTXpipitBelum ada peringkat
- TERMOKIMIADokumen9 halamanTERMOKIMIAikke febri yenikaBelum ada peringkat
- Termokimia PDFDokumen42 halamanTermokimia PDFstrygwyrgtBelum ada peringkat
- MATERI Kim XI TermokimiaDokumen10 halamanMATERI Kim XI Termokimiasatyajulian4Belum ada peringkat
- Termokimia PDFDokumen7 halamanTermokimia PDFraftwarriorBelum ada peringkat
- TERMOKIMIADokumen14 halamanTERMOKIMIAIzzul MuttaqinBelum ada peringkat
- Felisa M. Termokimia NotesDokumen4 halamanFelisa M. Termokimia NotesFelisa MutiarahmaBelum ada peringkat
- Termokimia 2Dokumen83 halamanTermokimia 2Smahangtuah MakassarBelum ada peringkat
- 3.TERMOKIMIA 220911 PowerpointDokumen36 halaman3.TERMOKIMIA 220911 PowerpointDevi Arum Zulyhani0% (1)
- Bab 2 TermokimiaDokumen17 halamanBab 2 TermokimiamaawsBelum ada peringkat
- Termokimia (12-13) PDFDokumen83 halamanTermokimia (12-13) PDFYuliantari YuliantariBelum ada peringkat
- 3 TermokimiaDokumen9 halaman3 TermokimiaIvan ApriBelum ada peringkat
- KD Mesin 7 8Dokumen40 halamanKD Mesin 7 8Saverianus JakBelum ada peringkat
- Term Okimi ADokumen5 halamanTerm Okimi AWiwied Rizky Puspita RahayuBelum ada peringkat
- Materi TermokimiaDokumen32 halamanMateri Termokimianurhikmah_88Belum ada peringkat
- Term Odin A MikaDokumen73 halamanTerm Odin A MikaFadhiil faridhzaBelum ada peringkat
- Termokimia Perte 1 Dan 2Dokumen97 halamanTermokimia Perte 1 Dan 2mesi nubatonisBelum ada peringkat
- Term Okimi ADokumen82 halamanTerm Okimi AFriska AprilBelum ada peringkat
- Ental PiDokumen18 halamanEntal Pijuli ahmadBelum ada peringkat
- Materi Termokimia MicroDokumen10 halamanMateri Termokimia MicroSitiNurAzizah A.TBelum ada peringkat
- Termokimia PPTXDokumen23 halamanTermokimia PPTXEfrin SitumorangBelum ada peringkat
- TermokimiaDokumen25 halamanTermokimiaidzni desrifaniBelum ada peringkat
- 3 TermokimiaDokumen32 halaman3 TermokimiaernaBelum ada peringkat
- Termokimia SMADokumen23 halamanTermokimia SMAWahid ArdaniBelum ada peringkat
- 15 TermokimiaDokumen46 halaman15 TermokimialistiBelum ada peringkat
- Bahan Ajar Termokimia KD 3.4Dokumen7 halamanBahan Ajar Termokimia KD 3.4Nafilatul ArfaBelum ada peringkat
- TermokimiaDokumen17 halamanTermokimiaYosep Kevin DamanikBelum ada peringkat
- Termokimia TGTDokumen18 halamanTermokimia TGTSyafira TiaradipaBelum ada peringkat
- 15 TermokimiaDokumen46 halaman15 TermokimiaasysyifaBelum ada peringkat
- Termokimia 1Dokumen21 halamanTermokimia 1Desi wulandariBelum ada peringkat
- Termo KimiaDokumen26 halamanTermo KimiaDjoko Sriyadi67% (3)
- TermokimiaDokumen14 halamanTermokimiaAr Rahman MugaBelum ada peringkat
- 14 TermokimiaDokumen23 halaman14 TermokimiaAdamDio ZaidanDhuhaBelum ada peringkat
- TERMOKIMIADokumen37 halamanTERMOKIMIATM-21-084 RIFQI TUBAGUS HILMIBelum ada peringkat
- 18 Termokimia1Dokumen47 halaman18 Termokimia1najmahanifah253Belum ada peringkat
- TERMOKIMIADokumen44 halamanTERMOKIMIAIqna AmaliyahBelum ada peringkat
- LKPD tERMOKIMIADokumen11 halamanLKPD tERMOKIMIAKrisostomus AnsaBelum ada peringkat
- Pengantar Termodinamika 1-1Dokumen13 halamanPengantar Termodinamika 1-1AgusBelum ada peringkat
- TermokimiaDokumen40 halamanTermokimiaMega RestiaBelum ada peringkat
- Term Okimi ADokumen35 halamanTerm Okimi ANurainiazzahroBelum ada peringkat
- 5 TermokimiaDokumen43 halaman5 TermokimiaFikri HaikalBelum ada peringkat
- TERMOKIMIADokumen9 halamanTERMOKIMIARahayu LestariBelum ada peringkat
- TermokimiaDokumen32 halamanTermokimiaTin InBelum ada peringkat
- Pert Emu A 1Dokumen58 halamanPert Emu A 1_Raqhuel_ALouc_2087Belum ada peringkat
- TERMOKIMIA MateriDokumen29 halamanTERMOKIMIA MateriZaisith Asputri FellyBelum ada peringkat
- TermokimiaDokumen65 halamanTermokimiaDarmawan Ardyansyah 17Belum ada peringkat