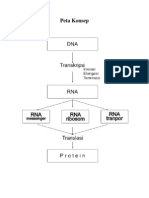
Peta Konsep Sel Volta
Diunggah oleh
Ahmad Gilang Indra Salam0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
709 tayangan1 halamanSel Volta
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOC, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniSel Volta
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
709 tayangan1 halamanPeta Konsep Sel Volta
Diunggah oleh
Ahmad Gilang Indra SalamSel Volta
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOC, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 1
NAMA : ANINDA INDRIANI
Elektrokimia
NIM / OFFERING : 110331406401 / B
Berhubungan
dengan
EnergI
bebas dan
konstanta
kesetimban
gan
berhubunga
n
mempunyai
Standart
potensial sel,
Eo
EnergI
kimia
EnergI
listrik
Aspek
kuantitatif
Hukum
Faraday
Diubah melalui
Proses disebut
Sel
volta
Dihitung
dari
Potensial
reduksi
standar
Digunakan
pada
Pesamaan
Nernst
Terjadi
reaksi
Oksidasi-reduksi
Spontan
Reaksi oksidasi
terjadi di
Sel
elektrolisis
Terjadi
reaksi
Oksidasi reduksi
Tidak Spontan
G = -
G = +
Eosel =
+
Eosel =
-
Anoda
Katod
a
Reaksi reduksi
terjadi di
Elektrolisis
Anda mungkin juga menyukai
- Bahan FisikaDokumen22 halamanBahan FisikarisnaBelum ada peringkat
- Kimia 10 IpaDokumen3 halamanKimia 10 Ipawildan100% (2)
- Kisi - Kisi Kimia 2024Dokumen2 halamanKisi - Kisi Kimia 2024gracejulita288Belum ada peringkat
- Surat Kecil Untuk TuhanDokumen2 halamanSurat Kecil Untuk TuhanMrs. DarcyBelum ada peringkat
- Soal Hots Kelas XiDokumen5 halamanSoal Hots Kelas XiSri Agustini HidayantiBelum ada peringkat
- Induksi ElektromagnetikDokumen5 halamanInduksi ElektromagnetikTyas EstiningsihBelum ada peringkat
- DiskusiDokumen2 halamanDiskusiNoprianti SantikaBelum ada peringkat
- Peta Konsep Teori Kuantum-DikonversiDokumen1 halamanPeta Konsep Teori Kuantum-DikonversiRida RamdaniBelum ada peringkat
- Matematika (Umum)Dokumen32 halamanMatematika (Umum)Parlindungan SitanggangBelum ada peringkat
- Pengaruh Spektrum Warna Cahaya Terhadap TumbuhanDokumen14 halamanPengaruh Spektrum Warna Cahaya Terhadap TumbuhanfadillaBelum ada peringkat
- A24 Soal Ina SMPDokumen18 halamanA24 Soal Ina SMPAgung AntaraniBelum ada peringkat
- Soal Usp Metlit 2021Dokumen10 halamanSoal Usp Metlit 2021Dimas LesmanaBelum ada peringkat
- Gejala Gelombang PDFDokumen28 halamanGejala Gelombang PDFHeruko Fatimah100% (1)
- Artikel Penyusun AtomDokumen5 halamanArtikel Penyusun AtomHaryawan WahyuBelum ada peringkat
- Sel Volta: 1. Perhatikan Reaksi Setengah Sel Dari Beberapa Logam BerikutDokumen18 halamanSel Volta: 1. Perhatikan Reaksi Setengah Sel Dari Beberapa Logam BerikutNanam naaBelum ada peringkat
- Rangkuman KSPDokumen3 halamanRangkuman KSPAnonymous INQWLEBelum ada peringkat
- ELEKTROKIMIADokumen11 halamanELEKTROKIMIAZulfatan ArafatBelum ada peringkat
- RNADokumen7 halamanRNAsaktiyonnie0% (1)
- Laporan Uji Golongan DarahDokumen4 halamanLaporan Uji Golongan DarahNursyam PujiBelum ada peringkat
- 3.6. Induksi Elektromagnetik: Medan MagnetikDokumen6 halaman3.6. Induksi Elektromagnetik: Medan MagnetikGinta Eureka WongQtoBelum ada peringkat
- Laporan Bio Pert Tumb.Dokumen5 halamanLaporan Bio Pert Tumb.Zhafirah GhitaBelum ada peringkat
- Dekarboksilasi OksidatifDokumen7 halamanDekarboksilasi Oksidatifindah sinagaBelum ada peringkat
- Eksperimen KimiaDokumen2 halamanEksperimen Kimiatangkas eghanBelum ada peringkat
- Gelombang PanasDokumen4 halamanGelombang Panasstella gresica100% (2)
- KwuDokumen57 halamanKwuMeta DelisaBelum ada peringkat
- Bab III UNSUR - UNSUR GOLONGAN UTAMADokumen36 halamanBab III UNSUR - UNSUR GOLONGAN UTAMAfajar alaqshaBelum ada peringkat
- Format Laporan Praktikum Biologi (Mutasi) - 2Dokumen9 halamanFormat Laporan Praktikum Biologi (Mutasi) - 2Yogi Dwi SaputraBelum ada peringkat
- Praktikum Kapasitor MSGDDokumen12 halamanPraktikum Kapasitor MSGDdxlusiionBelum ada peringkat
- Laporan PenelitianDokumen2 halamanLaporan PenelitianikhaBelum ada peringkat
- Pembuatan KoloidDokumen7 halamanPembuatan KoloidAnam_AgestyaBelum ada peringkat
- Tugas Kimia Bertrand Siagian XII IPA 2Dokumen2 halamanTugas Kimia Bertrand Siagian XII IPA 2Bertrand SiagianBelum ada peringkat
- Kimia Klompok 1 LDokumen17 halamanKimia Klompok 1 LAli SamudraBelum ada peringkat
- Materi Ajar RE RMDokumen4 halamanMateri Ajar RE RMeskawatiBelum ada peringkat
- Manfaat RadioaktifDokumen8 halamanManfaat RadioaktifamaliazafitriBelum ada peringkat
- Sinopsis Novel Sejarah Misteri Gajah Mada IslamDokumen17 halamanSinopsis Novel Sejarah Misteri Gajah Mada IslamRika YantiBelum ada peringkat
- Rangkuman BenzenaDokumen2 halamanRangkuman BenzenaRohman Abduhan100% (1)
- Soal Dan JawabanDokumen3 halamanSoal Dan JawabanAningBelum ada peringkat
- AnilinDokumen2 halamanAnilinLinaLathifahIIBelum ada peringkat
- Ulangan HarianDokumen9 halamanUlangan HarianNadyatun KhasanahBelum ada peringkat
- Listrik StatisDokumen16 halamanListrik StatisalenaBelum ada peringkat
- Bab X Fisika Inti Dan RadioaktivitasDokumen8 halamanBab X Fisika Inti Dan RadioaktivitasRika Nike SariBelum ada peringkat
- Konsentrasi LarutanDokumen7 halamanKonsentrasi LarutanYuliani PurwitasariBelum ada peringkat
- Contoh Soal Senyawa Organik SBMPTNDokumen7 halamanContoh Soal Senyawa Organik SBMPTNDoyok PurwadiBelum ada peringkat
- Sebuah Ayunan Bandul Sederhana Membuat 30 Ayunan Dalam 1 MenitDokumen2 halamanSebuah Ayunan Bandul Sederhana Membuat 30 Ayunan Dalam 1 MenitPak SuBelum ada peringkat
- Ayunan SederhanaDokumen11 halamanAyunan SederhanaPramuji HandrajadiBelum ada peringkat
- Bahan Ajar KeduaDokumen9 halamanBahan Ajar KeduatianBelum ada peringkat
- Soal Kimia LanjutDokumen1 halamanSoal Kimia LanjutNurulBelum ada peringkat
- XII - Fisika - KD 3.3Dokumen36 halamanXII - Fisika - KD 3.3usman asegafBelum ada peringkat
- Elektrolisis Larutan KiDokumen3 halamanElektrolisis Larutan Kikheisya idhanBelum ada peringkat
- Latihan PPKN Kelas XI-20 April 2020-BAB 6Dokumen2 halamanLatihan PPKN Kelas XI-20 April 2020-BAB 6Zeross StephenBelum ada peringkat
- BAB 2 LKS 4 Mat Minat Sukino K13 Revisi 2016 Hudamath DonateDokumen3 halamanBAB 2 LKS 4 Mat Minat Sukino K13 Revisi 2016 Hudamath DonateHola Holi100% (1)
- STD Bab 1 PPT Kimia 3Dokumen17 halamanSTD Bab 1 PPT Kimia 3Anonymous vDMrfyYqjoBelum ada peringkat
- Tugas Indo Riyan 2Dokumen4 halamanTugas Indo Riyan 2Tidak Diketahui100% (1)
- Laporan Ligan - YeniDokumen16 halamanLaporan Ligan - YeniyeniBelum ada peringkat
- Laporan Pertanggungjawaban Managemen Produksi Pertunjukan Dram1Dokumen9 halamanLaporan Pertanggungjawaban Managemen Produksi Pertunjukan Dram1Retchi Lucia100% (1)
- PolimerDokumen5 halamanPolimerJessica SatrioBelum ada peringkat
- Elektrolisis Lelehan Nacl Dengan Elektoda PTDokumen5 halamanElektrolisis Lelehan Nacl Dengan Elektoda PTAlfaDinaPrianotoBelum ada peringkat
- Tugas Kf. Kelompok 8Dokumen22 halamanTugas Kf. Kelompok 8Grace Elga Etlin Siregar 2103114083Belum ada peringkat
- SpontanDokumen4 halamanSpontanAchmad FauziBelum ada peringkat
- Laporan Praktikum Kimia Fisika ElektrokimiaDokumen17 halamanLaporan Praktikum Kimia Fisika ElektrokimiaDewi Sunarti100% (1)
- Khutbah Bersenang-Senang Dalam Pandangan IslamDokumen6 halamanKhutbah Bersenang-Senang Dalam Pandangan IslamAhmad Gilang Indra SalamBelum ada peringkat
- Pidato Bahas Inggris Dan Indonesia TPQDokumen2 halamanPidato Bahas Inggris Dan Indonesia TPQAhmad Gilang Indra SalamBelum ada peringkat
- Khutbah-Jumat-Nasihat-Bagi-yang-Meremehkan-Shalat-revisi 2Dokumen8 halamanKhutbah-Jumat-Nasihat-Bagi-yang-Meremehkan-Shalat-revisi 2Ahmad Gilang Indra SalamBelum ada peringkat
- Silabus Science Gamer XiDokumen16 halamanSilabus Science Gamer XiAhmad Gilang Indra SalamBelum ada peringkat
- Khutbah Jumat Kapan Kita BershalawatDokumen11 halamanKhutbah Jumat Kapan Kita BershalawatN HBelum ada peringkat
- Tabel RDokumen5 halamanTabel Rseryx50% (4)
- Laporan Sulfat Spektronik 20Dokumen12 halamanLaporan Sulfat Spektronik 20nurBelum ada peringkat
- Puisi KarawangDokumen1 halamanPuisi KarawangAhmad Gilang Indra SalamBelum ada peringkat
- 100 Permainan Untuk Training (Ice Breaking)Dokumen146 halaman100 Permainan Untuk Training (Ice Breaking)lee_nez100% (2)
- Laporan PotensiometriDokumen23 halamanLaporan PotensiometriRizqan JamalBelum ada peringkat
- Pengendapan VolhardDokumen8 halamanPengendapan VolhardAhmad Gilang Indra SalamBelum ada peringkat
- Alkali MetriDokumen12 halamanAlkali MetriAhmad Gilang Indra SalamBelum ada peringkat