Kimia - Larutan Penyangga
Diunggah oleh
Novianti TandirerungDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Kimia - Larutan Penyangga
Diunggah oleh
Novianti TandirerungHak Cipta:
Format Tersedia
LKPD 1
- Temukan topik yang ada pada bacaan di atas. Jelaskan kaitannya dengan materi yang sedang kita
pelajari
Jawaban : Bacaan di atas berbicara mengenai bagaimana larutan penyangga membantu menstabilkan
pH dalam darah dengan menyangga pH supaya tidak berubah meskipun diberikan sedikit
asam, sedikit basa, atau diencerkan. Dalam kimia, larutan penyangga ini sering disebut juga
dengan larutan buffer.
- Catatlah masalah- masalah yang anda temukan dari bacaan sebelumnya, kemukakan dalam
pertanyaan sebayak- banyaknya!
Jawaban :
- Setelah mendiskusikan topik di atas dengan teman kelompok, apakah yang dimaksud dengan larutan
penyangga?
Jawaban : Berdasarkan hasil diskusi kami, yang dimaksud dengan larutan penyangga adalah larutan
yang fungsinya berfungsi untuk menjaga pH tubuh supaya tetap stabil dan sehat.
- Bagaimana sifat dan prinsip kerja larutan penyangga di dalam darah dan obat tetes mata?
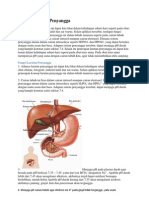
Jawaban : Di dalam darah, senyawa penyangga ini ada dalam bentuk H2CO3 dan HCO3- . Kalau kita
perhatikan, kedua senyawa tersebut punya sifat yang berbeda: H2CO3 bersifat asam,
sementara HCO3- adalah basa konjugasi. Senyawa yang ada di dalam darah, apabila ada
makanan asam (H+) yang masuk ke dalam tubuh, maka akan dikat oleh senyawa penyangga
basa konjugasi (HPO42-). Sebaliknya, apabila ada makanan/minuman yang mengandung
basa masuk ke dalam sel, maka akan ditangkap oleh senyawa penyangga asam (H2PO4-).
Sedangkan Karakteristik yang penting pada obat tetes mata yaitu buffer (larutan penyangga)
atau pH. Idealnya sediaan optalmik harus diformulasikan pada pH yang ekuivalen dengan pH
cairan air mata yaitu 7,4. Pada kenyataannya, hal ini jarang digunakan.
LKPD 2
- Setelah mendiskusikan topik di atas dengan teman kelompok anda, apa saja komponen larutan
penyangga di dalam darah dan obat tetes mata?
Jawaban : terdiri atas komponen asam dan basa. Komponen asam berfungsi menahan kenaikan pH,
sedangkan komponen basa berfungsi menahan penurunan pH.
- Setelah mendengarkan penjelasan dan mnegerjakan contoh soal , diskusikan dengan teman kelompok
anda dan kerjakan latihan soal :
1. Sebanyak 25 mL larutan asam asetat CH3COOH 0,1M dicampur dengan 25 mL larutan kalsium asetat
(CH3COO))2Ca 0,1M. Hitunglah Ph campuran larutan jika Ka = 1 x 10*-5?
Jawaban :
2. Sebanyak 100 ml larutan NH4OH 0,1 M (Kb=10*-5) dicampur dengan 50 mL larutan NH4NO3 0,1 M.
Tuliskan reaksi kesetimbangan basa yang terjadi dalam larutan dan tentukan pH larutan setelah
pencampuran?
Jawabann :
LKPD ndak tau ke berapa (acak juga)
- Kemukakan menurut pendapatmu, bagaimana fungsi larutan penyangga dalam makhluk hidup!
Jawaban : Fungsi larutan penyangga dalam makhluk hidup tentunya Menjaga tingkat keasaman pada
tubuh, menetralisir zat asam atau basa yang masuk ke dalam tubuh serta memastikan agar
enzim dapat bekerja.
- Selain yang telah dijelaskan oleh guru, kemukakan fungsi lain dari larutan penyangga dalam makhuk
hidup.
Jawaban : Larutan juga digunakan dalam berbagai bidang, seperti kimia analitis, biokimia,
bakteriologi, obat- obatan (farmasi), fotografi, industri kulit, zat warna, industri makanan
pertanian, dan pengolahan limbah industri.
- Sebutkan salah satu produk aplikasi larutan penyangga dalam kehidupan sehari – hari yang kamu
ketahui zat apa yang berfungsi sebagai penyangga?
Jawaban : Misalnya asam sitrat dan natrium sitrat. Kedua zat tersebut merupakan larutan penyangga
yang biasa ditambahkan pada buah-buahan yang dikalengkan. Selain itu, asam sitrat juga
biasa digunakan untuk mengatur tingkat keasaman pada produk air susu, selai, dan jeli. Jika
pH terjaga maka produk makanan tersebut tidak mudah rusak oleh bakteri.
- Bagaimana cara kerja larutan penyangga dalam produk pada soal no.2?
Jawaban :
Anda mungkin juga menyukai
- Ekonomi dopamin: Bagaimana neurotransmitter kesenangan memengaruhi keputusan dan perilaku kita dalam kehidupan sehari-hariDari EverandEkonomi dopamin: Bagaimana neurotransmitter kesenangan memengaruhi keputusan dan perilaku kita dalam kehidupan sehari-hariBelum ada peringkat
- Kajian Ontologi, Epistemologi, AksiologiDokumen3 halamanKajian Ontologi, Epistemologi, AksiologiRossi Nur FajrianiBelum ada peringkat
- Buffer IndahDokumen9 halamanBuffer Indahwidyatmokobeni purwiantoBelum ada peringkat
- KIMIA-Bahan Ajar-PenyanggaDokumen21 halamanKIMIA-Bahan Ajar-PenyanggaAfli Sindri Dacosta AlnabeBelum ada peringkat
- Kimia - Larutan PenyanggaDokumen30 halamanKimia - Larutan PenyanggaAqila FakhiraBelum ada peringkat
- Lembaran Kerja Mahasiswa (LKM) Matfar 2013 Topik 1Dokumen8 halamanLembaran Kerja Mahasiswa (LKM) Matfar 2013 Topik 1Fandi HarmikiBelum ada peringkat
- RPP Larutan PenyanggaDokumen9 halamanRPP Larutan PenyanggaBurhan CfBelum ada peringkat
- Makalah Larutan PenyanggaDokumen11 halamanMakalah Larutan PenyanggaTomy RifandiBelum ada peringkat
- Lap 3aDokumen22 halamanLap 3aPelajaran ParsaBelum ada peringkat
- Larutan Buffer 2022Dokumen22 halamanLarutan Buffer 2022Alexandra Audrey AureliaBelum ada peringkat
- Makalah Indra Rohimat Mipa 4Dokumen8 halamanMakalah Indra Rohimat Mipa 4Fitrah OfficialBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen4 halamanFungsi Larutan PenyanggaNur Desi YaniBelum ada peringkat
- LARUTAN PENYANGGA (Manfaat Larutan Penyangga Dalam Kehidupan Sehari)Dokumen1 halamanLARUTAN PENYANGGA (Manfaat Larutan Penyangga Dalam Kehidupan Sehari)Josefin Desiana SitungkirBelum ada peringkat
- Larutan Penyangga2Dokumen18 halamanLarutan Penyangga2Muhammad Hanif100% (1)
- Larutan PenyanggaDokumen6 halamanLarutan PenyanggaPuput AriantikaBelum ada peringkat
- Peranan Larutan Penyangga Kelompok 3Dokumen11 halamanPeranan Larutan Penyangga Kelompok 3Della DwisaputriBelum ada peringkat
- Modul Larutan PenyanggaDokumen18 halamanModul Larutan PenyanggaLatifah SariBelum ada peringkat
- LKPD Larutan PenyanggaDokumen25 halamanLKPD Larutan PenyangganovariyantiBelum ada peringkat
- Aplikasi Larutan Buffer Dalam Kehidupan SehariDokumen5 halamanAplikasi Larutan Buffer Dalam Kehidupan SehariAnonymous iXl3xk0% (1)
- Aplikasi Larutan Buffer PDFDokumen6 halamanAplikasi Larutan Buffer PDFYuliaDelestiBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen2 halamanFungsi Larutan PenyanggacindyokhotanBelum ada peringkat
- Larutan PenyanggaDokumen8 halamanLarutan PenyanggaArman Dahlan Wiranto100% (1)
- Pengertian Larutan PenyanggaDokumen12 halamanPengertian Larutan PenyanggaTiara MahardikaBelum ada peringkat
- RPP Larutan PenyanggaDokumen17 halamanRPP Larutan PenyanggaAlawiyah NurBelum ada peringkat
- LKPD Kimia Berbasis PBL Pada Materi Larutan PenyanggaDokumen25 halamanLKPD Kimia Berbasis PBL Pada Materi Larutan PenyanggaNurmalita FatimahBelum ada peringkat
- Bab 1 Kimdas NadiaDokumen4 halamanBab 1 Kimdas NadiaFahdalis MassiBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen11 halamanFungsi Larutan PenyanggaDesi Sari100% (1)
- Laporan Praktikum Buffer Dan Sifat Larutan, Lukman Sahrul Kamal 1328120010Dokumen29 halamanLaporan Praktikum Buffer Dan Sifat Larutan, Lukman Sahrul Kamal 1328120010Lukman KamalBelum ada peringkat
- LKM Kimia Larutan (P-6) - TIA - 007Dokumen15 halamanLKM Kimia Larutan (P-6) - TIA - 007Kadek Junia100% (1)
- MateriDokumen12 halamanMateriKetut SeptiBelum ada peringkat
- Peranan Dan Manfaat Larutan Buffer DalamDokumen3 halamanPeranan Dan Manfaat Larutan Buffer DalamhanifahBelum ada peringkat
- TUGAS PENDAHULUAN 1 ZulfitrianiDokumen4 halamanTUGAS PENDAHULUAN 1 ZulfitrianiZul FitrianiBelum ada peringkat
- LKM Kimia Larutan (P-6)Dokumen15 halamanLKM Kimia Larutan (P-6)Anik 5Belum ada peringkat
- PernahDokumen4 halamanPernahRuth JBelum ada peringkat
- Media Pembelajaran Interaktif Larutan PenyanggaDokumen24 halamanMedia Pembelajaran Interaktif Larutan Penyanggaنداء الحسنةBelum ada peringkat
- Laporan Dan TP Olivia Cantika Agustam 199Dokumen12 halamanLaporan Dan TP Olivia Cantika Agustam 199Olivia AnandaBelum ada peringkat
- Laporan Praktikum Biologi Sel Dan Molekuler Buffer AjengDokumen19 halamanLaporan Praktikum Biologi Sel Dan Molekuler Buffer AjengAjeng NarulitaBelum ada peringkat
- Larutan PenyanggaDokumen2 halamanLarutan PenyanggaYunizar Farla PermataBelum ada peringkat
- Buffer - Farmasi FisikDokumen13 halamanBuffer - Farmasi FisikMama RioFiqaBelum ada peringkat
- Laporan Praktikum KimiaDokumen5 halamanLaporan Praktikum KimiadolphinpurpleBelum ada peringkat
- Y4 - Firman Nur Baskoro Edhi - Larutan Penyangga (BUFFER)Dokumen18 halamanY4 - Firman Nur Baskoro Edhi - Larutan Penyangga (BUFFER)Firman Nur Baskoro EdhiBelum ada peringkat
- Larutan Penyangga - Kegunaannya Dalam Kehidupan Sehari-HariDokumen5 halamanLarutan Penyangga - Kegunaannya Dalam Kehidupan Sehari-HariZhazha NetBelum ada peringkat
- Larutan Penyangga Mapel Kimia Crisdayanti Sinaga XI IPA 3Dokumen22 halamanLarutan Penyangga Mapel Kimia Crisdayanti Sinaga XI IPA 3Zacky FranciskoBelum ada peringkat
- Laporan Pembuatan Larutan Dapar 206Dokumen14 halamanLaporan Pembuatan Larutan Dapar 206Nur AwaliahBelum ada peringkat
- Kimia Larutan BufferDokumen8 halamanKimia Larutan BufferFahd DzulqornainBelum ada peringkat
- Larutan PenyanggaDokumen6 halamanLarutan PenyanggaSevriadyBelum ada peringkat
- Haidar Makalah Larutan PenyanggaDokumen8 halamanHaidar Makalah Larutan Penyanggadewi netBelum ada peringkat
- UntitledDokumen2 halamanUntitledUmamBelum ada peringkat
- 0 Larutan Penyangga PPT FixDokumen16 halaman0 Larutan Penyangga PPT FixLaila Majnun HutagaolBelum ada peringkat
- Modul Larutan PenyanggaDokumen12 halamanModul Larutan PenyanggaRETNO EKA NIANTIBelum ada peringkat
- Makalah Gangguan Keseimbangan Asam BasaDokumen22 halamanMakalah Gangguan Keseimbangan Asam BasaNabila Ulfany Ulfa75% (4)
- Larutan Penyangga 2Dokumen8 halamanLarutan Penyangga 2ahmadBelum ada peringkat
- Makalah Kimia Larutan PenyanggaDokumen10 halamanMakalah Kimia Larutan PenyanggaNhiia Nounha Muetz AbiesBelum ada peringkat
- Larutan PenyanggaDokumen29 halamanLarutan PenyanggaJatmiko Eko Saputro100% (13)
- Larutan BufferDokumen19 halamanLarutan BufferMawaqit Makani100% (2)
- Makalah BufferrDokumen23 halamanMakalah Bufferrwisudadwi56% (9)
- Asam Kuat Basa KuatDokumen11 halamanAsam Kuat Basa KuatQonita Puja KesumaBelum ada peringkat
- Sistem Buffer Tubuh ManusiaDokumen6 halamanSistem Buffer Tubuh ManusiaUpEngBelum ada peringkat
- Larutan Penyangga BufferDokumen20 halamanLarutan Penyangga BufferHeksa GGBelum ada peringkat
- Sejarah Pramuka Dunia Dan IndonesiaDokumen14 halamanSejarah Pramuka Dunia Dan IndonesiaNovianti TandirerungBelum ada peringkat
- Makalah SPM Kelompok 5Dokumen14 halamanMakalah SPM Kelompok 5Novianti TandirerungBelum ada peringkat
- Kadar Kapitalisme Dan SosialismeDokumen2 halamanKadar Kapitalisme Dan SosialismeNovianti TandirerungBelum ada peringkat
- Alat Optik: Tiara Putri Tandi Rerung Xi Ipa 2Dokumen4 halamanAlat Optik: Tiara Putri Tandi Rerung Xi Ipa 2Novianti TandirerungBelum ada peringkat
- Tanaman ViolcesDokumen6 halamanTanaman ViolcesNovianti TandirerungBelum ada peringkat