Ikatan Kimia
Ikatan Kimia
Diunggah oleh
Agus TridjokoDeskripsi Asli:
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Ikatan Kimia
Ikatan Kimia
Diunggah oleh
Agus TridjokoHak Cipta:
Format Tersedia
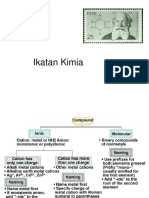
IKATAN KIMIA
Ikatan kimia adalah ikatan antar atom yang terjadi IKATAN KIMIA
agar atom yang berikatan di dalamnya memiliki
konfigurasi elektron yang stabil 1. Ikatan ion (elektrovalen)
Pada umumnya : Logam – Non Logam
Konfigurasi Elektron Valensi = 2 (duplet) 2. Ikatan kovalen
elektron stabil Pada umumnya : Non Logam – Non Logam
Seperti 3. Ikatan logam
Gas mulia Elektron Valensi = 8 (oktet) • Logam – Logam
• Terjadi dalam satu jenis logam
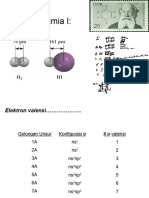
2He : 1s² =2
10Ne : [He] 2s² 2p⁶ = 2, 8
18Ar : [Ne] 3s² 3p⁶ = 2, 8, 8
36Kr : [Ar] 4s² 3d¹⁰ 4p⁶ = 2, 8, 18, 8
54Xe : [Kr] 5s² 4d¹⁰ 5p⁶ = 2, 8, 18, 18, 8
86Rn : [Xe] 6s² 5d¹⁰ 6p⁶ = 2, 8, 18, 32, 18, 8
Catatan: Harus diingat bahwa
elektron velensi (eV)
sangat berperan dalam
terbentuknya ikatan kimia
IKATAN ION / ELEKTROVALEN
Ikatan ion ⇒ Terjadi serah terima elektron
11Na dan 17Cl Na
Sifat-sifat senyawa dengan ikatan ionik
• Umumnya larut dalam pelarut polar, seperti air
• Memiliki titik didih dan titik leleh yang tinggi 2, 8, 7
Cl
2, 8, 1
• Baik larutan maupun lelehannya bersifat _
elektrolit ( dapat menghantarkan arus listrik)
Lepas 1 e- Terima 1 e-
• Keras dan mudah patah
Na+ Cl
Logam - Non Logam Na+ : 2, 8 Cl- : 2, 8, 8
IA, IIA, IIIA IVA, VA, VIA, VIIA
Na+ + Cl- → NaCl NaCl
Transfer e-
Lepas e- Serah-terima e-
Terima e-
Muatan = No Atom – No Gas Mulia
Ion + Ion - +1 -1
Kation Anion 2
He 11Na + 17Cl → NaCl
Elektron Valensi = Golongan 10
Ne 11 – 10 = +1 17 – 18 = -1
IA = 1 ⇒ melepas 1e Ar +2 -1
12Mg + 17Cl → MgCl2
IIA = 2 ⇒ melepas 2e Lepas e- 18
IIIA = 3 ⇒ melepas 1e Kr 12 – 10 = +2 17 – 18 = -1
36
IVA = 4 ⇒ menerima 4e
VA = 5 ⇒ menerima 3e 54
Xe +3 -2
VIA = 6 ⇒ menerima 2e Terima e- Rn 13Al + 16S → Al2S3
VIIA = 7 ⇒ menerima 1e 86 13 – 10 = +3 16 – 18 = -2
IKATAN KOVALEN
IKATAN KOVALEN ⇒ Join Elektron Berdasarkan electron yang Cara menggambar
⇓ Pemakaian bersama digunakan Bersama, Kovalen Struktur LEWIS
pasangan electron dibagi tiga :
STABIL CH4 NH3
⇓ ➢ Kovalen Tunggal : HCl
Konfigurasi
electron Saling menangkap e H
valensinya
H Cl ⟹ H – Cl
C H H N H
Non Non H
Logam Logam ➢ Kovalen Rangkap 2 : O2 H
2 8 H
Duplet Oktet O O ⟹ O=O
PCl3 PCl5
IA IIA IIIA IVA VA VIA
VIIA VIIIA
➢ Kovalen Rangkap 3 : N2
1 2 3 4 5 7 6 8 ⇒ e Valensi Cl P Cl
H Be B C N F O
Li Si P Cl S
N N ⟹ N≡N
Cl Cl P Cl
Br Kr
➢ Kovalen Koordinasi : NH4+
I Xe
H Cl
Huruf depan di dalam kotak ini ⇒ KOVALEN F
H N H+ XeF2 Xe
Misal : HBr , CH4 , PCl5 , XeF2
H Kov. Koordinasi
BENTUK GEOMETRI MOLEKUL
Bentuk molekul bergantung pada Bentuk Geometri Molekul Polar : AX3E ⇒ Trigonal piramidal
▪ jumlah Pasangan Elentron Ikatan (PEI) dan Non Polar : AX2 ⇒ Linier AX2E2 ⇒ Bentuk V
AX3 ⇒ Trigonal planar AX4E ⇒ Jungkat jungkit
▪ jumlah Pasangan Elektron Bebas (PEB) AX4 ⇒ Tetrahedral AX3E2 ⇒ Huruf T
Cara memperkirakan Bentuk Molekul AX5 ⇒ Trigonal bipiramidal AX5E ⇒ Segiempat piramidal
AX6 ⇒ Oktahedral
IA IIA IIIA IVA VA VIA VIIA VIIIA AX7 ⇒ Dekahedral
3. CO2
1 2 3 4 5 6 7 8 ⇒ e Valensi AX2E3 ⇒ Linier 4+2.0
AX4E2 ⇒ Segiempat datar BK = =2
H Be B C N O F 2
Li Si P S Cl CONTOH : X=3–1=2
Br Kr 1. CH4 E=2–2=0
I Xe Jum Atom = 5 AX2 ⇒ Linier
n = 4, pyb H = 1 4. NH4+
Rumus Molekul : AX… E… 4+4 .1
BK = 2 = 4 BK =
5 +4 . 1 −1
=4
2
A = Atom pusat X=5–1=4 X=5–1=4
X = Pasangan electron ikatan E=4–4=0 E=4–4=0
E = Pasangan electron bebas AX4E0 ⇒ AX4 (tetrahedral) AX4 ⇒ Tetrahedral
X = Juml Atom – 1
E = BK – X H =1 2. H2O 5. SO42-
6+2 . 1 6 +4 . 0 + 2
𝑒𝑣 + 𝑛 . 𝑝𝑦𝑏 BK = =4 BK = =4
BK = Pyb O, S = 0 2 2
2
BK = Bilangan koordinasi X=3–1=2 X=5–1=4
F, Cl, Br, I = 1 E=4–2=2
Pyb = penyumbang E=4–4=0
AX2E2 ⇒ Bentuk V AX4 ⇒ Tetrahedral
GAYA ANTAR MOLEKUL
Kovalen Polar
Diatom ⇒ Atom tak sejenis : HCl, HBr, CO 2) Ikatan Hidrogen
Ikatan Poliatom ⇒ Biasanya punya pasangan electron bebas ➢ Terdapat ikatan antara atom H dengan
Kovalen Kovalen Non Polar atom yang sangat elektronegatif (F, O, N)
Diatom ⇒ Atom sejenis : H2, Br2 , O2 , S8 , P4 HF, H2O, NH3, CH3OH, H2SO4
Poliatom ⇒ Tak punya pasangan electron bebas ➢ Titik didih ikatan Hidrogen jauh lebih
PCl5 tinggi dari Gaya Van der Waals walaupun
CH4 H PCl3
Non Mr nya lebih kecil.
H C H Cl P Cl polar
Non Cl P Cl
polar H Polar Cl
Cl 3) Ikatan Logam
1) Gaya Van der Waals Ikatan kimia yang terbentuk karena
Gaya dipol-dipol/dipol permanen adanya Tarik menarik antara atom-atom
Kov polar vs Kov polar logam karena terdapat lautan electron.
PCl3 vs PCl3 PCl3 vs HCl
Makin banyak electron yang digunakan
Gaya Gaya dipol terimbas/dipol permanen dalam ikatan logam makin kuat maka titik
Van der Waals Kov non polar vs Kov polar didih dan titik leleh logam makin tinggi
CH4 vs PCl3 Contoh : Na < Ca < Al , karena Na satu e,
Makin besar Mr Gaya dipol sesaat/Gaya London Ca dua e, dan Al tiga e.
Titik didh makin tinggi Kov non polar vs Kov non polar
CH4 vs CH4 Cl2 vs Cl2 CH4 vs Cl2
Titik didih : Ik. Ion > Ik. Hidrogen > Ik. Polar > Ik. Non polar
Tekanan uap makin rendah
Bila jenis ikatan sama ⇒ Mr besar > Mr Kecil
Anda mungkin juga menyukai
- LKPD Ikatan KimiaDokumen6 halamanLKPD Ikatan KimiaShinta88% (8)
- MateriDokumen36 halamanMateriNanda NaimahBelum ada peringkat
- Ikatan KimiaDokumen22 halamanIkatan KimiaBalla BallaBelum ada peringkat
- Bismillah Ikatan KimiaDokumen29 halamanBismillah Ikatan KimiaHaafizh SejatiBelum ada peringkat
- Media UmiDokumen20 halamanMedia UmiUhmie KalsumBelum ada peringkat
- Ikatan Kimia 1 - Kestabilan Gas Mulia, Ikatan Ion Dan Ikatan KovalenDokumen13 halamanIkatan Kimia 1 - Kestabilan Gas Mulia, Ikatan Ion Dan Ikatan KovalenKayla Calita chandraBelum ada peringkat
- Ikatan Kimia 1 - Kestabilan Gas Mulia, Ikatan Ion Dan Ikatan KovalenDokumen13 halamanIkatan Kimia 1 - Kestabilan Gas Mulia, Ikatan Ion Dan Ikatan KovalenKayla Calita chandraBelum ada peringkat
- Ikatan KimiaDokumen44 halamanIkatan Kimiaandromeda altairBelum ada peringkat
- Ikatan KimiaDokumen18 halamanIkatan KimiaPutri NadlifahBelum ada peringkat
- 5 Ikatan Kimia Dan Struktur Molekul-RevDokumen41 halaman5 Ikatan Kimia Dan Struktur Molekul-Rev11 Jela SukmawanBelum ada peringkat
- Pertemuan 6 Pengantar Ikatan KimiaDokumen52 halamanPertemuan 6 Pengantar Ikatan KimiaRizma ElfizaBelum ada peringkat
- Bab 3. Konsep Ikatan Kimia-01Dokumen25 halamanBab 3. Konsep Ikatan Kimia-01Muhammad IlhamBelum ada peringkat
- Kimia Dasar Farmasi 4 - Ikatan KimiaDokumen49 halamanKimia Dasar Farmasi 4 - Ikatan KimiaSITI ANISABelum ada peringkat
- KD Bab 7 Ikatan KimiaDokumen35 halamanKD Bab 7 Ikatan KimiaRestu Rahmi tazkiyaBelum ada peringkat
- Ikatan Kimia Dan Struktur Molekul PDFDokumen58 halamanIkatan Kimia Dan Struktur Molekul PDFPAMAN DNYBelum ada peringkat
- LKS Ikatan KimiaDokumen6 halamanLKS Ikatan KimiaLIABelum ada peringkat
- Kunci Jawaban Lks Struktur Lewis Dan Ikatan Ion 3 JPDokumen9 halamanKunci Jawaban Lks Struktur Lewis Dan Ikatan Ion 3 JPmaya nifu100% (1)
- Ikatan KimiaDokumen2 halamanIkatan Kimiairma nirmayantiBelum ada peringkat
- Bahan Ajar KD Ikatan Ion Kelas XDokumen3 halamanBahan Ajar KD Ikatan Ion Kelas XNadia BnaBelum ada peringkat
- Ikatan KimiaDokumen41 halamanIkatan KimiaAmmar HaikalBelum ada peringkat
- Lembar Kerja Siswa: Nama: Kelas: Mapel: KimiaDokumen4 halamanLembar Kerja Siswa: Nama: Kelas: Mapel: KimiaAGUSTONI pUJIATOBelum ada peringkat
- Materi Minggu Ke 2Dokumen55 halamanMateri Minggu Ke 2Naufal PrasetyaBelum ada peringkat
- Chapter 8 - Chemical Bonding, General ConceptsDokumen48 halamanChapter 8 - Chemical Bonding, General Conceptssubgm003Belum ada peringkat
- Ikatan KimiaDokumen47 halamanIkatan KimiaRifai Al FariziBelum ada peringkat
- Kelompok 9:: Lina Efitasari (221109001) Lina Efitasari (221109001) Lina Efitasari (221109001)Dokumen19 halamanKelompok 9:: Lina Efitasari (221109001) Lina Efitasari (221109001) Lina Efitasari (221109001)Safir RaBelum ada peringkat
- A. PPT Kestabilan Unsur Dan Ikatan IonDokumen20 halamanA. PPT Kestabilan Unsur Dan Ikatan IonLittle Ayu100% (1)
- Ikatan KimiaDokumen81 halamanIkatan KimiaMuhammad Aldi SetiawanBelum ada peringkat
- LKPD Kestabilan Dan Struktur LewisDokumen11 halamanLKPD Kestabilan Dan Struktur Lewistriyas100% (2)
- LKPD Kestabilan Unsur Dan Struktur LewisDokumen7 halamanLKPD Kestabilan Unsur Dan Struktur LewisRusdi ana100% (1)
- Ikatan KimiaDokumen51 halamanIkatan KimiaBurung NiasBelum ada peringkat
- Ikatan K1mi1aDokumen8 halamanIkatan K1mi1aRichoBelum ada peringkat
- Ringkasan Olimpiade KimiaDokumen113 halamanRingkasan Olimpiade Kimiahendra kusumaBelum ada peringkat
- Ikatan KimiaDokumen9 halamanIkatan KimiaFristian ChayyiBelum ada peringkat
- Bab 7 Ikatan Kimia - Struktur Molekul Sem1 2022 2023Dokumen52 halamanBab 7 Ikatan Kimia - Struktur Molekul Sem1 2022 2023yerBelum ada peringkat
- Ikatan KimiaDokumen16 halamanIkatan Kimiaai nurlelaBelum ada peringkat
- Ikatan IonDokumen16 halamanIkatan IonSindi MintaBelum ada peringkat
- Bab3 - Konsep Ikatan KimiaDokumen46 halamanBab3 - Konsep Ikatan Kimiaheksta purnamaBelum ada peringkat
- SEL VOLTA Elma Dan RiskiDokumen8 halamanSEL VOLTA Elma Dan RiskiChomsatus ShaumiBelum ada peringkat
- 08 Ikatan Kimia-1Dokumen32 halaman08 Ikatan Kimia-1wahyudinsysBelum ada peringkat
- Bab 3 - Ikatan Kimia 40 - STD yDokumen44 halamanBab 3 - Ikatan Kimia 40 - STD yNicholas SMBelum ada peringkat
- Ikatan Kimia Bab9Dokumen35 halamanIkatan Kimia Bab9Sofia TyasniBelum ada peringkat
- Ikatan Kimia IDokumen24 halamanIkatan Kimia IGreaces HananiaBelum ada peringkat
- Ikatan KimiaDokumen19 halamanIkatan KimiaAYUBelum ada peringkat
- 2.ikatan Kimia PowerpointDokumen25 halaman2.ikatan Kimia Powerpointnindiginting05Belum ada peringkat
- Adoc - Pub - Teori Ikatan Ikatan Kimia I Ikatan KovalenDokumen6 halamanAdoc - Pub - Teori Ikatan Ikatan Kimia I Ikatan KovalenLeto KeyBelum ada peringkat
- Ikatan IonDokumen12 halamanIkatan Iontisha aurelyaBelum ada peringkat
- ElektrokimiaDokumen29 halamanElektrokimiaChyntia MellyzaBelum ada peringkat
- Bab3-Konsep Ikatan KimiaDokumen42 halamanBab3-Konsep Ikatan KimiaNauratul IslamiyahBelum ada peringkat
- Materi 7 - Ikatan Kimia IDokumen33 halamanMateri 7 - Ikatan Kimia IRIFKI ANDIKHA MAULANABelum ada peringkat
- 12 ElektrokimiaDokumen41 halaman12 ElektrokimiaIrwan ProssBelum ada peringkat
- LKPD Ikatan KimiaDokumen7 halamanLKPD Ikatan KimiaMasrurotul Khoirin Najah 2110247762Belum ada peringkat
- Unit 2 Ikatan KimiaDokumen26 halamanUnit 2 Ikatan KimiaAhmad AlhaqBelum ada peringkat
- Penjelasan Pengecualian Aturan Oktet Dan Ikatan Ion PDFDokumen4 halamanPenjelasan Pengecualian Aturan Oktet Dan Ikatan Ion PDFyehuda pramanaBelum ada peringkat
- 2.IKATAN KIMIA PowerpointDokumen25 halaman2.IKATAN KIMIA PowerpointYulida erdaniBelum ada peringkat
- Ikatan KimiaDokumen97 halamanIkatan KimiaAnisa Fitri AnjaniBelum ada peringkat
- LKPD KESTABILANDokumen8 halamanLKPD KESTABILANgita geniati saragihBelum ada peringkat
- Ikatan Ion Dan KovalenDokumen27 halamanIkatan Ion Dan Kovalenaurellio faeyzaBelum ada peringkat